> Approche diagnostique par l'imagerie de l'incontinence urinaire du jeune : quel choix ? Échographie, scanner, place de la radiographie et de la radiographie avec produit de contraste
Bordeaux France
I- Introduction
Les hypothèses diagnostiques lors d’incontinence urinaire chez un jeune chien ou un jeune chat incluent une incompétence sphinctérienne, une ectopie urétérale et moins probablement une incontinence neurogène ou une autre anomalie congénitale plus rare (vessie pelvienne, fistule urétro-vaginale, persistance de l’Ouraque par exemple). Il faut également envisager le rôle d’une complication infectieuse dans ces maladies.
II- Applications de l'imagerie
Les examens complémentaires recommandés sont l’analyse d’urine, l’imagerie et/ou l’endoscopie des voies urinaires et l’exploration fonctionnelle des voies urinaires (profil urodynamique).
Le rôle de l’imagerie est principalement de mettre en évidence une ectopie urétérale ou une autre anomalie congénitale des voies urinaires basses. L’incompétence sphinctérienne est un diagnostic d’exclusion.
Le choix de la modalité d’imagerie entre l’urographie intraveineuse, l’échographie et le scanner dépend de plusieurs facteurs :
- la disponibilité de la modalité;
- l’expérience de l’opérateur;
- la qualité de la machine;
- l’état clinique de l’animal (anesthésie à risque);
- la taille de l’animal (trop petit pour l’endoscopie des voies urinaires).
1. Echographie
L’examen de première intention est souvent l’échographie. Sur animal vigile, on peut détecter des lésions évidentes de méga-uretère, que l’on peut suivre facilement pour déterminer si l’abouchement est normal ou pas. Lors de cas plus subtils, on peut réaliser l’échographie après injection intraveineuse de 1 mg/kg de furosémide (en l’absence de contrindications). Cela permet de bien visualiser les jets urétéraux dans la vessie, leur origine précise, leur orientation et leur latéralisation. Le Doppler aide à leur visualisation.
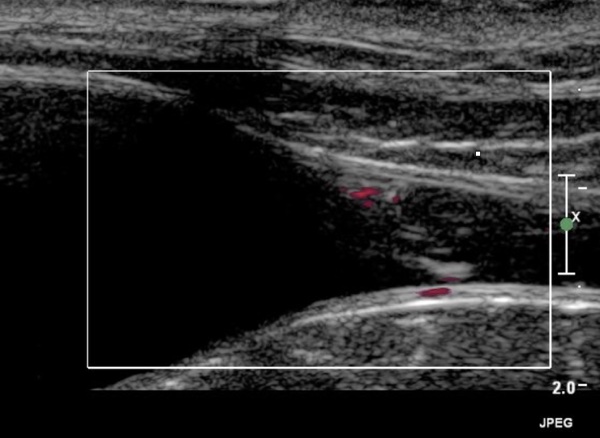
Figure 1 : jet urétéral d'origine trop caudale dans l'urètre en coupe sagittale
Lorsque le vétérinaire n’a pas d’expérience en échographie, l’urographie intraveineuse reste un examen utile dans le diagnostic des uretères ectopiques. Il demande cependant une certaine rigueur de préparation, d’exécution et d’interprétation. On utilise un produit de contraste iodé non-ionique à 600 mg d'iode / kg par voie intraveineuse. Les contrindications strictes sont l’anurie, la déshydratation et l’allergie à l’iode. Il faut toutefois faire attention lors d’insuffisance rénale et d’hypotension. Même sur un animal sain, une injection intraveineuse de produit de contraste peut provoquer une insuffisance rénale idiosyncrasique. Dans ce cas, le nephrogramme est bon mais l’opacité rénale persistante augmente et le pyélogramme est retardé.
L’urographie intraveineuse est réalisée sous anesthésie sur un animal bien hydraté auparavant. Un lavement doit être programmé au moins deux heures avant la procédure. Attention, il est important de réaliser l’analyse d’urine avant l’injection de produit de contraste iodé car celui-ci altère la densité urinaire et inhibe la croissance bactérienne. Il faut toujours réaliser deux projections orthogonales sans préparation, puis après remplissage de la vessie par du gaz (cystographie : volume à contrôler par palpation). On réalise ensuite des projections ventrodorsales en série jusqu’à obtention de l’urétérogramme, en général après 3 à 5 minutes. On réalise alors des vues obliques et latérales en sus.
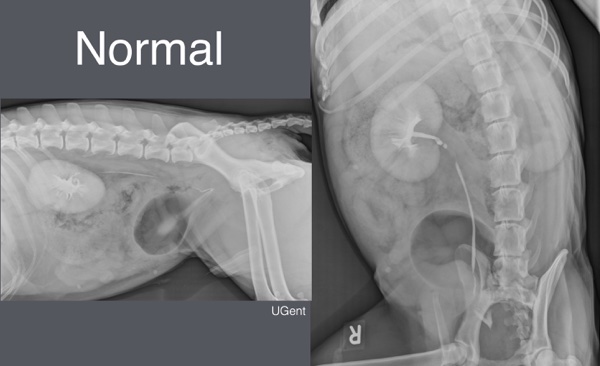
Figure 2 : urographie intraveineuse normale de chien mâle
2. Scanner
L’uroscanner est désormais l’examen d’imagerie ayant montré la meilleure efficacité à la fois dans le diagnostic de l’ectopie urétérale et dans la détermination de la localisation et du type d’abouchement des uretères ectopiques. Grâce à l’imagerie globale du bassin, du rachis et de l’abdomen, il permet également d’explorer d’autres causes d’incontinence telles que des origines nerveuses (rachidienne par exemple), une malposition vésicale, des fistules urogénitales ou urodigestives.
Il est possible de suivre les uretères sur un examen tomodensitométrique de l’abdomen et du bassin après injection intraveineuse de produit de contraste. Après un pic entre 50 secondes et 3 minutes (série post-contraste précoce), on observe un plateau de remplissage des uretères autour de 20 minutes après la fin de l’injection intraveineuse de produit de contraste iodé non-ionique (400-600 mgI d'iode / kg), il s’agit donc d’une série post-contraste retardée. Mais le péristaltisme des uretères crée des défauts de remplissage aléatoires sur certaines portions variables de l’uretère. Il est donc nécessaire de répéter la série post-contraste pour espérer obtenir l’abouchement précis des 2 uretères. Ce n’est pas idéal en terme de radioprotection et de temps d’examen.
Un protocole avec la fragmentation du bolus de produit de contraste en deux injections a été décrit : une première injection de 30%, une seconde de 70% de la dose après 9 minutes puis une série post-contraste 50 secondes après la seconde injection. Il permet d’avoir un meilleur marquage simultané du rein et du système collecteur en ne faisant qu’une seule série post-contraste.
Il est également possible d’utiliser un outil de bolus tracking disponible sur la plupart des machines pour repérer l’uretère distal et déclencher automatiquement la série abdomino-pelvienne retardée exactement lorsque la machine détecte le produit de contraste dans l’uretère. Il est souvent nécessaire de répéter l’opération pour le deuxième uretère.
Mais la méthode de choix est l’uroscanner en 4D, uniquement disponible sur des scanners haut de gamme et récents. Lorsque le détecteur du scanner est suffisamment large, il permet de scanner de manière continue un volume d’environ 4 cm de long cranio-caudalement qui inclut l’abouchement des uretères. Cela permet une imagerie dynamique du remplissage urétéral et des flux urétéro-vésicaux.
La limite de l’uroscanner est la difficulté de caractérisation du trajet intramural ou extramural. Si l’uretère extramural est accolé à la paroi urétrale, il peut être confondu avec un trajet intramural par exemple.
3. Radiographie
De manière plus anecdotique, la radiographie permet de détecter facilement une vessie pelvienne. Des procédures de type (vagino-)urétrographie rétrograde ou colonographie, permettent de détecter des fistules congénitales.
III- Conclusion
Il n’y a pas de modalité idéale pour le diagnostic et la caractérisation de l’incontinence urinaire. Il est souvent nécessaire de combiner des examens selon le coût, la disponibilité, les savoir-faire, la taille de l’animal et le risque anesthésique.
Bibliographie
- Samii VF, McLoughlin MA, Mattoon JS, Drost WT, Chew DJ, DiBartola SP, Hoshaw-Woodard S. Digital fluoroscopic excretory urography, digital fluoroscopic urethrography, helical computed tomography, and cystoscopy in 24 dogs with suspected ureteral ectopia. J Vet Intern Med. 2004 May-Jun;18(3):271-81.
- Schwarz T, Bommer N, Parys M, Thierry F, Bouvard J, Pérez-Accino J, Saunders J, Longo M. Four-dimensional CT excretory urography is an accurate technique for diagnosis of canine ureteral ectopia. Vet Radiol Ultrasound. 2021 Mar;62(2):190-198.
> Diagnostiquer l'incontinence
France
I- Objectifs d’apprentissage
- être capable de reconnaitre une incontinence urinaire d’une situation confondante (pollakiruie, polyurie) ;
- être capable de comprendre le mécanisme de l’incontinence urinaire : défaut de stockage versus défaut de vidange ;
- être capable, une fois le mécanisme de l’incontinence compris, de hiérarchiser les hypothèses étiologiques pour guider la démarche diagnostique.
II- Définitions et classification.
L’incontinence est définie comme une perte du contrôle volontaire de la miction avec des écoulements involontaires d’urine.
Il s’agit d’un motif de consultation relativement fréquent chez le chien, recouvrant de nombreuses entités cliniques. L’approche diagnostique peut reposer sur différents examens complémentaires : analyses urinaires, imagerie médicale, exploration dynamique…
Pour le clinicien, la formulation des hypothèses diagnostiques peut s’aider d’une réfelxion en 3 étapes incontournables :
- s’agit-il d’une incontinence vraie ? N’y a-t-il pas une situation ou un facteur confondant pour le propriétaire : PUPD, pollakiurie, nocturie, marquage...?
- Quel est le mécanisme à l’origine de la perte involontaire d’urine (la description des mictions et des situations de pertes d’urines est alors cruciale) : s’agit-il d’un défaut de stockage ou d’un défaut de vidange ?
- Une fois compris le mécanisme (défaut de stockage versus de vidange), quelles hypothèses lésionnelles ou fonctionnelles peuvent être formulées compte tenu du contexte épidémiologique et clinique ?
De nombreuses classifications étiologiques existent : incontinence neurogène ou non neurogène ou encore incontinence acquise ou incontinence congénitale. Ces classifications n’apportent qu’une aide limitée en pratique dans le raisonnement diagnostique du praticien et elles trouvent de grandes limites (caractère neurologique difficilement confirmable, affection congénitale se manifestant tardivement etc…) ; ainsi la distinction « défaut de stockage » ou « défaut de vidange » semble plus pragmatique pour le praticien qui peut alors rapidement s’orienter, une fois compris le mécanisme en jeu pour un individu donné.
III- Confirmer l’incontinence
Il est nécessaire de distinguer toutes les situations confondantes : pollakiurie, polyurie, nocturie. La localisation des pertes urinaires, le volume des urines émises involontairement et la quantification de l’abreuvement sont autant de détails à préciser au cours du questionnaire anamnestique. L’analyse urinaire permet également d’apporter des informations cruciales sur la présence ou l’absence d’une inflammation du tractus urinaire ou d’une dilution des urines dans le cas d’une PUPD.
1. Incontinence par défaut de stockage
Dans le cas d’un défaut de stockage, l’urine peut être perdue en continu (ectopie urétérale) ou par épisode dans des situations particulières (en position couchée lors d’incompétence sphincterienne et/ou de vessie pelvienne). L’animal est par ailleurs en mesure de présenter des mictions (mise en position et émission d’urine), dont le déroulement apparait comme normal (absence de dysurie, de strangurie). A l’examen clinique, peu d’anomalies sont alors présentes à l’exception d’une dermite urineuse éventuelle ; l’animal ne présente pas, au contraire d’un défaut de vidange, de globe vésical ou de gêne vésicale.
Une fois que le mécanisme de défaut de stockage est suspecté, le praticien peut alors formuler 3 hypothèses : incompétence sphinctérienne, une dérivation de l’apparition vésico-sphinctérien et enfin un défaut de compliance ou de capacité vésicale.
2. Dérivation de l’appareil vésico-sphinctérien
Cette catégorie est illustrée par l’ectopie urétérale. A nouveau dans ce contexte, des prédispositions raciales (Golden Retriever, Entlebucher). Lors d’ectopie urétérale, 70 % des animaux présentent en plus une incompétence sphinctérienne qui peut expliquer que le couchage aggrave les fuites. Les mictions sont par ailleurs normales tout particulièrement si l’ectopie est unilatérale mais lors d’ectopie bilatérale il n’est pas rare qu’ un reflux urétro-vésical soit présent et participe à un remplissage rétrograde de la vessie et ainsi des mictions normales persistent malgré une atteinte bilatérale.
D’autres anomalies congénitales ou acquises sont possibles mais bien plus rares : fistule vagino-rectale, persistance du canal de l’ouraque … Dans ces cas-ci, la perte d’urine n’est alors pas située au travers du méat urinaire externe.
3. Incompétence sphinctérienne
Il s’agit le plus souvent d’une incompétence du sphincter lisse. La cause la plus commune est la stérilisation dans l’espèce canine. La femelle est bien plus sensible que le mâle et de nombreuses races, de gabarit moyen (> 20kg) à grand, semblent prédisposées.
Selon les races, l’incidence pourrait varier entre 8 % et 20 % des chiennes stérilisées avec un délai entre la stérilisation et l’apparition des premiers symptômes particulièrement variable (de quelques semaines et jusqu’à 12 ans après la stérilisation) ; 75% des chiennes stérilisées deviennent incontinentes dans les 3 premières années.
Le diagnostic de certitude repose sur une exploration dynamique (profil urodynamique), malheureusement peu disponible. Une excellente réponse clinique à l’utilisation d’un alpha-mimétique conforte toutefois le clinicien.
Enfin, lors d’urétrite marquée, pouvant accompagner une infection urinaire ou des sondages répétés, une baisse de tonus du sphincter urétral est parfois observable, occasionnant une incontinence souvent discrète.
4. Défaut de compliance ou de capacité vésicale
Chez le jeune chien, une malposition vésicale (vessie pelvienne) est un exemple de situation occasionnant un défaut de capacité vésicale. Le plus souvent, la présence d’une vessie pelvienne accompagne d’autres anomalies : ectopie urétérale ou incompétence sphinctérienne. Un autre exemple de défaut de compliance correspond à la présence d’une volumineuse tumeur vésicale ou de volumineux calculs vésicaux. Dans ce dernier contexte, le praticien pourra s’attendre à la présence concomitante de signes cliniques évocateurs d’une atteinte vésicale : pollakiurie, hématurie.
5. Incontinence par défaut de vidange
Dans le cas d’un défaut de vidange, le contexte anamnestique et clinique apparait différent ; les pertes involontaires d’urines se font par « trop plein » ; des anomalies mictionnelles sont alors attendues : période prolongée d’anurie, dysurie, hématurie, strangurie. A l’examen clinique, une forte réplétion vésicale est alors détectable. Selon les causes de défaut de vidange, d’autres anomalies anamnestico-cliniques sont alors potentiellement observables : troubles de la démarche et de la coordination (hernie discale et hypertonie sphinctérienne [vessie MNC], syndrome queue de cheval et vessie MNP…), prostatomégalie…
Une fois que le mécanisme de défaut de vidange est cliniquement suspecté, le praticien peut alors formuler 3 hypothèses : une hypertonie sphinctérienne, une atonie primaire ou secondaire du détrusor et un obstacle sur les voies urinaires.
Dans l’ensemble, les situations correspondant à un défaut de vidange sont davantage retrouvées chez des animaux âgés àl'inverse des défauts de stockage pour lesquels des affections congénitales (ectopie urétérale, vessie pelvienne) ou touchant le jeune adulte (incontinence de stérilisation) sont alors fréquentes.
6. Hypertonie du sphincter urétral
L’hypertonie sphinctérienne peut s’observer dans un contexte de myélopathie thoracolombaire (vessie appelée alors de type MNC) ; il s’agira d’atteinte médullaire le plus souvent compressive, en amont de la 7e vertèbre lombaire.
A l’examen clinique, la réplétion vésicale est notable et la vessie est souvent ferme et difficilement vidangeable. La miction doit être observée directement lors d’une promenade du patient ; celle-ci apparait longue, entrecoupée.
La dyssynergie vésico-sphinctérienne est une affection rare, touchant les chiens mâles de gabarit moyen à grand et se caractérisant par un tonus urétral se maintenant au cours de la phase mictionnelle, parallèlement à la contraction du détrusor ; dans ce cas, aucune anomalie de l’examen neurologique n’est remarquée. Cette entité s’accompagnant d’un défaut de vidange prolongé, les principales complications regroupent une infection urinaire secondaire (stase) et une atonie secondaire du détrusor (cf infra).
7. Hypo ou atonie du détrusor, d’origine primaire ou secondaire
Une hypotonie du détrusor peut faire suite à une distension exagérée et prolongée de la vessie ou être secondaire à une atteinte médullaire (le plus souvent compressive) en région sacrée (L7-S3) ou encore des nerfs honteux ou pelviens (syndrome de queue de cheval) ; dans ces deux cas, l’hypotonie ou atonie du détrusor est dite secondaire et le contexte ainsi que l’examen neurologique permettent d’en comprendre l’origine. L’examen clinique révèle alors une distension vésicale, la vessie apparait non ferme et aisément vidangeable. S’il s’agit d’un chien mâle, l’observation du jet d’urine lors d’une miction peut être intéressante lors d’hypotonie du détrusor ; celui-ci apparait faible, sans pression, et plutôt vertical.
8. Obstruction du col vésical ou de l’urètre = incontinence paradoxale
Une incontinence paradoxale correspond à la présente de pertes d’urines dans un contexte d’obstruction du col ou de l’urètre (tumeur vésicale ou urétrale, sténose urétrale, lithiases, syndrome prostatique grave) ; lorsque la vessie est alors excessivement distendue du fait de l’obstruction, la pression vésicale peut excéder la résistance et occasionner une fuite d’urine. A nouveau, le contexte voire l’examen clinique (prostatomégalie) permet d’orienter vers la cause.
IV- Démarche diagnostique et traitement
Le recueil de l’anamnèse, le contexte épidémiologique et l’examen clinique suffisent au clinicien pour confirmer la présence d’une incontinence, d’en comprendre le mécanisme (défaut de stockage ou de vidange) et de formuler des hypothèses. La démarche diagnostique est alors ensuite aisément dictée par la formulation des hypothèses privilégiées ; celle-ci comprend de, manière systématique, une analyse d’urines comprenant une culture (infection urinaire confondante ou aggravante) et de l’imagerie médicale (échographie, urétrographie de contraste). Dans certains cas, un scanner ou une endoscopie complèteront la démarche (cas de l’ectopie urétérale notamment) et dans d’autres situations, le recours à un examen dynamique de profilométrie s’avèrera indispensable (dyssynergie vésico-sphinctérienne, incompétence sphinctérienne réfractaire à un essai probabiliste d’alpha-mimétique). L’examen sanguin (fonction rénale) sera exigé en cas de défaut de vidange pour rechercher la présence éventuelle d’une azotémie post-rénale +/- hyperkaliémie.
Le traitement est évidemment spécifique de l’entité diagnostiquée ; certaines situations déboucheront sur une prise en charge médicale (incompétence sphinctérienne, atonie du détrusor, dyssyngergie vésicosphinctérienne, tumeur vésicale et uétrale) et d’autres nécessiteront une intervention chirurgicale (ectopie urétérale, lithiases, vessie pelvienne, incompétence sphinctérienne réfractaire).
Bibliographie
- Acierno MJ, Labato MA. Canine Incontinence. Vet Clin North Am Small Anim Pract. 2019 Mar;49(2):125-140.
- Bartges JW, Callens AJ. Congenital diseases of the lower urinary tract. Vet Clin North Am Small Anim Pract. 2015 Jul;45(4):703-19.
- Davidson AP, Westropp JL. Diagnosis and management of urinary ectopia. Vet Clin North Am Small Anim Pract. 2014 Mar;44(2):343-53.
- Owen LJ. Ureteral ectopia and urethral sphincter mechanism incompetence: an update on diagnosis and management options. J Small Anim Pract. 2019 Jan;60(1):3-17.
> Incompétence sphinctérienne
Nantes France
I- Introduction
L’incontinence urinaire se définit comme la perte d’urine involontaire durant la phase de stockage urinaire. La présentation la plus commune est l’écoulement intermittent ou continu d’urine avec des épisodes de miction normale.
Les femelles sont en moyenne sept fois plus représentées que les mâles.
Et dans 85% des cas il y a une ectopie urétérale, une incompétence sphinctérienne ou les deux.
Chez la jeune chienne, l’incontinence urinaire est causée par une ectopie urétérale dans 45% des cas, et par une incompétence sphinctérienne dans 34%.
Chez la chienne adulte, l’incontinence urinaire est majoritairement liée (71% des cas) à une incompétence sphinctérienne.
II- Mécanismes de l’incompétence sphinctérienne
Les mécanismes exacts de ce dérèglement demeurent toujours nébuleux. Par ailleurs plusieurs schémas de dysfonctionnement peuvent aboutir à une incompétence sphinctérienne.
Globalement la fuite d’urine se produit si l’urètre n’est pas suffisamment « fermé » lors des phases de stockage, ou bien si la pression vésicale est trop importante en amont et force l’urètre à « s’ouvrir ».
Des études ont montré que la baisse de tonus urétral est un acteur clé de l’incontinence. Il est d’ailleurs prouvé qu’il diminue chez les chiennes stérilisées. Il a également été montré que la paroi de l’urètre se modifie avec la stérilisation : le taux de fibres musculaires diminue au profit du taux de collagène.
La longueur de l’urètre influence aussi la continence : les chiennes ou chattes incontinentes peuvent avoir un urètre plus court.
Une autre explication est la théorie du hamac, développée par De Lancey en médecine humaine pour expliquer l’incontinence urinaire dite « à l’effort ». La théorie de De Lancey veut que la continence soit assurée à partir du moment où les moyens de fixation de l’urètre et du col vésical, appelés hamac sous-urétral, sont intacts. Ces moyens assurent un soutien de la région vésico-urétrale permettant d’exercer un effet antifuite lorsque la pression vient à augmenter dans la cavité abdominale à la suite d’un effort. Cette théorie rejoint le concept de « vessie pelvienne » décrit en médecine vétérinaire.
Enfin, l’incontinence urinaire peut provenir d’un dysfonctionnement vésical. Dans cette forme d’incontinence urinaire, les fuites urinaires vont se produire parce que la pression intra-vésicale va dépasser la pression sphinctérienne.
En médecine vétérinaire on parle d’instabilité du detrusor. Lors du remplissage de la vessie une contraction involontaire du detrusor peut apparaître. Sur le plan clinique cette contraction involontaire de la vessie se manifestera par un besoin mictionnel urgent associé le plus souvent à une pollakiurie. En médecine humaine, l’hyperactivité du detrusor relève de plusieurs causes :
- une atteinte neurologique perturbant la régulation neurologique de l’automatisme vésico-sphinctérien. Les causes sont nombreuses et il peut s’agir par exemple des sections complètes ou partielles de la moelle, de la sclérose en plaque, des atteintes médullaires diverses ou des atteintes cérébrales (accident vasculaire, maladie de Parkinson) ;
- une « épine irritative » vésicale : infection urinaire, calcul vésical, tumeur de la vessie, compression vésicale par une tumeur de voisinage, etc. ;
- une obstruction infra-vésicale avec hyperactivité du detrusor réactionnelle ;
- idiopathique, c’est-à-dire sans cause identifiable.
Une augmentation anormale involontaire de la pression intra-vésicale peut aussi résulter d’un défaut de la compliance vésicale et être source d’une incontinence urinaire. Ce défaut de compliance signifie que les propriétés viscoélastiques vésicales sont altérées et ne permettent pas un remplissage à basse pression.
Le défaut de compliance vésicale peut être secondaire à une atteinte neurologique, à une sclérose ou fibrose de la paroi musculaire de la vessie suite à une irradiation ou à des interventions chirurgicales répétées.
Très souvent plusieurs facteurs sont associés pour aboutir à l’incompétence sphinctérienne.
Chez le mâle, les facteurs impliqués sont globalement les mêmes (mêmes prédispositions raciales également) sauf la longueur urétrale.
III- Traitements
Le traitement de l’incompétence sphinctérienne est complexe et il faut bien comprendre que la plupart des thérapies corrigent seulement un des facteurs d’incontinence précédemment discutés.
Il est donc illusoire de penser qu’un traitement unique apportera 100% de succès.
Le principe du traitement chirurgical de l’incompétence sphinctérienne est soit d’augmenter la résistance de l’urètre soit de diminuer la pression vésicale, pendant la phase de stockage.
Les traitements chirurgicaux de référence ont longtemps été la colposuspension et l’urétropexie, la transobturator vaginal tape inside-out » (TVT-O) ou encore l’injection de collagène intra-pariétal. Actuellement la pose d’un sphincter urétral artificiel est privilégiée.
1. La colposuspension
Cette technique chirurgicale consiste à tendre l’urètre et à le fixer au niveau du plancher pelvien à l’aide du vagin. La technique consiste à passer une suture de chaque côté du vagin dans son épaisseur et de les fixer autour du tendon prépubien ipsilatéral. Deux sutures de chaque côté sont utilisées chez les chiennes de taille moyenne et grande. Le point en U (monofilament irrésorbable 0 ou 1) est tout d’abord passé latéralement au tendon prépubien puis dans l’épaisseur du vagin et enfin médialement au tendon prépubien ipsilatéral. On vérifie l’absence de compression de l’urètre entre le pubis et le vagin à l’aide d’un clamp de Carmalt.
Les complications sont rares. Des cas de dysurie ont été décrits.
Les résultats sont immédiats. Une amélioration de la continence est observée dans les trois jours postopératoires. En revanche les succés sont plus mitigés : une guérison dans 53% des cas, une amélioration dans 37% des cas et une absence d’amélioration dans 10% des cas.
2. L’urétropexie
L’urètre est cette fois ancré au niveau de la sangle abdominale ventrale au niveau du rebord crânial du pubis en plaçant deux sutures de polypropylène d’un tendon prépubien à l’autre en passant par l’épaisseur de l’urètre sans traverser son lumen.
Les résultats de cette technique sur 100 chiennes montrent 56 chiennes guéries, 27 améliorées, et 17 inchangées avec un taux de complication de 21% (pollakiurie, dysurie et anurie) se résolvant dans les 2 semaines suite à la chirurgie.
3. La TVT-O
La TVT-O (transobturator vaginal tape « inside-out ») est une technique actuellement à l’étude, elle est directement inspirée de la chirurgie actuellement réalisée chez la femme. Par voie vaginale, un ruban est passé autour de l’urètre distal puis fixé en passant à travers les trous obturés. Ce ruban est soit cranté en polypropylène (Gynecare TVTs Obturator System, Ethicon) et n’a pas besoin d’être fixé, il est placé sans tension au niveau urétral, soit il est en polyamide (NYLON TAPE, Ethicon) et il est noué sous tension en position sous-cutanée en regard du pubis.
Une étude rétrospective sur les effets à long terme chez 12 chiennes a rapporté seulement 40% de chiennes continentes avec cette technique.
4. Les injections de collagène
L’injection de collagène en péri-urétral par endoscopie est séduisante, les résultats sont bons (68% de chiennes continentes) à court terme, mais il y a une tendance au retour de l’incontinence par dégradation du collagène injecté au bout d’un an.
5. Le sphincter urétral artificiel
On utilise un système d’occlusion hydraulique (AUS, Norfolkvetproducts.com) qui est posé chirurgicalement au niveau de l’urètre proximal. Le système est composé d’un occludeur, d’un tuyau de connexion et d’une chambre d’implantation.
Le diamètre de l’urètre est mesuré soit échographiquement avant la chirurgie soit pendant la chirurgie avec un morceau de suture qui sera ensuite mesuré et une taille supérieure de diamètre sera choisie. La taille de sphincter est choisie en fonction de sa largeur (11 mm pour les chats et 14 mm pour les chiens) et son diamètre (4, 6, 8, 10, 12, 14, et 16 mm).
Une laparotomie caudale est réalisée, la vessie est rétractée crânialement et une portion de 2 cm d’urètre pelvien est disséquée 3 à 4 cm caudalement au trigone. Avant la mise en place du sphincter, tout l’air de la lumière de l’occludeur et du tuyau de connexion est retiré en remplissant le système avec du NaCl. La quantité maximale possible de NaCl pouvant être injectée dans le système est mesurée. Le système est ensuite vidé du liquide et l’occludeur est placé autour de l’urètre et refermé par une suture au polypropylène 2/0 (photo 6). Son tuyau le connectant à son réservoir de remplissage est passé à travers la paroi abdominale en position latérale. Le réservoir de remplissage est positionné et fixé par 4 points au polypropylène en région sous cutanée au niveau de la paroi abdominale. Le réservoir est laissé dégonflé pendant 6 semaines après l’intervention, puis si l’incontinence persiste 0,1 à 0,2 ml sont injectés dans la chambre d’implantation avec une seringue et une aiguille de Huber chaque semaine jusqu’à obtention de la continence.
Les principales complications sont la formation de sérome au niveau de la chambre d’implantation, la sténose urétrale et l’infection.
Les résultats arrivent en général quelques semaines et quelques visites d’ajustement chez le chirurgien.
Dans une étude publiée en 2013 portant sur des chiens à incontinence congénitale et acquise, tous les chiens ont été améliorés dans leur continence avec cette technique. 22 des 24 propriétaires de chiens traités étaient très satisfaits. Cette étude rapporte peu de complications majeures (2 cas – fibrose autour de l’implant et adhérence de la tubulure à une anse intestinale), qui ont nécessité le retrait du sphincter hydraulique.
Une étude de 2018, à visée rétrospective sur le long terme, rapporte 90% de chiennes parfaitement continentes, avec un suivi à deux ans, et une seule complication majeure ayant nécessité le retrait de l’implant. La complication mineure la plus courante (infection du tractus urinaire) a cependant été observée fréquemment (40% des cas) mais gérée à chaque fois par une antibiothérapie appropriée.
IV- Conclusion
Il est important de retenir que plusieurs facteurs entrent en jeu pour aboutir à une incontinence par incompétence sphinctérienne, qu’elle soit congénitale ou acquise. De ce fait la prise en charge peut être multimodale et évoluer avec le temps sur un même patient.
À ce jour, la chirurgie offre de bons résultats avec le sphincter artificiel hydraulique. C’est un dispositif chirurgical assez peu invasif mais qui nécessite, comme tout implant synthétique, un suivi régulier.
Bibliographie
- Noel S et coll. Acquired urinary incontinence in the bitch: update and perspectives from human medicine. Part 2: The urethral component, pathophysiology, and medical treatment. The Veterinary Journal 2010; 186:8-24.
- Arnold S. Urinary incontinence in castrated bitches. Part 1: Significance, clinical aspects and etiopathogenesis. Schweiz Arch Tierheilkd 1997; 139(6):271-6.
- Applegate R et coll. Urethral Sphincter Mechanism Incompetence in Dogs: An Update. J Am Anim Hosp Assoc 2018; 54(1):22-29.
- Saussine C. L’incontinence urinaire chez la femme. Progrès en urologie 2009 ; 19 : 279—284.
- Holt P. Canine urethral sphincter mechanims incompetence. In: Mechanisms of disease in small animal surgery. Third ed. 2010: 409-13.
- Bohlen M, Nickel R. Artificial urethral sphincter in male dogs with urethral sphincter mechanism incompetence: 19 cases (2010–2017). Journal of Small Animal Practice 2022; 63: 397-402.
- Reeves L et coll. Outcome after Placement of an Artificial Urethral Sphincter in 27 Dogs. Veterinary Surgery 2013. 42 : 12–18.
- Gomes C et coll. Long-term outcome of female dogs treated with static hydraulic urethral sphincter for urethral sphincter mechanism incompetence. J Am Anim Hosp Assoc 2018; 54 : 1-9.
> Uretère ectopique
Bordeaux France
Les deux causes les plus fréquentes d’incontinence urinaire chez le chien sont l’uretère ectopique (UE) chez le chiot (52%) et l’incompétence sphinctérienne (IS) chez l’adulte.
I- Types d’uretères ectopiques
1. Intramural (>95% des cas chez le chien)
L’UE intramural entre à la surface séreuse dorso-latérale de la vessie (localisation normale du trigone vésical). Cependant, il présente un passage au sein de la sous-muqueuse pariétale vésicale (tunnélisation), pour s’aboucher à différentes localisations du tractus uro-génital distalement au trigone vésical. [1,2]
2. Extramural
L’UE extramural est séparé de la vessie, court-circuite le trigone vésical et s’abouche le long du tractus uro-génital distal. [1,2]
II- Abouchement de l’uretère ectopique
L’abouchement de l’UE est décrit comme proximal quand il se situe sur le col vésical ou dans la portion abdominale de l’urètre, distal quand il se situe dans la portion moyenne ou distale de l’urètre, le vagin ou le vestibule. L’abouchement se fait dans l’urètre chez 30%, sur le col vésical chez 18%, dans le vagin chez 2%, dans le vestibule chez 1%. Chez 48%, l’abouchement est tellement distal qu’il n’est pas possible de le localiser avec précision.
III- Pathologies concomitantes
Dans 80% des cas d’UE, d’autres anomalies congénitales sont présentes : l’agénésie/dysgénésie rénale ou vésicale, l’hydro-uretère, l’hydronéphrose, l’urétérocèle, la vessie pelvienne, l’IS urétrale, les brides vestibulo-vaginales vestigiales, l’os clitoridien, le septum urétral, la cryptorchidie et les vulves encapuchonnées. [1,2,3,4]
IV- Traitements
Les interventions chirurgicales sont uniquement réalisées chez les chiens avec ECBU négatif. Le choix d’une intervention chirurgicale chez les chiots de moins de 5 mois dépend des anomalies urétérales : si les UE sont dilatés, l'intervention est réalisée aussi rapidement que possible. S’ils sont de taille normale, l'intervention est réalisée à l’âge de 6 mois.
1. UE intramural
a) Néo-uretérostomie
Une cystotomie ventrale est réalisée. Une incision au travers de la muqueuse vésicale dorsale jusqu’à la lumière de l’UE permet de créer le nouvel abouchement urétéral à la localisation appropriée. Le segment distal de l’UE est ensuite ligaturé ou retiré.
La principale controverse des techniques de néo-urétérostomie intravésicale est de savoir si le segment urétéral distal doit être ou non retiré, ou si la ligature +/- dissection est à préférer. La comparaison entre ces 2 techniques, n’a montré aucune différence significative. Même si la résection de l’uretère distal empêche sa recanalisation, une dissection importante des tissus au sein du trigone reste requise contrairement à la ligature qui est techniquement moins complexe [2]
Une étude décrit une néo-urétérostomie avec dissection de l’uretère restreinte à sa portion intravésicale, après ligature de la partie plus distale, pour préserver le sphincter urétral.
b) Chirurgie sous cystoscopie
Les chirurgies mini-invasives sous cystoscopie sont également décrites, comme l’ablation par laser, ou la dissection aux ciseaux: elles consistent en une incision de l’UE depuis son abouchement luminal distal jusqu’en regard du trigone, en retirant tout l’uretère restant. Deux types de laser peuvent être utilisés : le laser « holmium yttrium aluminium garnet » et le laser diode. La dissection aux ciseaux nécessite des ciseaux endoscopiques et flexibles.
Ces procédures sont réalisées en ambulatoire, en réduisant l’hospitalisation et en utilisant le même équipement pour le diagnostic et le traitement sous une même anesthésie. Leur caractère mini-invasif réduit les traumatismes engendrés sur l’urètre et permet de réséquer la longueur totale de l’UE s’ouvrant distalement. En revanche, ces techniques ne sont uniquement applicables qu’aux UE intramuraux. La cystoscopie permet également de traiter les anomalies vestibulo-vaginales concomitantes.
Les résultats indiquent que la dissection aux ciseaux sous cystoscopie fournit une alternative minimalement invasive, sûre et efficace en l’absence d’une technologie utilisant le laser, dans le traitement de ces uretères ectopiques intramuraux. [3]
2. UE extramural
Le traitement de choix est l’urétéronéocystostomie consistant en la ligature de l’uretère distal et sa ré-implantation restant dans la vessie au niveau du trigone vésical.
Le taux de complication de cette technique est décrit comme relativement élevé, la plus fréquente étant l’hydronéphrose ou l’hydro-uretère secondaire à l’œdème de la muqueuse, au trauma chirurgical ou à la formation d’une sténose au site de ré-implantation.
3. Chirurgies associées
Nécessité d’une néphrectomie ?
L’urétéronéphrectomie peut s’avérer être l’unique option thérapeutique pour les patients présentant une hydronéphrose grave ou une pyélonéphrite secondaires à l’obstruction fonctionnelle de l’UE et/ou une infection ascendante. Cette procédure est associée à peu de complications, mais résulte en une perte immédiate de 50% des néphrons du chien : elle devrait donc être évitée chez les jeunes chiens.
Intérêt de l’ovariectomie ?
L’ablation des gonades résulte en la diminution de la pression de fermeture de l’urètre, pouvant conduire à l’incontinence urinaire. L’UE étant héréditaire chez beaucoup de races de chiens, la castration/stérilisation est souvent recommandée, particulièrement lors de chirurgies ouvertes réalisées chez les chiennes. Cependant, la stérilisation pourrait mener au développement, ou à l’aggravation, de l’IS urétrale, facteur contributif d’une incontinence persistante après correction chirurgicale d’un UE. L’incompétence sphincterienne étant souvent combinée à l’UE, il n’est donc pas recommandé de stériliser les chiens atteints d’UE. Une seule étude a évalué la stérilisation comme facteur pronostique de l’incontinence urinaire persistante et a mis en évidence l’absence d’effet négatif de celle-ci [1].
Chirurgie associée lors d’incompétence sphinctérienne
En combinaison du traitement de l’UE, peuvent être réalisées le traitement de l’IS. Ces procédures ont des indications limitées chez les chiots présentant un UE traité car une amélioration spontanée de l’IS juvénile a été rapportée chez approximativement 50% des chiens avec une augmentation significative de la résistance urétrale et de la capacité vésicale [1]
Une étude récente rapportant la gestion chirurgicale d’UE chez des chiens dont la moyenne d’âge était de 14 mois, n’a pas montré de bénéfice de la colposuspension sur la continence à long terme. [1]
V- Complications
Les complications post-opératoires incluent l’incontinence persistante, l’hydronéphrose, les symptômes du bas appareil urinaire (hématurie, pollakiurie, dysurie, strangurie), l’uroabdomen, la sténose du site d’implantation urétéral résultant en un flux rétrograde urinaire, et la dégradation d’une hydronéphrose pré-existante (par pyélonéphrite et cystite multirésistante). [2]
Les symptômes du bas appareil urinaire sont plus fréquents après néo-urétérostomie (100% des cas) et durent plus longtemps, en comparaison avec l’ablation au laser sous cystoscopie (13% des cas) [4]. Ces éléments reflètent le caractère invasif de la correction chirurgicale de l’UE.
Les complications potentielles des techniques mini-invasives incluent la perforation du tractus urinaire avec uro-abdomen, l’hémorragie et la recanalisation [5]
Incontinence persistante
Le résultat après correction d’un UE semble inconstant, indépendamment de la technique utilisée, avec un taux de continence post-opératoire immédiat allant de 36% à 88% après intervention chirurgicale seule, cystoscopie ou en associant un traitement médical et chirurgical. A long terme, ces valeurs sont globalement similaires, que ce soit l’ablation au laser sous cystoscopie ou les autres traitements : il n’y a donc pas de technique idéale. [4]
De nombreuses études ont examiné les facteurs pronostiques de l’UE (comme la race, le sexe, l’aspect unilétaral/bilatéral, l’aspect extramural/intramural, d’autres anomalies urogénitales, une vessie pelvienne, l’âge au moment de l'intervention, la stérilisation, et la colposuspension), mais aucun n’a été identifié pour être en corrélation avec le score de continence post-opératoire [1].
L’incontinence persistante peut résulter de multiples origines : infection du bas appareil urinaire causant une instabilité du muscle détrusor, la présence de multiples abouchements urétéraux, une IS concomitante, la recanalisation d’un uretère ligaturé, un segment urétéral intra-urétral restant, causé par une inaccessibilité chirurgicale, une fermeture urétrale genée par un UE intramural résiduel, un trop faible développement du trigone vésical, une hypoplasie vésicale, une sténose vestibulo-vaginale, des troubles neurologiques, un déséquilibre hormonal, une intervention chirurgicale inadéquate ou la combinaison de ces facteurs.
La plupart des auteurs attribue le défaut de fermeture urétrale et l’incontinence urinaire, à un UE résiduel au sein de la paroi urétrale. Ainsi, l’ablation totale de l’UE intra-mural serait recommandée. Cependant, la comparaison entre néo-urétérostomie avec ligature ou avec résection du segment urétéral distal et ablation par laser sous cystoscopie ne corrobore pas cette hypothèse car ne montre pas de différences [2]
Incontinence persistante : quelle solution ?
Chez ces patients, un ECBU doit être réalisé, ainsi qu’une échographie. Un ECBU post-opératoire devrait toujours être réalisé avant de conclure que l’incontinence persistante est causée par des anomalies anatomiques résiduelles. La plupart des cas d’incontinence persistante nécessitent une nouvelle cystoscopie pour ré-évaluer les abouchements urétéraux. [5]
Quand toutes les causes d’incontinence urinaire (autres que l’IS) ont été écartées, l’incontinence persistante post-opératoire peut être gérée médicalement, avec du phénylpropanolamine, des composés oestrogéniques.
Une thérapie additionnelle pour l’incontinence persistante a été administrée dans 25% des cas traités chirurgicalement (néo-urétérostomie). La résolution de l’incontinence urinaire a été complète chez 54% des cas [2] Pour l’ablation au laser sous cystoscopie, le taux de continence à long terme rapporté est de 31% à 47% sans médicament ajouté, et de 69% à 77% avec médicament [5] Pour la dissection aux ciseaux sous cystoscopie, le taux de continence post-opératoire est d’environ 42%. 84% des chiens sont continents avec thérapie médicamenteuse additionnelle.
Récidive de l’incontinence
Le taux de récidive de l’incontinence est de 25% à une médiane de 24,9 mois après l'intervention chirurgicale et a été observé seulement sur les cas de néo-urétérostomie et sur aucun cas d’ablation au laser [5] Tous les chiens ont retrouvé une continence avec des traitements médicaux [5]
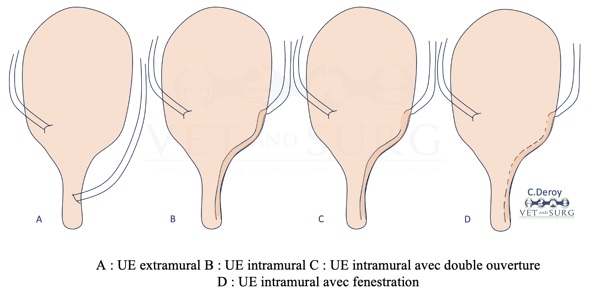
Figure 1
Bibliographie
- Noel SM, et coll. Surgical management of ectopic ureters in dogs: clinical outcome and prognostic factors for long-term continence. Vet Surg. 2017;46:631-641.
- Reichler IM et coll. Ectopic ureters in dogs: clinical features, surgical techniques and outcome. Vet Surg. 2012;41:515-522.
- Jacobson E et coll, Cystoscopic-guided scissor transection of intramural ectopic ureters as a novel alternate minimally invasive treatment option to laser ablation in female dogs:8 cases (2011–2020). JAVMA 2022; 260: 12-20
- Dekerle B, et coll, Outcomes of 25 female dogs treated for ectopic ureters by open surgery or cystoscopic-guided laser ablation, Veterinary Surgery. 2022;51:568–575
- Berent AC, et coll. Evaluation of cystoscopic-guided laser ablation of intramural ectopic ureters in female dogs. J Am Vet Med Assoc. 2012;240:716-725.
