📃 Abcès intracrânien chez cinq chats : diagnostic et prise en charge
Introduction
Les abcès intracrâniens sont rares chez le chat. Ils peuvent être encapsulés au sein du parenchyme (abcès cérébral) ou se collecter dans une cavité préexistante (empyème sous-dural ou péridural).
Ils résultent fréquemment d'une plaie pénétrante au niveau du crâne (morsure, corps étranger) ou de l'extension directe d'une infection des sinus, des oreilles ou des yeux. Des foyers infectieux éloignés disséminés par voie hématogène sont également rapportés.
Matériel et résultats
Cette série de 5 cas présente la prise en charge et le suivi d'abcès intracrâniens de causes variées.
Trois cas résultent de l'extension d'une otite. Ces patients étaient présentés pour ataxie et l'un d'entre eux présentait également des crises convulsives partielles. Dans les trois cas, un examen scanner a mis en évidence une otite moyenne associée à une lésion intracrânienne extra-axiale adjacente, évoquant un empyème méningé. Dans le premier cas, un traitement antibiotique probabiliste permet la résolution des signes cliniques. Dans le deuxième cas, des prélèvements par vidéo-otoscopie permet d'identifier la présence de Staphylococcus felis. Un traitement antibiotique ciblé entraîne la résolution des signes cliniques. Dans le troisième cas, l'examen vidéo-otoscopique permet l'identification de Pseudomonas spp. Malgré une antibiothérapie adaptée, l'état clinique du patient se détériore. Un nouvel examen scanner montre une aggravation de l'empyème méningé. Une craniotomie est réalisée et permet le débridement de l'empyème. Cette intervention, associée à une corticothérapie et la poursuite de l'antibiothérapie, permettent la résolution des signes cliniques.
Nous présentons également un cas d'extension d'une rhino-sinusite infectieuse chez un chat présentant une ataxie. Un scanner montre des lésions naso-sinusales agressives avec lyse de la paroi sinusale frontale et empyème méningé adjacent. Une trépanation du sinus frontal permet de réaliser des prélèvements pour analyses bactériologiques et mycologiques. Un traitement antibiotique ciblé permet une bonne évolution clinique.
Le dernier cas de notre étude est un chat présenté pour ataxie et dont le scanner montre une fracture ponctiforme de l'os pariétal gauche du crâne avec abcès intracrânien et sous-cutané, probablement secondaires à un traumatisme. Un traitement médical est mis en place. Après une amélioration transitoire de son état général, le patient décède trois jours plus tard.
Conclusion
Pour tous les cas de notre étude, une ataxie fait partie des signes cliniques. Dans la littérature, le signe clinique le plus fréquent des abcès intracrâniens est un état de conscience altéré. Par ailleurs, chez trois patients de notre étude, une absence d'hyperthermie et de signes hématologiques d'inflammation étaient notés. Ceci peut s'expliquer par un manque de réponse systémique aux infections du système nerveux central.
De ce fait, les examens d'imagerie en coupes sont essentiels pour diagnostiquer les abcès intracrâniens. Nous rapportons leur aspect au scanner mais détaillons également leurs caractéristiques à l'examen d'IRM.
L'antibiothérapie est fondamentale pour traiter les abcès intracrâniens. En médecine vétérinaire, le métronidazole et les β-lactamines sont les molécules les plus fréquemment utilisées. La mise en place d'une corticothérapie est controversée à cause de ses effets sur la barrière hémato-encéphalique. Le traitement chirurgical des abcès intracrâniens est décrit chez le chat, mais il a été montré que les taux de survie sont identiques pour des chats traités médicalement ou chirurgicalement. Ainsi, une craniotomie n'est pas toujours indispensable, en particulier lorsque l'agent pathogène peut être identifié autrement (vidéo-otoscopie, trépanation du sinus frontal par exemple). En revanche, l'intérêt majeur de la prise en charge chirurgicale est le retrait de fragments d'os crâniens ou de corps étrangers dans le cadre d'une perforation de la boîte crânienne.
Ainsi, l'abcès intracrânien devrait être considéré dans le cadre d'un diagnostic différentiel chez tous les chats présentant des troubles nerveux, même sans signes d'inflammation. L'étiologie de cette affection est variée et inclut les traumatismes crâniens et les infections de structures adjacentes au crâne, notamment les oreilles et les cavités naso-sinusales. Le traitement de ces affections repose sur une antibiothérapie adaptée et une utilisation raisonnée des corticoïdes. Enfin, une prise en charge chirurgicale semble ne pas être forcément indispensable.
Bibliographie
- STURGES BK, DICKINSON PJ, KORTZ GD, BERRY WL, VERNAU KM, WISNER ER, LECOUTEUR RA. Clinical signs, magnetic resonance imaging features, and outcome after surgical and medical treatment of otogenic intracranial infection in 11 cats and 4 dogs. J Vet Intern Med. 2006 May-Jun;20(3):648-56.
- COSTANZO C, GAROSI LS, GLASS EN, RUSBRIDGE C, STALIN CE, VOLK HA. Brain abscess in seven cats due to a bite wound: MRI findings, surgical management and outcome. J Feline Med Surg. 2011 Sep;13(9):672-80.
- BARRS VR, NICOLL RG, CHURCHER RK, BECK JA, BEATTY JA. Intracranial empyema: literature review and two novel cases in cats. J Small Anim Pract. 2007 Aug;48(8):449-54.
- MARTIN S, DREES R, SZLADOVITS B, BELTRAN E. Comparison of medical and/or surgical management of 23 cats with intracranial empyema or abscessation. J Feline Med Surg. 2019 Jun;21(6):566-574.
- WOUTERS EG, BEUKERS M, THEYSE LF. Surgical treatment of a cerebral brain abscess in a cat. Vet Comp Orthop Traumatol. 2011;24(1):72-5.
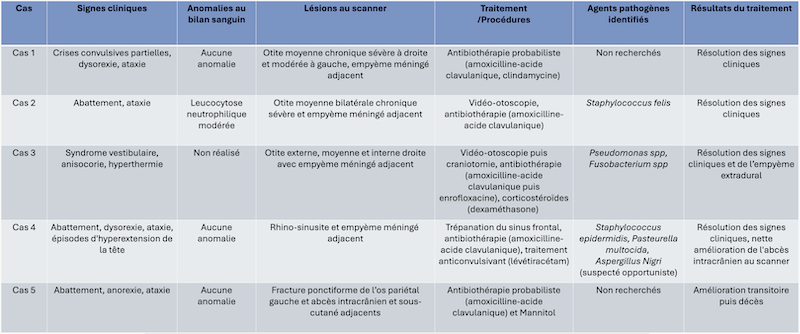
Figure 1
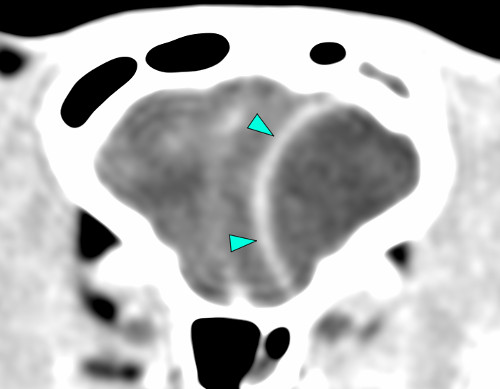
Figure 2
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Affections hépatiques : l'animal et son propriétaire, le clinicien et un bilan biologique adapté
Mérignac, France
I. Introduction
Les maladies hépatiques et des voies biliaires sont très nombreuses et ont été classées par la WSAVA en 2006, afin d'homogénéiser la nomenclature.
L'expression clinique des affections hépatiques et biliaires est très variable. Classiquement, des troubles gastro-intestinaux, urinaires, nerveux et vasculaires peuvent être observés. Les patients peuvent aussi être parfaitement asymptomatiques.
L'objectif de cette présentation est de rappeler les moyens d'exploration biologique des maladies hépatiques et biliaires chez le chien et le chat, d'en comprendre les mécanismes, et d'en connaître les indications, dans le respect des choix de la famille du patient.
II. Le premier contact avec le patient et sa famille
Avant de prescrire un bilan biologique dans un contexte de suspicion d'affection hépato-biliaire, le clinicien doit établir un dialogue avec la famille du patient, afin d'obtenir un maximum d'informations concernant les commémoratifs et l'anamnèse. Cette étape constitue le socle sur lequel tout le reste de la prise en charge médicale et/ou chirurgicale du patient va reposer. Elle est donc capitale.
Vient ensuite le temps de l'examen clinique du patient. Celui-ci doit être le plus détaillé possible, sous réserve de la coopération du patient.
Un examen neurologique est parfois nécessaire en complément de l'examen clinique.
III. Proposer un bilan biologique « d'orientation »
Il s'agit pour le clinicien de rechercher des éléments lui permettant de confirmer ou d'infirmer la suspicion anamnestico-clinique d'une atteinte de la sphère hépato-biliaire. Pour cela, la biologie médicale propose des paramètres permettant d'évaluer les lésions hépato-biliaires d'une part (ALAT, ASAT, PAL, GGT, LDH) et des marqueurs fonctionnels d'autre part (bilirubinémie, albuminémie, urémie, cholestérolémie, glycémie).
Une analyse d'urine apporte aussi des indications utiles dans la prise en charge de ces patients.
Une numération-formule sanguine vient compléter le bilan « d'orientation », pour avoir une image complète du patient.
IV. L'activité des enzymes hépatiques : marqueurs lésionnels
1. Marqueurs de cytolyse hépatique : ALAT (Alanine Aminotransférase) et ASAT (Aspartate Aminotransférase)
Ces enzymes sont contenues dans le cytoplasme des hépatocytes, et aussi dans d'autres cellules (dont les cellules musculaires surtout pour ASAT).
Lors de cytolyse hépatique, elles sont larguées immédiatement dans la circulation sanguine, ce qui se traduit par une augmentation de leur activité plasmatique très rapide. Le degré d'augmentation d'activité reflète la quantité d'hépatocytes lysés, mais n'est pas lié au pronostic. Celui-ci dépend de la cause à l'origine de la cytolyse et de sa réversibilité ou non.
En revanche, le suivi de l'activité ALAT et ASAT dans le temps est utile pour évaluer le pronostic. Lors d'un épisode aigu auto-résolutif d'hépatite chez le chien, l'amélioration de l'activité ALAT et ASAT se produit en quelques jours, avec normalisation en 2 à 3 semaines. La demi-vie de l'ALAT est d'environ 40 à 60 h et de l'ASAT de 22 h chez le chien.
Lors d'affections chroniques (de type hépatite chronique du chien ou cirrhose), une diminution de l'activité ALAT au cours du temps est un élément péjoratif, signant une diminution du nombre d'hépatocytes.
Chez le chat, la demi-vie de ces enzymes est très courte (3 à 4 h pour ALAT ; 77 minutes pour ASAT), ce qui rend la détection d'une augmentation de l'activité ALAT ou ASAT toujours très pertinente. S'il arrive de « temporiser » les investigations face à une augmentation discrète et isolée d'activité ALAT chez le chien, ce n'est pas le cas chez le chat.
La LDH (lactate déshydrogénase), une enzyme permettant la conversion du lactate en pyruvate, est présente dans le cytoplasme de toutes les cellules. Elle est souvent utilisée chez les autres espèces, mais présente peu d'intérêt chez le chien et le chat.
2. Marqueurs de cholestase : PAL (phosphatase alcaline) et GGT (gamma-glutamyltransférase)
Ces deux enzymes se trouvent à la surface des canalicules biliaires : les PAL sont liées à la membrane des canalicules biliaires et la GGT est liée aux cellules épithéliales des canaux biliaires.
Lors de cholestase, la production de ces deux enzymes est stimulée, ce qui prend du temps avant d'observer une augmentation de leur activité plasmatique.
Plusieurs iso-enzymes des PAL existent : hépatique (induite lors de cholestase ou d'atteinte hépatique), osseuse (pendant la croissance jusqu'à 7 mois, lors de tumeur osseuse ou d'ostéomyélite intense) et induite par les médicaments (notamment les corticoïdes et le phénobarbital chez le chien, mais pas chez le chat).
La demi-vie des PAL est de 2 à 3 jours chez le chien, contre 6 h chez le chat.
L'augmentation d'activité des PAL est très sensible d'une atteinte hépato-biliaire, mais très peu spécifique.
L'activité de la GGT augmente lors d'hypercorticisme (spontané ou iatrogène) chez le chien uniquement. Le colostrum et le lait contiennent de grandes quantités de GGT, d'où une augmentation d'activité de cette enzyme chez les jeunes pendant l'allaitement. En revanche, les affections osseuses et la croissance n'ont pas d'effet sur l'activité de la GGT, ni les médicaments anti-convulsivants. Une activité GGT augmentée est peu sensible d'une atteinte hépatique chez le chien, mais plus spécifique que l'activité PAL.
Une augmentation concomitante d'activité PAL et GGT renforce la spécificité d'un diagnostic d'affection hépato-biliaire.
V. Les marqueurs de fonction hépatique
Une hypoalbuminémie est fréquemment observée lors d'insuffisance hépatique (secondaire à une cirrhose ou lors d'anomalies vasculaires congénitales), lorsqu'au moins 60% des capacités de synthèse hépatique sont détruites chez le chien. L'hypoalbuminémie est plus rare chez le chat.
Elle n'est pas spécifique d'une maladie hépatique puisqu'on peut également l'observer lors de pertes digestives (entéropathies exsudatives), rénales (glomérulopathies) ou lors de réactions inflammatoires systémiques aiguës ou de brûlures étendues.
L'hypocholestérolémie peut refléter un défaut de synthèse hépatique. Elle doit être recherchée systématiquement lors de suspicion d'une atteinte hépatique grave, en vérifiant que le prélèvement sanguin est effectué, idéalement après un jeûne de 12 heures.
À l'inverse, lors de maladie cholestatique (obstruction des voies biliaires extra-hépatiques en particulier), il est fréquent de noter une hypercholestérolémie (suite au défaut de clairance biliaire du cholestérol).
L'hypoglycémie est un signe d'appel fréquent d'anomalies hépatiques congénitales (vasculaire ou maladie de surcharge). Elle est plus rarement observée lors d'une insuffisance hépatique acquise. Ce n'est pas un marqueur très sensible d'insuffisance hépatique.
Une hypourémie peut être mise en évidence lors d'insuffisance hépatique, mais ce n'est pas un paramètre sensible ni spécifique. Elle découle généralement d'un dysfonctionnement grave du foie affectant le cycle de l'urée. Isolément, l'hypourémie n'est pas spécifique de maladies hépatiques puisqu'on l'observe également lors de diurèses importantes, d'apports protéiques alimentaires bas ou exceptionnellement lors de déficits congénitaux en arginosuccinate synthétase (enzyme du cycle de l'urée).
Une hyperbilirubinémie (se traduisant par un ictère) est possible lors d'une atteinte hépatique ou des voies biliaires. Elle n'est toutefois pas spécifique puisqu'on peut également l'observer lors d'hémolyse importante, ou lors de pancréatite (en raison de la proximité du canal cholédoque et des canaux pancréatiques). On ne l'observe jamais lors d'une anomalie vasculaire congénitale. Elle est très fréquente lors d'une atteinte hépatique aiguë et moins fréquente lors d'une maladie hépatique chronique.
VI. Analyse d'urine et maladies hépato-biliaires
La densité urinaire est variable lors de maladie hépato-biliaire. Une isosthénurie (d.u. 1,008 à 1,012) ou une hyposthénurie (d.u. < 1,007) sont fréquentes lors de shunt porto-systémique congénital. La bilirubinurie est toujours pathologique chez le chat. La présence de cristaux d'urate d'ammonium doit faire rechercher un shunt porto-systémique (congénital ou shunts multiples acquis).
VII. Hématologie et maladies hépato-biliaires
L'observation d'une microcytose (VGM < 60 fl) isolée (sans anémie) est un signe d'appel fort d'un shunt porto-systémique (sauf chez certaines races asiatiques comme les Akita Inu qui ont une microcytose physiologique).
Il est fréquent de noter la présence d'une anémie modérée, souvent non régénérative, normocytaire (lors d'inflammation chronique) ou microcytaire (lors de saignement gastro-intestinal chronique ou de shunt porto-systémique).
Des anomalies morphologiques des hématies sont souvent présentes (poïkylocytes, corps de Heinz), traduisant le plus souvent une souffrance de la membrane des hématies suite à un défaut d'activité anti-oxydante du foie (déficit en glutathion).
VIII. Proposer des examens de deuxième intention, plus « ciblés »
1. Ammoniémie
L'hyperammoniémie est très sensible dans la détection des anomalies vasculaires hépatiques, sous réserve de pouvoir en réaliser le dosage très rapidement (au maximum dans les 20 minutes après la prise de sang) et sans hémolyse du prélèvement.
2. Cinétique des acides biliaires
Il s'agit bien ici d'une cinétique (valeur pré-prandiale et valeur post-prandiale) et non d'un dosage isolé qui n'a que très peu de valeur diagnostique, surtout s'il est normal.
Ce test biologique est réalisé en deuxième intention, lorsque le clinicien a une suspicion de maladie hépatique sur la base des résultats des examens initiaux. Dans ces conditions, la sensibilité du test augmente de manière très nette.
L'augmentation de la concentration sérique en acides biliaires est spécifique d'une insuffisance fonctionnelle hépatique. Cela se produit avant l'apparition de l'ictère (pas besoin de mesurer les acides biliaires chez un patient ictérique).
La cinétique des acides biliaires ne permet pas de préciser la nature de la maladie hépatique. Les anomalies parenchymateuses, vasculaires ou des voies biliaires peuvent toutes être à l'origine de cette augmentation. L'hypercorticisme ou la prise d'acide ursodéoxycholique per os, peuvent aussi provoquer cette augmentation.
L'ampleur de l'augmentation n'est pas corrélée à l'importance des lésions hépato-biliaires ou du shunt vasculaire.
Enfin, dans environ 15% des cas, la valeur post-prandiale est supérieure à la valeur à jeun. Cela n'affecte en rien les performances du test ni son interprétation.
3. Hémostase et maladies hépato-biliaires
Les troubles de l'hémostase sont fréquents lors de maladies hépato-biliaires (rarement cliniques).
Lors de cholestase chronique, la vitamine K (liposoluble) n'est plus absorbée et des troubles de l'hémostase en résultent (augmentation du TQ en particulier).
Lors d'insuffisance hépatique marquée, le défaut de synthèse des facteurs de coagulation, du fibrinogène et des protéines anti-coagulantes (antithrombine III, protéine C, protéine S) conduit à des résultats évocateurs d'une CIVD.
La fibrinogénémie est un très bon indicateur du risque de saignement post-biopsie. Si elle est inférieure à 0,5 g/l, cela constitue une contre-indication absolue à la réalisation de biopsie hépatique. Une transfusion de plasma frais congelé peut être nécessaire au préalable, pour apporter les protéines nécessaires au patient et limiter les risques.
Conclusion
Il n'existe pas un moyen unique d'appréhender les maladies hépato-biliaires. L'approche du clinicien doit obligatoirement passer par un interrogatoire minutieux des propriétaires de l'animal malade et un examen clinique approfondi, avant de décider de la meilleure façon d'appréhender le patient. De nombreux outils sont à disposition du clinicien. L'objectif est d'arriver à sélectionner les bons examens, à réaliser au bon moment, pour obtenir un diagnostic précis et ajuster au mieux la thérapeutique.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Affections hépatiques : la cytologie et l'anatomie pathologique, des amis pour la vie
Toulouse, France.
I. Objectif de la présentation
Au travers de plusieurs cas cliniques illustrés, nous évoquerons la complémentarité de l'examen cytologique et histopathologique dans le diagnostic des affections hépatiques.
II. Évaluation morphologique du foie en situation clinique
L'évaluation morphologique du foie est généralement réalisée à la suite d'une anomalie biochimique et d'imagerie suggérant une atteinte hépatique, ou dans le cadre d'un bilan d'extension de processus tumoral. Elle nécessite une collaboration étroite entre le clinicien, l'imageur, les biologistes et les pathologistes.
Cette évaluation morphologique peut être réalisée partiellement à partir de prélèvements cellulaires obtenus à l'aide de ponction à l'aiguille fine échoguidée (pour une analyse cytologique) et/ou plus largement à partir de prélèvements tissulaires à l'aide de biopsies hépatiques (pour une analyse histologique). Le choix d'une méthode par rapport à l'autre dépend de plusieurs facteurs incluant entre autres l'état clinique du patient et le processus pathologique suspecté.
Les complications pour ces deux types de prélèvement incluent le risque hémorragique particulièrement en cas de biopsie, l'essaimage tumoral (rare), et l'apparition d'une péritonite septique ou biliaire (lors de ponction de la vésicule biliaire). Ainsi, un bilan d'hémostase est recommandé, particulièrement en cas d'atteinte hépatique avérée biologiquement, et l'évaluation de la balance bénéfices-risques à la réalisation de ce type de prélèvement est primordiale.
Pour optimiser l'interprétation de ces examens, il est absolument indispensable de transmettre un maximum d'informations utiles, issues de l'anamnèse et des commémoratifs, du bilan biologique comprenant entre autres un bilan hépatique mais aussi hématologique, et les résultats de l'imagerie médicale.
III. Cytologie
L'examen cytologique est un examen complémentaire pouvant s'avérer utile d'un point de vue diagnostique pour identifier certaines affections hépatiques, bien qu'il présente un certain nombre de limites. Il peut en effet permettre d'obtenir un diagnostic précis dans certains cas, mais il permet parfois principalement de mettre en évidence des modifications du parenchyme hépatique plus ou moins « spécifiques » et pour lesquelles la cause sous-jacente reste indéterminée ou incertaine.
Parmi les avantages de l'examen cytologique, on peut citer le caractère peu coûteux, facile d'accès, relativement peu invasif et peu risqué (lorsque des troubles de l'hémostase sont écartés), ainsi que la rapidité d'obtention des résultats. La qualité du prélèvement cytologique dépend principalement de la technique de prélèvement : il est préférable de réaliser une technique de ponction sans aspiration (cela a été démontré chez le chien) afin d'optimiser la richesse et l'intégrité cellulaires, et de limiter la contamination sanguine.
Elle dépend également du processus lésionnel sous-jacent : à titre d'exemple, certaines affections associées à un contexte fibrotique ou les tumeurs de type sarcome sont moins exfoliatives, donc moins propices à l'analyse cytologique. Il est par ailleurs pertinent, lorsque cela est envisageable, de prélever divers territoires lors de l'investigation d'affections hépatiques diffuses, et de ponctionner des territoires adjacents à la lésion d'intérêt en cas de lésion nodulaire hépatique, afin d'améliorer la sensibilité diagnostique de l'examen cytologique.
Lorsque le prélèvement cytologique est de bonne qualité, il permet essentiellement d'évaluer les types et détails cellulaires (cyto-nucléaires) accessibles, sans toutefois bénéficier d'information concernant la topographie lésionnelle.
La concordance diagnostique entre la cytologie et l'histologie est rapportée comme très variable selon les études, et dépend largement de l'ensemble des types d'affections hépatiques considérés. La cytologie est relativement efficace pour mettre en évidence des lésions diffuses, de surcharge (ex : lipidose hépatique féline) ou d'infiltration tumorale (notamment à cellules rondes), et certaines lésions multi-nodulaires ou nodulaires de type tumorale. Parmi les défis cytologiques, on peut citer :
- la détection et la caractérisation des affections hépatiques inflammatoires, en raison de la potentielle contamination des prélèvements par des cellules inflammatoires d'origine sanguine, et de l'incapacité à établir la topographie des infiltrats inflammatoires en général ;
- les hépatopathies chroniques, associées ou non à un contexte fibrotique ou à une surcharge en cuivre chez le chien (en raison d'une exfoliation cellulaire potentiellement amoindrie et de la difficulté à visualiser et quantifier les dépôts de cuivre sans coloration spécifique) ;
- certains processus tumoraux pouvant peu exfolier ou étant délicats à différencier de lésions bénignes notamment lors de ponction de masse hépatique unique chez le chien.
- L'examen cytologique ne présente par ailleurs pas d'intérêt pour la recherche d'anomalie vasculaire hépatique.
IV. Histologie
Contrairement à l'examen cytologique, la réalisation d'une biopsie hépatique permet de conserver l'architecture tissulaire et la topographie lésionnelle, tout en bénéficiant d'un volume tissulaire plus important. L'évaluation histopathologique permet :
- de préciser la distribution lésionnelle qui ne serait pas identifiable en cytologie (ex : distribution zonale d'une hépatite toxique) ;
- de déterminer la sous-compartimentation d'un processus inflammatoire (ex : inflammation portale, cholangio-centrique, dans le cadre d'une cholangite féline) ;
- d'évaluer finement le réseau vasculaire portal et intralobulaire (ex : intérêt dans l'identification d'anomalies vasculaires) ;
- un diagnostic plus aisé des hépatites chroniques et une distinction plus facile des processus hyperplasiques et tumoraux hépatiques.
L'inclusion en paraffine de la biopsie hépatique permet en outre la réalisation de multiples coupes tissulaires, et ouvre l'accès à un large éventail de techniques complémentaires. Parmi elles, les colorations histochimiques sont particulièrement utiles pour confirmer la présence d'une surcharge (ex : coloration à la rhodanine pour la mise en évidence de cuivre), de remaniements fibrotiques (ex : trichrome de Masson), d'un agent pathogène (ex : coloration de Warthin-Starry pour la détection des spirochètes), etc.
L'immunohistochimie peut être également employée, notamment dans le cadre de l'immunophénotypage tumoral et de la détermination de l'index de prolifération d'une tumeur.
Enfin, une extraction d'acides nucléiques à partir de blocs tissulaires peut dans certains cas permettre la réalisation de méthodes de biologie moléculaire : par exemple, le test de clonalité PARR peut contribuer à discriminer une inflammation chronique,d'un lymphome à petites cellules.
V. Conclusion
En conclusion, l'examen cytologique est un examen complémentaire pouvant être considéré comme préliminaire ou de première intention dans l'exploration des diverses affections hépatiques. Il permet parfois d'établir un diagnostic précis notamment dans le cadre de processus tumoraux ou d'affection diffuse, telle que la lipidose hépatique féline. Toutefois, dans un certain nombre de cas, une analyse histologique s'avère être la suite logique et nécessaire afin de confirmer, compléter ou établir un diagnostic lésionnel, en permettant de préciser la topographie des lésions et/ou la réalisation d'analyses complémentaires clés (ex : colorations spécifiques, immunomarquages).
Ces deux examens sont complémentaires, et leur valeur interprétative est grandement dépendante des informations cliniques et d'imagerie médicale transmises par le clinicien.
Bibliographie
- COURTMAN, N., & QUILEZ, E. (2025). Cytologic Evaluation of the Liver. Veterinary Clinics: Small Animal Practice, 55(4), 539-558.
- WEISS, D. J., & MORITZ, A. (2002). Liver cytology. Veterinary Clinics: Small Animal Practice, 32(6), 1267-1291.
- CRAY, M., HOKAMP, J., ABRAMS, B., HUSBANDS, B. D., GRIMES, J. A., GLEASON, H., ... & SELMIC, L. E. (2023). Clinical utility of cytology from preoperative percutaneous fine needle aspirates of solitary liver masses in 220 dogs: a retrospective study (2009–2019). Journal of the American Animal Hospital Association, 59(1), 12-19
- MASSERDOTTI C. Canine and feline liver cytology. Wiley Blackwell. 2024, Hoboken, New Jersey.
- RASKIN RE, MEYER J.M, BOES K.M. Canine and feline cytology. A color atlas and interpretation guide. 4th edition. 2022, Elsevier.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Agressivité du lapin : lien avec un environnement et un mode de vie inadaptés
Eschau France
I. Introduction
L'agressivité chez le lapin de compagnie est un problème qui nous est régulièrement rapporté par les propriétaires. Ce comportement, fréquent mais dont l'importance est souvent minimisée, est la plupart du temps mal compris et mal interprété : perçue comme de la méchanceté ou un défaut de caractère, l'agressivité est en réalité un symptôme, et notre rôle est d'en comprendre l'origine pour mieux y répondre.
D'une part, le lapin est un animal captif, que nous faisons vivre dans un environnement bien plus petit et bien moins riche en occupations que dans son milieu naturel. Il dépend donc totalement du mode de vie proposé pour ses activités (alimentation, possibilités de déplacements, interactions sociales) [1,2]. Il est actif principalement à l'aube et au crépuscule, ce qui peut, dans certains cas, très bien coïncider avec le mode de vie proposé, et dans d'autres cas, mettre aussi bien la famille que l'animal en difficulté. Une étude anglaise [3] montre qu'il y a un gros manque de sensibilisation sur les bonnes pratiques de détention des lapins, notamment concernant la taille adéquate de leur espace de vie. Beaucoup de personnes continuent de privilégier des habitats traditionnels comme les cages, souvent influencées par ce qu'elles voient dans les animaleries. 81,3 % des personnes interrogées ne connaissaient pas la taille minimale conseillée pour héberger un lapin, et beaucoup ont été surprises par l'ampleur de cette recommandation.
D'autre part, avant d'être un animal de compagnie, le lapin domestique est une proie. Il présente une forte sensibilité au stress et sa stratégie de survie est d'éviter le danger.
L'agressivité (= but de mise à distance) est une stratégie coûteuse et risquée, qu'il emploie en dernier recours. Elle est à considérer comme un signal d'alarme, et arrive souvent après toute une série de comportements de communication qui n'ont pas été vus ou compris, et parfois même qui ont été ignorés. Il ne s'agit pas d'une volonté de nuire mais bien d'une réponse à la peur, à la douleur ou encore à une frustration liée à un environnement physique et social inadapté.
II. Recherche des causes de l'agressivité
Quand un lapin présente des comportements agressifs, on peut les catégoriser en 2 types : intra ou interspécifique.
1. L'agressivité interspécifique
Le plus souvent dirigée vers l'humain, mais peut aussi avoir lieu envers d'autres espèces avec lesquelles le lapin est en contact. La cause principale est la peur et il s'agit donc une agressivité défensive, amplifiée par des interactions intrusives (intervention dans la cage ou l'enclos, fait d'être porté, manipulations, bruits et gestes brusques donc effrayants, notamment de la part d'enfants, etc.). D'autres causes d'agressivité sont possibles : défense du territoire, de ressources, agressivité redirigée, autoprotection lors de douleurs ainsi que le résultat d'apprentissages suite à de mauvaises expériences préalables.
Une étude de 2016 [4] basée sur un questionnaire concernant plus de 600 lapins, a cherché s'il y avait un lien entre le sexe du lapin et l'agressivité envers les humains. Bien que les femelles soient ressorties comme plus agressives que les mâles, l'étude a aussi relevé de nombreux biais qui pourraient influencer ce résultat : ces comportements agressifs avaient lieu quand on les manipulait ou qu'on les portait, elles vivaient plus en cage que les mâles, et les individus vivant seuls étaient plus agressifs. Cette étude n'a pas montré d'impact de la stérilisation sur le comportement agressif des femelles.
Les mâles stérilisés étaient plus agressifs que les mâles entiers, et l'étude soulève des biais possibles : ont-ils été stérilisés car ils étaient agressifs ? Étaient-ils plus peureux et moins explorateurs car ils étaient castrés ?
Le point clef à retenir est que l'agressivité envers les humains est quasiment toujours liée à de la peur [1,5].
2. L'agressivité intraspécifique (entre individus de la même espèce)
Elle peut survenir pour plusieurs motifs : mise en cohabitation mal réalisée, conflits liés aux ressources, stress, douleur ou inconfort. La qualité du lien, l'environnement physique et social, la réponse aux besoins éthologiques, la frustration ainsi que l'état de santé sont alors à évaluer.
Les facteurs aggravants à investiguer sont un petit espace de vie, l'isolement social, un défaut de socialisation, un environnement pauvre ou anxiogène, la présence de facteurs de stress multiples, le manque de ressources clefs, une alimentation inadéquate, le manque de contrôle sur l'environnement, de l'inconfort, de la douleur, des expériences négatives (voire traumatisantes) préalables, ou encore le statut hormonal. [1,2,5]
III. Prise en charge comportementale
La première chose qu'on peut faire est de guider les propriétaires vers la mise en place d'un environnement adapté.
Sur le plan matériel, l'environnement doit répondre aux divers besoins éthologiques : besoin de sécurité avec de multiples cachettes, suffisamment grandes, solides et fiables, avec plusieurs possibilités de sorties (comme dans les terriers). L'animal doit avoir la possibilité de se déplacer et ne pas être confiné dans un petit espace. Son activité principale est la recherche de nourriture (foraging). Chez le lapin domestique en semi-liberté, se nourrir et se déplacer représentent plus de 50 % de son budget d'activité quotidien.
Sur le plan social, là aussi, le besoin de se sentir en sécurité est essentiel. Le lapin doit avoir accès à des interactions (non subies) qu'il peut initier et interrompre à sa guise. Ses signaux de communications doivent être connus des propriétaires et respectés. La présence d'un congénère est un élément clef de son bien-être (cf présentation sur la cohabitation).
Une fois l'environnement optimisé, il reste à mettre en place le travail de ses apprentissages via une thérapie comportementale. En effet, l'agressivité étant le dernier recours du lapin, quand le comportement est présent, c'est que le lapin a appris que c'est une stratégie efficace pour résoudre ses problèmes.
Une partie de la thérapie consiste à développer des stratégies pour éviter que le lapin recoure à l'agressivité (ex : changement du mode de distribution de l'alimentation, nettoyer quand il n'est pas à proximité et qu'il est occupé). On supprime alors la situation anxiogène, avec pour objectif, si c'est vraiment nécessaire, de pouvoir ensuite la remettre en place d'une façon adaptée, progressive et non stressante, lorsque la relation lapin-humain sera apaisée.
L'autre axe du travail comportemental est la mise en place d'un processus de désensibilisation, avec la création d'un nouveau conditionnement. On veut alors que le lapin fasse une association positive avec la présence de l'humain (ou de l'autre animal), puis lors d'une interaction. Le cadre de travail devra être sécurisé et contrôlé. Il est essentiel de respecter le rythme et l'état émotionnel du lapin afin de ne pas le mettre en immersion (état où la peur prend le dessus) et qu'il se sensibilise encore plus.
Un exemple de situation anxiogène qu'il est nécessaire de travailler est, par exemple, de faire rentrer le lapin dans une boite de transport. Lui apprendre à être porté avec le moins de stress possible est également utile, mais en revanche, il est très rarement nécessaire de devoir le porter car d'autres stratégies bien plus adaptées et bien moins stressantes existent (ex : le faire venir sur une serviette pour lui faire des soins).
Dans le cas d'agressivité intraspécifique, le travail consiste à revoir les bases de la cohabitation, et notamment la création d'un conditionnement provoquant un état émotionnel positif chez les deux individus lorsqu'ils sont en présence de l'autre (cf. présentation « Créer du lien : la cohabitation entre lapins »).
IV. Conclusion
L'agressivité du lapin en dehors de toute cause médicale est donc bien souvent le symptôme d'un environnement physique et/ou social inapproprié. Sa prise en charge réside dans l'adaptation fine du cadre de vie ainsi que la reconnaissance et la prise en compte des signaux de mal-être.
Bibliographie
- BRADBURY G. Behavioural Problems in Rabbits - A clinical approach. 5M publishing ; 2018.
- BUSETH M E, SAUNDERS R. Rabbit behaviour, health and care. CABI ; 2015.
- POWDRILL-WELLS N. « Well, You Think Rabbits, You Think Rabbit Hutch » - Public Perception of Companion Rabbit Ownership and Accommodation. Journal of Applied Animal Welfare Science. 2025 ; 1-13.
- D'OVIDIO D, PIERANTONI L, NOVIELLO E and PIRRONE F. Sex differences in human-directed social behavior in pet rabbits. Journal of Veterinary Behavior: Clinical Applications and Research. 2016. 15 : 37–42.
- CROWELL-DAVIS, S. Behavior problems in pet rabbits. Journal of Exotic Pet Medicine. 2007 ; 16, n° 1 : 38–44. et CROWELL-DAVIS, S. Rabbit behavior. Vet Clin Exot Anim. 2021 ; 24 : 53–62.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Aider les lapins lors de la consultation et de la vaccination : les effets de la phéromone maternelle apaisante
Pietro ASPRONI
Coauteurs : E. CODECASA, P. ASPRONI, M. MARCET-RIUS, J. DEMELLIER, E. DESCOUT, M. VERBAERE, P. PAGEAT, A. COZZI
Introduction
Les lapins de compagnie sont fréquemment exposés à plusieurs challenges qui affectent leur bien-être, en augmentant leur niveau de stress et en les obligeant à de continuels efforts pour s'adapter à ces situations. Les procédures vétérinaires représentent une source de stress très importante chez le lapin comme pour les autres animaux de compagnie. Chez le chat et le chien, des études précédentes ont montré que l'utilisation des analogues de phéromones aide les animaux à mieux faire face à ces procédures. L'objectif de cette étude était d'évaluer si l'exposition continue à la phéromone maternelle apaisante de lapin (RAP, de l'anglais Rabbit Appeasing Pheromone) peut aider les lapins de compagnie dans l'adaptation au challenge représenté par la consultation clinique et l'acte de la vaccination.
Matériel et méthode
L'étude a été approuvée par le Ministère de l'Enseignement supérieur et de la recherche (APAFIS #27008-2020080716514330 v6) et a impliqué 24 lapins de race néo-zélandaise albinos.
Les lapins étaient hébergés dans deux salles identiques mais séparées pendant 43 jours, 12 lapins avec le traitement RAP et 12 lapins avec le placebo. Le traitement RAP était dilué à 2% dans une solution complexe d'alcools et d'antioxydants dans un récipient de verre et libéré grâce à six bâtonnets en rotin. Le groupe placebo a reçu la même solution sans la RAP, dans le même type de récipient et avec les six bâtonnets.
Les animaux ont été vaccinés 8 jours après leur arrivée, et pendant la vaccination, leur comportement a été évalué grâce à des échelles visuelles analogiques (EVA) et des vidéos. En outre, les lapins ont été aussi soumis à sept consultations hebdomadaires, toujours en utilisant des EVA et des vidéos pour évaluer leur comportement.
Résultats
L'analyse des vidéos a montré que les lapins traités avec la RAP étaient moins inhibés (p=0.03) et plus en contact avec le vétérinaire (p=0.039) pendant la vaccination, alors que les lapins du groupe contrôle gardaient les oreilles aplaties le long du dos (p=0.003), ce qui est un signe d'un état émotionnel négatif. L'analyse des EVA a aussi montré que, pendant la consultation, les lapins du groupe RAP étaient moins agités (p=0.02). En ce qui concerne la consultation, l'analyse des EVA a révélé que les lapins traités à la RAP ont montré une meilleure évolution de leur état et de leur réactivité lors de l'enchaînement des consultations cliniques (effet traitement*jour, p<0.0001).
Conclusion
Ces résultats montrent que l'exposition continue à la RAP aide les lapins à mieux gérer et mieux s'adapter à l'acte de la vaccination et aux consultations cliniques, comme déjà démontré précédemment chez le chat et le chien. Le lapin étant une proie par nature, malgré sa domestication, il continue à percevoir l'homme comme une source potentielle de danger, ce qui rend toute manipulation stressante et nécessitant un processus d'adaptation. Dans ces situations, la RAP peut donc faciliter ce type d'interactions qui sont nécessaires pour toutes les espèces de compagnie.
Par rapport à d'autres traitements visant à réduire le stress chez les animaux de compagnie, l'utilisation de phéromones présente l'avantage de ne pas avoir d'effets indésirables ou d'interactions avec d'autres traitements, de ne pas avoir un effet sédatif et d'être simple à utiliser. En outre, cette nouvelle technologie de diffusion capillaire passive ne nécessite pas d'électricité, ce qui rend ce système sans danger.
Même si d'autres études sont nécessaires afin d'évaluer l'efficacité de la RAP dans d'autres situations stressantes, notre étude ouvre la voie à l'utilisation de ce traitement pour faciliter l'adaptation et améliorer le bien-être du lapin de compagnie, un animal qui est toujours de plus en plus présent dans la vie des propriétaires d'animaux.
Bibliographie
- FEILBERG, E.; LORRAINE CORRIDAN, C. ; BUCKLEY, L.A. A cross-sectional survey of UK veterinary practices to determine prevalence of patient stress-reducing and welfare-enhancing approaches believed to be undertaken in companion animal practice. J. Vet. Behav. 2021, 43, 14-23.
- LLOYD, J.K.F. Minimising Stress for Patients in the Veterinary Hospital: Why It Is Important and What Can Be Done about It. Vet. Sci. 2017, 4, 22.
- MILLS, D.; DUBE, M.B.; ZULCH, H. Stress and Pheromonatherapy in the Veterinary Clinic. In Stress and Pheromonatherapy in Small Animal Clinical Behaviour, 1st ed.; MILLS, D., DUBE, M.B., ZULCH, H., Eds.; WILEY-BLACKWELL: CHICHESTER, WEST SUSSEX, UK, 2013; pp. 242-256.
- PEREIRA, J.S.; FRAGOSO, S.; BECK, A.; LAVIGNE, S.; VEREGAO, A.S.; PEREIRA, G. Improving the feline veterinary consultation: the usefulness of Feliway spray in reducing cats' stress. J. Fel. Med. Surg. 2015, 18, 959-964.
- SIRACUSA, C.; MANTECA, X.; CUENCA, R.; DEL MAR ALCALÁ, M.; ALBA, A.; LAVÍN, S.; PASTOR, J. Effect of a Synthetic Appeasing Pheromone on Behavioral, Neuroendocrine, Immune, and Acute-Phase Perioperative Stress Responses in Dogs. J. Am. Vet. Med. Assoc. 2010, 237, 673-681.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Alimentation et prévention de maladies chez le Chat
Maisons-Alfort France
I. Introduction
Grâce à une bonne connaissance des liens entre l'alimentation et certaines maladies chez le chat, le praticien pourra conseiller le propriétaire pour mieux prévenir notamment l'obésité, le diabète, la pathologie urinaire.
Objectif(s) pédagogique(s) :
- Savoir prescrire un type d'alimentation adapté à différents profils de chat en bonne santé pour aider à prévenir l'obésité, le diabète et les maladies urinaires.
- Savoir quelles modalités de distribution recommander chez le chat.
- Savoir recommander des transitions alimentaires adaptées au chat.
Comme les chats vivent de plus en plus confinés, donc sans possibilité de se déplacer, et qu'ils sont souvent stérilisés/castrés, le risque est l'acquisition progressive d'un surpoids et d'une obésité, et/ou de troubles urinaires. Or, l'obésité favorise le diabète, l'arthrose, les maladies cardiaques, les maladies urinaires et réduit l'espérance de vie. Aussi, le choix de l'aliment distribué et les modalités de distribution sont à considérer pour éviter la prise de poids et les troubles urinaires (Bartges et Corbee, 2023).
II. Peut-on distribuer l'aliment au chat à volonté ?
Théoriquement, pour des raisons comportementales et de variation de pH urinaire au cours du temps, il serait préférable de donner au chat son aliment à volonté. En effet, s'il était dans la nature, le chat ferait de fréquents petits repas. Reproduire cette modalité permet au chat de pouvoir en effet consommer ce qu'il désire et quand il le désire, ce qui limite son stress.
Si le chat est sédentaire, il faudra cependant, a minima, distribuer un aliment « encombrant » et compliquer son accès. Encombrant signifie que l'aliment doit être, par nature, non seulement pauvre en calories (donc en matières grasses) et riche en fibres et/ou en eau. En effet, si la régulation de l'appétit se fait surtout de manière métabolique chez le chat, l'encombrement de la ration, s'il est important, peut jouer un rôle : on parle alors de régulation physique de l'appétit. Certains aliments, même en croquettes, du commerce semblent permettre une telle régulation, tout en étant appétents. Ils sont donc appétents et satiétogènes, et leur utilisation a réussi, par exemple, à conserver en vie un chat présentant un pica catastrophique lié à une tumeur cérébrale (observation personnelle). Ce type d'aliment, très riche en fibres, peut même au sens nutritionnel être considéré comme un fourrage car sa teneur en cellulose brute est très élevée (i.e un fourrage est un aliment contenant plus de 18% de cellulose brute (CB) par rapport à la matière sèche (MS)).
III. Et si la distribution à volonté est impossible ?
Certains chats, même avec un aliment très encombrant, semblent réfractaires à la distribution à volonté. Même après une période d'essai à volonté où, en général, le chat surconsomme de l'aliment au départ, la plupart des chats arrivent à se réguler ensuite. S'il n'y a aucune adaptation, le chat continue à se jeter sur la nourriture dès qu'elle est distribuée, quitte à manger très vite puis à vomir, et à recommencer. Cela peut être observé chez certains chats qui ont eu faim dans leur vie et il semble que le souvenir de cette faim soit indélébile (exemple du chaton abandonné jeune, avant de pouvoir subvenir à ses besoins, et qui semble ensuite obnubilé par la nourriture). Dans ce cas, il ne sera pas possible de distribuer un quelconque aliment complet à volonté.
Une solution à tenter dans ce cas est de restreindre la quantité d'aliment distribué aux besoins de l'animal, et de donner des courgettes à volonté. En effet, la faible teneur en calories et la forte teneur en eau des courgettes, permettent de « caler » le chat et, en sus, de lui donner à manger une grande quantité d'eau, ce qui a aussi un effet positif sur les troubles urinaires.
Enfin, la distribution de repas humides permet aussi d'obtenir un effet satiétogène. Cependant, les aliments humides présentent l'inconvénient majeur d'avoir besoin d'être distribués régulièrement, car ils ne se conservent pas à température ambiante (et donc ils entrainent beaucoup de gaspillage car il faut jeter les refus et nettoyer soigneusement la gamelle à chaque nouveau repas). Or, le fait de distribuer un repas stimule l'appétit du chat.
IV. Le choix des aliments
Pour diminuer le risque de prise de poids, dans le cas d'aliments complets, le choix devra se porter sur des aliments riches en protéines, pauvres en lipides et en amidon/sucres et riches en fibres. Attention, il faut calculer la concentration énergétique des aliments car beaucoup d'aliments dits « light » ou « destinés à des animaux stérilisés » ne sont pas assez restreints en énergie. Toute restriction énergétique doit s'accompagner d'une augmentation des apports relatifs en protéines (et théoriquement en minéraux, vitamines, acides gras essentiels…), afin de couvrir le besoin en protéines. Cela signifie que, plus la restriction énergétique choisie pour le chat augmente, plus le rapport protido-calorique (RPC) de l'aliment complet choisi doit augmenter.
De même, les à-côtés/récompenses doivent être restreints au maximum à 10% du besoin énergétique quotidien, en veillant à éviter les à-côtés riches en lipides ou en glucides.
Pour diminuer le risque de calculs urinaires, il est nécessaire de regarder d'autres caractéristiques de l'aliment. En particulier, la formation de calculs se faisant autour de minéraux, il est raisonnable de couvrir le besoin des animaux en minéraux, sans excès. Par exemple, il a été montré que réduire l'apport en magnésium permettait de prévenir la formation de cristaux de struvite et de maintenir un pH urinaire équilibré, réduisant ainsi le risque de formation de ces cristaux. En effet, la précipitation de certains calculs est favorisée en milieu basique (ceux de struvite) ou très acide. Dans l'idéal donc, l'apport en cations et en anions devrait permettre d'obtenir un pH urinaire proche de 6,2-6,5. Si l'équilibre anion/cations de la ration ne le permet pas, l'ajout d'acidifiants, comme la DL méthionine ou le chlorure d'ammonium permet de diminuer le pH urinaire, donc prévient l'apparition de struvites. À l'inverse, l'ajout de citrate de potassium dans la ration permet de prévenir les précipités d'oxalate de calcium : dans l'urine, l'acide citrique se combine au calcium pour former des complexes solubles, réduisant ainsi la concentration urinaire de calcium ionique et inhibant directement la nucléation des cristaux de calcium et d'oxalate.
Dans tous les cas, la capacité des urines à former des cristaux peut avoir été objectivée par le fabricant par la mesure de la saturation relative (RSS). Pour un chat à risque, il sera nécessaire de chercher un aliment indiquant ce sigle , avec un RSS qui est le plus faible possible et qui tend vers un. Le RSS obtenu est plus faible pour un aliment humide que pour un aliment sec (Passlack et al., 2018) et les aliments destinés à prévenir la rechute de la formation de calculs urinaires possèdent aussi un RSS faible. Cependant, il a été montré que l'ajout de courgettes à la dose de 10 g/kg à un aliment quelconque semble avoir aussi un effet sur le RSS (BLANCHARD et al., 2022).
Enfin, d'autres voies sont en cours d'exploration. Par exemple, il a été mis en évidence la présence d'Oxalobacter formigenes dans les fèces de chat. Or, cette espèce bactérienne est capable de métaboliser les oxalates dans le tube digestif donc, potentiellement, de diminuer le risque de calculs d'oxalate de calcium. De même, certaines plantes auraient montré un effet, chez le chat, contre la formation de cristaux de struvite.
V. Respecter dans tous les cas une période de transition alimentaire
Tout changement brutal d'alimentation chez le chat est susceptible de provoquer des troubles digestifs avec diarrhées, vomissements, voire refus de s'alimenter (Marks, 2006). Le changement de texture de l'aliment, comme le passage d'une alimentation humide à une alimentation sèche, est aussi à considérer. En effet, le chat s'adapte mal et lentement à la siccité des aliments. Or, le faible abreuvement spontané du chat, ou de certains chats, favorise les troubles urinaires.
VI. Favoriser la prise de boisson
Comme le chat est naturellement un animal qui boit peu, et qui a donc une densité urinaire élevée, c'est une espèce à risque de troubles urinaires. Il faut donc encourager la prise de boisson.
VII. Accompagnement au long terme
Le propriétaire doit surveiller le poids de son animal, et peser régulièrement son chat, à la maison ou chez le vétérinaire. En parallèle, surtout si le chat est sédentaire et qu'il bouge relativement peu, le propriétaire doit l'inciter à bouger en jouant avec lui, et en distribuant son alimentation en hauteur.
VIII. Conclusion
Le vétérinaire peut et doit prendre conscience de l'impact de l'alimentation sur la santé des chats, à court, moyen et long terme. Comme le disait Hippocrate, médecin grec de l'Antiquité qui avait affirmé la primauté de l'alimentation dans la santé : « Que ton alimentation soit ta première médecine ». Cette assertion doit se traduire par des conseils avisés des vétérinaires auprès des propriétaires pour les aider à nourrir le mieux possible leur chat et ainsi préserver sa santé.
Bibliographie
- BARTGES J et CORBEE RJ. Nutritional Management of Lower Urinary Tract Disease. In: Applied Veterinary Clinical Nutrition (eds. FASCETTI EJ et coll.), 2023, 412-41.
- BLANCHARD G et coll. Beneficial effects of a prescription home-prepared diet and of zucchini on urine calcium oxalate supersaturation and urinary parameters in adult cats. J Feline Med Surg. 2022 24(12):1203-1211.
- PASSLACK N et coll. Influence of protein concentration and quality in a canned diet on urine composition, apparent nutrient digestibility and energy supply in adult cats. BMC Vet Res. 2018;14(1):225.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Alimentation et prévention de maladies chez le Chien
Six-Fours Les Plages, France
I. Introduction
L'alimentation est essentielle pour la santé et la prévention des maladies chez le chien. Elle influence l'espérance de vie, la qualité de vie et la résistance aux maladies chroniques. La nutrition préventive assure que l'énergie et les nutriments correspondent aux besoins spécifiques de chaque chien, basés sur son espèce, son mode de vie et ses prédispositions.
Au cours du siècle dernier, une meilleure compréhension des besoins nutritionnels a réduit ou éliminé des maladies liées aux carences. Aujourd'hui, la nutrition vise à garantir la meilleure qualité de vie possible en prévenant les affections et en réduisant les risques de maladies.
L'évaluation nutritionnelle, incluant les antécédents alimentaires, le poids, l'état corporel et la condition musculaire, est le cinquième signe vital à vérifier lors des consultations vétérinaires. Les vétérinaires conseillent les propriétaires sur des stratégies nutritionnelles fondées sur des preuves scientifiques pour améliorer et prolonger la vie de leurs animaux.
II. Qualités des nutriments indispensables en prévention
Chaque nutriment indispensable possède des qualités spécifiques qui contribuent à la prévention des maladies et au maintien d'une santé optimale chez le chien.
1. Les protéines et acides aminés : qualité, digestibilité et rôles multifacettes
Les protéines sont essentielles à la santé des chiens. Elles fournissent des acides aminés vitaux pour la croissance et la réparation des tissus comme les muscles, la peau et le pelage. Elles aident aussi à produire des enzymes et des hormones qui régulent le métabolisme, l'immunité et le renouvellement cellulaire. Un bon apport en protéines de haute qualité aide à maintenir la masse musculaire, ce qui est important pour la satiété, la gestion du poids, la prévention de l'obésité et le ralentissement de l'arthrose. Les protéines de faible qualité, comme le collagène, peuvent manquer d'acides aminés essentiels et être mal digérées, nuisant à la santé.
Les chiots en croissance, les chiennes gestantes ou allaitantes et les chiens de sport ont besoin de plus de protéines pour éviter les carences et soutenir leur corps. Ne restreignez pas inutilement les protéines, sauf pour des problèmes de santé spécifiques comme l'encéphalopathie hépatique sévère ou l'urémie, car cela peut causer une perte de masse maigre et de la malnutrition. Les chiens produisent de la taurine, un acide aminé, à partir de la méthionine et de la cystéine, mais elle est parfois essentielle. Un manque de taurine peut causer une myocardiopathie dilatée (CMD) dans des races comme le Golden ou le Labrador Retriever, le Cocker Spaniel, le Doberman et le Boxer. Les aliments « sans céréales » ou riches en légumineuses peuvent réduire la taurine et causer une CMD. Supplémentez en taurine en cas de CMD ou de forte suspicion, même sans carence prouvée, pour ses effets antioxydants, osmorégulateurs et inotropes positifs.
2. Les lipides et acides gras essentiels : énergie et bouclier protecteur
Les lipides sont une source d'énergie dense et sont indispensables au transport des vitamines liposolubles (A, D, E, K). Les acides gras essentiels (AGE), en particulier les oméga-3 (EPA et DHA), jouent un rôle majeur en prévention :
- Avantages cardiovasculaires : régule la pression artérielle, stabilise le rythme cardiaque et réduit les taux de cholestérol, diminuant ainsi le risque d'arythmies et de maladies cardiaques.
- Avantages anti-inflammatoires : réduit la douleur articulaire, améliore la mobilité et ralentit la dégradation du cartilage chez les chiens atteints d'arthrose.
- Avantages cognitifs : soutient la fonction cognitive chez les chiots en croissance et les chiens âgés, améliorant la mémoire et les capacités d'apprentissage.
Les sources principales d'oméga-3 sont les poissons gras et les huiles de poisson. Cependant, un apport excessif en matières grasses doit être évité en cas de pancréatite ou d'hyperlipidémie.
3. Les glucides et fibres : régulateurs énergétiques et digestifs
a) Les glucides digestibles
Bien que non strictement essentiels, ils sont une source d'énergie rapide, particulièrement utile pour les chiens actifs.
b) Les fibres alimentaires
Ce sont des composants cruciaux en prévention. Elles contribuent efficacement à la gestion du poids en diluant l'énergie de la ration et en favorisant la satiété, ce qui est essentiel pour prévenir l'obésité.
Les fibres régulent le transit intestinal et contribuent à l'équilibre d'un microbiote sain (en tant que prébiotiques), prévenant ainsi les troubles digestifs comme la constipation ou la diarrhée. Pour les chiens diabétiques, les fibres solubles, en modulant la digestion des glucides, aident à contrôler la réponse glycémique postprandiale. Elles sont également bénéfiques dans la prise en charge des entéropathies chroniques.
4. Les Vitamines : catalyseurs et Protecteurs
Les vitamines sont des micronutriments indispensables à de nombreuses fonctions métaboliques.
La vitamine A est essentielle à la santé oculaire et à la fonction immunitaire.
Les vitamines du groupe B, notamment la cobalamine (B12), agissent comme cofacteurs métaboliques importants. Leurs carences peuvent entraîner des désordres nerveux ou des troubles de croissance. L'hypocobalaminémie est fréquemment observée dans les entéropathies chroniques, l'insuffisance pancréatique exocrine (IPE), la pancréatite et la maladie rénale chronique (MRC) ; sa supplémentation est souvent nécessaire.
Les vitamines C et E, ainsi que le sélénium et le bêta-carotène, sont de puissants antioxydants qui protègent l'organisme contre le stress oxydatif, un facteur clé du vieillissement cellulaire et de la progression de maladies chroniques telles que les troubles cognitifs, l'arthrose, les hépatopathies et les néphropathies.
Une attention particulière est requise pour la vitamine D, dont un excès peut causer des calcifications anormales et des problèmes rénaux.
5. Les minéraux et oligo-éléments : les fondations de l'équilibre
Les minéraux et oligo-éléments sont essentiels à de multiples fonctions physiologiques.
Un bon équilibre entre calcium et phosphore est crucial pour la santé osseuse. Un excès de phosphore, surtout le phosphore inorganique facilement digestible, nuit aux reins vieillissants et peut causer une maladie rénale chronique (MRC) chez les chats. Limiter le phosphore est donc essentiel pour prévenir et traiter la MRC.
Le contrôle de l'apport en sodium est essentiel pour prévenir et gérer les maladies cardiaques et rénales. Les friandises et l'alimentation humaine, souvent riches en sodium, doivent être limitées à moins de 10% de l'apport calorique quotidien total. Un apport contrôlé en sodium peut également favoriser la dilution urinaire, ce qui est bénéfique dans la prévention de l'urolithiase.
Une supplémentation en potassium est parfois nécessaire pour les animaux atteints de MRC présentant une hypokaliémie. Le rapport K/Na est important à considérer
Le zinc et le cuivre sont importants pour la santé cutanée, la reproduction et préviennent les dépigmentations du pelage. Une surveillance est nécessaire en cas de suspicion d'hépatite par surcharge en cuivre et le zinc peut réduire son absorption. D'autres oligo-éléments comme le sélénium et le fer peuvent être déficients dans les entéropathies chroniques.
6. L'Eau : le nutriment oublié mais Indispensable
L'eau est essentielle pour l'hydratation, la régulation de la température corporelle et la santé rénale. Une bonne consommation d'eau prévient l'urolithiase en diluant les urines et soutient la fonction rénale chez les animaux à risque ou malades. Les aliments humides augmentent l'apport hydrique.
7. La digestibilité et la qualité générale de l'aliment : la clé de l'absorption
Une bonne digestibilité des aliments est essentielle pour une absorption optimale des nutriments et une meilleure qualité des selles, ce qui influence le microbiote intestinal. La qualité des aliments industriels varie, donc ne vous fiez pas aux allégations marketing. Choisissez des fabricants fiables qui fournissent des informations claires sur la composition et mènent des études de digestibilité. Les aliments « complets et équilibrés » ne conviennent pas toujours aux besoins spécifiques des chiens en fonction de leur âge, leur statut physiologique ou pathologique.
III. La prévention globale par la nutrition
1. La gestion du poids est un pilier de la prévention.
L'obésité est un problème majeur qui favorise l'émergence de nombreuses comorbidités graves telles que le diabète, les maladies cardiaques et les affections articulaires. L'utilisation d'aliments à densité énergétique contrôlée et riches en nutriments essentiels est indispensable pour prévenir le surpoids chez les chiens sédentaires ou stérilisés.
2. L'individualisation de l'alimentation est fondamentale.
Chaque chien est unique, ses besoins nutritionnels varient en fonction de son âge, sa race, son niveau d'activité, son statut physiologique (croissance, stérilisation, gestation, lactation) et son état de santé. Une nutrition adaptée doit tenir compte de ces multiples facteurs.
3. La prudence est de mise avec les aliments « non conventionnels »
Les régimes sans céréales, végétariens, végans ou BARF, bien que populaires pour leur approche « naturelle », n'ont pas montré de bénéfices pour la santé par rapport aux céréales. Ils peuvent causer des déséquilibres nutritionnels, comme des carences en taurine, entraînant des cardiomyopathies dilatées. Les régimes à base de viande crue présentent aussi des risques sanitaires et nécessitent une formulation rigoureuse par un nutritionniste vétérinaire.
4. Le rôle du vétérinaire est essentiel
Il doit informer et éduquer les propriétaires sur l'importance d'une alimentation équilibrée et adaptée, réaliser des évaluations nutritionnelles continues et ajuster les régimes alimentaires tout au long de la vie de l'animal.
La science de la nutrition animale est en constante évolution et il est essentiel de s'appuyer sur des données factuelles pour guider les recommandations. Plusieurs institutions s'efforcent de diffuser les dernières connaissances scientifiques et stratégies nutritionnelles pour améliorer et prolonger la vie des animaux.
IV. Conclusion
En somme, l'alimentation est un levier de prévention majeur pour la santé du chien. Une approche nutritionnelle raisonnée et individualisée, s'appuyant sur une compréhension approfondie des qualités et des rôles de chaque nutriment essentiel, permet de prévenir un large éventail de maladies, de maintenir un poids optimal, de soutenir les fonctions vitales et de favoriser une meilleure qualité de vie et une longévité accrue.
La collaboration entre les propriétaires et les professionnels vétérinaires, guidée par les dernières avancées scientifiques, est indispensable pour déverrouiller le plein potentiel de la nutrition dans la prévention des maladies canines.
Bibliographie
- LEFEBVRE, S. (2020). Nutrition vétérinaire du chien et du chat. École vétérinaire de Lyon, VetAgro Sup.
- BLANCHARD, G., & PARAGON, B.-M. (s.d.). L'alimentation des chiens. Éditions France Agricole.
- VOLK, H. (2023). Troubles cérébraux chez le chien et le chat. Dans C. LENOX, R. CORBEE, & A. SPARKES (Eds.), Manuel de nutrition clinique canine et féline du Purina Institute (pp. 20-25). Saint Louis, Missouri: Purina Institute.
- BALTZER, W. (2023). L'arthrose chez le chien. Dans C. LENOX, R. CORBEE, & A. SPARKES (Eds.), Manuel de nutrition clinique canine et féline du Purina Institute (pp. 212-220). Saint Louis, Missouri: Purina Institute
- ROLLINS, A., & MURPHY, M. (2023). Urolithiases à struvite et à oxalate de calcium chez le chien. Dans C. LENOX, R. CORBEE, & A. SPARKES (Eds.), Manuel de nutrition clinique canine et féline du Purina Institute (pp. 249-254). Saint Louis, Missouri: Purina Institute.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Alternative à la stérilisation, les implants comme moyen de contraception
Nantes France
I. Introduction
La stérilisation chirurgicale reste la méthode de contrôle de la reproduction la plus couramment utilisée chez le chien et le chat. Toutefois, des alternatives médicales, telles que les implants à base de desloréline (agoniste de la GnRH) et de mélatonine, offrent des solutions temporaires, réversibles et parfois préférables dans certaines situations cliniques. Cette présentation vise à fournir un état des lieux actualisé sur l'utilisation de ces implants, leurs indications, contre-indications, intérêts spécifiques chez les reproducteurs, et leur place comme « galop d'essai » avant une stérilisation définitive.
II. Principes des implants contraceptifs
1. Implants à base de desloréline
a) Mécanisme d'action
La desloréline est un agoniste de la GnRH qui, administré en continu, induit une suppression réversible de la fonction gonadotrope hypophysaire. Après une phase initiale de stimulation (« flare-up »), il entraîne une inhibition de la sécrétion des gonadotrophines (LH, FSH), supprimant la production de testostérone chez le mâle et d'œstrogènes/progestérone chez la femelle.
b) Présentation et durée d'action
Les implants (Suprelorin®) existent en deux dosages : 4,7 mg (efficacité 6 mois) et 9,4 mg (efficacité 12 mois), principalement utilisés chez le mâle (chien et chat), la chienne prépubère mais aussi hors AMM chez la chatte et exceptionnellement chez la chienne.
2. Implants à base de mélatonine
a) Mécanisme d'action
La mélatonine intervient dans la régulation saisonnière de la reproduction, notamment chez les espèces à reproduction saisonnière. Son usage est donc réservé à la chatte. L'utilisation est hors AMM.
b) Présentation et durée d'action
Les implants commercialisés (Melovine®) contiennent 18 mg de mélatonine. L'AMM est attribuée pour les ovins avec comme indication le déclenchement de l'activité sexuelle en avance de saison chez la brebis et l'agnelle sexuellement mature.
III. Indications et intérêts des implants
1. Indications principales
Les indications précises pour l'utilisation des implants comme alternative à la stérilisation chez le chien et le chat sont les suivantes :
a) Contraception temporaire et réversible
Les implants à base de desloréline sont indiqués pour induire une infertilité temporaire chez les animaux dont la stérilisation chirurgicale n'est pas souhaitée ou possible, notamment chez les propriétaires qui souhaitent préserver la fertilité future de leur animal ou qui hésitent à opter pour une intervention définitive.
Cette contraception peut être proposée dans le cadre de l'AMM chez le chien pubère, le chat et la chienne prépubère ou hors AMM dans les autres cas.
L'utilisation de la mélatonine est réservée à la chatte de par la physiologie de ses cycles.
b) Refus de la chirurgie
De nombreuses études montrent que certains propriétaires sont réticents à la castration. Cette réticence peut être motivée par différentes raisons comme le coût, l'aspect invasif de la procédure, la vision de la castration comme une mutilation, la crainte de l'anesthésie générale nécessaire, etc. La confession religieuse, l'ethnie, l'âge ou encore le sexe peuvent être des facteurs influençant la vision des propriétaires à l'égard de la castration. Concernant la différence de vision entre les propriétaires masculins et les propriétaires féminines sur la castration, les hommes ont tendance à être davantage opposés à la castration que les femmes. Les hommes semblent associer la castration à la suppression de la masculinité du chien et pensent que la castration peut changer la personnalité du chien ou de la chienne.
c) Galop d'essai avant castration chirurgicale
Ils permettent d'évaluer les effets comportementaux et physiologiques d'une suppression hormonale (par exemple, sur l'agressivité, la libido ou certains troubles du comportement) avant de prendre la décision d'une stérilisation irréversible. [1]
d) Gestion de la reproduction chez les reproducteurs
Les implants sont utilisés pour mettre temporairement au repos des animaux reproducteurs sans compromettre leur fertilité à long terme, ce qui est particulièrement utile en élevage ou pour planifier les périodes de reproduction. [2]
e) Animaux à risque anesthésique ou chirurgical
Chez les animaux présentant des contre-indications à l'anesthésie générale ou à la chirurgie (par exemple, pathologies cardiovasculaires ou autres maladies systémiques), les implants offrent une alternative médicale sûre pour contrôler la reproduction. [1]
f) Postposer la puberté ou l'œstrus chez la femelle
Chez la chienne, notamment prépubère, l'implant peut être utilisé pour retarder l'apparition des premières chaleurs, ce qui peut présenter un intérêt dans certains contextes d'élevage ou pour la gestion de la santé reproductive.
g) Cas particuliers de pathologies hormono-dépendantes
Dans certaines situations, comme la gestion de pathologies liées aux hormones sexuelles (ex. : hyperplasie prostatique chez le mâle), les implants peuvent être utilisés dans un second temps comme alternative à la castration chirurgicale. [1]
2. Intérêts spécifiques
a) Réversibilité
La fertilité est généralement restaurée quelques semaines à plusieurs mois après l'arrêt de l'effet de l'implant.
b) Absence de chirurgie
Réduit les risques anesthésiques et chirurgicaux, notamment chez les animaux à risque mais aussi comme réponse au désir de non mutilation de certains propriétaires.
c) Gestion flexible
Particulièrement utile en élevage pour adapter la période de reproduction.
IV. Limites et contre-indications
1. Contre-indications
a) Animaux prépubères
L'utilisation chez l'animal immature hors AMM est à envisager avec précautions, la fonction reproductrice n'ayant pas été évaluée.
b) Femelles en gestation ou lactation
c) Tout animal en mauvaise santé et/ou présentant des troubles de la fertilité ou des pathologies de l'appareil reproducteur
2. Limites d'utilisation
a) Effets secondaires
Le « flare-up » initial peut aggraver temporairement certains comportements ou pathologies hormono-dépendantes (hypersexualité, hyperplasie prostatique, tumeurs hormono-dépendantes).
b) Effet retardé
La suppression de la fertilité n'est pas immédiate : compter 6 à 8 semaines pour une suppression complète chez le mâle.
c) Reprise de la fertilité variable
Le délai de retour à la fertilité peut varier selon l'espèce, le sexe, l'âge et la durée d'utilisation de l'implant. Il ne s'agit en aucun cas d'un produit on-off. Le retrait de l'implant n'est pas la solution magique, surtout s'il est en place depuis plusieurs semaines/mois. Il est parfois délicat et parfois quasi impossible.
d) Utilisation hors AMM
Chez la chatte et la chienne pubère, l'utilisation reste hors autorisation de mise sur le marché, nécessitant une information claire du propriétaire et un consentement éclairé.
V. Utilisation chez les reproducteurs
1. Repos reproducteur temporaire
La gestion de la reproduction surtout lors d'élevage familial est parfois compliquée. L'utilisation d'implant permet de suspendre la reproduction pour des raisons sanitaires, logistiques ou de planification d'élevage.
2. Préservation de la fertilité
Les études montrent un retour à la fertilité dans la majorité des cas, mais des cas isolés d'infertilité prolongée ont été rapportés, notamment après des utilisations répétées ou prolongées.
3. Gestion des chaleurs chez la femelle
L'implant peut être utilisé pour différer ou supprimer temporairement les chaleurs, mais le protocole doit être adapté au cycle de l'animal pour éviter les complications (kystes ovariens, métrite).
VI. Implémentation en pratique
1. Protocole d'administration
a) Implantation sous-cutanée
Sans préparation, sous anesthésie locale ou légère sédation, l'implant est injecté après tonte et désinfection soit en zone rétro-ombilicale, zone de choix s'il doit être retiré, ou entre les épaules.
b) Procédure pour le Suprelorin®
- Enfoncer l'aiguille sous la peau sur toute sa longueur puis enfoncer complètement le piston tout en retirant lentement l'aiguille.
- Appuyer sur la peau au site d'insertion après le retrait de l'aiguille et maintenir une pression pendant 30 secondes.
- Examiner la seringue et l'aiguille pour vérifier que l'implant n'est pas resté dans la seringue ou l'aiguille et que l'espaceur est visible. Il peut être possible de palper l'implant in situ.
2. Surveillance
La longue durée d'action ne doit pas être synonyme de tranquillité. Un suivi clinique recommandé pour détecter d'éventuels effets secondaires (modification du comportement, prise de poids, troubles cutanés au site d'implantation, affection de l'appareil génital).
3. Communication avec le propriétaire
a) Information sur la réversibilité
En aucun cas, il s'agit d'un traitement magique on-off de manipulation des cycles. Il est important d'insister sur la variabilité du délai de retour à la fertilité même après retrait.
b) Gestion des attentes
L'effet flare-up initial et la nécessité parfois d'une contraception complémentaire en début de traitement doivent être connus et compris du propriétaire.
VII. Conclusion
Les implants à base de desloréline représentent une alternative intéressante à la stérilisation chirurgicale chez le chien et le chat, offrant une contraception temporaire, réversible et adaptable. Leur utilisation doit cependant être raisonnée, en tenant compte des indications, des limites, des contre-indications et des attentes des propriétaires. La stérilisation chimique par la desloréline ou la mélatonine a-t-elle les mêmes conséquences que l'ablation des gonades ? Une question sans réponse encore… De nombreuses études sont en cours. Le dialogue vétérinaire-propriétaire est essentiel pour garantir une utilisation optimale et sécurisée de ces dispositifs. Toutes les informations doivent être fournies au propriétaire et le consentement éclairé est fortement recommandé lors d'utilisation hors AMM.
Bibliographie
- FONTAINE E. (2015). "Use of Deslorelin Acetate Implants for Reversible Fertility Control in Male and Female Dogs and Male Cats: A Review." Theriogenology, 84(5), 647-658.
- TRIGG TE, DOYLE AG, WALSH JD, SWANGCHAN-UTHAI T. (2006). "A review of advances in the use of the GnRH agonist deslorelin in control of reproduction." Theriogenology, 66(6-7), 1507-1512.
- GOERICKE-PESCH S. (2017). "Deslorelin acetate implant (Suprelorin®) for temporary suppression of fertility in male and female dogs and male cats." Reproduction in Domestic Animals, 52(Suppl 2), 22-27.
- JUNAIDI A. et al. (2009). "Use of melatonin implants for the control of reproduction in domestic animals." Animal Reproduction Science, 110(3-4), 371-384.
- GOERICKE-PESCH S. (2018). "Update on contraception in dogs and cats." Reproduction in Domestic Animals, 53(Suppl 3), 2-13.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Alternative à la stérilisation, les implants comme traitement des troubles du comportement
Cabrières-d'Avignon, France
Nantes, France
I. Introduction
Chez le chien, l'adolescence s'accompagne souvent de changements comportementaux jugés gênants par les propriétaires : agressivité, marquage urinaire, fugues, chevauchements, impulsivité ou refus de la contrainte. Ces troubles, fréquemment attribués à la puberté, motivent souvent la demande d'une stérilisation chirurgicale. Pourtant, les résultats sont très inconstants. Certains comportements disparaissent après suppression gonadique, d'autres non, voire s'aggravent. Cela impose au vétérinaire une grande prudence dans l'établissement du pronostic. Une question essentielle émerge : quelles alternatives à la stérilisation chirurgicale existent et que peut-on en attendre sur le plan comportemental ?
II. Hormones et adolescence : organisation versus activation
Les hormones gonadiques agissent sur le cerveau selon deux modes distincts : effets organisationnels, durables, liés au remodelage des réseaux neuronaux (neurogenèse, apoptose, élagage synaptique, différenciation sexuelle) ; effets activationnels, transitoires, dépendants de la présence des hormones dans la circulation. Ces deux niveaux expliquent pourquoi certains comportements apparus à l'adolescence relèvent d'une activation hormonale réversible, alors que d'autres traduisent une réorganisation organisationnelle durable, insensible à la suppression gonadique. [1]
Ainsi, les comportements directement liés à la compétition sexuelle — agressivité entre mâles, fugues vers les femelles, marquage urinaire intensifié, chevauchements — sont plus susceptibles de régresser après suppression hormonale. [2] Chez les femelles, les modifications comportementales liées aux cycles (agitation, irritabilité en période œstrale ainsi que le vol et la protection d'objets deux mois après l'œstrus) seront contrôlées après suppression hormonale. En revanche, l'impulsivité, l'hyperémotivité, la prise de risque ou les difficultés de contrôle apparaissant à la puberté reflètent des changements organisationnels et nécessitent une approche comportementale spécifique.
III. Limites de la stérilisation chirurgicale
La stérilisation chirurgicale est souvent demandée comme solution à un problème comportemental apparu à la puberté. Si elle peut être efficace pour les comportements sexuels, son efficacité est limitée, voire nulle, pour les troubles liés à une vulnérabilité comportementale préexistante. Chez les chiens présentant une fragilité émotionnelle depuis l'adoption (chiens craintifs, pauvres en autocontrôle, sensibles à la frustration), la puberté agit comme un révélateur ou un amplificateur. Dans ces cas, la stérilisation risque d'être perçue comme inefficace, voire d'être accusée d'avoir aggravé le problème. L'erreur d'interprétation est d'autant plus fréquente que les troubles apparaissent à un âge concomitant à la demande de stérilisation. Il est donc crucial de rappeler que la stérilisation chirurgicale ne constitue pas une solution universelle et que les attentes doivent être soigneusement calibrées. [3]
IV. Implants de desloréline : une alternative réversible
Les implants de desloréline (agoniste de la GnRH) suppriment la fonction gonadique pour une durée de 6 à 12 mois, selon le dosage. Leur effet n'apparaît qu'au bout de 3 à 6 semaines, et un flare-up initial (transitoire aggravation de l'agressivité inter-mâles ou du marquage) peut être observé. L'administration concomitante d'acétate de cyprotérone pendant le 1er mois permet de limiter ce phénomène. Leur principal avantage réside dans leur réversibilité, très appréciée des propriétaires. L'implant constitue également un outil diagnostique : il permet de prédire si un comportement est sensible à la suppression hormonale avant d'envisager une stérilisation définitive. [4,5] Chez la femelle, les implants peuvent être utilisés pour contrôler les chaleurs ou moduler certains comportements périœstraux, mais leur usage reste plus marginal.
V. Cyprotérone : un complément possible
L'acétate de cyprotérone est un progestatif anti-androgène capable de réduire l'agressivité intrasexe. Au-delà de son effet périphérique, cette molécule agit sur le système nerveux central en augmentant la disponibilité en sérotonine et en dopamine, ce qui en fait un anti-impulsif intéressant. Cependant, ses effets secondaires relativement nombreux et parfois graves, notamment l'augmentation d'appétit, la gynécomastie et les atteintes pancréatiques et hépatiques, limitent son utilisation prolongée. Il est réservé aux prises en charge comportementales de grands agressifs où l'action de la fluoxétine est insuffisante et où le risque d'abandon ou d'euthanasie est élevé.
VI. Conclusion
Les implants de desloréline représentent une alternative crédible à la stérilisation chirurgicale pour les troubles liés à la compétition sexuelle et apparus à la puberté. Leur caractère réversible et leur rôle prédictif en font un outil thérapeutique et diagnostique de choix. Toutefois, leur efficacité est limitée aux comportements d'activation hormonale. Les troubles révélés par une vulnérabilité comportementale antérieure nécessitent une prise en charge spécifique combinant thérapie comportementale et, le cas échéant, psychopharmacologie. La distinction entre ces deux types de troubles est essentielle pour éviter les attentes irréalistes des propriétaires et construire un plan thérapeutique adapté. L'implant apparaît alors non seulement comme un traitement, mais aussi comme un outil de clarification diagnostique, permettant au vétérinaire d'orienter la décision thérapeutique en connaissance de cause.
Bibliographie
- SISK CL, FOSTER DL. The neural basis of puberty and adolescence. Nat Neurosci. 2004;7(10):1040-7.
- MASSON S et coll. Psychiatrie vétérinaire du chien. NoLedge Editions; 2023.
- NEILSON JC et coll. Effects of castration on problem behaviors in male dogs. J Am Vet Med Assoc. 1997;211(2):180-2.
- DE GIER J et coll. Behavioural evaluation of male dogs treated with GnRH-agonist implant. Appl Anim Behav Sci. 2012;141:158-69.
- BEATA C et coll. Effects of deslorelin implants on behaviour in male dogs. Vet Rec. 2016;178(1):25-30.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Analyse quantitative des lymphocytes T CD3+ dans la muqueuse intestinale de chiens présentant une inflammation chronique
Juan HERNANDEZ
Coauteurs :
G. BOUILLET,
G. GONEL,
T. MERIC,
R. O. LEAL,
M. RIQUELME,
C. BERTOLANI,
E. DARNIS,
O. TOULZA,
M. HUGONNARD,
M. DOMÍNGUEZ-RUIZ,
A-C. BARROT,
Moez RHIMI,
T. LARCHER,
J. HERNANDEZI. Introduction
Chez le chien, les maladies inflammatoires chroniques de l'intestin (MICI) se traduisent par des signes gastro-intestinaux persistants, résistants aux modifications alimentaires ainsi qu'aux stratégies de modulation du microbiote.
L'inflammation de la muqueuse intestinale s'accompagne classiquement d'une infiltration accrue de lymphocytes T CD3+ dans la lamina propria et l'épithélium intestinal [1-2]. Toutefois, ces données proviennent d'études anciennes, menées sur de petites cohortes, souvent sans groupe témoin, et n'ont pas permis d'établir de lien solide entre cette infiltration, la sévérité clinique ou la réponse au traitement.
Plus récemment, une étude a remis en question ce paradigme en rapportant, de manière inattendue, une diminution de la densité de lymphocytes T dans la muqueuse iléale et colique de chiens normoalbuminémiques atteints de MICI, suggérant une hétérogénéité des profils immunitaires au sein de cette affection [3].
II. Matériel et méthodes
Face à ces résultats contradictoires, notre étude avait pour objectif de caractériser l'infiltration lymphocytaire intestinale CD3+ dans un large échantillon de chiens. Pour cela, nous avons comparé la densité des cellules CD3+ dans le duodénum, l'iléon et le côlon entre un groupe de chiens atteints de MICI et un groupe de chiens sains, et exploré les éventuelles associations avec des marqueurs cliniques et biologiques de la maladie.
Les chiens inclus provenaient de six hôpitaux vétérinaires en Europe et ont été recrutés entre janvier 2020 et décembre 2023. Le diagnostic de MICI reposait sur des critères standardisés : présence de signes digestifs persistants depuis plus de trois semaines, échec des traitements diététiques et microbiotiques, et confirmation histologique d'une inflammation intestinale, après exclusion de causes extradigestives, infectieuses ou tumorales.
Les échantillons analysés correspondaient à des biopsies réalisées à des fins diagnostiques, fixées au formol, incluses en paraffine, et utilisées dans le cadre de cette étude en tant que matériel résiduel. En parallèle, des biopsies intestinales issues d'études terminales indépendantes ont été obtenues chez douze chiens de laboratoire sains, également disponibles sous forme de blocs de paraffine, et ont constitué le groupe témoin.
Le marquage immunohistochimique des lymphocytes T a été réalisé à l'aide d'un anticorps commercial anti-CD3 (Dako #A0452). Les cellules marquées ont été quantifiées automatiquement à l'aide du logiciel Qupath®. Les résultats ont été exprimés sous forme de ratio entre les cellules CD3+ et le nombre total de cellules nucléées (RCD3).
Les comparaisons entre groupes ont été réalisées à l'aide des tests de Mann-Whitney ou de Kruskal-Wallis, selon les cas. Les corrélations entre le RCD3 et les scores cliniques (CIBDAI, CCECAI) ainsi que les paramètres biologiques (albuminémie, cobalaminémie, hématocrite...) ont été évaluées à l'aide du test de Kendall. L'ensemble des analyses a été effectué avec le logiciel R, en considérant une valeur de p < 0,05 comme statistiquement significative.
III. Résultats
Au total, 47 chiens atteints de MICI et 12 chiens sains ont été inclus dans l'analyse.
Chez les témoins, les valeurs de RCD3 étaient faibles et relativement homogènes entre les régions intestinales : médiane de 1,42 % (IQR 2,00) dans le duodénum, 0,85 % (IQR 1,73) dans l'iléon, et 1,32 % (IQR 1,73) dans le côlon.
En revanche, une augmentation significative du RCD3 a été observée chez les chiens atteints de MICI dans le duodénum (6,34 %, IQR 8,55 ; p = 0,03), l'iléon (9,79 %, IQR 8,86 ; p < 0,01) et le côlon (3,88 %, IQR 4,26 ; p < 0,01) par rapport aux chiens sains.
Les chiens malades ont ensuite été répartis en deux sous-groupes selon leur statut albuminémique : 22 étaient hypoalbuminémiques, tandis que 25 avaient une albuminémie normale. Aucune différence significative de RCD3 n'a été mise en évidence entre ces deux sous-groupes, quel que soit le segment intestinal analysé. Par ailleurs, aucune corrélation statistiquement significative n'a été observée entre le RCD3 et les scores cliniques (CIBDAI, CCECAI) ni avec les paramètres biologiques.
IV. Discussion
Nos résultats confirment une augmentation de la densité des lymphocytes T CD3+ dans la muqueuse intestinale chez les chiens atteints de MICI, en accord avec les données historiques. Toutefois, plusieurs éléments méritent d'être discutés. D'une part, les valeurs de RCD3 chez les chiens sains étaient homogènes entre les segments intestinaux, ce qui contraste avec certaines études antérieures décrivant une densité moindre au niveau colique [1-2]. D'autre part, bien que l'augmentation de la densité lymphocytaire CD3+ chez les chiens malades soit statistiquement significative, elle était marquée par une forte variabilité interindividuelle. À chaque étage intestinal, entre 30 et 40 % des chiens atteints de MICI présentaient des valeurs de RCD3 comparables à celles des chiens sains, indépendamment de leur score clinique ou de leur albuminémie.
V. Conclusion
Cette étude met en évidence une infiltration accrue de lymphocytes T CD3+ chez la majorité des chiens atteints de MICI, tout en soulignant une hétérogénéité importante et un chevauchement partiel avec les valeurs observées chez les chiens sains. L'absence de corrélation entre la densité lymphocytaire et les marqueurs cliniques ou biologiques questionne la pertinence du RCD3 en tant qu'indicateur de sévérité ou de suivi de la maladie.
La prise en compte conjointe de paramètres immunitaires, microbiotiques et cliniques apparaît aujourd’hui essentielle pour mieux caractériser les profils inflammatoires individuels. Une telle approche multidimensionnelle pourrait contribuer à une meilleure compréhension de l’hétérogénéité des MICI du chien, permettre d’identifier des sous-types pathologiques plus homogènes, et ainsi ouvrir la voie à une médecine de précision en gastro-entérologie vétérinaire.
Références
- German AJ, Hall EJ, Day MJ. Immune cell populations within the duodenal mucosa of dogs with enteropathies. J Vet Intern Med. 2001;15(1):14‑25.
- German AJ, Hall EJ, Day MJ. Analysis of Leucocyte Subsets in the Canine Intestine. Vol. 120, J. Comp. Path. 1999.
- Hernandez J, Rouillé E, Chocteau F, Allard M, Haurogné K, Lezin F, et al. Nonhypoalbuminemic inflammatory Bowel disease in dogs as disease model. Inflamm Bowel Dis. 1 déc 2021;27(12):1975‑85.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Analyse rétrospective des abcès faciaux chez le lapin de compagnie : étude tomodensitométrique de 500 cas (2021-2025)
Introduction
Les abcès faciaux sont une affection fréquente chez le lapin de compagnie, souvent en lien avec une pathologie dentaire sous-jacente. Cette étude rétrospective analyse 500 cas diagnostiqués entre 2021 et 2025 afin d'évaluer leurs caractéristiques radiographiques et tomodensitométriques.
Matériel et résultats
L'imagerie a permis d'étudier la localisation des abcès et leur lien avec les structures anatomiques environnantes. Une attention particulière a été portée à l'origine dentaire ou non des lésions, ainsi qu'à leur distribution au sein du crâne. L'étude a également examiné les signes tomodensitométriques associés, tels que la lyse osseuse, la réaction périostée et la présence d'ostéomyélite ainsi que la relation à une structure anatomique (dentaire, salivaire ou autre).
Conclusion
Ces résultats soulignent l'importance du scanner dans l'identification de l'origine des abcès faciaux et l'évaluation des structures osseuses atteintes. L'imagerie avancée constitue un outil essentiel pour améliorer le diagnostic et mieux comprendre la distribution anatomique de ces lésions chez le lapin.
Bibliographie
- ARTILES CA, SANCHEZ-MIGALLON GUZMAN D, BEAUFRÈRE H, PHILLIPS KL. Computed tomographic findings of dental disease in domestic rabbits (Oryctolagus cuniculus): 100 cases (2009-2017). J Am Vet Med Assoc. 2020 Aug 1;257(3):313-327
- BORAWSKI W, KIEŁBOWICZ Z, KUBIAK-NOWAK D, PRZĄDKA P, PASTERNAK G. Computed Tomographic Findings of Dental Disease and Secondary Diseases of the Head Area in Client-Owned Domestic Rabbits (Oryctolagus cuniculus): 90 Cases. Animals (Basel). 2024 Apr 11;14(8):1160.
- JEKL V, JEKLOVA E, HAUPTMAN K. Radical debridement guided by advanced imaging and frequent monitoring is an effective approach for the treatment of odontogenic abscesses and jaw osteomyelitis in rabbits: a review of 200 cases (2018-2023). J Am Vet Med Assoc. 2023 Oct 9;261(S2):S52-S61.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Anesthésie-analgésie en odontostomatologie
Nantes, France
Velizy, France
I. Introduction
La chirurgie maxillo-faciale vétérinaire couvre un large éventail de procédures, depuis les extractions dentaires simples jusqu'aux résections osseuses majeures telles que la maxillectomie ou la mandibulectomie. Le caractère invasif de ces actes, a fortiori dans un contexte de douleur chronique, génère une douleur aiguë intense. Ces procédures sont parfois longues et souvent réalisées sur des patients âgés et de petit format, augmentant le risque de complications respiratoires, hémodynamiques, thermorégulatrices et/ou neurologiques. Un protocole associant une stratégie de prévention des risques avec une anesthésie générale combinée à des techniques locorégionales améliore significativement la qualité de l'anesthésie et de l'analgésie per- et postopératoire.
II. Évaluation pré-anesthésique
Contre toutes les idées reçues, les interventions de dentisterie sont tout sauf des anesthésies de routine. En chirurgie maxillofaciale, il est fréquent de recevoir des patients âgés souffrant de multiples comorbidités (endocrinopathies, cardiopathies, insuffisance rénale, etc.), des animaux brachycéphales ou des patients polytraumatisés. Un examen préanesthésique complet associé, au besoin, à un bilan sanguin biochimique et hématologique et une évaluation de la fonction cardiorespiratoire sont essentiels afin de caractériser les risques périopératoires et établir un plan de prévention adapté.
III. Risques anesthésiques et peropératoires spécifiques à la chirurgie maxillofaciale
1. Une gestion des voies aériennes délicate
L'intubation endotrachéale est évidemment indispensable pendant une anesthésie pour une chirurgie maxillofaciale / dentisterie. Le risque de fausse route et de bronchopneumonie est sévèrement accru, en raison de la présence de débris tissulaires, de saignements et de l'irrigation réalisée dans la cavité buccale. Le positionnement de la tête en situation déclive par rapport au reste du corps limite l'accumulation pharyngée des liquides d'irrigation ; l'utilisation d'un pack pharyngé retiré en fin d'intervention peut limiter la persistance de débris pharyngés au moment du réveil. Mais un contrôle pré-réveil systématique de la région pharyngée est indispensable pour s'assurer de la bonne perméabilité des voies aériennes avant le réveil.
L'intubation endotrachéale peut être difficile en cas de stomatite hyperproliférative, de sécrétions respiratoires abondantes, de trismus (impossibilité d'ouverture de la cavité orale), de masses orales volumineuses ou de traumatismes faciaux. La préoxygénation de 3 à 5 minutes avant induction augmente le temps avant désaturation en cas d'apnée ou d'obstruction respiratoire. Une bonne planification de l'intubation inclue l'accès immédiat aux outils d'aide à l'intubation : laryngoscope voire endoscope, lidocaine, spray, compresses, système d'aspiration, guide sonde à bout mousse, capnographe. Dans les cas les plus complexes, une intubation alternative telle qu'une trachéotomie doit être envisagée et préparée.
L'obstruction laryngo-trachéale est un risque majeur à considérer au moment de l'extubation lors de chirurgie invasive, d'inflammation étendue associée à un œdème tissulaire, ou de traumatisme facial. Le risque d'obstruction respiratoire est également important lors de réveil avec une mâchoire fixée en occlusion par une résine. Une extubation tardive sous surveillance des réflexes de déglutition doit être prévue.
Chez le chat, les risques liés à l'utilisation d'une sonde sont particulièrement fréquents en dentisterie. En cas de stomatite sévère, il est fréquent d'observer une obstruction subtotale voire totale per opératoire de la sonde d'intubation par un agrégat de sécrétions trachéales. La surveillance capnographique permet de rapidement détecter cette complication qui impose de changer, parfois à plusieurs reprises, la sonde trachéale.
La fragilité de la trachée féline expose à un risque accru de lésion ou de lacération trachéale lors des manipulations cervicales et de changement de décubitus. On préfèrera l'utilisation des sondes trachéales à ballonnet « grand volume et faible pression » (pression d'insufflation autour de 30 cmH20). Les changements de décubitus ne devront par ailleurs être réalisés qu'après déconnexion temporaire entre la sonde et le circuit anesthésique.
Pour certaines interventions maxillofaciales, le passage oral de la sonde trachéale est problématique (lors de chirurgie oncologique de résection large, l'évaluation précise de l'occlusion est indispensable). Dans ce cas, des intubations alternatives peuvent être réalisées, telles que la trachéotomie, la pharyngotomie ou l'intubation Trans mylohyoïdienne.
2. Le syndrome du pas-d'âne chez le chat
L'ouverture sous contrainte de la mâchoire, en particulier avec des pas d'ânes à ressort, engendre chez le chat une compression de l'artère maxillaire avec une ischémie cérébrale susceptible de conduire à des troubles neurologiques temporaires ou permanents (cécité, surdité, mortalité…).
Chez le chat, l'utilisation du pas-d'âne est donc à proscrire tout comme le maintien de l'ouverture buccale en position extrême, quel que soit le moyen employé.
3. Autres complications anesthésiques fréquentes
L'exposition buccale prolongée et l'irrigation à température ambiante favorisent l'hypothermie, en particulier chez les animaux de petit format. La prévention de l'hypothermie passe par le maintien au sec du patient par tout moyen imaginable. L'utilisation d'un récupérateur des eaux d'irrigation (baignoire, caillebotis…) sous la tête est un préalable. Le maintien de la normothermie doit être la règle et obtenu par des moyens actifs et agressifs de réchauffement du patient si nécessaire. En pratique, toute anesthésie d'une durée supérieure à 15 minutes doit impliquer la mise en place d'un moyen de réchauffement actif : tapis chauffant, soufflerie d'air chaud…
Le risque d'ulcère cornéen par exposition et dessication est connu chez le chien et le chat. Il est particulièrement vrai en chirurgie maxillofaciale ou les cornées sont largement exposées aux manipulations et projections diverses.
La douleur maxillofaciale et les contraintes appliquées aux mouvements de la face (bandages, résines, sondes diverses) sont souvent source de dysphorie de réveil, incluant des signes d'agitation, vocalises, panique voire automutilation. L'amélioration de la qualité du réveil passe par une analgésie soignée et l'administration de sédatifs à faible dose pour les patients les plus anxieux.
IV. Technique anesthésique et surveillance
Le choix des molécules d'anesthésie générale sera évidemment guidé par les caractéristiques physiologiques du patient et se conformera aux recommandations actuelles. Conformément aux recommandations de bonnes pratiques, l'intubation trachéale, le maintien d'une voie veineuse à demeure, une fluidothérapie adaptée au patient et le réchauffement du patient seront obligatoirement mis en place.
Un monitoring physiologique standard est recommandé (ECG, capnographie, SpO2, pression artérielle non invasive et température centrale). Il peut être compliqué de maintenir un capteur d'oxymétrie lingual pendant les interventions dans la cavité buccale. Des sites alternatifs peuvent être employés, tels que les oreilles, les doigts ou les plis interdigités, la vulve ou le fourreau. Une emphase particulière est à noter sur l'utilité de la capnographie dans la détection précoce des obstructions de la sonde trachéale chez le chat.
Les particularités de la technique d'anesthésie sont principalement relatives à la mise en œuvre de l'analgésie pour les douleurs périopératoires maxillofaciales comme nous allons le détailler ci-dessous.
V. Analgésie multimodale périopératoire
1. Analgésie systémique
L'analgésie multimodale repose sur l'association de plusieurs classes pharmacologiques, afin de réduire la dose et les effets secondaires de chaque agent. Dans le contexte périopératoire, l'association d'un AINS, d'un morphinique (agoniste complet des récepteurs tels que la morphine, le fentanyl ou la méthadone) et de techniques d'anesthésie locale est recommandée. Si la douleur est insuffisamment contrôlée par cette association, lorsque l'anesthésie locale est ineffective ou impossible notamment, ou lors de douleur chronique sévère, l'ajout d'analgésiques systémiques, le plus souvent utilisés en perfusion continue, peut être envisagée (kétamine, lidocaïne,(dex-)médétomidine, magnésium).
2. Blocs locorégionaux maxillo-faciaux
La réalisation d'une anesthésie locale sur un patient anesthésié permet de réduire considérablement les besoins en anesthésiques généraux et permet de produire une anesthésie remarquablement stable avec peu d'anesthésiques systémiques, quel que soit le degré invasif de la chirurgie. Selon la durée d'action des anesthésiques locaux sélectionnés, l'analgésie peut se prolonger pendant la période postopératoire et ainsi contribuer à améliorer le confort du patient au réveil.
L'insensibilisation du massif maxillofacial est réalisée par l'anesthésie du nerf trijumeau ou de ses différentes branches. L'anesthésie du nerf trijumeau nécessite un abord échoguidé dans l'espace rétro-orbitaire à réserver aux vétérinaires familiers de cette technique et de l'anatomie rétro-orbitaire. Plus superficielles et facilement accessibles à l'aide de repères anatomiques simples, les branches maxillaires et leur prolongement infra-orbitaire, et les branches mandibulaires sont couramment anesthésiées pour la réalisation des chirurgies maxillaires ou mandibulaires. (Figure 1) et (Figure 2)
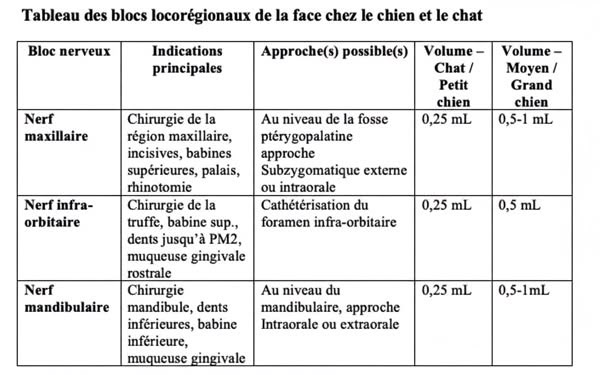
Figure 1
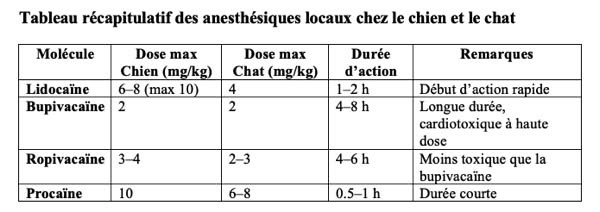
Figure 2
Les techniques d'anesthésie locorégionales sont rapides à maitriser avec une formation théorique et pratique appropriée. Les complications sont rares et incluent la formation d'un hématome péri-nerveux, un œdème local, l'injection intravasculaire entraînant une toxicité systémique (tremblements, convulsions, arythmies) et une neuropathie transitoire ou permanente en cas de geste intraneural. Un échec partiel peut survenir si la diffusion de l'anesthésique est insuffisante.
3. Analgésie postopératoire
L'analgésie post-opératoire repose sur l'administration d'anti-inflammatoires en première intention et de morphiniques si les anti-inflammatoires sont insuffisants.
L'hospitalisation est parfois nécessaire pour l'analgésie lors de douleur post-opératoire intense, afin d'administrer des morphiniques par voie parentérale. Lors de douleurs sévères et en particulier lors de douleur chronique préexistante, les adjuvants à visée anti-hyperalgésique tels que la kétamine peuvent être utilisés en perfusion continue.
L'analgésie postopératoire à domicile est basée principalement sur les AINS. En cas de contre-indication à l'usage des AINS classiques, d'autres analgésiques peuvent être employés bien qu'il n'existe que peu de données sur cet usage : le grapiprant peut être utilisé chez le chien ou le chat (hors AMM) et le paracétamol peut être envisagé chez le chien exclusivement.
Si la prise alimentaire est difficile ou impossible, une alimentation molle est à considérer. Dans les cas les plus extrêmes, il faut anticiper le risque d'anorexie et placer une sonde d'alimentation entérale pour permettre la réalimentation postopératoire rapide.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Anesthésie-analgésie en ophtalmologie
Vauxl Milieu France
Marcy L'étoile France
C'est dans le domaine de l'anesthésie pour les interventions ophtalmologiques que la triade anesthésique devient essentielle. Au cours de l'intervention, l'anesthésiste sera confronté à plus ou moins de difficultés selon le type d'intervention chirurgicale (extraoculaire ou intraoculaire), la nature de l'affection oculaire, l'état de santé du patient et l'existence ou non de maladies concomitantes. Dans tous les cas, assurer à nos patients l’hypnose, l’analgésie, et l’immobilité sont la règle, et d’extrême importance. Afin de respecter cette triade nous allons administrer des molécules qui vont avoir une répercussion, à un degré plus ou moins élevé, sur la pression intraoculaire (PIO), donc susceptibles de mettre en danger l’intégrité anatomique de l'œil de nos patients.
1. Une augmentation de la PIO peut entraîner une hémorragie intraoculaire ou un décollement de la rétine.
La capacité à influer sur la PIO est donc un élément très important de la prise en charge anesthésique en chirurgie ophtalmique. Malgré les effets de l'anesthésie sur la PIO étudiés depuis plus de 40 ans chez le chien, leur effet sur des sujets atteints d'affections oculaires reste encore inconnu.
2. De nombreux anesthésiques n’induisent pas de changements cliniquement significatifs de la PIO chez les chiens à yeux normaux.
3. L'effet de l'anesthésie sur la PIO chez les patients atteints de glaucome, par exemple, est moins préoccupant, car, si une augmentation de la PIO peut nuire à la fonction du nerf optique, ces patients en sont déjà affectés.
4. Les bloquants neuromusculaires ou curares peuvent être utilisés en ophtalmologie vétérinaire.
Ces médicaments agissent sur la plaque neuromusculaire en inhibant temporairement la contraction musculaire. Il en résulte une relaxation musculaire extrême qui empêche le patient de bouger, ainsi qu'une position centrale de l'œil, ce qui facilite la chirurgie.
Les muscles intercostaux ainsi que le diaphragme sont également affectés par l'utilisation de curares, provoquant chez le patient une hypoventilation sévère, voire une apnée. C'est pourquoi les patients qui reçoivent des bloquants neuromusculaires doivent bénéficier d'une assistance ventilatoire adéquate pendant toute la durée de l'intervention. Bien que le patient soit incapable de bouger, ces molécules n'ont aucun effet sur l'état d'hypnose et n'ont pas non plus de propriétés analgésiques. Un niveau anesthésique et une couverture analgésique adéquats doivent être obtenus par l'utilisation d'anesthésiques (injectables ou volatils) ainsi que d'analgésiques systémiques et/ou par l'utilisation d'une anesthésie locorégionale.
Avant le réveil de l'anesthésie, il est essentiel de s'assurer que les effets des curares ont complètement disparu de l'organisme, afin d'éviter une hypoventilation et une hypoxie. Pour ce faire, divers tests sont réalisés, tels que le «train of four » ou le « double burst » (à l'aide d'un neurostimulateur adapté), sans oublier la possibilité d'utiliser des agents de réversion.
Outre les médicaments anesthésiques, d'autres facteurs influencent la PIO :
- la production et surtout le drainage de l'humeur aqueuse ;
- le volume sanguin intraoculaire (qui est lui-même influencé par la pression artérielle, le tonus vasculaire et le retour veineux) ;
- la position du corps ;
- le tonus des muscles extra oculaires ;
- la rigidité de la tunique cornéo-sclérale ;
- la pression externe exercé directement sûr l’œil (une masse comprimant le globe ou le résultat des manipulations lors de l’examen ophtalmologique).
Bibliographie
- PiePierce-Tomlin T, Shaughnessy MR, Hofmeister EH. A systematic review of the effects of injectable sedative and anesthetic drugs and inhalant anesthetics on intraocular pressure in the dog. Vet Anaesth Analg. 2020 Mar;47(2):145-151. doi: 10.1016/j.vaa.2019.10.006. Epub 2019 Nov 14. PMID: 32014398.rce-Tomlin et al.
- Shilo-Benjamini Y, Pe'er O, Abu Ahmad W, Ofri R. Effect of anesthetic induction with propofol, alfaxalone or ketamine on intraocular pressure in cats: a randomized masked clinical investigation. Vet Anaesth Analg. 2023 Jan;50(1):63-71. doi: 10.1016/j.vaa.2022.11.005. Epub 2022 Nov 19. PMID: 36528512.
- Flaherty D, Auckburally A. Neuromuscular blocking agents. In: Duke-Novakovski T, de Vries M, Seymour C. BSAVA Manal of Canine and Feline Anaesthesia and Analgesia. 3rd Edition. BSAVA, 2016: 214-224.
- Jolliffe C. Ophtalmic surgery. In: Duke-Novakovski T, de Vries M, Seymour C. BSAVA Manal of Canine and Feline Anaesthesia and Analgesia. 3rd Edition. BSAVA, 2016: 258-271.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Apithérapie, un lien entre les abeilles et les soins vétérinaires en pratique canine. Un atout pour une pratique vétérinaire plus durable
Saint Martin De Crau, France
I. Introduction
La ruche est la plus petite et la plus complète des pharmacies naturelles. Les abeilles produisent essentiellement 6 produits :
3 produits sécrétés :
- La cire
- Le venin
- La gelée royale
3 produits transformés :
- La propolis
- Le miel
- Le pollen
II. Contexte historique et scientifique
Utilisée depuis que l'Homme côtoie les abeilles, l'apithérapie est tombée dans l'oubli en Europe, sauf peut-être pour l'utilisation du miel dans le soin des plaies. Depuis une trentaine d'années, des études scientifiques ont validé de nombreuses propriétés supposées des produits de la ruche. Leurs mécanismes d'action commencent même à être élucidés. Malheureusement, l'absence d'études in vivo, l'absence de protocoles de traitement clairs et la méconnaissance des critères qualité des produits freinent l'utilisation clinique des produits de la ruche.
III. Expérience pratique
Dans notre pratique quotidienne, nous utilisons les produits de la ruche quotidiennement avec des résultats surprenants. La plupart de nos modestes observations cliniques trouvent une explication dans les différentes études scientifiques publiées.
Nous avons commencé notre pratique d'apithérapeute en utilisant le miel dans le soin des plaies. Les résultats obtenus ont complètement modifié notre gestion des plaies. Les mécanismes d'actions sont maintenant bien connus, de nombreux vétérinaires réutilisent le miel dans cette indication. C'est souvent la seule qu'ils connaissent.
IV. Applications thérapeutiques
Les autres produits de la ruche ont de nombreuses indications intéressantes dans la recherche d'une pratique vétérinaire plus durable. Ils peuvent être utilisés seuls ou en complément d'une thérapeutique classique qu'ils potentialisent. Nous nous focaliserons par manque de temps sur la propolis. À partir de plusieurs cas cliniques, en pratique canine, représentatifs de pathologies difficiles à traiter, tels que maladies auto-immunes, entéropathies, diabète sucré, cancers ou infections bactériennes résistantes, nous pensons pouvoir montrer l'intérêt de cet outil thérapeutique.
Les pathologies choisies sont souvent problématiques pour les vétérinaires car les traitements préconisés ont de nombreux effets secondaires pour un résultat parfois décevant. Dans le cadre de nombreux cancers, les traitements de chimiothérapie sont souvent refusés et parfois mal tolérés. Dans ces indications, l'apithérapie est très intéressante seule comme traitement palliatif ou dans un protocole de thérapie intégrative.
V. Enjeux actuels
Enfin, l'antibio-résistance est une urgence sanitaire mondiale selon l'OMS, les propriétés anti-infectieuses des produits de la ruche, largement validées scientifiquement, ne demandent qu'à être exploitées.
VI. Perspectives et qualité
Il est cependant nécessaire d'utiliser des produits de qualité, pour espérer un effet thérapeutique reproductible. Il convient de valider les observations cliniques isolées par des études cliniques en double aveugle sur des populations statistiquement significatives, ce qui permettra de proposer des protocoles thérapeutiques faciles à utiliser par les praticiens vétérinaires. Enfin, l'utilisation à plus large échelle de l'apithérapie peut faire évoluer la filière apicole vers la production de produits de qualité thérapeutique plus valorisante pour l'apiculteur.
Ce ne sont pas les abeilles qui ont besoin de nous, c'est nous qui avons besoin d'elles !
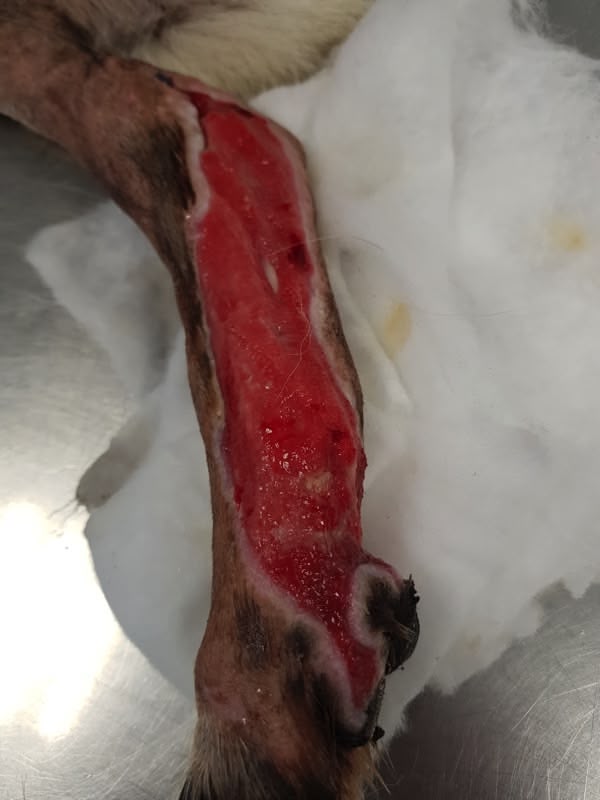
Photo 1 : Plaie par abrasion ancienne de la face interne du membre postérieur chez un Berger Belge.
Luxation ouverte du tarse stabilisée par ostéosynthèse avec irrigation intra-articulaire de propolis en solution hydroalcoolique. Pansements au miel. Antibiotérapie de très courte durée. Pas d'autre traitement.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Appliquer des exercices au cabinet sans hydrothérapie : plateforme de proprioception, tapis de marche sec, barres, plots, haricots
La Madeleine, France
I. Introduction
La physiothérapie joue un rôle majeur dans la récupération locomotrice des animaux présentant une paralysie. L'hydrothérapie est souvent conseillée, mais de nombreux vétérinaires n'y ont pas accès. Heureusement, il est possible de mettre en œuvre de nombreuses techniques en cabinet, en utilisant des outils simples comme ses mains, des coussins de proprioception, barres, plots, plateformes de proprioception, ou tapis sec. Ces exercices, bien ciblés, permettent de stimuler l'animal dans toutes les étapes de sa récupération neurologique, ils seront adaptés aux capacités fonctionnelles de l'animal.
II. Animal paralysé sans mouvements volontaires : stades IV et V
Lorsque l'animal ne présente aucune motricité volontaire et ne tient pas debout, l'objectif est double : prévenir les complications musculo-squelettiques liées à l'immobilité, et stimuler les voies nerveuses pour préparer la récupération.
1. Massages
Les massages doux des membres paralysés ont plusieurs effets bénéfiques :
- amélioration du flux sanguin périphérique, souvent réduit en cas d'immobilité ;
- préservation de l'élasticité des tissus mous (tendons, ligaments, muscles) ;
- stimulation proprioceptive et sensitive, via les mécanorécepteurs cutanés.
NB : Lors de paralysie postérieure, ne pas négliger les muscles des antérieurs. Les tensions musculaires excessives y sont fréquentes et peuvent générer des douleurs importantes. Les massages sont particulièrement indiqués pour soulager celles-ci.
2. Mobilisations passives
Les mobilisations articulaires douces (flexion/extension passive) sont essentielles pour :
- préserver l'amplitude articulaire ;
- prévenir les rétractions tendineuses, musculaires et les ankyloses ;
- stimuler les récepteurs articulaires et musculaires.
Réaliser ces mouvements de flexion extension lentement, sans forcer, 10 à 30 répétitions, articulation par articulation, 3 à 6 fois par jour.
3. Stimulation du réflexe de retrait
En pinçant entre les doigts, l'animal fléchit involontairement son membre, cela permet d'obtenir une contraction musculaire réflexe.
NB : Cette stimulation fonctionnera mieux sur un chien MNC, car lorsque l'animal est MNP les réflexes sont diminués ou absents.
4. Électrothérapie
L'électrostimulation neuromusculaire peut aider à préserver la force et le volume musculaire. Elle sera développée plus en détail dans une autre partie de ce module.
5. Stimuler station debout avec assistance
Positionner l'animal debout avec soutien permet de :
- stimuler les récepteurs posturaux et le tonus musculaire ;
- préparer la remise en charge des membres.
Utiliser un ballon, une serviette sous l'abdomen ou un harnais pour soulager partiellement le poids du corps. On incite doucement l'animal à pousser sur ses membres pour tenir debout.
III. Animal avec début de motricité, station debout avec soutien, non ambulatoire, stade III
Lorsque des mouvements volontaires réapparaissent, mais que l'animal ne marche pas encore, l'objectif est de favoriser l'activation posturale, l'équilibre et la proprioception.
1. Stimulation de la station debout avec assistance
Stimulation de la station debout avec assistance (ballon sous le ventre, harnais, treuil…), puis on essaie progressivement de retirer le soutien, pour encourager la stabilisation active.
2. Travail de l'équilibre et de la proprioception
En station debout, l'application de légères pressions latérales déséquilibre l'animal et stimule les ajustements posturaux. Au début, les exercices sont réalisés sur sol ferme, puis lorsque l'animal est à l'aise, on augmente la difficulté en les effectuant sur surface instable : coussin proprioceptif, plateau de Freeman, ballon (selon taille et stabilité de l'animal). Ce travail permet une réactivation des muscles posturaux profonds, essentiels à la station debout et à la marche.
3. Plateforme de proprioception motorisée
Les mouvements de la plateforme déplacent le centre de gravité de l'animal. Celui-ci doit procéder à un ajustement de sa position pour ne pas chuter. Cet ajustement fait intervenir toute la boucle de régulation de l'équilibre (récepteurs sensoriels proprioceptifs, intégration dans les centres nerveux, maintien de la posture par coordination des muscles agonistes-antagonistes).
4. Travail du report de poids
L'animal, ayant perdu de la motricité postérieure a tendance à transférer naturellement la majorité de son poids sur les membres antérieurs. Les exercices de report de poids servent à inciter l'animal à mettre en charge ses postérieurs :
Lever un antérieur ou positionner les antérieurs surélevés (step, marche) engage mécaniquement les postérieurs dans la stabilisation.
5. Marche assistée
La marche assistée constitue une étape clé dans la rééducation des animaux non ambulatoires :
- elle permet la mise en charge progressive des membres et de réactiver le schéma moteur de la marche ;
- elle permet de redonner confiance à l'animal, dans ses capacités motrices ;
- elle permet l'engagement actif du patient, même en cas de faiblesse importante.
Il est possible d'utiliser un harnais, une serviette ou un soutien manuel selon le gabarit de l'animal et son niveau d'autonomie, en veillant à ne pas porter tout le poids à sa place. L'animal doit être ralenti à l'aide d'une laisse et un collier ou harnais (ne pas faire la brouette avec l'animal !).
6. Tapis sec
Le tapis roulant sec est un outil utile pour renforcer la motricité et améliorer la coordination chez les animaux en rééducation :
- Il permet de travailler la régularité de la démarche dans un environnement contrôlé.
- Il favorise la symétrie des appuis et le report de poids vers les membres déficients.
- Il améliore l'endurance musculaire et la concentration grâce à un rythme de marche constant.
NB : Toujours commencer à faible vitesse, avec une surveillance rapprochée, pour éviter la fatigue ou la perte d'équilibre. Le travail en tapis permet de faire de la marche assistée plus facilement car l'animal reste sur place.
IV. Animal avec mouvements volontaires, subambulatoire à ambulatoire quelques pas stade II-III
À ce stade, l'animal commence à retrouver une autonomie partielle à la marche, mais reste fragile, il manque de coordination, et les chutes sont fréquentes. L'objectif est de renforcer la stabilité, donner confiance à l'animal, affiner les ajustements posturaux et améliorer la fluidité du mouvement.
1. Gestion du sol
Un sol non glissant est fondamental pour favoriser les progrès moteurs :
- il permet à l'animal de prendre appui plus facilement pour se mettre debout ;
- il facilite l'engagement actif des postérieurs, encore faibles ou hésitants ;
- il limite les risques de chutes et encourage des déplacements plus sûrs.
Utiliser des tapis antidérapants/tapis de gym ou dalles en caoutchouc dans les zones où l'animal passe fréquemment, éviter carrelage, lino ou surfaces trop lisses. Il est également possible à ce stade d'utiliser des chaussettes antidérapantes.
2. Travail de l'équilibre, de la proprioception et du report de poids
Vu dans le paragraphe précédent, ils restent fortement recommandés ; la difficulté/durée de ces exercices peut être augmentée à ce stade.
3. Cavalettis bas
Les barres au sol ou légèrement surélevées incitent l'animal à bien décomposer son mouvement et améliorent la qualité de la marche :
- élévation active des membres et contrôle des appuis ;
- travail de la coordination, de l'amplitude articulaire et du rythme.
Les cavaletti (3 à 5 barres) sont espacés de la longueur de l'animal pour débuter, et leur hauteur sera comprise entre le carpe et mi-radius de l'animal. On commence par 1 à 3 allers-retours, puis on augmente à mesure que l'animal progresse. Il est très important que l'animal passe les barres lentement, une patte après l'autre, sans sauter. L'aide d'une friandise est souvent très appréciée !
4. Marche en cercle
Tourner en cercle stimule la répartition du poids, sollicite les muscles fléchisseurs/extenseurs différemment selon le côté, et améliore l'équilibre dynamique et la fluidité du mouvement.
On commence les exercices en cercle avec de grands cercles pour faciliter les déplacements. Le diamètre est ensuite réduit progressivement pour augmenter la difficulté et solliciter davantage l'équilibre et la coordination.
5. Slalom
Le slalom entre des cônes permet un travail dynamique de flexion latérale du tronc et de proprioception. Ils aident l'animal à mieux gérer les changements de direction, souvent sources de chutes. Ils sont espacés de 1 à 1,5 fois la longueur de l'animal pour un passage fluide sans contrainte.
6. Assis debout
L'exercice assis-debout est un mouvement simple mais très efficace en rééducation fonctionnelle, il travaille la force de relevé dans les postérieurs. Il est à réaliser sur une surface non glissante, en guidant doucement l'animal si besoin. Commencer avec du soutien ou à mi-hauteur pour aider l'animal à se relever, peu de répétitions, puis augmenter progressivement selon l'endurance. Il est essentiel de vérifier que l'animal ait une position assise droite.
V. Animal ambulatoire avec ataxie stade II
Lorsque l'animal a retrouvé une marche fonctionnelle mais présente une ataxie résiduelle (incoordination, appuis irréguliers, postérieurs en extension), les exercices visent à affiner la précision motrice, améliorer la force et le contrôle volontaire du mouvement.
Tous les exercices précédents peuvent être proposés, en augmentant la difficulté (nombre de répétitions, intensité, durée, hauteur…).
1. Cavaletti hauts (hauteur coude max)
Relever les barres accentue la difficulté de l'exercice :
- sollicitation active des muscles fléchisseurs, souvent déficients en cas d'ataxie ;
- travail de la précision du mouvement et la conscience de l'espace (schéma corporel).
2. Parcours proprioceptif
Il est possible de combiner cavalettis (hauteur, sens différents…), coussins proprioceptif, dalles proprioceptives… Ceci augmente la difficulté et stimule davantage la coordination et le proprioceptif.
3. Travail avec ballon cacahuète
Positionner les antérieurs de l'animal sur un ballon en forme de haricot ou cacahuète, les postérieurs au sol :
- induit un transfert de poids vers l'arrière, encourageant l'engagement actif des postérieurs ;
- travaille la stabilisation dynamique du tronc ;
- stimule la proprioception et le gainage.
Le ballon est bloqué contre un mur pour éviter qu'il ne roule vers l'avant, on positionne les antérieurs sur le ballon (ne pas hésiter à maintenir l'animal au début s'il n'est pas à l'aise), et on peut appliquer de légers déséquilibres. Les sessions sont courtes : 30 s à 1 min plusieurs fois par jour.
4. Objectifs spécifiques à ce stade
- Réduire les pertes d'équilibre, les appuis hésitants et les erreurs de placement.
- Renforcer la coordination motrice.
- Améliorer l'anticipation et la précision du mouvement.
- Restaurer la confiance et l'autonomie en déplacement, y compris dans des environnements plus complexes.
VI. Conclusion
La rééducation d'un animal atteint de troubles neurologiques peut être menée de manière qualitative en cabinet, même si l'on ne dispose pas de l'hydrothérapie, grâce à des outils simples et bien ciblés. Du stade de paralysie sans mouvements à la reprise de la marche, chaque étape doit s'appuyer sur des exercices adaptés au niveau de récupération et à la tolérance de l'animal. Le travail au sol permet d'améliorer le tonus, la coordination, la proprioception et la confiance dans le mouvement. En combinant observation clinique, progressivité et engagement du propriétaire, ces protocoles optimisent les chances de récupération fonctionnelle.
Bibliographie
- MILLIS, D., & LEVINE, D. (2013). Canine rehabilitation and physical therapy. Elsevier Health Sciences.
- BOCKSTAHLER, B., WITTEK, K., LEVINE, D., MAIERL, J., & MILLIS, D. L. (2019). Essential facts of physical medicine, rehabilitation and sports medicine in companion animals. Munich, Germany:: VBS GmbH.
- OLBY, N., HALLING, K. B., & GLICK, T. R. (2005). Rehabilitation for the neurologic patient. Veterinary clinics: small animal practice, 35(6), 1389-1409.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Approche clinique des luxations de la rotule : diagnostic et orientation thérapeutique
Tours, France
I. Introduction
La luxation de la rotule correspond à un déplacement médial ou latéral de la rotule. Cette atteinte correspond la plupart du temps à une anomalie de développement.
Elle a été décrite dans toutes les races de chiens, les chats peuvent également être atteints bien que moins fréquemment décrits. La gêne clinique peut se révéler à tout âge et correspond à une boiterie assez typique. Lorsque la boiterie intervient tardivement, ou qu'elle est permanente, une atteinte concomitante du ligament croisé est à suspecter. Le lien entre luxation de rotule et atteinte du ligament croisé crânial secondaire souvent évoqué continue à faire débat. Les atteintes bilatérales sont rapportées entre 25 et 60 % des cas des atteintes congénitales de la luxation de rotule.
II. Ethiopathogénie et grading
La luxation médiale de rotule est plus fréquemment rencontrée chez les races naines mais aussi chez les races géantes, avec une origine congénitale et/ou développementale. La luxation latérale de rotule semble être plutôt rare chez les races de petit format et est alors souvent d'origine traumatique.
1. Luxation médiale de rotule chez les races naines
Dans ce type de races, la luxation médiale de rotule est une pathologie qu'on appelle « développementale » et non congénitale. En effet, la luxation en elle-même n'est pas présente dès la naissance, à la différence des déformations osseuses qui en sont à l'origine. L'origine de la luxation médiale de la rotule chez les chiens de petites races est le plus souvent due à un mauvais alignement du mécanisme extenseur du membre, dont notamment un varus du fémur ou du genou, une absence de développement de la trochlée fémorale, un déplacement médial de la tubérosité tibiale, une rotation interne du tibia, un varus du tibia proximal ou une torsion/rotation du tibia.
Chez les petites races de chien, la luxation est médiale dans 95 à 98 % des cas, alors que les luxations latérales ne représentent que 2 à 5 % des cas rapportés.
2. Luxation médiale de rotule chez les grandes races
Comme chez les races de petits formats, la luxation médiale de rotule chez le chien de grand format est encore partiellement incomprise. Il semblerait cependant que des malformations osseuses soient une nouvelle fois en cause dans cette pathologie. Chez les chiens de grands formats, une coxa vara ou une antéversion trop faible de la hanche seraient les deux malformations les plus souvent mises en cause. Dans la même idée que chez les petites races, ces anomalies entrainent un mauvais alignement du mécanisme extenseur du membre et de tout le quadriceps.
La luxation médiale est nettement plus fréquente que la luxation latérale, même chez les grandes races (+/- 67 à 81 % des cas de luxation médiale).
Une cause plus fréquente de luxation médiale de rotule chez les chiens de grandes races est l'atteinte postopératoire en tant que complication secondaire à une chirurgie de rupture du ligament croisé crânial.
3. Luxation latérale de rotule chez le chien
La luxation latérale de rotule intervient le plus souvent chez les grands chiens, et est assez rare chez les races de petit format. Elle est également décrite lors de luxation de rotule bidirectionnelle, c'est-à-dire aussi bien latérale que médiale. Des malformations osseuses sont encore une fois à l'origine de cette atteinte, et regroupent cette fois-ci la coxa valga, une augmentation de l'angle d'antéversion et un genu valgum.
En effet, chez la luxation latérale de rotule semble avoir la représentation suivante :
- Petites races : 2 % des cas seulement.
- Races moyennes : 17 % des cas de luxation de rotule sont latérales.
- Grands formats : 37 % des cas sont des luxations latérales de rotule.
4. Grading des luxations de rotule chez le chien
Un grading existe afin de permettre à toute la communauté vétérinaire de parler un langage commun, international, et compréhensible par tous.
Le grade I est souvent une découverte fortuite, lors d'un examen de routine et n'est pas par définition associé à une gêne clinique ou une boiterie. Dans ce type de cas, la rotule est luxable manuellement.
Le grade II représente une luxation spontanée qui s'exprime par des signes cliniques, avec une boiterie typique de démarche à cloche-pied.
Le grade III est une luxation permanente de la rotule, qui peut encore être réduite manuellement. Ce grade est souvent lié à de nombreuses malformations osseuses. La boiterie est souvent permanente avec une position semi-fléchie du membre, associée à une rotation interne.
Le grade IV est une luxation permanente dont la luxation médiale de rotule est alors non réductible. Le tibia est souvent en rotation interne marquée.
III. Quel bilan lésionnel doit être réalisé ?
Il a été souvent décrit des déformations osseuses et malformations angulaires en lien avec le grading précédemment cité. Cependant, chaque cas doit avoir son évaluation des malformations et répercussions osseuses de la luxation de rotule, et chaque cas doit faire l'objet d'un examen orthopédique clinique approfondi. L'examen clinique est nécessaire dans la démarche diagnostique, notamment pour déterminer le grading de la luxation de rotule. Cet examen permet également de pouvoir évaluer et/ou anticiper la présence d'une lésion du ligament croisé crânial concomitante à la luxation de rotule. Ceci pouvant déjà être clairement suspecté pendant l'anamnèse et la description de la boiterie par les propriétaires.
L'examen clinique orthopédique commence toujours par l'évaluation de la démarche et de l'éventuelle boiterie. La réalisation de cette évaluation dans un couloir ou dans un espace suffisamment grand en extérieur est recommandée. Une évaluation clinique de la démarche au pas, puis à la course est recommandée. L'examen rapproché doit être réalisé sur patient debout afin notamment d'évaluer les symétries musculaires et osseuses. L'évaluation de la position naturelle de la rotule est très importante. Dans certains cas, et notamment dans des cas de luxation de rotule avancée et/ou chronique, la palpation de la rotule peut être rendue difficile par son mauvais positionnement ou l'inflammation périarticulaire marquée. La position de la crête tibiale peut également être évaluée à ce stade. En cas de luxation de rotule permanente (grade 3 et 4), une tentative de réduction de la luxation de la rotule est indispensable afin de préciser le grading.
En ce qui concerne les éventuels examens complémentaires à réaliser, l'examen radiographique est actuellement l'examen le plus simple à réaliser et qui permet une excellente évaluation des anomalies liées à la luxation de rotule. Cet examen permet notamment d'évaluer les malformations osseuses pouvant induire une luxation de rotule. La réalisation d'un examen radiographique normal, avec une rotule en place, ne permet bien évidemment pas d'écarter une luxation de rotule, qui est par essence même une pathologie dynamique. Les vues de face et de profil du grasset, du fémur et du tibia doivent être réalisées à minima. Une vue « Skyline » du fémur, c'est-à-dire une vue tangentielle de la trochlée fémorale peut être réalisée afin d'estimer la profondeur de la trochlée fémorale.
Se développant de plus en plus, l'examen tomodensitométrique peut être conseillé pour évaluer toutes ces affections. Dans les cas de déformations osseuses avérées, cet examen complémentaire doit même être recommandé. Le scanner permet notamment d'avoir une meilleure compréhension et visualisation des déformations osseuses. Cette évaluation peut se faire par la modélisation 3D virtuelle informatique du membre, ou parfois dans certains cas via la modélisation par impression 3D, d'après les images du scanner, du membre et des déformations osseuses. Cette approche améliore la partie diagnostique, mais également la prise en charge thérapeutique du patient. En effet, la modélisation 3D améliorer l'anticipation des techniques chirurgicales, peut permettre de prémodeler des implants, et peut surtout apporter un gain de temps chirurgical non négligeable.
IV. Quand décider d'intervenir chirurgicalement ?
Le grading permet également de définir l'atteinte qui peut ou non nécessiter une intervention chirurgicale. L'atteinte est classée en fonction de sa sévérité, du grade 1 à 4, une indication de prise en charge chirurgicale est assez consensuelle à partir du grade 3. Les grades 2 sont traités lors de gêne clinique fréquente, l'âge du patient est aussi à considérer. En résumé, dès qu'une boiterie est mise en évidence, cette atteinte doit faire l'objet d'une suggestion de prise en charge chirurgicale. Le grade 2 est donc le grade dont l'intervention est à clairement discuter entre la balance bénéfices-risques liée à l'intervention chirurgicale.
La réussite du traitement chirurgical dépend de la bonne évaluation des anomalies à corriger et de la capacité à correctement réaligner l'axe mécanique du grasset. Les différents critères objectifs à prendre en compte sont le degré de malformation osseuse, la présence d'arthrose, et la présence d'instabilité articulaire.
Les décisions chirurgicales les plus compliquées à prendre résident le plus souvent chez des patients très jeunes, qui ont encore un potentiel de croissance élevé. Toutes les techniques relevant de changements osseux doivent être réellement débattues avant leur mise en œuvre, notamment au regard de leur impact sur les cartilages de croissances distal du fémur ou proximal du tibia. Dans ce type de cas, une prise en charge en deux étapes est souvent recommandée.
V. Techniques chirurgicales
Les différentes techniques décrites ,utilisées seules mais le plus souvent combinées, sont :
- Creusement de la trochlée fémorale : chondroplastie (élévation cartilagineuse possible uniquement chez le très jeune animal), sulcoplastie (abrasion cartilagineuse), trochloplastie (élévation de la trochlée incluant la partie cartilagineuse et sous-chondrale) en coin ou en bloc.
- Relâchement rétinacle/capsule para-patellaire (desmotomie).
- Remise en tension de la capsule/rétinacle controlatéral (imbrication).
- Suture anti-rotatoire fabello-rotulienne.
- Relâchement musculaire : quadriceps et portion crâniale du sartorius notamment.
- Transposition de la tubérosité tibiale.
- Correction angulaire distale du fémur distal par ostéotomie/ostectomie en coin.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Approche d'une maladie chronique: exemple du parcours oncologique
Ploemeur, France
I. Introduction
Les maladies chroniques se définissent par une évolution lente, sans tendance à la guérison, nécessitant un suivi au long cours. Elles sont souvent associées à des notions négatives comme la dépendance à un traitement parfois quotidien, l'impact sur la qualité de vie de l'animal comme sur celle de son propriétaire, l'existence de complications, la diminution potentielle de l'espérance de vie, etc. Les maladies chroniques incluent des affections fréquentes en pratique vétérinaire (maladie rénale chronique, cardiopathies, endocrinopathies, épilepsie, maladies dysimmunitaires, dermatite atopique, etc.) et le cancer en constitue un exemple à part entière. Si nos animaux vivent de plus en plus longtemps, ils partagent notre environnement et sont exposés aux mêmes agents cancérogènes que nous. Un chien sur quatre et un chat sur cinq développeront un cancer au cours de leur vie, représentant près de 50% des causes de mortalité chez les animaux de plus de dix ans. La prise en charge de ces maladies dépasse le cadre médical. Elle engage une relation tripartite entre l'animal, le propriétaire et le vétérinaire, dans laquelle la dimension psychologique joue un rôle déterminant.
II. Le lien propriétaire–vétérinaire dans le parcours oncologique
Le vétérinaire n'est pas seulement celui qui établit le diagnostic et qui prescrit le traitement, il accompagne le propriétaire tout au long du parcours.
L'annonce du cancer constitue une étape majeure. Elle nécessite empathie et pédagogie, en évitant un langage trop technique ou anxiogène.
La deuxième étape du parcours correspond aux décisions thérapeutiques, qui reposent aujourd'hui sur une offre large et multimodale : chirurgie, radiothérapie, chimiothérapie à dose maximale tolérée ou métronomique, thérapies ciblées, immunothérapie, électrochimiothérapie ou thérapies complémentaires. La prise en charge de la douleur a beaucoup progressé et les praticiens de première ligne peuvent désormais s'appuyer sur des spécialistes pour les cas les plus complexes. Mais l'objectif doit être clarifié : guérison (souvent inaccessible), contrôle ou stabilisation, ralentissement de la progression de la maladie, augmentation de l'espérance de vie ou encore préservation du confort et de la qualité de vie. Une autre manière de présenter les objectifs du traitement est d'expliquer au propriétaire que l'on va faire en sorte de faire disparaître les symptômes de la maladie (amaigrissement, troubles digestifs, troubles de l'appétit, boiterie /douleur, plaie, difficultés respiratoires, crises convulsives, dysurie, dyschézie, etc.). Cette étape confronte également le propriétaire à des critères éthiques et financiers.
Enfin, l'alliance thérapeutique constitue un pilier central. Le vétérinaire doit être à l'écoute du propriétaire. La co-construction du plan de soins est essentielle. Propriétaire et vétérinaire doivent s'accorder sur les objectifs du traitement et sur ses contraintes (coût, réalisation, effets secondaires, visites régulières chez le vétérinaire) avant d'entamer les soins. C'est l'étape qui impacte le plus psychologiquement le propriétaire, d'où l'importance de la détailler et de la chiffrer (devis) avec précision. Des outils (grilles d'évaluation) permettent d'impliquer activement le propriétaire et permettent de mesurer l'efficacité du traitement, la gestion de la douleur, la qualité de vie et aident le duo vétérinaire / propriétaire à adapter ses décisions. Le suivi doit être continu avec des rendez-vous permettant d'ajuster la prise en charge, d'accompagner les doutes et les contraintes, et de vérifier l'adéquation entre l'évolution de la maladie et les objectifs fixés.
III. Le propriétaire et l'impact de son rôle d'aidant
Lorsqu'un cancer est diagnostiqué, la relation affective et quotidienne du propriétaire avec l'animal est bouleversée. Le propriétaire devient un proche aidant. Il administre les traitements (contrainte organisationnelle, technique, psychique), gère les symptômes (douleur, amaigrissement, troubles digestifs, crises, plaies, troubles respiratoires), supporte une charge émotionnelle importante (peur, tristesse, impuissance, anxiété, stress), et subit le coût des traitements et des suivis. À ces contraintes s'ajoute souvent un deuil anticipé : le propriétaire sait que le temps est compté et que, tôt ou tard, la maladie évoluera et l'animal décédera. Cette conscience génère une souffrance particulière, faite de tristesse projetée, d'angoisse de la séparation et parfois de culpabilité.
La qualité de vie du propriétaire est affectée dans ses dimensions psychologique, physique, sociale, temporelle et financière, proportionnellement à la sévérité de la maladie de l'animal. L'attente et l'incertitude face à l'évolution de la maladie engendrent un état de vigilance permanente, proche de celui décrit chez les aidants humains : sommeil perturbé, isolement social, épuisement émotionnel, difficultés à maintenir les activités quotidiennes habituelles. Le ressenti du propriétaire conditionne directement la continuité des soins et l'adhésion thérapeutique. Mais il influence aussi la qualité de la relation à l'animal, car l'anxiété, la peur de mal faire ou la projection de la perte peuvent altérer le vécu partagé des derniers mois. En outre, selon les personnalités et les profils des propriétaires, les réactions face au cancer varient. Certains se montrent combatifs, d'autres pragmatiques, anxieux ou en retrait. Bien connaître le propriétaire permet d'adapter son discours, de garder la confiance et de favoriser l'adhésion.
IV. Accompagner jusqu'au bout
La question de la fin de vie fait partie intégrante du parcours oncologique. Elle doit être anticipée pour éviter les décisions prises dans l'urgence, sous le coup de la douleur ou de la culpabilité. Mais savoir quand aborder le sujet reste délicat : trop tôt, le risque est de susciter un rejet de la part du propriétaire, effrayé par une perspective qu'il n'est pas prêt à envisager ; trop tard, on prive la famille de repères clairs pour préparer sereinement la toute fin de vie.
Définir avec le propriétaire des critères objectifs de qualité de vie (évaluation de la douleur, maintien de l'appétit, autonomie, interactions sociales) permet de donner des points d'appui concrets. Ces repères évitent l'acharnement thérapeutique et aident à choisir le moment où les traitements n'apportent plus de bénéfice réel pour l'animal. Cela permet également de prévenir les regrets ultérieurs, fréquents lorsque les familles ont le sentiment d'avoir prolongé inutilement la souffrance.
Un autre enjeu survient lorsque les attentes divergent : le vétérinaire peut estimer que les soins restent raisonnables et adaptés, alors que le propriétaire exprime le souhait d'une euthanasie. Ces situations génèrent souvent un malaise éthique et un sentiment d'échec pour le praticien. La tentation est grande de convaincre à tout prix, mais il est essentiel de rappeler que la décision finale appartient au propriétaire, dans le respect de son vécu, de ses valeurs et de ses contraintes. Le rôle du vétérinaire est alors d'expliciter les alternatives possibles (soins palliatifs, ajustements thérapeutiques, suivi de la qualité de vie), tout en gardant une évaluation objective de la souffrance animale. Malgré tout, certains propriétaires choisiront une euthanasie anticipée. Reconnaître cette réalité, l'accueillir sans jugement et préserver la relation de confiance fait aussi partie de la mission vétérinaire.
V. Conclusion
Le cancer illustre la complexité des maladies chroniques vétérinaires : une prise en charge médicale exigeante, mais aussi un impact profond sur la qualité de vie du propriétaire. Ce dernier est un acteur central. L'alliance thérapeutique, basée sur l'écoute, la co-décision et l'adaptation au profil du propriétaire, constitue la clé d'un accompagnement réussi jusqu'à la fin de vie. Le vétérinaire doit trouver un équilibre entre soins de l'animal et accompagnement humain. Dans le cadre du cancer, la démarche est souvent palliative : elle vise à préserver une qualité de vie acceptable, tant pour l'animal que pour son propriétaire.
Bibliographie
- BELSHAW Z., DEAN R.S., ASHER L. Quality of life assessment in domestic dogs: An evidence-based rapid review. Vet J. 2020;263:105524.
- DEELEN, MEIJBOOM, TOBIAS, KOSTER, HESSELINK, RODENBURG. Handling End-of-Life Situations in Small Animal Practice: What Strategies do Veterinarians Contemplate During their Decision-Making Process? Journal of Applied Animal Welfare Science, 2023; DOI: 10.1080/10888705.2023.2268516.
- GAGNAIRE Z. Impact d'une maladie chronique d'un chien ou d'un chat sur la qualité de vie de son propriétaire. Thèse de doctorat vétérinaire, Université Claude Bernard Lyon 1, 2023.
- KNESL O, HART BL, FINE AH, COOPER L, PATTERSON-KANE E, HOULIHAN KE, ANTHONY R. 2017. Veterinarians and humane endings: when is it the right time to euthanize a companion animal? Frontiers in Veterinary Science.
- MATTE AR, KHOSA DP, COE JB, MEEHAN MP. 2019. Impacts of the process and decision- making around companion animal euthanasia on veterinary wellbeing.VetRecord.
- Shaw and Lagoni, End-of-life communication in veterinary medicine: delivering bad news and euthanasia decision making, Veterinary clinics: small animal practice, 2007; 37(1): 95-108.
- SPRINGER S, AXIAK FLAMMER S, DÜRNBERGER C. Veterinary medicine is not finished when I have diagnosed an incurable disease, that's when it starts for me. Frontiers in Veterinary Sciences. 2024; 11:144040.
- TESTONI I., De Cataldo L., RONCONI L., COLOMBO E.S., STEFANINI C., DAL ZOTTO B., ZAMPERINI A. 2019. Pet grief: tools to assess owners' bereavement and veterinary communication skills. Animals.
- WITHROW S.J., VAIL D.M., PAGE R.L. Withrow and MacEwen's Small Animal Clinical Oncology. 6th ed. St Louis : Elsevier, 2019.
Liens d'intérêt : Pour Marie Cibot : Solâme, entreprise vétérinaire dédiée à l'accompagnement de la fin de vie des animaux
📃 Approche du client mécontent : gestion de la colère, établir des barrières
La Seyne-Sur-Mer, France
Paris, France
I. Introduction
Les incivilités et agressions envers les vétérinaires connaissent une progression constante. [1]
En 2023, 470 déclarations ont été enregistrées par l'Ordre national, soit un ratio de 2,25% des inscrits et une augmentation de plus de 50% par rapport à 2022. Les femmes représentent 65,3% des déclarations et les auxiliaires sont impliqués dans près de 35% des faits. En 2025, les chiffres ont encore progressé. Si la majorité des incidents sont classés comme « sans gravité » sur le plan factuel, ils sont vécus comme graves ou extrêmement graves dans plus de 80% des cas, avec des conséquences émotionnelles significatives (choc, anxiété, troubles du sommeil, colère). [2]
II. Contexte sociétal et évolution du lien humain-animal
Cette augmentation du mécontentement s'inscrit dans un contexte sociétal marqué par l'évolution du lien entre les humains et leurs animaux compagnons. Le développement du pet-parenting, c'est-à-dire le fait de considérer son animal comme un membre de la famille, voire comme un enfant, augmente les attentes, parfois irréalistes, des clients vis-à-vis des vétérinaires et de leur équipe. La bibliographie scientifique souligne que les défauts de communication sont l'une des principales causes de plaintes et que la relation de soins doit être centrée sur un partenariat actif (en anglais : relationship-centered care).
III. Situations génératrices de tensions
Les situations génératrices de tensions sont diverses (voir tableau 1) : désaccord thérapeutique, pronostic défavorable, coût jugé excessif, délais d'attente, manque de confiance, échec thérapeutique, décès ou euthanasie, ou encore suspicion d'erreur médicale. Certaines configurations, comme les conflits familiaux préexistants ou les attentes divergentes entre proches, constituent des contextes à haut risque. La perception de difficulté varie selon l'expérience, les traits de personnalité et l'état psychologique du praticien.
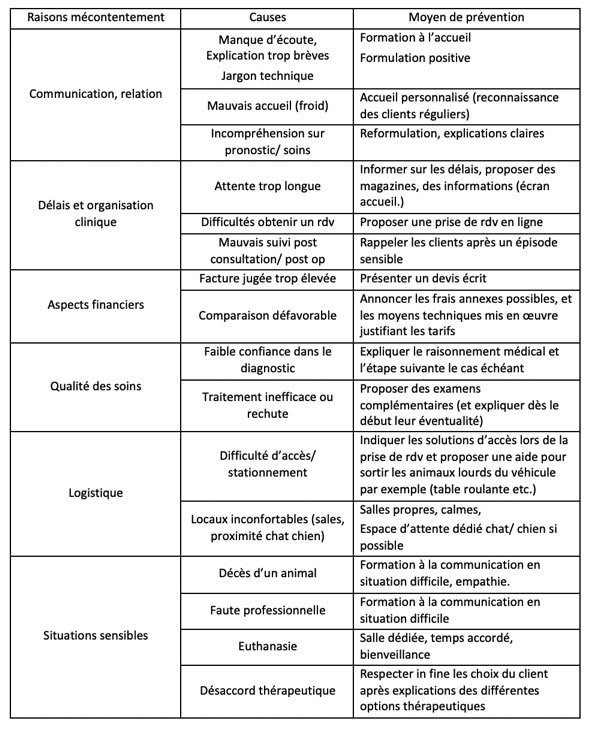
Tableau 1
IV. Gestion du client mécontent
La gestion du client mécontent repose sur deux piliers [3,4] :
1. Gérer la colère
Adopter une posture non-verbale contenante (distance, voix posée, gestes mesurés), reconnaître l'émotion sans entrer dans la confrontation, recentrer la discussion sur un objectif commun : le bien-être de l'animal. Utiliser la reformulation et l'empathie calibrée pour valider la difficulté perçue, tout en évitant les promesses irréalistes. Favoriser les questions ouvertes pour permettre au client de narrer sa version ou son histoire. Rester sincère et honnête. Protéger également son équilibre émotionnel grâce à des pauses, relais d'équipe et préparation des entretiens sensibles.
2. Poser un cadre clair
Expliciter les responsabilités et les limites professionnelles, présenter les options médicales et leurs coûts (devis, frais annexes), définir les règles de communication (interlocuteur unique, canaux privilégiés), assurer une traçabilité écrite des échanges et des décisions. En cas de non-respect du cadre, savoir orienter ou mettre fin au contrat de soins.
V. Prévention
La prévention s'appuie sur [5] :
- Avant/pendant la consultation : accueil personnalisé, gestion proactive des attentes (horaires, délais), langage accessible, explication du raisonnement médical et des étapes à venir, vérification des contraintes et valeurs du client.
- Après la consultation : assurer un suivi actif et personnalisé, par exemple en contactant le propriétaire après une intervention chirurgicale, un soin lourd ou un événement sensible (mauvaise nouvelle, changement de traitement, incident). Proposer des outils pratiques comme la prise de rendez-vous en ligne pour faciliter l'accès aux soins. Maintenir un interlocuteur unique au sein de la clinique (vétérinaire ou auxiliaire référent) pour centraliser les échanges et éviter les messages contradictoires ou répétés.
- Situations sensibles : prévoir un environnement adapté (salle dédiée pour l'euthanasie), un temps suffisant, la présence d'un second professionnel, et orienter vers des ressources d'accompagnement au deuil ou de soutien psychologique.
VI. Protection professionnelle
La protection de soi est une compétence professionnelle à part entière : elle inclut l'organisation interne (briefings/débriefings, relais), la formation continue en communication et gestion des conflits, la supervision, ainsi que le recours aux dispositifs d'aide existants (SPS, Vétos-Entraide). La formation initiale des vétérinaires dans ce domaine doit être encouragée.
VII. Messages clés
- Le mécontentement est fréquent et émotionnellement coûteux : il nécessite un travail simultané sur le cadre, la communication et la protection de l'équipe.
- La relation centrée sur le partenariat améliore l'adhésion du client, à condition de savoir poser des limites.
- Les profils à risque et situations sensibles peuvent être anticipés ; des protocoles simples de désescalade et de suivi doivent être intégrés à la pratique.
- La protection de soi et de l'équipe est indispensable pour préserver la qualité des soins et la santé professionnelle.
Bibliographie
- BISMARRE C. "Observatoire des agressions et incivilités : bilan de l'année 2023. Revue de l'ordre national des vétérinaires, 2024, 90, p8-9
- TRUCHOT D." La santé des vétérinaires français : une approche longitudinale". CNOV & Vétos-Entraide, 2024, 109p.
- SHAW J.R., « Four Core communications skills of highly effective practitioners", Vet Clin Small anim 36 (2006), 385-396
- DUNAND M. "Typologie des profils psycho-sociaux des clients perçus comme difficiles". Thèse d'exercice, ENVT, 2018, 197P.
- MAHÉ F. "Les situations difficiles en clientèle vétérinaire", École Nationale Vétérinaire de Nantes, conférence, 26 mars 2003.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Approche du deuil et de l'euthanasie avec les enfants
Ploemeur, France
I. Introduction
L'euthanasie d'un animal de compagnie représente un moment singulier, à la croisée de la médecine vétérinaire, de l'éthique et de la psychologie. Les familles qui traversent cette expérience vivent un bouleversement émotionnel majeur. Lorsqu'un enfant est présent au sein de la famille, la complexité s'accroît : comment expliquer la maladie, la mort, l'euthanasie ? Faut-il protéger l'enfant de la douleur en l'écartant, ou au contraire lui donner la possibilité d'être acteur de cette étape ? Les enfants sont des membres à part entière de la cellule familiale et construisent, eux aussi, un lien affectif souvent très fort avec l'animal. Reconnaître leur place et les accompagner de manière adaptée est essentiel, tant pour l'équilibre psychologique de l'enfant que pour la qualité de la relation entre le vétérinaire et la famille.
II. Deuil animalier chez l'enfant
Le deuil est un processus d'adaptation psychologique, émotionnelle et sociale à la perte d'un être cher. Chez l'adulte, il s'exprime par des réactions multiples : tristesse, colère, culpabilité, désorganisation, fatigue, parfois soulagement. Le modèle théorique décrit un processus en plusieurs étapes non linéaires. Chez l'enfant, les manifestations sont particulièrement hétérogènes. Elles peuvent être émotionnelles comme chez l'adulte mais aussi comportementales (opposition, troubles du sommeil, plaintes somatiques, etc.). La forme que prend le deuil dépend de la maturité, de la culture familiale et du degré d'attachement à l'animal. Ces réactions peuvent surgir immédiatement après la mort ou à distance, après un temps de latence.
Chez l'enfant, le vécu du deuil dépend aussi directement du développement cognitif et affectif. Avant l'âge de 3 ans, les enfants ont une compréhension limitée de la mort malgré le fait qu'ils puissent ressentir la perte d'un être cher. Entre 3 et 6 ans, les jeunes enfants commencent à développer une compréhension plus concrète de la mort, mais elle est souvent perçue comme évitable et teintée de pensée magique. L'enfant peut poser les mêmes questions à répétition, ou s'attendre au retour de l'animal. Les enfants d'âge scolaire (6-10 ans) commencent à développer une compréhension plus complexe de la mort. La mort est perçue comme un événement réel, mais parfois « contagieux » ou causé par des comportements. Les enfants peuvent se sentir responsables de la mort de l'animal. Les adolescents ont généralement une compréhension plus mature de la mort et qui se rapproche de celle des adultes mais ils peuvent avoir des réactions émotionnelles intenses. Les adolescents peuvent commencer à explorer des questions existentielles et philosophiques liées à la mort.
Du point de vue développemental, l'aspect biologique de la mort se structure chez l'enfant, autour de sous-concepts qui ne sont donc pas acquis simultanément : l'irréversibilité (souvent le premier aspect compris, vers 3 ans) ; l'inévitabilité (tous les êtres vivants meurent) ; l'applicabilité (seules les choses vivantes peuvent mourir) ; la cessation (toutes les fonctions corporelles s'arrêtent après la mort) ; la causalité (la mort résulte de la rupture des fonctions vitales, généralement acquise autour de 8 ans).
La spécificité du deuil animalier réside dans l'intensité du lien affectif, parfois fusionnel, et dans l'absence de rituels sociaux codifiés. L'euthanasie, acte volontairement choisi conjointement par la famille et par le vétérinaire, introduit une dimension supplémentaire : les enfants doivent intégrer que la mort a été « décidée », ce qui peut générer des questionnements éthiques précoces.
III. Soignant, quelle posture adopter ?
Il reste fréquent de vouloir « protéger » les enfants en les excluant des conversations et des décisions liées à la fin de vie animale. Les données actuelles montrent pourtant que l'exclusion peut accentuer l'angoisse et générer des malentendus. La posture recommandée est donc d'intégrer les enfants, selon leur âge et leur maturité, dans le processus d'accompagnement. Parler de la maladie et de la mort avec un enfant, c'est lui offrir la possibilité d'exprimer ses émotions, de poser ses questions, et de se sentir légitimé dans son lien avec l'animal. Cela demande une posture d'écoute, d'ouverture, et une capacité à accueillir ses mots parfois déconcertants. Toutefois, chaque enfant, chaque relation à l'animal et chaque deuil sont singuliers : l'accompagnement doit donc se modeler au cas par cas.
L'échange avec l'enfant repose sur une vérité sans détour et sur des formulations adaptées à son vocabulaire. Il est possible de nommer les choses avec des mots doux, accessibles et exacts. Plus l'enfant est jeune, moins il est pertinent de multiplier les détails. L'objectif, pour les parents comme pour le vétérinaire, est d'identifier ce qu'il souhaite savoir, d'accueillir ses questions et ses ressentis. La qualité de présence des adultes est centrale : avec l'accord des parents, l'équipe soignante peut apporter un appui pour clarifier ce moment. Dire que « le chien est parti » ou qu'il « s'est endormi » peut créer de la confusion, voire des peurs irrationnelles (par exemple peur du sommeil). Employer le mot « mort » et expliquer simplement l'euthanasie (« Je suis vétérinaire et je vais aider Coca à mourir. Je vais donner à Coca une injection remplie de médicament qui va arrêter son cœur, tout doucement. Quand son cœur s'arrêtera, elle ne pourra plus respirer toute seule. Rassure-toi, elle ne ressentira aucune douleur. ») permet de poser un cadre clair et rassurant. Le vétérinaire peut également, dans une juste mesure, reconnaître ses propres émotions. Cette authenticité nourrit la relation de confiance. L'important est de maintenir une posture contenante : accueillir la tristesse des enfants sans se laisser déborder par la sienne.
En outre, la maturation de ces notions s'effectue par l'exposition médiatique et artistique (livres, podcasts, dessins animés, etc.) et la communication parentale. Aussi, il est important d'inciter les parents à échanger en amont avec leurs enfants pour les préparer au décès de l'animal et pour honorer les liens qui les unissent.
IV. Accueillir et accompagner les enfants dans sa structure vétérinaire
Dès les consultations d'annonce et de soins palliatifs, l'enfant peut participer aux discussions entre la famille et l'équipe vétérinaire. Toutefois, l'implication d'un enfant consiste à lui donner une place et une voix, non la responsabilité du choix. Ainsi, on pourra par exemple expliquer à un enfant que : « Quand un animal souffre, nous pouvons choisir de l'aider à mourir. C'est un choix très difficile et qui amène beaucoup de tristesse pour toute ta famille. Mais c'est un choix auquel nous devons réfléchir, tes parents et moi, car Chipie est très malade et on ne souhaite pas qu'elle souffre. Tu peux poser toutes tes questions et nous dire ce que tu souhaites pour lui dire au revoir ».
Le jour de l'euthanasie, la présence d'enfants doit être anticipée. Assister à ce dernier moment peut rassurer l'enfant sur ce que signifie réellement l'euthanasie et la mort de son animal. La réalité et l'irréversibilité de la mort deviennent alors concrètes. Deux écueils sont néanmoins à prévenir : qu'un jeune enfant interfère avec la procédure, et qu'il ne garde que cette ultime image de son animal. D'où l'importance de proposer sans imposer : les parents offrent l'option et soutiennent l'enfant dans son choix, quel qu'il soit. Si les enfants sont présents, leur préparer un espace dédié (un fauteuil, un coussin, un jouet, du papier et des crayons, une housse funéraire à décorer, des fleurs à mettre dans la housse) leur permet de trouver une place adaptée à leur âge. Permettre à l'enfant de dire au revoir, de caresser ou de parler à l'animal fait partie intégrante du processus. Certains enfants souhaitent être présents tout du long, d'autres préfèrent entrer et sortir. Enfin, la présence peut aussi être symbolique, via une peluche, un dessin ou un objet déposé auprès de l'animal.
L'équipe vétérinaire peut aussi assez facilement proposer des rituels. Ils aident à symboliser la séparation et à inscrire la mémoire de l'animal. Ils peuvent être simples (allumer une bougie, écrire un mot, dessiner, planter une fleur) ou plus élaborés (créer une boîte à souvenirs, organiser une petite cérémonie familiale). Des souvenirs concrets peuvent être proposés avec l'accord des parents : empreinte de patte, mèche de poils, photo, collier. De nombreux supports existent aujourd'hui pour accompagner les enfants. Le vétérinaire peut jouer un rôle actif en orientant les familles vers ces ressources, en fonction de l'âge des enfants et de leur sensibilité (voir ci-dessous la bibliographie destinée au jeune public). L'équipe vétérinaire peut aussi proposer de se revoir quelques jours plus tard pour répondre aux questions qui peuvent surgir après coup.
V. Conclusion
L'euthanasie d'un animal en présence d'enfants constitue un moment particulièrement sensible de la pratique vétérinaire. Elle mobilise des compétences médicales, mais aussi relationnelles et psychologiques. Comprendre le deuil, en particulier dans ses spécificités infantiles, permet au vétérinaire d'adopter une posture ajustée : honnête, empathique et rassurante. Accompagner les enfants, c'est leur permettre de trouver un sens à ce qu'ils vivent, de légitimer leur chagrin, et de préserver la qualité du lien qu'ils garderont avec leur animal décédé. C'est aussi soutenir les parents dans leur rôle éducatif et affectif, en leur offrant des repères concrets et des ressources adaptées. Ainsi, l'approche du deuil et de l'euthanasie avec les enfants dépasse la sphère individuelle : elle contribue à ancrer la pratique vétérinaire dans une dimension profondément humaine, où le soin à l'animal s'accompagne d'un soin à la famille.
Bibliographie
- Alvis L, Zhang N, Sandler IN, Kaplow JB. Developmental manifestations of grief in children and adolescents: caregivers as key grief facilitators. 2023; 16: 447-457.
- Caux A. L'enfant de 2 à 9 ans face à l'euthanasie de son animal. Mémoire DIE de vétérinaire comportementaliste. 2014.
- Crawford KM, Zhu Y, Davis KA et coll. The mental health effects of pet death during childhood: is it better to have loved and lost than never to have loved at Eur. Child Adolesc. Psychiatry. 2021; 30(10): 1547-1558.
- Longbottom S, Slaughter V. Sources of children's knowledge about death and dying. Phil. Trans. R. Soc. B. 2018; 373:20170267.
- Smit E, Smith BP. Dealing with death: the role of animal-themed literature in supporting children with grief and loss. Human-Animal Interactions. 2023; doi: 10.1079/hai.2023.0002.
Bibliographie à destination du jeune public
Le deuil animalier
- Les trois enterrements de mon chien, 2020, Guillaume GUÉRARD, Éditions du Rouergue
- L'arbre, le chat, le grand-père, 2020, Pauline ALPHEN, Nathan
- Chamour, 2016, Émilie VAST, Éditions MeMo
- Le chien de Max et Lili est mort, 2005, Dominique de SAINT MARS, Serge BLOCH, Éditions Calligram
- Le deuil de mon animal de compagnie, 2018, Annique LAVERGNE & Yves DUMONT, Éditions Petit Homme
- Le deuil d'Olivia, 2022, Martine LATULIPPE, Nathalie PARENT, Catherine PETIT, Éditions Saint-Jean
- Mon amie pour la vie, 2023, Amandine LAUDEBAT & Audrey ASSELIN, Éditions Jets D'encre
- Quand ton animal meurt, 2016, Victoria RYAN, Éditions Signe
- Sacha & Gribouille, 2019, Anaïs CAUX, Édition Anima Care
- Mingan les nuages, 2017, Marie-Andréa ARSENAULT & Amélie DUBOIS, Éditions de l'isatis
Liens d'intérêt : Pour Marie CIBOT : Solâme, entreprise vétérinaire dédiée à l'accompagnement de la fin de vie des animaux
📃 Approche médicale allopathique de la douleur chronique
Marcy L'étoile, France
I. Introduction
La douleur chronique est définie par la Société française d'étude de la douleur comme un syndrome multidimensionnel qui persiste ou est récurrent au-delà de ce qui est habituel pour la cause initiale présumée, répond insuffisamment au traitement, ou entraîne une détérioration significative et progressive des capacités fonctionnelles et relationnelles du patient. Cette douleur chronique est considérée comme une maladie et diffère de la douleur aiguë, en particulier par son traitement.
II. Les challenges du traitement de la douleur chronique
Les douleurs chroniques, insidieuses, sont souvent négligées car jugées comme la conséquence d'une maladie concomitante. Pour autant, leur traitement fait partie intégrante de la prise en charge thérapeutique de ces maladies.
Son évaluation peut s'avérer délicate, en particulier du fait de l'expression variable de la douleur chez les patients, du comportement différent de l'animal chez le vétérinaire et à la maison, et enfin du fait de la diversité de son origine. L'avis du propriétaire est donc fondamental dans ce cadre, mais disposer d'outils de gradation de cette douleur est aussi très important.
Du point de vue du traitement lui-même, étant administré généralement sur le moyen à long terme, des problèmes de tolérance et d'observance peuvent être rencontrés. L'évolution de l'affection sous-jacente peut aussi nécessiter un réajustement du traitement.
III. L'arsenal thérapeutique allopathique de la douleur chronique
Le traitement de la douleur chronique comprend plusieurs défis, le premier d'entre eux étant la tolérance d'un traitement mis en place sur le long terme, le deuxième étant l'observance de ce traitement et le troisième l'évolution de l'affection sous-jacente, pouvant nécessiter un réajustement parfois compliqué du traitement.
Une approche thérapeutique multimodale est recommandée. La base du traitement d'une douleur chronique repose la plupart du temps sur l'administration d'anti-inflammatoires non stéroïdiens (AINS), combinés à des autres classes médicamenteuses et des adjuvants de l'analgésie. Le recours à des techniques non médicamenteuses, non développé ici, constitue souvent une solution complémentaire pertinente.
1. Les AINS
Dès lors qu'une douleur est présente dans un contexte inflammatoire, le recours aux AINS apparaît légitime. La difficulté repose sur la tolérance à moyen et long termes. Dans cette optique, il apparaît préférable d'avoir recours à des médicaments inhibiteurs préférentiels ou spécifiques des cyclo-oxygénases de type 2 (COX-2). Même si quelques études ont conclu à la possible utilisation sur plusieurs semaines d'AINS et à leur efficacité thérapeutique, les risques d'ulcérations gastro-intestinales et d'insuffisance rénale restent présents, un suivi médical rapproché est donc important dès lors qu'un traitement anti-inflammatoire à long terme est instauré. [1]
Le grapiprant, molécule apparentée aux AINS mais avec un mécanisme d'action différent, est intéressant sur le principe. Il n'agit pas sur les COX et la production de prostaglandines, mais directement sur les récepteurs EP4 aux prostaglandines E2, il est donc théoriquement associé à une meilleure tolérance gastro-intestinale et rénale. Si les premières études d'efficacité sont apparues prometteuses, le médicament n'en est pas pour autant dépourvu d'effets secondaires. En particulier, des vomissements et de la diarrhée ont été rapportés chez le chien mais à ce jour aucune altération de la fonction rénale. Il ne possède pas d'AMM chez le chat.
2. Le paracétamol
Le paracétamol a un mécanisme d'action différent des AINS, qui reste à préciser : il semble agir sur plusieurs voies, en particulier la voie des COX (action centrale, sans action anti-inflammatoire périphérique), la voie sérotoninergique et la voie endocannabinoïde, et peut ainsi participer à limiter la sensibilisation du système nerveux nociceptif. Le paracétamol est formellement contre-indiqué chez le chat, mais il est utilisable chez le chien à une dose de 10-15 mg/kg PO BID. [2] N'ayant pas un mécanisme d'action similaire aux AINS, il peut constituer soit un complément, soit une alternative à ces derniers.
3. Les morphiniques
À l'inverse des douleurs aiguës, les morphiniques ne constituent pas la classe thérapeutique de choix pour le traitement des douleurs chroniques. Ces dernières répondent en effet modérément aux morphiniques, d'autant que l'administration sur le long terme de cette classe de médicaments peut s'accompagner d'effets secondaires (ralentissement du transit digestif, rétention urinaire, sédation/dysphorie en particulier). Ils peuvent néanmoins constituer une option en cas de crise algique au décours de la maladie. Les morphiniques faibles comme le tramadol ou la codéine peut constituer une option en complément ou en alternative aux AINS en cas de contre-indication ou d'intolérance à ces derniers. [2]
4. Les adjuvants de l'analgésie
Les adjuvants de l'analgésie sont des médicaments qui n'ont pas été développés pour leur valence analgésique, mais cette dernière, insuffisante bien souvent si utilisée seule, peut s'avérer intéressante dans le cadre d'un protocole d'analgésie multimodale. [2] Parmi les molécules intéressantes, on peut signaler les anticonvulsivants (gabapentine, prégabaline), les antiparkinsoniens (amantadine, mémantine), les antidépresseurs tricycliques (amitriptyline, imipramine).
La gabapentine et la prégabaline sont des médicaments anticonvulsivants qui permettent de réduire la libération de neurotransmetteurs pronociceptifs et stimulent les voies descendantes modulatrices dans la moelle épinière, limitant les phénomènes d'hypersensibilisation. La gabapentine est la plus utilisée en médecine vétérinaire, à la dose de 2-20 mg/kg PO BID à TID chez le chien, et 1-10 mg/kg PO BID chez le chat. Son efficacité a été démontrée dans le cadre de douleur aigüe comme de douleur chronique chez les carnivores domestiques, elle est également prescrite chez le chat pour lutter contre l'anxiété et facilité le transport.
L'amantadine et la mémantine sont des médicaments antiparkinsoniens et antiviraux, qui agissent sur les récepteurs au N-méthyl D aspartate (NMDA) et préviennent par cette voie les phénomènes de sensibilisation et d'hyperalgésie. Dans une étude sur des chiens présentant une douleur arthrosique, l'amantadine associée au méloxicam a permis d'obtenir des scores de qualité de vie meilleurs qu'avec le méloxicam seul. Du fait de ses propriétés antivirales, l'amandatine n'est à ce jour plus accessible aux vétérinaires, mais la mémantine peut la remplacer avantageusement.
Pour les antiépileptiques comme pour les antiparkinsoniens, il est préférable d'instaurer et respecter un traitement d'au moins une quinzaine de jours avant de tirer des conclusions sur l'efficacité ou l'inefficacité du traitement.
Les antidépresseurs tricycliques agissent sur la recapture de la sérotonine. Leur efficacité a été démontrée chez l'homme mais les évidences scientifiques restent faibles en médecine vétérinaire. L'amitriptyline et l'imipramine sont les molécules les plus décrites pour cette indication, mais leurs effets secondaires (sédation et effets anticholinergiques en particulier) limitent leur utilisation en cas d'échec avec la gabapentine et l'amantadine. La clomipramine, qui dispose d'une AMM chez le chien, peut aussi être utilisée, mais il existe peu de données pour supporter son utilisation lors de douleur chronique chez les carnivores domestiques. Dans tous les cas, cette classe de médicaments ne doit pas être associée au tramadol, qui agit également sur la recapture de la sérotonine, au risque de voir survenir un syndrome sérotoninergique.
5. Les thérapies immunomodulatrices : anticorps monoclonaux anti-NGF
Les anticorps monoclonaux sont des anticorps ne reconnaissant qu'un seul type d'épitope sur un antigène donné. Il existe de multiples mécanismes par lesquels les anticorps monoclonaux produisent leur effet. Ceux-ci incluent le blocage de l'interaction ligand-récepteur ou des voies de signalisation ou l'altération de populations cellulaires par l'activation du complément ou de la cytotoxicité à médiation cellulaire dépendant de l'anticorps. Les anticorps monoclonaux ont montré leur efficacité thérapeutique dans diverses affections chez l'homme : maladies auto-immunes, maladies infectieuses, oncologie. La douleur chronique constitue une autre cible thérapeutique. En effet, plusieurs médiateurs de l'inflammation jouent un rôle clé dans la sensibilisation et la chronicisation de la douleur, en particulier des cytokines comme le tumor necrosis factor (TNF) et le nerve growth factor (NGF). Ce dernier est un facteur clé de la douleur inflammatoire et neuropathique, et constitue ainsi une cible privilégiée pour des anticorps monoclonaux.
Les anticorps monoclonaux anti-NGF chez le chien (bedinvetmab) et le chat (frunevetmab) ont connu un essor important en raison de leur facilité d'administration, leur présumée sécurité d'emploi, couplée à une durée d'action et une efficacité souvent assez spectaculaire après la première administration. [4] Pour autant, récemment, des cas de suspicions d'arthropathie destructrice d'évolution rapide ont été rapportés chez le chien, avec une issue fatale dans la majorité des cas. [5] Chez le chat, des complications cutanées sévères ont été rapportées. La survenue de ces effets secondaires, même si très rares considérant le volume de prescription, incite à une certaine prudence et à relativiser leur utilisation en première intention dans le cadre de l'arthrose.
6. Les dérivés du cannabis
À ce jour, seuls des médicaments dépourvus de tétrahydrocannabinol (THC), substance psychoactive, sont autorisés en France sous forme de compléments alimentaires à base de cannabidiol (CBD), substance dépourvue de propriétés psychoactives et aux propriétés antalgiques et anticonvulsivantes. Ils ont été récemment mis sur le marché en France et en Europe, mais leur concentration en principe actif est faible et la preuve de leur efficacité thérapeutique reste à confirmer chez les animaux de compagnie.
IV. Conclusion
Le traitement de la douleur chronique reste un défi, tant par le choix du traitement et des associations réalisées, que par les problèmes d'observance et de tolérance. C'est pourquoi une information éclairée du propriétaire et son implication dans le suivi de l'animal et de son traitement sont nécessaires. Différentes options allopathiques sont disponibles, qui peuvent également être complémentées d'autres approches thérapeutiques.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Approche physiothérapeutique et nutritionnelle de la douleur chronique
Lausanne, Suisse
I. Introduction
La douleur chronique, et en particulier l'ostéoarthrose (OA), constitue un défi majeur en médecine vétérinaire. Multifactorielle et encore trop souvent sous-estimée, elle altère profondément la qualité de vie de nos patients. Elle entraîne une baisse d'activité, une fonte musculaire, une modification du comportement, un isolement social et une anxiété accrue, tout en aggravant l'inflammation et en favorisant des comorbidités métaboliques. Chez le chien de compagnie, cela se traduit par une perte d'envie de jouer ou de se promener. Chez le chien de sport ou de travail, les répercussions sont encore plus visibles, compromettant directement ses performances et sa carrière.
L'OA est une affection dégénérative et évolutive, caractérisée par la dégradation progressive du cartilage, une inflammation de bas grade et un remodelage de l'articulation. Elle induit une douleur mixte : nociceptive, neuropathique et émotionnelle. La chronicité entraîne une sensibilisation centrale et périphérique : de simples stimulations deviennent douloureuses. Briser ce cercle vicieux douleur–inactivité–amyotrophie est essentiel et nécessite une approche multimodale individualisée. [1]
La gestion de l'OA associe pharmacologie, interventions orthopédiques, physiothérapie, nutrition et médecines complémentaires. Parmi ces piliers, la physiothérapie et la nutrition se distinguent par leur rôle central et durable.
II. Gestion physiothérapeutique
La physiothérapie agit sur la douleur, l'inflammation, la mécanique articulaire et la condition générale. [1,2] Ses outils incluent.
- Laser (photobiomodulation) : réduit l'inflammation de bas grade et améliore la production d'ATP. [2]
- Électrothérapie (TENS, NMES) : bloque la transmission nociceptive et préserve la masse musculaire. [1]
- Modalités thermiques : le froid jugule les poussées inflammatoires et la vitesse de conduction nerveuse, la chaleur diminue l'ankylose articulaire et prépare le système musculosquelettique à l'effort. [1]
- Exercices thérapeutiques : cœur du traitement, ils restaurent mobilité, force et proprioception [1-2].
- Rééducation proprioceptive : améliore la stabilité posturale et réduit le risque de blessures. [2]
- Hydrothérapie : grâce à la poussée d'Archimède et à la résistance de l'eau, l'hydrothérapie permet un travail musculaire efficace et sans surcharge articulaire. [2]
L'implication active du propriétaire est cruciale : sans régularité, ni suivi des consignes à domicile, les bénéfices de la physiothérapie sont limités.
III. Gestion nutritionnelle
La nutrition constitue le deuxième pilier. Le contrôle du poids est fondamental, chaque kilo excédentaire augmentant les contraintes mécaniques et l'inflammation systémique. [3] Des nutriments spécifiques complètent cette approche. :
- Oméga-3 (EPA, DHA) : modulateurs puissants de l'inflammation, réduisent la douleur et le recours aux AINS [2-4].
- Glucosamine et chondroïtine : précurseurs et constituants de la matrice cartilagineuse, possèdent des effets chrondroprotecteurs ralentissant la dégradation du cartilage articulaire. [2]
- L-carnitine : favorise la perte de masse grasse et soutient la masse musculaire, clé du maintien fonctionnel.
Autres ingrédients : collagène de type II non dénaturé, antioxydants et extraits végétaux comme la curcumine ou le Boswellia offrent un soutien complémentaire [2-5].
Un suivi nutritionnel régulier, associant pesées, adaptation des rations et suivi de la composition corporelle, optimise les résultats et renforce l'adhésion des propriétaires.
IV. Conclusion
En conclusion, la gestion de l'arthrose canine repose sur une approche intégrative. La physiothérapie agit directement sur la douleur et restaure une fonction active, tandis que la nutrition constitue un traitement de fond agissant sur l'inflammation et le contrôle pondéral. La clé du succès réside dans une coordination entre vétérinaires, physiothérapeutes et propriétaires, chacun jouant un rôle actif dans un projet thérapeutique commun. Cette alliance permet non seulement de contrôler la douleur chronique, mais aussi de redonner aux chiens arthrosiques une vie plus confortable, active et digne. Elle illustre l'évolution de la médecine vétérinaire vers une approche globale et préventive, centrée sur le bien-être durable de l'animal.
Bibliographie
- MILLIS DL, LEVINE D. Canine Rehabilitation and Physical Therapy. 2e ed. Elsevier; 2014.
- MOSLEY C, EDWARDS T, ROMANO L, TRUCHETTI G, DUNBAR L, SCHILLER T, et al. Proposed Canadian Consensus Guidelines on Osteoarthritis Treatment Based on OA-COAST Stages 1–4. Front Vet Sci. 2022 Apr 26;9.
- KEALY RD, LAWLER DF, BALLAM JM, et al. Effects of diet restriction on life span and age-related changes in dogs. J Am Vet Med Assoc. 2002;220(9):1315–20.
- ROUSH JK, CROSS AR. Evaluation of the effects of dietary supplementation with fish oil omega-3 fatty acids on weight bearing in dogs with osteoarthritis. J Am Vet Med Assoc. 2010;236(5):535-9.
- MARCELLIN-LITTLE DJ, HULSE DA, HUNTINGFORD JL, GRUBB T, BRUNKE MW, MARKLEY AP, et al. A proposed framework for practical multimodal management of osteoarthritis in growing dogs. Front Vet Sci. 2025 Apr 28;12.
Liens d'intérêt : Conseiller scientifique pour la société AllCare innovations.
📃 Arthrite fongique due à Trichosporon spp. chez un chien berger blanc suisse
Lucie BONNEAU
Coauteurs : L. BONNEAU, P-O. GODART
Introduction
Les atteintes ostéoarticulaires d'origine fongique (ostéomyélite, arthrite) sont rares en Europe. Elles sont plus fréquentes en Amérique du Nord où certains agents tels que Coccidioïdes, Blastomyces, Histoplasma ou Cryptococcus sont endémiques. nous rapportons ici un cas original d'arthrite fongique due à Trichosporon spp.
Anamnèse
Un chien de race berger blanc suisse, mâle entier, de 4 ans est présenté pour l'exploration d'une boiterie chronique du membre pelvien gauche évoluant depuis 1 mois, réfractaire au traitement anti-inflammatoire non stéroïdien mis en place en première intention.
Examen clinique
L'examen général est normal. L'examen orthopédique montre une boiterie sans appui du membre pelvien gauche avec une tuméfaction et une déviation en valgus du tarse gauche dont la manipulation est inconfortable. Aucune lésion cutanée n'est retrouvée sur le membre, ni ailleurs sur le corps.
Démarche diagnostique
Le bilan radiographique du tarse gauche montre une tuméfaction des tissus mous avec une lésion mixte ostéolytique/ostéoproliférative des calcanéus et talus. Le scanner du thorax, de l'abdomen et des membres pelviens montre une lésion du tarse gauche agressive, polyostotique, monoarticulaire, impliquant principalement le talus et le calcanéus. Des biopsies osseuses sont réalisées pour analyse histologique et culture bactérienne, laquelle est négative. L'histopathologie révèle une ostéomyélite nécrotique avec la présence d'éléments fongiques. Les biopsies sont renouvelées pour culture fongique, celle-ci est négative.
Traitement
Un traitement antifongique à base d'itraconazole (5 mg/kg PO, une fois par jour) est initié avec un suivi mensuel, radiographique et sanguin. Le port d'une attelle est conseillé. Le chien a présenté une évolution satisfaisante avec une reprise d'appui, malgré l'apparition d'une plantigradie modérée et la persistance du valgus. Une consolidation osseuse significative identifiée radiographiquement motive l'arrêt du traitement après 4 mois. Les signes cliniques et les lésions radiographiques restent stables deux mois plus tard (Figure 1).
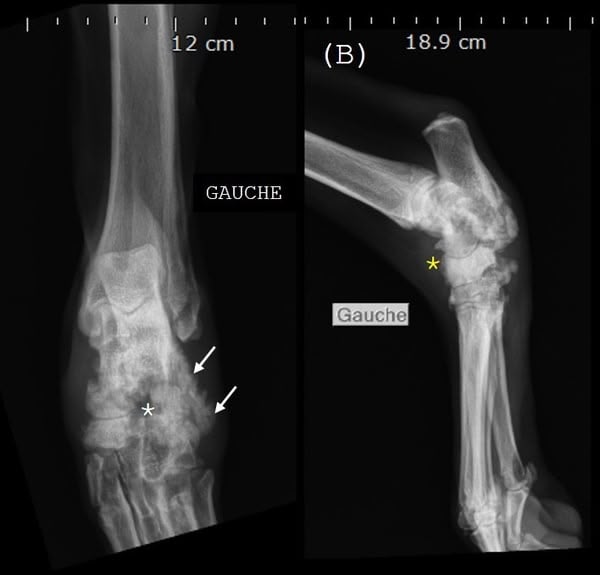
Figure 1
Radiographies de face (figure 1A) et de profil (figure 1B) du tarse gauche 2 mois après l'arrêt du traitement antifongique. Les os du tarse paraissent mieux consolidés. Des réactions périostées spiculées modérées restent visibles, principalement sur la face latérale du tarse (flèches blanches).
Une ostéolyse centrale persiste, caractérisée par un foyer radiotransparent centré sur l'articulation talocalcanéenne (astérisque blanche). Une tuméfaction des tissus mous péri-articulaires est présente (astérisque jaune). On note une légère bascule dorso-proximale du calcanéus.
Dix mois après la première présentation, le chien est présenté pour les mêmes signes cliniques et un abattement marqué. L'animal est hyperthermique et le tarse gauche est très tuméfié. Les radiographies montrent une aggravation franche des lésions ostéolytiques du tarse gauche. Un prélèvement (biopsie et épanchement articulaire) pour culture fongique permet de révéler Trichosporon spp, sans antifongigramme associé. Le même traitement médical est prescrit. Une amélioration clinique partielle est notée avec une régression de la tuméfaction, la reprise d'un appui partiel, et un animal en meilleur état général. L'aggravation progressive des lésions radiographiques (Figure 2) motive la réalisation de nouveaux prélèvements pour réaliser un antifongigramme, qui s'est révélé non concluant. L'aggravation de la boiterie, de nouveau sans appui, invite à proposer l'amputation du membre pelvien gauche.
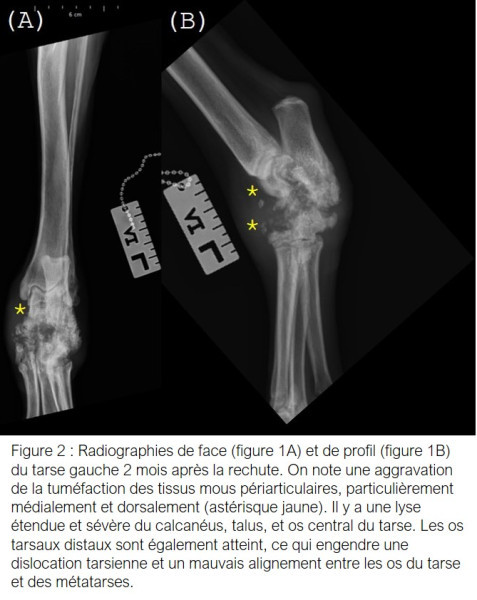
Discussion
Le chien présenté ici souffrait d'une arthrite d'origine fongique due à Trichosporon spp. En cas d'atteintes osseuses causées par une maladie fongique systémique, les lésions observées affectent majoritairement la métaphyse des os longs, sont souvent polyostotiques, et plus rarement articulaires. Dans le cas présent, les lésions concernaient uniquement le tarse gauche, sans autre lésion osseuse ou articulaire identifiée. La distribution lésionnelle et la nature de l'agent infectieux en font un cas original. Très peu d'informations concernant Trichosporon spp. sont rapportées dans la littérature vétérinaire. Il s'agit d'un organisme saprophyte qui n'est généralement pas considéré comme pathogène mais qui peut le devenir chez les individus immunodéprimés (1), ce qui n'était pas le cas ici. On le retrouve dans l'environnement ainsi qu'au sein de la flore cutanée et muqueuse de l'homme et des animaux (1). Chez l'homme, il est à l'origine de maladies graves, parfois mortelles, et généralement résistantes au traitement antifongique (1). Quelques cas sporadiques sont rapportés en médecine vétérinaire (endocardite valvulaire, méningoencéphalite (2), infection respiratoire (3), ...), sans description d'atteinte ostéoarticulaire (1). Différentes souches de Trichosporon spp. existent, avec des sensibilités variables aux antifongiques (4,5). Cela n'a pu être identifié par le laboratoire.
Conclusion
Il s'agit du premier cas rapporté en médecine vétérinaire d'arthrite fongique due à Trichosporon spp. L'arthrite fongique doit faire partie du diagnostic différentiel des lésions monoarticulaires agressives en Europe.
Bibliographie
- GREENE CE. Trichosporonosis. In: Infections Diseases of the dog and cat. 4th edition, St Louis, Missouri: ELSEVIER SAUNDERS; 2012. p. 672-5.
- BRYAN LK, et al. Meningoencephalitis in a dog due to TRICHOSPORON MONTEVIDEENSE. J Comp Pathol. 2014; 151(2-3): 157-61.
- BIEGASKA MJ, et al. Mixed Infection of Respiratory Tract in a Dog Caused by Rhodotorula mucilaginosa and Trichosporon jirovecii: A Case Report. Mycopathologia. juin 2018; 183(3): 637-44.
- COLOMBO AL, et al. Current knowledge of Trichosporon spp. and Trichosporonosis. Clin Microbiol Rev. 2011; 24(4): 682-700.
- NAVARRO BS, et al. Antifungal sensitivity and species of yeasts in oral mucosa of street mixed-breed dogs. J Mycol Med. 2020; 30(4): 101010.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Arthrodèse partielle du carpe chez 13 chiens (14 carpes) avec une plaque LCP© condylienne:
Julien CABASSU
Coauteurs : Camille DURBEC, Julien CABASSU, Stéphane IVANOFF
Introduction
De nombreuses techniques ont été décrites pour réaliser une arthrodèse partielle, principalement l'utilisation de broches en croix ou droites, l'application d'une plaque dorsale ou une combinaison des deux. Différentes plaques, verrouillées ou non, ont été décrites sans qu'un implant ne montre une supériorité évidente. Cela a mené les chirurgiens à utiliser des implants plus récents voire même à développer certains implants spécifiques. Dans notre structure, nous utilisons depuis plusieurs années la plaque LCP© condylienne de DEPUY SYNTHES. Le but de cette étude est de décrire le résultat à long-terme des chiens traités par une arthrodèse partielle du carpe suite à une lésion d'hypertension atteignant l'étage intercarpien ou carpo-métacarpien par l'évaluation de la qualité de la fusion, du résultat fonctionnel et du taux de retrait d'implant.
Matériel et Méthode
Les chiens opérés d'une arthrodèse partielle dans notre clinique à l'aide d'une plaque LCP© condylienne avec un suivi minimum de 6 mois postopératoires ont été revus de manière rétrospective. Un examen radiographique avec des vues en contrainte (hyperextension, varus, valgus) a été systématiquement réalisé. Après anesthésie générale, les patients ont été placés en décubitus latéral. Après exposition des articulations de l'étage intercarpien, radio-carpien et une exposition minimale de l'étage radio-carpien, une plaque LCP© condylienne est appliquée avec une vis verrouillée dans un des deux trous les plus proximaux, dans l'os radial du carpe et une vis corticale dans le trou le plus distal dans le métacarpe III. La position de la plaque est alors vérifiée puis la plaque est retirée. La plaque a été auparavant contournée légèrement pour orienter les deux vis proximales dans un axe cranio-distal à caudo-proximal. Le cartilage articulaire intercarpien et capo-métacarpien est alors débridé à l'aide d'une fraise chirurgicale. Une greffe auto spongieuse est prélevée puis déposée. La plaque est appliquée à l'aide des deux vis préplacées, puis les autre vis sont insérées. Les trous distaux sont remplis selon la préférence du chirurgien. Un pansement contentif avec attelle palmaire est systématiquement appliqué pendant 6 à 8 semaines jusqu'aux radiographies de contrôle. La localisation de l'instabilité, la taille des implants, nombre et le type de vis et la nécessité éventuelle du retrait de l'implant sont rapportés. Les radiographies de suivi sont évaluées pour déterminer la qualité de la fusion. Les propriétaires ont été contactés par téléphone et le résultat fonctionnel a été évalué par un questionnaire LOAD.
Résultats
Quatorze arthrodèses partielles sur 13 chiens (un chien a eu une arthrodèse bilatérale) opérés entre 2017 et 2024 ont été incluses dans cette étude, avec un suivi minimal de 7 mois. L'étage intercarpien était le seul étage atteint dans 4 cas, carpo-métacarpien dans 8 cas, et une combinaison des deux étages dans 2 cas. Une plaque condylienne de 2 mm a été utilisée sur un chien (13 kg), une 2,4 mm sur un chien (14 kg) et une 2,7 mm sur tous les autres chiens (22-43 kg). Tous les chiens ont eu une attelle palmaire sans complication rapportée. À la radiographie de contrôle, tous les chiens avaient une fusion osseuse estimée suffisante pour le retrait de l'attelle. Aucune intervention chirurgicale supplémentaire n'a été requise pour obtenir ce niveau de fusion. Un retrait de plaque a été effectué sur 7 cas (6 à cause d'une boiterie, et 1 préventivement sur le cas bilatéral après retrait de la première plaque). Quatre chiens ont eu une récupération fonctionnelle complète après le retrait de la plaque. Un chien a eu une nette amélioration mais persistance d'une boiterie, et un chien é été perdu dans le suivi. Le suivi fonctionnel par score LOAD a été évalué chez 10 chiens. Sept chiens ont un score entre 0 et 10 (lésion articulaire minime), 2 entre 11 et 20 (lésion articulaire modérée) et 1 entre 21 et 30 (lésion articulaire sévère) dont la plaque a été retirée récemment.
Discussion
Les résultats cliniques obtenus sont satisfaisants et comparables aux résultats lors de l'utilisation d'une autre plaque. Dans une étude (2) rapportant 45 arthrodèses partielles du carpe, des résultats satisfaisants ont été obtenus suite à un questionnaire adressé à tous les propriétaires. L'ablation des implants dans d'autres études est rapportée jusqu'à 100% lors de l'utilisation de broches seules, et dans 25 à 41%des cas lors de l'utilisation de plaques, entre 22 et 235 jours postopératoires. Dans notre étude, le retrait de plaque a été effectué sur 50% des cas avec un suivi minimum de 6 mois après l'arthrodèse. Dans une autre étude (1), après retrait des implants, 75% des chiens ont eu une récupération fonctionnelle complète ou acceptable et 25% ont continué à boiter. Nous avons observé des résultats similaires chez nos chiens avec une majorité de patients (4 sur 5 suivis) qui ont eu une bonne fonction après le retrait des implants. Aucune complication catastrophique n'a été observée, notamment suite au retrait des plaques.
Bibliographie
- DENNY HR, BARR ARS. Partial carpal and pancarpal arthrodesis in the dog: a review of 50 cases. J Small Anim Pract. (1991)
- PARKER RB, BROWN SG, WIND AP. Pancarpal arthrodesis in the dog: a review of fort-five cases. Vet Surg. (1981)
- WILLER RL, JOHNSON KA, TURNER TM, PIERMATTEI DL. Partial carpal arthrodesis for third degree carpal sprains: a review of 45 carpi. Vet Surg. (1990)
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Autosuture digestive
Ollioules, France
I. Introduction
Les sutures digestives, rencontrées lors de gastrotomie/gastrectomie ou entérotomie/entérectomie, sont communément réalisées de manière manuelle à l'aide de fil de suture. Toutefois, il existe des techniques dites d'« autosuture » ou « d'agrafage chirurgical » qui présentent certains intérêts. Il est nécessaire de connaître les spécificités des agrafes chirurgicales ainsi que la technique opératoire afin de bénéficier des intérêts de ce matériel.
Les pinces à auto-suture s'utilisent majoritairement lors d'anastomose intestinale ou colique après résection intestinale. Elles peuvent également être utiles lors de gastrectomie. Les pinces à autosuture ne sont toutefois pas utilisables pour suturer une entérotomie ou une gastrotomie, mais l'utilisation d'agrafeuses cutanées pour suturer une entérotomie ou une gastrotomie a été décrite à plusieurs reprises avec de bons résultats. La plus large étude portant sur la suture d'entérotomie, gastrotomie ou colotomie para agrafe cutanée chez le chien fait état de 333 chiens avec un taux de complication de 3,3% dont 1,2% de déhiscence.
II. Présentation des techniques chirurgicales d'anastomose digestive et des différentes pinces à autosuture
Comme énoncé précédemment, les pinces à autosuture sont majoritairement utilisées pour réaliser des anastomoses digestives, qui sont dites :
- soit termino-terminales : les deux sections intestinales sont apposées l'une à l'autre, exactement comme lors d'une anastomose manuelle ;
- soit latéro-latérale, dite également termino-terminale fonctionnelle : les deux segments intestinaux sectionnés sont apposés parallèlement l'un à l'autre, mettant en contact leurs deux bords anti-mésentériques. L'utilisation de pinces spécifiques va créer l'union des segments intestinaux en recréant une lumière intestinale large.
Les agrafeuses linéaires, dites pinces TA® (pour Thoraco-Abdominal), sont disponibles en plusieurs longueurs : 30 mm, 45 mm, 60 mm, 90 mm (figure n°1). Lors de leur utilisation, les pinces TA vont déployer 2 rangées d'agrafes en quinconce dans les tissus. Les agrafes déployées par la pince sont disponibles soit en 3,8 mm de hauteur – 1,5 mm de hauteur une fois comprimées (recharges bleues), soit en 4,8 mm de hauteur – 2,0 mm de hauteur une fois comprimées (recharges vertes). Le choix doit donc se faire en fonction du tissu agrafé et de la taille du patient.
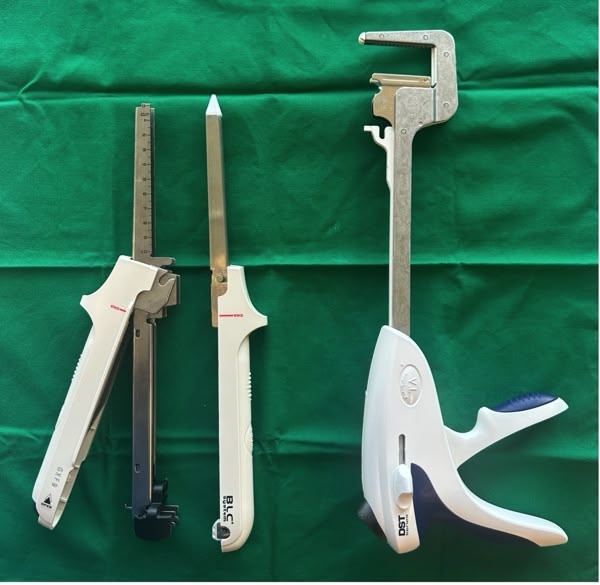
Figure 1
Ces pinces TA® seront utilisées pour réaliser des gastrectomies ou pour réaliser la seconde ligne d'agrafage lors d'une anastomose intestinale latéro-latérale.
Certaines agrafeuses chirurgicales ont également la possibilité de couper entre les rangées d'agrafes déployées : les pinces GIA® (pour Gastro-intestinal Anastomosis). Elles vont, de la même manière que les pinces TA®, déployer des agrafes de 3,5 ou 4,8 mm de hauteur (figure n°1). La différence par rapport à la pince TA® est que la pince GIA® va déployer 2 rangées d'agrafes de part et d'autre d'une ligne de section, soit 4 rangées d'agrafes au total. La section entre les 4 rangées d'agrafes se fait de manière automatique lors du déclenchement de la pince GIA®. Elles sont disponibles également en plusieurs longueurs : 60 mm, 80 mm ou 100 mm. Elles sont également disponibles sous la forme de pinces « endo-GIA® », initialement mises au point pour être utilisables en cœlioscopie ou thoracoscopie. L'avantage de ces pinces endo-GIA® pour les anastomoses digestives est leur taille plus réduite, permettant de les utiliser sur des petits chiens ou chez le chat, lorsque les pinces GIA® conventionnelles sont trop larges pour rentrer dans la lumière intestinale.
Ces pinces GIA® seront utilisées pour réaliser la première ligne d'agrafage lors d'une anastomose intestinale latéro-latérale.
Enfin, les pinces dites EEA (End to End Anastomosis) permettent de réaliser les anastomoses termino-terminales, comme lors d'une suture manuelle classique. Ces pinces sont constituées de deux parties (une petite et une grande qui contient le dispositif de déclenchement des agrafes) qui seront insérées chacune dans un des deux segments intestinaux à anastomoser, puis enfin réunies entre elles avant le déploiement des agrafes. La partie renfermant les agrafes, la plus volumineuse, peut être insérée directement via le rectum en cas d'anastomose colique, ou via une entérotomie proximale au site d'anastomose en cas d'anastomose jéjunale.
III. Avantages et inconvénients de l'utilisation des autosutures en chirurgie digestive
Les principaux avantages de l'utilisation des pinces à auto-suture sont :
- le gain de temps chirurgical ;
- la diminution de la manipulation du tractus digestif, limitant les risque de contamination, d'inflammation et de troubles ischémiques ;
- la conservation d'un diamètre luminal large ;
- la meilleure résistance initiale de la suture pendant la phase inflammatoire ,
- la possibilité d'anastomoser facilement deux segments digestifs de diamètre différent, notamment en cas de dilatation intestinale majeure du segment oral après occlusion digestive ou en cas d'anastomose entéro-colique après exérèse de la valvule iléo-cæco-colique.
Les principaux désavantages de l'utilisation des pinces à auto-suture sont :
- le coût des cartouches d'agrafes ;
- la technicité à maîtriser ;
- la taille parfois trop large des pinces GIA. Dans ce cas de figure, notamment chez le chat ou les chiens de petite race, des pinces endo-GIA, moins larges, peuvent être utilisées ;,
- La nécessité d'avoir une certaine longueur avant la valvule iléo-caeco-colique en cas d'anastomose iléale afin de pour pouvoir passer l'intégralité du mord de la pince GIA et s'assurer que toutes les agrafes soient déployées pour obtenir une ouverture suffisante en matière de diamètre fonctionnel.
En matière de déhiscence postopératoire, il n'existe pas de supériorité claire des techniques par autosuture en comparaison avec les sutures digestives manuelles. En effet, un taux inférieur de déhiscence a été observé dans une étude sur 180 chiens (5% de déhiscence avec auto-sutures VS 13% avec suture manuelle) [2], tandis que deux autres études sur 210 cas et 214 cas n'ont pas montré de différence de taux de déhiscence postopératoire. [3,4] Une différence significative a toutefois été démontrée lorsque l'anastomose digestive est réalisée dans un contexte de péritonite septique, lors de reprise d'une première déhiscence notamment. Dans ce contexte de péritonite, le taux de déhiscence faisant suite à une anastomose par pince à auto-suture est de 0 à 9,7%, comparé à un taux de 28,9% à 60% en cas de suture manuelle. [2,3]. Il en ressort qu'en cas de reprise chirurgicale d'une déhiscence faisant suite à une chirurgie préalable ou en cas de péritonite septique secondaire à une perforation intestinale, l'utilisation de pince à autosuture est recommandée pour la réalisation de l'anastomose digestive aux dépens d'une suture manuelle.
La durée de chirurgie est significativement inférieure lors d'utilisation de pinces à auto-suture en comparaison avec les sutures manuelles pour une anastomose digestive (108 minutes VS 140 minutes). [4]
IV. En pratique : anastomose intestinale par pince à autosuture après entérectomie
La réalisation d'une entérectomie jéjunale avec anastomose latéro-latérale (dite termino-terminale fonctionnelle) par pinces automatiques se fait selon les étapes suivantes :
- fenestration du mésentère et hémostase mésentérique selon le même procédé que pour une suture manuelle ;
- section intestinale et exérèse de la portion intestinale d'intérêt ;
- insertion des deux mords de la pince GIA® dans chacun des segments intestinaux ;
- apposition des deux segments intestinaux parallèlement l'un à l'autre, leurs bords antimésentériques étant accolés l'un à l'autre ;
- pour cette étape et afin de limiter le risque de contamination peropératoire, les mords de la pince GIA® peuvent être insérés via deux petites entérotomies sur le bord mésentérique, oralement et aboralement à la zone d'entérectomie, la zone intestinale d'intérêt étant alors réséquée dans un second temps ;
- une fois les mors de la pince GIA® insérés dans les portions intestinales à anastomoser, ils sont joints l'un à l'autre puis la pince est déclenchée, permettant ainsi le déploiement de 4 rangées d'agrafes avec section dans le même temps, laissant 2 rangées d'agrafes de part et d'autre et la section. Cette zone de section, dont la longueur dépend de la longueur de la pince utilisée (60, 80 ou 100 mm), détermine alors le diamètre de la lumière intestinale future ;
- un second agrafage est alors réalisé, à l'aide d'une pince TA® ou d'une seconde recharge de pince GIA®, de manière orthogonale à l'axe des intestins et de la première rangée d'agrafe déployée. Cette seconde ligne d'agrafe permet de fermer la lumière intestinale et donc de terminer l'anastomose termino-terminale fonctionnelle (figure n°2) ;
- un surjet simple est ensuite ajouté au-dessus de la seconde ligne d'agrafage afin de réduire le risque de déhiscence [5] ;
- un ou deux points simples sont ajoutés à l'extrémité de la première ligne de suture, là où les deux segments intestinaux se séparent, afin de limiter le risque de déhiscence ;
- le mésentère est enfin suturé pour éviter le passage d'anses intestinales dans la fenestration mésentérique.
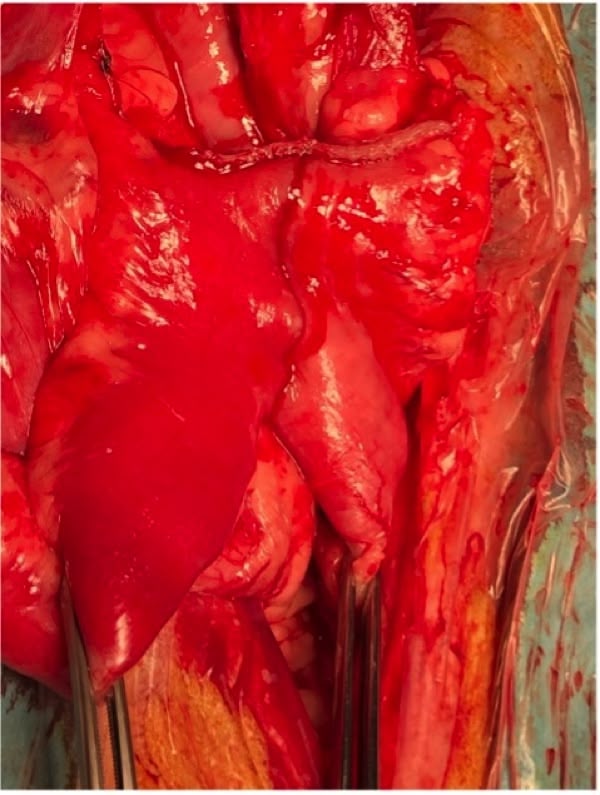
Figure 2
Lors d'un éventuel suivi échographique postopératoire, il est important de préciser à l'opérateur réalisant l'échographie qu'une anastomose par pince automatique a été réalisée et non une suture manuelle, leur appréciation du site chirurgical étant faussée sinon.
Enfin, les anastomoses termino-terminales fonctionnelles vont localement se remodeler pour redevenir un tube intestinal continu et linéaire, comme c'est régulièrement constaté lors de nouvelles laparotomies plusieurs mois à années plus tard sur les patients ayant subi une anastomose par pince à autosuture.
En conclusion, les pinces à autosuture permettent une intervention plus rapide et au moins aussi sécuritaire qu'avec une suture manuelle. Elles présentent un réel avantage en cas de péritonite septique installée au moment de l'intervention chirurgicale en permettant de réduire le risque de déhiscence postopératoire par rapport aux sutures manuelles.
Bibliographie
- SCHWARTZ Z, COOLMAN BR. Disposable skin staplers for closure of linear gastrointestinal incisions in dogs. Vet Surg. 2018 Feb;47(2):285-292.
- DE POMPEO CM et coll. Intra-abdominal complications following intestinal anastomoses by suture and staple techniques in dogs. J Am Vet Med Assoc. 2018 Aug 15;253(4):437-443.
- DAVIS DJ et coll. Influence of preoperative septic peritonitis and anastomotic technique on the dehiscence of enterectomy sites in dogs: A retrospective review of 210 anastomoses. Vet Surg. 2018 Jan;47(1):125-129.
- DUELL JR et coll. Frequency of Dehiscence in Hand-Sutured and Stapled Intestinal Anastomoses in Dogs Vet Surg. 2016 Jan;45(1):100-3
- SUMNER SM et coll. Evaluation of suture reinforcement for stapled intestinal anastomoses: 77 dogs (2008-2018) Vet Surg. 2019 Oct;48(7):1188-1193
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Autres indications des implants de desloréline
Isle Jourdain, France
I. Introduction
Agoniste de la GnRH à libération prolongée, la desloréline (Suprelorin®) permet une suppression réversible de la fonction gonadique. Au-delà de la contraception, plusieurs usages hors AMM sont documentés chez le chien (et plus marginalement chez le chat) : hyperplasie bénigne de la prostate (HBP), comportements d'origine sexuelle, dermatologie (alopécie X), adénomes des glandes périanales et incontinence urinaire post-stérilisation (IMSU). Cette synthèse reprend les éléments cliniques essentiels, leurs limites, et les implications pratiques pour le clinicien.
II. Pharmacologie en deux mots
Les implants déclenchent un bref « flare-up » (hausse de LH/FSH/stéroïdes), suivi d'une down-regulation hypophysaire entraînant hypogonadisme réversible. La cinétique d'installation et la durée d'effet varient selon l'individu et la dose. Les données récentes précisent la fenêtre du flare-up et le délai jusqu'à l'azoospermie (typiquement J35–J77). [1,3]
III. Hyperplasie bénigne de la prostate du chien : positionnement par rapport à l'osatérone
L'HBP est androgéno-dépendante ; la desloréline entraîne une réduction du volume prostatique et une amélioration clinique en 4–6 semaines, avec une persistance prolongée. Dans une étude comparative randomisée, l'osatérone procure une amélioration plus rapide mais moins durable, tandis que la desloréline agit plus lentement mais s'inscrit dans le temps. [2] Les revues de portée confirment cette cinétique « délai vs durée » et le bon profil de tolérance. [1] En pratique, la desloréline constitue une option d'entretien/relais ou une alternative lorsque la chirurgie n'est pas souhaitée.
IV. Comportements d'origine sexuelle (chien mâle)
Objectif : apprécier la part hormonale des troubles (chevauchement, marquage, errance, conflits inter-mâles) et proposer une option réversible lorsque pertinent. Les synthèses disponibles rapportent, chez une majorité de chiens, une diminution nette des comportements androgéno-dépendants, avec un délai d'installation de 3–7 semaines correspondant à la down-regulation. [1] Le flare-up initial peut transitoirement majorer les comportements ; la planification et l'information des propriétaires sont essentielles. Les données chez le chat restent limitées et surtout contraceptives. [1]
V. Dermatologie : alopécie X (Hair-cycle arrest)
Plusieurs séries/cas suggèrent un bénéfice sur la repousse du pelage chez des chiens sélectionnés. Une étude prospective rapporte une repousse visible à ≈ 3 mois chez une proportion substantielle de mâles entiers, avec bonne tolérance. [4] Les critères de sélection des répondeurs, la gestion des rechutes et le schéma de ré-implantation méritent d'être précisés. Les données ne soutiennent pas, à ce stade, l'usage en CFA/SFA ; le « puppy coat » post-OVE dispose d'indices encourageants, mais la littérature reste parcellaire. [1]
VI. Adénomes des glandes périanales (chien mâle entier)
Tumeurs cutanées androgéno-dépendantes, les adénomes des glandes périanales peuvent bénéficier d'une castration chimique réversible. Les séries cliniques rapportent une réduction progressive de la taille, parfois jusqu'à la disparition, particulièrement lorsque la chirurgie n'est pas souhaitée ou doit être différée. [1] Cette indication s'intègre comme option néo-adjuvante, d'attente ou d'alternative, avec un suivi clinique régulier.
VII. Incontinence urinaire post-stérilisation (IMSU, chienne)
Les analogues de la GnRH peuvent réduire les épisodes d'incontinence chez certaines chiennes, sans modifier significativement la MUCP ; les auteurs d'une étude évoquent un effet préférentiellement vésical (compliance) plutôt que strictement sphinctérien. [5] Au plan clinique, l'efficacité est inférieure aux alpha-agonistes en première intention, mais l'implant peut être utile en recours et/ou en association chez des chiennes réfractaires ou lorsque les traitements oraux sont contre-indiqués. La tolérance générale est bonne. [1,5]
VIII. Chat (bref)
Les usages hors castration sont peu documentés. L'essentiel des publications concerne la suppression/induction réversible de la cyclicité et les effets comportementaux associés ; peu de signaux en dermatologie féline similaires à l'alopécie X canine. [1]
IX. Pratique, sécurité, suivi
- Atouts : réversibilité, profil de tolérance favorable, souplesse de positionnement (essai thérapeutique encadré, traitement d'entretien, adjonction).
- Points d'attention : variabilité interindividuelle, délai d'installation, gestion du flare-up. [3]
Le suivi clinique/échographique (HBP) et la mesure d'objectifs comportementaux aident à documenter la réponse et à décider des ré-implantations. [1,2]
X. Conclusion
Suprelorin® n'est pas seulement un contraceptif réversible : c'est un outil thérapeutique polyvalent qui ouvre des options intermédiaires entre abstention et chirurgie. Sa place est solide en HBP (entretien/relais), utile dans certains troubles comportementaux et l'alopécie X sélectionnée, pertinente en glandes périanales lorsque la chirurgie n'est pas souhaitée, et adaptée en recours/association dans l'IMSU. Compte tenu de sa réversibilité, de sa tolérance et de son spectre d'action, il est probablement sous-utilisé en pratique quotidienne. L'accumulation de données contrôlées devrait consolider et affiner ses indications dans les prochaines années [1–5].
Bibliographie
- DRIANCOURT MA, et al. Deslorelin in animals: a review. Animals (Basel). 2020;10(8).
- NIŻAŃSKI W, OCHOTA M, FONTAINE C, PASIKOWSKA J. Deslorelin vs osaterone in canine BPH: randomized comparison. Animals. 2020;10(10):1936.
- STEMPEL S, et al. Flare-up and down-regulation after 4,7 mg implant in male dogs. Animals. 2022;12:2379.
- ALBANESE F, et al. Deslorelin for hair-cycle arrest (Alopecia X) in dogs. Vet Dermatol. 2014;25:519-e86.
- REICHLER IM, et al. GnRH analogue vs placebo in bitches with USMI. Theriogenology. 2006;66:1227-1236.
Liens d'intérêt : Je travaille régulièrement avec la compagnie Virbac(r) sur différents sujets. Je le précise par souci de transparence. Néanmoins, cela n'altère en rien le contenu de ma présentation et mon objectivité quand à l'utilisation d'un de ses produits commercialisé
📃 AVC : rôle des maladies cardiaques
Paris, France
I. Introduction
Le lien entre le cœur et le cerveau est un sujet de grand intérêt pour la communauté scientifique. L'une des associations les plus établies entre les deux est que le cœur est une source significative d'emboles et est responsable de 20 à 25% des accidents vasculaires cérébraux ischémiques chez l'homme.
II. Définition
L'accident vasculaire cérébral (AVC) ischémique est défini comme un infarctus artériel cérébral dû à un embole généré hors du cerveau ou à la formation d'un thrombus localement. Les plus fréquentes causes de cardio-embolie (embolies provenant du cœur) sont la fibrillation atriale, les valvulopathies et les myocardiopathies secondaires à un infarctus du myocarde ou une hypertension artérielle systémique (HTA) chez l'homme.
III. Fréquence et étiologie
En médecine vétérinaire, les données concernant la cardio-embolie cérébrale sont rares.
- Parmi ces AVC, ceux d'origine cardiaque représentent probablement moins de 10%.
- La fréquence estimée des AVC cardio-emboliques est de < 0,1% chez le chien.
Cependant, la fréquence des AVC d'origine cardiaque est possiblement sous-estimée car une IRM n'est pas réalisée systématiquement pour confirmer l'AVC en raison du risque anesthésique chez un animal présentant une cardiopathie évoluée. Malgré sa rareté, la cardio-embolie est bien décrite en médecine vétérinaire et peut survenir en cas d'endocardite, de myocardiopathie et d'arythmie.
IV. Diagnostic des affections à l'origine d'une cardio-embolie
Les myocardiopathies chez le chat, mais aussi toute affection cardiaque à l'origine d'une dilatation atriale, sont bien connues pour être à l'origine de la formation des thrombi dans le cœur. Une échocardiographie est donc indiquée lors de suspicion de cardio-embolie. À noter qu'une myocardiopathie n'est pas toujours associée à une auscultation anormale.
D'autre part, la présence d'une arythmie de type fibrillation atriale peut augmenter le risque de thrombose. Un électrocardiogramme est nécessaire pour diagnostiquer l'arythmie.
Le chien est moins prédisposé à la formation de thrombi en cas de myocardiopathie ; cependant en cas d'affection concomitante à l'origine d'une hypercoagulabilité, par exemple syndrome de Cushing, entéropathie exsudative, néphropathie avec perte protéique, des thrombi peuvent être formés dans le cœur et emboliser. L'échocardiographie dans ce cas-là permet parfois de visualiser un thrombus intracardiaque.
Une situation rare, mais reconnue comme cause d'AVC est l'endocardite infectieuse qui implique la colonisation microbienne des surfaces endothéliales du cœur, principalement des valves cardiaques et de l'endocarde mural, entraînant souvent des lésions prolifératives ou érosives des structures cardiaques affectées. Des complications majeures telles que l'insuffisance cardiaque congestive et des conséquences de l'embolie (par exemple, dysfonction rénale, AVC ischémique, infarctus du myocarde, formation d'abcès dans plusieurs organes) peuvent survenir.
V. Rôle de l'hypertension artérielle systémique
Bien que l'HTA ne soit pas une cause de cardio-embolie, elle fait partie des causes d'AVC ischémique. Dans une étude rétrospective réalisée au sein du CHV ADVETIA en 2024 chez 17 chats avec un AVC ischémique dont l'objectif était de décrire les modifications cardiovasculaires chez des chats ayant un diagnostic présumé d'AVC ischémique, l'HTA a été l'affection cardiovasculaire prédominante.
En cas d'HTA, l'autorégulation maintient normalement une pression de perfusion cérébrale constante en réponse aux variations de la pression artérielle (PA) grâce à une vasoconstriction ou une dilatation réflexe myogénique. Des augmentations soudaines et importantes de PA peuvent dépasser les mécanismes d'autorégulation car les artérioles sont limitées dans leur capacité à se constricter. La PA intracérébrale augmente alors et la barrière hémato-encéphalique est franchie. Le résultat est une diffusion de fluide vasculaire à travers les membranes capillaires dans le parenchyme cérébral, entraînant un œdème cérébral, une augmentation de la pression intracrânienne, et potentiellement des déficits neurologiques. Ceci est à l'origine des déficits neurologiques connus comme l'encéphalopathie hypertensive.
Dans l'HTA chronique, la vascularisation cérébrale subit des adaptations, telles que l'hypertrophie artériolaire, pour permettre une meilleure autorégulation. Ces changements dans la vascularisation cérébrale peuvent entraîner une perte de tonus régulateur et des modifications des parois des vaisseaux. Un déplacement vers la droite de la PA nécessaire pour maintenir un flux sanguin cérébral constant se produit. En conséquence, des réductions de la pression artérielle peuvent contribuer à l'hypoperfusion cérébrale et à l'AVC ischémique.
En cas de suspicion clinique d'AVC, il est indispensable de réaliser au moins une mesure de la PA. Cependant, au moment de la présentation clinique, la PA peut être normale ; il est possible que des affections systémiques à l'origine des fluctuations de la PA soient plus fréquemment liées à un AVC par rapport à des affections qui provoquent une HTA constante. Il est donc indispensable de rechercher toutes les causes d'une HTA, même lorsque la PA est dans les normes.
VI. Examens complémentaires pour rechercher les causes d'une HTA et pour la confirmer
Un bilan biochimique de base, une analyse d'urine, un ionogramme et un dosage de la T4 chez le chat pour la recherche d'une hyperthyroïdie sont nécessaires ; parfois une échographie abdominale est indiquée afin de rechercher aussi une masse surrénalienne pouvant être à l'origine d'un hyperaldostéronisme chez le chat ou d'un phéochromocytome chez le chien. En cas de suspicion d'une HTA, les autres organes cibles doivent être recherchés pour d'éventuelles lésions ; un examen du fond d'œil peut aider au diagnostic d'une HTA chez des animaux avec un doute.
Une échocardiographie peut également mettre en évidence des lésions cardiaques en faveur d'une HTA telles qu'une hypertrophie du myocarde, symétrique ou asymétrique, une dilatation de l'aorte (rarement avec un anévrisme), une insuffisance aortique, une dysfonction diastolique. Ces éléments peuvent être à la fois utiles pour la confirmation d'une HTA mais aussi pour la réalisation d'une anesthésie la moins risquée possible, pour la réalisation d'une IRM.
VII. Prise en charge
En cas de suspicion d'AVC d'origine cardiaque, il est nécessaire de traiter la cardiopathie sous-jacente (traitement de l'insuffisance cardiaque, traitement de l'arythmie, antibiothérapie en cas d'endocardite), mais aussi de mettre en place un traitement pour éviter la formation de nouveaux thrombus. Pendant l'hospitalisation une héparinothérapie avec de l'héparine de bas poids moléculaire est mise en place (enoxaparine 1,5 mg/kg ou 80 à 100 UI/kg SC BID ou TID). Du clopidogrel, un antiagrégant plaquettaire, à la dose de 2-3 mg/kg chez le chien et 18,75 mg chez le chat est utilisé dès que l'animal peut avaler. Au retour à la maison du rivaroxaban, un anticoagulant qui inhibe le facteur Xa, peut remplacer l'héparine notamment pour les cas avec un thrombus visible dans le cœur. Les doses recommandées sont comme suit :
- chien : 0,5-1 mg/kg PO toutes les 24 heures ou toutes les 12 heures en se basant sur les données in vivo ou 1-2 mg/kg PO toutes les 24 heures ;
- chat : 1,25-2,5 mg/chat PO toutes les 24 heures.
En cas d'hypertension, un antihypertenseur associé au traitement de la cause initiale doit être instauré. L'amlodipine est l'antihypertenseur de 1ère intention.
En conclusion, les AVC d'origine cardiaque sont rares mais un bilan cardiaque (échocardiographie et mesure de pression artérielle) sont fortement conseillés lors de suspicion clinique ou de diagnostic d'un AVC par IRM cérébrale.
Bibliographie
- ETTINGER SJ, FELDMAN EC, COTE, E. (Eds). Ettinger's Textbook of Veterinary Internal Medicine-eBook. Elsevier Health Sciences, 2024.
- ESCUDERO-MARTINEZ I, MORALES-CABA L, SEGURA T. Atrial fibrillation and stroke: A review and new insights. Trends Cardiovasc Med, 2023;33:23-9.
- FESKE SK. Ischemic stroke. Am J Med, 2021;134:1457-64.
- GAROSI LS. Cerebrovascular disease in dogs and cats. Vet Clin North Am Small Anim Pract, 2010;40:65-79.
- WHITTAKER DE, DREES R, BELTRAN E. MRI and clinical characteristics of suspected cerebrovascular accident in nine cats. J Feline Med Surg, 2018;20:674-84.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Bactériurie subclinique chez les chats atteints de maladie rénale chronique : impact sur la progression de la maladie et la mortalité - étude rétrospective sur 287 chats
Erwan LE CORRE
Coauteurs : N. JOUSSERAND, C. MAUREY, E. KRAFFT, R. LAVOUÉ, A. DRUT, A. ROSTANG
Introduction
Les maladies rénales chroniques (MRC) constituent un facteur prédisposant aux bactériuries subcliniques (BSU) chez le chat[1],[2]. La présence d'une BSU chez ces animaux soulève des questionnements quant à ses conséquences cliniques potentielles, notamment le risque d'infection ascendante pouvant conduire à une pyélonéphrite et aggraver la MRC[3]. À ce jour, peu d'études ont évalué l'impact de la BSU sur la mortalité et la progression de la MRC. Par ailleurs, aucune recommandation ne guide sa prise en charge.
Matériel et méthodes
Il s'agit d'une étude rétrospective multicentrique réalisée chez des chats suivis dans 4 centres hospitaliers entre 2015 et 2024. Les critères d'inclusions dans les deux cohortes (avec ou sans BSU) comprenaient :
- un diagnostic de MRC
- un résultat de culture urinaire disponible après cystocentèse
- l'absence de signes cliniques d'infection du bas appareil urinaire.
L'analyse de survie a été effectuée à l'aide de l'estimateur de KAPLAN-MEIER et un modèle de COX multivarié. La progression de la MRC était définie comme une augmentation de la créatininémie supérieure à 25% dans les 12 mois.
Résultats
Deux cent quatre-vingt-sept chats correspondaient aux critères d'inclusion (109 dans le groupe BSU, 178 dans le groupe contrôle). Les femelles présentaient un risque significativement plus élevé que les mâles de présenter une BSU (83%, p<0,001). L'espèce bactérienne la plus fréquemment isolée était Escherichia coli (68%), suivie d'Enterococcus spp. (17%).
La présence d'une BSU n'a pas significativement influencé la mortalité (hazard ratio [HR]=0,68; intervalle de confiance [IC] à 95%=0,39-1,16; p=0,16), ni la progression de la MRC (p=0,84). En revanche, la créatininémie (HR=1,02; IC95%=1,00-1,03; p=0,01) et la note d'état corporel (HR=0,80; IC95%=0,67-0,95; p=0,01) étaient associées à une augmentation du risque de mortalité.
Un traitement antibiotique a été initié dans 78% des cas. L'antibiothérapie n'a pas permis de stériliser les urines à long terme dans 62% (37/60) des cas où un suivi est disponible. Lors de persistance ou de récidive, la bactériurie restait principalement subclinique (69%, 36/52), bien qu'une cystite bactérienne (17%, 9/52) ou une pyélonéphrite (13%, 7/52) ait été observée pour quelques animaux, dans des proportions similaires entre les groupes traités et non-traités par antibiotique. La persistance ou la récidive d'une BSU n'a pas été associée à une progression de la MRC (p=0,22).
Discussion et conclusion
Les résultats de notre étude n'ont pas montré d'influence significative de la présence d'une BSU sur la mortalité et la progression d'une MRC chez le chat. Ces observations sont cohérentes avec des études antérieures sur des chats atteints de MRC et présentant une culture urinaire positive (infection du tractus urinaire et BSU) [3],[4]. Nos résultats ne soutiennent pas l'utilisation systématique d'antibiotiques dans cette situation. Des études prospectives sont nécessaires pour mieux comprendre l'impact de l'absence d'antibiothérapie et établir des recommandations fondées sur des preuves solides.
Bibliographie
- MOBERG FS, LANGHORN R, BERTELSEN PV, et al. Subclinical bacteriuria in a mixed population of 179 middle-aged and elderly cats: a prospective cross-sectional study. J Feline Med Surg. 2020;22(8):678-684.
- PUCHOT ML, COOK AK, POHLIT C. Subclinical bacteriuria in cats: prevalence, findings on contemporaneous urinalyses and clinical risk factors. J Feline Med Surg. 2017;19(12):1238-1244.
- HINDAR C, CHANG YM, SYME HM, JEPSON RE. The association of bacteriuria with survival and disease progression in cats with azotemic chronic kidney disease. J Vet Intern Med. 2020;34(6):2516-2524.
- WHITE JD, STEVENSON M, MALIK R, SNOW D, NORRIS JM. Urinary tract infections in cats with chronic kidney disease. J Feline Med Surg. 2013;15(6):459-465.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Biopsie intestinale en pleine épaisseur au tru-cut : une technique sûre, rapide, efficace et moins invasive que la biopsie incisionnelle standard chez les chiens et les chats
Romane SAVY
Coauteurs : Adrien MAGGIAR, DVM Juliette ANDRÉJAK-BÉNIT, DVM, MSc Julien MICLARD, DVM, DECVP Delphine SARRAN, DVM, DECVS Jean-Philippe BILLET, DVM, DECVS
Introduction
Les maladies intestinales chroniques, notamment les MICI et lymphomes, sont fréquentes chez les chiens et chats. Leur diagnostic repose sur des biopsies transpariétales obtenues par laparotomie ou laparoscopie. La méthode de référence consiste en une biopsie incisionnelle, qui n'est toutefois pas exempte de limitations, notamment en raison de sa durée de réalisation, de son caractère invasif et des complications potentielles qu'elle peut engendrer, en particulier chez les patients présentant une hypoalbuminémie ou une altération de l'intégrité pariétale intestinale.
Objectif : Évaluer la faisabilité, la sécurité et la qualité diagnostique d'une alternative : la biopsie transpariétale à l'aide d'un TRU-CUT à coupe semi-automatisée par laparotomie.
Matériel et méthodes
Vingt animaux (3 chiens et 17 chats) atteints de troubles gastro-intestinaux chroniques (>3 semaines) ont été inclus prospectivement entre 2022 et 2023. Chaque animal a reçu des biopsies sur les trois segments de l'intestin grêle (duodénum, jéjunum, iléon), à la fois par technique incisionnelle classique et par TRU-CUT (aiguille semi-automatisée de 16G x 9 cm, angulation de 45°). Les échantillons ont été évalués histologiquement selon le WSAVA GI STANDARDISATION GROUP et par immunohistochimie (CD3, CD20). Le temps de prélèvement, les complications per- et post-opératoires et la qualité des échantillons ont été enregistrés. La présence de maladies inflammatoires ou tumorales, le type d'infiltrat et la qualité du tissu ont été comparés entre les deux techniques.
Résultats
Les biopsies TRU-CUT ont été significativement plus rapides (262 ± 75 s) que les biopsies incisionnelles (599 ± 204 s ; p < 0,000001). Un examen échographique de contrôle a été réalisé en moyenne deux jours après l'intervention chirurgicale et n'a mis en évidence aucune anomalie dans 95 % des cas. Trois complications postopératoires ont été observées : deux mineures (hématome, sérome) secondaires au léchage du site de laparotomie et une majeure (péritonite septique à la suite d'une déhiscence sur un site de biopsie incisionnelle dans un contexte de péritonite biliaire pré-opératoire).
L'analyse histologique a montré une concordance diagnostique de 100 % entre les deux techniques pour distinguer MICI et lymphome. Concernant le type d'infiltrat inflammatoire (lymphoplasmocytaire, éosinophilique ou neutrophilique), la concordance entre les deux techniques variait entre 90 et 100 %. Les deux méthodes ont identifié 16 MICI et 5 lymphomes. Cinq des quarante biopsies incisionnelles réalisées ont été insuffisantes pour permettre une évaluation histologique. L'ensemble des quarantes biopsies TRU-CUT ont été diagnostiques. L'immunohistochimie a permis de confirmer les distinctions histopathologiques entre les MICI et les lymphomes (CD3+, CD20+).
Discussion
La biopsie par TRU-CUT transpariétale via laparotomie est une méthode rapide, fiable et moins invasive que l'incisionnelle. Elle permet un gain de temps significatif, ce qui réduit la durée anesthésique. Contrairement aux incisions, elle nécessite un unique point simple, limitant le risque de déhiscence. Les sites de prélèvement, en particulier au niveau de l'iléon, sont plus facilement accessibles sans manipulation excessive. Le nombre idéal de biopsies reste néanmoins à étudier afin d'assurer le diagnostic lésionnel.
La technique semble sûre, même chez les animaux à risques. L'absence de complication liée aux prélèvements par TRU-CUT est un atout majeur, particulièrement dans un contexte d'hypoalbuminémie ou de paroi intestinale altérée. Le coût du dispositif (~18EUR) est raisonnable et rend son usage envisageable même en routine. La longueur recommandée de TRU-CUT est de 9 cm, une longueur supérieure étant plus difficile à manipuler. De même le caractère semi-automatique est à respecter, permettant un contrôle de la profondeur lors de l'insertion de l'instrument, en comparaison avec un système automatique.
L'angle de prélèvement à 45° permet de limiter le risque de léser le bord mésentérique, de maintenir le stylet interne du TRU-CUT en contact étroit avec la paroi intestinale pendant la biopsie garantissant un bon prélèvement et pourrait améliorer l'étanchéité des tissus une fois l'instrument retiré.
Les limites de l'étude sont la petite taille de l'échantillon et l'absence de clonage PCR pour les lymphomes.
Conclusion
La biopsie transpariétale au TRU-CUT par laparotomie est une alternative sûre, rapide et efficace à la technique incisionnelle pour le diagnostic des MICI et lymphomes intestinaux chez le chien et le chat. Elle permet un prélèvement de qualité avec un risque réduit de complications, et pourrait devenir la méthode de choix, notamment dans les cas cliniques complexes ou à risques. Une hospitalisation post-opératoire de 48 h reste recommandée.
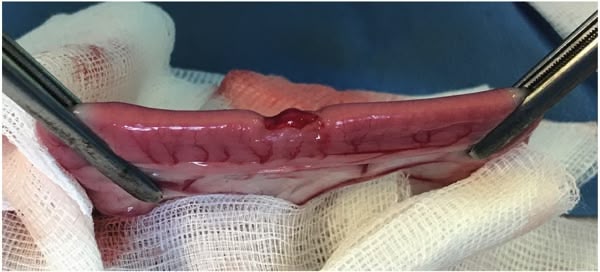
Figure 1
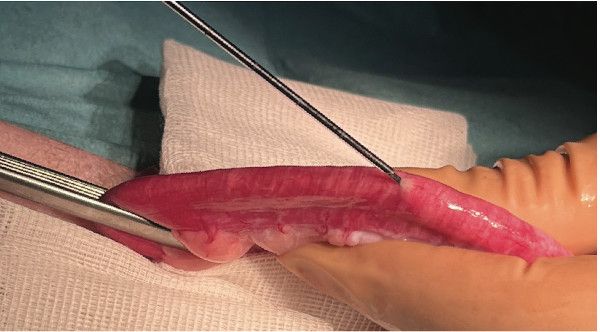
Figure 2
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Blocs cellulaires basés sur des biopsies par aspiration à l'aiguille fine de tumeurs comme alternative aux biopsies chirurgicales
Lucile DUNAND
Coauteurs : DE COCK Hilde, DE ROOSTER Hilde
Introduction
Cette étude a pour objectif de décrire la méthodologie de la technique de bloc cellulaire, encore peu utilisée en médecine vétérinaire, et de mettre en lumière son utilité diagnostique dans l'évaluation des masses tumorales chez les chiens et les chats. Elle vise également à comparer les résultats obtenus par trois techniques diagnostiques pathologiques, dont la technique de bloc cellulaire.
Matériel et méthodes
Il s'agit d'une étude prospective portant sur 41 masses suspectées d'être néoplasiques chez 4 chats et 37 chiens. Pour chaque masse, un examen cytologique par aspiration à l'aiguille fine, un examen histopathologique à partir de matériel prélevé par aspiration à l'aiguille fine (technique de bloc cellulaire) et un examen histopathologique de routine sur des biopsies réalisées après ablation chirurgicale ont été effectués. Plusieurs protocoles ont été testés sur les blocs cellulaires afin de déterminer la méthode optimale garantissant une précision maximale des résultats. Lorsque nécessaire, une analyse immunohistochimique a été réalisée pour affiner ou confirmer le diagnostic.
Résultats
L'ajout d'encre de marquage tissulaire bleue dans un environnement de formol, combiné à l'utilisation de matériel provenant de 10 aspirations à l'aiguille fine, a amélioré la visualisation microscopique et la précision diagnostique de la technique de bloc cellulaire. Globalement, 27 des 41 blocs cellulaires (66 %) ont produit des résultats histologiques complètement compatibles avec ceux obtenus par l'histopathologie de routine. Quatre des 41 échantillons (10 %) ont fourni un diagnostic partiellement compatible, tandis que 7 échantillons (17 %) n'ont pas permis de poser de diagnostic, en raison d'un rendement cellulaire insuffisant. Enfin, dans 3 cas sur 41 (7 %), les résultats obtenus par la technique de bloc cellulaire différaient de ceux de l'histopathologie classique. Parmi les différents types de tumeurs, ce sont les tumeurs mésenchymateuses pour lesquelles cette technique s'est révélée la moins sensible.
Discussion
Dans 34 % des cas où les résultats n'étaient pas totalement compatibles avec ceux de l'examen histologique de routine, la faible cellularité obtenue par les prélèvements répétés d'aspiration à l'aiguille fine semble être une cause majeure. De plus, une variabilité significative du succès de la technique a été observée en fonction du type de tumeur. La difficulté à diagnostiquer les tumeurs mésenchymateuses pourrait être liée à leur faible exfoliation cellulaire. En effet, ces tumeurs, comme les sarcomes des tissus mous, libèrent peu de cellules, ce qui entraîne une insuffisance de matériel lors de l'aspiration à l'aiguille fine et complique l'évaluation.
Conclusion
La technique de bloc cellulaire constitue une méthode mini-invasive, simple à réaliser et peu coûteuse. Elle offre une alternative intéressante à la biopsie, en particulier chez les patients présentant des comorbidités ou des risques liés à l'anesthésie. Cette technique améliore le taux de diagnostic par rapport à la cytologie standard, permettant un diagnostic histologique complet ou partiel dans 76 % des cas. Cependant, une confirmation histologique reste toujours recommandée pour valider les résultats obtenus par cette méthode.
Bibliographie
- GHISLENI G, ROCCABIANCA P, CERUTI R, STEFANELLO D, BERTAZZOLO W, BONFANTI U, CANIATTI M. Correlation between fine-needle aspiration cytology and histopathology in the evaluation of cutaneous and subcutaneous masses from dogs and cats. Veterinary Clinical Pathology. 2006; 35(1):24 30.
- KROGERUS L, KHOLOVÁ I. Cell Block in Cytological Diagnostics: Review of Preparatory Techniques. Acta Cytol. 2018;62(4):237-243.
- NATHAN NA, NARAYAN E, SMITH MM, HORN MJ. Cell block cytology. Improved preparation and its efficacy in diagnostic cytology. Am J Clin Pathol. 2000;114:599-606.
- MARRINHAS C et al. Needle rinse cell blocks as an ancillary technique: Diagnostic and clinical utility in gastrointestinal neoplasia. Vet Clin Pathol. 2022;50:47-54.
- NGA ME, LIM GL, BARBRO N, CHAN NH. Successful retrieval of fine-needle aspiration biopsy material from previously stained smears for immunocytochemistry: a novel technique applied to three soft tissue tumors. Mod Pathol. 2005; 18(5):728-732.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Ca urge, il convulse !
Saint-Laurent-Du-Var, France
Nantes, France
I. Introduction
Les épisodes épileptiques, notamment un status epilepticus (SE) et les crises convulsives groupées (cluster seizures, CS), sont des urgences neurologiques fréquentes qui sont associées à une morbidité et une mortalité élevées. Le SE, en particulier, reste un défi thérapeutique avec un taux de mortalité de 25,3 % à 38,5 %, pouvant entraîner des lésions cérébrales irréversibles et des complications systémiques. Les crises peuvent rapidement devenir auto-entretenues et réfractaires aux anticonvulsivants classiques. [1]
II. Définitions
- Crise épileptique : manifestation transitoire de signes moteurs/autonomiques/sensitifs, secondaire à une activité neuronale cérébrale anormale/excessive, souvent autolimitée.
- Status epilepticus (SE) : couramment défini comme une activité convulsive durant plus de 5 minutes, ou comme la survenue de deux crises ou plus sans reprise de conscience.
- Crises groupées (cluster) : plusieurs crises en 24 h (animal normal entre les crises).
- Status epilepticus réfractaire : SE qui ne répond pas au traitement de première intention.
- Status epilepticus superréfractaire : SE qui continue ou rechute après 24 h de traitement avec des agents anesthésiques.
III. Physiopathologie d'un status epilepticus
Incapacité d'arrêter l'activité épileptique. Le SE est une affection résultant soit de la défaillance des mécanismes responsables de la fin des crises, soit de l'initiation de mécanismes conduisant à des crises anormalement prolongées (après T1 = 5 minutes) ; elle peut avoir des conséquences à long terme (après T2 = 30 minutes), notamment la mort neuronale et l'altération des réseaux neuronaux. [2,3]
IV. Effets systémiques du status epilepticus
Le SE a des effets systémiques en deux phases :
- Phase I (SE compensé) : l'activité des crises provoque une stimulation autonome accrue, entraînant hypertension, tachycardie, hyperglycémie, hyperthermie et d'autres troubles métaboliques. La demande cérébrale en oxygène augmente, mais reste compensée.
- Phase II (SE non compensé) : après environ 30 minutes de convulsions continues, la régulation du flux sanguin cérébral échoue, provoquant une hypotension systémique, une hypoxie, une défaillance respiratoire et des troubles métaboliques sévères, aggravant les lésions neuronales. [3]
V. Causes d'un Status epilepticus
Toute cause pouvant provoquer une crise épileptique peut également provoquer un status epilepticus.
Lors de SE sans historique d'une épilepsie, l'intoxication semble le plus probable.
Un SE peut être la première manifestation d'un événement épileptique, quelle que soit la cause !
VI. La démarche diagnostique
La démarche diagnostique lors d'un SE est similaire à celle d'une crise convulsive isolée, avec une attention particulière portée à l'anamnèse (antécédents de traumatisme, diabète traité, possible intoxication, événements épileptiques précédents).
Même si l'arrêt de crises et la stabilisation du patient est primordiale lors d'un SE, les premières démarches diagnostiques doivent se faire durant les phases initiales de la prise en charge – notamment l'exploration métabolique :
- Gaz du sang avec une glycémie
- Biochimie de base + numération formule
- Dosage d'acides biliaires et NH3 si possible
- Dosage du traitement antiépileptique si celui est en cours (prélèvement préférable avant dose de charge )
1. Causes métaboliques :
- Intoxications
- Hypoglycémie : insulinome, animaux diabétiques sous traitement, sepsis, animaux jeunes ou de petites races après un jeûne prolongé
- Encéphalose hépatique (shunt porto-systémique, dysplasie microvasculaire, lipidose hépatique)
- Hypo/hypercalcémie
- Hypo/hypernatrémie
- IRA/IRC terminale
- Hypertension artérielle
- Polycythémie
- Carence en thiamine
- Toxiques
2. Causes intracrâniennes :
- Traumatisme
- Accidents vasculaires cérébraux
- Maladies inflammatoires/infectieuses
- Néoplasie (surtout chez le chien)
- Malformations
- Maladies dégénératives (ex. maladie de Lafora)
3. Épilepsie idiopathique
- Première manifestation
- Épilepsie idiopathique traité : dosage de médicament si possible
VII. Le traitement
1. Traitement du status epilepticus
Les recommandations de traitement sont basées sur le consensus de l'ACVIM (American College of Veterinary Internal Medicine) pour la gestion du status epilepticus et des crises groupées chez les chiens et les chats (CHARALAMBOUS et al., cité plus haut).
2. Traitement de première intention
Le traitement des convulsions est une urgence absolue. Il n'est pas nécessaire de réaliser un recueil de l'anamnèse ni un examen clinique approfondi et à a fortiori des examens complémentaires pour commencer à traiter. L'important est l'arrêt des convulsions, pas le diagnostic de la cause. Une hypoglycémie doit cependant être systématiquement écartée car son traitement est spécifique. Le traitement initial des convulsions est non spécifique, c'est à dire commun à tous les chiens et chats qui convulsent. Des adaptations ultérieures auront lieu selon la cause sous-jacente.
a) Molécule
Le traitement de première intention du SE est une benzodiazépine (BZP). Les BZP sont efficaces et très sûres chez le chien comme chez le chat.
Le Midazolam, Hypnovel® ou Midazolam Aguettant®, est considéré comme plus sûre et plus efficace que le Diazépam (Diazépam TVM®).
Il est très simple de se procurer du Diazépam TVM® qui est un médicament vétérinaire, alors qu'il est plus difficile de se procurer du Midazolam car c'est un médicament humain réservé à l'usage hospitalier ; il faut le commander directement auprès du laboratoire AGUETTANT.
La durée d'action mérite d'être considérée dans l'évaluation du prix et la praticité.
Le Diazépam n'est pratiquement pas efficace par voie IM et a fortiori par voie SC.
La voie intraveineuse (IV) est une voie idéale, mais elle n'est pas toujours facile à mettre en place chez un animal qui convulse. Une alternative a longtemps été l'utilisation de la voie rectale de Diazépam (en introduisant la seringue sans l'aiguille !), mais une étude relativement récente montre que cette molécule par cette voie rectale ne conduisait à l'arrêt des convulsions que dans 20 % des cas contre 76 % avec le Midazolam administré par voie intranasale (IN) (Charalambous et al., JVIM, 2017). La voie IN est facile et plus rapide encore que la voie IV, c'est pourquoi nous la considérons que la voie de choix si l'animal n'a pas déjà un cathéter.
Il n'y a pas la moitié des cliniques vétérinaires qui possèdent du Midazolam. Ce n'est pas une catastrophe : le Diazépam convient très bien : Cf. l'étude pharmacocinétique de Musulin, Mariani et Papich(2011) et celle de Platt et al. (2000).
b) Dose
On dit souvent que le Midazolam est plus efficace que le Diazépam. Il serait parfois plus juste de dire qu'il est efficace à une dose deux fois moindre. Là où la dose de Midazolam est de 0,25 à 0,5 mg/kg, la dose du Diazépam est de 0,5 à 1 mg/kg. Compte tenu des présentations des spécialités, les volumes sont les mêmes pour les deux molécules/spécialités : 1 ml/10 kg chez le chien pour la dose faible, 1 ampoule de 2 ml de Diazépam /10 kg pour la dose forte (1 mg/kg). Compte tenu de l'innocuité des BZP et de la nécessité d'interrompre urgemment les convulsions, je suggère d'utiliser d'emblée les doses élevées : 0,5 mg/kg pour le Midazolam et 1 mg/kg pour le Diazépam voire le double ! Et afin de ne pas perdre de temps, je suggère de commencer par la voie IN dès l'admission de l'animal puis de mettre en place tranquillement un cathéter sur un animal apaisé.
c) Précaution
Le Diazépam s'utilise uniquement par bolus via le site d'injection du cathéter, tandis que le Midazolam est préféré pour les CRI et il est même efficace par voie IM.
3. Traitement de seconde intention
Si les convulsions persistent après l'administration de deux doses successives de BZP, une troisième injection peut être réalisée. Au-delà, un traitement de deuxième ligne, soit en utilisant un barbiturique (le Phénobarbital), soit en utilisant le Lévétiracétam (une autre BZP).
a) Phénobarbital
À ce stade, le Phénobarbital, Gardénal®, est l'antiépileptique de choix. On provoque ainsi un coma barbiturique. Ce barbiturique, d'une grande efficacité clinique et doté d'une longue demi-vie d'élimination, est administré à la dose de charge allant jusqu'à 15 mg/kg (10 mg/kg chez le chat) par voie intraveineuse stricte, sur une durée d'environ 10 minutes. Une pratique prudente consiste à réaliser 4 injections de 4 mg/kg en une heure (donc à 15 minutes d'intervalle). Les injections doivent être lentes. Le Gardénal® coûte 160 € pour traiter un Labrador ! La forme de Gardénal disponible en officine est très peu concentrée d'où la nécessité de grands volumes : 1 ml/4 kg.
Il est impératif de s'assurer de la parfaite position du cathéter intraveineux, car toute extravasation du Gardénal® expose à un risque élevé de phlébite dramatique, longue à traiter. Si du Phénobarbital a été injecté en périveineux il faut « rincer » le pourtour de la veine avec de la Lidocaïne à 2 %, le risque de phlébite diminue alors considérablement.
La dose de charge est obtenue par de petites injections lentes fractionnées sur 10 minutes, avec une surveillance continue de la respiration, le Phénobarbital étant fortement dépresseur respiratoire. Le clinicien doit donc être prêt à intuber l'animal, voire à instaurer une ventilation assistée au ballon type Ambu® si nécessaire. Si l'animal n'est pas intubé, nous conseillons l'injection de Maropitant car il est exposé aux pneumonies par fausse déglutition.
Il n'est pratiquement pas possible qu'un animal convulse encore sous Gardénal® à dose élevée, la question est de trouver la dose qui lui permette encore de respirer spontanément... Si le contrôle des crises est obtenu à une demi-dose ou quart de dose (4 mg/kg), il faut se contenter de cette dose efficace.
b) Lévétiracétam
En alternative, le Lévétiracétam, Keppra®, peut être administré à la dose de charge de 30 à 60 mg/kg IV (30 mg/kg chez le chat) en dix minutes toutes les 6 à 8 heures.
c) Anesthésiques
La Kétamine peut être utilisée sous forme de perfusion continue, après une dose initiale allant jusqu'à 5 mg/kg IV, suivie d'une perfusion d'entretien à raison de 5 mg/kg/heure.
Le Propofol constitue une option, avec une dose de charge de 2 à 5 mg/kg IV, suivie d'une perfusion continue (CRI) de 0,1 à 0,5 mg/kg/min.
Le traitement étiologique, le traitement des complications, le traitement de soutien et le sevrage seront exposés à l'oral.
Bibliographie
- BLADES GOLUBOVIC S, ROSSMEISL JH Jr. Status epilepticus in dogs and cats, part 1: etiopathogenesis, epidemiology, and diagnosis. J Vet Emerg Crit Care (San Antonio). 2017;27(3):278-287. doi:10.1111/vec.12605
- CHARALAMBOUS M et coll. ACVIM Consensus Statement on the management of status epilepticus and cluster seizures in dogs and cats. J Vet Intern Med. 2024;38(1):19-40. doi:10.1111/jvim.16928
- PLATT S. Et coll. Small Animal neurological Emergencies, 1st ed. Manson Publishing Ltd.: 2012
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Ca urge, il est dans le coma !
Ollioules, France
Montpellier, France
I. Introduction
L'évaluation du niveau de conscience d'un animal est l'un des éléments les plus importants de l'examen neurologique. L'altération de la conscience est généralement liée à des anomalies du tronc cérébral et/ou du cerveau. L'évaluation de la conscience repose sur les réponses de l'animal, appropriées ou non, à son environnement, et sur les stimuli, normaux ou non, dans son environnement.
Un comportement inapproprié ou une diminution du niveau de conscience sont des indicateurs forts de maladie intracrânienne. Cependant, une maladie systémique grave, telle qu'une insuffisance cardiorespiratoire, une maladie métabolique et l'exposition à des toxines exogènes, peut également entraîner des effets secondaires produisant des signes cliniques similaires, voire identiques.
1. Niveaux de conscience
L'état mental peut être classé comme :
- Vigilant et alerte : normal.
- Léthargique : conscient, mais avec une activité réduite et une réactivité diminuée aux stimuli environnementaux. Il peut y avoir une tendance accrue à dormir en l'absence de stimulation. Il s'agit d'un signe non spécifique, car il peut résulter d'une maladie systémique aussi bien que d'une atteinte du système nerveux central (SNC).
- Stuporeux : dort ou ne réagit pas aux stimuli inoffensifs tels que le bruit, mais réagit aux stimuli douloureux.
- Comateux : état d'inconscience. Ne peut être réveillé, même par des stimuli douloureux, bien que certains réflexes simples puissent être présents. Cela résulte également d'une atteinte diffuse des deux hémisphères cérébraux et/ou du tronc cérébral.
Attention : la stabilisation cardiovasculaire avant l'évaluation neurologique est nécessaire !
II. Définitions importantes
- La PIC (pression intracrânienne) est la pression exercée à l'intérieur du crâne par le contenu intracrânien. Chez le chien, la PIC normale se situe entre 5 et 12 mm Hg.
- La PPC (pression de perfusion cérébrale) : la pression du sang circulant vers le cerveau.
Dépend d'un équilibre entre la PAM (pression artérielle moyenne) et la PIC : PPC = PAM - PIC - Une augmentation de la PIC peut avoir un impact significatif sur la PPC, entraînant une diminution de la perfusion cérébrale.
- Le DSC (débit sanguin cérébral) est la vitesse à laquelle le sang est acheminé vers le cerveau. Il est principalement déterminé par la PPC. Le DSC est régulé par l'activité métabolique cérébrale, la pression partielle en oxygène et la pression partielle en dioxyde de carbone. La relation entre la PPC, le DCF et la résistance vasculaire cérébrale (RVC) est la suivante : DSC = PPC / RVC
- La RVC dépend principalement de la viscosité du sang et du diamètre des vaisseaux.
- L'autorégulation est la capacité intrinsèque du cerveau à maintenir une perfusion cérébrale adéquate malgré les variations de pression artérielle.
- La compliance est la capacité du contenu intracrânien à diminuer de volume afin de maintenir une pression intracrânienne (PIC) normale.
- Augmentation de la pression intracrânienne = diminution de la perfusion cérébrale = ischémie cérébrale
1. Pression intracrânienne – homéostase
L'espace intracrânien est occupé par trois éléments : le parenchyme cérébral, le LCR et le sang. Toute modification de l'un de ces trois éléments entraîne des mécanismes compensatoires destinés à rétablir l'équilibre et à maintenir une pression intracrânienne stable. La pression exercée entre le cerveau et le crâne est appelée pression intracrânienne (PIC), qui se situe normalement entre 5 et 12 mm Hg chez les chiens et les chats.
Principaux mécanismes compensatoires :
- Réduction de la quantité de LCR (augmentation de la résorption, diminution de la production et évacuation vers l'espace sous-arachnoïdien médullaire)
- Diminution du volume sanguin (donc réduction de la perfusion sanguine)
III. Signes d'une hypertension intracrânienne
1. Triade de Cushing
Réaction compensatoire secondaire à une augmentation de la pression intracrânienne (plus précisément à la diminution de la perfusion cérébrale).
Physiopathologie : une diminution du flux sanguin vers les centres vasomoteurs du tronc cérébral entraîne une réduction de l'élimination du dioxyde de carbone. L'élévation locale de la concentration en CO₂ stimule alors le système nerveux sympathique à augmenter la pression artérielle moyenne (PAM). Il en résulte une hypertension artérielle systémique, destinée à maintenir une perfusion cérébrale adéquate.
Les barorécepteurs situés dans l'aorte et le sinus carotidien détectent cette élévation de pression et envoient un signal aux centres vagaux du tronc cérébral. Cela entraîne une bradycardie réflexe : c'est le réflexe de Cushing.
Ainsi, l'association d'une hypertension artérielle et d'une bradycardie peut indiquer une élévation de la PIC chez un patient présentant un traumatisme crânien.
Triade de Cushing :
- Bradycardie
- Hypertension artérielle
- Respiration ataxique — respiration irrégulière en fréquence, rythme et amplitude
L'altération de l'état mental de l'animal est indispensable pour suspecter une hypertension intracrânienne !
2. Autres signes évocateurs d'une HIC
- Hypotonie des membres
- Nystagmus positionnel (+ état de vigilance diminué / stupeur / coma) : signe d'une hernie du cervelet par le foramen magnum
- Absence de réflexe oculo-céphalique : signe de compression du tronc cérébral
IV. Causes les plus fréquentes d'une hypertension intracrânienne
- Lésions avec effet de masse — néoplasie cérébrale, abcès cérébral
- Traumatisme crânien
- Accident vasculaire cérébral hémorragique
- Hypertension artérielle (rare)
- Malformations — hydrocéphalie hypertensive (rare)
- Maladies infectieuses — PIF !!!
V. Prise en charge du patient en hypertension intracrânienne
Les 3 objectifs principaux vont être de :
- Réduire la pression intracrânienne (PIC) ;
- Maintenir une perfusion cérébrale adéquate (pression de perfusion cérébrale, PPC) ;
- Prévenir l'aggravation des lésions cérébrales (ischémie, œdème).
Il est important de respecter des mesures générales afin de prévenir une aggravation du patient et pour prévenir toute augmentation de la PIC.
- Stabilisation vitale (ABC) : assurer la ventilation, le dégagement des voies respiratoires et la circulation. Les patients vétérinaires peuvent avoir subi un traumatisme inconnu nécessitant un dépistage d'autres lésions traumatiques, comme des radiographies thoraciques et abdominales. Par ailleurs, si un scanner cérébral est déjà réalisé ou envisagé en raison de préoccupations cliniques concernant une pathologie supplémentaire, un scanner thoracique et/ou abdominal peut être ajouté. Obtenir une pression artérielle systolique > 100 mmHg grâce à la fluidothérapie (bolus de cristalloide isotonique 10-20 ml/kg sur 10-15 min ou hypertonique 2-4 ml/kg sur 10-15 min)
- Oxygénothérapie si hypoxie. Maintenir une Sp02 > 94 %
- Éviter l'hyperthermie (augmente la consommation d'oxygène cérébral or nous voulons mettre le cerveau au repos pour diminuer son métabolisme de base).
- Éviter les manipulations brutales et assurer l'analgésie (stimulation douloureuse → élève la PIC). Considérer des CRI de fentanyl, des injections de méthadone (pouvoir émétisant < morphine)
- Tête surélevée de 15–30°, cou dégagé → favorise le drainage veineux cérébral vers le cœur et la perfusion cérébrale tout en diminuant la PIC
- Éviter les vomissements (vomissement → augmentation de la PIC)
- Éviter les prises de sang jugulaires (augmente la PIC)
- Favoriser la sédation du patient pour prévenir l'agitation et l'augmentation de la PIC associée
- L'évaluation neurologique du patient atteint d'HTIC doit être réalisée plusieurs fois par jour en s'aidant du Score de Glasgow modifié.
VI. Traitement médicamenteux de l'hypertension intracrânienne
Les agents hyperosmolaires, le plus souvent le NaCl hypertonique (3 %, 7,5 %, 23,4 %) ou le mannitol, sont couramment utilisés pour améliorer la PAM et réduire l'œdème interstitiel contribuant à l'HIC.
Des études comparatives en médecine humaine suggèrent que le NaCl hypertonique pourrait être plus efficace pour diminuer la pression intracrânienne. Il présente également l'avantage d'apporter un soutien aux patients hypovolémiques, contrairement au mannitol (qui a lui un effet diurétique donc contre-indiqué chez les patients hypovolémiés). Le furosémide pour réduire l'œdème cérébral n'est pas recommandé. Le choix entre les agents hyperosmolaires est souvent basé sur des critères supplémentaires du patient, notamment l'état d'hydratation et une hypernatrémie préexistante. Une hémorragie intracrânienne ou d'autres perturbations de la barrière hémato-encéphalique permettent aux molécules osmotiquement actives administrées de s'accumuler dans le crâne et d'entraîner de l'eau. Cela peut entraîner des complications similaires à celles de l'HIC et de l'œdème cérébral.
Le choix entre le mannitol et le NaCl hypertonique en médecine vétérinaire est également incertain. Une étude pilote menée auprès de deux chats et d'un chien a montré qu'en dose unique, le mannitol et le sérum physiologique hypertonique à 3 % étaient tous deux efficaces pour réduire la pression intracrânienne et augmenter la pression de perfusion cérébrale.
Les liquides hyperosmolaires sont le plus souvent administrés sous forme de bolus plutôt que de perfusions continues: 0,5 a 1 g/kg de Mannitol sur 20 min ou un bolus de 2 a 4 ml/kg de NaCl hypertonique. En humaines, les perfusions continues de thérapie hyperosmolaire pour traiter l'HIC sont sûres et associées à une amélioration de la survie à 90 jours. Il n'existe actuellement aucune information concernant les perfusions continues d'agents hyperosmolaires chez les chiens ou les chats atteints de traumatisme crânien.
VII. Autres points important sur la gestion de l'HTIC
1. Corticothérapie
- Indiquée seulement en cas de tumeur, méningiome, méningite.
- Ex : dexaméthasone 0,1–0,2 mg/kg IV.
- Contre-indiquée en cas de traumatisme crânien (risque aggravation).
2. Contrôle de l'activité cérébrale
- Anticonvulsivants : si crises → diazépam, midazolam, phénobarbital.
- Sédation (propofol, midazolam, fentanyl, etc.) si agitation → ↓ consommation O₂ cérébrale et PIC.
3. Ventilation & gaz du sang
- Objectif PaO₂ > 100 mmHg (éviter hypoxie).
- Objectif PaCO₂ : 35–40 mmHg (normocapnie).
→ Hyperventilation entraine une vasodilatation cérébrale.
→ Hypoventilation entraine une vasoconstriction cérébrale contrôlée.
4. Mesures complémentaires
- Éviter hyperglycémie et hypoglycémie (surveillance glycémie).
- Antibiotiques si suspicion de méningite/infection intracrânienne.
- Chirurgie décompressive (craniectomie, drainage hématome, exérèse tumeur) si cause chirurgicale.
5. Surveillance
- Score neurologique (ex. échelle de Glasgow modifiée vétérinaire).
- Paramètres vitaux (FR, FC, PAM, SpO₂).
- Signes de herniation cérébrale : mydriase unilatérale, anomalies respiratoires, bradycardie.
Le traitement de l'HTIC chez l'animal repose sur osmothérapie (mannitol ou NaCl hypertonique), maintien de la perfusion et de l'oxygénation cérébrale, contrôle des convulsions et de l'agitation, et mesures générales de nursing.
La chirurgie n'est indiquée que si la cause le nécessite (rarement) et que le personnel compétent est disponible.
Bibliographie
- PLATT S. Et coll. Small Animal neurological Emergencies, 1er ed. Manson Publishing Ltd.: 2012
- KAMEL H et coll. Hypertonic saline versus mannitol for the treatment of elevated intracranial pressure: a meta-analysis of randomized clinical trials. Crit Care Med. 2011;39(3):554–559.
- PATIL H, GUPTA R. A comparative study of bolus dose of hypertonic saline, mannitol, and mannitol plus glycerol combination in patients with severe traumatic brain injury. World Neurosurg. 2019;125:e221–e228.
- BALLOCCO I et coll.. A pilot study evaluating the effect of mannitol and hypertonic saline solution in the treatment of increased intracranial pressure in 2 cats and 1 dog naturally affected by traumatic brain injury. J Vet Emerg Crit Care. 2019;29(5):578–584.
- KUO WK. Head trauma. Vet Clin North Am Small Anim Pract. 2018 Jan;48(1):111-128
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Ca urge, il est paralysé !
Montpellier, France
Paris, France
I. Introduction
La prise en charge d'un animal paralysé peut varier suivant que l'animal est en décubitus et non ambulatoire, plégique ou parétique, qu'il est capable d'uriner de lui-même ou s'il nécessite une assistance. Des complications peuvent en découler incluant escarres, douleur, dysfonctionnement digestif, infection urinaire et perte de masse musculaire pouvant aggraver le tableau clinique initial.
Prendre soin d'un animal paralysé nécessite un soutien médical et infirmier considérable et il sera toujours plus facile de prendre en charge un animal paralysé de petit format (<15 kg) que des chiens de gros gabarit.
Il sera important de porter attention à :
II. Nursing général
Lorsqu'un animal est en décubitus ou non ambulatoire.
- Important d'installer ces patients sur des surfaces fermes et confortables (tapis, matelas anti-escarre), mettre des « donuts » sur les parties du corps favorables aux plaies/escarres (coudes, pointe de la hanche)
- Important de tourner le patient toutes les 4 h : rotation ventrale pour limiter les complications (SDTE) et favoriser la position de décubitus sternal avec rotation des hanches q4h
- Soins buccaux (animaux touchés par des paralysies flasques ou tétanos par exemple) avec chlorhexidine diluée, en surveillant la possible présence d'ulcères buccaux et celle du réflexe de déglutition avant de les nourrir
- Examen physique complet au moins 2 fois par jour (auscultation pulmonaire et température rectale), ces patients étant plus sujets aux bronchopneumonies par fausse déglutition.
- Lubrification cornéenne q4 et contrôle de la possible présence d'ulcère cornéens spécialement pour les races à risque dès que suspicion.
- Bols d'eau et de nourriture facilement accessibles.
- Surveillance régulière du poids (a minima 2 fois par jour) car les animaux immobiles en décubitus ont tendance à prendre du poids (drainage lymphatique perturbé causant œdème et diminution de la production d'urine).
III. Gestion de la douleur
Le confort de nos patients et le contrôle de la douleur doivent être une de nos priorités : nombreuses molécules disponibles à utiliser en injections répétées ou en infusions continues suivant le besoin :
- opioïdes : méthadone, morphine, fentanyl : forts, puissants analgésiques opioïdes. Buprénorphine (0,01-0,02 mg/kg IV q6-8) peut venir en transition lorsque le patient est moins douloureux.
- addition de kétamine en perfusion continue si besoin : Kétamine 2,5-10 μg/kg/min avec initial bolus 0,25-0,5 mg/kg.
- gabapentine : très efficace pour les douleurs neurologiques : 5-20 mg/kg TID PO.
- paracétamol (chien) : 10-15 mg/kg IV q8-12h. INTERDIT chez le chat.
- AINS.
IV. Gestion du stress
Part importante du traitement des animaux paralysés, le stress pouvant engendrer des effets secondaires néfastes sur l'organisme.
- acepromazine : 0,005-0,03 mg/kg q6-8h.
- trazadone 5-10 mg/kg PO jusqu'à q8-12h.
- médétomidine : 0,001-0,003 mg/kg IV bolus ou infusion continue 0,00025-0,003 mg/kg/h.
V. Gestion des mictions
Les chiens présentant une atteinte de type motoneurone central peuvent avoir des difficultés à uriner.
- Expression manuelle q6-8h avec contrôle échographique pour s'assurer que la vessie est vide
- Pose d'une sonde urinaire est parfois nécessaire (ATTENTION À L'HYGIÈNE !).
Les chiens en décubitus vont avoir tendance à s'uriner dessus et peuvent avoir des productions d'urine inadéquates qu'il faudra peut-être traiter.
- Un cathéter urinaire peut être nécessaire.
- Petite dose de furosémide si production d'urine basse et prise de poids/œdème : 0,1-0,2 mg/kg IV.
Risques d'infection urinaire augmentés lorsqu'il y a :
- Incapacité à vidanger une vessie complètement.
- Pose de sonde urinaire et soins urinaires inappropriés.
- Troubles digestifs incluant de la diarrhée.
La pose de cathéter urinaire doit être réfléchie, estimant les avantages et les possibles inconvénients.
La gestion du cathéter urinaire à demeure contre les infections nosocomiales est importante pour prévenir les infections multirésistantes des voies urinaires, mais elle est également vitale pour le bien-être du patient.
Une fois le cathéter urinaire en place, un système de prélèvement fermé doit être fixé pour l'hygiène du patient et pour surveiller le débit urinaire et éviter le développement d'infections.
Système de collecte fermé : il permet le calcul de la diurèse, qui doit être comprise entre 1 et 2 ml / kg/h. Si diurèse diminuée : cathéter obstrué, patient déshydraté, ou qui urine autour de son cathéter, ou production est diminuée.
La mise en place d'antibiotiques en prophylaxie EST CONTRE-INDIQUÉE.
La décision de commencer des antibiotiques lors de la découverte de bactéries sur un culot urinaire pris à partir de la poche d'urine doit être réfléchi.
VI. Gestion des défécations
L'animal paralysé qui ne bouge pas va avoir un transit digestif perturbé, les iléus sont fréquents chez ces patients encore plus s'ils ont subi une intervention chirurgicale. Des laxatifs pourront être donnés si nécessaire même si cela est rarement le cas. Privilégier les alimentations riches en fibres.
VII. Physiothérapie
Le but principal est d'accélérer la récupération de la fonction locomotrice, éviter l'ankylose articulaire, minimiser l'amyotrophie, et améliorer le confort de l'animal. La thérapie aide à maintenir la masse musculaire et la qualité de vie. La considération la plus importante lors de l'ajout d'activité physique à la routine de soins d'un chien avec troubles neurologiques est qu'il existe un juste équilibre entre pas assez et trop.
Certaines procédures peuvent être réalisées dans n'importe quelle structure vétérinaire, telles que massages, mobilisations passives, actives, application de froid (cryothérapie).
VIII. Cas particulier de l'animal paralysé suite à un traumatisme
1. Stabilisation de l'animal
- Évaluation rapide : conscience, respiration, circulation, douleur.
- Stabilisation des fonctions vitales : oxygénation, perfusion IV, analgésie.
- Immobilisation stricte : limiter toute manipulation du rachis. Transport sur un plan dur si suspicion de lésion vertébrale.
2. Prévention des lésions secondaires
- Maintien de la perfusion médullaire : fluidothérapie adaptée, contrôle de la pression artérielle.
- Oxygénation optimale.
- Anti-inflammatoires / corticoïdes : selon les protocoles en vigueur et l'étiologie suspectée.
- La communication avec les propriétaires est très importante et leur consentement à poursuivre des traitements doit être éclairé : le propriétaire doit être conscient des possibles complications à court, moyen et long terme de la prise en charge d'un animal paralysé.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Calicivirus, quel lien avec la gingivostomatite chronique féline ?
Vélizy-Villacoublay, France
I. Introduction
Le calicivirus félin (FCV) est un virus très répandu dans la population féline, avec une prévalence pouvant atteindre 85% dans certaines populations de chats [1]. Il est classiquement associé à des atteintes des voies respiratoires supérieures, des ulcères linguaux, et plus rarement à des formes systémiques graves (calicivirose hypervirulente). Le virus est régulièrement incriminé comme la cause de la gingivostomatite chronique féline (GSCF) car il est présent chez les chats atteints de cette maladie.
II. La gingivostomatite: une maladie inflammatoire multifactorielle
La GSCF est une affection orale douloureuse et souvent débilitante, qui touche entre 0,7% et 12% des chats selon les études. [2] Bien que son étiologie exacte soit encore mal comprise, la communauté scientifique s'accorde sur le fait que c'est une affection dysimmunitaire buccale multifactorielle.
Il est essentiel de bien comprendre que la GSCF est une maladie inflammatoire qui n'est ni contagieuse, ni causée par un seul pathogène mais que les virus impliqués peuvent être transmis sans pour autant causer la maladie. La GSCF résulte d'une réponse immunitaire excessive aux pathogènes de la cavité buccale (bactéries et virus) et pour laquelle il existe des facteurs prédisposants (comorbidités, génétique, stress).
Figure 1 :étiologie de la GSCF de manière simplifiée (image générée par intelligence artificielle)
III. Le calicivirus: quel est son rôle dans la maladie ?
Le FCV est retrouvé chez la quasi-totalité des chats atteints de GSCF, ce qui a longtemps alimenté l'idée qu'il en serait l'agent causal principal. Pourtant, malgré cette association constante, aucun lien de causalité n'a pu être démontré : les postulats de Koch ne sont pas remplis [3,4]. Autrement dit, la simple infection par le calicivirus ne suffit pas à déclencher la maladie. D'ailleurs, le virus peut également être détecté chez une grande proportion de chats cliniquement sains, jusqu'à 83%.
IV. Implications pour la prise en charge
Considérer le FCV comme un facteur parmi d'autres, plutôt que comme la cause unique, change profondément l'approche thérapeutique.
La stratégie repose sur une prise en charge globale et individualisée, avec, dans l'ordre :
- la diminution de la charge bactérienne orale : extractions dentaires multiples ou totales, hygiène buccale ;
- si nécessaire, la modulation de la réponse immunitaire par l'utilisation de traitements immunomodulateurs (interferon omega félin recombiné par voie oromuqueuse ou ciclosporine notamment).
Et, à tout moment, une attention particulière doit être mise sur la gestion de la douleur, la surveillance de l'appétit, de l'état général de l'animal et la diminution des facteurs de stress.
Il est donc inutile de "traquer le calicivirus" seul : traiter la GSCF, c'est d'abord agir sur la charge bactérienne bucco-dentaire puis, si nécessaire moduler la réponse immunitaire.
V. Conclusion
La gingivostomatite chronique féline est une pathologie complexe et multifactorielle. Le calicivirus y est impliqué, mais n'est qu'un facteur parmi d'autres dans cette affection. Il faut dépasser l'idée simpliste du virus unique pour adopter une approche globale, raisonnée et multimodale, essentielle à la réussite thérapeutique.
Si vous voulez en savoir plus sur la GSCF, ses causes et les traitements qui font consensus, je vous recommande de lire le dernier article de synthèse de Maria SOLTERO-RIVEIRA et collaborateurs. [5]
Bibliographie
- DALL'ARA P et coll. Prevalence of serum antibody titres against feline panleukopenia, herpesvirus and calicivirus infections in stray cats of Milan, Italy. Prev Vet Med. 2019; 167:32-38.
- ANDERSON G, HENNET P. Vet Clin North Am Small Anim Pract. 2022; 52(1):159-184
- QUIMBY JM et coll. Evaluation of the association of Bartonella species, feline herpesvirus 1, feline calicivirus, feline leukemia virus and feline immunodeficiency virus with chronic feline gingivostomatitis. 2008; 10(1):66-72
- HOU et coll. European molecular epidemiology and strain diversity of feline calicivirus. Veterinary Record. 2016; 178:114-115
- SOLTERO-RIVEIRA M. et coll. Feline chronic gingivostomatitis current concepts in clinical management. J Feline Med Surg. 2023; 25:1-16
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Cancer : un traitement adapté
Ollioules, France
I. Introduction
De la même façon que pour l'extension, l'objectif est ici de répondre à deux questions :
- est-ce qu'un traitement local est indiqué, si oui lequel ?
- est-ce qu'un traitement systémique est indiqué et si oui, lequel ?
En sachant qu'il y a toujours plusieurs possibilités mais qu'elles sont rarement d'efficacité similaire.
Connaître les traitements envisageables et leur bénéfice permettra finalement de mettre en place la thérapie la plus adaptée à l'animal, son cancer et son foyer. En effet, le traitement de choix théorique n'est pas forcément le traitement de choix individuel.
Nous allons revoir les différents traitements disponibles et discuterons de situations cliniques pour mettre en lumière le fait que le pronostic est central dans la décision thérapeutique et que toute situation doit être adaptée à l'interprétation du pronostic par les membres du foyer.
II. Traitements locaux
- La chirurgie carcinologique est le premier choix dans la majorité des cas où un traitement local est indiqué. Il s'agit d'une chirurgie radicale visant à retirer l'entièreté de la tumeur dès la première intervention. Pour cela, nous utilisons généralement un système de marges avec 2-5 cm macroscopique en fonction des tumeurs et un à deux plans de profondeur. En fonction de la région anatomique, cela n'est pas toujours réalisable et parfois une intervention chirurgicale moins radicale, suivie d'une thérapie locale adjuvante est nécessaire. Il est important de retenir que l'interprétation des marges dépend systématiquement de la procédure chirurgicale. De fait, un compte-rendu opératoire, même bref, est indispensable pour toute chirurgie carcinologique et doit contenir les informations suivantes : intention chirurgicale (volonté de tout retirer ou non) et l'impression chirurgicale (a-t-on retiré l'entièreté du tissu tumoral visible ou non ?).
- La radiothérapie externe par mégavoltage est le premier choix pour les tumeurs intracrâniennes ou les tumeurs nasales. Elle peut également être équivalente à la chirurgie et moins délabrante pour des cas plus particuliers (notamment certains stades d'adénocarcinomes des glandes anales, plasmocytomes oraux, etc.). Enfin, elle est souvent utilisée de manière adjuvante à la prise en charge chirurgicale pour traiter les marges d'exérèse microscopiquement infiltrées lorsqu'elles ne peuvent pas être retirées assez largement chirurgicalement. D'autres types de radiothérapie existent avec notamment la curiethérapie ou la radiothérapie par orthovoltage mais leurs intérêts sont plus limités (intérêt surtout pour des lésions superficielles). À noter que les indications de radiothérapie sont en perpétuelle expansion.
- L'électrochimiothérapie est une thérapie locale permettant de concentrer une grande quantité d'agent cytotoxique dans une zone prédéfinie (en l'occurrence, la tumeur à traiter) par le biais de l'électroporation, aboutissant à la mort des cellules tumorales ciblées. Son utilité principale est le carcinome épidermoïde cutané félin pour lequel elle présente une efficacité équivalente à la chirurgie ou la radiothérapie externe, tout en restant beaucoup plus conservatrice. Elle peut également être utilisée dans de nombreuses indications en traitement alternatif à la chirurgie et/ou la radiothérapie lorsque ceux-ci ne sont pas souhaités mais avec une efficacité et un recul moindres.
- De nombreuses autres thérapies locales alternatives existent, par exemple : l'ablation micro-ondes vise à appliquer un champ magnétique à la tumeur, aboutissant à une augmentation de la température intra-tumorale et à une mort cellulaire par nécrose de coagulation ; la chimio-embolisation consiste en l'administration intratumorale d'agent de chimiothérapie associée à l'embolisation des principales artères nourricières d'une tumeur non résécable chirurgicalement et particulièrement employée pour les tumeurs épithéliales hépatiques massiques ou plus récemment, les carcinomes prostatiques ; enfin le tigilanol tiglate est un agent anti-cancéreux entrainant la nécrose des mastocytomes après injection intra-tumorale.
III. Traitements systémiques
- Les principaux traitements systémiques sont :
- chimiothérapie en hospitalisation (à doses maximales tolérées, administrées à intervalles réguliers) : particulièrement indiquée pour la prise en charge de tumeurs diffuses de haut grade ou de tumeurs solides à haut risque métastatique, sans métastases au diagnostic. ;
- chimiothérapie au domicile (métronomique, petites doses administrées quotidiennement ou presque) : particulièrement indiquée pour la prise en charge de tumeurs diffuses de bas grade ou de tumeurs solides métastasées, de manière palliative ;
- thérapies ciblées (inhibiteurs de tyrosine kinase) : initialement développées pour la prise en charge des mastocytomes pour lesquels ils sont surtout utiles palliativement, ils présentent aujourd'hui un intérêt démontré pour la prise en charge des tumeurs neuro-endocrines, des adénocarcinomes des glandes anales ou encore des GIST métastasés ;
- immunothérapie (encore peu accessible mais en cours de développement) ;
- traitement de support : alimentation, phytothérapie, mycothérapie.
Il est important de saisir la différence entre les deux grands types d'utilisation de la chimiothérapie. La chimiothérapie à doses maximales tolérées interagit avec les cellules en division et entraine la mort cellulaire des cellules en cycle, c'est pourquoi elle est adaptée aux tumeurs de haut grade (avec un fort index de prolifération) et inutile sur les tumeurs de bas grade (qui se divisent très peu). La chimiothérapie métronomique interagit avec le microenvironnement cellulaire, elle inhibe la néoangiogénèse, stimule l'immunité anti-tumorale et inhibe l'immunité protumorale mais interagit très peu avec les cellules tumorales elles-mêmes ; elle est donc adaptée aux tumeurs de bas grade, qui se divisent peu, ou aux tumeurs solides de stade avancé pour lesquelles il est trop tard pour ne s'attaquer qu'aux cellules tumorales.
IV. Adapter le traitement à la situation
1. La lymphadénectomie préventive
En cas de mastocytome, la lymphadénectomie est recommandée en cas de stade 2 où elle diminue le risque de progression tumorale par 5,5 et le risque de décès en lien avec la tumeur par 3,6 [1]. Pour les autres cas, il n'y a pas de consensus mais de plus en plus d'arguments pour préconiser un traitement préventif du NL sentinelle dont on estime que la moitié peut être métastatique malgré une évaluation clinique normale et que jusqu'à 20% des métastases nodales ne sont pas identifiées à l'examen [2–4]. L'intérêt est plus discutable pour des mastocytomes de bas grade et sans infiltration nodale [5]. Finalement, il est recommandé de retirer le NL sentinelle dans tous les cas, mais d'autant plus lorsque le grade est élevé. Cela doit être évalué au cas par cas, en fonction du risque de la procédure ; par exemple, pour un mastocytome en regard du grasset, si le NL sentinelle est le NL poplité, il peut être réséqué facilement, alors que si c'est le NL iliaque médial, la procédure apparait plus complexe et plus risquée.
La lymphadénectomie préventive est également fortement recommandée en cas de mélanome oral. Dans ce cas, il est généralement recommandé de retirer les NL mandibulaires et rétropharyngiens bilatéraux car les métastases sont fréquemment controlatérales et concernent fréquemment plusieurs lymphocentres [6]. La détection du NL sentinelle pourrait permettre de limiter cette recommandation au(x) NL sentinelle(s) en l'absence d'anomalie tomodensitométrique, sous réserve de preuves que cela permette la même efficacité (i.e. que tous les lymphocentres soient détectés d'emblée en cas de drainage multiple). Pour le moment, aucune étude sur l'impact de la lymphadénectomie préventive sur la survie pour les mélanomes oraux n'est disponible, à notre connaissance.
Il s'agit des deux principales indications de lymphadénectomie préventive. À noter qu'elle est aussi fréquemment réalisée en cas de carcinome mammaire (retrait du NL inguinal en même temps que la chaine mammaire) et peut être fortement utile en cas d'adénocarcinome des glandes anales, mais rarement réalisée en l'absence de lymphadénomégalie en raison de la difficulté d'extirpation des NL incriminés (sacré, iliaques internes, iliaques médiaux).
2. Comment ça, on peut traiter des métastases ?
Pour certaines tumeurs, la métastasectomie fait partie du standard de soin. La situation la plus classique est alors la lymphadénectomie thérapeutique. Il s'agit par exemple des insulinomes, des adénocarcinomes des glandes apocrines des sac anaux (AGASA) ou des mastocytomes avec métastase nodale pour qui la lymphadénectomie augmente significativement la durée de vie. Dans le cas des insulinomes, les métastatectomies hépatiques sont également recommandées dans le but de limiter au maximum la charge tumorale et donc l'hypoglycémie associée. Il ne s'agit pas ici de thérapies de la dernière chance ; par exemple un chien atteint d'un mastocytome avec métastase nodale traitée chirurgicalement ou par radiothérapie externe puis par chimiothérapie adjuvante a une durée de vie médiane de 1 an en cas de haut grade et plus de 1,5 an en cas de bas grade [1,7] et un chien avec un AGASA métastasé aux nœuds lymphatiques pris en charge par exérèse de la tumeur et des NL tumoraux, ou par radiothérapie externe par mégavoltage des mêmes sites, présente une durée de vie médiane de 11 à 15 mois [8,9]. Concernant les insulinomes, en cas de métastase nodale, la durée de vie médiane est de l'ordre de 1,5 an après prise en charge chirurgicale ; en cas de métastase à distance, le pronostic post-opératoire est avant tout influencé par la résolution post-opératoire de l'hypoglycémie avec une durée de vie médiane de 1 an en cas de résolution et de 6 mois en l'absence de résolution [10–12].
Enfin, de manière générale, les métastasectomies sont adaptées pour des tumeurs d'évolution lente présentant une métastase au cours de la vie de l'animal ; si l'on revient au cas des AGASA, en cas de métastase nodale à distance de la prise en charge initiale, une prise en charge locale (chirurgie ou radiothérapie) sera à nouveau adaptée malgré le caractère récidivant. La prise en charge locale des métastases est également adaptée en cas de lésion douloureuse ou handicapante ; c'est le cas d'une métastase osseuse isolée douloureuse par exemple (un protocole de radiothérapie antidouleur peut être mis en place) ou en cours de saignement. Pour ces autres situations, l'intérêt de la prise en charge locale de métastase est à évaluer au cas par cas.
3. Au cas par cas
Tout le monde ne souhaitera pas réaliser des procédures aussi complexes. Il faut retenir qu'il y a toujours des alternatives et que métastase n'est pas synonyme de mort imminente ; par exemple les insulinomes métastatiques pris en charge médicalement sans traitement anti-cancéreux ont une durée de vie médiane de 8 mois et en cas d'ajout de toceranib, cette médiane dépasse 1 an.
V. Conclusion
En cancérologie vétérinaire, chaque décision thérapeutique doit être adaptée au cas par cas. L'influence du pronostic est double : d'une part le pronostic dépend du traitement entrepris et d'autre part le choix du traitement dépend du pronostic attendu. Pour cela il est nécessaire d'avoir des connaissances approfondies de la situation afin de guider au mieux les propriétaires dans leur choix : la présence de métastases n’équivaut pas nécessairement à un pronostic désespéré et le traitement théoriquement le plus efficace n’est pas toujours celui qui sera retenu. Le choix final repose sur l’équilibre entre la nature de la tumeur, l’état général de l’animal, les attentes des propriétaires et les contraintes pratiques, afin de proposer une prise en charge cohérente et personnalisée.
Bibliographie
Disponible auprès de l'auteur.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Caractéristiques tomodensitométriques de cas confirmés d'atrésie du conduit auditif chez 7 chiens et 1 chat
Claire BERTINOT
Coauteurs : LAUNAY Mahéva, LEVY Alice, VIAUD Sébastien
Introduction
L'atrésie du conduit auditif est une affection rare, caractérisée par une interruption partielle ou complète du conduit auditif, d'origine inflammatoire, traumatique ou congénitale, pouvant entraîner des complications affectant notamment l'oreille moyenne. L'examen tomodensitométrique de la tête est un outil de diagnostic central dans l'évaluation des otites chroniques permettant d'évaluer les répercussions sur l'oreille moyenne, non accessible par otoscopie. Cette série de cas vise à décrire les caractéristiques tomodensitométriques de cas confirmés d'atrésie afin d'en améliorer le diagnostic et, ainsi, sa prise en charge thérapeutique.
Matériel et Méthodes
Huit patients (7 chiens, 1 chat) référés en consultation de dermatologie pour des signes d'otite externe chronique ont bénéficié d'un examen tomodensitométrique de la tête, réalisé sous anesthésie générale, avant et après injection intraveineuse de produit de contraste iodé. Les images ont été interprétées conjointement par un résident en imagerie et deux radiologues diplômés.
Résultats
Dans tous les cas, le scanner a révélé une interruption nette et complète de la lumière du conduit auditif en portion horizontale, de localisation variable. La paroi était épaissie, rehaussante et parfois minéralisée. Une accumulation de liquide était souvent présente entre le site d'atrésie et la bulle tympanique, associée dans certains cas à un élargissement anormal du conduit. La bulle tympanique ipsilatérale contenait fréquemment un matériel d'atténuation tissu mou, avec parfois des modifications osseuses discrètes au niveau de sa paroi. Un épaississement discret des noeuds lymphatiques locorégionaux était observée dans plusieurs cas. L'examen cytologique ou bactériologique, lorsqu'il était réalisé, n'a pas systématiquement révélé la présence de bactéries et / ou de levures. Tous les patients ont été traités chirurgicalement par ablation du conduit auditif et ostéotomie latérale de la bulle tympanique, avec une évolution postopératoire favorable.
Discussion
La localisation de l'atrésie du conduit auditif est variable et semble dépendre de sa cause initiale. Un examen otoscopique, idéalement par oto-endoscopique, est systématiquement nécessaire afin de confirmer la présence ou non d'une interruption de lumière au sein du conduit auditif, après réalisation d'une détersion si celle-ci s'avère nécessaire. Il peut être difficile, dans certains cas, de distinguer une origine traumatique d'une cause congénitale, bien que cette distinction ait une influence limitée sur la prise en charge. En effet, la majorité des patients bénéficie d'un traitement chirurgical consistant en une ablation du conduit auditif externe, associée à une ostéotomie latérale et un curetage de la bulle tympanique. Toutefois, quelques cas de reconstruction du conduit auditif ont été rapportés dans la littérature, uniquement dans un contexte de rupture traumatique. Cette approche vise à restaurer la perméabilité du conduit et potentiellement à préserver une certaine fonction auditive. Néanmoins, les données concernant l'évolution à moyen et long terme de ces patients restent limitées. La présence de bactéries ou de levures à l'examen cytologique ou bactériologique par écouvillonnage intra-auriculaire ne s'est pas révélée être un marqueur fiable de l'étiologie de l'atrésie dans cette série de cas, contrairement à ce que suggéraient certaines publications antérieures. L'imagerie par résonance magnétique (IRM) a été utilisée dans quelques cas cliniques d'atrésie, mais son intérêt semble restreint en l'absence de signes neurologiques associés à l'otite. Enfin, cette affection peut évoluer vers des complications sévères, notamment la formation d'un abcès para-aural, source de douleurs marquées, voire de signes neurologiques. Ces formes avancées imposent une prise en charge chirurgicale plus lourde, soulignant l'importance d'un diagnostic précoce et fiable.
Conclusion
L'aspect tomodensitométrique typique d'une atrésie comprend une interruption focale de la lumière du conduit auditif, associée à des modifications inflammatoires secondaires. L'identification précoce de cette affection permet d'orienter rapidement vers une prise en charge chirurgicale des animaux atteints, puisque les traitements médicaux, topiques notamment, sont inefficaces. Cette prise en charge précoce a également pour but d'éviter ou de traiter les complications sévères qui peuvent être secondaires à cette affection.
Bibliographie
- ALKHEDER, A., ALHIRAKI, I., ALAHMAD, M., ALSHAMI, F. O., JAMAL, L., & YOUSFAN, A. (2024). The effective surgical management of traumatic external auditory canal atresia resulting from a dog bite using a stent silicone prosthesis. International Journal of Surgery Case Reports, 117, 109540.
- ANWER, C., SCHWARZ, T., VOLK, S. W., & VITE, C. (2011). BAER testing in a dog with bilateral external ear canal atresia. Journal of the American Animal Hospital Association, 47(5), 370-374.
- CAINE, A. R., HERRTAGE, M. E., & LADLOW, J. F. (2008). Imaging diagnosis--ear canal distension following external auditory canal atresia. Veterinary Radiology & Ultrasound, 49(3), 267-269.
- COLE, L. K. (2004). Otoscopic evaluation of the ear canal. Veterinary Clinics of North America : Small Animal Practice, 34(2), 397-410.
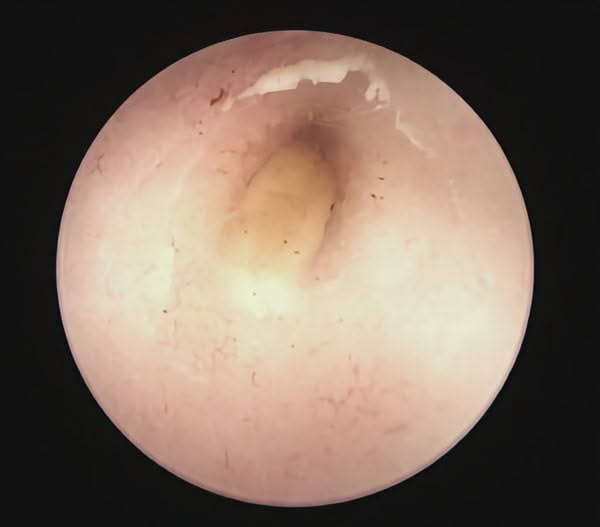
Figure 1 : Photo d'un examen vidéo-otoscopique montrant une atrésie du conduit auditif
après détersion du conduit auditif externe.
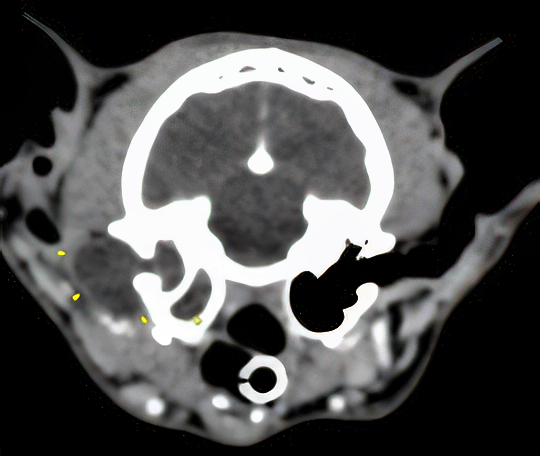
Figure 2 : Image scanner en filtre parenchymateux après injection de produit de contraste montrant une interruption totale et focale de la lumière du conduit auditif droit à sa jonction entre la partie verticale et horizontale avec accumulation de liquide entre le site d'atrésie et la bulle tympanique. Un comblement liquidien de la bulle tympanique avec épaississement de sa paroi est également visible.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Chirurgies otologiques assistées par needle-scopie : 11 cas
Jennyfer THIBAUD
Coauteurs : Laura CUDDY et Sacha DEVEREUX
Introduction
Pour les chiens qui présentent des otites chroniques ou les chats présentant un polype auriculaire, la chirurgie est souvent envisagée, sous forme d'une TECA-LBO (ablation totale du conduit auditif externe avec ostéotomie latérale de la bulle tympanique) ou d'une VBO (ostéotomie ventrale de la bulle tympanique).
Le Nanoneedle (NANOSCOPE™, ARTHREX, NAPLES, FL, USA) est un système vidéo-endoscopique de nouvelle génération. Cet instrument, principalement dédié aux chirurgies arthroscopiques en médecine humaine, est ici utilisé dans le cadre de chirurgies otologiques chez le chien et le chat.
L'objectif : décrire l'utilisation de la needle-scopie dans la chirurgie otologique chez le chat et le chien, ainsi que les résultats obtenus sur une cohorte de onze patients.
Matériel et méthodes
Cette étude rétrospective inclut des chiens et des chats référés pour une intervention otologique : TECA-LBO ou VBO, au cours de laquelle le Nanoneedle a été utilisé, entre 2024 et 2025.
Dans le cas d'une TECA-LBO, le Nanoneedle est introduit dans la cavité tympanique après curetage et permet de confirmer le retrait total de l'épithélium tympanique, ainsi que l'exérèse complète du canal auditif externe à hauteur du méat acoustique externe.
Dans le cas d'une VBO, le Nanoneedle est introduit après retrait du polype ou de la masse, dans la bulle tympanique via le site d'ostéotomie ventrale, puis dans le conduit auditif externe, dans le but de confirmer le retrait du polype ou de la masse et de vérifier la perméabilité du conduit.
Le Nanoneedle permet également le rinçage abondant de la cavité tympanique avant fermeture du site opératoire.
Un échantillonnage histopathologique et un prélèvement bactériologique sont ensuite envoyés au laboratoire. Le suivi est réalisé au contrôle à 2 semaines postopératoires.
Résultats
Cinq chiens et quatre chats ont rempli les critères d'inclusion, huit TECA-LBOs et trois VBOs ont été réalisées. L'âge moyen des patients était de 6,4 ans (9 mois à 17 ans) et le poids moyen était de 9 kg (2.19 à 49,5 kg).
Sept TECA-LBOs ont été réalisées dans un contexte d'otite chronique réfractaire au traitement médical et une TECA-LBO a été programmée dans le but de retirer une masse. Les VBOs ont été réalisées dans le but de retirer une masse polypoïde.
La chirurgie vidéo-assistée a été faisable dans tous les cas.
Une complication peropératoire mineure a été recensée. Quatre complications postopératoires temporaires ont également été décrites.
L'examen histopathologique a confirmé la présence de polype inflammatoire dans deux cas, d'un carcinome à cellules squameuses dans deux cas et d'une otite hyperplasique chronique dans sept cas.
Discussion
Plusieurs études cadavériques et cliniques ont déjà prouvé l'efficacité des chirurgies otoscopiques chez le chien. Parmi les avantages mentionnés, nous retrouvons la visualisation de certaines structures anatomiques de l'oreille moyenne, telles que le promontoire, les osselets ou encore la fenêtre ovale [2, 3]. L'endoscopie peropératoire permet également, dans la majorité des cas, de maximiser le retrait de l'épithélium tympanique après une ablation totale du conduit auditif externe avec ostéotomie latérale de la bulle tympanique [4]. Une étude cadavérique a en effet démontré que l'otoscopie peropératoire permet de détecter la persistance d'épithélium tympanique dans 100 % des cas après la réalisation d'une TECA-LBO [4].
Le needle-scope est un instrument, initialement dédié aux chirurgies orthopédiques, qui a été développé il y a plusieurs années pour la médecine humaine. Plus récemment, son utilisation en chirurgie thoracique, urologique ou abdominale a été décrite dans de nombreux articles de médecine humaine [1]. Quelques cas cliniques isolés en médecine vétérinaire mentionnent son application dans le diagnostic de la dysplasie du coude ou encore des lésions méniscales chez le chien. L'utilisation du Nanoneedle en chirurgie des tissus mous chez les animaux de compagnie a également fait l'objet d'un poster scientifique (laparoscopic ovariectomy in dogs <10 kg with a nanoscope, BEER, VÖK & VÖP 2024, SALZBURG, AUSTRIA), ainsi que d'une communication orale (How does nanoscopy benefit my everyday practice? CUDDY, ESVOT 2024, PORTO).
Conclusion
La chirurgie auriculaire assistée par needle-scopie est une alternative aux techniques traditionnelles permettant une excellente visualisation de la cavité tympanique, du conduit auditif externe, ainsi que du méat acoustique externe chez le chat et le chien. Subjectivement, l'utilisation du Nanoneedle augmente la qualité du geste chirurgical.
Bibliographie
- VIANI EC, HUDSON CC, COLEMAN KA, ALLEN PI. Anatomic structures of the canine middle ear visible during endoscopic examination through a ventral or lateral approach. J Am Vet Med Assoc. 2022 Aug 25;260(13):1663-1667. doi: 10.2460/javma.22.05.0192. PMID: 36006915.
- BHUTTA MF, MORRISON LR, KURESHI M. Endoscope and image-guided ventral bulla osteotomy in the dog: A cadaveric and patient study. Vet Rec. 2021 Sep;189(5):e510. doi: 10.1002/vetr.510. Epub 2021 May 24. PMID: 34028840.
- WATT MM, REGIER PJ, FERRIGNO CRA, MCCONKEY MJ, FOX-ALVAREZ WA, BERTRAN J. Otoscopic evaluation of epithelial remnants in the tympanic cavity after total ear canal ablation and lateral bulla osteotomy. Vet Surg. 2020 Oct;49(7):1406-1411. doi: 10.1111/vsu.13492. Epub 2020 Jul 27. PMID: 32716063.
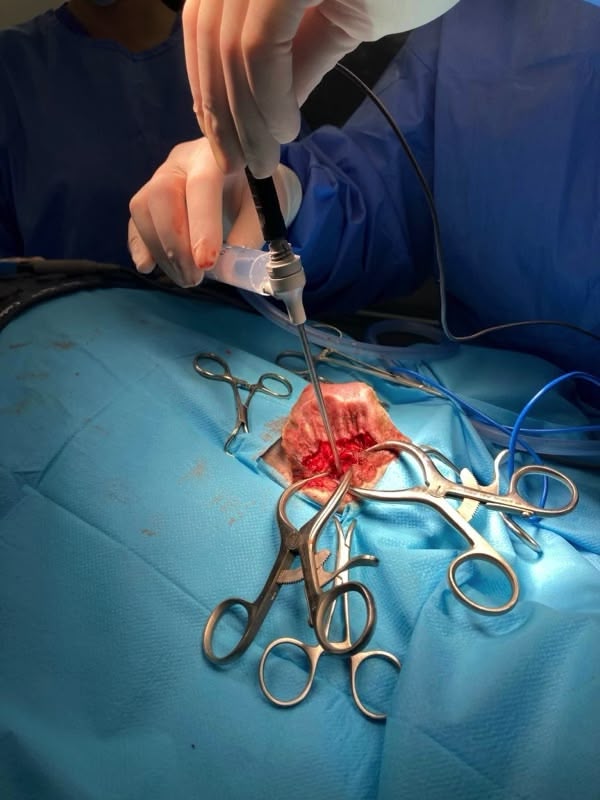
Figure 1 : Utilisation du NanoNeedle au cours d’une TECA-LBO chez un chien atteint d’otite chronique, réfractaire au traitement médical.
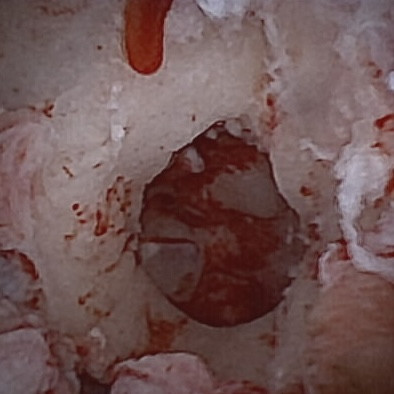
Figure 2 : Image needle-scopique mettant en evidence le méat acoustique externe après ablation du conduit auditif externe dans le cadre d’une TECA-LBO.
Liens d'intérêt : Laura Cuddy est consultante pour Arthrex Vet Systems
📃 Combinaison d'une mini-hémilaminectomie et corpectomie latérale partielle réduite dans la prise en charge des hernies discales chroniques chez le chien
Luna BERLEMONT
Coauteurs : L. BONDONNY, M. TARONI, FX. FERRAND
Introduction
La corpectomie latérale partielle (CLP), décrite par Moissonnier est recommandée pour les hernies protrusives. L’objectif de cette étude est d’évaluer l’efficacité de son association avec une mini-hémilaminectomie (mH) dans la prise en charge des hernies discales chroniques.
Matériels et méthodes
Les chiens ayant subi une CLP associée à une mH avec un examen tomodensitométrique post-opératoire immédiat ont été répertoriés.
Résultats
Quarante-huit espaces intervertébraux de 36 chiens ont été traités. Les fenêtres de corpectomie étaient inférieures aux recommandations. La décompression médullaire était significative pour tous les chiens. La majorité des chiens présentaient un statut neurologique stable à court terme. A long terme 66% étaient améliorés.
Discussion
Cette technique permet de traiter convenablement les cas de hernies discales chroniques. Les fenêtres osseuses étaient de plus petites dimensions que celles recommandées. L’évolution clinique est semblable aux études précédentes. Les limites de cette étude sont inhérentes à son caractère rétrospectif.
Conclusion
L’association d’une mH à une CLP permet de réduire les dimensions de fenêtre tout en offrant ainsi une décompression médullaire adaptée et un pronostic à court et long terme satisfaisant.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Comment bien réaliser une culture bactérienne
Marcy L'étoile, France
I. Introduction
La culture bactérienne est un examen complémentaire très important permettant d'identifier le germe en cause dans la pyodermite et de cibler le traitement efficace pour l'animal. Pourtant, sa valeur diagnostique dépend étroitement de la qualité du prélèvement, du moment choisi, de la méthode d'envoi et de l'interprétation des résultats. Cette présentation propose une démarche rigoureuse pour optimiser les prélèvements bactériologiques en pratique dermatologique.
II. Quand faut-il réaliser une culture bactérienne ?
Il existe trois types de pyodermite : de surface, superficielle et profonde. Les recommandations actuelles précisent que les deux premières doivent toujours être traitées avec des traitements topiques antiseptiques. Des antibiotiques seront prescrits si une pyodermite superficielle ne s'améliore pas sous topiques antiseptiques et lors de pyodermites profondes. C'est dans ces cas que la culture bactérienne pourra être indiquée.
La culture est recommandée dans plusieurs contextes :
- Échec thérapeutique après antibiothérapie empirique
- Présence d'une bactérie multirésistante isolée dans le passé
- Visualisation de bacilles à l'examen cytologique
- Prescription d'antibiotiques critiques
- Pyodermites profondes graves
- Pyodermite chronique avec des lésions résiduelles après 4 à 6 semaines de traitement
Elle est fortement conseillée en dermatologie, même en dehors de ces conditions, car la durée de traitement est longue : en moyenne 4 à 6 semaines minimum.
III. Quelles lésions faut-il cibler ?
Si elles sont présentes, il faut prélever des lésions primaires récentes, sinon des lésions secondaires pourront être utilisées.
- Pour les pyodermites superficielles : pustules intactes en priorité, collerettes épidermiques sinon.
- Pour les pyodermites profondes : furoncles intacts en priorité, furoncles percés, fistules ou cellulites sinon.
- Pour les otites : conduit auditif externe
III. Quelle méthode utiliser pour prélever ?
La méthode dépend de la lésion. Dans tous les cas, le port de gants stériles et un nettoyage au sérum physiologique stérile (pas d'antiseptique qui risque d'inhiber la croissance bactérienne) sont recommandés. En fonction des lésions, la méthode de prélèvement sera :
- Face à une lésion à contenu liquidien, intacte (pustule, furoncle) : une pression pour extraire son contenu ou une ponction à l'aiguille fine ;
- Face à une collerette épidermique : frottement de la zone périphérique ;
- Si la lésion est une coalescence de furoncles (cellulite) : biopsie cutanée avec retrait de l'épiderme.
Bien replacer l'écouvillon dans le tube de transport et la biopsie dans un tube contenant du liquide physiologique stérile.
V. Comment conserver et envoyer l'échantillon ?
- L'échantillon doit être conservé à température ambiante et envoyé au laboratoire bactériologique vétérinaire dans un délai de 24 à 48 h. Une fiche détaillée précisant : l'espèce, le site, le type de lésion, les traitements en cours et les hypothèses diagnostiques doit accompagner le prélèvement.
- Éviter le frigo sauf si transport > 48 h.
- Ne pas exposer au soleil ni à des variations de température.
VI. Comment interpréter les résultats ?
L'interprétation d'une culture ne se fait jamais seule : elle doit être corrélée aux résultats de l'examen cytologique, aux signes cliniques et aux traitements en cours. La présence d'un germe ne signifie pas forcément infection : il peut s'agir de colonisation ou de contamination. La bactérie isolée doit être une bactérie pathogène (Staphylococcus pseudintermedius, Pseudomonas aerugisnosa par exemple) et il est important de garder son sens critique lors de l'isolement d'un germe contaminant (Enterococcus faecalis, Corynebacterium auriscanis par exemple). Les résultats sont plus pertinents si une souche pure a poussé lors de la culture. L'antibiogramme guide la décision thérapeutique mais ne remplace pas l'évaluation de la pertinence clinique. La culture permet aussi de surveiller les tendances de résistance, notamment pour le Staphylococcus pseudintermedius, et de s'inscrire dans une démarche d'antibiothérapie raisonnée.
VII. Conclusion
La culture bactérienne est un outil indispensable à condition d'être utilisée à bon escient, dans des conditions rigoureuses, et toujours interprétée en lien avec le contexte clinique. Sa bonne utilisation participe à la lutte contre l'antibiorésistance et à l'amélioration des soins dermatologiques chez le chien et le chat.
Bibliographie
- LOEFFLER A, CAIN CL, FERRER L et al. Antimicrobial use guidelines for canine pyoderma by the International Society for Companion Animal Infectious Diseases (ISCAID). Vet Dermatol. 2025 (36):234–282.
- MILLER WH, GRIFFIN CE, CAMPBELL KL. Muller and Kirk's Small Animal Dermatology. 7th ed. Saunders Elsevier, 2013.
- WEESE JS, BLONDEAU J, BOOTHE D, et al. International Society for Companion Animal Infectious Diseases (ISCAID) guidelines for the diagnosis and antimicrobial therapy of canine superficial bacterial folliculitis. Vet Dermatol. 2014;25(3):163–e43.
- HILLIER A, LLOYD DH, WEESE JS, et al. Guidelines for the diagnosis and antimicrobial therapy of canine superficial bacterial folliculitis. Vet Dermatol. 2014;25(3):163–e43.
- GUARDABASSI L, PRESCOTT JF. Antimicrobial stewardship in small animal veterinary practice: from theory to practice. Vet Clin North Am Small Anim Pract. 2015;45(2):361–376.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Comment choisir entre un calque par impression et un scotch-test
Toulouse, France
I. Introduction
L'examen cytologique permet de visualiser les cellules (de la peau, inflammatoires) et les agents infectieux éventuels.
On distinguera deux types de prélèvement en fonction de la zone prélevée :
- Les scotch-tests à privilégier pour des lésions squameuses de surface, non suintantes ;
- Les calques par impression ou par étalement qui permettent d'analyser des liquides/exsudats.
I. Les techniques de prélèvements
1. Le scotch test
Réservé aux lésions squameuses et sèches, il permet surtout de mettre en évidence des éléments infectieux en grande quantité associés aux kératinocytes. Cela définit les syndromes de prolifération de surface.
Un morceau de 7 cm environ est apposé 3 fois successivement sur le même endroit du scotch et dans le même territoire cutané.
Il est ensuite coloré, sans être plongé dans le fixateur (dissolution de la colle, opacification), donc dans l'éosine (10 secondes) puis dans le bleu (10 secondes) et enfin rincé.
Le scotch peut également être utile pour prélever des zones difficiles d'accès où la production est grasse (enduit), comme dans les plis de la face ou encore de la queue.
De manière plus anecdotique, le scotch peut permettre de récolter des parasites. Cette technique a été publiée par une équipe espagnole pour le diagnostic de la démodécie après réalisation d'un pli de peau et récolte sur le scotch des matériels qui ont été expulsés des follicules. Cette technique est aussi voire plus sensible que le raclage cutané. Le scotch ne doit pas être coloré et doit être examiné sur une lame avec une goutte d'huile de paraffine entre la lame et le ruban adhésif. Cette technique permet également de récupérer les acariens pilicoles comme les Cheyletiella et peut s'avérer intéressante chez les petits mammifères comme les souris et les cobayes.
2. Le calque par impression ou par étalement
Il s'agit de l'apposition d'un liquide sur une lame.
Si le suintement est directement accessible, la lame est apposée sur la zone, séchée et colorée. Si les croûtes recouvrent la zone, celles-ci doivent être décollées préalablement (calque sous-crustacé).
Les pustules et les furoncles peuvent être ponctionnées ou le toit des lésions peut être délicatement soulevé avec l'angle de la lame.
La fixation a lieu dans le premier pot pendant 5 secondes puis 10 secondes dans l'éosine et 10 secondes dans le bleu. La lame est rincée à l'eau du robinet, puis délicatement séchée.
III. Les différents types cellulaires
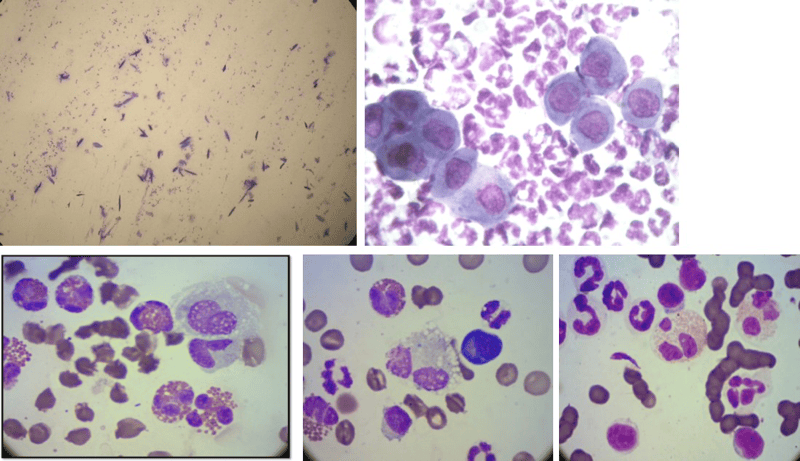
Photo 1 : cellules cutanées et inflammatoire. Présence de cornéocytes (gauche) de kératinocytes acantholysés (droite) et de cellules inflammatoires ( en bas eosinophiles, neutrophiles, macrophages, plasmocytes et lymphocytes).
1. Les cellules épithéliales :
- Les cornéocytes : ils procèdent de la différentiation terminale du kératinocyte. Ils constituent la couche cornée (stratum corneum), la couche la plus externe de l'épiderme. On les reconnait à leur aspect typique de papier plié, polygonaux, anucléés.
- Les kératinocytes des autres couches : anguleux et nucléés.
- Kératinocyte acantholytique : il s'agit d'un kératinocyte qui s'est détaché du massif épidermique par perte de ses adhésions protéiques. Ce phénomène s'appelle l'acantholyse. Elle peut être auto-immune (pemphigus superficiel) ou infectieuse (bactérienne, fongique). Sous l'influence de la perte d'adhésion, ces cellules perdent leur caractère anguleux (rondes). Elles conservent leur noyau.
2. Les cellules inflammatoires :
Les polynucléaires neutrophiles, éosinophiles, les macrophages, les lymphocytes, les mastocytes et les plasmocytes.
3. Les agents infectieux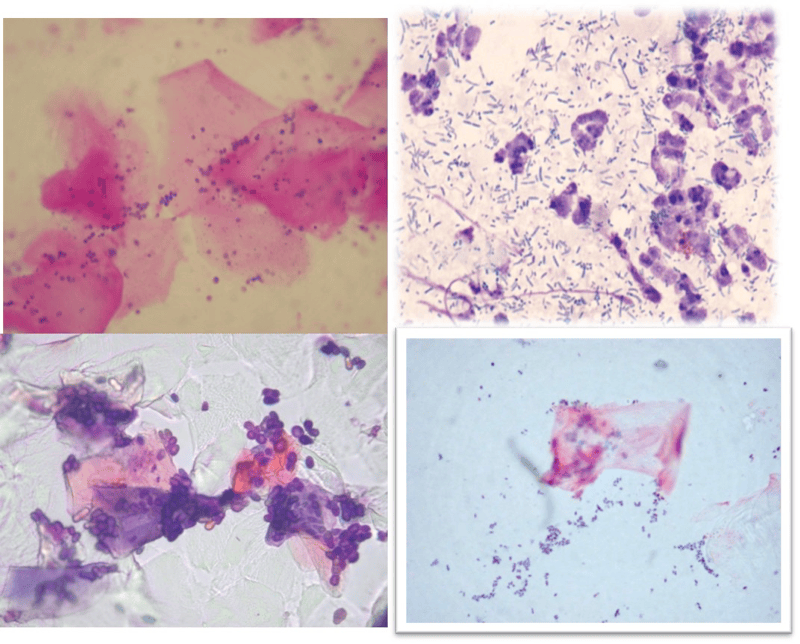
Photo 2 : agents infectieux; bactéries de type coccies (en haut à gauche), bacilles et neutrophiles (en haut à droite), coccies bacilles et coccobacilles (en bas à droite) et malassezias (en bas à gauche).
a) Les bactéries
Ce sont des éléments de petite taille, environ 1 µm de diamètre, ronds, ovoïdes ou en forme de bâtonnet. Elles prennent une coloration bleue soutenue homogène. On les trouve en position extra-cellulaire ou en position intra-cytoplasmique (images de phagocytose) au sein des macrophages et/ou des granulocytes neutrophiles.
b) Les levures
Il s'agit de levures de type Malassezia. Elles prennent un aspect typique en empreinte de pas. De plus grande taille qu'une bactérie, elles mesurent en moyenne 7 µm. Leur coloration (rose, bleu, violet) varie en fonction du temps passé dans les colorants et de la séborrhée de l'animal. En effet, les lipides empêchent la bonne coloration de ces agents qui restent transparents.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Comment optimiser les biopsies cutanées ?
Marcy L'étoile, France
I. Introduction
La biopsie cutanée est un examen de référence en dermatologie vétérinaire pour établir un diagnostic histopathologique précis. Pourtant, sa performance dépend largement des conditions de prélèvement, du traitement des échantillons et de la qualité des informations transmises au pathologiste. L'objectif de cette présentation est de proposer une optimisation de chaque étape de la biopsie cutanée, depuis l'indication jusqu'à l'interprétation, afin d'en améliorer la valeur diagnostique.
II. Quand biopsier ?
La biopsie n'est pas un acte de dernier recours. Elle doit toujours être envisagée quand une hypothèse diagnostique a été établie et que son diagnostic repose sur l'examen histopathologique de biopsies cutanées. Il est parfois difficile d'avoir une hypothèse diagnostique et la biopsie peut être réalisée (même s'il est conseillé de référer lorsqu'aucune hypothèse diagnostique n'est envisagée) face à des lésions atypiques. Des contextes particuliers comme les dermatoses nodulaires, les maladies bulleuses ou les dermatites exfoliatives justifient cet acte complémentaire. Il est recommandé de traiter les complications infectieuses secondaires et d'arrêter tout traitement immunomodulateur avant de réaliser la biopsie cutanée (15 jours minimum). Certaines affections doivent être biopsiées rapidement telles que les vascularites. En effet, l'observation de lésions cutanées signent une destruction vasculaire déjà réalisée (plus de signe actif d'attaque). Dans ce cas, il faut cibler les lésions les plus récentes.
III. Quoi prélever ?
Le choix du type de lésion, de son stade évolutif et de sa topographie est fondamental. Une erreur fréquente est de biopsier des lésions terminales (croûtes, ulcères, zones cicatricielles) peu informatives. Il est préférable de cibler des lésions primaires ou les plus récentes. Le site de prélèvement doit être discuté en fonction de la physiopathologie suspectée. Par exemple, dans le cadre d'un pemphigus foliacé, il faut viser des pustules ; si elles ont déjà évolué, une croute pourra apporter des informations intéressantes (attention de ne pas jeter la croute si elle se détache lors du prélèvement). Pour un diagnostic de lupus cutané, une zone dépigmentée, érythémateuse mais pas ulcérée, sera ciblée, la jonction dermo-épidermique étant la zone qui permettra à l'anatomopathologiste de conclure.
IV. Combien de prélèvements faut-il faire ?
Il est recommandé de réaliser au moins 3 à 5 biopsies, sur différentes zones représentatives, afin d'augmenter la sensibilité de l'examen. Cela permet d'éviter les faux négatifs.
V. Comment prélever ?
L'usage d'un trépan à biopsie (biopsy punch) est généralement recommandé. La taille du trépan doit être de 6 mm, sauf pour des lésions plus grandes (et il sera possible d'utiliser un punch de 8 mm ou de faire une côte de melon) ou pour des zones petites, telles que les paupières, les lèvres, la truffe (pour lesquelles un punch de 4 mm pourra être envisagé). Il est recommandé de tondre la zone au préalable mais de ne pas la désinfecter (sauf pour des prélèvements pour culture bactérienne et antibiogramme). Les biopsies doivent être manipulées avec douceur, sans pince traumatisante, pour éviter les artéfacts. Elles sont essuyées sur une compresse (élimination du sang), puis fixées immédiatement dans du formol tamponné à 10%. Le délai avant fixation, la présence de poils longs ou de sang, peuvent nuire à la lisibilité de la coupe histologique.
VI. Comment l'envoyer ?
Le pot de formol doit être placé dans un emballage prévu et envoyé à un laboratoire de diagnostic anatomopathogique. Une fiche d'accompagnement précise est indispensable. Elle doit contenir l'anamnèse, la distribution lésionnelle, les traitements en cours ou antérieurs, les hypothèses diagnostiques et les zones biopsiées. Le vétérinaire clinicien est responsable de la décision de biopsier; le pathologiste, quant à lui, est un interlocuteur à solliciter en cas de doute sur les modalités de prélèvement ou d'interprétation.
VII. Conclusion
La biopsie cutanée est un outil diagnostique très intéressant, mais exigeant. Optimiser sa réalisation passe par une rigueur méthodologique qui commence par un choix raisonné de cet examen complémentaire.
Bibliographie
- GROSS TL, IHRKE PJ, WALDER EJ, AFFOLTER VK. Skin Diseases of the Dog and Cat: Clinical and Histopathologic Diagnosis, 2è ed. Wiley Blackwell, 2005.
- SCOTT DW, MILLER WH, GRIFFIN CE. Muller and Kirk's Small Animal Dermatology, 7è ed. Saunders Elsevier, 2012.
- MAULDIN EA, PETERS-KENNEDY J. In: Jubb, Kennedy, and Palmer's Pathology of Domestic Animals, Vol. 1. Elsevier, 2016.
- NISCHAL U et al. Techniques of Skin Biopsy and Practical Considerations. J Cutan Aesthet Surg. 2008 Jul-Dec;1(2):107–111.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Comment s'équiper correctement et à quel coût ? (dont radiologie)
Bandol, France
I. Introduction
L'investissement peut sembler conséquent, mais il conditionne la qualité des soins et la rentabilité de l'activité. L'objectif de cette présentation est de vous familiariser avec les coûts d'acquisition du matériel nécessaire pour s'équiper adéquatement en dentisterie vétérinaire. Nous nous concentrerons sur l'équipement indispensable pour la pratique du détartrage supra et sous-gingival, le débridement des poches parodontales et les extractions dentaires chez les carnivores domestiques, qui constituent la majeure partie de l'activité dentaire en structure généraliste. Les domaines plus spécialisés comme la dentisterie restauratrice, l'endodontie, la prothèse, l'orthodontie ou la dentisterie des Nouveaux Animaux de Compagnie (NAC) nécessitent des équipements additionnels qui ne seront pas abordés ici.
II. L'Instrumentation manuelle : un premier pas essentiel
L'instrumentation manuelle est la base de toute intervention dentaire, permettant des actions précises et complémentaires au matériel mécanique.
1. Inventaire détaillé par usage
a) Pour le diagnostic et l'examen clinique
- Équipement de protection individuelle (EPI) : lunettes, masque, gants, pour la sécurité du praticien.
- Source de lumière et loupes de grossissement (x2,5) : indispensables pour une visualisation optimale de la cavité buccale.
- Sonde parodontale (type Williams ou UNC 15) : utilisée pour mesurer et évaluer l'indice de gingivite, la profondeur du sulcus/poche, le degré d'hypertrophie/récession gingivale et l'exposition de la furcation.
- Sonde exploratrice dentaire (n° 23 en forme de faucille) : la plus courante pour détecter les anomalies de surface des dents.
- Écarteur de lèvres (Minnesota ou labial) : améliore considérablement le champ de vision.
b) Pour la prophylaxie (nettoyage et prévention)
- Pince à enlever le tartre : pour les gros dépôts de tartre.
- Instruments parodontaux :
- Supra-gingivaux (faucille, crochet) : pour éliminer les dépôts au-dessus de la gencive.
- Sous-gingivaux (Gracey, universelle) : pour nettoyer sous la gencive. Le détartrage mécanique par ultrasons est privilégié pour sa rapidité et facilité, mais il est idéalement combiné au nettoyage manuel.
- Canule de 22 Gauge avec seringue : pour l'irrigation sous-gingivale.
c) Pour les extractions dentaires :
- Syndesmotome faucille de CHOMPRET : sert à décoller la gencive et sectionner les fibres du desmodonte autour de la dent.
- Manche de bistouri (n°3 ou n°3G) : pour les lames n° 11 ou 15, utilisé pour les incisions gingivales.
- Décolleur à périoste de MOLT : permet de soulever la gencive et de créer un lambeau si nécessaire.
- Luxateurs dentaires : plus fins et tranchants que les élévateurs, ils sont conçus pour rompre le ligament parodontal sans faire levier (lames de 1 à 4 mm).
- Élévateurs dentaires : utilisés pour faire levier et écarter la racine (tailles de 1 à 6 mm).
- Daviers dentaires : idéalement, trois types sont recommandés : pédiatrique droit, davier à racines, et davier adulte à mors larges, pour retirer la dent ou la racine.
- Curettes à os (VOLKMAN ou LUCAS) : pour cureter les alvéoles après l'extraction (2 à 3 tailles).
- Instruments de suture :pince ADSON, ciseaux de METZENBAUM courbes, ciseaux à dissection fine, et porte-aiguille fin (type MAYO-HEGAR ou CRILE WOOD).
2. Coût de l'instrumentation manuelle
Pour un premier équipement en instrumentation manuelle, il est raisonnable de prévoir un budget d'environ 1000€ HT. Ce kit peut être complété "à la carte" par la suite.
Voici quelques exemples de prix de kits et d'instruments spécifiques :
a) Kits complets ou semi-complets
- Kit de 15 instruments pour dentisterie PA (CENTRAVET, code KIT713) : 603,83€ HT. Il comprend curette sous-gingivale PV1, sonde parondontale graduée 15 mm, sonde double, élévateurs de CAMBRAY avant et arrière 2 mm, décolleurs de MOLT (4,5/3,5 mm et 7/5 mm), syndesmotome de CHOMPRET lame 3, curette HEMINGWAY, curette DARBY, pince à tenons, 2 daviers dentaires, 2 élévateurs (2 et 3 mm). (Figure 1)
- Trousse de 14 instruments iM3 (ALCYON, code 8199403) : 261,17€ HT. Inclut élévateurs de 1 à 5 mm, sonde droite, davier, écarteur à joue, pince à ôter le tartre, curette subgingivale, curette supragingivale, curette faucille, sonde exploratrice, élévateur à périoste double.
- Set de 12 instruments iM3 (ALCYON, code 1024930) : 261,17€ HT. Composé de 6 élévateurs sur manche court (1 à 6 mm), davier extraction petites dents 12,5 cm, élévateur à périoste double, porte-aiguille de MAYO HEGARD, pince à disséquer ADSON BROWN, paire de ciseaux de LAGRANGE, manche de bistouri.
- Trousse d'extraction (4 instruments) (COVETO, code 679452) : 215,06€ HT. Contient syndesmotome courbe, élévateurs droits 2 et 3 mm, élévateur courbe 2,5 mm.

Figure 1
b) Luxateurs :
- Kit de 5 luxateurs + 1 aiguiseur (LUXATOR) distribué par COVETO (code 810549 : 368,77€ HT). Comprend 5 luxateurs (3 lames droites, 1 courbe, 1 contre-coudée) et un aiguiseur.
- Set de 5 luxateurs avec support (iM3) (ALCYON, code 112080) : 279,51€ HT. Comprend 5 luxateurs : pointu pour racines, 2, 3, 4, 5 mm (Longueur : 125 mm).
c) Daviers dentaires :
- Davier dentaire de WITZEL pour esquilles : prix variant de 40,23€ HT (qualité standard par ALCYON, code 8046869) à 165,52€ HT (qualité AESCULAP par CENTRAVET, code DAV018).
- Davier dentaire à mors larges : prix variant de 31,77 € HT (COVETO, code 804720) à 49,23€ HT (ALCYON, code 8047225).
d) Autres instruments spécifiques :
- Curette alvéolaire double (ALCYON) : 26,11€ HT l'unité - tailles Small (code 1109540) et Large (code 1109550).
e) Loupes et sources de lumière :
- Lunettes loupes HEINE (HR) 2,5x avec bandeau Professional (CENTRAVET, code LUN716) : 1153,62€ HT – distance de travail 420 mm - option : lampe LOUPELIGHT 2 HEINE à LED de Haute Qualité (CENTRAVET, LAM704) : 852,28€ HT
- Lunettes loupe sur monture iM3 Regular : grossisement 2,5x - Distance de travail : 36 - 46 cm – ALCYON, code 1110120 : 290,41€ HT – option : lampe frontale à LED universelle.
III. Matériel rotatif et détartreur : le cœur de l'unité dentaire
Les unités dentaires modernes intègrent souvent à la fois le matériel rotatif et le détartreur, optimisant ainsi l'espace et l'efficacité.
1. Matériel rotatif : choisir la bonne vitesse
En dentisterie généraliste, deux vitesses de rotation sont nécessaires :
- Basse vitesse (3000-4000 tr/min) : pour le polissage des surfaces dentaires.
- Haute vitesse (150 000-200 000 tr/min) : indispensable pour la section d'une dent, la réalisation d'une alvéolotomie ou d'une alvéoloplastie.
Deux types d'unités dentaires sont disponibles : pneumatiques et électriques. Il est fortement recommandé de privilégier un système permettant une irrigation interne des pièces à main pour un meilleur refroidissement et une plus grande longévité de l'équipement.
- La Turbine : c'est une pièce à main haute vitesse (jusqu'à 400 000 tr/min à vide) alimentée par air comprimé. Elle offre un faible couple et est compatible avec les fraises FG.
- Le Contre-angle : fonctionne avec un moteur électrique ou pneumatique. Des bagues de couleur indiquent la multiplication ou la réduction de vitesse (rouge pour multiplier, bleue pour 1:1, verte pour réduire). Il est compatible avec les fraises CA ou FG.
- La Pièce à main droite : sa vitesse de rotation est identique à celle du moteur et elle est principalement utilisée pour le polissage. Elle est compatible avec les fraises PM.
2. Détartreur ultrasonique : la technologie piézoélectrique
Le détartreur ultrasonique piézoélectrique est à privilégier. Il fonctionne à l'électricité, offrant un meilleur refroidissement et une vibration d'insert fiable (20-50 kHz).
Des inserts spécifiques sont disponibles pour diverses utilisations (exemples avec les inserts ACTÉON) : Insert 1 (détartrage supragingival pour chiens > 5 kg), Insert 1S (plus fin, pour petits chiens/chats et poches < 2 mm), Insert 10Z (gradué, sous-gingival), Insert PV1 (spécifique vétérinaire, pour poches profondes > 4 mm).
3. Exemples d'unités dentaires :
- Unité dentaire GS Start iM3 (ALCYON, code 1006280) : 3 974,54 € HT. C'est une excellente option pour débuter si vous possédez déjà un détartreur piézoélectrique. Elle est équipée d'une seringue air/eau, d'une pièce à main spéciale polissage, d'un contre-angle à 400 000 tr/min avec spray refroidissant (turbine), et d'un compresseur silencieux sans huile. Elle est livrée avec un raccord pour détartreur.
- Cocoon Hygiénist LED avec pièces à main et autres accessoires commercialisés par ACTÉON. (Figure 2)
Figure 2
IV. La radiologie dentaire : un outil indispensable et rentable
Parler de dentisterie vétérinaire sans intégrer la radiographie dentaire est comparable à aborder la chirurgie orthopédique sans imagerie. L'examen clinique seul ne permet de déceler qu'une fraction des problèmes : plus de 60% des lésions dentaires significatives (résorptions félines, fractures radiculaires, abcès périapicaux, parodontites profondes) sont invisibles sans imagerie. [1,2]
Cet outil va au-delà du simple diagnostic ; il est également un moyen pédagogique essentiel pour expliquer aux propriétaires la nécessité des soins, ce qui améliore l'adhésion thérapeutique et valorise économiquement les actes. La question n'est donc pas de savoir si la radiographie dentaire est utile, mais de comprendre son coût d'investissement par rapport à son retour clinique et économique.
Un équipement complet typique, incluant un générateur mural X-Mind DC Vet et un système numérique SOPIX2 HD, se situe autour de 10 300 € HT.
En optant pour un financement par crédit-bail, cela représente environ 190,98 € HT par mois sur 60 mois, soit un peu plus de 6 € HT par jour, frais inclus.
Pour illustrer sa rentabilité : avec à peine 4 bilans radiographiques bouche complète (chat/petit chien) facturés 130€ TTC par mois, l'appareil est largement autofinancé tout en rémunérant son temps de travail !
L'acquisition d'un système de radiographie dentaire n'est donc pas une dépense, mais un investissement stratégique qui non seulement améliore la qualité des soins médicaux, mais renforce également l'engagement des clients et se rentabilise rapidement grâce à une meilleure valorisation des actes.
V. Conclusion
Pour pleinement valoriser les soins dentaires en clinique vétérinaire, il est impératif de s'équiper du matériel nécessaire et de se former continuellement dans cette discipline. Avec un équipement adéquat et une formation solide, environ 80% des soins dentaires deviennent accessibles pour un praticien généraliste. Investir dans la dentisterie est un choix qui améliore la qualité des soins offerts et contribue significativement à la croissance économique de la clinique.
Bibliographie
- VERSTRAETE FJM, KASS PH, TERPAK CH. Diagnostic value of full-mouth radiography in cats. Am J Vet Res 1998 ; 59(6) : 692–695.
- NIEMIEC BA. Veterinary Dental Radiographic Interpretation. Ames, Iowa : Wiley-Blackwell ; 2013.
- DEBETTE F. Développer l'activité de dentisterie au sein d'une clientèle généraliste. Prat Vet 2014 ; 49 : 522-525.
Liens d'intérêt : Contrat de consultant/conférencier avec Finapolline (Actéon Group)
📃 Comparaison biomécanique de 3 techniques de sternotomie médiane et de 3 implants pour leur réparation à l'aide d'un modèle de sternum de chien
Introduction
La sternotomie est associée à un haut taux de complications compris entre 14 et 79%, avec une prévalence plus élevée chez les chiens de grande race [1], potentiellement causée par un défaut de stabilité de réparation. Il est recommandé de réaliser une sternotomie partielle plutôt que totale, mais aucune étude n'a été réalisée pour le confirmer. Plusieurs implants sont disponibles pour la fermeture des sternotomies comme le cerclage métallique et différentes sutures dont le Fibertape®. Ces implants n'ont jamais été soumis à des essais de fatigue sur le sternum de chien. L'objectif de notre étude est de valider un modèle analogique osseux de sternum de chien dans le but de comparer les performances biomécaniques de trois implants et trois types de sternotomies.
Matériels et méthodes
Un modèle de sternum a été conçu en polyuréthane à partir d'un scanner de chien de 28 kg. Pour la validation du modèle, 5 sternums cadavériques et 5 modèles ont été utilisés. Une sternotomie totale (TS) a été réalisée et fermée avec du polydioxanone USP 1 (PDS). Des tests de traction en distraction latérale (10 mm/s) de 20 N à 160 N ont été réalisés. Les déplacements du manubrium, du sternum moyen et du xiphoïde ont été comparés.
Après validation, 40 modèles ont été répartis en 8 groupes selon le type de sternotomie (ST, sternotomie partielle avec préservation du manubrium (SPM) ou du xiphoïde (SPX)), l'implant utilisé (PDS, cerclage métallique de calibre 20 (WC) ou Fibertape 2 mm (FT)) et les tests biomécaniques (test de traction seul ou associé à un test cyclique préalable (C)) réalisés. Les tests ont été effectués en distraction latérale, de 45 à 85 N pendant 5000 cycles à 2 Hz pour les essais cycliques. Le déplacement entre les hémisternums a été enregistré. Les tests de traction ont été réalisés de 45 N jusqu'à la rupture à 100 mm/min. La charge de rupture (CR), le déplacement total (DT), la charge à 1 mm de déplacement (C1D) et la rigidité ont été notés. Les groupes ont été utilisés pour comparer les implants (PDS-ST-C, FT-ST-C, WC-ST-C) et les types de sternotomies (PDS-ST, PDS-SPM, PDS-SPX), ainsi que pour évaluer l'impact des cycles sur les performances de traction (PDS-ST-C/PDS-ST, FT-ST-C/FT-ST, WC-ST-C/WC-ST).
Résultats
Les résultats des tests cycliques n'ont pas montré de différences entre les implants. Seulement le DT de WC a été impactée par les cycles. Le PDS était l'implant le moins performant pour la ST : PDS-ST-C avait une C1D et une rigidité plus faibles, ainsi qu'un DT plus élevé que WC-ST-C et FT-ST-C. Lorsqu'il était associé à une SPX, il avait une CR, une C1D et une rigidité similaires à celles de WC-ST. PDS-SPX avait une CR, une C1D et une rigidité plus élevées que PDS-SPM et PDS-ST. PDS-ST avait un DT plus élevé et une rigidité plus faible que PDS-SPM et PDS-SPX. Ces résultats montrent la supériorité de SPX pour le type de sternotomie.
Discussion
Un scanner de chien de grande race a été utilisé pour la conception du modèle au vu des complications rapportées chez les chiens de plus de 20 kg [1]. Le polyuréthane a servi à la conception d'un modèle de sternum humain validé[2], expliquant notre choix. Notre modèle est le seul modèle canin validé car le modèle de sternum de chien précédemment conçu en polycarbonate n'a pas été validé[3]. La distraction latérale a été choisie puisqu'il s'agit de la force la plus sollicitante sur le sternum humain[4] et chez le porc[5]. Cependant, cela semble remis en question par une étude récente chez le chien[3]. Des tests supplémentaires sont en cours concernant les forces de cisaillement longitudinal et de torsion. Aucune donnée n'étant disponible sur les forces réelles s'appliquant sur le sternum de chien, les forces s'appliquant au cours de la toux et du pic inspiratoire chez le porc ont été utilisées[5]. La réalisation de 5 000 cycles représente 3 à 4 épisodes de toux par heure pendant 2 mois. Il n'y a pas de cicatrisation osseuse complète à 1 mois post-opératoire d'une sternotomie, nous avons donc estimé une cicatrisation complète à 2 mois.
Conclusion
Les tests cycliques suggèrent qu'il n'y a pas de différence entre les 3 implants pour les sternotomies totales. Au vu des résultats des essais en traction, l'utilisation de cerclage métallique ou de Fibertape® serait plus appropriée pour la réparation des sternotomies totale mais le polydioxanone pourrait être raisonnablement utilisé pour les sternotomies partielles. La section du manubrium parait moins délétère en terme de stabilité du sternum que celle du xiphoïde.
Bibliographie
- PILOT M et al. Comparison of median sternotomy closure-related complication rates using orthopedic wire or suture in dogs: A multi-institutional observational treatment effect analysis. Veterinary Surgery. 2022;51(6):990-1001.
- TRUMBLE D et al. Validation of a bone analog model for studies of sternal closure. The Annals of Thoracic Surgery. sept 2002;74(3):739-44.
- PARK Y et al. Biomechanical comparison of bone staple fixation methods with suture material for median sternotomy closure using 3D-printed bone models. New Zealand Veterinary Journal. 2024;72(5):265-74.
- CASHA A et al. A biomechanical study of median sternotomy closure techniques. European Journal of Cardio-Thoracic Surgery. mars 1999;15(3):365-9.
- PAI S et al. Characterization of Forces on the Sternal Midline Following Median Sternotomy in a Porcine Model. Journal of Biomechanical Engineering. 2008;130(5):051004.
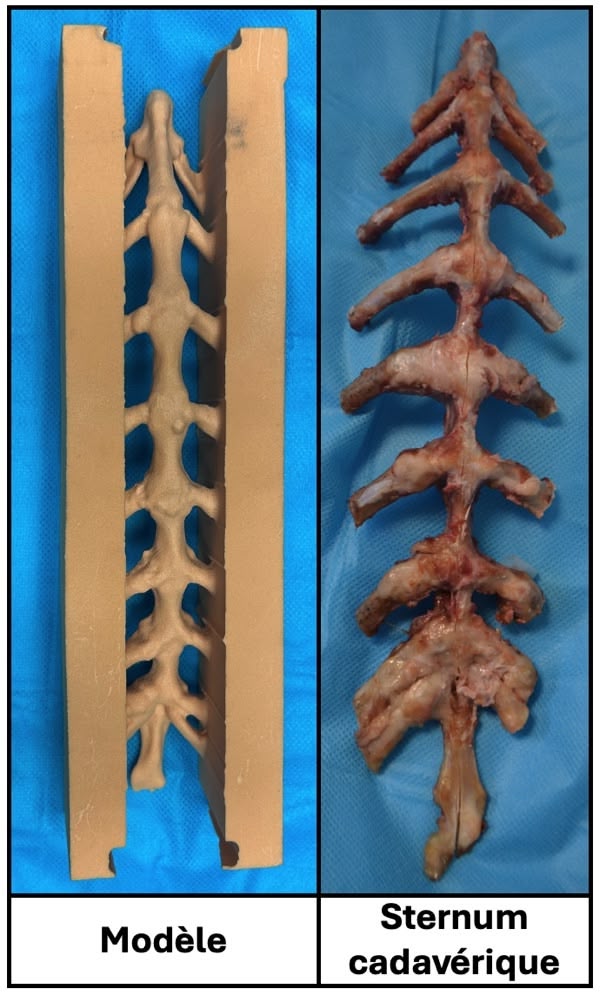
Figure 1

Figure 2
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Comparaison entre la pose d'une lentille de contact et le recouvrement par la membrane nictitante sur les résultats postopératoires de chirurgies cornéennes : étude rétrospective sur 554 yeux
Eva MARDUEL
Coauteurs: Maria CABRERO, Alexandre GUYONNET, Aurelie BOURGUET
Objectifs
Comparer les résultats postopératoires, les complications et les facteurs de risque au retard de cicatrisation après une chirurgie cornéenne avec application d'une lentille de contact versus la réalisation d'un recouvrement par la membrane nictitante (RMN) en postopératoire immédiat.
Matériel et méthodes
Recensement des données médicales des animaux ayant subi une chirurgie cornéenne (kératectomie superficielle ou greffe cornéenne) entre janvier 2018 et décembre 2024. L'âge, l'espèce, la race, le caractère brachycéphale ou non, la profondeur et la taille des ulcères cornéens, les techniques chirurgicales pratiquées, la taille du trépan, le taux de cicatrisation et les complications post-opératoires ont été recueillis et comparés entre les deux groupes lors du premier suivi, où les recouvrements ont été retirés. Un modèle de régression logistique multivariée a été utilisé pour identifier les facteurs de risque d'une réépithélialisation incomplète.
Résultats
Au total, 470 animaux ont été inclus : 306 chiens (365 yeux) et 165 chats (189 yeux). Dans le groupe des kératectomies (281 yeux) : au premier suivi (12,2 ± 5,2 jours), 86,7 % des yeux traités avec une lentille étaient cicatrisés contre 77,3 % avec RMN. Dans le groupe des greffes (273 yeux) : au premier suivi (9,1 ± 3,8 jours), 48,0 % des yeux avec une lentille étaient cicatrisés contre 38,2 % avec RMN. Aucune différence significative n'a été observée en termes de réépithélialisation complète selon le type de recouvrement pour le groupe kératectomie (p = 0,051) ou le groupe greffe (p = 0,112). Pour les deux techniques chirurgicales, le statut brachycéphale ou l'espèce n'ont pas eu d'influence significative sur la cicatrisation. L'analyse de régression logistique multivariée a identifié la taille du trépan (p = 0,007) comme un facteur de risque de réépithélialisation incomplète dans le cadre de la greffe, mais pas pour les kératectomies superficielles. Les réactions inflammatoires et les complications post-opératoires n'étaient pas significativement différentes entre les deux types de couverture quelle que soit l'intervention réalisée.
Discussion
Le facteur clé de la réussite d'une chirurgie cornéenne est la réépithélialisation du site chirurgical et l'absence de complications majeures (surinfection, perforation secondaire à une digestion/ déhiscence du greffon). Pour favoriser la réépithélialisation postopératoire et améliorer le confort de l'animal, des techniques de recouvrement (RMN ou pose de lentille cornéenne) sont classiquement réalisées en postopératoire immédiat. L'effet positif de la mise en place de lentille sur le confort et la cicatrisation des ulcères superficiels a été largement décrit lors de gestion des ulcères superficiels à bords décollés du chien suite à une kératotomie grillagée ou suite à un débridement mécanique au Diamond Burr (GRINNINGER et al, 2015; GOSLING et al, 2013; DEES et al, 2017; WOOFF et al, 2015). Inversement, seule une étude compare l'efficacité du RMN versus le traitement médical seul pour la cicatrisation d'ulcères cornéens profonds, ne montrant pas de différences significatives dans la réépithélialisation entre les deux groupes. (IMCHAROON et al, 2022) Cette étude est donc la première à comparer l'effet de la pose d'une lentille de contact ou de la réalisation d'un RMN sur la cicatrisation cornéenne suite à une chirurgie de kératectomie superficielle ou de greffe cornéenne. Les résultats mettent en évidence un taux de ré-épithélialisation, au premier suivi, qui ne diffère pas en fonction du type de recouvrement utilisé, sans effet d'espèce, de caractère brachycéphale ou de taille de l'ulcère. Il n'a également pas de différences significatives dans le taux de complication postopératoire entre les deux groupes.
Conclusion
Le type de recouvrement n'influence donc pas les résultats postopératoires. Les lentilles constituent une alternative sûre au recouvrement par la membrane nictitante après une chirurgie cornéenne permettant notamment, de par son caractère transparent, une meilleure visualisation de l'évolution cornéenne.
Mots-clés : cornée, lentille, recouvrement par la membrane nictitante, kératectomie superficielle, greffe cornéenne
Bibliographie
- DEES DD, FRITZ KJ, WAGNER L, PAGLIA D, KNOLLINGER AM, MADSEN R. Effect of bandage contact lens wear and postoperative medical therapies on corneal healing rate after diamond burr debridement in dogs. Vet Ophthalmol. 2017 Sep;20(5):382-389.
- GRINNINGER P, VERBRUGGEN AM, KRAIJER-HUVER IM, DJAJADININGRAT-LAANEN SC, TESKE E, BOEVÉ MH. Use of bandage contact lenses for treatment of spontaneous chronic corneal epithelial defects in dogs. J Small Anim Pract. 2015 Jul;56(7):446-9.
- GOSLING AA, LABELLE AL, BREAUX CB. Management of spontaneous chronic corneal epithelial defects (SCCEDs) in dogs with diamond burr debridement and placement of a bandage contact lens. Vet Ophthalmol. 2013 Mar;16(2):83-8.
- IMCHAROON K, PINYOSNIT N, SRILERT P, NGAMPONGSAI T, HUNPRASIT V, TUNTIVANICH N, JATURAKAN O. Comparative study of healing time of canine non-infectious deep ulcerative keratitis between medical therapy alone and combined treatment with medical therapy and a nictitating membrane flap: A retrospective study. Open Vet J. 2022 Nov-Dec;12(6):815-821.
- WOOFF PJ, NORMAN JC. Effect of corneal contact lens wear on healing time and comfort post LGK for treatment of SCCEDs in boxers. Vet Ophthalmol. 2015 Sep;18(5):364-70.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Comprimés antiparasitaires combos vs non-combos chez le chien : quelles différences en matière d'innocuité ?
Nantes, France
Fougères, France
I. Introduction
Il y a maintenant plus de dix ans, est apparue dans l'arsenal thérapeutique vétérinaire canin une nouvelle classe de molécules à action antiparasitaire externe : les isoxazolines. Révolutionnaires par leur durée d'action prolongée, leur spectre étendu et leur propriété adulticide, les médicaments concernés sont aujourd'hui connus et reconnus pour leur efficacité. Ces dernières années, le marché vétérinaire s'est étoffé des formes combos, ajoutant à l'isoxazoline présente dans le comprimé précédent (forme solo) un antiparasitaire interne. Or, les effets indésirables attendus pour les seuls antiparasitaires internes ajoutés sont très proches de ceux attendus avec les isoxazolines. On peut donc logiquement se questionner sur un risque additionnel à attendre avec les formes combos : la fréquence d'apparition d'un effet indésirable est-elle supérieure avec un combo ? Qu'en est-il de sa potentielle gravité ? Certaines populations canines pourraient-elles être plus à risque ?
II. Méthodologie
Pour répondre à ces questions, l'Agence Nationale du Médicament Vétérinaire a mené une étude rétrospective sur les déclarations d'évènements indésirables liés à l'utilisation de 3 isoxazolines (afoxolaner, lotilaner et sarolaner) et de leur équivalent combo, sous forme de comprimés à croquer pour chien en France, sur la période 2015-2024. Son objectif visait à comparer la fréquence et la nature des réactions déclarées ainsi que le profil des chiens ayant réagi suite à la prise d'un de ces antiparasitaires solos ou combos.
III. Résultats et discussion
Si, à la lecture des RCPs, il apparaît que les effets indésirables des médicaments combos sont jusqu'à 100 fois plus fréquents que les médicaments dits solos, notre étude, qui a porté sur les cas français uniquement, n'a pas permis de confirmer ces chiffres puisque la tolérance s'est révélée équivalente pour les solos comme pour les combos, aussi bien en termes de profil des événements que de fréquence (très rare) et de gravité.
L'analyse des sous-populations (âge et race notamment) n'a pas non plus mis en évidence une sous-population plus à risque.
Cependant, si certains biais inhérents aux processus de déclaration en pharmacovigilance vétérinaire et à la méthodologie employée ont été identifiés, les résultats obtenus indiquent que les antiparasitaires combos ne semblent pas être à l'origine de réactions plus graves ou plus fréquentes que leurs équivalents non combinés chez le chien. Le profil des effets indésirables déclarés est cohérent avec les RCPs.
Les combos semblent donc aussi bien tolérés que les solos quelle que soit la population canine. L'utilisation de ces antiparasitaires à large spectre doit toutefois rester raisonnée et adaptée au besoin de l'animal, en raison de leur impact potentiel en écotoxicité et sur la sélection de résistance.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Construire un plan de prévention
Toulouse, France
I. Introduction
Un plan de prévention est un ensemble d'actes de prévention définis d'un commun accord entre le vétérinaire et son client. Cette définition le distingue d'un plan de santé ou d'une assurance qui sont respectivement une offre de soins organisés ou des contrats avec un assureur permettant le remboursement de soins vétérinaires.
Le plan de prévention est à construire en fonction de la situation et du besoin de l'animal. En règle générale, il est planifié sur une durée convenue avec le propriétaire, souvent d'un an, avec une facilité de paiement par mensualisation, associé à des visites et soins réguliers de l'animal qui doivent être définis en amont pour la construction du plan. Le but d'un plan de prévention en consultation de médecine préventive est de préserver la bonne santé de l'animal tout au long de sa vie et le plus longtemps possible en proposant des visites régulières, notamment durant la phase de croissance ainsi qu'une mensualisation des paiements.
II. Contexte et mise en place
Les plans de prévention sont arrivés en France en 2015. Selon différentes études, 45% des propriétaires déclarent qu'ils iraient plus souvent chez le vétérinaire s'ils pouvaient mensualiser leurs dépenses et 57% des vétérinaires jugent les plans intéressants. Leur mise en place doit être gérée comme un projet d'équipe car il est essentiel d'emporter l'adhésion de l'ensemble des vétérinaires et des ASV de la clinique. Il ne s'agit pas de forcer un propriétaire à consommer des actes non souhaités mais de lui proposer une solution simple et définie ensemble pour accéder à des soins, qu'il aura délibérément choisis, avec une possibilité d'étalement des dépenses.
III. Facteurs déterminants
La construction et le contenu d'un plan de prévention dépend de plusieurs facteurs :
- l'espèce,
- l'âge de l'animal à la première visite,
- la durée du plan souhaité,
- le budget du propriétaire alloué à la prévention.
IV. Bénéfices
1. Pour le client
Le but d'un plan de prévention pour le client est de :
- planifier des soins personnalisés ;
- maîtriser le budget de prévention ;
- permettre un étalement paiement (mensuel) ;
- concevoir et gérer sur-mesure au cas par cas.
2. Pour la clinique
Le but d'un plan de prévention pour la clinique est :
- d'augmenter la fréquence des visites ;
- une meilleure observance ;
- le principe d'entrées mensuelles ;
- la fidélisation clients ;
- un suivi de santé régulier des animaux ;
- le dépistage précoce d'affections et maladies ;
- la prévention de maladies.
Bibliographie
- https://www.aaha.org/resources/pet-health-resources/preventive-care/
- https://www.depecheveterinaire.com/plans-de-prevention-un-travail-d-equipe-base-sur-l-analyse-des-risques_679D56893E6FAC6D.html
- https://fr.yummypets.com/mag/2016/12/05/83254/les-plans-de-prevention-veterinaires-arrivent-en-france
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Construire une visite pubertaire
Médecine préventive, École Nationale Vétérinaire de Toulouse,Toulouse, France
I. Introduction
Peu de cliniques ont pour le moment développé une vraie consultation pubertaire en plus des 3 visites pédiatriques entre 2 et 4 mois d'âge du chiot ou du chaton. Or cette consultation est une étape clé dans le suivi de santé et de la croissance du jeune animal. Elle permet d'instaurer une étape intermédiaire après les consultations pédiatriques et les bilans de santé de l'animal adulte et d'aborder des sujets et questions non évoqués pendant les consultations pédiatriques. Pendant cette consultation, le vétérinaire doit faire un point sur le développement de l'animal et ne surtout pas se limiter à la seule discussion autour du projet de reproduction.
II. Continuer le suivi sanitaire débuté pendant la période pédiatrique
Sur le plan immunitaire, le vétérinaire doit vérifier les vaccinations déjà réalisées et compléter le protocole vaccinal si nécessaire. Après une analyse de risque, se basant sur le mode de vie de l'animal et son entourage, le vétérinaire doit informer le propriétaire sur les autres vaccins disponibles (vaccins vectoriels par exemple) et les mettre en place selon les besoins de l'individu.
La prévention parasitaire est à adapter selon une analyse de risque et le mode de vie du chiot ou du chaton. L'entourage humain de l'animal est également à prendre en considération. L'accès souvent plus libre à l'extérieur, le comportement de chasse, les activités sociales et les modifications alimentaires accroissent les risques d'infestation. Pourtant, à cet âge, peu d'animaux bénéficient d'une évaluation individualisée du risque parasitaire et d'une prescription régulière.
De nos jours, le protocole de prévention parasitaire doit également prendre en considération l'impact environnemental.
III. Présenter les différentes options de gestion de l'activité génitale
Pendant la consultation pubertaire, les propriétaires sont particulièrement réceptifs à l'exposition des différentes options possibles, tant chirurgicales que médicales. Si elles leur ont déjà été présentées lors de la consultation à l'âge de 16 semaines, ils ont eu le temps de mûrir leur choix. Dans le cas contraire, la consultation pubertaire permet d'accompagner les propriétaires dans leur réflexion. Cette consultation est aussi l'occasion de statuer sur la présence des testicules dans le scrotum, d'examiner la conformation vulvaire (vulve encapuchonnée ou non) ainsi que de détecter précocement des troubles comportementaux contre-indiquant (au moins provisoirement) l'exérèse des gonades.
Les différentes options sont
1. Chirurgicales
- L'ablation chirurgicale des gonades (chien, chat, chienne, chatte) ;
- La vasectomie (chien), l'épidydimectomie (chat) (éventuellement l'hystérectomie pour la chienne et la chatte).
2. Médicales
- Implant de desloréline (Chien Chat Chienne Chatte) sachant que la réversibilité de l'effet d'un implant posé en phase prépubertaire des mâles est sujette à caution
- Implant de mélatonine (Chat Chatte)
Également l'absence de prise en charge chirurgicale ou médicale (sous réserve que les propriétaires soient capables de contrôler la reproduction de leur animal afin d'éviter les portées non désirées).
Trois questions permettent d'aiguiller le choix
- Existe-t-il un projet de mise à la reproduction (y compris dans les années à venir) ?
- Les manifestations de l'activité génitale (pertes de sang, miaulements, attraction du sexe opposé, complications de morsures…) sont-elles gênantes pour les propriétaires ?
- L'ablation chirurgicale des gonades est-elle potentiellement associée à un risque particulier chez l'animal considéré (risque anesthésique, comportemental ou risque racial pathologique de surpoids, d'incontinence urinaire, d'affection tumorale ou orthopédique ; HART et al 2024 ; PEGRAM et al 2019) ?
IV. Faire le bilan de la croissance physique et mentale
Un suivi de poids ainsi qu'une évaluation de la note d'état corporel de l'animal permettent d'ajuster la ration alimentaire aux besoins changeants à l'approche de la puberté et la fin de croissance. Cette prise en charge est essentielle pour éviter tout risque de surpoids juvénile, fréquemment observé, mais également toute carence. Le suivi de la courbe de croissance permet de surveiller tout éventuel décrochage et de le corriger afin d'éviter l'installation d'une surcharge pondérale précoce. Le moment de la consultation pubertaire est souvent concomitant de la stérilisation de l'animal. Il est important de prendre en considération ce changement de statut physiologique et d'adapter la ration alimentaire aux besoins évolutifs ainsi que d'expliquer au propriétaire en quoi consistent ces changements.
Un examen de la cavité buccale permet de vérifier une éventuelle persistance de dents de lait ou problème d'occlusion. Une inspection systématique de la cavité buccale à chaque consultation est recommandée durant toute la phase de croissance. Un contrôle des dents définitives, déjà en place, est à effectuer pour déceler toute possible fracture ou lésion dentaire. À la consultation pubertaire doit également de nouveau être abordée la prévention dentaire si ceci n'a pas déjà été discuté pendant les consultations pédiatriques.
Sur le plan éducatif et du comportement, la consultation pubertaire est un moment clé pour vérifier sa bonne évolution. La puberté constitue une période de grande fragilité et vulnérabilité, pendant laquelle les affections comportementales peuvent soit apparaître, soit s'aggraver nettement. À cet âge, différents points sont à contrôler comme l'attachement, le lien social, la communication ainsi que l'apprentissage des autocontrôles. L'attachement et l'insertion sociale sont plus susceptibles de changement dans cette phase du développement. La détection d'un trouble du comportement de type phobie ou anxiété devrait en particulier conduire à sursoir à l'ablation des gonades.
V. Conclusion
À la différence des consultations pédiatriques à 2, 3 et 4 mois d'âge, aucun acte n'est le plus souvent réalisé lors de la consultation pubertaire. C'est une des raisons pour lesquelles elle peine à se mettre en place en pratique. Il s'agit pourtant d'une consultation intervenant à un moment clé de la vie de l'animal où il est possible de prendre des décisions qui auront un impact à long terme sur la qualité de la relation entre l'animal et son propriétaire. Il s'agit ainsi d'une pierre angulaire de la démarche de médecine préventive.
Bibliographie
- HART LA, THIGPEN AP, HART BL, WILLITS NH, LEE M, BABCHUK MM, LEE J, HO M, CLARKSON ST, CHOU JW. Assisting decision-making on age of neutering for German Short/Wirehaired Pointer, Mastiff, Newfoundland, Rhodesian Ridgeback, Siberian Husky: associated joint disorders, cancers, and urinary incontinence. Front Vet Sci. 2024 Apr 12;11:1322276. doi: 10.3389/fvets.2024.1322276. PMID: 38681849; PMCID: PMC11046931.
- PEGRAM C, O'NEILL DG, CHURCH DB, HALL J, OWEN L, BRODBELT DC. Spaying and urinary incontinence in bitches under UK primary veterinary care: a case-control study. J Small Anim Pract. 2019 Jul;60(7):395-403. doi: 10.1111/jsap.13014. Epub 2019 Apr 29. PMID: 31037739; PMCID: PMC6850460.
- ESCCAP : https://www.esccap.org/uploads/docs/tgqujds5_esccapfranceguide4formata4.pdf
- FREYBURGER L. La consultation en médecine préventive. La Dépêche Technique. 2021 ; 183, 25-27.
- http://vetbrain.fr/wp-content/uploads/2023/04/3edC-travail-Nutrition_veterinaire_S-Lefebvre-coul.pdf
- MASSON S, BLEUER-ELSNER S, MULLER G, MÉDAM T, CHEVALLIER J, GAULTIER E. Veterinary psychiatry in the daily life of the general veterinarian practitioner. In: Veterinary Psychiatry of the Dog. Cham: Springer Nature Switzerland; 2024 [cité 9 avr 2025]. p. 967-97. Disponible sur: https://link.springer.com/10.1007/978-3-031-53012-8_32
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Constuire une visite pédiatrique
Toulouse, France
I. Introduction
Les visites pédiatriques sont un moment clé au début de la vie d'un animal et dans la prise en charge médicale des chiots et chatons. Ils sont également un moment privilégié pour créer un lien de confiance avec l'animal et son propriétaire. Ces visites doivent apporter des soins, prescriptions et conseils adaptés et individualisés à chaque animal et permettre un suivi rapproché pour assurer un bon développement, une bonne santé, une croissance harmonieuse et une bonne intégration dans sa nouvelle famille.
II. Organisation des visites pendant la phase de croissance
Durant la phase de croissance, vous êtes amenés à voir l'animal et son propriétaire entre 2 et 5 fois (dépendant de l'âge auquel l'animal vous est présenté pour la première fois). Dans l'idéal, le vétérinaire voit le chiot ou le chaton pour la première fois directement après l'adoption, à l'âge de 2 mois, puis à 3 et 4 mois d'âge avec une dernière visite au moment de la puberté. Pendant ces consultations, de multiples sujets sont à aborder en partant de la vaccination, l'alimentation, l'éducation, du comportement, de la prévention parasitaire, des soins courants, du projet de reproduction, jusqu'aux éventuels voyages et questions réglementaires. Selon l'âge auquel la première consultation aura lieu, les sujets à aborder pendant la consultation varient et doivent être individuellement adaptés à l'animal et son propriétaire, et ceci d'autant plus s'ils sont primo-adoptant.
1. Visite à 2 mois
À l'âge de 2 mois, les sujets qui ont le plus d'importance pour le propriétaire sont l'éducation et le comportement et plus spécialement l'acquisition de la propreté et l'inhibition de la morsure ou griffure ainsi que le choix alimentaire et la vaccination. Des sujets comme les soins courants et la prévention parasitaire seront également à aborder. Selon les connaissances du propriétaire, c'est également le moment de l'informer sur les bases réglementaires.
2. Visite à 3 mois
À 3 mois d'âge, l'essentiel est de contrôler le bon développement de l'animal et de détecter tout problème comportemental. Toute anomalie non détectée et non prise en charge à cette visite peut devenir pathologique par la suite. Le 2ème sujet essentiel durant cette consultation est le suivi de croissance avec la vérification et l'ajustement de la ration alimentation avant de s'intéresser à la suite de la vaccination, la prévention parasitaire, les questions réglementaires (avec la vaccination antirabique) et le projet de reproduction.
3. Visite à 4 mois
La visite du 4ème mois clôture la première partie du protocole de primovaccinations. C'est également pendant cette consultation qu'est abordé le projet de reproduction ou de stérilisation avec l'approche de la puberté. Cette visite permet de faire un bilan des premiers mois, d'aborder des sujets jusqu'à là non traités ou non évoqués avec le propriétaire et permet de faire un premier bilan avant la visite pubertaire et du bilan à l'âge adulte de l'animal.
III. Adaptation des consultations selon le propriétaire
Selon les connaissances du propriétaire et ses sources d'information (éleveur, internet, famille, …) les sujets à aborder peuvent fortement varier autant que le temps nécessaire pour recueillir une anamnèse complète puis d'apporter les conseils et prescriptions nécessaires pour le bon développement de l'animal. Il est important de ne pas noyer le propriétaire avec trop d'informations d'un coup au moment de la première visite et de partager les sujets à traiter sur les différentes consultations selon leur degré d'importance pour l'animal et ou son propriétaire.
IV. Importance de l'anamnèse
Le recueil d'une anamnèse détaillée sur la provenance et le mode de vie de l'animal, son alimentation, les éventuels traitements déjà reçus, les connaissances du propriétaire etc. déterminent la suite des différentes consultations et leur contenu. Le recueil d'une anamnèse la plus complète à la première visite, même en amont de la consultation, permettront de mieux appréhender l'organisation des différentes consultations.
Le contenu précis des consultations dépend donc de l'âge à laquelle l'animal vous est présenté, son bilan clinique, ses particularités et des connaissances et besoins de son propriétaire.
V. Objectifs de la conférence
Le but de cette conférence est de donner des éléments clés à aborder avec un propriétaire de chiot ou de chaton pendant ces premières consultations de médecine préventive, de savoir construire et mener une consultation de médecine préventive pédiatrique puis d'adapter les soins et conseils à chaque individu et selon les besoins éventuels du propriétaire.
Bibliographie
- FREYBURGER L. La médecine préventive du chien et du chat : histoire et structuration d'une discipline clinique. Académie vétérinaire : https://academieveterinairedefrance.org/fileadmin/user_upload/Publication/BulletinAVF/BAVF_2021/Freyburger_med_prev_chat_chien_bavf_2021.pdf
- FREYBURGER L et coll. La médecine préventive du chien et du chat. Pratique Vét. 2016a ; 51 : 542-552.
- FREYBURGER L. Planification des consultations de médecine préventive. Pratique Vét. 2016b ; 51, 17-21.
- FREYBURGER L. La consultation en médecine préventive. La Dépêche Technique. 2021 ; 183, 25-27.
- https://www.esccap.fr/arthropodes-ectoparasites-du-chien-et-du-chat.html
- https://www.esccap.fr/nematodes-et-cestodes-guide-1.html
- http://vetbrain.fr/wp-content/uploads/2023/04/3edC-travail-Nutrition_veterinaire_S-Lefebvre-coul.pdf
- MASSON S, BLEUER-ELSNER S, MULLER G, MÉDAM T, CHEVALLIER J, GAULTIER E. Veterinary psychiatry in the daily life of the general veterinarian practitioner. In: Veterinary Psychiatry of the Dog [Internet]. Cham: Springer Nature Switzerland; 2024 [cité 9 avr 2025]. p. 967-97. Disponible sur: https://link.springer.com/10.1007/978-3-031-53012-8_32
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Créer du lien : cohabitation entre lapins
Eschau, France
I. Introduction
Le lapin domestique (Oryctolagus cuniculus) est une espèce sociale issue du lapin sauvage, qui vit en garennes structurées dans la nature. Ce mode de vie en groupe repose sur une organisation sociale, une territorialité et de nombreuses interactions, qui présentent un avantage nécessaire à assurer la survie de cette espèce ayant un statut de proie.
II. Besoins éthologiques et environnement inadapté
Les besoins éthologiques, et notamment le budget d'activité, du lapin domestique sont également proches de celui du lapin sauvage. Ils sont souvent mal connus des humains et source d'un environnement inadapté causant ennui, manque d'activités et multiples sources de stress. De nombreux vendeurs de lapins, principalement les animaleries, n'ont pas les connaissances nécessaires et vont indiquer à nos clients qu'il est normal qu'un lapin vive seul et en cage.
Pourtant, à l'état domestique, les comportements sociaux des lapins persistent et constituent un enjeu majeur du bien-être dans cette espèce.
III. Comportements sociaux et cohabitation
Une étude britannique (ROONEY et al., 2014) montre que les comportements affiliatifs sont fréquents entre lapins vivant ensemble, avec principalement du toilettage mutuel, du repos en contact, et des jeux. Toutefois, la cohabitation peut échouer si les besoins éthologiques et environnementaux ne sont pas respectés.
Les conflits peuvent naître d'une mauvaise mise en cohabitation, d'un environnement physique ou social inadapté ou de la présence de facteurs de stress. L'état de santé des animaux va également avoir un très fort impact sur leur comportement. Les interactions agonistiques (bagarres, chevauchements, arrachage de poils) sont alors possibles, surtout chez les mâles pubères ou en contexte de compétition.
1. Éléments essentiels pour réussir une cohabitation
Pour réussir une cohabitation, trois éléments sont essentiels :
- choix du congénère (compatibilité comportementale) ;
- environnement physique sécurisé (cachettes, ressources suffisantes, espace neutre pour la mise en contact, absence de prédateurs et de perception de menace) ;
- lien avec les humains et qualité de l'environnement social (relation apaisée, sans peur).
2. Gestion des conflits
En cas de conflit, il est indispensable d'en identifier la cause : mauvaise qualité du lien ou de la mise en cohabitation, frustration, douleur, changement de statut sexuel ou encore sources de stress dans l'environnement. Les ajustements portent sur la reprise de contacts progressifs qui soient agréables et non anxiogènes pour les lapins concernés, la correction du cadre de vie et la prise en charge de l'état de santé (stérilisation incluse).
IV. Risques de la vie en solitaire
La vie en solitaire d'un lapin n'est pas anodine et doit faire l'objet d'une balance bénéfices-risques pour la qualité de vie de l'animal. Ce choix présente des risques élevés concernant le niveau de stress de l'individu (l'animal ne peut compter que sur lui-même pour la surveillance de l'environnement), l'ennui, le déséquilibre du budget d'activité, l'absence de réponse à une partie de ses besoins éthologiques, dont certains sont impossibles à compenser par une autre espèce (comportements et interactions species-specific). En résulte souvent l'apparition de stéréotypies, témoignant du mal-être de l'animal.
V. Conclusion
En conclusion, la cohabitation, bénéfique pour le bien-être du lapin, ne s'improvise pas. Elle nécessite du temps, de l'observation et une adaptation permanente de l'environnement physique et social. Tout changement dans la dynamique de la relation entre des lapins vivant ensemble doit être considéré comme un signe d'alerte à explorer exhaustivement.
Bibliographie
- BRADBURY G. (2018) Behavioural Problems in Rabbits - a clinical approach, 5M publishing
- BUSETH M E, SAUNDERS R. (2015) Rabbit behaviour, health and care, CABI
- CHU L-R, GARNER J and MENCH J. "A Behavioral Comparison of New Zealand White Rabbits (Oryctolagus Cuniculus) Housed Individually or in Pairs in Conventional Laboratory Cages." Applied Animal Behaviour Science 85, no. 1–2 (January 2004): 121–39.
- CROWELL-DAVIS, S. "Behavior Problems in Pet Rabbits." Journal of Exotic Pet Medicine 16, no. 1 (January 2007): 38–44.
- ROONEY N, BLACKWELL E, MULLAN S, et al. "The Current State of Welfare, Housing and Husbandry of the English Pet Rabbit Population." BMC Research Notes 7, no. 1 (2014): 942.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Créer du lien propriétaire - animal : le training médical des NAC
Le Cannet, France
I. Introduction
Chez les nouveaux animaux de compagnie (NAC), et particulièrement les lapins, furets, oiseaux et reptiles, la médicalisation peut représenter un défi majeur. Espèces proies, souvent stressées par la contention, ces animaux développent facilement des réponses de fuite ou d'agression, compromettant à la fois leur bien-être et l'efficacité des soins. Le training médical basé sur le renforcement positif (Positive Reinforcement Training, PRT) apparaît comme un levier essentiel : il favorise la coopération volontaire de l'animal, réduit le recours à l'anesthésie ou à la contention forcée, et améliore l'observance thérapeutique par les propriétaires. [2]
L'enjeu dépasse le seul acte médical : il s'agit de construire un lien positif propriétaire-animal, en transformant chaque soin en une interaction éducative, préventive et enrichissante.
II. Fondements éthologiques et physiologiques
Les particularités anatomiques et physiologiques des lagomorphes et rongeurs [1]– fragilité osseuse, respiration nasale obligatoire, forte sensibilité au stress – rendent critique la recherche d'alternatives à la contention. Les études comportementales montrent que 57% des lapins luttent lorsqu'ils sont soulevés et 75% manifestent de la peur lorsqu'ils sont manipulés par un étranger [1]. Le PRT, en permettant une participation volontaire, répond directement à cette problématique.
III. Le principe du renforcement positif
Le renforcement positif consiste à associer un comportement coopératif à une récompense motivante (friandise, jeu, contact social). L'animal choisit d'y participer, et le comportement désiré est consolidé par étapes (shaping). HEIDENREICH rappelle que ce processus s'appuie sur des techniques standardisées : signaux de pont (clicker, mot bref), désensibilisation graduelle, capture et mise sous signal des comportements utiles. Contrairement à certaines idées reçues, le PRT ne nécessite aucune privation alimentaire : les renforçateurs peuvent provenir de la ration quotidienne, enrichis de friandises à forte valeur pour l'animal. [1]
IV. Mise en place préventive
Pour être efficace, le training médical doit être initié avant qu'un soin contraignant ne soit nécessaire. Cela permet d'associer les manipulations à des expériences positives et de construire un capital de confiance. [4] L'auteur propose la métaphore du « trust account » : chaque interaction positive alimente ce compte, tandis que les expériences négatives le diminuent. Cette notion est particulièrement pertinente pour les NAC, où la relation propriétaire-animal conditionne l'observance thérapeutique.
V. Applications pratiques aux NAC domestiques
1. Digestif
Les affections digestives (stase, troubles de la motilité, dysbiose) sont fréquentes chez le lapin. [1] Le training médical permet de préparer l'animal à accepter l'administration volontaire de liquides ou compléments via seringue, le gavage assisté de façon non coercitive, et l'habituation au transporteur pour les visites vétérinaires.
2. Respiratoire
Les lapins étant des respirateurs nasaux obligatoires, [1] toute obstruction nasale est critique. Le training peut inclure l'habituation à la nébulisation : apprendre à rester dans une cage de nébulisation associée à des renforçateurs.
3. Urinaire et reproductif
Les affections urinaires (cystites, urolithiases) et les pathologies utérines sont fréquentes. [1] Un protocole de « litter training médical » peut être mis en place pour recueillir facilement des échantillons d'urine.
4. Dermatologique
En cas de pododermatite ou d'abcès, [1] l'animal peut être entraîné à présenter volontairement ses pattes pour inspection et soin topique.
5. Neurologique et locomoteur
Dans les affections neurologiques (encéphalitozoonose, torticolis) ou arthrosiques, [1] des exercices de mobilité douce, physiothérapie et stationnement volontaire facilitent l'examen clinique.
6. Cardiovasculaire et oncologique
Les examens nécessitant contention (échocardiographie, radiographies, cytoponctions) peuvent être facilités par le training. [1] Des protocoles existent déjà en zoo pour conditionner les animaux à accepter des échographies ou prises de sang [2], transposables aux NAC.
VI. Progression et désensibilisation
La clé du succès réside dans une progression adaptée : introduire un objet neutre (seringue bouchée, stéthoscope, thermomètre…), associer chaque contact à une récompense, augmenter progressivement la contrainte (durée de manipulation, intensité du contact), valider chaque étape avant de progresser. Cette démarche permet une désensibilisation généralisée : l'animal devient plus tolérant face à la nouveauté, réduisant son stress global. [2]
VII. Un outil pédagogique et sociétal
Le training médical n'est pas qu'un outil vétérinaire : il constitue une interface éducative pour les propriétaires. En leur enseignant à identifier les renforçateurs, à mettre en place des séquences adaptées et à respecter la progression de leur animal, on améliore à la fois l'observance thérapeutique et la qualité de la relation. ESPINOSA GARCÍA-SAN ROMÁN et al. insistent sur l'évolution de la médecine zoologique et la nécessité de former les praticiens aux NAC dans une approche intégrée One Health. Le training médical, en réduisant stress, zoonoses et accidents, répond pleinement à cette demande sociétale.
VIII. Conclusion
Le training médical par renforcement positif est un outil majeur pour la prise en charge des NAC. Il permet d'améliorer la médicalisation, de réduire le stress et la contention, de favoriser la compliance thérapeutique, et de renforcer le lien entre le propriétaire et son animal. Initié de façon préventive, il s'inscrit dans une médecine vétérinaire moderne, centrée sur le bien-être et la participation volontaire. Il appartient aux praticiens d'intégrer ces techniques dans leur routine et leur pédagogie, et aux structures de formation de les inclure pour répondre aux attentes croissantes des propriétaires de NAC.
Bibliographie
- LAULE G., WHITAKER M. (2003). The Use of Positive Reinforcement Techniques in the Medical Management of Captive Animals. Active Environments.
- QUESENBERRY K. et al. (2020). Ferrets, Rabbits and Rodents: Clinical Medicine and Surgery, 3e éd. Elsevier.
- HEIDENREICH B. (2007). An Introduction to the Application of Science-Based Training Technology. International Avian Trainers Certification.
- MARTIN S. (2024). A Reexamination of the Relationship between Training Practices and Welfare in the Management of Ambassador Animals. Animals, 14(736).
- ESPINOSA GARCÍA-SAN ROMÁN J., QUESADA-CANALES Ó., ARBELO HERNÁNDEZ M., et al. (2023). Veterinary Education and Training on Non-Traditional Companion Animals, Exotic, Zoo, and Wild Animals. Vet Sci, 10(357).
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Cystotomie assistée par needle-scopie pour le retrait des urolithes chez le chien et le chat : 14 cas
Jennyfer THIBAUD
Coauteurs : Laura CUDDY et Poppy BRISTOW
Introduction
Les calculs urinaires sont une affection communément rencontrée chez nos animaux de compagnie. La chirurgie est recommandée lorsque les lithiases ne peuvent être dissoutes par une alimentation adaptée ou lorsque que celles-ci induisent une obstruction urétrale ou des infections urinaires à répétition. [1, 2]
De multiples techniques chirurgicales ont été décrites pour le traitement des calculs urinaires chez le chien et le chat. La cystotomie traditionnelle est associée à de multiples complications, notamment le retrait incomplet des lithiases (décrite dans environ 20 % des cas).
Le NANONEEDLE (NANOSCOPE™, ARTHREX, NAPLES, FL, USA) est un système vidéo-endoscopique de nouvelle génération. Cet instrument, principalement dédié aux chirurgies arthroscopiques en médecine humaine, est ici utilisé dans le cadre d'interventions chirurgicales du bas appareil urinaire chez le chat et le chien.
L'objectif de cet article est de décrire la cystotomie assistée par needle-scopie chez le chat et le chien, ainsi que les résultats obtenus sur une cohorte de quatorze patients.
Matériel et méthodes
Cette étude rétrospective inclut des chiens et chats référés pour le retrait de calculs urinaires. L'âge des patients était compris entre 2-11 ans et leur poids était compris entre 3.9-23 kg.
Un bilan hématologique et biochimique complet, ainsi qu'un bilan radiographique, ont été réalisés pour l'intégralité des patients. La radio-densité ainsi que le nombre de calculs ont été estimés en préopératoire, tout comme la longueur de l'urètre. Dans les cas de lithiases urétrales, une urohydropropulsion rétrograde, a été réalisée en amont de l'intervention.
Technique chirurgicale
Le patient est positionné en décubitus dorsal en salle opératoire. Une cœliotomie caudale ou une incision paramédiane caudale est réalisée en fonction du sexe de l'animal. La vessie est isolée, 3 sutures de traction sont placées (au niveau de l'apex puis de chaque côté de l'incision vésicale). La vessie est incisée et les calculs urinaires visibles sont ensuite retirés. Un cathéter urinaire rigide est ensuite introduit de façon normograde et retrograde dans le but de flusher l'urètre. Avant fermeture de la paroi vésicale, le needle scope (125 mm 1,9 mm) est introduit de façon normograde puis rétrograde (Figure 1) dans le but d'inspecter la paroi vésicale et urétrale (masse, structure, inflammation), ainsi que de confirmer le retrait de la totalité des lithiases (Figure 2).
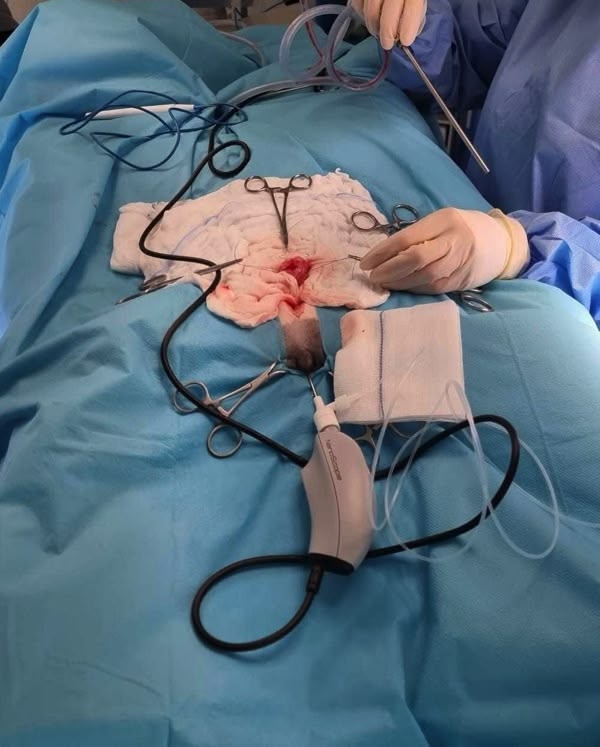
Figure 1
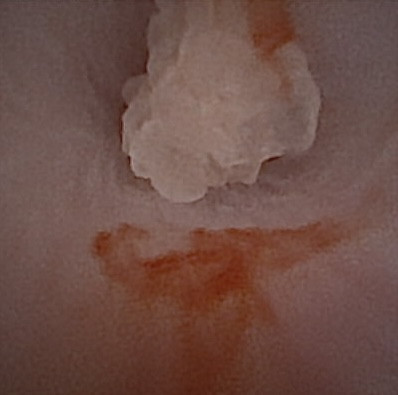
Figure 2
Résultats
L'étude de la base de données a identifié 12 chiens et 2 chats. L'étude a porté sur une durée de 2 ans et demi.
13/14 calculs étaient radio-opaques en préopératoire. La longueur moyenne de l'urètre dans cette population était de 221 mm. La cystotomie assistée par needle-scopie a été faisable dans 100 % des cas. Aucune complication peropératoire n'a été documentée.
100% de la longueur urétrale a été visualisée chez les chats (après urétrostomie périnéale), chattes et chiennes. On estime que 90 à 100 % de l'urètre a été visualisé chez les chiens.
Le NANONEEDLE a permis de diagnostiquer une structure urétrale dans 2 cas.
Un agent bactérien a été identifié dans 4 cas sur 10. L'analyse des urolithes a montré la présence de calculs de cystine dans 5 cas, d'oxalate de calcium dans 5 cas, et d'urate d'ammonium dans 2 cas.
Une radiographie postopératoire a été effectuée dans 6 cas, démontrant l'absence de lithiases.
Le suivi à moyen terme n'a pas permis de mettre en évidence de ré-obstruction ou de récidive.
Discussion
L'intégration du needle-scope peropératoire à la cystotomie ouverte a permis une élimination complète des urolithes dans cette cohorte, sans aucune ré-obstruction urétrale postopératoire. L'endoscopie facilite la détection et l'extraction de petits calculs qui pourraient passer inaperçus lors d'une chirurgie conventionnelle, ainsi que la caractérisation des lésions urétrales et vésicales.
Un NANONEEDLE de 125 mm de long a été utilisé dans cette étude. La longueur moyenne de l'urètre canin dans cette étude était de 221 mm, ce qui correspond aux rapports précédents indiquant une longueur de 225 mm en moyenne. Nous avions anticipé que la longueur et la courbure de l'urètre constitueraient un facteur limitant pour l'utilisation du needle-scope chez les chiens de grande ou très grande race. Des contraintes ont effectivement été observées au niveau de la flexure urétrale. Cependant, un rinçage rétrograde et normograde sous visualisation directe de cette zone large de l'urètre a permis d'atténuer ces difficultés. Un needle-scope de 180 ou 250 mm aurait pu offrir un certain avantage pour nos patients les plus grands.
Conclusion
La cystotomie assistée par needle-scopie est une technique simple à réaliser, offrant une visualisation complète de l'urètre chez le chat (mâle/femelle) ainsi que chez la chienne, et de 90 à 100 % chez le chien mâle. Elle permet de détecter la présence de lithiases persistantes dans l'urètre et de diagnostiquer des lésions urétrales.
Bibliographie
- OSBORNE CA, LULICH JP, KRUGER JM, ULRICH LK, KOEHLER LA. Analysis of 451,891 canine uroliths, feline uroliths, and feline urethral plugs from 1981 to 2007: Perspectives from the Minnesota Urolith Center. Vet Clin Small Anim 2008;39:183-197.
- LOW WW, UHL JM, KASS PH, RUBY AL, WESTROPP JL. Evaluation of trends in urolith composition and characteristics in dogs with urolithiasis: 25,499 cases (1985-2006). J Am Vet Med Assoc 2010;236:193-200.
Liens d'intérêt : Laura Cuddy est consultante pour Arthrex Vet Systems
📃 Dentisterie : être à l'aise avec ses prix
Vélizy-Villacoublay, France
I. Introduction
La dentisterie vétérinaire, lorsqu'elle est pratiquée de manière rigoureuse, est une discipline à la fois technique, exigeante et chronophage. Elle mérite une attention particulière en raison de la très forte prévalence des affections bucco-dentaires, notamment la maladie parodontale, qui constitue de loin la pathologie la plus fréquemment rencontrée en pratique générale. [1,2 ]Face à cette fréquence élevée et à la demande croissante des propriétaires, l'odonto-stomatologie représente non seulement un enjeu de santé animale, mais également une opportunité significative de développement et de valorisation pour la structure vétérinaire.
II. Un examen clinique rigoureux… et long
Un examen bucco-dentaire complet implique une exploration minutieuse de nombreuses structures : muqueuses alvéolaire, jugale, labiale, langue, amygdales, palais dur et mou, plancher buccal… sans oublier, bien sûr, chaque dent, individuellement à l'aide d'une sonde parodontale et d'une sonde exploratrice. On parle de 30 dents chez le chat, 42 chez le chien, chacune avec sa propre morphologie, sa position, ses particularités.
Lorsque l'équipement est disponible, l'examen est complété par des clichés radiographiques intra-oraux, indispensables pour détecter des lésions invisibles à l'œil nu. L'interprétation de ces images demande du temps, du savoir-faire et une mise en perspective avec les observations cliniques.
III. Une prise en charge globale et individualisée
L'étape diagnostique est suivie d'une réflexion thérapeutique, qui doit intégrer les capacités de soins post-opératoires à court et à long terme, le niveau d'observance du propriétaire et, bien sûr, le bien-être de l'animal. Tout cela aboutit à la proposition d'un ou plusieurs plans de traitement. Ce processus est exigeant, il mérite d'être reconnu et valorisé à sa juste mesure.
IV. Un matériel spécifique, des compétences pointues
Le matériel nécessaire à une prise en charge de qualité en dentisterie a un coût : unité dentaire, détartreur, générateur pour radiographie intra-orale, capteurs numériques ou plaques phosphores, instrumentation spécifique, etc. Ces équipements doivent être entretenus, renouvelés et amortis.
À cela s'ajoute la compétence du vétérinaire : si vous avez suivi des formations complémentaires, souvent coûteuses en temps et en argent, c'est pour offrir des soins de meilleure qualité. Cette expertise fait partie intégrante de la valeur de l'acte, et doit être prise en compte dans la tarification.
V. Ce raisonnement s'applique à d'autres disciplines
Le raisonnement que l'on applique ici à la dentisterie vaut tout autant pour d'autres actes techniques ou chirurgicaux, comme une laparotomie exploratrice. Temps de travail, technicité, investissements matériels, charges fixes, salaires… Tous ces éléments doivent entrer dans la réflexion tarifaire.
Et au-delà de l'amortissement des coûts, il est légitime de viser un bénéfice : c'est ce qui permet d'assurer la pérennité de la structure, de continuer à former l'équipe, de maintenir un haut niveau d'équipement et de soins.
VI. Transparence et pédagogie : clés de la confiance
Les soins dentaires sont souvent mieux acceptés par les clients quand ils comprennent leur complexité. Faire le lien avec la dentisterie humaine peut s'avérer utile : chacun sait que ce sont des soins coûteux, souvent mal remboursés. Cela facilite l'acceptation du coût en médecine vétérinaire.
Il est important de prendre le temps d'expliquer que ce que l'on voit à l'œil nu n'est que la partie émergée de l'iceberg. Que chaque dent est sondée à l'aide d'instruments spécifiques. Que l'examen détaillé et complet ne peut se faire que sous anesthésie générale, avec induction, surveillance anesthésique, intubation, protection des voies respiratoires. Que la morphologie dentaire chez l'animal est plus complexe que chez l'humain.
Ce temps consacré à l'explication renforce la confiance du client et facilite l'adhésion au plan de soins. Il s'inscrit dans une attente croissante de transparence : les propriétaires souhaitent aujourd'hui être pleinement informés, tant sur la nature des actes que sur leur coût.
Une enquête récente a montré que les clients préfèrent être informés des coûts potentiels à l'avance, notamment pour les soins techniques comme la dentisterie, et souhaitent participer à la décision thérapeutique. [3]
VII. Conclusion
Prendre le temps de réfléchir à sa tarification — même de manière simple — en intégrant le temps consacré, la technicité des actes, les coûts engagés, les charges de la structure, et être conscient de la valeur ajoutée des soins pour l'animal, permet d'être naturellement plus à l'aise pour annoncer ses prix. Mais cela ne suffit pas : l'acceptation du coût par le client repose aussi sur sa compréhension de la situation médicale. Plus le propriétaire perçoit la gravité de la maladie, la nécessité des soins et leur impact positif sur le bien-être de son animal, plus il sera enclin à accepter et valoriser la démarche thérapeutique proposée. En somme, plus vous êtes convaincus de la justesse de vos tarifs, et plus vous aidez le client à comprendre ce qu'il y a derrière chaque acte, plus vous augmentez les chances qu'il y adhère. [4]
Bibliographie
- O'NEILL DG. et coll. Prevalence of commonly diagnosed disorders in UK dogs under primary veterinary care: results and applications. BMC Vet Res. 2021; 17(1) 69.
- O'NEILL DG. et coll. Prevalence of disorders recorded in cats attending primary-care veterinary practices in England, The Veterinary Journal. 2014; 202 (2): 286-291
- GROVES CNH. et coll. Clients prefer collaborative decision-making with veterinarians regardless of appointment type. J Am Vet Med Assoc. 2025; 263(1):1-11.
- American Animal Hospital Association (AAHA). How to boost dental revenue: Educate clients, price accurately, and improve team confidence. Trends Magazine. Consultable sur : https://www.aaha.org/trends-magazine/publications/how-to-boost-dental-revenue. Dernier accès le 1er août 2025.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Description d'une série de cinq chiens atteints d'échinococcose alvéolaire dans l'Est de la France
Alice KÉFER
Coauteurs : BETTING Adeline, BAILLY Laurence, MAHINC Mathias, RANNOU Benoît, LECOINDRE Alexis
Introduction
L'échinococcose alvéolaire est une zoonose parasitaire affectant principalement le foie, causée par des larves d'Echinococcus multilocularis, endémique en Europe centrale. En France, elle est présente dans la moitié Nord-Est et progresse vers le Sud-Ouest [1]. Elle peut être mortelle pour l'homme, qui s'infecte par ingestion de nourriture souillée ou contact direct avec des selles infectées. Elle se manifeste par une masse hépatique kystique pouvant provoquer des lésions à distance[2]. Le parasite affecte les renards et autres canidés, hôtes définitifs, qui libèrent des œufs dans leurs matières fécales. Les œufs sont ingérés par des rongeurs, hôtes intermédiaires. Les chiens deviennent hôtes définitifs en ingérant un rongeur infecté. Des cas de chiens devenus hôtes intermédiaires par ingestion d'œufs et développant la maladie ont été rapportés[2]. L'échinococcose alvéolaire canine est peu documentée et probablement sous-diagnostiquée. Le diagnostic différentiel inclut les abcès et processus néoplasiques hépatiques[3].
Anamnèse et examen clinique
Cinq chiens sont présentés dans trois cliniques vétérinaires de l'Est de la France pour distension abdominale et perte de poids depuis plusieurs semaines. Leur moyenne d'âge est de 4 ans. L'examen clinique révèle une masse abdominale crâniale palpable avec un état général relativement conservé.
Démarche diagnostique
Un bilan sanguin hémato-biochimique est systématiquement réalisé. Une échographie abdominale et un scanner thoraco-abdominal révèlent la présence d'au moins une volumineuse masse hépatique cavitaire. Chez deux chiens, des nodules pulmonaires sont également observés. Une cytologie du liquide kystique est effectuée chez quatre chiens, révélant des structures membranaires parasitaires. Une PCR sur liquide kystique est positive pour l'ADN d'Echinococcus multilocularis chez trois chiens. Deux chiens ont subi une chirurgie, confirmant histologiquement la présence de larves de cestodes. Un troisième chien a subi des biopsies hépatiques par TRU-CUT, confirmant l'échinococcose.
Traitement
Deux chiens, sans métastases parasitaires ni envahissement abdominal, ont subi une chirurgie. Le premier présentait une atteinte trop étendue du foie pour une lobectomie. La cavité a été drainée puis omentalisée. Il a été traité avec de l'albendazole à vie et présente un bon état général 2,5 ans après le diagnostic. Le second a subi une lobectomie hépatique suivie d'un traitement mensuel au praziquantel. Une récidive a été observée 1,5 an après l'intervention avec dissémination abdominale de kystes parasitaires. L'étendue des lésions n'a pas permis une seconde chirurgie. Un an plus tard, son état général s'est sévèrement dégradé et il a été euthanasié 2,5 ans après le diagnostic.
Trois chiens n'ont pas bénéficié de chirurgie en raison de la complexité de l'intervention et de la présence de métastases parasitaires pulmonaires. Le premier a été traité avec de l'albendazole à vie et présente un bon état général huit mois après le diagnostic. Le deuxième, avec envahissement de la veine cave caudale et métastases pulmonaires, a été traité avec de l'albendazole à vie. Huit mois après le diagnostic, il a présenté une récidive avec aggravation de l'invasion de la veine cave caudale aux examens d'imagerie. Il a conservé un bon état général pendant 10 mois après le diagnostic avant d'être euthanasié pour des raisons sanitaires. Le dernier chien n'a reçu aucun traitement médical. Aucun suivi n'est disponible.
Conclusion
Bien que les chiens développant la forme larvaire de l'échinococcose alvéolaire ne soient généralement pas contaminants pour l'homme, ils pourraient héberger des adultes dans leur intestin, s'auto-infecter et infecter l'homme via l'environnement [3],[4]. Il est donc crucial pour le vétérinaire de diagnostiquer la maladie afin de prévenir les propriétaires. Le diagnostic est souvent tardif, rendant la résection complète parfois impossible[4]. L'échinococcose canine évolue plus rapidement que chez l'homme, étant donné le jeune âge des chiens affectés. Ces éléments soulignent l'importance de la prévention et du diagnostic précoce dans les zones endémiques. Des recherches sont menées chez le chien pour développer une technique sérologique permettant un diagnostic plus précoce [4]. La durée de vie médiane ne diffère pas significativement entre les chiens ayant subi une résection incomplète suivie d'un traitement médical et ceux traités uniquement médicalement [2]. La chirurgie devrait être envisagée uniquement lorsque la résection complète est possible[2]. Le traitement médical repose sur l'utilisation d'albendazole, seul ou après une chirurgie [2]. L'utilisation mensuelle de praziquantel dans les régions endémiques est recommandée afin de limiter la dispersion d'œufs dans l'environnement et de réduire le risque zoonotique [3]. Le pronostic reste réservé et la survie au long terme limitée.
Bibliographie
- COMBES B. Alveolar echinococcosis a full spreading zoonotic disease. Bull Acad Natl Med 2019
- CORSINI M, GEISSBÜHLER U, HOWARD J, GOTTSTEIN B, SPRENG D, FREY CF. Clinical presentation, diagnosis, therapy and outcome of alveolar echinococcosis in dogs. Vet Record 2015
- PINARD C, CUQ B, GIBSON T, et al. Case Report Alveolar Echinococcosis in an Ontario Dog Resembling an Hepatic Abscess. Can Vet J 2019
- FREY CF, MARREROS N, RENNEKER S, et al. Dogs as victims of their own worms: Serodiagnosis of canine alveolar echinococcosis. Parasites & Vectors 2017
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Deux cas de méga-estomac consécutifs à un épisode de dilatation et torsion de l'estomac traités par gastrectomie longitudinale
Andréa DELEANI
Coauteurs : Diego ROSSETTI, Olivier DOSSIN, Jean-Philippe BILLET
Introduction
Le syndrome de dilatation et torsion de l'estomac (SDTE) est une affection fréquente chez les chiens de grande race, nécessitant en premier lieu une prise en charge d'urgence associée par la suite à une gastropexie. La récidive est rapportée dans 2 à 10 % des cas. Des anomalies de la motilité et un retard de vidange gastrique ont déjà été rapportés après un SDTE. Aucune complication à long terme, comme une dilatation gastrique chronique, n'a été rapportée. Deux cas de dilatation gastrique chronique et sévère, appelés méga-estomacs, sont décrits chez deux jeunes chiens de grande race ayant été pris en charge pour un SDTE par gastropexie et ayant nécessité par la suite une gastrectomie longitudinale en raison d'une hypomotilité gastrique réfractaire.
Matériel et résultats
Deux chiens de grande race, un Bouvier Bernois femelle stérilisée et un Saint-Bernard mâle castré, ont été pris en charge pour un ,respectivement à l'âge de 1 et 5 ans. Ils ont été traités par gastropexie incisionnelle. Environ une semaine après la chirurgie, des épisodes récurrents de vomissements alimentaires tardifs associés à plusieurs dilatations gastriques nécessitant une prise en charge médicale sont rapportés. Après plusieurs mois sans amélioration une prise en charge chirurgicale par gastrectomie longitudinale a été décidée.
Le Bouvier Bernois a présenté les premiers vomissements alimentaires 5 jours après la gastropexie. Un mois plus tard, une dilatation sévère a nécessité une laparotomie exploratrice, révélant une déhiscence de la gastropexie. Une nouvelle fixation et des biopsies gastriques ont été réalisées, montrant une gastrite fundique chronique légère. Une hypomotilité gastrique a été mise en évidence sous échographie. Un hypocorticisme a été écarté. Des échographies de suivi ont révélé une hypokinésie et un retard de vidange gastrique. Une gastroduodénoscopie, réalisée quatre mois après le SDTE, a confirmé une hypomotilité sévère et une topographie gastrique modifiée.
Le Saint-Bernard a également présenté des vomissements alimentaires réguliers et une récidive de dilatation traitée par sondage et laparotomie exploratrice, lors de laquelle une gastropexie bilatérale a été réalisée. Trois semaines plus tard, un nouvel épisode de dilatation sévère a nécessité une prise en charge spécialisée. Une gastroduodénoscopie a mis en évidence une atonie gastrique majeure. Les biopsies ont montré une gastrite fundique discrète et un scanner thoraco-abdominal a confirmé la dilatation importante de l'estomac. Un hypocorticisme a également été exclu.
Un traitement médical symptomatique a été instauré, comprenant maropitant, métoclopramide, oméprazole et sucralfate, associé à une alimentation hyperdigestible administrée de manière fractionnée. En raison de la persistance des symptômes, une gastrectomie longitudinale a été décidée. Cette intervention a consisté en une exérèse verticale du fundus, réduisant la taille de l'estomac d'environ deux tiers. Une technique de suture conventionnelle a été utilisée pour l'un des chiens, tandis que des agrafes automatiques ont été ajoutées pour l'autre. La période postopératoire s'est déroulée sans complications et les chiens ont rapidement repris une alimentation humide et hyperdigestible. Le Bouvier Bernois a reçu du maropitant et du sucralfate à la sortie d'hospitalisation, tandis que le Saint-Bernard n'a reçu qu'un antibiotique. Les deux chiens ont retrouvé leur poids de forme en peu de temps. À trois mois postopératoires, le Bouvier Bernois présentait encore deux épisodes de vomissements par semaine, tandis que le Saint-Bernard n'en avait qu'un par semaine un an après l'intervention. Les vomissements ne sont plus alimentaires. Aucun des deux n'était plus sous traitement.
Discussion
Aucune publication scientifique ne décrit à ce jour l'apparition d'une dilatation sévère et chronique de l'estomac après un SDTE. Ce phénomène pourrait être lié à une distension irréversible des fibres musculaires gastriques ou potentiellement à un dysfonctionnement des cellules interstitielles de CAJAL, qui agissent comme pacemaker gastrique. La gastrectomie longitudinale, aussi appelée « sleeve gastrectomie », est peu utilisée en médecine vétérinaire. Toutefois, dans ces deux cas, elle a permis une amélioration clinique notable avec peu de complications, hormis des vomissements non alimentaires occasionnels et du pica.
Conclusion
Le méga-estomac est une complication du SDTE encore jamais décrite. Ses signes cliniques initiaux étant relativement communs, il est essentiel de rechercher précocement une hypomotilité gastrique, en particulier lorsque la dilatation devient chronique et sévère. Si cette dernière ne répond pas au traitement médical, la gastrectomie longitudinale apparaît comme une option chirurgicale efficace, permettant une amélioration clinique des patients.
Bibliographie
- COLEMAN and al - Evaluation of gastric motility in nine dogs before and after prophylactic laparoscopic gastropexy: a pilot study - Aust Vet J 2019;97:225-230
- PRZYWARA and al - Occurrence and recurrence of gastric dilatation with or without volvulus after incisional gastropexy - Can Vet J 2014;55:981-984
- GAZZOLA and al - The Relationship Between Gastrointestinal Motility and Gastric Dilatation-Volvulus in Dogs - Topics in Companion An Med 29 (2014)
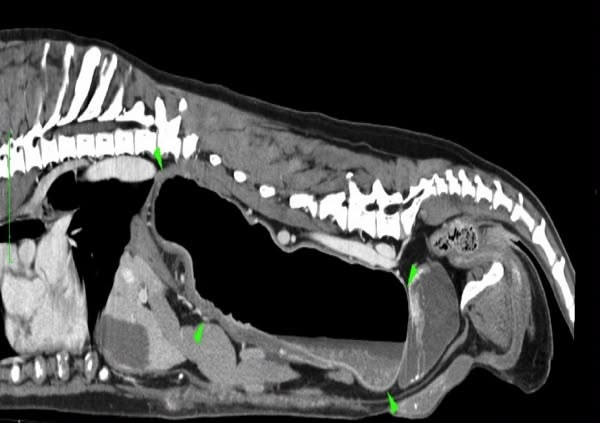
Figure 1 : dilatation marquée de l'estomac mise en évidence au scanner. Vue de profil.
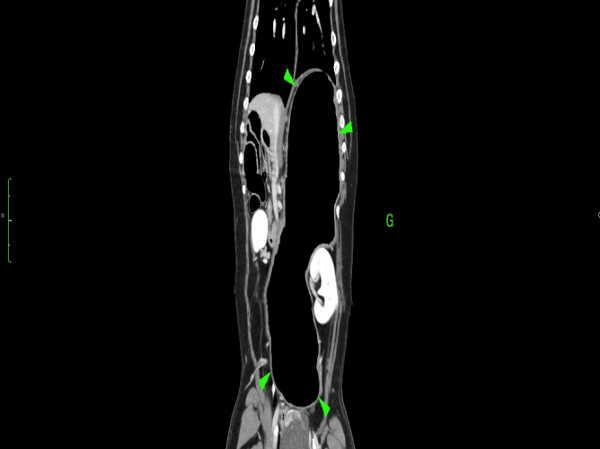
Figure 2 : dilatation marquée de l'estomac mise en évidence au scanner. Vue de face.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Développement et validation d'un questionnaire d'évaluation de la qualité de vie des chiens atteints d'entéropathie chronique
Juan HERNANDEZ
Coauteurs : Claire VEROLLET, Florian OGGIANO, Capucine VITU, Amandine DRUT, Odile SÉNÉCAT, Cyril DUPERRIER-SIMOND, Moez RHIMI, Rodolfo OLIVEIRA LEAL, Suzy VALENTIN, Elodie DARNIS, Tristan MÉRIC, Juan HERNANDEZ
Introduction
Les entéropathies chroniques (EC) du chien regroupent des affections digestives caractérisées par des signes cliniques récurrents ou persistants, nécessitant fréquemment un traitement au long cours et des consultations vétérinaires régulières. Ces maladies peuvent altérer durablement la qualité de vie (QV) des chiens, mais aussi celle de leurs propriétaires. Or, aucun outil validé à ce jour ne permet une évaluation fiable et reproductible de cette QV [1-3]. L'objectif de cette étude est de développer et valider un questionnaire destiné à évaluer la QV des chiens atteints d'EC ainsi que celle de leurs propriétaires.
Matériel et méthodes
Le questionnaire a été construit selon une démarche psychométrique rigoureuse. Les items ont été élaborés à partir d'une revue de la littérature, d'outils existants en médecine humaine et vétérinaire et d'une consultation d'experts vétérinaires. Chaque item comprenait deux volets : la fréquence de survenue et l'impact perçu de l'événement sur la QV. Après une première relecture par un panel de vétérinaires et un prétest auprès de propriétaires de chiens, la version finale du questionnaire a été diffusée en ligne, en français et en anglais, entre septembre 2024 et mars 2025 via des vétérinaires et les réseaux sociaux. Les propriétaires de chiens atteints d'EC, atteints d'une autre maladie chronique ou sains étaient invités à répondre au questionnaire de façon anonyme. La cohérence interne du questionnaire a été mesurée avec un coefficient a de Cronbach. Les réponses étaient ensuite analysées pour sélectionner les items les plus pertinents : seuls ceux différenciant les groupes selon un test U de Mann-Whitney (p < 0,2), présentant une corrélation suffisante avec l'ensemble des autres questions (r >= 0,3) et non redondants (r selon Pearson < 0,7) ont été conservés. Un score global était obtenu en multipliant les scores des deux volets de chaque item puis en calculant la somme des scores individuels des items. La validité a été évaluée par corrélation de Spearman avec une évaluation globale de la QV (échelle de 1 à 10) et la fidélité test-retest et inter-observateur par coefficients de corrélation intraclasse (CCI).
Résultats
Au total, 296 questionnaires complets ont été analysés : 118 pour des chiens atteints d'EC, 73 pour des chiens atteints d'autres maladies chroniques et 105 pour des chiens sains. Vingt-huit items ont été retenus dans la version finale du questionnaire, avec une excellente cohérence interne (a = 0,89). Le score global différenciait significativement les trois groupes (EC > autres maladies > chiens sains ; p < 0,001). Il était fortement corrélé à la note de QV (rho = -0,67 ; p < 0,001). La fidélité inter-observateur était excellente (CCI = 0,97) et la fidélité intra-observateur bonne (CCI = 0,76). Les items ayant le plus de poids étaient majoritairement liés au ressenti par le propriétaire.
Discussion
La validation de ce questionnaire met en évidence l'intérêt d'une approche standardisée pour évaluer la QV des chiens atteints d'EC et de leurs propriétaires. La forte cohérence interne et les bons indices de fidélité suggèrent une bonne stabilité de l'outil dans le temps et entre observateurs. La capacité du score global à différencier les chiens atteints d'EC des chiens sains ou présentant d'autres maladies chroniques confirme sa pertinence clinique et sa spécificité. Les items les plus fortement pondérés concernaient majoritairement ceux évaluant la perception du propriétaire, ce qui souligne l'importance de la charge émotionnelle et organisationnelle que représente la gestion d'un animal atteint d'EC au quotidien. Cette dimension "charge de l'aidant", bien décrite en médecine humaine dans les maladies inflammatoires chroniques de l'intestin, est encore peu explorée en médecine vétérinaire. La prise en compte du ressenti du propriétaire dans l'évaluation de la qualité de vie constitue une avancée importante, à la fois pour orienter la prise de décision thérapeutique mais aussi pour renforcer le lien entre le vétérinaire et le propriétaire.
Conclusion
Ces résultats valident l'utilisation de ce questionnaire comme outil fiable d'évaluation de la QV des chiens atteints d'EC. Il permet d'objectiver l'impact de la maladie et de guider les décisions cliniques. Son intégration en pratique vétérinaire pourrait renforcer la prise en compte du bien-être animal et du vécu des propriétaires dans la gestion à long terme de ces affections.
Bibliographie
- DÍAZ-REGAÑÓN D et al., 2023. Assessing the Quality of Life of Dogs with Inflammatory Bowel Disease and Their Owners. Vet Sci. 10(7):405.
- LYNGBY JG et al., 2025. Chronic enteropathy in dogs affects the quality of life in both dogs and their owners-are veterinarians proficient in handling the caregiver burden? Front Vet Sci. 11:1488917.
- MARCHETTI V et al., 2021. The Impact of Chronic Inflammatory Enteropathy on Dogs' Quality of Life and Dog-Owner Relationship. Vet Sci. 8(8):166.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Diabète sucré : le point de vue de l'interniste
Gentilly, France
I. Introduction
Le diabète sucré est l'une des endocrinopathies les plus fréquemment rencontrées en pratique vétérinaire. Il s'agit d'une affection chronique complexe, ayant un impact important sur la qualité de vie de l'animal et sur l'investissement des propriétaires. Sa prise en charge nécessite une compréhension approfondie de sa physiopathologie, de ses comorbidités fréquentes et des différentes options thérapeutiques disponibles.
II. Diagnostic
Le diabète sucré se manifeste classiquement par un syndrome polyuro-polydipsique associé à une polyphagie et un amaigrissement progressif. Le diagnostic repose sur la mise en évidence d'une hyperglycémie persistante, souvent associée à une glycosurie, et peut être confirmé par le dosage de la fructosamine. Chez le chien, la majorité des cas correspond à un diabète insulinodépendant, secondaire à une destruction des cellules bêta pancréatiques. Chez le chat, en revanche, la maladie s'apparente davantage au diabète de type II de l'homme, associant insulinorésistance et déficit relatif en insuline, avec une possible réversibilité si la prise en charge est initiée précocement.
III. Comorbidités et pathologies associées
Le diabète sucré ne doit pas être envisagé comme une maladie isolée. De nombreuses affections concomitantes peuvent influencer son expression clinique et compliquer son équilibre (pancréatite chronique, lipidose hépatique, polyneuropathie, infection urinaire entre autres).
Sur le plan endocrinien, plusieurs pathologies doivent être envisagées comme sources d'insulinorésistance. L'hyperadrénocorticisme chez le chien et l'hyperthyroïdie chez le chat en sont des exemples bien connus. L'acromégalie féline, ou plus particulièrement l'hypersomatotropisme résulte d'une hypersécrétion d'hormone de croissance par une tumeur hypophysaire. Cette affection, probablement sous-diagnostiquée, est responsable d'une résistance marquée à l'insuline et doit être suspectée chez les chats nécessitant des doses d'insuline supérieures à 1,5–2 U/kg. Le diagnostic repose sur la mise en évidence d'une élévation de l'IGF-1 et peut être confirmé par une imagerie cérébrale.
IV. Prise en charge thérapeutique et monitoring
Plusieurs évolutions ont marqué les dernières années dans le monitoring et la prise en charge du diabète sucré des animaux de compagnie.
1. Technologies de monitoring
La technologie des glucomètres a considérablement évolué depuis les années 1990, aboutissant récemment à des dispositifs miniaturisés de mesure continue du glucose interstitiel, utilisables chez les animaux de compagnie. Le système le plus répandu est le FreeStyle Libre ND (Abbott), composé d'un capteur à usage unique actif pendant 10 à 14 jours, inséré intradermiquement et délivrant les valeurs de glucose instantanément via un lecteur ou un smartphone (Del Baldo, 2023).
Ce dispositif permet la détection des épisodes hypoglycémiques et le suivi de la glycémie au quotidien, facilitant l'adaptation de l'insulinothérapie sans hospitalisation ni stress pour l'animal. Plusieurs études ont validé la corrélation entre glucose interstitiel et glycémie chez le chien et le chat, y compris en cas d'acidocétose, bien que des limites existent lors de changements rapides de glycémie ou d'hypoglycémies importantes (<2,7 mmol/L), nécessitant une vérification par mesure classique (Del Baldo, 2020).
L'intérêt principal réside dans l'identification précise des nadirs et des hypoglycémies. Les ajustements d'insuline basés sur les données continues sont en général plus fins qu'avec des mesures ponctuelles, réduisant le risque de surdosage. Cependant, la variabilité glycémique inter-journalière, souvent supérieure à 60 % chez le chien et observée également chez le chat, oblige à interpréter plusieurs jours de données pour éviter des conclusions hâtives.
Enfin, l'accès permanent aux données peut générer du stress chez certains propriétaires, 12 % des sondés rapportant une anxiété liée au suivi intensif, et le coût récurrent de ces dispositifs doit être pris en compte dans la gestion à long terme du diabète (Re et al., 2022).
2. Insulinothérapie
Concernant la prise en charge thérapeutique, l'insulinothérapie demeure le traitement de référence du diabète sucré chez le chien comme chez le chat. Les insulines de longue action sont celles dont l'action est supérieure à 24 heures chez l'homme. L'intérêt de ces molécules est de diminuer les variations de glycémie sur 24 heures et d'une injection à l'autre. Cela a aussi pour conséquence la diminution du nombre d'administrations. Chez le chien et le chat, deux insulines dominent dans cette indication : l'insuline glargine U-300 (Toujeo Nd, Sanofi= insuline glargine, similaire au Lantus ND, mais 3 fois plus concentrée), et l'insuline degludec (Tresiba ND, Novo Nordisk). Cette dernière est un analogue d'insuline humaine, où l'acide aminé 30 est remplacé par un d'ester d'acide gras, permettant de former un dépôt dans le tissu sous-cutané, d'où une libération plus lente.
Chez le chien, son effet hypoglycémiant semble moins prononcé, la rendant intéressante pour les traitements des chiens de petite taille. Là aussi, d'autres données à grande échelle sont nécessaires.
3. Inhibiteurs SGLT2
De nouvelles perspectives thérapeutiques se sont ouvertes récemment avec l'introduction des inhibiteurs du cotransporteur sodium-glucose de type 2 (SGLT2), ou gliflozines. Les protéines SGLT sont des protéines transmembranaires co-transport du glucose. Plusieurs formes, SGLT1 et SGLT2, sont présentes dans le rein, dans les néphrons. Le récepteur SGLT1 est aussi présent dans la paroi de l'intestin grêle. L'utilisation d'un inhibiteur SGLT2, appelé glifozine, permet donc d'inhiber cette réabsorption, permettant d'abaisser la glycémie en favorisant l'excrétion urinaire du glucose. (Figure 1)
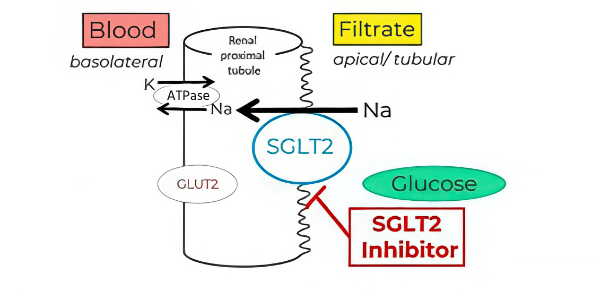
Figure 1 : récepteur SGLT2 au niveau rénal (d'après https://tmedweb.tulane.edu/pharmwiki/doku.php/sglt2_inhibitors)
Cette action est indépendante de l'insuline. Plusieurs molécules existent sur le marché humain (canaglifozin, dapaglifozin, empaglifozin, ertugloflozin) et deux sont disponibles aux États-Unis avec une AMM chez le chat. (Tableau 1)
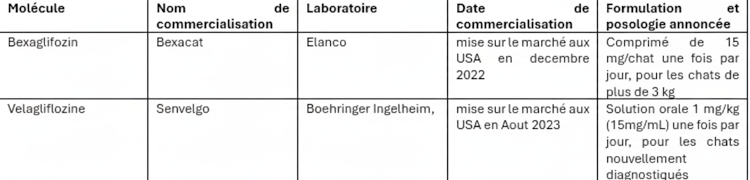
Tableau 1 : Inhibiteurs du cotransporteur de sodium-glucose de type 2 chez l'animal
Chez l'homme, cette classe thérapeutique est utilisée depuis 2012 et semble améliorer le contrôle glycémique, favoriser la perte de poids chez les patients atteints de diabète sucré de type 2 et améliorer la fonction des cellules pancréatiques B lors d'état de glucotoxicité. Chez le chat, étant donné certaines caractéristiques communes (insulino-resistance, état de surpoids, persistance d'une petite proportion de cellules B fonctionnelles), l'utilisation des glifozines dans le traitement du diabète sucré a été envisagée. Les intérêts avancés du traitement seraient de baisser rapidement la glycémie, d'améliorer la sensibilité à l'insuline produite de manière endogène, et pour le pancréas, d'être moins exposé à la glucotoxicité, améliorant ainsi la survie et la fonction des cellules B des îlots pancréatiques.
Depuis la première description de l'utilisation de velaglifozin en 2018, plusieurs études, dont les études terrains pour obtenir une AMM ont été réalisées, amenant à des résultats prometteurs (Hadd et al, 2023, Niessen et al, 2023). La cible de traitement est constituée par les chats de plus de 2 ans, nouvellement diagnostiqués, sans état d'acido-cétose. Parmi les résultats, on observe une amélioration de signes cliniques (polyphagie, polyurie, polydipsie) pour plus de 80 % des chats traités, et un contrôle glycémique jugé satisfaisant. Il est à noter que les critères d'inclusion ne sont pas identiques entre les études (chats nouvellement diagnostiqués diabétiques ou traitement précédent par insuline notamment), et que pour certaines d'entre elles, il n'y a pas de comparaison de cette nouvelle classe de traitement au gold standard par insulinothérapie. Enfin, la définition d'acido-cétose est parfois basée sur un test urinaire (détection d'acétate et acéto-acétate, souvent stade plus avancé) ou sanguin (mesure du B-hydroxybutyrate sanguin, anormal si supérieur à 1 mmol/L, acido cétose confirmée si supérieure à 2,5 mmol/L).
Parmi les effets secondaires observés, les troubles digestifs sont les plus fréquents (diarrhée, vomissements, notamment par interaction avec le récepteur SGLT-1 au niveau digestif). Aucun animal n'a présenté à priori d'hypoglycémie clinique. L'effet secondaire le plus sérieux demeure le risque d'acido-cétose avec une situation particulière d'euglycémie : la trilogie d'une cétonurie/cétonémie + une glycémie inférieure ou égale à 2,5 g/L + une acidémie chez un animal débilité est alors caractéristique. Cela tranche avec la situation classique d'hyperglycémie habituellement rencontrée chez les chats traités par insuline. Selon les données fournies par les études, les complications cétosiques surviennent 1 à 2 semaines après l'initiation du traitement et pour 5 à 15 % des chats traités.
En conclusion, ces molécules présentent l'avantage d'une administration orale quotidienne, ce qui peut constituer une alternative attractive pour certains propriétaires réticents aux injections. Néanmoins, elles ne remplacent pas l'insuline et doivent être utilisées avec prudence, en raison de risques potentiels tels que les infections urinaires, la déshydratation ou, plus rarement, l'acidocétose diabétique euglycémique. La population cible recommandée pour ce traitement est constituée par les chats nouvellement diagnostiqués diabétiques, en état corporel normal ou avec embonpoint, et avec un appétit conservé, et ce pour diminuer les risques d'acido-cétose. Mais son utilisation sous contrôle très rigoureux et hors AMM est décrite et publiée dans des séries de cas, dans des situations autres : chat acromégale, chien traité de manière simultanée avec une insuline injectable, …
4. Gestion nutritionnelle
La gestion nutritionnelle demeure enfin un pilier complémentaire. Chez le chien, l'accent est mis sur le contrôle pondéral et une alimentation équilibrée, tandis que chez le chat, une ration riche en protéines et pauvre en glucides est recommandée afin de réduire l'insulinorésistance et de favoriser une éventuelle rémission.
Bibliographie
- DEL BALDO et coll. Continuous glucose monitoring in dogs and cats. Application of new technology to an old problem. Vet Clin Small Anim 2023; 53:591-613.
- DEL BALDO et coll. Comparison between a flash glucose monitoring system and a portable blood glucose meter for monitoring dogs with diabetes mellitus. J vet Intern Med 2020; 34:2296-305
- RE et coll. Monitoring of diabetes mellitus with flash glucose monitoring system: the owner's point of view. 32nd ECVIM-CA congress September 1-32022: Gothenburg, Sweden.
- HADD et coll. Safety and effectiveness of the sodim-glucose cotransporter inhibitor bexaglifozin in cats newly diagnosed with diabetes mellitus. J Vet Med Intern 2023; 37: 915-24
- NIESSEN et coll. Once-Daily Therapy for Feline Diabetes Mellitus: SGLT-2- Inhibitor Velagliflozin as Standalone Therapy Compared to Insulin Injection Therapy in Diabetic Cats. ECVIM-CA congress September 1-32022: Gothenburg, Sweden.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Diabète sucré : le point de vue de l'ophtalmologiste
Toulouse, France
I. Introduction
Le diabète sucré est une maladie endocrinienne fréquente chez le chien et le chat, avec des répercussions notables sur l'œil, en particulier chez le chien. [1]
II. Complications oculaires chez le chien
Chez ce dernier, la complication oculaire majeure est la cataracte diabétique, souvent bilatérale et à évolution rapide. Son mécanisme repose sur l'activation de la voie des polyols : l'excès de glucose est converti en sorbitol dans le cristallin, provoquant un influx osmotique, un gonflement et une rupture des fibres cristalliniennes [2]. Ce processus conduit à une opacification rapide, parfois en quelques jours ou semaines. La cataracte peut s'accompagner d'une uvéite phacolytique, source de douleur et de risque de glaucome secondaire [3].
Le diabète est également à l'origine de neuropathies périphériques dont un des symptômes oculaires est la kératoconjonctivite sèche (KCS) : le dysfonctionnement glandulaire lié à l'hyperglycémie et la perturbation du flux d'innervation autonome parasympathique associé au nerf crânial VII conduisent à une diminution de la sécrétion lacrymale. Sa mesure régulière peut être un outil de dépistage ou de suivi du diabète [4].
Enfin, bien que rare, une rétinopathie peut également se manifester chez les sujets souffrant de diabète chronique. Depuis l'avènement de la phacoémulsification il convient d'intégrer l'examen du fond d'œil dans le suivi post-opératoire des chirurgies de la cataracte. En effet, la neurorétine peut être altérée par la surexpression de protéines mitochondriales pro-apoptotiques (cytochrome C, AIF) et par des lésions vasculaires endothéliales se traduisant cliniquement par des microhémorragies et un œdème rétinien [5].
III. Complications oculaires chez le chat
Chez le chat, la cataracte est beaucoup plus rare, lente d'évolution et souvent secondaire à d'autres affections oculaires. Les neuropathies diabétiques peuvent se traduire par un ptosis ou des anomalies pupillaires, et la rétinopathie reste exceptionnelle.
IV. Examen oculaire ciblé
Ainsi, l'examen oculaire ciblé chez un animal diabétique doit systématiquement inclure :
- Un test de Schirmer (STT 1) pour dépister une KCS, surtout chez le chien. Bien que soumis aux conditions de réalisation du test, il est admis qu'une valeur <15 mm/min doit alerter et qu'une valeur <10 mm/min est pathologique.
- Une dilatation pupillaire au tropicamide pour examiner en détail le cristallin et dépister précocement une cataracte débutante. Cette étape est à réaliser après mesure de la pression intraoculaire et en l'absence de glaucome ou d'uvéite active.
- Une observation attentive du fond d'œil, pour rechercher les signes d'atteinte rétinienne.
V. Traitement chirurgical
Le traitement chirurgical de la cataracte par phacoémulsification est le traitement de choix. L'uvéite phacolytique pouvant être rapide et délétère, il est conseillé de réaliser l'intervention précocement lors des premiers signes d'altération du cristallin, sous réserve que l'état général et oculaire l'autorise. L'échographie oculaire et l'électrorétinographie préopératoires permettent de vérifier la pertinence de cette prise en charge. Lorsque ces examens sont corrects, cette intervention offre un taux élevé de récupération visuelle et une nette amélioration de la qualité de vie.
VI. Conclusion
Le suivi ophtalmologique des chiens et chats diabétiques est essentiel pour dépister et traiter précocement les complications. Le test de Schirmer et la dilatation pupillaire sont des gestes simples mais cruciaux. Un dépistage et une chirurgie précoces de la cataracte optimisent les résultats visuels et le confort de vie des animaux diabétiques.
Bibliographie
- BASHER AW, ROBERTS SM. Ocular manifestations of diabetes mellitus: diabetic cataracts in dogs. Vet Clin North Am Small Anim Pract. 1995 May;25(3):661-76.
- DAVIDSON MG, NELMS SR. Diseases of the lens and cataract formation. In: Slatter's Fundamentals of Veterinary Ophthalmology, 6th ed., Elsevier, 2018: 355-377.
- MILLER PE, PICKETT JP, MAJORS LJ, KURZMAN ID. Evaluation of risk factors for cataract in diabetic dogs. Vet Ophthalmol. 1998;1(2-3):89-96.
- WILLIAMS DL, BURG P. Comparative aspects of diabetic ocular disease in dogs and humans. Vet J. 2006;172(3):472-486.
- WILLIAMS DL, BEAM SL. Ocular manifestations of systemic disease. In: MAGGS DJ, MILLER PE, OFRI R. Slatter's Fundamentals of Veterinary Ophthalmology, 6th ed., Elsevier, 2018: 435-456.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Diabète sucré : le point de vue de l'urgentiste
Fort Collins, États-Unis d'Amérique
I. Introduction
Cette session se concentre sur la surveillance et la prise en charge du chien et du chat diabétiques, notamment ceux atteints d'une acidocétose diabétique (ACD) ou d'un syndrome hyperglycémique hyperosmolaire (SHHO), également appelé syndrome hyperosmolaire non-kétotique (HONK). La prise en charge de ces patients repose sur quatre piliers :
- La fluidothérapie
- L'insulinothérapie
- La gestion et la correction des anomalies électrolytiques et acido-basiques
- La correction de la cause précipitante (non abordée dans ce document).
II. Fluidothérapie chez le patient diabétique malade
La fluidothérapie chez les patients atteints d'ACD/SHHO peut être complexe en raison d'une déshydratation sévère, d'une diurèse osmotique et d'une hyponatrémie quelquefois sévère. Cependant, les questions de base pour la fluidothérapie restent applicables : quel fluide ? Quelle quantité ? Quelle vitesse ?
Les chiens et chats présentent généralement de fortes pertes de fluide interstitiel, nécessitant une solution isotonique. Les modifications de la natrémie liées à l'hyperglycémie compliquent parfois le choix du soluté. Les diabétiques présentent souvent une hyponatrémie normo-osmolaire, appelée « pseudo-hyponatrémie ». Contrairement à une croyance répandue, l'hyponatrémie n'est pas due à une perte de sodium mais au passage d'eau du compartiment intracellulaire vers le compartiment extracellulaire, ce qui aboutit à une dilution du sodium. Il est aussi important de noter qu'une diurèse osmotique est une perte d'eau, ce qui induit une hypernatrémie. Un facteur de correction permet d'obtenir la natrémie « corrigée ». Il est traditionnellement de 1,6–1,7 mEq/l par 5,5 mmol/l (100 mg/dl) de glucose au-dessus de la normale [1].
La natrémie corrigée doit être utilisée pour guider le choix du soluté. Ainsi, le sérum physiologique (NaCl 0,9%) n'est pas toujours indiqué. Il est plus opportun de privilégier un soluté isotonique avec des précurseurs de bicarbonates, comme le Ringer-lactate ou le Plasmalyte. En cas de choc hypovolémique et de besoin de remplissage vasculaire rapide, une solution équilibrée dont la teneur en sodium est proche (±10 mEq/l) de la natrémie corrigée du patient est préférable.
Il est commun que les chiens et les chats atteints d'ACD/SHHO soient très déshydratés. Il convient alors de les réhydrater relativement rapidement. Le volume est calculé sur la base du pourcentage de déshydratation multiplié par le poids de l'animal. La vitesse de réhydration est souvent calculée sur moins de 12 heures. À cela, il faut ajouter la fluidothérapie de maintenance, ainsi que les pertes, qui sont aussi souvent majeures à cause de la diurèse osmotique et des pertes liquidiennes par les vomissements ou la diarrhée.
Il est donc courant de perfuser ces animaux avec des débits assez élevés.
III. Insulinothérapie chez le patient diabétique malade
L'insuline est essentielle pour faire entrer le glucose dans les cellules, alimenter le cycle de Krebs et limiter la cétogenèse. L'administration continue intraveineuse d'insuline régulière (regular insulin en anglais) est recommandée pour ramener harmonieusement la glycémie à la normale. Pour les ACD légères et non compliquées, les voies SC ou IM peuvent être envisagées.
Chez l'homme, l'American Diabetes Association (ADA) a récemment ajusté ses recommandations, à travers une publication de 2024 [2], dans laquelle est recommandée une perfusion continue IV à 0,1 UI/kg/h, éventuellement précédée d'un bolus de 0,1 UI/kg, notamment s'il y a un délai avant de débuter la perfusion continue. Lorsque la glycémie atteint 13,9 mmol/l (250 mg/dl), réduire à perfusion continue à 0,05 UI/kg/h. Il est à noter que ces recommandations n'incluent pas d'attendre le remplissage vasculaire. Pour le SHHO, le protocole est similaire, mais la perfusion continue est commencée à 0,05 UI/kg/h. Encore une fois, il n'y a pas besoin d'attendre plusieurs heures pour commencer la perfusion d'insuline dans les cas de SHHO, ce qui contredit certains protocoles vétérinaires (Figure 1).

Figure 1 : protocole de gestion des crises hyperglycémiques chez l'homme (adaptée de [2])
Le protocole vétérinaire classique, dit de MACINTIRE, prévoyait l'arrêt de l'insuline sous 100 mg/dl, mais les recommandations humaines préconisent de maintenir l'la perfusion et d'augmenter le dextrose [3].
Bien que certains aient recommandé de ne pas commencer l'insulinothérapie avant que les patients ne soient réhydratés, par crainte d'une biodisponibilité imprévisible de l'insuline administrée par voie sous-cutanée (s.c.) ou intramusculaire (i.m.), l'utilisation de la voie intraveineuse rend cette recommandation inutile. En effet, une étude expérimentale sur des petits animaux a montré qu'une administration précoce d'insuline était associée à une résolution plus rapide de l'ACD, sans augmentation concomitante du taux de complications [1].
Ces dernières années, deux publications ont rapporté l'utilisation de différentes insulines humaines à action rapide, comme par exemple la Lispro ou l'insuline aspartate, chez des chiens atteints d'ACD. Ni l'insuline lispro ni l'insuline asparte n'ont été testées chez le chat.
La surveillance de la glycémie est essentielle lors de l'administration d'insuline. La surveillance traditionnelle nécessite des mesures de glycémie toutes les 2 heures et peut durer plus de 48 heures, nécessitant chez de nombreux patients la mise en place d'un cathéter veineux central. Un appareil portatif validé pour les petits animaux, avec un code spécifique à l'espèce permettant d'ajuster l'algorithme (par ex. GlucoPet, AlphaTrack 2), doit être utilisé. Ces dernières années, les systèmes de surveillance continue du glucose (CGMS), tels que le FreeStyle Libre, ont été étudiés. Ils représentent une alternative intéressante à la surveillance traditionnelle et ont été utilisés et validés en milieu hospitalier chez les chiens atteints d'ACD. Le CGMS mesure le glucose du liquide interstitiel et a été largement étudié chez le chien et l'humain. L'utilité clinique globale du CGMS a été jugée acceptable chez les patients atteints d'ACD dans une étude récente utilisant le FreeStyle Libre [5].
IV. Correction des anomalies des électrolytes et troubles acido-basiques
1. Hyponatrémie
L'hyponatrémie est fréquente chez les patients atteints d'ACD/SHH. Comme nous l'avons vu précédemment, une correction doit être appliquée et l'ancien dogme qui privilégiait le NaCl 0,9% comme soluté de choix doit être oublié pour privilégier une solution électrolytique équilibrée, adaptée au taux de sodium. Le sodium doit être surveillé toutes les 4 à 12 heures selon le taux initial et l'agressivité du traitement. Le sodium doit se normaliser après la réhydratation par des fluides isotoniques et le traitement de l'hyperglycémie par l'insuline.
2. Potassium
Malgré un déficit global en potassium, une hyperkaliémie légère à modérée est fréquente chez les patients en crise hyperglycémique. L'insulinothérapie, la correction de l'acidose et l'expansion volémique diminuent la concentration sérique en potassium. Afin de prévenir l'hypokaliémie, la supplémentation potassique est initiée lorsque les valeurs sériques passent sous la limite supérieure de la normale, avec pour objectif de maintenir la kaliémie dans la fourchette normale de 4–5 mEq/l. En général, une supplémentation de 20–30 mEq/l est suffisante pour maintenir la kaliémie dans la normale, mais certains patients peuvent nécessiter davantage. La plupart des cliniciens utilisent l'échelle de SCOTT pour ajuster la supplémentation potassique. Une alternative à la supplémentation par les fluides est l'utilisation d'une perfusion continue (CRI) de potassium, débutée à 0,1 mEq/kg/h et titrée jusqu'à 0,5 mEq/kg/h selon les besoins. Cela peut être plus simple chez les patients nécessitant des réhydratations agressives ou avec des débits de fluides fréquemment modifiés. Le potassium doit être surveillé toutes les 6 à 12 heures chez les patients atteints d'ACD/SHH.
3. Acidose métabolique
L'utilisation du bicarbonate dans l'ACD est controversée, car les corps cétoniques diminuent avec le traitement par fluidothérapie et l'insulinotherapie, et donc l'acidose métabolique se corrige spontanément. Chez l'homme, les études montrent que la thérapie par bicarbonate dans l'ACD n'apporte aucun avantage en termes d'amélioration de la fonction cardiaque ou neurologique, ni sur la vitesse de correction de l'hyperglycémie et de l'acidocétose. De plus, plusieurs effets délétères ont été rapportés : risque accru d'hypokaliémie, diminution de l'oxygénation tissulaire, œdème cérébral et développement d'une acidose paradoxale du système nerveux central. Toutefois, le traitement par bicarbonate est recommandé lorsque le pH est inférieur à 6,9. Dans ce cas, l'évaluation de l'équilibre acido-basique doit être répétée toutes les 4 à 8 heures. La dose habituelle de bicarbonate est de 1–2 mEq/kg administrée sur 30 minutes à 6 heures, bien qu'une formule de calcul du déficit en bicarbonate puisse également être utilisée.
4. Phosphore
Malgré un déficit global en phosphate dans l'ACD, la phosphatémie est souvent normale ou augmentée à la présentation. Cependant, la concentration en phosphate diminue avec l'insulinothérapie en raison de l'utilisation intracellulaire de phosphore pour la production d'ATP dans le cycle de Krebs. Des études prospectives randomisées n'ont pas montré de bénéfice clinique à la supplémentation en phosphate dans l'ACD chez l'homme. Toutefois, afin d'éviter une faiblesse musculaire cardiaque ou squelettique due à une hypophosphatémie, une supplémentation prudente peut être indiquée chez certains patients avec hypophosphatémie documentée ou présentant des signes cliniques. Si nécessaire, 20–30 mEq/l de phosphate de potassium peuvent être ajoutés aux fluides de remplacement. Beaucoup de cliniciens associent la supplémentation potassique avec ½ KCl et ½ KPhos. Le débit maximal de correction du phosphate généralement considéré comme sûr pour traiter une hypophosphatémie sévère est de 4,5 mmol/h (1,5 ml/h de KPO₄). La phosphatémie doit être surveillée toutes les 12 à 24 heures.
V. Correction de la cause précipitante
Nous n'aborderons pas ici la correction de la cause précipitante, mais il est primordial de l'identifier et de la corriger. Une infection urinaire ou une pancréatite aiguë, notamment, doivent être traitées.
Bibliographie
- HILLIER, T. A., et coll. J. Hyponatremia: evaluating the correction factor for hyperglycemia. Am. J. Med. 106, 399–403 (1999).
- UMPIERREZ GE, et coll. Hyperglycaemic crises in adults with diabetes: a consensus report. Diabetologia. 2024 Aug;67(8):1455-1479.
- MACINTIRE, D. K. Treatment of diabetic ketoacidosis in dogs by continuous low-dose intravenous infusion of insulin. J. Am. Vet. Med. Assoc. 202, 1266–1272 (1993).
- DIFAZIO J, FLETCHER DJ. Retrospective comparison of early- versus late-insulin therapy regarding effect on time to resolution of diabetic ketosis and ketoacidosis in dogs and cats: 60 cases (2003-2013). J Vet Emerg Crit Care (San Antonio).
- MALERBA E, et coll. Accuracy of a flash glucose monitoring system in dogs with diabetic ketoacidosis. J Vet Intern Med. 2020 Jan;34(1):83-91. doi: 10.1111/jvim.15657. Epub 2019 Nov 14. PMID: 31725202; PMCID: PMC6979271.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Diagnostic de la teigne : focus culture fongique
Toulouse, France
I. Introduction
Les dermatophytoses sont souvent suspectées mais leur diagnostic définitif est souvent complexe. Dany SCOTT et D.N. CARLOTTI disaient « Si cela ressemble à de la teigne ce n'en est probablement pas, mais si cela n'y ressemble pas cela pourrait bien en être… ».
Ce diagnostic peut donc nécessiter la mise en œuvre d'examens complémentaires de sensibilité et de spécificité variable.
Ces examens vont être abordés rapidement et l'accent sera volontairement porté sur la culture fongique qui constitue l'examen complémentaire de choix à l'heure actuelle pour le diagnostic à la fois qualitatif et quantitatif.
II. Les examens complémentaires au chevet du patient
1. Examen en lumière de Wood
Cet examen est basé sur la fluorescence de la ptéridine qui est un élément synthétisé en vie parasitaire. Elle est pratiquée dans une pièce sombre avec une lampe UV de longueur d'onde comprise entre 320-400 nm. La fluorescence est vert pomme et suit la tige pilaire de façon à former des tubes.
En médecine vétérinaire, seul Microsporum canis est fluorescent dans 30-80% des cas suivant les études. Cette technique est présente une bonne valeur prédictive positive (90%) et permet de détecter les porteurs asymptomatiques si l'examen est minutieux et attentif. En revanche si l'examen est négatif, d'autres techniques doivent être mises en œuvre. Il existe de nombreux faux positifs (application de dérivés iodés, squames, fibres textiles, manchons pilaires) et faux négatifs inhérents (application d'alcool ou d'éther) à cette méthode qui sont conditionnés par l'expérience du clinicien.
2. Examen direct des tiges pilaires (examen trichoscopique)
Cet examen est souvent intéressant mais présente de nombreuses limites.
Il s'agit de l'observation au microscope des poils infectés. La technique de prélèvement permet d'augmenter la sensibilité de l'examen. Il faut préférer le raclage à l'épilation. Le raclage permet de récolter les tiges pilaires fragilisées par l'infection qui ne seront pas récupérées avec l'épilation.
Il faut chercher, à faible grossissement et avec une luminosité faible et du contraste, des tiges pilaires irrégulières, foncées. Les structures du poil, cuticule, cortex et medulla ne peuvent pas être distinguées. Le passage à plus fort grossissement (X10, X40), en conservant toujours une faible luminosité et du contraste, permet de visualiser les spores en périphérie et les hyphes au centre du poil.
3. Dermatoscopie
Cet examen est de plus en plus pratiqué en raison de sa facilité et sa rapidité. De rares publications détaillent son intérêt. En médecine humaine, il est très utilisé surtout dans les formes du cuir chevelu (tinea capitis) où les poils infectés prennent un aspect en virgule. Chez le chat à pelage clair, les poils teigneux sont plus faciles à identifier, ils sont plus épais, opaques, légèrement recourbés et cassés.
III. Les examens différés
1. Culture fongique
Cette technique demeure l'examen complémentaire de choix. Elle s'utilise pour confirmer une infection, pour l'exclure, pour détecter les porteurs asymptomatiques et pour réaliser le suivi des patients. Elle permet une identification des espèces (qualitatif) et une évaluation de la charge infectieuse (semi-quantitatif, nombre de colonies).
La récolte de l'échantillon conditionne la qualité du résultat. Deux techniques sont possibles : le carré de moquette (technique de Mariat) et la brosse à dents (technique de MacKenzie). Dans tous les cas, il est impératif de récupérer un maximum d'éléments (poils, squames, croûtes). Pour les formes asymptomatiques, le carré de moquette doit être appliqué sur l'ensemble du pelage pendant 1 minute. Chez le chat, il faut insister sur les zones refuges (face, oreille, extrémités digitées).
Il peut être nécessaire d'appliquer préalablement de l'alcool à 70° sur la lésion afin d'éliminer les contaminants. Les dermatophytes ne seront pas altérés par l'application du produit.
Pour les formes profondes type kérion ou mycétome, une biopsie cutanée est nécessaire pour prélever les éléments fongiques dans leur localisation.
Le prélèvement est mis en culture à 25-30°C dans une gélose de Sabouraud. La lecture se fait entre 10 et 15 jours et les prélèvements sont conservés jusqu'à 3 semaines. L'identification se fait par l'examen des macroconidies, microconidies et éléments d'ornement.
a) Avantages
- Diagnostic d'espèce, important pour l'enquête épidémiologique qui en découle. Pour identifier l'origine potentielle du dermatophyte et son caractère zoonotique.
- L'évaluation quantitative avec le nombre de colonies. Cela est notamment important pour le suivi des patients et les cultures fongiques de contrôle.
- Cela permet d'effectuer le tri des entrants dans les effectifs comme les refuges et les SPA.
- Cela permet d'exclure la maladie
- Cela permet de détecter les porteurs asymptomatiques.
b) Inconvénients
- La culture ne permet pas de distinguer les malades, des porteurs sains (infection réelle mais sans symptômes visibles), des véhicules (simple transport mécanique des spores sans infection établie).
- La sensibilité est de 80%.
- La qualité du prélèvement est directement en lien avec le résultat, technique choisie, récolte des contaminants.
- Un traitement antifongique en cours peut entrainer des faux négatifs.
Les tests DTM sont des géloses de Sabouraud avec du rouge phénol. La couleur jaune initiale vire au rouge lorsqu'il y a une alcalinisation du milieu. Cette alcalinisation se produit en quelques jours avec les dermatophytes. La sensibilité/spécificité n'est pas suffisante pour le diagnostic. Il faut compléter par un examen des colonies au microscope qui reste délicat et qui doit être réservé à des mycologistes avertis.
2. Place de la biologie moléculaire PCR
C'est un examen complémentaire d'apparition récente qui propose la détection récente de l'ADN des dermatophytes. Cet examen permet de mettre en évidence Microsporum sp et Trichophyton sp.
Cette technique, comme la culture fongique ne permet pas de différencier les infectés des porteurs asymptomatiques ou des véhicules. La PCR apporte une réponse rapide (48-72h) mais ne permet pas une identification précise des espèces ni une quantification de la charge infectieuse. Elle ne préjuge pas de l'infectiosité et de la viabilité des spores.
- Une PCR négative sur un suivi de patient est en faveur d'une guérison.
- La PCR peut permettre de rapidement décider du statut lors de l'intégration d'un individu dans une collectivité.
- Une PCR positive nécessite d'être couplée à une culture fongique pour préciser l'espèce et le niveau d'infection.
- La PCR est donc particulièrement intéressante quand elle est négative.
Bibliographie
- SCARAMPELLA F, ZANNA G, PEANO A. Dermoscopic features in canine dermatophytosis: some preliminary observations. Veterinary dermatology. 2017;28(2):255-6.
- DONG C, ANGUS J, SCARAMPELLA F, NERADILEK M. Evaluation of dermoscopy in the diagnosis of naturally occurring dermatophytosis in cats. Veterinary dermatology. 2016;27(4):275-e65.
- MORIELLO KA, LEUTENEGGER CM. Use of a commercial qPCR assay in 52 high risk shelter cats for disease identification of dermatophytosis and mycological cure. Veterinary dermatology. 2018;29(1):66-e26.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Doit-on faire appel à l'imagerie pour évaluer une luxation de rotule ? Quelles modalités pour quel apport ?
Marcy L'étoile, France
I. Introduction
Les luxations de rotule sont une affection fréquente chez nos carnivores domestiques. Principalement médiales, elles sont associées à des déformations osseuses plus ou moins importantes. L'évaluation des anomalies à l'origine de la luxation de rotule est indispensable pour prendre en charge correctement ces dernières et limiter le risque de récidive. Cependant, l'évaluation clinique de ces anomalies est difficile et nécessite de choisir correctement ces examens complémentaires.
II. Rappels
Chez le chien, les luxations de rotule sont dans la majorité des cas médiaux et sont d'origine congénitale. Ainsi elles sont le plus souvent secondaires à des anomalies de conformation osseuse qu'il est important de comprendre et de rechercher. On retrouve classiquement :
- une agénésie plus ou moins importante de la trochlée ;
- des déformations fémorales (varus/valgus-torsion) ;
- des déformations tibiales (torsion, varus/valgus) ;
- un déplacement proximal ou distal de la rotule (patella alta ou patella baja).
Il est important de ne pas confondre une rotation, qui est un mouvement autour d'un axe sans déformation osseuse associée, et une torsion qui est, au contraire, une déformation osseuse permanente et désigne la vrille de l'os selon son axe longitudinal. Il est à noter que le sens de torsion est donné par rapport au déplacement de l'épiphyse distale de l'os.
III. Évaluation orthopédique
L'examen orthopédique lors de luxation de rotule doit permettre de déterminer, bien sûr, le grade de luxation et la concomitance d'une rupture du ligament croisé crânial mais également d'évaluer subjectivement la profondeur de la trochlée et la présence d'une éventuelle torsion tibiale.
L'évaluation orthopédique est prolongée par des examens complémentaires : radiographies et/ou scanner.
Les luxations de haut grade (III et IV) sont associées à des déformations osseuses relativement importantess qui nécessitent le plus souvent une correction.
IV. Examen radiographique
L'évaluation radiographique précise de l'alignement osseux est difficile et nécessite une anesthésie générale et un positionnement parfait de l'animal pour éviter les artefacts de positionnement. La présence d'une luxation de rotule rend ce positionnement particulièrement délicat, ce qui explique certaines limites de l'examen radiographique.
A minima, une vue de face et de profil du fémur et du tibia est nécessaire. Au besoin, une vue axiale du fémur peut permettre d'évaluer la version fémorale.
1. Examen radiographique du fémur
Il est impératif que le fémur soit parallèle et que le faisceau radiographique soit perpendiculaire à la cassette radiographique ou au détecteur. Lors de perte d'extension de la hanche, le faisceau de rayons X et la cassette ou le détecteur peuvent être inclinés de manière à ce que le faisceau de rayons X soit perpendiculaire à l'axe du fémur, et que la cassette ou le détecteur soit perpendiculaire au faisceau. Il est également possible d'élever le patient, d'obtenir un faisceau horizontal ou une vue caudo-craniale en flexion. Sur une vue bien positionnée, les sésamoïdes semblent coupés en deux par les corticales fémorales, les berges de la trochlée sont deux lignes parallèles bien visibles distinctes et le petit trochanter n'est que partiellement visible ; souvent le foramen nourricier proximal peut être identifié au centre du fémur proximal. L'angle de varus (ou de valgus) fémoral est déterminé par l'intersection de l'axe mécanique fémoral proximal et l'axe mécanique fémoral distal. La vue de profil permet d'évaluer subjectivement la torsion et un éventuel varus ou valgus distal. Elle doit être également parfaitement positionnée. La vue axiale du fémur est obtenue en plaçant le patient en décubitus dorsal et en fléchissant l'articulation de la hanche de manière à ce que le faisceau de rayons X soit dirigé vers le centre de la diaphyse fémorale, avec la cassette sous l'articulation de la hanche. L'angle d'antéversion est déterminé par l'intersection de l'axe transcondylaire et d'un axe passant par le centre de la tête et du col du fémur.
2. Examen radiographique du tibia
Deux clichés radiographiques orthogonaux sont nécessaires pour évaluer correctement le tibia dans les plans frontal et transversal. La projection caudo-craniale est réalisée sur le ventre. Le tibia est bien positionné lorsque la corticale médiale du calcanéum coupe en deux la trochlée de l'astragale tibiale. La position de la tubérosité tibiale et l'aspect du tibia proximal peuvent permettre d'évaluer subjectivement la torsion tibiale. Le valgus et/ou varus du tibia proximal sont évalués sur cette vue également.
La vue de profil permet de mesurer la pente tibiale lors de rupture du ligament croisé crânial associé à la luxation de rotule.
3. Évaluation d'une éventuelle patella baja ou alta
Une radiographie du grasset est un bon examen pour évaluer la position de la rotule par rapport à la trochlée ; cela se fait sur une vue de profil à 90° et sur la vue de face. Si une évaluation subjective de la position de la rotule est possible, la mesure d'indice peut être conseillée.
4. Limites de l'examen radiographique
Les mesures radiographiques de l'alignement osseux du membre pelvien sont extrêmement sensibles aux artefacts de position. Ainsi les mesures radiographiques sont largement moins précises que celles réalisées sur un scanner. Cependant, il est intéressant de noter que la radiographie a une valeur prédictive négative pour une ostéotomie fémorale relativement forte (96%). Ainsi, si sur une radiographie bien positionnée, aucune déformation fémorale n'est notée, une ostéotomie fémorale est rarement indiquée. Au contraire, se fonder sur la simple radiographie pour indiquer une ostéotomie fémorale entraîne une surindication dans plus de 30% des cas.
Ainsi, si la radiographie reste un bon examen pour contre-indiquer une ostéotomie fémorale, le recours au scanner est nécessaire pour valider l'indication et planifier l'intervention.
V. Examen tomodensitométrique
Le scanner permet une reconstruction en 3D du fémur et du tibia, permettant ainsi de s'affranchir des artefacts de positionnement. Il permet de mesurer de manière plus précise les déformations fémorales ou tibiales. Les mesures réalisées sont identiques à celles décrites pour la radiographie mais permettent de positionner parfaitement le segment osseux. Le scanner permet également une meilleure évaluation de la trochlée fémorale.
Ainsi, le scanner est indiqué lors de luxation de rotule de grade élevé III et IV mais également lors d'anomalie angulaire notable sur la radiographie. En plus de permettre une mesure correcte des déformations, le scanner permet de mieux planifier sa chirurgie par l'utilisation de l'impression 3D.
VI. Conclusion
Ainsi l'évaluation d'une luxation de rotule associe une évaluation clinique rigoureuse et un choix raisonné des examens complémentaires. Si la radiographie reste l'examen de choix en première intention, ses limites font que le recours au scanner est de plus en plus intéressant pour la planification d'une correction de luxation de rotule.
Liens d'intérêt : Consultant ArthrexConsultant PorteVetConsultant NovetechConsultant ZoetisConsultant Elanco
📃 Dysplasie de la hanche : support génétique, influence de l'alimentation et de l'exercice dans l'expression clinique
Paris, France
I. Introduction
La dysplasie de la hanche (DH) est une affection développementale multifactorielle et polygénique caractérisée par une laxité articulaire, des anomalies de conformation de l’articulation coxo-fémorale et le développement progressif d’une ostéoarthrose (OA). Elle ne touche pas que les chiens de grand format et certaines races de petite taille sont de plus en plus souvent affectée de DH (Cocker spaniel anglais par exemple). Bien que sa copmposante génétique soit clairement établie, de nombreux facteurs environnementaux, notamment l’alimentation et l’exercice physique, influencent son expression clinique.
Cette synthèse propose une mise à jour des connaissances actuelles sur ces trois leviers d’action.
II. Support génétique : une complexité entravant la sélection
De nombreuses études ont mis en évidence l’héritabilité de la DH, avec un coefficient oscillant entre 0,2 et 0,6 selon les races, les critères diagnostiques et les méthodologies utilisées. La DH est une maladie polygénique complexe : plusieurs loci ont été identifiés sur les chromosomes CFA01, CFA08, CFA10 et CFA37, impliquant des gènes codant pour des protéines matricielles, des facteurs de croissance ou de l’ossification endochondrale (ex. FBN2, PTPRD, NOG). Des études sur près de 2 000 Retrievers golden et du Labrador, entre 1980 et 1996, montrent une réduction de la prévalence cliniquement évaluée de 30 à 10 % chez les Retrievers du Labradorset cette reduction est également observée chez les Bergers allemands en moins de cinq générations, confirmant l’héritabilité élevée (20-60 %) et le potentiel de cette sélection pour la reproduction. Cependant, d’autres analyses en France (10 à 17 races, 1993–2019) soulignent l’effet limité des programmes de sélection : seule la Berger picard montre une baisse significative ; la majorité des races présentent des changements non significatifs. Ces résultats attestent que, malgré des progrès, la sélection génétique seule peine à réduire la prévalence de manière notable.
La grande variabilité phénotypique de la DH, les interactions génotype-environnement, l’hétérogénéité des critères diagnostiques (score FCI, OFA, PennHIP), l’évaluation plus ou moins rigoureuse (un an est sans doute trop tôt pour pouvoir vraiment grader l’arthrose) et le sérieux de certains éleveurs sont sans doute des éléments impactant cette sélection génétique. De nouveaux outils tels que les indices génomiques ou les modèles de sélection multivariée sont à l’étude, mais leur valeur prédictive reste encore limitée à ce jour.
III. Rôle de l’alimentation : une influence majeure à tous les stades de vie
1. Pendant la croissance
Une croissance trop rapide, un excès calorique ou minéral (calcium, phosphore) sont des facteurs favorisant l’apparition ou la sévérité de la DH. Les chiots nourris ad libitum, sans contrôle de la courbe de croissance, présentent un risque accru de développer des signes radiographiques et cliniques de la maladie. Dans une étude, à l'âge de 2 ans, 66 % des chiens nourris ad libitum présentaient des signes radiographiques de DH contre 22 % dans le groupe alimentation restreinte (KEALY JAVMA 1992). Il est recommandé de viser une croissance linéaire, en suivant des courbes de croissance adaptées à la race, et d’éviter les régimes hypercaloriques ou riches en minéraux.
D’autres études ont montré que le gain de poids rapide au cours des 2 premiers mois aprè le sevrage est également un facteur de risque significatif. La fenêtre critique semble se situer entre 3 et 8 mois, période durant laquelle la modulation de l’expression phénotypique par la nutrition est la plus marquée. Les régimes formulés pour grandes races, avec une densité énergétique modérée et un rapport Ca/P adapté, sont à privilégier.
2. Chez le chien adulte
Chez les chiens atteints, la gestion du poids corporel est essentielle pour limiter la douleur, améliorer la mobilité et ralentir l’évolution arthrosique. Une perte de poids de 6 à 9 % suffit à réduire significativement la boiterie. (voir présentation sur le sujet)
L’apport d’acides gras oméga-3, notamment issus de l’huile de poisson (EPA/DHA), diminue l’inflammation synoviale et améliore les scores fonctionnels. Selon la méta-analyse 2022, les acides gras oméga-3 (notamment EPA/DHA issus de l’huile de poisson) bénéficient du meilleur niveau de preuve clinique pour la prise en charge de la douleur et de la mobilité chez les chiens arthrosiques, incluant ceux atteints de dysplasie de la hanche. Les études contrôlées randomisées montrent une réduction significative des signes cliniques et des marqueurs inflammatoires.
Si on regarde les composants de nutraceutiques, les résultats sont souvent contradictoires ou issus d’études à faible puissance méthodologique. L’approche nutraceutique, si elle reste prometteuse, doit ainsi être considérée comme complémentaire à une prise en charge globale incluant gestion pondérale, activité physique et, si nécessaire, traitement pharmacologique.
IV. Activité physique : un modulateur adaptatif
1. Chez le chiot
L’activité physique précoce joue un rôle clé dans la modélisation articulaire et le développement neuromusculaire. Les exercices libres sur sol irrégulier (herbe, gravier) sont bénéfiques et contribuent à une meilleure stabilité articulaire. Une étude a montré que l’activité libre sur sol irrégulier durant les 3 premiers mois était associée à une réduction de 34 % du risque de DH clinique.
À l’inverse, certaines pratiques sont délétères :
- utilisation fréquente des escaliers avant 3 mois ;
- jeux violents (lancer de balle, sauts répétés) ;
- courses prolongées sur surfaces dures (béton, carrelage) ;
- sports canins structurés (agility, flyball) avant la fin de la croissance.
Une étude a montré que l’utilisation fréquente des escaliers avant l’âge de 3 mois augmentait de 1,6 à 2 fois le risque de développer une DH radiographique. Les activités doivent être courtes, variées, non traumatiques et toujours supervisées. Le jeu social modéré, la marche en laisse sur sol souple et l’exploration libre en extérieur constituent des formes d’exercice adaptées.
Un exemple de programme adapté serait :
- 0–3 mois : promenades en laisse de 5–10 minutes très régulièrement sur sols souples ou herbe ;
- 3–6 mois : allongement progressif des balades à des durées de 15 minutes/jour. Introduction de terrains légèrement accidentés (pelouse, gravier), favorisant la proprioception ;
- 6–9 mois : allongement progressif des balades à 20-30 minutes/jour, incluant courtes phases de jeu libre (1–2 minutes) sous surveillance, plutôt en fin de balade. Objectif : maximaliser la stabilité sans stress articulaire ;
- 9–12 mois : augmentation des durées de balades de 5 minutes par semaine. Commencer à travailler sur des montes douces (5–10 ° inclinaison) et jeux modérés, évitant sauts, escaliers, lancer de balle ou sports d’impulsion.
2. Chez l’adulte dysplasique
Chez les chiens déjà atteints de DH, le maintien d’une activité régulière est indispensable pour entretenir la masse musculaire, favoriser la mobilité articulaire et limiter la progression de l’arthrose. Les recommandations incluent :
- marche modérée quotidienne (minimum 2 fois 20-30 minutes) ;
- marche dans l’eau, natation ou tapis roulant immergé, excellents pour le travail musculaire sans contrainte articulaire ;
- exercices de proprioception douce, montées contrôlées sur plan inclinée, changements de position.
Une étude a montré une amélioration fonctionnelle moyenne de 25 à 30 % (réduction de la boiterie et amélioration des scores de mobilité) a été observée après 8 semaines de protocole incluant marche, natation, proprioception.
En revanche, il convient d’éviter :
- lancer de balle ou frisbee (mouvements explosifs, freinages brutaux) ;
- jeux de traction ou de poursuite ;
- sols glissants ou instables ;
- exercices prolongés sans pause.
Le programme d’exercice doit être progressif, individualisé, et réévalué régulièrement. La collaboration avec un vétérinaire en rééducation fonctionnelle est précieuse pour établir un protocole adapté.
V. Conclusion
La DH illustre l’interaction complexe entre hérédité polygénique et environnement. Bien que la sélection ait montré des signes de progrès, son impact actuel est limité. En revanche, la nutrition et l’exercice adaptés offrent des leviers tangibles et chiffrés pour moduler et freiner l’expression clinique. Un programme personnalisé et progressif dès le jeune âge, associé à une gestion rigoureuse de la croissance et à un régime contrôlé, offre aujourd’hui la meilleure stratégie pour améliorer le pronostic des chiens prédisposés ou dysplasiques.
Bibliographie
- Sur la génétique de la dysplasie de la hanche : BARTOLOMÉ E., et al. 2021. Understanding canine hip dysplasia genetics: advances and limitations.
- Sur la nutrition et la croissance : BEYNEN A.C. 2019. Diet and canine hip dysplasia: current knowledge and future directions.
- Sur l’activité physique : KRONTVEIT R. et al. 2012. Risk factors for hip-related clinical signs in a prospective cohort study of four large dog breeds in Norway.
- Sur les nutraceutiques : BARBEAU-GRÉGOIRE M. et al. 2022. Systematic Review and Meta-Analysis of Enriched Therapeutic Diets and Nutraceuticals in Canine and Feline Osteoarthritis.
Liens d'intérêt : Consultant Movora, Arthrex, Zoetis
📃 Effectuer et interpréter des radiographies en contrainte du carpe
Tours, France
I. Objectif clinique
Les traumatismes du carpe sont le plus souvent consécutifs à des chutes ou à des réceptions violentes sur les membres antérieurs. Les lésions les plus sévères entraînent des atteintes ostéo-articulaires et ligamentaires, responsables d’une instabilité palmaire par hyperextension, dont le traitement de référence est généralement une arthrodèse de l’articulation ou des articulations concernées.
Les fractures isolées des os du carpe, plus rares surviennent principalement chez les chiens de sport ou de travail. Leur prise en charge, toujours chirurgicale, dépend de l’os atteint et du type de fracture. Lorsqu'une réduction anatomique est possible, le traitement consiste en une ostéosynthèse par vissage. En revanche, les fractures comminutives ou anciennes imposent souvent une arthrodèse.
Les radiographies en contrainte du carpe (stress views) permettent d’évaluer la stabilité articulaire, de mettre en évidence des lésions ligamentaires, luxations ou subluxations invisibles en position neutre, et d’orienter le choix thérapeutique, notamment chirurgical ou conservateur.
II. Anatomie fonctionnelle du carpe
Carpe : 7 os organisés en deux rangées :
- rangée proximale : radial, ulnaire, accessoire ;
- rangée distale : os carpien I à IV.
Articulations principales : antébrachio-carpienne, carpienne moyenne, métacarpo-phalangienne.
Stabilisateurs communs :
- capsule articulaire ;
- ligaments intra- et extra-articulaires ;
- fibrocartilage palmaire ;
- tendons.
Contrairement aux collatéraux continus, le carpe présente des manchons fibreux courts renforcés.
III. Diagnostic multimodal
1. Radiographies
Radiographie neutre : dorsopalmaire et latérale, utile pour l’alignement osseux et la congruence articulaire.
Radiographies en contrainte : flexion/extension forcée, déviation médiale/latérale sous sédation ou anesthésie pour homogénéité de la contrainte.
2. Imagerie complémentaire
CT-Scan (tomodensitométrie) pour fractures complexes ou structures osseuses occultes.
3. Examen clinique
Examen physique orthopédique : boiterie, asymétrie, œdème, instabilité, tests dans les plans frontal, sagittal et transverse
IV. Interprétation radiographique
1. Critères normaux
- Alignement régulier des rangées carpiennes.
- Absence d’élargissement articulaire.
- Symétrie médiale/latérale.
2. Critères pathologiques
- Ouverture en valgus/varus → rupture partielle ou complète des ligaments collatéraux.
- Hyperextension → atteinte des ligaments palmaires et du fibrocartilage.
- Subluxation ou luxation sous contrainte extrême (carpo-métacarpienne).
Comparaison fondamentale avec le côté controlatéral pour déceler les différences.
V. Pathophysiologie
Hyperextension : souvent consécutive à un traumatisme (chute, choc), causant douleur, enflure, perte fonctionnelle ; souvent associée à des fractures intra-articulaires qui exigent une intervention chirurgicale rapide.
VI. Approches thérapeutiques
- Conservateur : entorses de 1er degré bénignes peuvent évoluer favorablement avec un traitement minimal.
- Chirurgical : entorses de 2e et 3e degré, fractures non réparables, instabilité sévère, nécessitent généralement une arthrodèse (totale ou partielle) pour stabiliser l’articulation et soulager la douleur.
VII. Intérêt clinique
- Diagnostiquer précocement les instabilités après traumatisme (accident, chute, morsure).
- Aide à planifier un traitement — arthrodèse partielle (stabiliser une partie du carpe) ou pancarpienne (fusion complète).
- Permet de distinguer entre contusion musculo-ligamentaire (traitement conservateur potentiel) et rupture ligamentaire menaçante pour la fonction.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Effectuer et interpréter des radiographies en contrainte du jarret
Marcy L'étoile, France
I. Introduction
Le tarse est une articulation complexe dont l’examen radiographique reste délicat, tant dans la réalisation que dans l’interprétation. L’examen de base du tarse comporte a minima deux vues orthogonales (face et profil) et des vues obliques afin de de superposer les structures.
Afin d’optimiser l’évaluation des lésions, notamment des instabilités, des vues supplémentaires de l’articulation sont souvent indiquées en plus de l’examen radiographique classique. Ainsi, des vues en hyperfexion, en hyperextension et de contraintes médiolatérales sont réalisées. Ces projections radiographiques permettent d'appliquer une contrainte à l'articulation du tarse afin d'identifier une instabilité d’un des étages articulaires.
II. Examen standard du tarse
Classiquement des vues de faces et profil du tarse sont réalisées. La vue de profil (médio latérale) est réalisée en décubitus latéral. La vue de face est réalisée préférentiellement en décubitus sternal le grasset et le tarse en extension.
Cet examen de base peut être complété par des vues obliques (dorso-lateral-plantaro-medial oblique ou dorso-medial-plantaro-lateral oblique) ; ces dernières permettent de mieux séparer les structures complexes du tarse comme par exemple les lèvres du talus ou les os des étages intertarsiens.
Une vue skyline peut également permettre de mieux visualiser les lèvres de la trochlée. Pour cela, l’animal est en décubitus dorsal, le tarse en flexion à 90° et une radio de face est réalisée.
Ces radiographies permettent de visualiser les structures osseuses et de rechercher une tuméfaction des tissus mous. Cependant, elles ne permettent pas de mettre en évidence une instabilité. Pour cela, des vues en contraintes sont nécessaires.
III. Vue en hyperflexion
L’animal est positionné en décubitus latéral, le grasset maintenu en extension et une flexion du tarse est induite en poussant sur la face palmaire des métatarses.
Cette vue permet de mettre en tension la partie palmaire du tarse. Elle est indispensable pour l’exploration d’une plantigrade afin de localiser l’étage instable. Une instabilité plantaire oriente vers une arthrodèse.
IV. Vue en hyperextension
De la même manière, l’animal est positionné en décubitus latéral, le grasset maintenu en extension et une hyper extension du tarse est induite en poussant sur la face dorsale du tarse.
Les instabilités dorsales sont mises en évidence par cette vue. Bien que plus rares, ces lésions sont généralement de bon pronostic car situées sur la face de compression de l’articulation.
V. Vue en contraintes médiolatérales
L’animal est positionné en décubitus sternal ou dorsal, le tarse doit être bien de face et maintenu en extension. Une contrainte médiale ou latérale est ensuite induite en poussant à l’aide d’un objet radio transparent (spatule de cuisine en bois par exemple).
Ces vues permettent de mettre en contraintes les ligaments collatéraux et de rechercher une instabilité en valgus ou varus.
VI. Interprétations
Ces vues en contraintes sont indispensables pour tester la stabilité du tarse. Si le scanner a remplacé les vues obliques ou skyline pour l’évaluation des structures osseuses complexes du tarse, il ne remplace pas cet examen radiographique spécifique.
L’analyse de l’instabilité doit permettre de choisir ensuite la thérapeutique la plus adaptée.
- En cas d’instabilité plantaire, une arthrodèse, partielle si l’étage talocrural est intact ou totale le cas échéant, sera toujours le traitement de choix.
- Lors d’instabilité dorsale, une contention externe est généralement suffisante. Dans certains cas, une stabilisation dorsale peut être indiquée.
- Lors d’instabilité en valgus ou varus isolée (sans lésions plantaires), une réparation ligamentaire, ou une fusion partielle sera le traitement de choix.
Liens d'intérêt : Consultant ArthrexConsultant PorteVetConsultant NovetechConsultant ZoetisConsultant Elanco
📃 Effet de l'anesthésie sur la réponse vaccinale : étude chez la chatte avec un vaccin à agent inactivé
Pierre BESSIÈRE
Coauteurs : P. BESSIÈRE, R. BREYSSE, M. CHRÉTIEN, S. BOULLIER, M. WASNIEWSKI, G. JOURDAN
Introduction
L'anesthésie est connue pour avoir des effets immunomodulateurs. Il est aujourd'hui bien établi que les molécules anesthésiques couramment utilisées exercent des effets immunomodulateurs, influençant divers mécanismes tels que l'activation des lymphocytes, la production de cytokines ou encore la phagocytose. Ces altérations pourraient théoriquement compromettre l'efficacité d'une vaccination administrée au cours d'une anesthésie, mais les données disponibles restent limitées, en particulier en médecine vétérinaire.
Matériel et résultats
Afin d'évaluer l'impact de l'anesthésie sur la réponse vaccinale, une cohorte de 36 chattes femelles, âgées de 6 à 12 mois, a été étudiée. 25 d'entre elles furent vaccinées avec un vaccin antirabique à agent inactivé pendant leur stérilisation et 11 d'entre elles au moins 5 jours avant ou après leur stérilisation. Du sang était récolté en fin d'anesthésie et un mois plus tard, afin de réaliser deux types d'analyse : de la stimulation de sang total et une sérologie antirabique. La stimulation de sang total consistait à incuber le sang avec l'adjuvant vaccinal (de l'hydroxyde d'aluminium), afin d'évaluer par PCR quantitative l'expression de gènes impliqués dans la réponse inflammatoire, et ainsi d'étudier les effets de l'anesthésie sur l'immunité innée. Les sérologies permettaient d'évaluer la réponse immunitaire adaptative en dosant le taux d'anticorps dirigés contre le virus de la rage.
Les stimulations de sang total ont révélé une forte induction de l'expression du gène TNFa, que la prise de sang ait été faite pendant l'anesthésie ou un mois plus tard. Les sérologies antirabiques sont toujours en cours avec des résultats non encore disponibles à ce jour (ils ne peuvent donc pas être inclus dans ce résumé).
Conclusion
Ces travaux montrent donc qu'en conditions contrôlées (des animaux homogènes en termes de sexe, âge et protocole anesthésique), l'anesthésie n'a pas d'impact sur la capacité des cellules sanguines à réagir suite à la stimulation par l'hydroxyde d'aluminium. Selon les résultats des sérologies, nous pourrons confirmer l'hypothèse que l'anesthésie n'est pas une contre-indication à la vaccination, ce qui peut se révéler très utile, notamment lors des campagnes de stérilisation d'animaux errants. Seules des investigations plus poussées permettront d'évaluer si cela est toujours le cas avec les vaccins à agent vivant atténué, mais le fait que les souches vaccinales se répliquent pendant plusieurs jours chez les individus vaccinés le laisse à penser.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Effets d'un bolus de pimobendane intraveineux sur la fonction cardiaque gauche évaluée par échocardiographie conventionnelle et avancée chez le chien sain
Pierre FOULEX
Coauteurs : M. MAGNIN; E. MOISSET; V. BONDOUX; A. DOUGÈRE; G. NOËL; C. POUZOT-NEVORET; E. TREHIOU; V. CHETBOUL
Introduction
Les effets pharmacologiques et cliniques bénéfiques du pimobendane administré par voie orale sont bien connus chez le chien. [1,2] En revanche, peu de données sont actuellement disponibles concernant la forme injectable de la molécule. L'objectif de cette étude préclinique a ainsi été d'analyser les effets d'un bolus intraveineux (IV) de pimobendane sur la fonction atriale et ventriculaire gauche évaluée par échocardiographie conventionnelle et avancée chez le chien sain.
Matériels et méthodes
Comité éthique
Cette étude a reçu l'autorisation d'un comité d'éthique (numéro d'acceptation :2413V5) ainsi qu'une validation par le Ministère de l'enseignement supérieur et de la recherche (numéro APAFIS : #48007-2024021917014478 v5).
Animaux
La taille de l'échantillon a été déterminée pour que l'étude puisse détecter une augmentation de 30% du débit cardiaque suivant l'administration de pimobendane. La valeur du débit cardiaque pré-traitement utilisée dans le calcul a été fixée à 3 L/min (+/- 0,3). Le calcul de la taille de l'échantillon a été effectué avec un niveau de signification de 0,05 et une puissance statistique de 0,90. Sur la base de ce calcul, un minimum de quatre chiens était requis. En tenant compte d'une potentielle exclusion de l'un des chiens, cinq chiens ont été finalement inclus dans l'étude.
Les critères d'inclusion étaient les suivants : les chiens devaient être des beagles adultes sains, sans anomalie à l'examen clinique et au bilan sanguin (bilan biochimique et numération formule sanguine) réalisés 3 jours avant le début de l'étude. Les animaux étaient exclus si l'une des procédures du protocole ne pouvait être réalisée ou s'ils montraient des signes de maladie au cours du protocole.
Protocole expérimental
Après réalisation d'un examen clinique complet et de la mise en place d'un cathéter IV dans la veine céphalique, les chiens étaient anesthésiés à l'aide d'un protocole composé d'alfaxalone, de butorphanol et de midazolam. Un cathéter artériel était introduit dans l'artère fémorale, puis une injection de meloxicam était réalisée lors du réveil.
Deux heures après l'induction de l'anesthésie, un bolus de pimobendane (0,15 mg/kg IV) était administré. La pression artérielle invasive et l'électrocardiogramme (ECG) étaient monitorés pendant une période de 8 heures. Du sang artériel (3mL) était collecté à T0, T0+10, 20 et 30 minutes, ainsi qu'à T0+1, 2, 4, 6, 8 et 24 heures pour la mesure des concentrations plasmatiques en pimobendane et son métabolite, le o-desméthyl-pimobendane (ODMP).
Examen écho-Doppler
Un examen écho-Doppler conventionnel et avancé, couplé à l'ECG, était réalisé par des opérateurs entrainés (DECVIM-CA, Cardiology et résident ECVIM-CA, Cardiology) avant l'injection de pimobendane (T0), puis 30 minutes et 2, 4, 6, 8 et 24 heures après. L'évolution des paramètres écho-Doppler au cours du temps est présentée sous forme de différence moyenne des 5 chiens entre l'instant T et T0 pour chacun d'entre eux.
Résultats
Une augmentation rapide des taux plasmatiques du pimobendane et de l'ODMP a été constatée, ce dernier ayant persisté plus longtemps dans le sang.
La fonction systolique ventriculaire gauche radiale et globale évaluée par examen écho-Doppler conventionnel était significativement augmentée de 30 minutes à 6 heures après l'injection, comme en témoigne respectivement la différence moyenne entre T2h et T0 pour les paramètres de contractilité radiale (diamètre ventriculaire gauche systolique (VGs)= -6,0 mm ; fraction de raccourcissement du VG= +19% ; distance E-septum (ES)= -2,3 mm) et globale (volume systolique et fraction d'éjection du VG respectivement par voie parasternale droite (VolVGs= -5,8 mL et FE= +23%) et gauche (VolVGs-gauche= -5,4 ml et FE= +21%) ; fraction de raccourcissement des aires du VG= +23%).
Le volume d'éjection systolique indirectement évalué par méthode Doppler était significativement augmenté de 30 minutes à 6 heures après l'injection (augmentation maximale à T2h= +8 ml). La vitesse de l'onde S mitrale mesurée en mode Doppler tissulaire pulsé à l'anneau mitral latéral (témoignant de la fonction systolique longitudinale) était significativement augmentée de 30 minutes à 6h après l'injection.
L'examen de la déformation radiale du myocarde ventriculaire gauche par speckle tracking imaging a révélé un strain systolique global significativement augmenté de 30 minutes à 6 heures après l'injection (augmentation maximale de +33% à T2h). La fonction systolique de l'atrium gauche était également significativement augmentée après l'injection (augmentation moyenne des fractions de raccourcissement et d'éjection de l'atrium gauche à T2h : +15% et +12%, respectivement).
Discussion et Conclusion
Cette étude démontre que l'administration IV d'un bolus de pimobendane augmente significativement la contractilité ventriculaire gauche radiale et longitudinale, ainsi que le volume d'éjection systolique entre 30 minutes et 6 heures après le bolus avec une augmentation maximale à T2h, ainsi que la contractilité de l'atrium gauche.
Bibliographie
- SUMMERFIELD NJ et al., J Vet Intern Med. 2012;26(6):1337-1349.
- BOSWOOD A et al., J Vet Intern Med. 2016;30(6):1765-1779.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Effets secondaires problématiques
Marcy L'Étoile, France
I. Introduction
Un événement indésirable est défini de manière large comme l’association entre un signe clinique et l’utilisation d’un médicament, que le signe soit considéré ou non comme en lien avec le médicament et que celui-ci ait été utilisé ou non selon ses indications. Le terme d’effet indésirable est utilisé lorsqu’il existe un certain degré de relation causale (imputabilité) et est défini comme une réaction nocive et non voulue.
II. Caractérisation des effets indésirables
On peut déjà distinguer les effets cliniques, des effets seulement biologiques, mais également classés les effets selon le système : signes généraux, digestifs, nerveux, etc. Les effets les plus fréquents sont non spécifiques (abattement par exemple) ou digestifs et hépatobiliaires, avec des différences selon l’espèce (cf. Tableau 1).
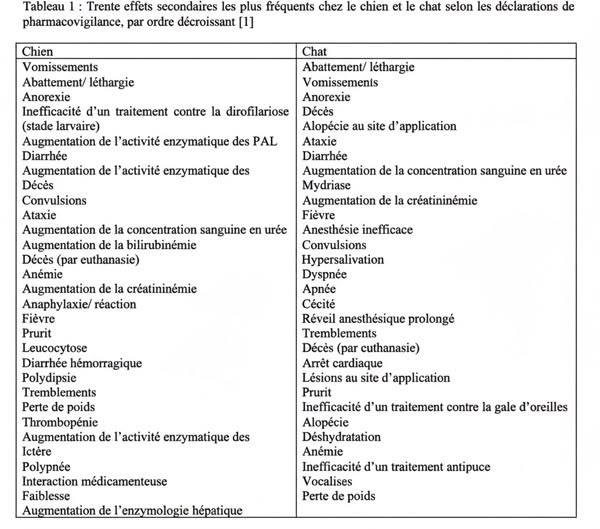
Tableau 1
1. Fréquence et gravité
De manière classique, dans les résumés des caractéristiques du produit (RCP), les effets secondaires sont présentés selon leur fréquence d’apparition et gravité.
Les effets secondaires liés aux propriétés pharmacologiques du médicament sont en général assez fréquents ; détectés dès les essais cliniques, ils seront pris en compte dans le dossier d’AMM et indiqués dans la notice. À l’inverse, les effets plus rares, notamment de type idiosyncrasique, n’ont que très peu de chance d’être observés durant la phase de développement et ne seront connus qu’après mise sur le marché, grâce aux déclarations de pharmacovigilance (info auprès de l'ANMV ou du fabricant) et publication de cas cliniques.
Les effets secondaires sont également caractérisés par leur morbidité / mortalité.
Un effet indésirable est considéré comme grave dès :
- Qu’il est fatal ou met en jeu le pronostic vital, ou
- Qu’il entraîne un avortement, une anomalie congénitale, une infertilité ou un handicap ou des séquelles, ou
- Qu’il nécessite une prise en charge « professionnelle »,
Un effet secondaire non grave reste problématique. En plus de l’altération de la qualité de vie de l’animal, il ne faut pas négliger l’impact sur les propriétaires : impact sur leur vie quotidienne (réveil nocturne lors de polyuropolydipsie, etc.), impact sur leur relation avec leur animal (sédation excessive par exemple) et inquiétude supplémentaire. Ces effets peuvent affecter l’observance du traitement par les propriétaires lorsqu’ils ont l’impression que le médicament fait plus du mal que de bien à leur animal. L’apparition d’effets secondaires peut aussi conduire à une méfiance envers le praticien, perçu comme responsable.
Le degré et la rapidité de réversibilité de l’effet secondaire sont également importants. Par exemple, une insuffisance lacrymale due aux sulfamides n’impacte par le pronostic vital mais sera problématique lorsqu’irréversible, car impliquant un traitement et des conséquences à long terme.
2. Mécanismes
Les effets indésirables peuvent être directement dus au médicament en raison d’une toxicité intrinsèque ou résulter d’une interaction médicament/animal particulière : variations interindividuelles pharmacocinétiques ou pharmacodynamiques (exemple mutation du gène MDR-1, allergie, réaction anaphylactode, par exemple libération d’histamine).
Les mécanismes des effets indésirables sont nombreux, les plus fréquents étant :
- Toxicité directe, de type contact (signes digestifs lors de prise orale, réaction cutanée lors de traitement topique, etc.)
- Toxicité liée au mécanisme d’action (propriétés pharmacologiques : effet thérapeutique trop important par exemple hypothyroïdie iatrogène sous thiamazole, toxicité hématologique de certains agents anticancéreux et immunomodulateurs, effet direct mais non thérapeutique par exemple inhibition de la synthèse des prostaglandines lors de traitement anti-inflammatoire...)
- Altération de la microflore, le plus souvent digestive. L’effet est direct avec les antibiotiques et les antiseptiques, de par leurs propriétés, mais ces effets sont par exemple incriminés lors de signes digestifs suite à la prise d’antiacide. Les effets sur la microflore digestive sont fréquents lors de prise par voie orale mais en théorie possible dès lors que le médicament ou ses métabolites sont excrétés par voie biliaire.
- Lié à sa pharmacodynamie (par exemple compétition avec l'absorption, le transport, le métabolisme ou l'excrétion de substances endogènes ou d'autres médicaments).
- Réactions immunoallergiques, anaphylactoïdes. Les effets secondaires observés sont souvent hématologiques, cutanés, plus rarement neuromusculaires, etc.
On distingue 2 catégories de toxicité avec un impact sur l’anticipation, le monitorage et la gestion des effets secondaires (cf. Tableau 2) :
- Toxicité intrinsèque, dose et temps dépendante, souvent précoce. La plupart des animaux exposés vont présenter cette toxicité à une dose suffisante.
- Toxicité idiosyncrasique, imprévisible et n’apparaissant que chez un faible nombre d’individus. Bien qu’elle soit souvent considérée comme dose-indépendante, une exposition minimale semble nécessaire. Elle apparaît après un temps de latence très variable de quelques jours à plusieurs années, parfois même à distance de l’arrêt du traitement.
Tableau 2
III. Démarche lors d'effet indésirable suspect
Lorsqu’un nouveau signe clinique apparaît ou qu’un signe déjà présent s’intensifie suite à la mise en place d’un traitement, la réponse la plus logique est d’arrêter le traitement. Toutefois, il convient de procéder par étapes, en évaluant le lien de causalité, puis le rapport bénéfice/risque.
1. Attribuer un signe clinique ou biologique à un effet indésirable
En pharmacovigilance, des algorithmes sont généralement utilisés pour évaluer le lien de causalité entre un médicament et un signe clinique, par exemple le système ABON employé par l’ANMV et le CPVL. En clinique, sont pris en compte :
- La fréquence de l’effet secondaire et les autres données de la littérature (pharmacologie, effet proche ou identique décrit dans d’autres espèces ou avec des substances apparentées, etc.)
- La temporalité et la dose, en gardant en tête le risque de réactions différées et idiosyncrasiques.
- Le lien anatomique (les effets secondaires digestifs sont fréquents avec des médicaments administrés par voie orale et ceux cutanés avec les topiques, mais un effet à distance reste possible, notamment par ingestion accidentelle d’un topique, par résorption systémique, par excrétion biliaire, etc.)
- Le contexte global: le signe peut-il être attribué à un autre médicament, à une interaction médicamenteuse (toxicité mais également altération de l’efficacité en défaut comme en excès), à une susceptibilité particulière de l’animal, à la maladie (traitement au contraire insuffisant ou erreur de diagnostic) ?
2. Conduite à tenir lors d'effet indésirable avéré ou suspect
Plusieurs options sont à envisager, depuis la simple poursuite du traitement sans modification, jusqu’à l’arrêt complet et définitif.
De nombreux effets secondaires sont surtout ressentis en début de traitement, puis s’estompent après quelques jours. D’autres doivent conduire à l’arrêt du traitement, soit parce qu’ils sont déjà graves, soit parce que les effets vont s’intensifier et non s’estomper en prolongeant l’administration.
Le choix va dépendre du rapport bénéfice/risque établi :
- De la gravité de l’effet secondaire et de sa réversibilité. Un effet transitoire peut être tout à fait tolérable si les propriétaires ont été prévenus à l’avance et/ou qu’un traitement symptomatique est instauré temporairement...
- De la maladie (gravité intrinsèque, autres options thérapeutiques disponibles).
- Du mode et du mécanisme d’apparition de l’effet secondaire
- Effet dose dépendant permettant une réduction de dose, si l’efficacité peut être maintenue à une dose plus faible. Cette option n’est pas envisageable lors de réaction idiosyncrasique.
- Effets secondaires pouvant être monitorés (par exemple, phénobarbitalémie, suivi de la toxicité hépatique du thiamazole à l’aide du monitorage des ALAT, suivi de toxicité hématopoïétique à l’aide de numération formule sanguine), permettant d’arrêter l’administration avant l’observation de signes cliniques souvent tardifs.
- Interaction médicamenteuse permettant de privilégier l’arrêt ou la réduction de dose de l’autre substance.
- Effets secondaires de type immunoallergiques : ils s’intensifient souvent avec le temps et doivent conduire à l’arrêt du traitement.
- De la possibilité de contrecarrer les effets indésirables à l’aide d’un autre médicament, voire d’un antidote (par exemple, administration d’antiacide lors de traitement AINS, antioxydant lors de toxicité hépatique, etc.). L’efficacité de cette prise en charge est souvent limitée et elle ne peut être considérée que lorsque que l’effet indésirable est peu marqué et/ou ses conséquences moins importantes qu’un arrêt de traitement.
Si l’arrêt du traitement est indiqué, le clinicien doit réfléchir à une alternative. Si l’alternative est une substance non apparentée, le risque d’un nouvel effet indésirable n’est pas spécialement plus important. Si l’utilisation de la même substance (autre médicament avec d’autres excipients ou une autre voie d’administration), d’une pro-drogue, ou d’une substance apparentée/même famille, est nécessaire, le risque d’effet secondaire est plus important et ceci n’est possible que lors d’effet non grave et...
- probablement lié à la voie d’administration et/ou l’excipient (exemple utilisation d’une voie transdermique lors d’intolérance digestive à un antithyrodien)
- probablement non lié à un mécanisme immunoallergique (les risques de réaction croisée étant important dans le cas contraire par exemple allergie croisée à l’ensemble des pénicillines)
Une bonne gestion des effets secondaires est cruciale pour un succès thérapeutique. Au-delà de la gestion de l’urgence vitale, leur anticipation est essentielle à une bonne alliance thérapeutique et à maintenir une relation de confiance entre le clinicien et le propriétaire.
Pour déclarer un effet indésirable survenant chez l’animal : télédéclaration en ligne ou formulaire téléchargeable en format papier sur le site de l’ANSES : https://pharmacovigilance-anmv.anses.fr
Bibliographie
- POST L. Reporting an adverse drug reaction to the Food and Drug Administration. In Bonagura JD and Twedt DC, eds, Kirks Current Veterinary Therapy. XIV ed. St. Louis Elsevier 2009 99-104.
- REINHART JM. Drug-Induced Liver Injury. Vet Clin North Am Small Anim Pract. 2025 55 717-30. doi 10.1016j.cvsm.2025.03.003. Epub 2025 Apr 24. PMID 40280782.
- Évaluation du lien de causalité entre un évènement indésirable et un médicament : le système ABON. Disponible à l’adresse https://www.anses.fr/fr/system/files/Evaluation%20du%20lien%20de%20causalité%20entre%20un%20evenement%20indesirable%20et%20un%20médicament.pdf (page consultée le 29/08/2025)
Liens d'intérêt : Subvention de recherche, prestations rémunérées d'expertise, frais d'hospitalité (Boehringer Ingelheim)Conférencière rémunérée (CEVA, Elanco, Bayer, Royal Canin)
📃 Efficacité d'un produit parasiticide contenant afoxolaner et milbemycin oxime, pour la prévention de transmission de Babesia canis chez le chien
Eric TIELEMANS
Coauteurs: Eric TIELEMANS, Carin RAUTENBACH, Alta VILJOEN, Frederic BEUGNET
Introduction
Les protozoaires du Genre Babesia (qui avec les Theileria sont aussi appelés piroplasmes) sont des parasites sanguins d'impact sanitaire et économique majeur affectant de nombreux vertébrés. Les nombreuses Babesia spp. connues sont présentes dans le monde entier et sont principalement transmises par des tiques. Les Babesia spp. sont généralement limitées régionalement, en dépendance à la présence de leur vecteur et de leur hôte vertébré. Chez la tique, elles effectuent un processus d'évolution complexe, durant la phase d'attachement et d'échange de fluide acarien/vertébré, résultant d'une migration de l'intestin aux glandes salivaires et d'une maturation en particule infectieuse, le sporozoïte. Transmis à l'hôte vertébré, le sporozoïte envahit et détruit les érythrocytes en s'y multipliant par réplication. Leur effet pathogène est donc notamment la conséquence d'une destruction massive d'érythrocytes [1,2,3].
Les nombreuses espèces canines connues de Babesia sont variables en termes de distribution géographique, vecteur, signes cliniques, pronostic et réponse aux traitements [2].
Babesia canis, une espèce majeure européenne transmise par la tique Dermacentor reticulatus, est l'agent de la babésiose canine. C'est une maladie vétérinaire significative, caractérisée par des réactions inflammatoires systémiques et des symptômes dus à l'hémolyse comme, par exemple, hémoglobinurie, ictère, anémie et insuffisance organique à plus long terme [3].
Matériels et résultats
Une étude expérimentale a été conduite pour vérifier la capacité de Nexgard Spectra® (IVP), une combinaison orale de l'isoxazoline afoxolaner (acaricide/insecticide) et du macrocyclique lactone milbemycin oxime (nématicide), à bloquer la transmission de B. canis par D. reticulatus chez le chien.
Trois groupes de 8 chiens ont été étudiés, un groupe traité à dose minimale avec l'IVP à Jour 0 et infesté aux Jours 1 et 28, un groupe contrôle non-traité infesté à Jour 1, et un groupe contrôle non-traité infesté à Jour 28. Chaque infestation était effectuée avec 50 D. reticulatus porteuses de B. canis à un taux de 23 %. Les tiques ont été retirées des chiens 6 jours après infestation.
Sept à neuf jours après leur infestation tous les chiens du groupe contrôle non traités ont exprimé des signes cliniques de babésiose canine (léthargie, et/ou urine sombre et/ou >39,5°C) confirmée positive par PCR et microscopie sur frottis sanguin. Ces chiens ont été immédiatement traités avec de l'imidocarb dipropionate, du diminazene aceturate et des traitements symptomatiques (antiémétiques, hépato-protecteurs, corticostéroïde). Deux à trois semaines après, ces chiens ont été confirmés positif par sérologie (IFA) et le PCR était devenu négatif, confirmant l'efficacité des traitements de support. Aucun des chiens traités avec l'IVP n'ont exprimé signes cliniques de babésiose canine ou n'ont eu un test PCR et IFA positif répétés pendant 2 mois.
Cette étude a démontré un modèle de transmission efficace chez les chiens contrôle non traités et une haute efficacité de l'afoxolaner pour le blocage de la transmission de cette maladie chez les chiens traités.
Conclusion
La thérapeutique de la babésiose canine est compliquée, peu de substances thérapeutiques à mécanisme d'action connu sont disponibles et ces substances, tout comme les vaccins, ont une efficacité variable selon la souche de B. canis [4]. Les isoxazolines tels que l'afoxolaner ont un mode d'action systémique et nécessitent que la tique s'attache à son hôte et échange des fluides avant d'être affectées par la substance acaricide. Néanmoins il semble que la maturation de B. canis nécessite suffisamment de temps pour que la tique se nourrissant sur l'animal traité ne soit pas en mesure de transmettre l'agent infectieux [5].
Cette étude a démontré que l'isoxazoline afoxolaner pourrait constituer une nouvelle solution de prévention contre la babésiose canine.
Bibliographie
- MALGWI SA, OGUNSAKIN RE, OLADEPO AD, ADELEKE MA, OKPEKU M. A Forty-Year Analysis of the Literature on Babesia Infection (1982-2022): A Systematic Bibliometric Approach. Int J Environ Res Public Health. 2023 Jun 16;20(12):6156.
- LEISEWITZ AL, MRLJAK V, DEAR JD, BIRKENHEUER A. The Diverse Pathogenicity of Various Babesia Parasite Species That Infect Dogs. Pathogens. 2023 Dec 11;12(12):1437. doi: 10.3390/pathogens12121437. PMID: 38133320; PMCID: PMC10746086.
- SOLANO-GALLEGO L, SAINZ Á, ROURA X, ESTRADA-PEÑA A, MIRÓ G. A review of canine babesiosis: the European perspective. Parasit Vectors. 2016 Jun 11;9(1):336. doi: 10.1186/s13071-016-1596-0. PMID: 27289223; PMCID: PMC4902949.
- BANETH G. Antiprotozoal treatment of canine babesiosis. Vet Parasitol. 2018 Apr 30;254:58-63. doi: 10.1016/j.vetpar.2018.03.001. Epub 2018 Mar 7. PMID: 29657012.
- OTRANTO D, MENDOZA-ROLDAN JA, BEUGNET F, BANETH G, DANTAS-TORRES F. New paradigms in the prevention of canine vector-borne diseases. Trends Parasitol. 2024 Jun;40(6):500-510. doi: 10.1016/j.pt.2024.04.009. Epub 2024 May 13. PMID: 38744542.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Endocardites bactériennes
Merignac, France
I. Définitions
Les endocardites sont des maladies rares (0,04 à 0,13 % d’incidence), souvent fatales et difficiles à diagnostiquer. Elles se caractérisent par une inflammation de l’endocarde, en général au niveau du tissu valvulaire. Elles peuvent être infectieuses ou non infectieuses mais seules les infectieuses sont bien décrites en médecine vétérinaire, et nous nous concentrerons sur elles dans notre présentation.
Les endocardites infectieuses sont causées par l’invasion d’un microbe au sein de l’endothélium valvulaire, résultant en des lésions prolifératives ou érosives et par voie de conséquence en des insuffisances valvulaires. Les animaux atteints succombent souvent d’insuffisance cardiaque, de maladie thromboembolique ou de mort subite. Des maladies immunitaires sont également souvent décrites dans le cours de la maladie (polyarthrites, glomérulopathies).
Les endocardites sont une entité difficile à diagnostiquer et le diagnostic fait appel à des critères précis (cf infra). Le clinicien devra donc connaître les manifestations cliniques, échographiques et biologiques des endocardites afin de suspecter cette entité de façon appropriée. Les endocardites sont en effet des affections systémiques se traduisant par une grande variété de signes et d’organes atteints.
II. Reconnaissance des facteurs prédisposant
- La bactériémie : il s’agit d’une condition nécessaire mais pas suffisante pour développer une endocardite. Les sources les plus fréquentes sont une spondylodiscite, une prostatite, une pneumonie, une infection urinaire, une infection cutanée, une maladie parodontale ou encore un cathéter veineux central. La présence d’une telle infection dans les semaines ou mois qui précèdent un épisode fébrile devrait donc attirer l’attention du clinicien vers une possible endocardite.
- Le signalement : les chiens mâles de grand format d’âge moyen à vieux sont prédisposés aux endocardites infectieuses. Il est donc très rare de rencontrer une endocardite sur un animal de petit format. Les Bergers Allemands semblent prédisposés plus que d’autres races, probablement en raison d’une immunité souvent déficiente ;
- Le rôle de la prise de corticoïdes n’est pas clairement établi.
- La présence d’une sténose aortique ou sous-aortique est reconnue comme étant un facteur clairement prédisposant [1].
- Contrairement aux idées reçues, le lien avec les infections parodontales et les détartrages n’est en revanche pas établi [2].
III. Présentation clinique
1. Anamnèse
Dans une étude de 2006 [3], le motif de consultation de plus fréquent était une boiterie (53 % des animaux atteints). Celle-ci est souvent fluctuante et affecte plusieurs membres. Suivent des signes moins spécifiques tels la léthargie, l’anorexie, la difficulté respiratoire, la faiblesse, les syncopes et les troubles digestifs. La raideur et les boiteries sont dues à une polyarthrite à médiation immunitaire alors que les douleurs abdominales peuvent être liées à des infarcti rénaux ou spléniques.
2. Examen clinique
La plupart des signes cliniques sont malheureusement non spécifiques.
Une fièvre est notée dans 50 à 90 % des cas.
Un souffle, surtout de survenue nouvelle devrait alerter le clinicien. Il est présent dans la majorité des cas d’endocardites (89 à 94 %) [1, 4]. Un souffle à composante diastolique forte associée à un pouls bondissant devrait élever la suspicion d’endocardite aortique. Il est à noter que 26 % des chiens atteints n’ont pas de souffle audible. Une endocardite n’est donc pas exclue en l’absence de souffle !
Des arythmies sont présentes dans 40 à 70 % des cas mais sont bien sûr non spécifiques. Les arythmies semblent plus fréquentes lors d’endocardite aortique. Un bloc du troisième degré peut être induit lors d’endocardite aortique. Ainsi, une endocardite devrait-elle être recherchée suite à un diagnostic de BAV3, notamment si l’animal est fébrile ou présente un nouveau souffle cardiaque.
Une insuffisance cardiaque est présente dans environ 50 % des cas, et il n’est pas rare que celle-ci survienne sans dilatation atriale gauche, la régurgitation étant souvent aiguë.
3. Séquelles systémiques
Des événements thromboemboliques (septique et non septiques) sont très fréquents chez les chiens atteints d’endocardite (70 à 80 % des animaux en étude nécropsique) [4]. Des infarcti rénaux ou spléniques sont régulièrement observés à l’échographie abdominale et peuvent orienter vers une endocardite si le reste du contexte clinique est en faveur.
Des maladies immunitaires, notamment des polyarthrites, et une glomérulopathie sont fréquemment observées lors d’endocardites (75 % et 36 % respectivement selon une étude).
4. Anomalies biologiques
La numération formule est souvent modifiée lors d’endocardite, 78 % des animaux présentant une leucocytose neutrophilique et plus de 50 % présentant une thrombopénie.
Une hypoalbuminémie et souvent présente à la biochimie. Une azotémie est également assez fréquente en raison du phénomène de thromboembolie au niveau rénal.
IV. Diagnostic
1. Hémoculture
Les hémocultures positives sont essentielles pour supporter un diagnostic d’endocardite (cf. infra). Malheureusement, 60 à 70 % des hémocultures ont été rapportées comme négatives, notamment en raison de traitements antibiotiques préexistants [1, 4].
Lors de culture positive, il est important d’avoir soumis 3 échantillons de 3 sites différents afin de s’assurer que la culture n’est pas un faux positif lié à une contamination par des germes cutanés. Ainsi il est préférable que le même organisme soit isolé sur les 3 échantillons. Les organismes les plus souvent isolés sont les staphylocoques (aureus et intermedius), les streptocoques, les E.Coli, les pseudomonas, les érysipèles. Plus récemment, les bartonelles ont été citées comme un agent assez fréquent d’endocardite notamment aortique aux États-Unis. La prévalence de cette infection en France et en Europe demeure inconnue.
2. Échocardiographie
Elle est aussi essentielle au diagnostic puisque celui-ci repose souvent sur la visualisation d’une lésion végétative sur une valve cardiaque. Les lésions végétatives apparaissent comme des structures hyperéchogènes et oscillantes, bougeant de façon indépendante par rapport à la valve. Un différentiel est une endocardiose sévère mais dans ces cas-là, c’est essentiellement le signalement de l’animal qui permet la différentiation des deux entités. La sensibilité de l’échocardiographie dans la détection des végétations n’a pas été établie en médecine vétérinaire mais elle est de l’ordre de 55 % chez l’Homme. Il est possible qu’ellle soit de l’ordre de 60 à 70 % chez nos patients. La présence d’une régurgitation aortique significative devrait également faire naître une suspicion d’endocardite.
3. Critères suggérés pour le diagnostic des endocardites
Comme nous l’avons vu, l’endocardite est une maladie à répercussion systémique, à signes non spécifiques dont le diagnostic est délicat. Un diagnostic par critère est donc en vigueur (appelés les critères de Duke modifiés). Il se fonde sur :
- des critères majeurs :
- échocardiogramme positif : lésion végétative, érosive, abcès ;
- insuffisance valvulaire nouvelle : notamment insuffisance aortique sans sténose aortique ;
- hémocultures positives : plus de 2 cultures positives, plus de 3 cultures positives s’il s’agit d’un contaminant cutané fréquent.
- des critères mineurs :
- fièvre ;
- chien de grande à moyenne taille ;
- sténose sous-aortique ;
- maladie thromboembolique ;
- maladie immunitaire : polyarthrite, glomérulopathie ;
- hémocultures positives ne satisfaisant pas le critère majeur évoqué plus haut ;
- sérologie Bartonelle supérieure à 1:1024 (ou PCR).
a) Diagnostic possible
Il se fonde sur 1 critère majeur et 1 critère mineur ou 3 critères mineurs.
b) Diagnostic définitif
- examen histopathologie de la valve ;
- 2 critères majeurs ;
- 1 critère majeur et 2 mineurs ;
c) Exclusion
- diagnostic d’une autre maladie ;
- résolution de la régurgitation ou de la végétation en moins de 4 jours de traitements ;
- résultat d'examen histopathologie non en faveur.
4. Traitement
Le traitement antibiotique bactéricide long terme est la pierre angulaire du traitement.
Une antibiothérapie empirique est débutée en attendant les résultats de culture, et peut être continuée en cas de réponse favorable si la culture est négative... Idéalement un traitement antibiotique intraveineux de une à deux semaines est nécessaire pour le traitement d’une endocardite aiguë. Puis une antibiothérapie par voie orale est mise en place pendant 6 à 8 semaines. Des contrôles cliniques, échocardiographiques et bactériologiques réguliers sont réalisés.
Chez l’Homme, un traitement antiplaquettaire de type aspirine n’est pas recommandé du fait de l’absence d’efficacité et d’une augmentation du risque hémorragique.
Un traitement d’insuffisance cardiaque classique sera mis en place le cas échéant.
5. Pronostic
Les animaux atteints d’endocardite aortique ont un pronostic le plus souvent sombre. Dans une étude, une médiane de survie de 3 jours a été décrite versus 476 jours lors d’atteinte de la valve mitrale [4]. Une autre étude a décrit une mortalité de 33 % durant la première semaine et 92 % durant les 5 mois suivant le diagnostic [1].
V. Conclusion
Le clinicien devra considérer comme possible une endocardite lorsqu’il sera confronté chez un chien de grand format à plusieurs signes d’appel telle une fièvre associée à une boiterie, un nouveau souffle cardiaque, des manifestations thromboemboliques. Ces signes d’appel devront alors motiver la réalisation d’une échocardiographie suivie ou non d’une hémoculture afin de confirmer le diagnostic. Un traitement antibiotique long terme basé sur les cultures devra être mis en place afin de ralentir la progression de cette maladie dévastatrice.
Bibliographie
- SISSON, D. and W.P. THOMAS, Endocarditis of the aortic valve in the dog. J Am Vet Med Assoc, 1984. 184(5): p. 570-7.
- PEDDLE, G.D., et al., Association of periodontal disease, oral procedures, and other clinical findings with bacterial endocarditis in dogs. J Am Vet Med Assoc, 2009. 234(1): p. 100-7.
- SYKES, J.E., et al., Clinicopathologic findings and outcome in dogs with infective endocarditis: 71 cases (1992-2005). J Am Vet Med Assoc, 2006. 228(11): p. 1735-47.
- MACDONALD, K.A., et al., A prospective study of canine infective endocarditis in northern California (1999-2001): emergence of Bartonella as a prevalent etiologic agent. J Vet Intern Med, 2004. 18(1): p. 56-64.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Environnement et cancer : notions de pathologie comparée
Nantes, France
L’influence de l’environnement sur la survenue et la progression de nombreux cancers est bien démontrée chez l’homme. On estime qu’environ 20% des cancers humains seraient liés à des expositions environnementales à des agents carcinogènes tels que la fumée de cigarette, l’amiante ou certains hydrocarbures aromatiques polycycliques (Owada et al., 2025, Res Vet Sci, 184:105517, PMID 39740499 ). Cette problématique s’étend aujourd’hui à la médecine vétérinaire comparée, où les chiens et les chats, exposés aux mêmes polluants domestiques et urbains que leurs propriétaires, apparaissent comme des modèles biologiques et épidémiologiques privilégiés pour l’étude des cancers d’origine environnementale.
Chez le chien, plusieurs associations entre environnement et tumeurs spontanées ont été documentées. Une étude récente réalisée dans le cadre de la Golden Retriever Lifetime Study a mis en évidence une corrélation entre l’exposition aux herbicides (2,4-D et glyphosate) et l’augmentation des lésions oxydatives de l’ADN, précédant la survenue de lymphomes multicentriques (Moore et al., 2025, J Vet Intern Med, PMID 40784785 ). Cette étude cas-témoin imbriquée a examiné l’exposition de 49 chiens de race Golden Retrievers atteints de lymphome à différentes sources de pollution (usines chimiques, décharges, incinérateurs, centrales à charbon, etc.). Bien qu’aucun facteur isolé ne soit significatif, la proximité de trois sources ou plus de pollution augmentait presque significativement le risque de lymphome multicentrique (OR = 2,6 ; IC95% [0,99–6,86]) ( Golden Retriever Lifetime Study, Vet Comp Oncol, 2022, PMCID PMC9287967 ). Cette tendance suggère un effet cumulatif des expositions multiples, similaire à ce qui est observé chez l’humain pour les cancers hématologiques.
Ces résultats confortent l’hypothèse selon laquelle certains pesticides et composés organiques volatils (COV) peuvent induire un stress oxydatif et contribuer à la cancérogenèse, parallèlement à ce qui est observé chez l’homme exposé à ces mêmes substances. Ainsi et d’un point de vue épidémiologique, les chiens vivant en milieu urbain présentent une incidence accrue de certaines tumeurs, notamment les lymphomes et carcinomes urothéliaux, potentiellement liée à la densité des polluants atmosphériques ou aux rejets industriels (Owada et al., 2025 ). Ainsi, les carcinomes de la vessie chez certaines races, notamment les Scottish Terriers, ont été associés à l’usage domestique d’herbicides. Une étude classique (Glickman et al.) a démontré que les chiens exposés à des pelouses traitées par herbicides et insecticides avaient un risque de carcinome urothélial multiplié par 7,19, et par 3,62 pour les herbicides seuls (J Am Vet Med Assoc, 2004; ). Plus récemment, une étude de 2024 a confirmé un lien entre la présence de sous-produits de chloration dans l’eau potable (trihalométhanes) et l’incidence accrue de carcinomes urothéliaux (UCC), suggérant que certaines expositions hydriques jouent un rôle carcinogène direct (Owada et al., Vet Comp Oncol, 2024; PMID 38388159 ).
Également, dans une étude consacrée aux tumeurs mammaires de la chienne comme modèle du cancer du sein de la femme, nous avons examiné l'association entre l'exposition à des polluants organiques persistants (POPs), notamment des PCB dioxin-like, et le cancer mammaire chez les chiens de compagnie. Des polychlorobiphényles spécifiques (PCB-118, PCB-156, PCB-105, PCB-114) ont été identifiés comme liés au cancer mammaire, corroborant des résultats humains. Le modèle chien peut donc aider à comprendre les liens environnementaux dans l’étiologie du cancer du sein humain.
Ces observations confortent la notion de chien sentinelle environnementale. Par sa cohabitation étroite avec l’homme, sa susceptibilité génétique contrôlable et sa longévité intermédiaire, il permet une détection précoce des effets cancérigènes environnementaux (Palmieri et al., 2024, Front Vet Sci, PMC11101696 ). L’étude conjointe des tumeurs canines et humaines offre donc une approche complémentaire pour caractériser les risques et élaborer des stratégies de prévention transversales.
L’intégration des approches épidémiologiques, moléculaires et comparatives souligne aujourd’hui la pertinence d’une vision One Health, unissant santé humaine, animale et environnementale. Dans ce contexte, le chien, par sa position unique à l’interface de l’homme et de l’environnement, constitue à la fois un modèle expérimental pertinent et un indicateur précoce des risques sanitaires émergents.
Bibliographie
- OWADA K. et al. Environmental exposure and cancer occurrence in dogs, Res Vet Sci, 2025; 184:105517. PMID: 39740499
- MOORE A. et al. Whole blood DNA damage precedes a diagnosis of canine lymphoma, J Vet Intern Med, 2025; PMID: 40784785
- KARLSSON E.K. et al. Comparative oncology: what dogs and other species can teach us about human cancers, Genome Biol, 2015; 16:90. PMID: 26136551
- SÉVÈRE, S., MARCHAND, P., GUIFFARD, I., MORIO, F., VENISSEAU, A., VEYRAND, B., LE BIZEC, B., ANTIGNAC, J.-P., & ABADIE, J. Pollutants in pet dogs: a model for environmental links to breast cancer. SpringerPlus, 4, 27. 2015
- PALMIERI C. et al. Domestic dogs as environmental sentinel in comparative oncology, Front Vet Sci, 2024; PMC11101696
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Erreurs diagnostiques en médecine interne : l'établissement de mauvais liens
Gentilly, France
I. Introduction
Le processus diagnostique en médecine vétérinaire repose sur une succession d’étapes cognitives, depuis la collecte des données cliniques jusqu’à l’interprétation des examens complémentaires. Toutefois, ce raisonnement est fréquemment influencé par des associations erronées, autrement dit des liens cliniques ou interprétatifs incorrects, susceptibles de conduire à une erreur diagnostique. Il existe peu de données sur la fréquence de ce type d’erreurs. Un article récent utilisant les données de 3 centres hospitaliers vétérinaires Américains indiquent que les erreurs diagnostiques ou de jugement représentent 10 à 15 % des erreurs médicales reportées dans un registre de cas sur une durée de 3 ans [Wallis J et coll, 2019]. Un exemple classique consiste à interpréter une image lésionnelle en échographie abdominale comme une seule affection possible, en écartant arbitrairement les autres possibilités diagnostiques. Ce type de confusion illustre bien l’importance de la vigilance dans l’analyse des données. Les conséquences pratiques sont loin d’être négligeables :
- sur-diagnostic
- anxiété inutile du propriétaire
- investigations coûteuses et parfois invasives
- initiation de traitements inadaptés
- dans les cas les plus graves, proposition d’une euthanasie non justifiée
II. Typologie des erreurs de raisonnement
Différents facteurs peuvent interférer avec l’obtention d’un diagnostic adéquat. Les principaux sont présents dans la figure 1.
Figure 1 Principaux facteurs influençant le processus diagnostique. D’après Vally et coll, 2023
On peut par ailleurs envisager plusieurs mécanismes cognitifs qui expliquent l’apparition de ces erreurs diagnostiques. Le biais de confirmation, tout d’abord, pousse le clinicien à interpréter les données de manière à conforter son hypothèse initiale. Ainsi, une masse visualisée en échographie est spontanément interprétée comme tumorale, sans envisager d’autres diagnostics possibles (lésion pyogranulomateuse, lésion de fibroplasie, corps étranger chronique, ...). Le biais de disponibilité, quant à lui, conduit à surestimer la probabilité d’une cause récemment rencontrée ou particulièrement marquante, ce qui tend à limiter la réflexion différentielle. À cela s’ajoute la tendance à établir des corrélations abusives, en reliant deux signes cliniques observés simultanément, mais sans lien réel.
III. Conséquences des erreurs d’interprétation
Les répercussions de ces erreurs de raisonnement sont multiples. Elles se traduisent d’abord par une augmentation du stress, aussi bien pour l’animal que pour son propriétaire. Elles peuvent également entraîner la réalisation d’examens complémentaires invasifs ou coûteux, qui se révèlent finalement inutiles. Plus grave encore, elles contribuent parfois à retarder l’identification de la véritable maladie, compromettant ainsi la qualité de la prise en charge. Enfin, lorsqu’une erreur flagrante est reconnue, la confiance du client envers le praticien s’en trouve durablement altérée.
IV. Stratégies de prévention
Il existe heureusement plusieurs moyens de limiter l’impact de ces biais cognitifs ou des facteurs d’influence, et ainsi de réduire la fréquence des erreurs diagnostiques... Tout d’abord, il est important de régulièrement encourager la prévention : notamment, d’organiser des réunions pour analyser les cas qui ont posé problème et/ou créer un plan de prévention dans la structure sont des points clés. Afin d’organiser ces rondes de morbidité-mortalité, l’utilisation de grilles afin de classifier les erreurs médicales peut être intéressante [Giles et coll, 2025].
L’adoption d’une démarche diagnostique systématisée constitue une première étape essentielle. Elle peut reposer sur l’utilisation et la mise à disposition d’accès facile à des listes de diagnostic différentiel par exemple, des livres de références à jour, concernant les dernières données médicales, ou l’accès à des données d’aide au raisonnement (intelligence artificielle, utilisation d’algorithmes d’aide au diagnostic). Le recul critique doit être encouragé : il s’agit de remettre régulièrement en question l’hypothèse initiale et de vérifier qu’aucune donnée nouvelle ne la contredit. Une corrélation étroite doit être retrouvée entre l’ensemble des données disponibles (cliniques, biologiques, d’imagerie ...).
Le recours à l’utilisation de rondes de cas collaboratives entre collègues s’avère par ailleurs précieux. Un avis d’expert externalisé peut aussi être sollicité, quel que soit le domaine (pathologie clinique, imagerie, médecine interne, discipline thérapeutique comme la chirurgie, oncologie ...).
Enfin, la formation continue joue un rôle central, en permettant aux praticiens de rester informés des limites et des pièges propres aux différentes techniques diagnostiques.
Il peut être important aussi de corriger ce qui a pu conduire/favoriser cette erreur diagnostique : surcharge de travail, environnement non propice à la réflexion (bruit, passage, ou l’échange autour des cas cliniques), pression des propriétaires, matériel inadéquate, cas inadapté à l’expérience du clinicien ou au contraire excès de confiance face au cas.
Une erreur médicale peut ainsi parfois aboutir à des remises en cause managériales ou matérielles. Malheureusement, peu de systèmes d’aide à la détection et la comptabilisation des erreurs diagnostiques pour réaliser un audit sont disponibles [Abimanyi-Ochom et coll, 2019].
V. Conclusion
Les erreurs de raisonnement clinique en médecine interne vétérinaire sont fréquentes mais loin d’être inéluctables. Leur reconnaissance et leur prévention passent par une vigilance méthodologique et une réflexion critique constante. La confrontation systématique des résultats avec le contexte clinique global demeure essentiel. L’adoption d’une posture de doute constructif et le recours à une approche multidisciplinaire apparaissent comme des atouts majeurs pour améliorer la fiabilité diagnostique.
En définitive, le message clé à retenir est simple, mais fondamental : ne pas s’arrêter à la première évidence.
Bibliographie
- ABIMANYI-OCHOM J et coll. Strategies to reduce diagnostic errors: a systematic review. BMC medical informatics and decision making 2019; 19, 174.
- GILES G et coll. Categorising reported errors and incidents from morbidity and mortality meetings (MandMs) in a small animal multi-specialty veterinary teaching hospital. Austr Vet J 1035; 267-275.
- VALLY ZI et coll. Errors in clinical diagnosis: a narrative review. Journal of International Medical Research 2023; 518, 1-10.
- WALLIS J et coll. Medical errors cause harm in veterinary hospitals. Front Vet Sci 2019; 6:12.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Est ce qu'il faut créer des liens avec d'autres professionnels ?
Verfeil, France
Paris, France
I. Introduction
Le recours à des collaborations structurées entre vétérinaires et autres professionnels du secteur animalier (éducateurs et comportementalistes canins ou félins, toiletteurs, promeneurs, pet-sitters, gestionnaires de pension, psychologues) présente de nombreux bénéfices pour la pratique vétérinaire et la santé globale des animaux. Sur le plan clinique, ces partenariats facilitent le repérage précoce de problématiques physiques ou comportementales, grâce à la présence régulière de ces intervenants auprès des animaux et à leur capacité d’observation en contexte quotidien. Ils favorisent la continuité des soins, en accompagnant la mise en œuvre de protocoles thérapeutiques ou à travers des programmes de rééducation comportementale, et en contribuant au suivi à domicile. Sur le plan préventif, ils permettent de réduire l’incidence de certains troubles (agressivité, anxiété, obésité…) par la mise en place d’activités adaptées, de conseils environnementaux et de mesures d’hygiène comportementale. Enfin, sur le plan relationnel et éthique, la coopération interprofessionnelle renforce le bien-être animal, soutient les propriétaires dans la gestion de situations complexes (deuil, maladie chronique, problématiques comportementales) et améliore l’adhésion aux recommandations vétérinaires.
II. État des lieux et freins
Les résultats de deux enquêtes récentes [PawLoVet, 2024, n = 277 ; enquête interne menée par Sarah JEANNIN, 2025, n = 88] mettent néanmoins en évidence un déficit de collaborations, souvent limitées à des initiatives ponctuelles et personnelles. Les principaux freins identifiés incluent la méconnaissance des métiers émergents et de leurs compétences spécifiques, l’absence de reconnaissance institutionnelle de ces professions, ainsi que des contraintes organisationnelles. Cette faible visibilité entrave l’intégration d’approches complémentaires pourtant susceptibles de renforcer la prise en charge globale.
III. Critères de sélection des partenaires
Dans ce contexte, il est essentiel de disposer de repères fiables pour identifier des partenaires compétents. Les critères de sélection incluent : la formation initiale et les diplômes éventuels, ainsi que l’évaluation des approches et outils employés, qui doivent être conformes aux données scientifiques, et respectueux du bien-être animal. Il convient également de vérifier si le professionnel actualise régulièrement ses connaissances théoriques et compétences pratiques au travers de la formation. L’adhésion à un réseau, un syndicat professionnel, un label de qualité ou une association spécialisée constitue un indicateur supplémentaire de sérieux et d’engagement, traduisant un investissement dans la profession et une ouverture à la coopération interdisciplinaire. Enfin, le respect de la réglementation administrative et sanitaire en vigueur (statut légal, obligations déclaratives, assurance, normes d’hygiène et d’hébergement) constitue un prérequis indispensable à toute collaboration.
IV. Recommandations et conclusion
Il est recommandé aux vétérinaires de s’appuyer selon ces repères — formation et diplômes, méthodes et outils, actualisation des connaissances, engagement professionnel, conformité réglementaire — pour évaluer les pratiques des intervenants de leur territoire. En structurant, sur cette base, des réseaux pluridisciplinaires de confiance, ils renforcent la qualité et la cohérence des parcours de soins, au bénéfice des animaux comme de leurs propriétaires.
Mots-clés
collaboration interprofessionnelle, médecine vétérinaire, métiers du secteur animalier, reconnaissance professionnelle, bien-être animal.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Etude comparative de 2 techniques d'étalements de prélèvement de moelle osseuse : étalement direct et étalement après enrichissement
Léonore THOUVENIN
Coauteurs : P. BERNARD, A. BERTIN, F. GRANAT, C. TRUMEL
Introduction
L'examen cytologique de la moelle osseuse (myélogramme) est un outil diagnostique utilisé par les praticiens vétérinaires pour l'évaluation de certaines affections hématologiques dont le diagnostic n'a pu être posé par des examens simples et non invasifs. La ponction de moelle est une procédure rapide à mettre en œuvre, nécessitant peu de matériel, et associée à un faible risque de complications majeures. Cependant, elle nécessite l'acquisition d'un savoir-faire fondé sur une formation adéquate et une mise en pratique régulière.
Malgré un geste adéquat, les spécimens reçus dans les laboratoires de biologie médicale ne sont pas toujours de qualité suffisante pour l'établissement d'un diagnostic. Un spécimen idéal se caractérise par une contamination sanguine minimale et la présence de nombreux grains de moelle correspondant à une structure complexe composée de précurseurs de cellules sanguines et d'une trame conjonctive associée à des adipocytes, des fibroblastes et des vaisseaux (Harvey, 2012). Leur observation est une condition nécessaire mais non suffisante de la qualité d'un prélèvement.
Les principaux échecs diagnostiques proviennent donc de spécimens dépourvus ou trop pauvres en grains de moelle, du fait notamment d'une trop forte hémodilution même lorsque le prélèvement a été effectué correctement. À ce jour, plusieurs méthodes d'étalement des spécimens de moelle sont décrites en médecine humaine et vétérinaire (Ettinger et al., 2024; Harvey, 2012; Lee et al., 2008; Stacy and Harvey, 2017), mais l'absence d'uniformisation de la technique peut entraîner des disparités dans l'interprétation cytologique, compromettant ainsi le diagnostic et par conséquent, la prise en charge thérapeutique.
Dans le cadre du consensus du myélogramme 2025, qui a pour objectif d'harmoniser les indications et les pratiques autour de l'examen de la moelle osseuse, nous avons mené une étude comparative de deux techniques d'étalement afin d'identifier la plus performante.
Matériel et méthodes
Cette étude prospective a été réalisée au cours de l'année scolaire 2024/2025. Lors de prélèvement de moelle osseuse réalisé par des vétérinaires praticiens du service de médecine interne, l'auteur travaillant au laboratoire était appelé afin de réaliser les étalements après avoir été formé en amont par un spécialiste en biologie médicale.
Deux techniques d'étalements ont été appliquées pour chaque spécimen de moelle préalablement transféré dans un tube EDTA :
Technique 1 dite directe : étalements directs du prélèvement provenant du tube EDTA à l'aide d'une pipette Pasteur déposé puis étalé entre deux lames selon la technique « squash ».
Technique 2 dite d'enrichissement : transfert préalable du contenu du tube EDTA dans une coupelle en verre inclinée afin de mettre en évidence les grains de moelle (figure 1). Ces grains sont ensuite récupérés à l'aide d'une pipette Pasteur puis transférés et étalés à l'aide de la même technique « squash ».
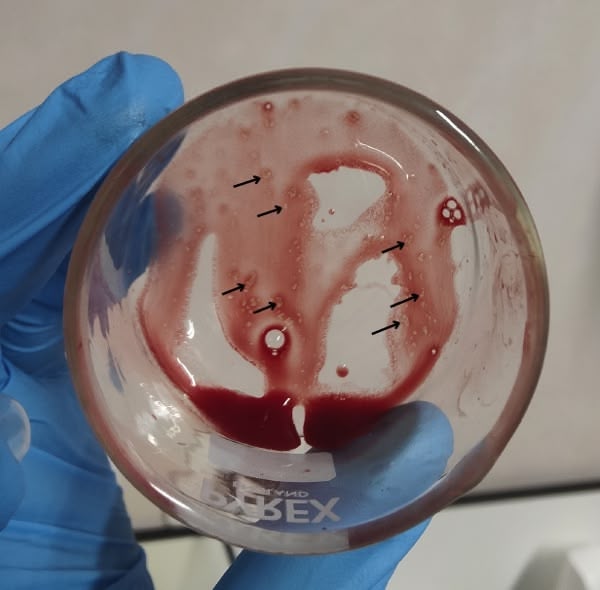
Figure 1
Après séchage à l'air libre, toutes les lames sont colorées au May-Grünwald-Giemsa (MGG) au laboratoire. L'évaluation de la qualité des étalements est réalisée par un spécialiste en biologie médicale à l'aide d'une grille d'analyse standardisée (tableau 1).
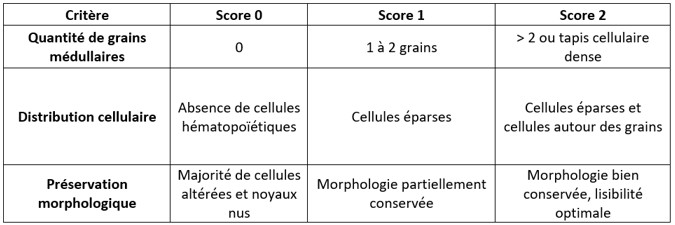
Tableau 1
Résultats
Onze spécimens de moelle osseuse ont été inclus, provenant de 8 chiens et 3 chats. Pour chaque spécimen, un nombre variable d'étalement a été réalisé pour chaque technique, allant de 4 à 12 lames, en fonction du volume prélevé et de la richesse en grains.
Il a été décidé de sélectionner aléatoirement 3 lames pour chacune des techniques, et de déterminer pour chacune un score de qualité correspondant à la somme des scores des trois critères de qualité. Les scores médians sont significativement différents, de 2,78 pour la première technique contre 5 pour la deuxième technique (p = 0,0469).
Discussion
À la connaissance des auteurs, bien que ces deux techniques d'étalement soient mentionnées dans la littérature, aucune étude comparative n'a été menée scientifiquement. Nous avons donc pu montrer que la technique d'enrichissement permettait d'obtenir des lames de meilleure qualité. Par ailleurs, notre expérience sur le terrain, ainsi que nos échanges avec de nombreux praticiens en France, ont révélé que cette technique demeure encore peu connue en pratique quotidienne.
Ce travail qui s'inscrit dans le cadre du consensus sur le myélogramme est une première étape. D'autres expérimentations restent à réaliser pour l'obtention de prélèvements de qualité comme par exemple l'intérêt de l'utilisation d'aiguilles à prélèvement de moelle préalablement tapissées d'EDTA pour éviter la formation de caillots.
Bibliographie
- ETTINGER, S.J., COTÉ, E., FELDMAN, E.C., 2024. Textbook of veterinary internal medicine: diseases of the dog and the cat. ELSEVIER, St. Louis, Missouri.
- HARVEY, J.W., 2012. Bone Marrow Examination, in: Veterinary Hematology. ELSEVIER, pp. 234-259. https://doi.org/10.1016/B978-1-4377-0173-9.00008-7
- LEE, S. -H., ERBER, W.N., PORWIT, A., TOMONAGA, M., PETERSON, L.C., International Council for Standardization In Hematology, 2008. ICSH guidelines for the standardization of bone marrow specimens and reports. Int. J. Lab. Hematol. 30, 349-364. https://doi.org/10.1111/j.1751-553X.2008.01100.x
- STACY, N.I., HARVEY, J.W., 2017. Bone Marrow Aspirate Evaluation. Vet. Clin. North Am. Small Anim. Pract. 47, 31-52. https://doi.org/10.1016/j.cvsm.2016.07.003
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Etude pilote de la corrélation entre la dangerosité et la mutation sur le gène SLC6A3-PolyA transporteur de la dopamine chez le Malinois
Christèle CROZIER
Introduction
La race des Bergers Belges Malinois a subi une forte croissance dans les dernières années, mais beaucoup de ces chiens finissent en refuge. Les abandons sont principalement dus à l'agressivité et à l'impulsivité des chiens. Le variant PolyA(22) du gène du transporteur de la dopamine (SLC6A3) a été associé à une augmentation de l'impulsivité, de l'agressivité et à un risque accru de crises d'épilepsie chez le Malinois (LIT L, BELANGER JM, BOEHM D, LYBARGER N, OBERBAUER AM, 2013).
Ayant constaté, comme de nombreux vétérinaires comportementalistes, un nombre de consultations de Malinois très élevé ces dernières années, j'ai cherché à connaitre l'impact de cette mutation sur les comportements impulsifs et agressifs des Malinois que je voyais en consultation.
Matériel et résultats
Méthode : 28 chiens venus en consultation de comportement pour morsure (n=20) ou impulsivité (n=8) ont été évalués et classés selon une échelle de dangerosité (1 = non dangereux, 4 = très dangereux). Le statut génétique des chiens a été déterminé par analyse moléculaire.
Le Dog Impulsivity Assessment Scale (DIAS) (WRIGHT, MILLS & POLLUX, 2011) a été utilisé pour mesurer, avec les propriétaires l'impulsivité, l'agressivité et la réactivité de leur animal (questionnaire réalisé en présentiel ou au téléphone).
Résultats : en appliquant les tests de SPEARMANS.
Les résultats d'évaluations classiques ne sont en aucun cas significatifs : ni avec le DIAS ni avec les résultats de mutation. Il n'y a aucune association significative entre le statut génétique (A0/A0, A0/A22, A22/A22) et le niveau de dangerosité (KRUSKAL-WALLIS, p = 0,194). Seule apparait une corrélation positive entre l'agressivité DIAS et la dangerosité (SPEARMAN, r = 0,46, p = 0,027).
Les résultats sont complètement différents si on évalue la dangerosité des chiens sans prendre en compte leur environnement : (tableaux 1 et 2).
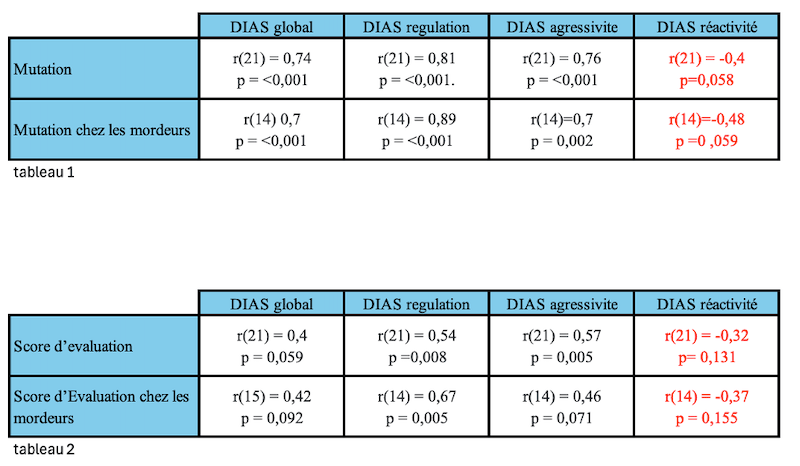
Tableaux 1 et 2
Le résultat de la corrélation de SPEARMAN a ainsi montré qu'il y avait une corrélation statistiquement significative entre le type de mutation et les résultats d'évaluation, r(26) = 0,58, p= ,001. Le résultat est quasiment identique pour le groupe des mordeurs : r(18) = 0,52, p = ,02.
Il n'y a pas de corrélation positive entre le score global ou le score de réactivité au DIAS et les résultats d'évaluation, mais la corrélation est positive concernant la régulation et l'agressivité, que les chiens soient mordeurs ou pas.
Le modèle de régression logistique ordinale n'a pas convergé, indiquant un échantillon insuffisant.
Discussion
L'évaluation, ainsi qu'elle est réalisée par les vétérinaires, c'est-à-dire en tenant compte du milieu de vie du chien, ne semble pas être un test pertinent pour cette étude. En effet, l'agressivité et l'impulsivité pourront être inhibées, ne seront pas repérées, ou au contraire pourront être exacerbées par des facteurs purement environnementaux ou les capacités éducatives des propriétaires. Il est donc impératif d'évaluer les chiens sans tenir compte de ces paramètres.
L'agressivité des chiens mordeurs n'est pas corrélée au niveau de dangerosité, mais ce point mériterait d'être étudié avec un échantillon plus large (ici n=14).
L'absence de groupe contrôle est gênant, mais n'a pas pu être mis en place au vu du coût des analyses et des évaluations.
La lecture de cette présente étude est gagne a être éclairée par celle d'une étude similaire réalisée chez le Border Collie (SL VAN BUREN, AM OBERBAUER, KM MINOR1, JM BELANGER, E FURROW, 2021) qui conclut à l'absence de corrélation entre mutation et agression chez le Border Collie. D'après cette étude, ces variantes pourraient ne pas être causales, mais marquer un haplotype contenant une variante de risque encore inconnue chez le Malinois.
Conclusion
Les résultats de cette étude préliminaire confirment une corrélation entre le variant PolyA(22) et la dangerosité chez le Malinois, sur des évaluations données sans tenir compte du contexte de vie du chien. L'agressivité évaluée par le DIAS est corrélée à la mutation et au niveau de dangerosité, à l'exception des chiens venus consulter pour morsure. Une étude plus large incluant des chiens témoins est nécessaire pour affiner ces conclusions et évaluer la pertinence d'un dépistage génétique.
Bibliographie
- LIT L, BELANGER JM, BOEHM D, LYBARGER N, OBERBAUER AM (2013)
- WRIGHT, MILLS & POLLUX, 2011
- SL VAN BUREN, AM OBERBAUER, KM MINOR, JM BELANGER, E FURROW, 2021
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Étude rétrospective de la prévalence des phénotypes transitoires chez le chat atteint de myocardiopathie
Justine COLASSE
Coauteurs : GUIGO Pierre, AUPEE Cécile, DOUAY Tiphaine, AMOYAL Suzanne, LE GALL Coline, FOUHETY Aurore, POISSONNIER Camille
Introduction
Les myocardiopathies transitoires ont été décrites chez le chat depuis 2018. Elles se caractérisent par un phénotype de type « myocardiopathie hypertrophique » (MCH) ou « myocardiopathie restrictive » (MCR), confirmé à l'examen échocardiographique, souvent décompensé, pour lequel les paramètres échocardiographiques se normalisent durant le suivi. Si plusieurs publications décrivent ces phénotypes, à notre connaissance aucune étude n'a évalué la proportion dans laquelle ces phénotypes sont retrouvés parmi les autres types de myocardiopathies.
Objectif : déterminer, au sein d'une population de chats atteints de cardiopathies, la prévalence des différents phénotypes et notamment celle des myocardiopathies transitoires.
Matériels et méthode
Étude rétrospective au sein d'une structure de référé, avec un recensement des chats présentés en consultation de cardiologie pour lesquels un suivi échocardiographique était disponible au moins 1 mois après la première présentation. Les critères d'inclusion pour le groupe « transitoires » étaient un diagnostic de myocardiopathie lors de la consultation initiale, associée à une normalisation des lésions. Les critères d'inclusion dans le groupe « persistants » sont le diagnostic d'une myocardiopathie toujours présente lors des suivis. Un minimum de 1 mois est exigé entre le diagnostic et le dernier contrôle.
Résultats
Entre janvier 2024 et janvier 2025, une cardiopathie a été diagnostiquée chez 229 chats lors d'un examen échocardiographique au sein du service de cardiologie.
Parmi ces 229 chats, un phénotype MCH était diagnostiqué chez 41 % (93/229), un phénotype MCR chez 10 % (22/229), un phénotype « myocardiopathie dilatée » (MCD) chez 2 % (4/229), un phénotype « myocardiopathie arythmogène droite » (ARVC) chez 2 % (4/229) et un phénotype « myocardiopathie non spécifique » (MNS) chez 2 % (5/229). Les autres chats étaient atteints de cardiopathies congénitales (n=16) ou d'une discrète insuffisance valvulaire sans conséquence cavitaire (n=90). Parmi ces chats, une consultation de suivi au minimum un mois après le diagnostic initial était disponible chez 49 chats : 80 % (39/49) souffraient de MCH dont 69 % (27/49) d'une forme obstructive de MCH, 12 % (6/49) de MCR, 4 % (2/53) de MCD, 2 % (1/49) d'ARVC et 2 % (1/49) de MNS.
Dans cette population, 28 présentaient des signes cliniques : difficultés respiratoires (n=19), parésie d'un ou plusieurs membres en raison d'un épisode de thromboembolie aortique (TEA, n=4), abattement (n=2), et intolérance à l'effort et au jeu (n=2). Un souffle cardiaque était audible chez 78 % (38/49) et un bruit de galop chez 6 % (3/49) d'entre eux. Lorsqu'il était présent, le souffle cardiaque était de haut grade (4/6) chez 60 % des chats concernés (23/38). Les chats avec souffle de haut grade présentaient majoritairement un phénotype de type MCH obstructif (21/23). Lorsque l'on considère la classification des myocardiopathies du collège américain de médecine interne (ACVIM), 33 % étaient au stade B1 (16/49), 16 % au stade B2 (8/49), et 45 % au stade C (22/49).
La durée médiane du suivi échocardiographique était de 242 jours (intervalle interquartile IQR = 111-484 jours). Un traitement avait été instauré chez 92 % (41/49) des chats suivis. Lors de ce suivi, une normalisation complète des dimensions cavitaires et épaisseurs pariétales a été observée chez 20 % des chats (10/49), confirmant un phénotype MCH ou MCR transitoire. Parmi ces chats avec phénotype transitoire, les lésions correspondaient à un phénotype MCH chez 7 chats, avec obstruction aortique chez 57 % d'entre eux (4/7), un phénotype MCR chez 2 chats et un phénotype ARVC chez un chat. Au sein des chats avec phénotype transitoire, malgré la normalisation des dimensions atriales, ventriculaires et de l'épaisseur pariétale, une inversion des ondes E et A mitrales diastoliques était observée chez 3 chats. Chez les chats ayant présenté un phénotype transitoire, un évènement dans les 15 jours précédant la première présentation était décrit chez 5/10 d'entre eux : stérilisation (n =2), vaccination (n=1), anesthésie (n=1) ou épisode de coryza (n=1). La majorité de ces chats (8/10) étaient au stade C ACVIM, dont 1 présenté pour TEA. Les chats atteints de phénotype transitoire (âge médian = 3,8 ans) étaient significativement plus jeunes que les chats avec phénotype non transitoire (âge médian = 7,9 ans, p=0,009).
Discussion
La majorité des phénotypes transitoires décrits étaient de type MCH (70 %), néanmoins il ne s'agissait pas du seul phénotype rencontré. Les chats atteints étaient majoritairement au stade C, décompensé, avec insuffisance cardiaque pour la majorité, et TEA chez seulement un chat.
Conclusion
Dans cette population, la prévalence des phénotypes était non négligeable (20 %), suggérant l'importance de suspecter ce type d'affection au pronostic excellent, notamment chez des chats jeunes et encourageant l'instauration d'un traitement de l'insuffisance cardiaque.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Étude rétrospective multicentrique et résultats des prothèses ostéointégrées imprimées en trois dimensions en médecine vétérinaire chez le chien et le chat - 18 cas
Guillaume REINSCH
Coauteurs : BOURSIER J.F, RAGETLY G, SANSPOUX F, BASSANINO J, FROIDEFOND B, LAPOUGE M, GODINEAU T, TASSEL A
Introduction
Chez le chien et le chat, lors d'une atteinte du membre nécessitant une amputation, une alternative pour maintenir la longueur du membre peut être à évoquer. Bien que l'amputation soit généralement bien tolérée, peu coûteuse et effectuée dans de nombreux centres vétérinaires, les chiens subissant cette intervention peuvent présenter des pertes d'équilibre lors d'amputation d'un membre antérieur ou une difficulté à courir lors d'amputation d'un membre postérieur.[1] La principale alternative après l'amputation est la mise en place d'une exoprothèse de moignon avec des complications fréquentes comme une inflammation/infection à l'interface peau-prothèse et une ambulation altérée. La mise en place d'une prothèse ostéo-intégrée permet d'obtenir de bons résultats en médecine vétérinaire mais n'a été effectuée que sur des chiens, en cas de pathologie tumorale et par la mise en place d'une prothèse par ancrage impacté seul.[2] Les objectifs de cette étude sont de décrire la faisabilité de la mise en place d'une prothèse ostéo-intégré, imprimée en trois dimensions (3D), associant un système de fixation impacté et verrouillé, chez le chien et le chat. Cette étude permet également de rapporter les indications, les résultats ainsi que les complications de cette technique alternative à l'amputation du membre.
Matériel et méthodes
Tous les dossiers médicaux des chiens et chats ayant été traités chirurgicalement par pose de prothèse ostéo-intégrée depuis 2020 à 2025 dans différents centres vétérinaires ont été examinés. Les critères d'inclusion de l'étude sont l'obtention d'un suivi médical complet, un suivi clinique et radiographique à court terme puis à moyen terme. Un suivi complet à 6 mois est nécessaire.
Résultats
Dix-huit animaux (5 chats et 13 chiens) de 8 centres vétérinaires différents ont répondu aux critères d'inclusion de l'étude. Près d'un tiers des animaux présentaient des tumeurs distales d'un membre et les animaux restants des traumatismes vasculaire et/ou neurologiques de la partie distale d'un membre. Les animaux ont été suivis tous les jours pendant 2 semaines après leur opération puis à la mise en place de l'exoprothèse définitive et à 6 mois post-opératoires. Des radiographies régulières ont été effectuées afin de s'assurer du bon ancrage osseux.
Discussion
La mise en place d'une prothèse ostéointégrée afin de traiter un traumatisme vasculaire, un processus tumoral et/ou neurologique important de la partie distale d'un membre est une solution viable et qui permet une vraie alternative à l'amputation. Les complications mineures sont assez fréquentes en postopératoires, notamment 80 % des animaux ont présenté une infection/inflammation à l'interface peau-prothèse à court/moyen terme, mais elles présentent peu de répercussion clinique et un traitement médical seul permet une régression satisfaisante de l'inflammation/infection à l'interface peau-prothèse. La mise en place d'une prothèse ostéointégrée à double stabilité permet de réduire le risque de fracture au niveau de l'interface os-prothèse, étant donné qu'aucun des animaux n'a présenté de fractures postopératoires tandis qu'un chien sur quatre en a présentées dans le cadre de la mise en place d'une prothèse ostéo-intégré par stabilité press-fit seul. La stabilisation additionnelle par vis verrouillées ajoute un avantage certain et constitue une avancée majeure dans la stabilisation osseuse de la prothèse. Malgré les complications fréquentes et chroniques à l'interface peau-prothèse, qui peuvent perdurer plusieurs mois après la mise en place de la prothèse, les répercussions cliniques sont mineures et à 6 mois post-opératoire, 86 % des propriétaires ont répondu que dans une situation similaire, ils conseilleraient la mise en place de ce type de prothèse ostéointégrée malgré les complications fréquentes et le suivi régulier. Les inconvénients de cette chirurgie sont le délai entre le trauma initial et la pose de la prothèse ce qui implique généralement l'amputation de la zone lésée dans un premier temps afin de soulager l'animal puis la mise en place de la prothèse, le cout de la prothèse, le suivi médical en post-opératoire et en cas de pathologie tumorale, la réalisation d'un bilan d'extension est fortement recommandée afin d'investiguer la présence de potentielles métastases.
Conclusion
La mise en place d'une prothèse ostéointégrée à double stabilité est une chirurgie de sauvetage du membre en cas de trauma ou de tumeurs distales du membre, qui permet une meilleure stabilité grâce à cette nouvelle technologie de double stabilité par méthode press-fit et de verrouillage osseux par vis, utilisable chez les chiens comme chez les chats, présentant régulièrement des complications mais généralement mineures et traitables médicalement. Le pronostic de récupération fonctionnel du membre est généralement très bon, mais un suivi régulier est impératif afin de s'assurer de la bonne intégration osseuse de la prothèse, de prévenir les potentielles complications mineures notamment à l'interface peau-prothèse et de les traiter en conséquence.
Bibliographie
- KIRPENSTEIJN J, VAN DEN BOS R, EDENBURG H: Adaption of dogs to the amputation of a limb and their owners satisfaction with the procedure. Vet Rec 1999;144:115-118
- FITZPATRICK N, SMITH TJ, PENDEGRASS CJ, YEADON R, RING M, GOODSHIP AE, BLUNN GW. Intraosseous transcutaneous amputation prosthesis (ITAP) for limb salvage in 4 dogs. Vet Surg. 2011 Dec;40(8):909-25
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Etude rétrospective sur la prise en charge thérapeutique des carcinomes urétraux par curiethérapie à l'iridium 192 à haute dose et AINS, par AINS seuls ou sans traitement
Jean-Baptiste EON
Coauteurs : Jérôme BENOIT, Christelle MAUREY, Marie BRUTILLE, Jérémy BÉGUIN
Introduction
Les carcinomes urétraux canins sont des cancers localement agressifs associés à un pronostic réservé. Les signes cliniques au diagnostic sont de la dysurie, de la pollakiurie et de l'hématurie et moins fréquemment une obstruction urinaire.
Les options thérapeutiques sont limitées. L'association des anti-inflammatoires non stéroïdiens (AINS) et de la chimiothérapie (vinblastine notamment) permet dans une étude récente d'atteindre une médiane de survie de 333 jours. Les autres options incluent la pose d'une sonde de cystotomie, la pose de stents urétraux (médiane de survie entre 20 et 78 jours) et une cytoréduction au laser. Enfin, la radiothérapie externe est également associée à des résultats décevants avec des médianes de survie faibles entre 70 et 150 jours.
La curiethérapie intraluminale à l'iridium 192, planifiée par ordinateur, permet de placer la source radioactive directement au contact de la tumeur lors du traitement. L'intérêt est d'administrer une radiothérapie à forte dose tout en épargnant les tissus environnants. En raison de l'infiltration diffuse du cancer le long de la paroi urétrale et de la forme tubulaire de l'urètre, cet outil thérapeutique représente une piste de traitement pour les chiens atteints de carcinomes urétraux.
L'objectif de cette étude est de comparer la médiane de survie des chiens traités par curiethérapie, par AINS ou sans traitement et d'évaluer la tolérance et la réponse clinique des chiens traités par curiethérapie.
Matériels et méthodes
Les dossiers médicaux de 2 structures de référés ont été examinés rétrospectivement. Les critères d'inclusion comprenaient les chiens avec un diagnostic cytologique ou histologique de carcinome localisé a minima à l'urètre. Les cas traités par radiothérapie externe sans curiethérapie associée ont été exclus de l'étude.
Les chiens ont été classés en fonction de leur traitement : groupe 1 (curiethérapie, AINS +/- chimiothérapie), groupe 2 (AINS) et groupe 3 (absence de traitement). Les données cliniques et thérapeutiques ont été collectées. La médiane de survie est définie par la durée entre le diagnostic de la tumeur et la date de décès ou de censure. La date de censure correspond soit à la date du dernier suivi si l'animal est encore en vie, soit à la date de perte de vue si l'animal n'est plus suivi et pas encore déclaré décédé. L'analyse statistique a été réalisée à l'aide du test du Log-rank et du KAPLAN-MEIER entre les différents groupes.
Résultats
- 45 chiens ont été inclus dans l'étude (groupe 1 : 27 chiens, groupe 2 : 11 chiens, groupe 3 : 7 chiens). Parmi les 27 chiens traités dont le suivi était disponible à 1 mois, une réponse clinique complète ou partielle a été observée chez 21 et 4 chiens respectivement, soit un taux de réponse de 92,5 %.
- Les médianes de survie pour le groupe 1, le groupe 2 et le groupe 3 étaient respectivement de 197 jours (11-1097), 128 jours (10-300) et 97 jours (0-111), avec une différence significative entre le groupe 1 et 3. Cependant, aucune différence significative n'a été vue entre le groupe 1 et 2. Parmi le groupe 1, la médiane de survie des chiens ayant reçu une dose totale de plus de 40 Gy n'était pas significativement différente de ceux ayant reçu une dose de moins de 40 Gy (197 vs 98 jours).
- Sur les 27 chiens traités par curiethérapie, 6 sont décédés à cause de la tumeur, 1 chien pour une autre cause non liée à la tumeur et 10 chiens d'une cause inconnue.
Discussion
Il s'agit de la première description de l'utilisation de la curiethérapie intraluminale dans le traitement des carcinomes urétraux. Une amélioration clinique a été observée dans la presque totalité des cas, ce qui équivaut au résultat des animaux suivis par chimiothérapie. Une médiane de survie de 197 jours est observée, ce qui reste statistiquement supérieur à la médiane de survie sans traitement (97 jours). Cette étude présente des limites principalement dues à son caractère rétrospectif. Les protocoles de traitement ne sont pas standardisés et certains animaux du groupe 1 ont reçu des traitements supplémentaires avec de la chimiothérapie et de la radiothérapie externe.
Le traitement par curiethérapie a montré une bonne tolérance sans effets secondaires associées. Aucun animal n'est décédé en raison du traitement.
Conclusion
Cette étude montre une amélioration marquée des signes cliniques dans la quasi-totalité des cas, suggérant une amélioration de la qualité de vie des chiens atteints de carcinome urétral. La médiane de survie atteinte est de 197 jours pour les chiens traités par curiethérapie pour 98 jours pour les chiens sans traitement. Cette étude suggère que la curiethérapie pourrait être une option thérapeutique intéressante dans la prise en charge du carcinome urétral. De nouvelles études prospectives sont attendues.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Évaluation d'un algorithme d'IA pour la détection des lignes B chez le Chien atteint d'œdème pulmonaire cardiogénique : SMART DOG study
Paris, France
I. Introduction
L'œdème pulmonaire cardiogénique (OPC) est une complication fréquente et grave de l’insuffisance cardiaque chez le chien, caractérisée par une accumulation de liquide dans les poumons. L’échographie thoracique réalisée au chevet du patient (POCUS) permet de détecter rapidement ce liquide à travers l’identification de lignes B. Toutefois, cette interprétation reste subjective et dépend fortement de l’expérience de l’opérateur. L’intelligence artificielle (IA) pourrait offrir une alternative standardisée, reproductible et rapide, mais son usage en médecine vétérinaire reste encore peu documenté.
Cette étude visait à évaluer la capacité d’un système d’échographie intégrant une IA à détecter et compter automatiquement les lignes B en temps réel chez le chien, et à comparer les résultats obtenus avec ceux de cliniciens expérimentés.
L’hypothèse était que l’algorithme d’IA serait capable de compter précisément les lignes B et que les résultats obtenus par cet algorithme seraient en forte concordance avec ceux des vétérinaires.
II. Matériels et méthodes
1. Population étudiée
Une étude prospective a été menée dans un centre hospitalier vétérinaire de référence entre novembre 2024 et mars 2025. Vingt chiens présentant des signes d’œdème pulmonaire cardiogénique ont été inclus, selon les critères suivants : examen clinique évocateur, plus de trois lignes B par champs pulmonaire au POCUS, rapport Ag:Ao ≥ 1,6:1 et amélioration clinique après administration de furosémide. Un groupe contrôle de 20 chiens sains sans signes respiratoires a également été constitué. Ces chiens ne présentaient pas d’antécédents cardio-respiratoires, avaient un examen clinique normal, un rapport Ag:Ao <1,6:1 et <3 lignes B par champs pulmonaire au POCUS.
2. Protocole échographique
L’échographie pulmonaire (POCUS) a été réalisée par un résident en urgences et soins intensifs formé au POCUS. L’examen a été effectué avec une sonde convexe (1–12 MHz) en position debout ou en décubitus latéral, sans tonte mais avec de l’alcool. Huit zones thoraciques ont été explorées selon le protocole Vet BLUE : région caudodorsale, périhilaire, moyenne et crâniale sur chaque hémithorax. À chaque zone, un clip échographique de 6 secondes a été enregistré.
3. Comptage des lignes B
Un algorithme d’IA (Auto B-line Counter, Butterfly Network) a été utilisé pour détecter et compter automatiquement les lignes B. L’IA signalait le nombre maximal de lignes B visibles par clip vidéo, avec un affichage visuel immédiat et une catégorisation (de 0 à >5 lignes). Tous les clips vidéos ont ensuite été anonymisés et relus de manière rétrospective par deux évaluateurs humains (un spécialiste ECVECC et un résident ECVECC formé au POCUS), à l’aveugle des résultats l’un de l’autre et de l’IA.
4. Analyse statistique
Les variables démographiques (âge, poids) ont été comparées entre groupes par le test de Mann-Whitney. La performance de l’IA a été évaluée par le taux de réussite du comptage, le nombre de tentatives nécessaires, et la comparaison des comptages avec ceux des opérateurs humains.
La concordance a été mesurée par le coefficient de corrélation intra-classe (ICC) pour les comptages bruts et la classification binaire (pathologique : > 3 lignes B vs normal : ≤ 3 lignes B). L’exactitude, la valeur prédictive positive (VPP), la valeur prédictive négative (VPN) et le taux de mauvaise classification ont été calculés, avec l’opérateur le plus expérimenté comme référence.
III. Résultats
1. Description démographique
Le groupe témoin avait une médiane d’âge de 8 ans (1,2–16,2 ans ; intervalle interquartile [IQR] : 4,7–10,4 ans). Le poids corporel médian était de 20,4 kg (2,8–72 kg ; IQR : 8,5– 33,0 kg). Les races étaient les suivantes :
- 3 Cavalier King Charles Spaniels
- 2 chiens de race mixte
- 2 Labrador Retrievers
- et un individu de chacune de ces races : Golden Retriever, Cocker Spaniel, Griffon, Grand Danois, American Staffordshire Terrier, Boxer, Pékinois, Teckel, Bulldog Français, Pinscher Miniature, Shiba Inu, Berger Allemand et Chihuahua.
Le groupe OPC avait une médiane d’âge de 11,5 ans (7,3–14,8 ans ; IQR : 10,2–12,8 ans), et un poids corporel médian de 6,7 kg (1,9–10,9 kg ; IQR : 5,0–8,6 kg). Les races étaient les suivantes :
- 7 Cavalier King Charles Spaniels
- 5 Chihuahuas
- 2 chiens de race mixte
- 2 Bichons Maltais
- et un individu de chacune de ces races : Pékinois, Caniche Toy, Shih Tzu et Bulldog Français.
Les chiens du groupe OPC étaient significativement plus âgés (p = 0,001379) et plus légers (p = 0,002164) que ceux du groupe témoin sain.
2. Taux de répétition et performance de l’IA
L’algorithme IA a fourni un comptage dans 100 % des cas. Cependant, un échec initial du comptage a été observé dans 14,2 % des clips vidéo, et plus fréquent dans le groupe OPC (11,8 %) que chez les témoins (2,4 % ; OR = 4,88, p < 0,0001).
Dans le groupe sain, 70 % des clips vidéo ont bénéficié d’un comptage par l’IA dès la première tentative, contre 55 % dans le groupe OPC. Dans ce groupe OPC, 35 % des clips vidéo ont nécessité trois tentatives ou plus, avec certains chiens requérant jusqu’à 13 tentatives.
3. Comptage des lignes B et concordance
Sur 320 clips vidéo, 4 (1,2 %) ont été exclus par l’opérateur 1 et 6 (1,9 %) par l’opérateur 2 pour mauvaise qualité du clip vidéo.
L’ICC entre les deux opérateurs et l’IA était de 0,88 pour le comptage absolu et de 0,85 pour la classification binaire (> 3 vs ≤ 3 lignes B).
L’IA a obtenu une exactitude de 84 % par rapport à l’opérateur 1 et de 86 % par rapport à l’opérateur 2 pour la détection des profils pathologiques.
Comparée à l’opérateur 1 (référence), l’opérateur 2 présentait une VPP de 78,8 %, une VPN de 92,2 % et un taux de mauvaise classification de 11,4 %. L’IA affichait une VPP de 75,0 %, une VPN de 86,3 % et un taux de mauvaise classification de 16,1 %.
IV. Discussion
Cette étude a évalué les performances en temps réel d’un algorithme d’intelligence artificielle (IA), initialement développé à partir de données humaines, pour la détection des lignes B chez des chiens suspects d’œdème pulmonaire cardiogénique (OPC). En le comparant à des cliniciens vétérinaires expérimentés, les résultats ont mis en évidence une excellente concordance, tant pour le comptage absolu (ICC = 0,88) que pour la classification binaire (ICC = 0,85). Cette classification simplifiée, déjà couramment utilisée en médecine humaine, semble particulièrement adaptée au contexte vétérinaire d’urgence où des décisions rapides sont nécessaires.
Plusieurs éléments peuvent expliquer ces performances élevées : l’homogénéité de la population étudiée (OPC suspecté uniquement), l’absence de pathologies pulmonaires confondantes comme des consolidations et la relative clarté des images obtenues, en dépit des défis liés à l'espèce (morphologie, mouvement respiratoire). L’utilisation d’opérateurs expérimentés et d’un protocole standardisé a probablement renforcé la fiabilité des analyses.
Cependant, l’algorithme présente certaines limites : un taux d’échec du comptage initial de 14,2 % des clips vidéo a été observé, plus fréquent chez les chiens avec OPC suspecté. Il est possible que l’IA soit moins performante face à des champs pulmonaires présentant des anomalies marquées, telles que des irrégularités pleurales ou des artéfacts confluents, ce qui suggérerait la nécessité d’un affinement de l’algorithme afin de mieux distinguer les véritables signes pathologiques (lignes B) des artéfacts visuels parasites (lignes E, I, Z). De plus, les chiens du groupe OPC étaient significativement plus petits et plus légers, ce qui pourrait rendre le contact entre la sonde et la cage thoracique plus difficile, en particulier dans un contexte de détresse respiratoire où l’animal est agité ou dyspnéique. Ces conditions peuvent altérer la qualité des vidéos acquises et compliquer l’interprétation automatisée par l’IA. Enfin, l’algorithme a également présenté un taux modéré de fausses classifications (jusqu’à 16,1 %) et une valeur prédictive positive (VPP) de 75 %, traduisant une tendance au surdiagnostic. Si cela peut se révéler prudent en médecine d’urgence, cela souligne néanmoins la nécessité d’adapter l’algorithme aux spécificités anatomiques et physiopathologiques des patients vétérinaires afin d’éviter des interventions inutiles.
Les performances globales de l’IA (exactitude : 84–86 %, VPN : 86,3 %) confirment son potentiel comme outil d’aide à la décision, notamment pour exclure une pathologie significative. Néanmoins, une validation plus large, intégrant une plus grande diversité de cas, de tailles, de races et de conditions pulmonaires, est nécessaire. La prise en compte de facteurs techniques comme l’orientation de la sonde, le protocole échographique utilisé ou la conformation thoracique pourrait aussi optimiser l’interprétation des images par l’algorithme.
V. Conclusion
L’algorithme d’IA testé révèle une très bonne concordance avec des cliniciens expérimentés, tant pour le comptage que pour la détection des profils pulmonaires pathologiques liés à l’OPC. Ces résultats soutiennent l’intérêt potentiel de l’IA comme outil d’aide à la décision pour la détection de l’OPC en médecine vétérinaire d’urgence et de soins intensifs. Son déploiement clinique nécessite encore un entraînement spécifique sur des données animales et une évaluation plus large pour garantir robustesse, fiabilité et sécurité dans des contextes variés.
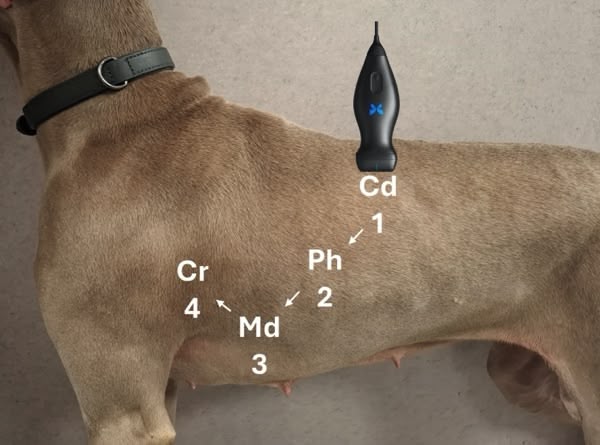
Figure 1
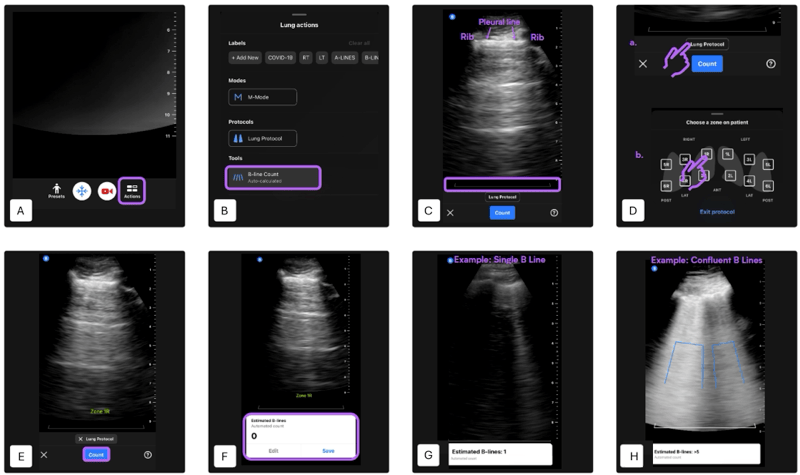
Figure 2
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Évaluation de l'étanchéité intestinale après réalisation de biopsies étagées sans suture à l'aide d'une aiguille à biopsie automatique
Meaux, France
Meaux, France
Meaux, France
I. Introduction
Les biopsies intestinales étagées sont couramment réalisées en médecine vétérinaire, à des fins diagnostiques. Pour une évaluation histologique fiable, des biopsies de pleine épaisseur sont souvent requises, permettant ainsi de distinguer diverses maladies intestinales chroniques, telles que les maladies inflammatoires intestinales (lympho-plasmocytaire, éosinophilique ou neutrophilique), la lymphangiectasie ou encore le lymphome intestinal. Les biopsies en épaisseur partielles obtenues par endoscopie offrent une précision diagnostique moindre comparée aux biopsies de pleine épaisseur. Traditionnellement, les biopsies intestinales sont réalisées par une technique incisionnelle. Récemment, la réalisation de biopsies intestinales en pleine épaisseur à l’aide d’une aiguille semi-automatique de 16 G a été décrite dans la littérature chez le chien et le chat. Cette technique est associée à une très bonne précision des résultats histologiques et un temps chirurgical minoré.
II. Objectifs
Le but de la présente étude est d’étudier les pressions de fuites intestinales obtenues après une biopsie à l’aiguille automatique de 16 G, sans suture du site. Nous supposons que la pression intraluminale de fuite, sera supérieure à la pression maximale intraluminale physiologique, décrite de 6 mmHg.
III. Matériels et méthode
Les tests sont effectués de façon prospective, sur des chiens et des chats subissant une entérectomie pour des raisons indépendantes de l’étude (masse digestive, corps étranger, perforation). Lors de l’intervention chirurgicale, des biopsies sont prélevées sur des tissus macroscopiquement sains, en partie orale et aborale de la lésion nécessitant l'entérectomie. La procédure de biopsie suit la même méthode que celle précédemment décrite par Maggiar et al. [2024]. Après le prélèvement, les sites d'échantillonnage de 1,3 mm sont laissés intacts sans fermeture et isolés par 2 pinces de Doyens. Deux cathéters de calibre 18 sont ensuite insérés dans la lumière intestinale. Dans le premier, une solution saline colorée d’une faible quantité de bleu de méthylène est perfusée à un débit de 500 ml/h, tandis que la pression intraluminale est enregistrée à l'aide d'un transducteur connecté au second cathéter. Les pressions de fuite initiales sont mesurées dans les deux zones de test. Enfin, le liquide de remplissage est aspiré et une entérectomie est pratiquée, enlevant la lésion primaire ainsi que les deux sites de biopsie. Ces mesures seront comparées à la pression intraluminale intestinale physiologique, précédemment rapportée chez le chien à 6 mmHg.
Cette étude est validée par le Comité d’Éthique Jacques Bonnod de VetAgro Sup (N° 2503).
IV. Résultats
Trois chats et 2 chiens sont inclus pour un total de 10 mesures de pression. La moyenne des valeurs obtenues est de 60,5 mmHg avec un écart-type de 29,9 mmHg. Ces valeurs sont nettement supérieures à la pression intraluminale physiologique décrite chez le chien et le chat, evaluée à 6 mmHg. Une analyse de puissance réalisée pour un test t à un seul échantillon a permis d’évaluer la capacité statistique des données actuelles. Avec une taille d’effet estimée à 1,78, un échantillon de cinq sujets offre une puissance de 84,24 %. Toutefois, afin d’assurer une meilleure fiabilité et le potentiel d'extrapolation des résultats, un échantillon de dix sujets sera considéré comme optimal.
V. Discussion
Cette étude évalue l’étanchéité intestinale après biopsie sans fermeture du site de prélèvement. Les premiers tests sur cadavres suggéraient une étanchéité insuffisante, tandis que les résultats préliminaires sur animaux vivants montrent que la fermeture pourrait ne pas être nécessaire. Les pressions mesurées dépassent largement la pression physiologique moyenne, et aucune fuite n’a été observée en dessous de 26 mmHg. Les biopsies intestinales sont actuellement réalisées par laparotomie, une procédure invasive et exclusivement diagnostique. Si nos résultats sont confirmés sur un échantillon plus large, ils pourraient ouvrir la voie à des techniques de prélèvement moins invasives (percutanées, laparoscopiques, éventuellement échoguidées). Ces techniques pourraient réduire le temps opératoire, anesthésique et la douleur post-opératoire.
VI. Conclusion
Les résultats préliminaires indiquent que la pression de fuite après biopsie intestinale à l’aiguille automatique est supérieure à la pression physiologique intestinale du chien et du chat. Le risque de fuite digestive pourrait ainsi être faible, même sans fermeture chirurgicale du site. Cependant, la variabilité des pressions mesurées souligne la nécessité de confirmer ces données sur un échantillon plus large et d’évaluer la tolérance clinique à long terme de cette approche.
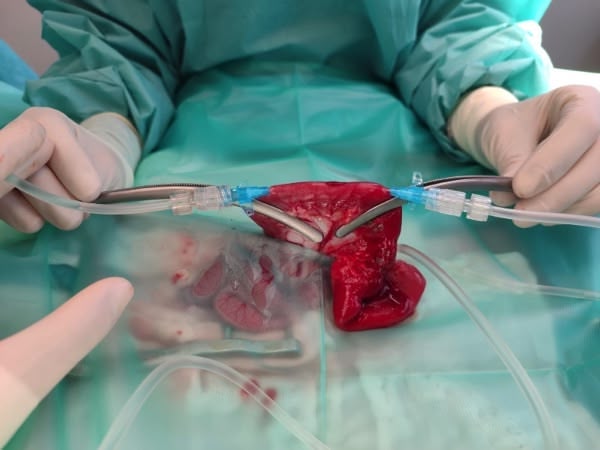
Figure 1
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Evaluation de l'oreille : comment établir un score OTIS-3
Toulouse, France
I. Introduction
Évaluer objectivement l’état lésionnel, que ce soit cutané ou auriculaire, demeure un défi. Les sensibilités peuvent varier entre les évaluateurs et pourtant ces scores lésionnels permettent de suivre objectivement un patient, évaluer la gravité de son affection ou tout simplement l’efficacité du ou des traitements mis en place.
Les scores lésionnels existent depuis de plusieurs années chez l’Homme pour le suivi de la dermatite atopique et a été plus récemment développé chez le chien (Score CADESI chez le chien) ou encore chez le chat (SCORFAD).
Concernant l’oreille, les différentes études ont longtemps utilisé des critères variés, quantitatifs ou semi-quantitatifs, tels que l’érythème, la douleur, le prurit, l’odeur, les sécrétions, la cytologie ou encore la culture.
II. Le score OTIS-3
En 2014, un nouveau score clinique validé a été proposé pour caractériser les otites chez le chien. Il s’agit du score OTIS-3 (Otitis Index Score). Ce score a été établi sur la base de sa validité, sa reproductibilité et de sa fiabilité. [1]
1. Paramètres du score
Quatre paramètres ont été retenus : (Figure 1)
- L’érythème
- L’hyperplasie
- Les sécrétions
- Les ulcères
Chacun de ces critères est évalué de 0-3 pour obtenir une note finale comprise entre 0 et 12 (figure 1).
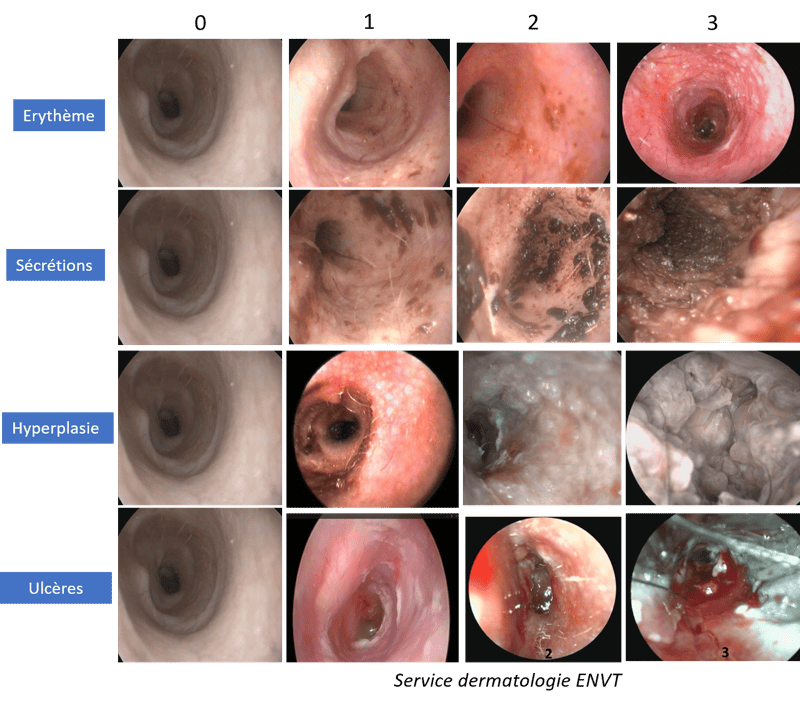
Figure 1
2. Interprétation du score
L’animal ayant un score total supérieur ou égal à 4 présente systématiquement une otite avec une spécificité de 100 %.
Un score inférieur à 4 définit une oreille normale avec une sensibilité de 91,1 % et une spécificité de 100 %.
3. Modalités de cotation
Il n’y a pas d’intérêt à distinguer le scoring du conduit vertical versus le conduit horizontal. Utiliser une seule cotation permet un examen plus rapide et tout aussi fiable.
4. Critères non retenus
Des critères tels que le prurit et la douleur n’ont pas été retenus. Ces derniers peuvent varier d’un individu à l’autre et ne pas être représentatifs de la gravité de l’otite.
III. Conclusion
Ce score permet donc d’évaluer la gravité de l’otite, de réaliser son suivi et constitue une évaluation objective de l’efficacité d’un traitement.
Bibliographie
- Nuttall T, Bensignor E. A pilot study to develop an objective clinical score for canine otitis externa. Veterinary dermatology. 2014;25(6):530-7, e91-2.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Evaluation des performances diagnostiques de la bandelette urinaire pour la détection d'une protéinurie douteuse ou pathologique chez le chat
Élise POSTIC
Coauteurs : A. BERTIN, B. REYNOLDS, C. TRUMEL, R. LAVOUÉ
Introduction
Les maladies rénales chroniques sont des affections communément diagnostiquées dans l'espèce féline, avec une prévalence estimée de 30 à 80 % chez l'animal de plus de 10 ans. La recherche d'une protéinurie et sa quantification sont essentielles lors de maladie rénale chronique (MRC) chez le chat, et ce d'autant plus qu'une protéinurie douteuse (PD) et pathologique (PP) ont été identifiées comme facteurs pronostiques lors de MRC féline. Ce constat renforce la nécessité et l'importance d'un dépistage précoce de la protéinurie. Bien que la bandelette urinaire (BU) soit le test le plus couramment utilisé pour dépister une protéinurie, sa fiabilité est controversée dans l'espèce féline et peu d'études incluant une quantité importante de chats se sont penchées sur le sujet.
Les objectifs de cette étude sont ainsi d'évaluer la fiabilité et les performances diagnostiques de la BU pour identifier une PD et une PP, en utilisant le rapport protéine/créatinine urinaire (RPCU) comme méthode de référence, dans un échantillon important de chats.
Matériel et résultats
Ont été collectés les résultats de chats ayant fait l'objet d'une analyse d'urine complète, incluant l'évaluation de la densité urinaire (DU) au réfractomètre, la réalisation d'une BU dont l'ensemble des résultats étaient disponibles, la détermination d'un RPCU. Les dossiers incomplets pour ces variables ont été exclus. Les données épidémiologiques et cliniques de chaque cas ont également été enregistrées. La fiabilité (méthode du k de Cohen) la sensibilité et la spécificité (logiciel Référence Value Advisor) des différents seuils de la BU pour la plage protéines ont été calculées pour l'ensemble des données et pour les échantillons répartis selon la DU (≤1,012, [1,013-1,034] ou ≥1,035). Un RPCU supérieur à 0,2 et à 0,4 indiquait respectivement une PD ou une PP.
Ainsi, 501 échantillons provenant de 293 chats ont été inclus. Le RPCU a identifié une PD et une PP dans respectivement 20 % et 44 % des échantillons. L'accord global entre la BU et le RPCU était faible à modéré (k compris entre 14 % et 39 %). La sensibilité la plus élevée de la BU pour identifier une PP a été atteinte avec des scores ≥1+ et une DU ≥1,035 (Se=97 %, Sp=8 %), tandis que la spécificité la plus élevée a été obtenue pour un score ≥2+ avec une DU ≤1,012 (Sp=100 %, Se=30 %). La sensibilité la plus élevée pour la PD a été trouvée avec un score ≥1+ et une DU ≥1,035 (Se=94 %, Sp=8 %), et la spécificité la plus élevée pour des scores ≥2+ avec une DU ≤1,012 (Sp=100 %, Se=27 %) et ≥3+ avec une DU ≥1,035 (Sp=100 %, Se=30 %). La sensibilité et la spécificité variaient de 18 % à 90 % et de 37 % à 100 %, respectivement, dans les échantillons ayant une DU [1,013-1,034].
Conclusion
Cette étude met en évidence une faible fiabilité de la BU pour dépister une protéinurie douteuse ou pathologique chez le chat. Contrairement aux données publiées chez le chien, la bandelette urinaire possède des performances diagnostiques médiocres dans l'espèce féline, notamment pour les densités urinaires les plus souvent retrouvées en cas de MRC. Il est vraisemblable que la nature principalement tubulo-interstitielle des néphropathies retrouvées chez le chat, et à l'origine d'une protéinurie de faible amplitude, soit l'une des raisons des résultats présentés ici. Chez les chats considérés à risque de protéinurie, dont la densité urinaire est entre 1,013 et 1,034, le RPCU devrait être systématiquement déterminé.
Bibliographie
- BARCHILON M., PEREZ-NIEVES N., PALERME JS., 2024. Evaluation of a urine dipstick protein to urine specific gravity ratio for the detection of proteinuria in dogs and cats. J Vet Intern Med. 38(2):1060-1067. doi: 10.1111/jvim.17001
- FIDALGO MA., LEAL RO., DUARTE-CORREIA JH., 2022. Urinary Protein/Creatinine Ratio in Feline Medicine: Reasons to Perform It and Its Role in Clinical Practice-A Retrospective Study. Animals (Basel). 12(12):1575. doi: 10.3390/ani12121575
- LÓPEZ MC., AYBAR V., ZATELLI A., VILA A., VEGA JJ., HERNANDO E., JIMÉNEZ A., ROURA X., 2021. Is proteinuria a rare condition in apparently healthy and sick cats. A feline practice experience (2007-2018). Open Vet J. 11(3):508-516. doi: 10.5455/OVJ.2021.v11.i3.24
- MORTIER F., DAMINET S., MARYNISSEN S., VERBEKE J., PAEPE D., 2025. Clinical importance of borderline proteinuria in nonazotemic cats and evaluation of other risk factors for the development of chronic kidney disease. J Vet Intern Med. 39(1):e17257. doi: 10.1111/jvim.17257
- ZATELLI A., PALTRINIERI S., NIZI F., ROURA X., ZINI E., 2010. Evaluation of a urine dipstick test for confirmation or exclusion of proteinuria in dogs. 71(2):235-40. doi: 10.2460/ajvr.71.2.235
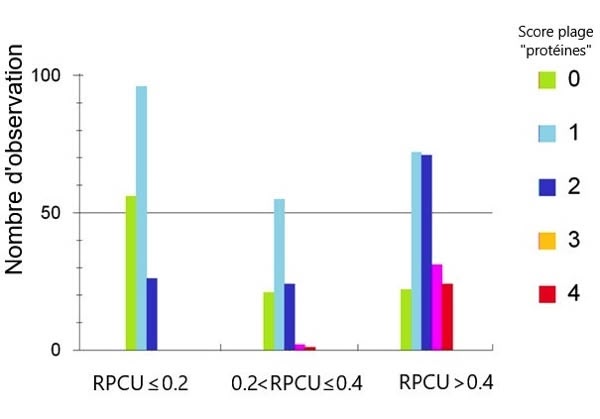
Figure 1
Répartition des scores de protéinurie à la bandelette urinaire (BU) en fonction du rapport protéine/créatinine urinaire (RPCU)
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Génétique et cancer : où en est-on ?
I. Introduction
L’origine génétique de certains cancers chez le chien est désormais bien établie. Certaines races présentent des prédispositions génétiques connues, avec des régions chromosomiques identifiées pour quelques tumeurs rares, comme le sarcome histiocytaire chez le Bouvier Bernois. Outre ces mutations prédisposantes, des mutations acquises s’accumulent au cours de la vie et contribuent également au développement de cancers. Ces mutations acquises commencent à être caractérisées chez le chien et sont exploitées à des fins diagnostiques (par exemple, mutation du gène BRAF), pronostiques, ou thérapeutiques (mutation du gène KIT et traitements par inhibiteurs ciblés). Cette présentation fait le point sur l’état actuel des connaissances concernant l’origine génétique du cancer chez le chien et ses implications diagnostiques, pronostiques et thérapeutiques potentielles.
1. Objectifs pédagogiques
Comprendre l’intérêt des mutations génétiques associées aux cancers chez le chien, qu’il s’agisse de prédispositions raciales ou de mutations ayant des conséquences diagnostiques ou thérapeutiques.
2. Le cancer, une maladie génétique
Le développement d’une tumeur résulte de l’accumulation de mutations qui touchent des gènes régulateurs de la prolifération, de la survie cellulaire, et de l’intégrité du génome, au sein d’une cellule de l’organisme. Ces gènes clés dans la cancérogénèse sont répartis en deux catégories : les gènes suppresseurs de tumeurs et les oncogènes. Ces mutations permettant la transformation en cellule tumorale concernent des gènes impliqués dans des voies clés. Elles confèrent à la nouvelle cellule tumorale de nouvelles capacités biologiques, ces caractéristiques du cancer sont appelées « cancer hallmarks » [1] (Figure 1). Chez l’Homme comme chez le chien, la majorité des cancers sont des maladies multifactorielles impliquant des facteurs de prédisposition et des facteurs environnementaux favorisant l’apparition de mutations au cours de la vie de l’individu, que l’on appelle mutations somatiques.
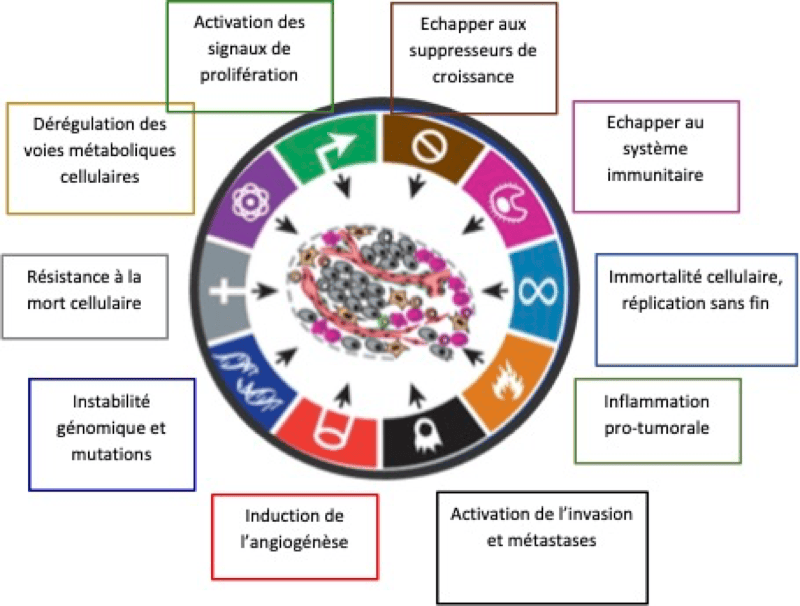
Figure 1
II. Les mutations et leurs intérêts en médecine vétérinaire
1. Les mutations prédisposantes
L’apparition de certains cancers est parfois favorisée par des mutations prédisposantes, dites « germinales », transmises de génération en génération et réduisant le nombre d’étapes nécessaires à la transformation tumorale. Ces mutations expliquent les nombreuses prédispositions raciales observées pour certains cancers spécifiques (cf. Tableau 1). Des études génétiques, menées à la fois intra- et inter-races, ont permis d’identifier des régions prédisposantes pour de nombreux cancers tels que le lymphome, l’hémangiosarcome, le mastocytome, le gliome ou encore le carcinome gastrique. Ces travaux ont montré que la prédisposition à un cancer est le plus souvent liée à l’accumulation de plusieurs régions prédisposantes et que certaines d’entre elles sont communes à différents types de cancers.
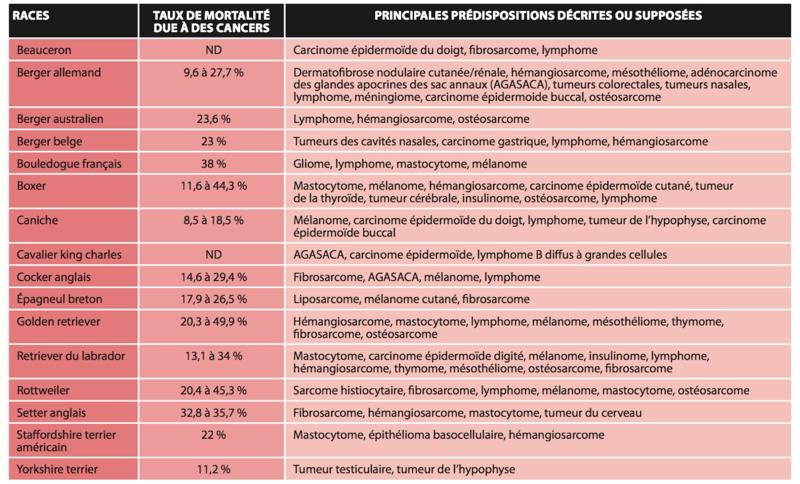
Tableau 1
Ces informations sont particulièrement utiles pour les éleveurs : elles pourraient être exploitées dans des programmes de sélection génétique afin d’écarter les reproducteurs porteurs de risques, d’identifier les individus susceptibles de développer une maladie de façon précoce (et qui pourraient bénéficier d’un dépistage adapté), et de définir des marqueurs potentiels pour prévenir ou réduire le risque de cancer.
Cependant, à l’heure actuelle, à l’exception du test génétique de risque pour le sarcome histiocytaire développé par le laboratoire Antagene et destiné à la sélection des reproducteurs dans la race Bouvier Bernois, la recherche fondamentale n’a pas encore conduit à des applications concrètes pour les éleveurs.
2. Les mutations somatiques
Les altérations somatiques correspondent à des modifications du génome apparues au cours du développement tumoral. Elles sont présentes dans l’ADN de la tumeur mais absentes de l’ADN sain de l’individu. Grâce aux récentes avancées du séquençage, certaines altérations spécifiques à des cancers humains, et récurrentes entre individus atteints, ont pu être identifiées.
Ces marqueurs somatiques ont quatre fonctions majeures :
- aide au diagnostic,
- valeur pronostique,
- orientation du choix thérapeutique,
- suivi du patient.
Ainsi, de l’ADN tumoral circulant est relargué dans le plasma des patients et peut être utilisé comme outil diagnostique non invasif, dans ce que l’on appelle une biopsie liquide. Cette approche est particulièrement pertinente pour les cancers hématopoïétiques tels que le lymphome, l’hémangiosarcome ou le sarcome histiocytaire, qui libèrent de grandes quantités d’ADN tumoral circulant. Dans le cas du sarcome histiocytaire, la détection de cet ADN tumoral peut précéder le diagnostic clinique d’environ six mois, ouvrant la voie à un dépistage précoce… L’ADN tumoral peut également être détecté dans d’autres liquides biologiques. Par exemple, pour les carcinomes urothéliaux et prostatiques, le test de dépistage des mutations BRAF à partir des sédiments urinaires chez le chien est déjà largement utilisé, avec une sensibilité pouvant atteindre 85 % et une spécificité proche de 100 %. Ce test permet de confirmer un diagnostic sans recourir à des biopsies tissulaires invasives.
Ces mutations somatiques offrent aussi la possibilité d’identifier de nouvelles cibles thérapeutiques et de sélectionner les patients susceptibles de répondre à un traitement donné. Un exemple emblématique est celui du mastocytome canin, dans lequel des mutations activatrices du gène KIT, codant pour le récepteur tyrosine kinase c-kit, ont été décrites. Normalement, ce récepteur est activé par le Stem Cell Factor (SCF), qui déclenche une cascade de signalisation contrôlant prolifération, motilité et survie cellulaire. Lorsqu’il est muté, le récepteur est activé de façon constitutive, indépendamment du SCF. Ces mutations, présentes dans 30 à 55 % des mastocytomes de grade II-III (classification de Patnaik) ou de haut grade (classification de Kiupel), sont associées à un phénotype tumoral plus agressif et à un pronostic défavorable. Elles constituent aujourd’hui un facteur pronostique reconnu, complémentaire aux systèmes de grading histologique. Elles orientent également le traitement : le masitinib (MASIVET®, AB SCIENCE, France), inhibiteur de KIT autorisé en Europe pour les mastocytomes canins non résécables, prolonge significativement le délai de progression chez les chiens porteurs d’un mastocytome muté (241 jours vs 141 jours en moyenne).
En combinant les données de séquençage à grande échelle issues du cancer canin avec les dossiers cliniques et les résultats de suivi, il sera possible d’identifier de nouveaux facteurs prédictifs du pronostic. Un autre intérêt majeur des approches génétiques est la simplification des procédures de stadification et le suivi mini-invasif des récidives. Plusieurs applications commerciales de ces technologies commencent déjà à émerger en médecine vétérinaire, tant pour le dépistage que pour la caractérisation moléculaire des tumeurs et l’identification de cibles thérapeutiques. Ces tests sont prometteurs en oncologie clinique et faire entrer la médecine vétérinaire dans l’ère de la médecine personnalisée.
Il faut toutefois garder à l’esprit que les données disponibles restent limitées chez l’animal de compagnie. Des études de validation à long terme sont encore nécessaires pour confirmer la robustesse et la précision de ces tests.
III. Conclusion : vers une médecine personnalisée en oncologie vétérinaire
Avec les progrès de la génétique, la caractérisation moléculaire des tumeurs devient une étape indispensable pour guider le choix thérapeutique. Pour l’instant, l’accès à ces outils en médecine vétérinaire reste limité, en raison de leur coût et de leur disponibilité restreinte à quelques centres spécialisés, principalement aux États-Unis.
Cependant, l’émergence de laboratoires proposant des services de diagnostic de cancers par biopsie liquide, capables d’identifier des marqueurs moléculaires utiles au diagnostic, au pronostic et au choix thérapeutique, ouvre la voie à une intégration progressive de ces outils dans la pratique clinique.
À terme, la constitution de bases de données cliniques et génétiques permettra d’affiner les prédictions et de renforcer la fiabilité de ces approches. Il est probable que ces techniques s’intègrent progressivement dans la prise en charge des cancers en médecine vétérinaire en Europe et en France dans les années à venir.
Bibliographie
- HANAHAN, D. & WEINBERG, R. A. Hallmarks of cancer: the next generation. Cell 144, 646–674 (2011).
- HÉDAN Benoît. Cancer chez le chien: prédispositions raciales et formes familiales. Le Point vétérinaire 54–62 (2015).
- ARENDT, M. et al. Genetics of canine cancer: a guide for the veterinary oncologist. Veterinary Oncology (2025) 2:9
- https://antagene.com/pdf/explications_test_SH.pdf
- https://igdr.univ-rennes.fr/cani-dna-oncodiagnostic
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Gérer un animal paralysé à la maison, confort/hygiène générale, contrôle des mictions, quand et comment appareiller
La Madeleine, France
I. Introduction
La paralysie temporaire ou définitive chez le chien ou le chat implique une réorganisation complète de la gestion quotidienne de l’animal à domicile par le propriétaire. Un accompagnement vétérinaire rigoureux et l’implication du propriétaire sont essentiels pour maintenir la qualité de vie, l’hygiène, prévenir les complications secondaires et favoriser la récupération fonctionnelle.
II. Confort et hygiène
1. L’importance du couchage
Le couchage de l’animal doit réduire les points de pression et prévenir les escarres. Un matelas épais, idéalement à mémoire de forme ou orthopédique, est recommandé. Le propriétaire peut disposer de plusieurs housses afin de faire un roulement lors des nettoyages en machine. L’utilisation de Drybed/vetbed ou d'alèses peut être particulièrement intéressante.
Un changement régulier de position (au moins toutes les 4 h) est crucial pour éviter les escarres, qui peuvent survenir dans 19 % des cas après une hernie discale (Gouveia et Al, 2023). Les chiens à risque accru d’escarres sont les animaux maigres, à peau fine et reliefs osseux proéminents (ex : Greyhound et Whippets). La peau doit être vérifiée plusieurs fois par jour avec une attention particulière sur les rougeurs en regard des points de contact (hanches, coudes, jarrets). Il faut mettre l'animal en position sternale plusieurs fois par jour, en le calant avec des serviettes roulées ou des coussins.
2. Toilettage et hygiène cutanée
Le nettoyage régulier est indispensable pour prévenir les dermatites urineuses, les macérations et les infections urinaires. Un douchage/ shampooing régulier de l’arrière-train permet également de stimuler la circulation sanguine et de limiter les escarres. Il est important de bien sécher l’animal pour éviter les macérations. L’utilisation de mousses sans rinçage peut être utile entre 2 douches. Une tonte hygiénique péri-anale peut faciliter le nettoyage.
3. Utilisation de couches
Lors d’incontinences, l’utilisation de couches peut grandement aider le propriétaire à la maison. Pour l’incontinence urinaire des mâles, elles forment un bandeau autour de l’abdomen, et elles tiennent bien même si l’animal se traîne. Il existe des couches lavables en tissu, qui seront plus écologiques et moins chères sur le long terme, elles présentent également l’avantage de créer moins de lésions de frottement. Un absorbant (serviette hygiénique, absorbant enfant…) peut être ajouté dans la couche lavable pour en augmenter la capacité d’absorption.
III. Gestion des mictions
Le contrôle des mictions est essentiel dans la gestion de l’animal paralysé ; si la vessie n’est pas vidée régulièrement, des complications graves ou irréversibles peuvent survenir.
1. Comprendre le type de vessie neurogène
Selon la localisation de la lésion médullaire, deux tableaux cliniques peuvent se présenter :
- vessie spastique (lésion au-dessus de L7-S1 MNC) : rétention urinaire, vessie pleine, sphincter hypertonique ;
- vessie flasque (lésion du plexus sacré ou nerf périphérique MNP) : vidange incomplète, vessie distendue et fuites.
2. Vérification vésicale
De nombreux patients neurologiques sont capables d’uriner seuls, mais ne le font pas. Une opportunité d’uriner dehors doit toujours être proposée en premier pour stimuler l’animal. S’il n’a pas uriné, la vessie est palpée : si elle est volumineuse, elle sera vidangée par taxis ou par sondage. Attention à bien différencier vidange volontaire et vidange par trop-plein : si de l’urine est présente dans la cage, il est important de quand même palper la vessie afin d’évaluer si l’animal a vidangé seul ou si c’est uniquement par trop-plein.
3. Expression manuelle de la vessie
L’expression de la vessie est indiquée en cas de rétention. Elle nécessite une formation du propriétaire pour repérer la vessie, (“consistance d’un ballon de baudruche rempli d’eau”).
L’animal est idéalement détendu, positionné en decubitus latéral ou debout. La vidange peut se faire à 1 main (petits chiens) ou 2 mains sur les grands chiens : les mains de part et d’autre de l’abdomen, en zone caudoventrale. L’opérateur applique une pression constante douce en zone crâniale de la vessie, sans provoquer de douleur. Lorsque l’urine commence à s’écouler, la pression est maintenue et intensifiée pour continuer la vidange. Elle peut être particulièrement difficile si l’abdomen est tendu ou si l’animal est en surpoids. Une étude (Cawardine et Al, 2017) a mesuré le volume résiduel d’urine après vidange par taxis sur 36 chiens paralysés ; En moyenne, environ 49 % du volume urinaire était vidangé par taxis.
La fréquence conseillée est de palper la vessie tous les 4 h et de vidanger a minima tous les 8 h.
4. Médicaments pouvant aider la vidange vésicale
Selon le consensus de l’ACVIM de (Olby et Al, 2022), bien que les données probantes manquent pour guider l'utilisation de médicaments pour détendre les sphincters urétraux chez les chiens paralysés, l'utilisation d'un antagoniste alpha-adrénergique (ex : Alfusozine - Xatral) pour détendre le sphincter urétral interne, avec ou sans myorelaxant à action centrale (Diazepam - Valium), pour détendre le sphincter externe, est recommandée chez les chiens dont la vessie ne peut pas être facilement vidée manuellement.
5. Sondage urinaire
Le sondage peut être une alternative dans les cas où le taxis est inefficace ou douloureux. Cependant, il comporte un risque d’infection urinaire accru. Chez les femelles, un dispositif en place type sonde de Foley est préférable car le sondage nécessite une sédation. Elle doit être vérifiée et nettoyée 4 fois par jour.
6. Sonde de cystotomie
Des sondes de cystotomie peuvent être mises en place de manière définitive pour les animaux restant paralysés et incontinents, afin de faciliter la gestion au quotidien par les propriétaires : une sonde est placée entre la vessie et la peau et le propriétaire effectue la vidange via celle-ci plusieurs fois par jour.
7. Complications possibles
Les complications possibles, si la gestion des mictions n’est pas adéquate, sont : distension excessive de la vessie avec dommages pariétaux potentiellement irréversibles, infections du tractus urinaire, avec possible remontée de germes au niveau rénal, pouvant aller jusqu’à l’IRA. Une étude (Stiffler et Al, 2006) a montré que la fréquence des infections du tractus urinaire était en moyenne de 27 % après une intervention chirurgicale de hernie discale.
IV. Appareillages et aides à la mobilité
1. Gestion sols et adhérence
Un revêtement de sol adapté contribue à limiter les complications cutanées et à favoriser la mobilité :
- chez un animal sub-ambulatoire, privilégier un sol adhérent (tapis de gym, herbe en extérieur) pour faciliter ses premiers appuis et sécuriser ses déplacements. Des chaussettes antidérapantes (ex. : Element Vet, Pawz) peuvent également être conseillées : elles aident l’animal à prendre appui en évitant les glissades et protègent les doigts contre les lésions de frottement. Préférer des modèles fins, souples et respirants ;
- chez un animal paralysé, préférer un sol lisse afin de réduire les risques de lésions de frottement lorsque l’animal se déplace en traînant les postérieurs.
Par ailleurs, il est recommandé d’encourager les sorties, même en l’absence de locomotion autonome, afin de maintenir la stimulation psychologique. L’utilisation d’une poussette adaptée ou le transport en voiture vers un parc permettent à l’animal de profiter d’un environnement enrichissant et de préserver son bien-être émotionnel.
2. Harnais de soutien
Les harnais de soutien peuvent être utilisés pour les animaux sub-ambulatoires en cours de récupération, afin de réduire la charge supportée par l’animal et faciliter ses déplacements. Leur utilisation nécessite toutefois quelques précautions :
- l’animal ne doit pas être tenu uniquement par le harnais de soutien ; il convient de contrôler la vitesse de marche avec une laisse fixée au collier ou à son harnais habituel ;
- les harnais peuvent également servir à porter complètement l’arrière-train lors de paralysie totale, afin de soulager le propriétaire. Dans ce cas, préférer des modèles totaux (Help'em Up) chez les grands chiens. Il faut bien régler la longueur des poignées pour que le propriétaire ait une position confortable.
3. Chariots : quand et comment appareiller ?
Le chariot soulage ou porte l’arrière-train, ce qui conduit la majorité du déplacement à être assurée par la traction des antérieurs. Ainsi, l’animal « apprend » à se déplacer essentiellement grâce à ses membres thoraciques, ce qui est non souhaitable en phase de récupération neurologique.
Le chariot est à conseiller pour les animaux qui resteront paralysés, sans perspective réaliste de retour à une locomotion autonome.
Le choix du chariot devra prendre en compte de nombreux critères : taille (avec un accompagnement du propriétaire pour prendre correctement les mesures), poids par rapport à l’animal, robustesse, stabilité taille et type de roues adaptées à l’environnement (ville ou campagne), prix, possibilité de réglage, remplacement pièces détachées… Certains propriétaires ingénieux fabriquent eux-mêmes un chariot à partir de tubes en PVC, mais ces dispositifs doivent toujours être ajustés avec soin.
Le réglage est déterminant pour le confort et la sécurité :
- le dos doit rester le plus droit possible ;
- les pattes postérieures doivent toucher le sol si l’on souhaite une participation active, ou être placées vers l’arrière en cas de paralysie totale pour éviter les plaies de frottement ;
- le cadre doit entourer l’animal à quelques cm sur les côtés et l’arrière ;
- les roues doivent être légèrement inclinées vers l’extérieur et l’arrière pour assurer la stabilité ;
- le harnais qui porte le chariot doit être correctement réglé pour ne pas limiter l’extension des épaules.
En pratique, il faudra commencer par des sessions courtes de 5 minutes, puis augmenter progressivement la durée ; il faut prendre en considération le travail enduré par les antérieurs !
À long terme, il est indispensable de surveiller régulièrement les zones inguinales et axillaires, particulièrement exposées aux frottements.
Des chariots avec pédaliers existent, ils permettent à l’animal de mobiliser ses postérieurs en même temps que le chariot avance ( amplitude de mouvement très faible). Ils ne sont actuellement plus disponibles en France.
V. Conclusion
Gérer un animal paralysé à la maison requiert une coordination étroite entre le vétérinaire, le physiothérapeute et le propriétaire. Le confort, l’hygiène, la gestion des fonctions éliminatoires et l’appareillage doivent être considérés ensemble pour garantir une qualité de vie acceptable à l’animal. Un suivi structuré et individualisé permet non seulement de prévenir les complications, mais aussi d’optimiser les chances de récupération fonctionnelle.
Bibliographie
- OLBY, N. J., MOORE, S. A., BRISSON, B., FENN, J., FLEGEL, T., KORTZ, G., ... & TIPOLD, A. (2022). ACVIM consensus statement on diagnosis and management of acute canine thoracolumbar intervertebral disc extrusion. Journal of Veterinary Internal Medicine, 36(5), 1570-1596.
- OLBY, N., HALLING, K. B., & GLICK, T. R. (2005). Rehabilitation for the neurologic patient. Veterinary clinics: small animal practice, 35(6), 1389-1409.
- CARWARDINE, D., ROSE, J., HARCOURT-BROWN, T. R., & GRANGER, N. (2017). Effectiveness of manual bladder expression in paraplegic dogs. American Journal of Veterinary Research, 78(1), 107-112.
- STIFFLER, K. S., STEVENSON, M. M., SANCHEZ, S., BARSANTI, J. A., HOFMEISTER, E., & BUDSBERG, S. C. (2006). Prevalence and characterization of urinary tract infections in dogs with surgically treated type 1 thoracolumbar intervertebral disc extrusion. Veterinary Surgery, 35(4), 330-336.
- GOUVEIA, D., FONSECA, S., CARVALHO, C., CARDOSO, A., ALMEIDA, A., GAMBOA, Ó., ... & MARTINS, Â. (2023). Clinical occurrences in the neurorehabilitation of dogs with severe spinal cord injury. Animals, 13(7), 1164.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Gestion de fractures de Salter Harris de type I du fémur distal chez le chat par l'utilisation d'une broche centromédullaire unique dynamique (placée en rush) : étude rétrospective sur 31 cas (2017-2023)
Loïc LARGUIER
Coauteurs : Alexandre THIBAULT, Irène LOISEAU
Introduction
Les fractures de Salter Harris (SH) du fémur distal du chat sont fréquentes après traumatisme. Bien qu'une stabilisation par bandage soit rapportée, une prise en charge chirurgicale est vivement conseillée afin d'obtenir un alignement satisfaisant [1]. Différentes techniques de stabilisation sont rapportées, notamment via une unique broche centromédullaire de gros diamètre, deux broches placées en rush, en croix ou plus récemment une broche centromédullaire unique avec une broche anti-rotatoire latérale [2]. Cette étude a pour but de rapporter les résultats d'une stabilisation par une broche unique centromédullaire de petit diamètre placée en rush chez le chat.
Matériel et méthodes
Les dossiers médicaux de tous les chats traités pour une fracture du fémur distal de type SH I dans une seule structure entre 2017 et 2023 sont étudiés. La réduction des fractures, le ratio diamètre de la broche / taille de la cavité médullaire, le nombre de corticales atteintes par la broche en rush et l'effraction de la fosse intertrochantérique proximale sont évalués sur les radiographies postopératoires. Les évolutions clinique et radiographique sont évaluées à 4 semaines après l'intervention. Un contact téléphonique à long terme (6 mois et plus) est effectué afin d'évaluer la satisfaction propriétaire.
Résultats
Trente-un cas chez 30 chats sont inclus. Le sexe ratio mâle/femelle est de 1,5:1. L'âge médian est de 8 mois (2-32 mois). La réduction est excellente pour les 24/31 cas, bonne pour 5/31 et moyenne pour 2 cas. Les broches de Kirschner utilisées varient de 1,2 à 1,8 et la cavité médullaire médiane est de 5,3 mm (3,0-6,6 mm) Le ratio médian broche / cavité médullaire est de 32,6 % (22,7-50,0 %). La broche atteint 3 corticales sur tous les cas (31/31). Cinq broches dépassent légèrement de la fosse intertrochantérique, sans conséquence clinique observée. Aucune complication per- ou post-opératoire n'est rapportée, notamment aucune migration de broche. Sept chats ont une radiographie à 1 mois post-opératoire et montrent une cicatrisation osseuse complète sans anomalie de position de l'implant. L'ensemble des patients (29/30) ont un suivi téléphonique à long terme, rapportant l'absence de boiterie, une vie normale et une satisfaction complète des propriétaires. Le dernier chat a été euthanasié pour des raisons autres que ce problème orthopédique.
Discussion
Cette étude montre qu'un montage dynamique avec une seule broche semble être une excellente alternative aux montages décrits pour les fractures de SH de type I chez le chat.
L'utilisation d'une broche unique est rendue possible grâce à l'anatomie particulière du cartilage de croissance (CC) distal du fémur de chat. La morphologie à 4 pointes du CC de l'épiphyse distale permet une congruence parfaite avec les 4 orifices du CC diaphysaire distal et permet ainsi de bloquer le phénomène rotatoire. Il est nécessaire de s'assurer du nettoyage des surfaces des abouts fracturaires avant la réduction et de la stabilité peropératoire après insertion de la broche. En cas de doute, l'ajout d'une seconde broche est conseillé.
Il a déjà été décrit l'utilisation d'une broche unique de gros diamètre dans le traitement de ces fractures [3]. Dans le cas de cette étude, une occupation de l'ordre de 1/3 de la cavité médullaire est effectuée, ce qui est même inférieur à la valeur d'occupation de la cavité médullaire lors de montage hybride plaque-broche centromédullaire lors de fracture diaphysaire (39,9-53 %) [4]. Une broche de petit diamètre a une élasticité plus élevée et donc permet une insertion en rush : la broche réagit à sa flexion en essayant de retrouver sa forme initiale, ce qui verrouille la position de la broche. Cette technique limite la destruction du cartilage de croissance par l'insertion d'une broche de petit diamètre mais également bloque la position de l'implant et donc limite le risque de migration. Ce deuxième point est observé dans notre étude avec l'absence de migration.
Cependant, un implant de taille diminuée augmente le risque de rupture d'implant. Ceci n'est pas observé dans notre étude. Plusieurs points peuvent expliquer l'absence de cette complication : la stabilité intrinsèque liée à l'anatomie du CC, la majorité des forces exercées sur cette fracture sont compressives et donc maintiennent la réduction, et enfin peu de ruptures d'implant sont rapportées lors de montage élastique chez des jeunes animaux [5].
En plus de son caractère rétrospectif, cette étude présente une limite principale avec un nombre restreint de radiographies de suivi.
Conclusion
Cette technique semble être une alternative aux autres techniques décrites dans le traitement des fractures SH de type 1 du fémur distal chez le chat.
Bibliographie
- GRAHAM JEB. SIMPLE FIXATION FOR DISTAL EPIPHYSEAL FRACTURES OF THE FEMUR AND TIBIA IN THE CAT AND DOG. Published online 1960.
- BONDONNY L. Utilisation d'une technique d'ostéosynthèse modifiée avec un implant centromédullaire pour la prise en charge des fractures de Salter-Harris de type I et II du fémur distal chez le chat : étude rétrospective sur 30 cas (2014 -2022). Presented at: AFVAC - Congrès national; December 2022; Marseille.
- BRINKER WO. Proceedings twenty-sixth annual meeting. A.A.H.A.1959:204-207.
- VEDRINE B, GÉRARD F. Veterinary Cuttable Plate in a Plate-Rod Construct for Repair of Diaphyseal Femoral Fractures in the Cat. Vet Comp Orthop Traumatol. 2018;31(06):479-487.
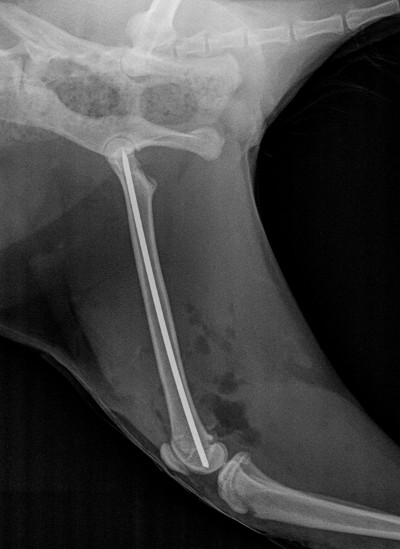
Figure 1
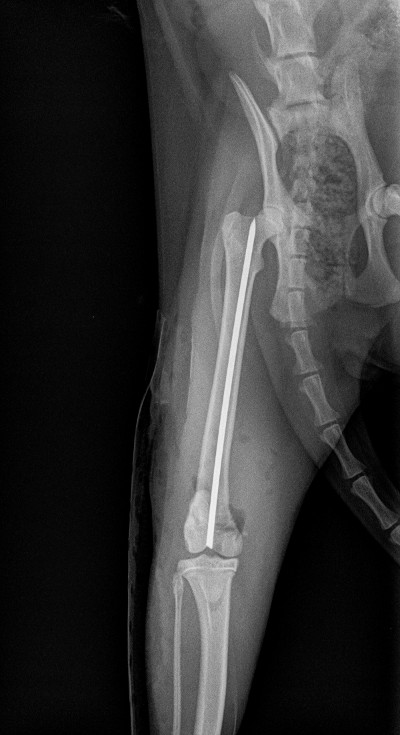
Figure 2
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Hanche : savoir évaluer la laxité coxo-fémorale chez le chien en croissance
Montréal, Canada
I. Introduction
La dysplasie de la hanche chez le chien est une affection développementale multifactorielle caractérisée par une laxité articulaire excessive, conduisant à une incongruence coxo-fémorale et à une arthrose secondaire. Chez le chien en croissance, la détection précoce de la laxité coxo-fémorale est essentielle pour orienter la gestion médicale ou chirurgicale et prévenir la progression de l’arthropathie. L’évaluation doit être à la fois clinique et radiographique, en tenant compte des facteurs de croissance et du développement musculaire.
II. Physiopathologie et fenêtre de dépistage
La laxité coxo-fémorale correspond à une mobilité anormale de la tête fémorale dans l’acétabulum, souvent liée à une laxité capsulo-ligamentaire et à un possible déficit de coaptation musculaire. Elle apparaît précocement (dès 8–12 semaines) mais peut fluctuer en fonction de la croissance et de la masse musculaire.
La période optimale de dépistage se situe généralement entre 3 et 6 mois pour les tests dynamiques, et entre 4 mois et 1 an pour les mesures radiographiques prédictives.
III. Évaluation clinique
1. Palpation
- Test de subluxation dynamique : vétérinaire en arrière du patient, mains sur les hanches alors que l’animal marche ; la sensation de « cloc » suggère une subluxation dynamique de la hanche ; test 100 % prédictif pour de la dysplasie de hanche
- Test d’Ortolani : chien en décubitus latéral ou dorsal (sous sédation), hanche fléchie à 90°, application d’une pression axiale puis abduction progressive. Un « cloc » à la réduction est signe de laxité. Sensible mais nécessite une bonne relaxation musculaire.
- Test de Barden : en décubitus latéral, traction latérale du fémur ; une déviation > 5 mm suggère une laxité significative.
- Test de Barlow : en décubitus dorsal, hanches fléchies et genoux à 90°, main sur le genou, pouce à l’intérieur de la cuisse et doigts à l’extérieur. On exerce une pression sur le genou tout en positionnant doucement le membre en adduction. Sensation de "clic" indiquant que la tête fémorale sort de l’acétabulum (subluxation provoquée).
Limites : la tonicité musculaire peut masquer la laxité ; une sédation peut être nécessaire pour mieux objectiver la laxité.
2. Goniométrie - Mesures des angles de réduction et subluxation de la hanche
Réalisées sous sédation profonde ou anesthésie, ces mesures réalisée entre 3 et 6 mois d’âge sur le patient peuvent nous aider à prédire le statut des hanches d’un chien adulte notamment lorsque qu’associée à la vue DAR (Dorsal Acetabular Rim)
IV. Évaluation radiographique
1. Techniques standardisées
- Projection en extension (OFA) : utile après 1 an, peu sensible aux laxités précoces ;
- Méthode de distraction (PennHIP) : mesure quantitative du Distraction Index (DI), valeur prédictive dès 16 semaines ;
- Vue DAR : utile sur les jeunes patients pour évaluer le rebord acétabulaire dorsal.
2. Précautions
- Positionnement rigoureux indispensable ;
- Sédation ou anesthésie courte nécessaire.
V. Interprétation et prise de décision
Corrélation clinique-radiographique : un test positif doit être accompagné par l’imagerie pour aider la prise de décision clinique ;
Stratification du risque : combiner âge, race, score et résultats cliniques.
VI. Points clés pour le praticien
- Commencer le dépistage clinique dès 12 semaines pour les races à risque.
- Utiliser palpation dynamique puis tests de palpation sous sédation/anesthésie pour limiter les faux négatifs.
- Intégrer les mesures quantitatives avec la goniométrie (angles de réduction et subluxation/PennHIP pour prédire la DH).
- Intégrer test d’imagerie à la palpation sous sédation/anesthésie.
- Réévaluer en croissance, car la laxité peut évoluer rapidement.
VII. Conclusion
La détection précoce de la laxité coxo-fémorale chez le chien en croissance repose sur une combinaison d’un examen clinique rigoureux par palpation et de techniques goniométriques et radiographiques quantitatives. La compréhension des limites de chaque méthode et la standardisation des protocoles sont essentielles pour optimiser la prise en charge et limiter l’impact de la dysplasie de hanche sur la vie du chien.
Bibliographie
- GATINEAU M, DUPUIS J, BEAUREGARD G, et al. Palpation and dorsal acetabular rim radiographic projection for early detection of canine hip dysplasia: a prospective study. Vet Surg. 2012;41(1):42–53.
- SMITH GK, et al. Evaluation of the accuracy of the PennHIP method for predicting radiographic hip dysplasia in dogs. Vet Surg. 1997;26(5):393–405.
- TOMLINSON JL, et al. Physical examination and palpation techniques for hip laxity in dogs. Vet Clin North Am Small Anim Pract. 2017;47(4):777-793.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Hémi-épiphysiodèse du radius distal pour la prise en charge d'une déformation de l'antebrachium chez un chien en croissance
Introduction
Les déformations de l'antebrachium sont fréquentes chez les chiens en croissance, dont la plus commune est le radius curvus, secondaire à une fermeture prématurée du cartilage de croissance de l'ulna distal. Cette croissance asynchrone entre le radius et l'ulna entraîne une altération de la mécanique articulaire, source de douleurs, boiterie et arthrose [1],[2].
Chez les jeunes chiens, l'ostectomie ulnaire distale est le traitement classique pour stopper la progression de la déformation, sans correction active [3]. Chez les patients adultes, les ostéotomies correctrices sont efficaces mais plus invasives et délicates à gérer en période de croissance.
Ce cas décrit l'utilisation combinée d'une hémi-épiphysiodèse radiale médiale distale et d'une ostectomie ulnaire pour corriger une déformation de l'antebrachium chez un jeune chien.
Anamnèse
Un Dobermann mâle entier de 4,5 mois (22 kg) est référé pour une déformation angulaire du membre thoracique droit apparue un mois après une morsure. Un traitement antibiotique et anti-inflammatoire a été prescrit sans amélioration.
Examen clinique
L'examen général est normal. Une boiterie associée à un valgus distal est notée, avec amyotrophie modérée et diminution de la flexion du carpe, sans douleur ni instabilité articulaire.
Démarche diagnostique
Des radiographies bilatérales confirment un valgus radial distal (aLDRA 51°) et un procurvatum à 36°, consécutifs à la fermeture prématurée du cartilage de croissance ulnaire distal. Le membre controlatéral (aLDRA 73°, procurvatum 18°) est utilisé comme référence. La torsion est jugée non significative.
Traitement
Une ostectomie ulnaire distale de 4 cm est réalisée par un abord latéro-distal de l'antebrachium et comblée par de la graisse sous-cutanée abdominale. Une hémi-épiphysiodèse radiale médiale est effectuée à l'aide d'une plaque LCP 2,7 mm à trois trous, contournée et fixée dorso-médialement avec deux vis corticales standard de part et d'autre du cartilage de croissance, sous guidage fluoroscopique.
Des contrôles bihebdomadaires sont réalisés. Une déhiscence cutanée secondaire à l'encombrement de l'implant survient à J15, justifiant soins locaux et antibiothérapie. À un mois, une cicatrisation prématurée de l'ostectomie ulnaire justifie la réalisation d'une seconde ostectomie de l'ulna distal. À 2 mois et 4 jours, l'aLDRA est de 88° et le procurvatum de 26°, motivant le retrait de l'implant pour éviter une surcorrection. Trois mois après le retrait de l'implant, l'alignement est satisfaisant (aLDRA : 81°, procurvatum : 22°) malgré un discret rebond de croissance.
Discussion
La prise en charge des déformations angulaires chez le jeune chien représente un véritable défi, notamment lorsqu'une intervention est envisagée avant la fin de la croissance. Le choix du moment opératoire et de la technique chirurgicale est essentiel pour éviter la progression de la déformation et prévenir les atteintes articulaires secondaires.
À la connaissance des auteurs, il s'agit de la première application clinique rapportée d'une hémi-épiphysiodèse radiale médiale distale combinée à une ostectomie ulnaire chez un chiot en croissance pour la correction d'une déformation de l'antebrachium.
Cette approche a permis d'arrêter temporairement la croissance du radius médial par compression au niveau de la plaque de croissance, favorisant une correction progressive de l'alignement de l'antebrachium pendant la croissance résiduelle. Bien que peu décrite en médecine vétérinaire, cette approche semble prometteuse, avec une normalisation de l'alignement sans complication majeure périopératoire.
La croissance résiduelle reste un facteur déterminant pour l'efficacité de cette procédure. Une discrète diminution de l'aLDRA après le retrait du matériel a été observée, probablement liée à un rebond de croissance [1]. Malgré une technique chirurgicale adaptée, une seconde ostectomie ulnaire s'est avérée nécessaire en raison d'une cicatrisation osseuse rapide de l'ulna et a probablement contribué à obtenir une correction plus complète. Un suivi postopératoire rigoureux associé à une évaluation régulière de l'alignement est indispensable pour optimiser les résultats de cette technique.
Conclusion
Ce cas démontre que l'hémi-épiphysiodèse radiale médiale distale combinée à l'ostectomie ulnaire peut permettre une correction progressive d'une déformation de l'antebrachium chez un chien en croissance. Cette technique a permis un réalignement satisfaisant du membre avec une fonction conservée. Des études complémentaires sont nécessaires pour évaluer sa reproductibilité et ses résultats à long terme.
Bibliographie
- VEZZONI L, et al. Hemiepiphysiodesis for the correction of distal femoral valgus in growing dogs. Vet Comp Orthop Traumatol. 2022;35(2):112-8.
- FOX DB. Radius and ulna. In: TOBIAS KM, JOHNSTON A, editors. Veterinary Surgery: Small Animal. 2nd ed. Elsevier; 2017. p. 760-784.
- CHRISTOPHER S. Short term outcomes and complications of distal ulnar ostectomy in 23 juvenile dogs with carpal valgus secondary to discordant radial-ulnar physeal growth. Front Vet Sci. 2022;9:971527.
- OLSEN AM, et al. Hemiepiphysiodesis for the correction of proximal tibial valgus in growing dogs. Vet Comp Orthop Traumatol. 2016;29(4):330-337.
- FOX DB, et al. Principles of angular limb deformity correction. In: TOBIAS KM, JOHNSTON A, editors. Veterinary surgery: small animal. 2nd ed. 2017. Elsevier. p. 657-668.
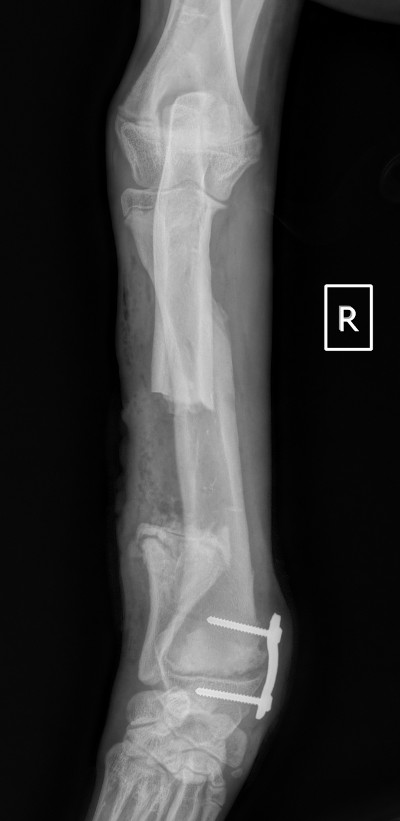
Figure 1
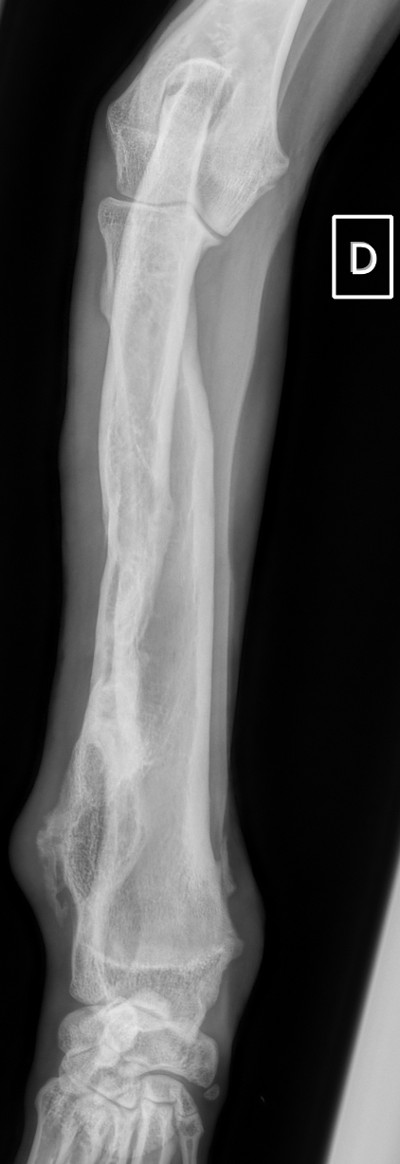
Figure 2
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Hypoplasie de l'émail chez un Shiba Inu de 7 mois : diagnostic, prise en charge et suivi
Introduction
L'hypoplasie de l'émail est une anomalie du développement dentaire caractérisée par un défaut de formation ou de maturation de l'émail entraînant une exposition de la dentine sous-jacente. Cette affection peut être systémique (due à une infection, une carence nutritionnelle ou une intoxication) ou traumatique (lésion locale sur un ou plusieurs germes dentaires). L'émail étant acellulaire et non vascularisé, il ne peut pas se réparer spontanément, une fois la dent éruptée, ce qui rend la prise en charge essentielle pour éviter l'hypersensibilité et la colonisation bactérienne.
Matériel et résultats
Un Shiba Inu mâle de 7 mois a été présenté pour douleurs à la mastication et coloration anormale des dents. L'examen clinique a révélé : décoloration brun-jaunâtre diffuse sur plusieurs dents, émail rugueux et irrégulier, absence localisée d'émail, anneaux de lésions homogènes autour des dents, indicateurs d'un épisode systémique survenu pendant l'amélogenèse, hypersensibilité marquée lors de la palpation intra-orale. Le propriétaire a rapporté que le chien mangeait de manière inhabituelle et laissait parfois tomber sa nourriture, suggérant une gêne dentaire.
Les hypothèses étiologiques incluaient une hypoplasie de l'émail d'origine systémique, probablement causée par un épisode fébrile entre 8 et 14 semaines d'âge, période critique pour l'amélogenèse. L'aspect bilatéral et symétrique des lésions ainsi que leur localisation à distance précise de la gencive, soutiennent cette hypothèse.
Les radiographies dentaires rétroalvéolaires par un capteur intra-oral ont permis de : confirmer l'absence d'infection endodontique et de lésions pulpo-radiculaires, écarter une odontodysplasie (qui affecte également les racines), identifier une structure dentaire globalement préservée, mais avec un émail dysplasique et fragile.
L'objectif thérapeutique était de réduire la sensibilité dentaire, protéger la dentine exposée et prévenir les complications à long terme. Préparation initiale : détartrage via un détartreur ultrasonique IM3 42-12 (moins agressif) pour éliminer l'émail non adhérent et les résidus de plaque sur les surfaces affectées. Scellement des tubules dentinaires : application d'un scellant dentaire pour réduire la sensibilité et empêcher la pénétration bactérienne. Matériaux utilisés : adhésif résineux photopolymérisable avec un léger prétraitement acide (etching) selon la gravité des lésions. Pose de couronnes protectrices : les crocs et carnassières, essentiels à la mastication, ont été protégés par des coiffes métalliques pour offrir une protection supplémentaire contre une infection endodontique via les tubules exposés. Hygiène dentaire stricte à domicile : brossage quotidien avec une pâte dentifrice à base de chlorhexidine pour limiter la plaque, Application périodique d'un vernis après chaque détartrage pour renforcer les surfaces exposées.
Conclusion
Suivi et pronostic : surveillance annuelle avec nettoyage professionnel, polissage doux et application d'une nouvelle couche de vernis sur les dents non coiffées. Réduction progressive de la sensibilité grâce au dépôt de dentine tertiaire. Surveillance de l'usure dentaire due à la mastication et ajustements éventuels des restaurations. Les propriétaires ont été informés que la coloration brune des dents était due à la dentine exposée, et qu'elle ne pouvait pas être esthétiquement corrigée. Toutefois, le traitement a permis une nette amélioration du confort masticatoire et aucun signe de pulpite ou d'infection n'a été observé aux premiers suivis.
Figure 1
Figure 2
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Impliquer le propriétaire dans la rééducation à la maison : thermothérapie, mécanothérapie, massages
Lausanne, Suisse
I. Introduction
La récupération d’un patient paralysé ne se limite pas aux séances de rééducation en clinique : l’implication du propriétaire à domicile est un levier déterminant du succès thérapeutique. Les gestes simples de nursing, de mobilisation et de stimulation neuro-musculaire assurent la continuité des soins, stimulent la plasticité neuronale, favorisent la récupération locomotrice et préviennent les complications futures.
La récupération s’appuie sur la réduction de la compression de la moelle épinière et la plasticité neuronale, qui suivent les quatre phases distinctes de récupération [1].
II. En phase aiguë (J1–J5)
L’objectif est de diminuer l'inflammation pour réduire la compression du SNC et ainsi prévenir les complications. Le propriétaire doit maintenir le confort et participer à prévenir et éviter les séquelles secondaires. Il doit assurer un nursing attentif (alternance de position, hygiène, soutien postural), réaliser des mouvements articulaires passifs, du stretching doux, ainsi que des massages légers favorisant la circulation et la stimulation sensorielle [1-2]. La thermothérapie peut être utilisée avec prudence et sous la direction du vétérinaire physiothérapeute (chaleur douce pour détendre et pratiquer du gate-control, froid en cas de phase inflammatoire pour limiter la conduction du signal douloureux) [2]. La station debout assistée et les transferts de poids doux constituent déjà un premier travail proprioceptif passif, préparant le corps pour la récupération fonctionnelle durant les phases suivantes de récupération [4]. L’utilisation du TENS à domicile peut être envisagée sous la supervision du vétérinaire réhabilitateur pour la gestion de la douleur post-opératoire [3]. La stimulation sensorielle constitue également un aspect incontournable de cette phase.
III. En phase subaiguë (J5–J21)
La baisse de l'inflammation et le bourgeonnement axonal permettent de réactiver les circuits locomoteurs spinaux et de voir apparaitre les premières contractions volontaires. Le propriétaire accompagne cette reprise en pratiquant la stimulation sensorielle, des massages actifs, des mobilisations assistées et des exercices thérapeutiques simples (station debout prolongée, transferts de poids, lever–assis assisté, cavalettis au sol, etc). La thermothérapie (application de chaleur avant exercice) prépare et soutient ces activités. L’utilisation du NMES peut venir compléter la poursuite de l’application du TENS pour favoriser la préservation de la masse musculaire et la stimulation de la jonction neuro-musculaire [3].
IV. En phase de consolidation (J21–J60)
Les circuits neuronaux se stabilisent. L’axe de travail durant cette phase est centré sur la coordination motrice. Le propriétaire peut introduire des exercices thérapeutiques plus avancés : exercices polyarticulaires (par exemple le assis-debout), transitions, marche contrôlée en laisse, cavalettis, obstacles variés et adaptés, et tous types de locomotion sur surfaces variées ou instables [1]. Les massages et la thermothérapie permettent de prodiguer une stimulation sensorielle et d’optimiser confort et récupération [2].
V. En phase d’organisation (J61+)
L’objectif de cette phase est d’optimiser endurance et symétrie. Le propriétaire accompagne le chien dans des exercices polyarticulaires plus complexes : obstacles et cavalettis plus hauts ou complexes, passage d’escaliers sous contrôle, changements de rythme de la locomotion, travail sur coussins instables [1]. Les massages réguliers entretiennent la souplesse et préviennent les tensions musculaires liées aux éventuelles courbatures [2].
VI. Conclusion
En résumé, le propriétaire devient le partenaire actif de la réhabilitation neurologique : par ses soins quotidiens, il consolide les progrès effectués en clinique, entretient la connexion neuromusculaire, et favorise la récupération fonctionnelle à long terme et le succès thérapeutique.
Toutefois, un plan de réhabilitation effectué par le propriétaire à la maison n’exclut pas le besoin de travailler en centre spécialisé afin d’augmenter le volume et la précision des stimulations neuro-musculaires appliquées au patient, et ainsi obtenir des résultats de rééducation optimaux.
Bibliographie
- BOCKSTAHLER B., LEVINE D., MILLIS D., et al. Essential Facts of Physical Medicine, Rehabilitation and Sports Medicine in Companion Animals. BE VetVerlag, 1re ed 2019.
- MILLIS D., LEVINE D. Canine Rehabilitation and Physical Therapy. 2nde ed. Elsevier, 2013
- MARTINS Â., GOUVEIA D., CARDOSO A., et al. A Controlled Clinical Study of Intensive Neurorehabilitation in Post-Surgical Dogs with Severe Acute Intervertebral Disc Extrusion. Animals (Basel). 2021;11(11):3034.
- GOUVEIA D, CARVALHO C, CARDOSO A, GAMBOA O, ALMEIDA A, FERREIRA A, et al. Early locomotor training in tetraplegic post-surgical dogs with cervical intervertebral disc disease. Animals (Basel). 2022;12:2369.
Liens d'intérêt : Conseiller scientifique pour la société AllCare innovations.
📃 Infection urinaire : cause ou complication ?
Guyancourt, France
I. Introduction
Les infections urinaires sont des motifs fréquents de consultation en médecine vétérinaire. Ces dernières peuvent entraîner des complications pouvant parfois être graves mais peuvent également être sentinelles d’une autre affection ou anomalie du tractus urinaire du chien et du chat. Séparer la cause et la conséquence de l’infection urinaire est parfois une affaire complexe et peut s’apparenter au dilemme de l'œuf ou de la poule. Les objectifs de cette présentation sont donc de comprendre les facteurs prédisposants d’une infection urinaire, les complications potentielles associées à la présence d’une infection urinaire et la gestion thérapeutique de cette dernière et de ses causes potentielles.
II. Définition d’une infection urinaire
Une infection urinaire se manifeste par la présence de signes en faveur d’une infection urinaire (signes du bas appareil urinaire dans le cas de cystite ; signes cliniques généraux en cas de pyélonéphrite) avec mise en évidence d’une bactériurie significative. Le milieu urinaire n’étant pas un milieu stérile l’infection urinaire est à différencier d’une bactériurie subclinique qui est la présence d’une bactériurie significative sans signes cliniques d’infection urinaire. Enfin, la définition d’une bactériurie significative est à relier à la méthode de collecte des urines (voir Tableau 1).
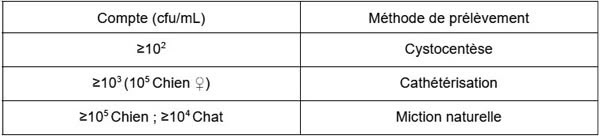
Tableau 1
III. Facteurs prédisposants
Les facteurs prédisposants à une infection urinaire sont multiples et se traduisent par la présence d’anomalie anatomique ou d’incontinence urinaire, la présence d’un nidus favorisant la prolifération bactérienne ou des facteurs environnementaux affectant la flore urinaire.
1. Anomalies anatomiques et incontinence urinaire
Toute anomalie entraînant la stagnation d’urine dans le tractus urinaire peut être sujette à la prolifération de bactéries dans ces urines stagnantes. En cas d’incontinence urinaire, les urines stagnent dans l’urètre, le vestibule, le vagin ou encore la vulve favorisant la prolifération bactérienne puis la colonisation bactérienne du reste du tractus urinaire. Dans les anomalies les plus fréquemment visualisées, on retrouve les uretères ectopiques, une persistance du canal de l’ouraque, une vulve encapuchonnée ou toute autre anomalie du développement du système génito-urinaire.
2. Présence d’un nidus
Dans le même ordre d’idée, tout tissu ou matériel présent dans le système urinaire et pouvant servir de niche pour la prolifération bactérienne peut être une cause d’infection urinaire. On y retrouve alors, les masses prolifératives potentiellement cancéreuses, les calculs urinaires, la présence de corps étrangers…
3. Facteurs environnementaux
L’environnement urinaire est un environnement très équilibré (pH, composition chimique, densité…) et possédant une flore bactérienne propre. Toute altération de cet équilibre peut amener à un déséquilibre au niveau de la flore bactérienne avec une espèce pouvant proliférer par rapport à une autre et conduire à une infection urinaire. Ainsi, l’alimentation, l’obésité et certaines maladies métaboliques (Cushing, diabète sucré) peuvent jouer sur la composition de l’urine et prédisposer à la genèse d’infections urinaires. Une antibiothérapie récente peut potentiellement impacter directement ou indirectement le microbiote urinaire et induire une dysbiose urinaire.
IV. Complications
Une infection urinaire non traitée peut aboutir à diverses complications plus ou moins graves pour le patient. L’évolution de l’infection vers une infection profonde est la plus redoutée avec atteinte de tissus plus difficiles à traiter (paroi vésicale ou urétrale, prostate, reins) pouvant parfois même évoluer vers l’urosepsis. Certaines infections à germes uréases positifs peuvent déboucher vers la formation de calculs urinaires pouvant compliquer l’infection urinaire et aboutir à d’autres signes cliniques. Enfin la présence de cystites récurrentes (rechute ou réinfection fréquente) peut être une des complications envisagées lors d’infection urinaire.
V. Approche thérapeutique
Une infection urinaire, à la différence d’une bactériurie subclinique, nécessite une antibiothérapie adaptée (durée et choix de l’antibiotique). Aussi, en cas d’infections profondes, la durée de traitement doit être prolongée (2-4 semaines ou plus) et le choix de l’antibiotique doit porter vers un antibiotique pouvant pénétrer dans la région d’intérêt. Dans le cas d’infections compliquées par la présence de calculs, les antibiotiques doivent être poursuivis jusqu’à fonte totale des calculs urinaires.
VI. Gestion des infections récurrentes
Dans le cas d’infections récurrentes il est nécessaire de différencier entre une rechute d’infection urinaire et une réinfection. Une rechute d’infection urinaire est le développement d’une infection urinaire dans les 4 semaines suivant le traitement de la première infection avec une bactérie similaire. Une réinfection est le développement d’une infection urinaire après une période de rémission clinique et secondaire à un nouvel agent infectieux ou un germe similaire plus de 4 semaines après son épisode précédent. Dans le cas d’une rechute, le traitement effectué peut ne pas avoir été efficace (antibiorésistance, défaut de pénétration dans le tissu cible, durée de traitement inadapté) et une culture urinaire avec antibiogramme est fortement recommandée afin de réajuster le traitement mis en place. En revanche, dans le cas d’une réinfection, il est important d’identifier toute cause prédisposante aux infections urinaires. La prise en charge repose alors en la gestion de l’infection urinaire et en la correction de la cause prédisposante : correction de l’uretère ectopique, vulve encapuchonnée, extraction de calculs urinaires non traitables médicalement…
VII. Conclusion
En conclusion, de nombreux facteurs peuvent prédisposer l’apparition d’infections urinaires chez nos animaux de compagnie et une infection urinaire non traitée peut aboutir à l’apparition de complications pouvant compliquer la prise en charge de l’animal. La distinction entre cause et conséquence peut parfois être compliquée dans le cas d’une infection urinaire à l’image de la présence de calculs pouvant être antérieurs ou postérieurs à l’infection urinaire. En cas de cystites récidivantes avec évidence de réinfection, il est primordial de recherhcher une cause prédisposante à l’infection urinaire et, si possible, de la corriger.
Bibliographie
- BYRON, J. K. (2019). Urinary Tract Infection. In Veterinary Clinics of North America - Small Animal Practice (Vol. 49, Issue 2, pp. 211–221). W.B. Saunders.
- DORSCH, R., TEICHMANN-KNORRN, S., & SJETNE LUND, H. (2019). Urinary tract infection and subclinical bacteriuria in cats: A clinical update. In Journal of Feline Medicine and Surgery (Vol. 21, Issue 11, pp. 1023–1038). SAGE Publications Ltd.
- WEESE JS, BLONDEAU J, BOOTHE D, GUARDABASSI LG, GUMLEY N, PAPICH M, JESSEN LR, LAPPIN M, RANKIN S, WESTROPP JL, SYKES J. International Society for Companion Animal Infectious Diseases (ISCAID) guidelines for the diagnosis and management of bacterial urinary tract infections in dogs and cats. Vet J. 2019 May;247:8-25.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Inflammation chronique et cancer : que sait-on ?
Nantes, France
I. Introduction
L’inflammation chronique est reconnue comme un des facteurs majeurs impliqués dans le développement de certains cancers chez l’humain. Cette relation, bien étudiée en médecine humaine, intrigue aussi la médecine vétérinaire. Chez le chien et le chat, la compréhension de l’impact de l’inflammation chronique sur la survenue de tumeurs cancéreuses progresse, mais reste encore partielle.
L’inflammation est une réponse physiologique normale destinée à protéger l’organisme contre une agression, qu’elle soit infectieuse, mécanique ou chimique. En phase aiguë, elle permet la réparation tissulaire. Cependant, lorsqu’elle devient chronique, l’inflammation persiste, avec une activation prolongée du système immunitaire et la production continue de médiateurs pro-inflammatoires. L’inflammation persistante, qu’elle soit d’origine infectieuse, traumatique ou immunitaire, crée un microenvironnement tumoral propice à la transformation cellulaire via des mécanismes combinant stress oxydatif, libération de cytokines pro-inflammatoires et stimulation excessive de la prolifération cellulaire (A Comparative Approach of Tumor-Associated Inflammation, PMCID PMC5178344).
Le mécanisme liant inflammation chronique et cancer repose sur plusieurs axes. D’une part, la production durable de radicaux libres entraîne des dommages à l’ADN des cellules, favorisant les mutations oncogéniques. D’autre part, les cytokines pro-inflammatoires comme le TNF-α, l’IL-6 ou l’IL-1β créent un microenvironnement tumorogène en stimulant la prolifération cellulaire et en inhibant l’apoptose. Enfin, l’inflammation chronique induit une angiogenèse excessive, facilitant la croissance et la diffusion des tumeurs.
L’identification de marqueurs inflammatoires spécifiques chez les animaux, ainsi que la compréhension des interactions entre cellules immunitaires et cellules tumorales, sont des axes de recherche prometteurs. Ces découvertes pourraient ouvrir la voie à des stratégies préventives ou thérapeutiques ciblant l’inflammation pour réduire le risque de cancer.
II. Le chat : modèle d’oncogenèse inflammatoire
Chez le Chat, la relation entre inflammation chronique et transformation tumorale est particulièrement illustrée par les sarcomes post-injection ou sarcomes associés aux sites d’injection (ISS). Décrits pour la première fois dans les années 1990, ces tumeurs se développent dans les zones de vaccination, d’injection ou d’implant sous-cutané, à la suite d’une réaction inflammatoire chronique granulomateuse. Cette inflammation persistante induit une production prolongée de médiateurs tels que l’IL-1β, le TNF-α et la COX-2, favorisant la mutation des fibroblastes et des myofibroblastes en cellules néoplasiques (Cats, Cancer and Comparative Oncology, PMCID PMC5644631) [2]
Le rôle de la réponse macrophagique et de la fibrose locale dans ces sarcomes a été démontré dans des études histopathologiques : les macrophages CD68+ et lymphocytes CD3+ infiltrants participent activement à la transformation et à la progression tumorale (Role of inflammation/wound healing in feline oncogenesis, PMCID PMC10911203). D’autres travaux ont mis en évidence le potentiel préventif de l’immunothérapie IL-2 recombinante (Oncept IL-2), qui réduit la récidive après exérèse chirurgicale, en modulant la réponse inflammatoire locale (PMCID PMC5644631).
- Les sarcomes oculaires post-traumatiques, survenant après rupture du cristallin ou uvéite chronique, résultent d’une dégénérescence néoplasique du tissu mésenchymateux sous une stimulation inflammatoire prolongée.
- Les lymphomes digestifs du chat sont souvent précédés d’un syndrome d’inflammation intestinale chronique (IBD-like), suggérant une transition progressive entre infiltration inflammatoire et néoplasie lymphoïde (ACVIM consensus statement on diagnosing and treating feline IBD and lymphoma, PMID 37130034) [4]
III. Le chien : des associations plus rares mais documentées
Chez le chien, bien que les preuves soient moins robustes, plusieurs contextes soutiennent une implication comparable. Une péricardite chronique a été suggérée comme facteur de risque de mésothéliome péricardique, via une stimulation continue du mésothélium. Des cas de sarcomes des tissus mous post-traumatiques et de lymphomes associés à des infections chroniques (Ehrlichia canis, Histoplasma capsulatum) ont aussi été rapportés, indiquant un rôle probable de l’inflammation infectieuse prolongée dans la transformation cellulaire (B-cell lymphoma in a dog with ehrlichiosis and histoplasmosis, PMCID PMC1800954 ).
À l’échelle moléculaire, l’expression accrue des marqueurs COX-2, MAC387 et CD3+ T-lymphocytes dans les tumeurs mammaires canines a été corrélée à un grade histologique élevé et à une survie réduite, soulignant que l’inflammation de l’environnement tumoral favorise la progression néoplasique (A Comparative Approach of Tumor-Associated Inflammation, PMCID PMC5178344) [1]
IV. Conclusion
Chez le chat comme chez le chien, l’inflammation chronique représente une interface physiopathologique critique entre réparation tissulaire et néoplasie. Les modèles félins, notamment le sarcome post-injection, permettent de mieux comprendre les mécanismes d’oncogenèse inflammatoire et d’envisager des stratégies de prévention étendues à la médecine comparée.
Ces observations renforcent l’hypothèse selon laquelle l’inflammation chronique joue un rôle initiateur ou promoteur majeur dans certaines tumeurs félines et canines. Sur le plan préventif, la réduction de la stimulation inflammatoire excessive est essentielle :
- utilisation raisonnée des sites d’injection (zones distales) chez le chat ;
- contrôle des affections inflammatoires chroniques (entérites, stomatites, kératites…) ;
- recours à des anti-inflammatoires (notamment ciblant COX-2) ou à des approches immunomodulatrices pour limiter la dérégulation du microenvironnement cellulaire.
Bibliographie
- PESAVENTO PA, et al. Role of inflammation/wound healing in feline oncogenesis. Vet Pathol. 2008; PMCID: PMC10911203.
- DOBSON J, et al. Cats, Cancer and Comparative Oncology. Vet J. 2015; PMCID: PMC5644631 .
- NIZA MMRE, et al. A Comparative Approach of Tumor-Associated Inflammation in Canine and Human Oncology. Vet J Sci. 2016; PMCID: PMC5178344.
- BRUNKER JD, HOOVER JP. B-cell lymphoma in a dog with ehrlichiosis and histoplasmosis. Can Vet J. 1997; PMCID: PMC1800954.
- WASHABAU RJ, et al. ACVIM consensus statement guidelines on diagnosing and managing feline intestinal inflammation and lymphoma. J Vet Intern Med. 2022; PMID: 37130034.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Intelligence artificielle : de quoi parle-t-on ?
Tréméoc, France
I. Définition
L’Acte européen sur l’Intelligence Artificielle (IA) de 2024 définit l’IA ainsi : « système à base de machine, conçu pour fonctionner avec divers degrés d’autonomie, qui infère à partir d’entrées comment générer des sorties (prédictions, contenus, décisions, etc.) influençant des environnements physiques ou virtuels ».
L’utilisation du verbe inférer est essentielle. L’inférence est le processus mental par lequel un individu tire des conclusions ou établit des relations logiques à partir d'informations disponibles, souvent incomplètes ou implicites. Elle permet de combler les lacunes informationnelles et de générer des interprétations cohérentes de situations complexes. [1,2]
D’autres définitions de l’IA se réfèrent à la notion de simulation de l’intelligence humaine. Cette référence est discutable. Elle pourrait laisser croire que l’IA pense comme un humain (or ce n’est qu’une simulation), et il n’est pas précisé à quelles intelligences humaines on se réfère : système intelligence heuristique / intelligence analytique selon Kahneman, intelligences logico-mathématique, spatiale, émotionnelle…
II. Piliers fonctionnels
L’IA est donc une machine qui accepte des entrées, les traite en fonction de son apprentissage pour générer des sorties et agir sur l’environnement.
1. Les entrées
L’acquisition des données d’entrée peut prendre plusieurs voies : textuelle (entrée clavier, voix, fichiers joints), images, base de données, résultats de recherche web, signaux physiques par le biais de capteurs… L’entrée image a des applications importantes en imagerie médicale.
2. L’apprentissage
On distingue plusieurs formes d’apprentissage. La plupart des IA développées actuellement en utilisent successivement plusieurs.
Apprentissage non-automatique : il repose uniquement sur l’expertise humaine, avec programmation manuelle de l’algorithme et supervision continue. Historiquement, c’est la base des systèmes experts. Il s’agit plus de programmation avancée que d’IA, et nécessite un travail considérable.
Apprentissage automatique : l’algorithme est généré par la machine, avec ou sans supervision humaine. Il existe plusieurs façons de procéder à l’apprentissage automatique. Exemples :
- Apprentissage supervisé : la machine reçoit des exemples d’entrées accompagnés de leur réponse correcte, par annotation humaine massive. Il apprend ainsi à établir des correspondances entre les données d'entrée et les résultats attendus. Cette méthode permet ensuite de prédire les réponses pour de nouvelles données non vues auparavant.
- Apprentissage non supervisé : la machine ne reçoit que les entrées et a pour tâche de trouver la structure cachée dans les données. Ce format peut être utilisé entre autres pour la génération (restitution de la distribution statistique des données d’entraînement).
- Apprentissage semi-supervisé : combinaison des deux précédents, ce qui permet de réduire la fourniture de données annotées par les humains.
- Apprentissage auto-supervisé : le modèle crée lui-même ses exercices d’entraînement à partir des données brutes. Par exemple, masquer des mots dans un texte et apprendre à les prédire, ou cacher des parties d'une image et apprendre à les reconstituer.
- Apprentissage par renforcement : méthode où un agent apprend par interaction avec son environnement. Le retour peut être automatisé ou par évaluation des résultats par les utilisateurs humains.
3. Le raisonnement
Il est fondamentalement différent du raisonnement humain. Ne pas perdre de vue que les IA n’ont pas une véritable compréhension du sens de nos demandes. On distingue 4 types de raisonnement, souvent combinés dans les solutions actuelles :
- Symbolique : utilise la logique formelle (systèmes experts).
- Connexionniste : le pseudo raisonnement émerge d’un réseau de neurones, selon un mécanisme opaque. Par exemple, un réseau de neurones peut apprendre à classer des images de chats et de chiens en ajustant des millions de paramètres internes lors de l’entraînement.
- Probabiliste : basé sur les probabilités et les statistiques (par exemple probabilité d’une maladie donnée connaissant tels symptômes).
- Évolutionniste : inspiré de la théorie darwinienne. L’algorithme génétique démarre avec un ensemble de solutions potentielles générées aléatoirement, puis à chaque génération il sélectionne et recombine les meilleures selon un critère de qualité, produisant ainsi une nouvelle génération améliorée.
Une avancée majeure est l’apparition chez les modèles avancés d’un raisonnement approfondi, mettant en jeu des mécanismes d’analyse et de découpage par étapes des demandes (chaîne de pensée), d’itérations et de retour en arrière [3].
4. Les sorties
Elles sont variées : texte, image, action physique sur l’environnement (robotique), mixtes… La nature des tâches accomplies permet une classification fonctionnelle.
- IA générative : crée du contenu nouveau (texte, image, vidéo, musique, code…) à partir d’une consigne ou de données d’entrée. On parle d’IA générative dès lors qu’un système synthétise du contenu qu’il n’a pas simplement mémorisé, en se basant sur une compréhension statistique des données.
- IA prédictive (analytique) : analyse des données pour prédire des résultats futurs ou inconnus, afin d’anticiper des événements ou de détecter des patterns cachés. C’est l’IA employée dans l’analyse prédictive en médecine (prédire l’évolution d’une épidémie, diagnostiquer une maladie sur imagerie, etc.). Ces systèmes combinent généralement des techniques de statistiques et de machine learning pour extraire des corrélations utiles. Son efficacité dépend beaucoup de la qualité des données d’entraînement et de la validité de l’hypothèse que le futur ressemblera au passé.
- IA décisionnelle (prescriptive/automatisation) : assiste ou automatise la prise de décision et l’exécution d’actions. Ici, l’IA ne se contente pas de fournir une prédiction ou une information, elle recommande directement une stratégie ou pilote un processus. On parle aussi d’IA « prescriptive » lorsque, sur la base d’analyses, elle suggère la meilleure action à entreprendre.
- IA interactive (conversationnelle) : gère des interactions avec les humains de manière naturelle, que ce soit via le langage (dialogue écrit/oral) ou d’autres moyens (gestes, interface). C’est l’IA visible dans les chatbots, agents virtuels, assistants vocaux, robots sociaux, etc.
- IA perceptive : analyse des données sensorielles brutes, typiquement visuelles ou sonores, pour en extraire une interprétation utile. Exemple : reconnaissance de formes, vision par ordinateur, reconnaissance vocale automatique, vidéosurveillance intelligente, outils de diagnostic médical assisté par image (détection de tumeurs sur des radiographies), transcription automatique…
- IA agentique : exécute des tâches complexes de façon autonome. L’IA utilise un ordinateur virtuel pour faire des recherches, traiter les documents, se connecter à différents services, et exécuter les tâches en toute autonomie.
III. Conclusion
L’IA n’est pas monolithique, elle est plurielle : une mosaïque de méthodes et d’objectifs, allant du plus déterministe au plus apprenant, du plus spécialisé au plus général. Les écosystèmes sont de plus en plus complexes, les systèmes d’aujourd’hui combinent plusieurs techniques, et cela ira en augmentant.
Les voies d’avenir semblent tracées : raisonnement approfondi, intégration multimodale, capacités agentique, autonomie. Un schéma apparaît : une IA généraliste faisant appel à une ou plusieurs IA spécialisées en fonction des besoins. On reste cependant encore éloigné de la notion d’IA forte (ou IA générale), une IA qui égalerait, voire dépasserait, l’intelligence humaine dans toute sa diversité.
Bibliographie
- JOHNSON-LAIRD P. N. Mental models: Towards a cognitive science of language, inference, and consciousness. Harvard University Press 1983.
- GRAESSER A. C. et coll. Constructing inferences during narrative text comprehension. Psychological Review 1994) ; 101(3), 371-395.
- RICHARDS D. , Top Reasoning AI Models in 2024: A Comprehensive Comparison, consultable sur https://ragaboutit.com/top-reasoning-ai-models-compared/
- CHAIZE P. et coll. et col. Rapport n° 170 [2024-2025], déposé le 28 novembre 2024 ChatGPT, et après ? Bilan et perspectives de l'intelligence artificielle, consultable sur https://www.senat.fr/rap/r24-170/r24-17012.html
- MUCCI T., STRYKER C. Qu’est-ce que la superintelligence artificielle ? ibm.com, décembre 2023, consultable sur https://www.ibm.com/fr-fr/think/topics/artificial-superintelligence
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Intelligence artificielle : les outils spécialisés d'aujourd'hui et de demain
Versailles, France
I. Introduction
En France, l’usage de l’intelligence artificielle connaît une croissance rapide, principalement portée par l’essor des IA génératives. Dans le secteur vétérinaire, de nouvelles solutions intégrant des algorithmes d’IA voient le jour. Elles visent à accélérer et fiabiliser les diagnostics, alléger les tâches administratives, faciliter l’accès aux données scientifiques, soutenir la prise de décision et assurer une surveillance en temps réel des animaux. Si les applications médicales de l’IA sont nombreuses, leur intégration dans la pratique quotidienne de la médecine des animaux de compagnie reste limitée. On observe aujourd’hui une multiplication d’expérimentations, mais pas encore une réelle généralisation de ces outils en clinique. En revanche, les vétérinaires ruraux sont déjà plus familiers de l’IA, notamment grâce aux dispositifs connectés équipés d’algorithmes et aux systèmes de vidéosurveillance des élevages utilisant la vision par ordinateur.
II. L’IA dans le diagnostic : un copilote pour les équipes vétérinaires ?
Nous présenterons plusieurs solutions intégrant l’intelligence artificielle déjà disponibles, en particulier celles dédiées à l’assistance au diagnostic par analyse et interprétation d’images. Les usages des IA génératives seront, quant à eux, abordés lors de la conférence suivante. Ces outils reposent sur des techniques de deep learning, notamment des réseaux de neurones convolutifs, et sont entraînés à partir de vastes bases d’images de haute qualité annotées par des experts.
1. Interprétation des radios
Ces solutions permettent d’analyser instantanément les clichés les plus courants (thorax, abdomen, hanches) et de proposer des hypothèses diagnostiques en indiquant la probabilité et la fiabilité des résultats. Déjà largement diffusées, elles ont atteint un bon niveau de maturité après l’analyse de centaines de milliers d’images et sont utilisées par plusieurs milliers de praticiens dans le monde. Picoxia, SignalPet, Vetology, VetAi, Radimal, X Caliber: l’abonnement à ces services peut inclure un accès 24 h / 24 à un vétérinaire spécialiste pour obtenir des précisions ou une validation humaine.
Leur taux de précision atteint 92 à 95 % pour la détection d’anomalies. Chaque pixel du cliché est comparé à une immense base d’images archivées, ce qui permet de repérer des signaux trop subtils pour l’œil humain. Ces IA offrent une rapidité d’exécution, une disponibilité continue et ne sont pas sujettes à la fatigue. Les performances (sensibilité, spécificité) font l’objet de publications dans des revues scientifiques, avec des comparaisons systématiques aux résultats obtenus par des radiologues vétérinaires spécialistes. [1] Les résultats sont particulièrement bons pour certaines maladies (ex. œdème pulmonaire cardiogénique, épanchements pleuraux), où la sensibilité et la spécificité dépassent 90 %. En revanche, les performances restent limitées pour l’analyse de masses ou nodules pulmonaires. Les mesures automatisées (VHS, dimensions cardiaques) affichent une excellente fiabilité.
2. Interprétation des images d’examens de prélèvements biologiques
Les sociétés de diagnostic vétérinaire proposent aujourd’hui des plateformes de microscopie numérique intégrant l’IA pour l’analyse automatique d’échantillons (selles, sédiment urinaire, dermatologie, frottis sanguin, masses sous-cutanées, cytologie). Ces appareils préparent l’échantillon, réalisent des clichés haute définition, puis, grâce à des algorithmes entraînés sur d’immenses bases annotées, fournissent en quelques minutes une analyse, un état des lieux et des orientations diagnostiques. Un accès rapide des pathologistes experts reste possible si nécessaire.
Parmi les solutions disponibles : Vetscan Imagyst (Zoetis), capable de réaliser 6 types d’analyses sur un même appareil, ou encore SediVue Dx (sédiments urinaires) et inVue Dx (morphologie cellulaire et cytologie auriculaire) d’Idexx. La fiabilité de ces systèmes est validée par comparaison aux méthodes traditionnelles : l’algorithme de Vetscan Imagyst, par exemple, affiche une sensibilité de 90 – 100 % et une spécificité supérieure à 96 % pour l’analyse coprologique, des performances équivalentes à celles d’un parasitologue expert. [2]
3. L’IA appliquée à l’auscultation
Le stéthoscope intelligent Withapet enregistre les sons cardiaques et pulmonaires du chien et du chat, les analyse et détecte précocement certaines maladies cardiaques (MVD stade B1) avec une précision de 90 %.
III. Des données massives pour prédire ou détecter précocement
Ces dernières années, de vastes entrepôts de données de santé animale ont émergé. VetCompass (Royaume-Uni) rassemble les données de 20 millions de chiens et chats provenant de 1 800 cliniques, tandis que la Mars Petcare Biobank (États-Unis) vise à suivre 20 000 animaux initialement en bonne santé sur dix ans. L’analyse de telles masses de données dépasse les capacités humaines. L’IA permet de croiser symptômes, antécédents, génétique, environnement, alimentation ou comportement, d’identifier des corrélations et de prédire le risque de maladies, parfois avant les premiers signes cliniques.
Un exemple concret est RenalTech, outil issu de 150 000 consultations sur 20 ans dans les cliniques Banfield. Il prédit la maladie rénale chronique du chat jusqu’à deux ans avant les symptômes, avec plus de 95 % de précision, à partir de six données biologiques et de l’âge. Les objets connectés (colliers, litières intelligentes) enrichissent aussi cette approche en transmettant en continu des données utiles à la détection précoce (cardiaque, urinaire). Au-delà de la prédiction des maladies, l’IA ouvre la voie à la personnalisation des traitements et une médecine vétérinaire de plus en plus proactive : passer de la détection à la prévention et l’adaptation des thérapies.
IV. Qu’en pensent les vétérinaires ?
Selon une enquête américaine menée en 2024, [3] seuls 8,6 % des vétérinaires prévoient d’intégrer rapidement l’IA à leur pratique. 30,1 % se disent intéressés mais prudents, tandis que 45,8 % hésitent encore et 15,5 % affichent une réticence ou une opposition nette.
Chez ceux qui l’utilisent déjà, l’IA sert principalement en imagerie médicale (39 %), suivie par la gestion des dossiers et les tâches administratives. Les bénéfices les plus attendus concernent le gain de temps et de productivité (60,6 %), la réduction de la charge administrative (56,1 %) et l’amélioration du diagnostic et du traitement (46,1 %). Pour favoriser une adoption plus large, les vétérinaires soulignent l’importance de disposer d’études scientifiques solides (56,9 %).
V. Intérêt des solutions IA en pratique vétérinaire
- Automatisation des tâches chronophages (interprétation d’images et de données biologiques, rédaction de comptes rendus…)
- Aide à la décision grâce à la proposition de pistes diagnostiques
- Médecine prédictive (détection précoce et traitement anticipé)
- Personnalisation des traitements adaptée à chaque patient
- Réduction des erreurs grâce à l’identification de signaux faibles ou d’anomalies difficiles à percevoir par l’œil humain
- Accès élargi à l’expertise et formation continue via des analyses spécialisées et des compétences diagnostiques avancées
VI. Limites et points de vigilance en pratique
- Fiabilité inégale, avec des performances variables selon les espèces, races, contextes cliniques et qualité des données d’entrée
- Biais algorithmiques (des bases d’apprentissage limitées à certaines populations réduisent la pertinence des résultats pour d’autres)
- Manque de transparence (le fonctionnement des algorithmes, souvent perçus comme des boîtes noires, complique la validation clinique)
- Cadre réglementaire insuffisant, laissant des zones d’incertitude sur la fiabilité, la sécurité et la responsabilité professionnelle
- Risque de sur-dépendance, pouvant diminuer l’acuité clinique si l’IA est utilisée comme substitut plutôt que comme aide
- Contraintes pratiques (impact environnemental, coûts élevés et besoin de formation spécifique)
- Responsabilité maintenue : le praticien reste pleinement responsable des décisions prises avec le soutien de l’IA
VII. Et demain ?
La révolution technologique progresse à une vitesse fulgurante, rendant les prévisions incertaines. Une chose est sûre: l’IA est désormais incontournable et son usage ne fera que s’étendre. Son développement sera porté par la disponibilité croissante de données de qualité, l’optimisation des algorithmes et la puissance accrue des machines. Parallèlement, la demande de preuves de fiabilité et de sécurité renforcera la publication d’études, complétées par des retours d’expérience en pratique quotidienne.
- Développement de nombreux outils d’aide à la décision (imagerie, ophtalmologie, dermatologie, cardiologie)
- Assistance à la détection précoce de maladies grâce à l’analyse des données (maladies chroniques)
- Automatisation des analyses biologiques
- Systèmes de prédiction des risques individuels et plans de prévention adaptés
- Simplification, optimisation des tâches administratives
- Automatisation de la transcription des consultations et des comptes rendus
- Interfaçage avec les logiciels métiers
- Analyse et suivi des indicateurs épidémiologiques
- Identification et accélération du développement de nouveaux médicaments
L’encadrement réglementaire, en dehors de l’IA Act en Europe, ne devrait pas être modifié. Contrairement à aujourd’hui, les entreprises qui développent des outils d’IA devront, dans les prochaines années, définir un modèle économique viable, garantissant un retour sur investissement suffisant pour assurer leur pérennité et leur développement.
VIII. Transparence et validation : incontournables !
La plupart des algorithmes d’IA fonctionnent comme des boîtes noires, fournissant un résultat sans en expliciter le raisonnement. Pourtant, dès lors qu’ils interviennent dans la décision thérapeutique, fiabilité, reproductibilité et transparence deviennent essentielles. Un modèle performant ne suffit pas : il doit être validé par des études cliniques indépendantes, produire des résultats reproductibles dans divers contextes et populations, et éviter l’introduction de biais systémiques.
Les données d’apprentissage sont-elles accessibles, équilibrées, multicentriques ? L’algorithme a-t-il fait l’objet d’une validation externe et indépendante ? Les performances sont-elles stables sur des sous-groupes (race, âge, sexe, comorbidités) ? Peut-on tracer et interpréter les recommandations ou alertes ? Le modèle est-il évolutif ? Peut-il être recalibré au fil du temps ? L’enjeu est d’avoir une IA performante aujourd’hui, et de garantir qu’elle le reste demain, dans un contexte clinique réel, avec ses incertitudes et ses variations.
Les bonnes pratiques
- Utiliser l’IA comme deuxième avis, jamais comme source unique
- Valider systématiquement les résultats par un examen clinique et le jugement humain
- Choisir des solutions transparentes sur leur méthodologie et validées par des études indépendantes
- Former l’équipe à l’utilisation et à l’interprétation des résultats
- Savoir gérer les désaccords entre l’IA et le praticien
Bibliographie
- BOISSADY, E, DE LA COMBLE, A, ZHU, X, and HESPEL, AM. Artificial intelligence evaluating primary thoracic lesions has an overall lower error rate compared to veterinarians or veterinarians in conjunction with the artificial intelligence. Vet Radiol Ultrasound. 2020; 61,619–627. doi: 10.1111/vru.12912.
- NAGAMORI Y, SEDLAK RH, DEROSA A, et al. Évaluation du VETSCAN IMAGYST, un système de détection de parasites fécaux canins et félins en clinique, intégré à un algorithme d'apprentissage profond. Vecteurs de parasites. 2020; 13,1346. doi: 10.1186/s13071-020-04215-x
- GABOR S, DANYLENKO G, VOEGELI B. Familiarity with artificial intelligence drives optimism and adoption among veterinary professionals (2024 survey). Am J Vet Res. 2025 Feb; 118(6S1): S63–S69. doi: 10.2460/ajvr.24.10.0293
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Intérêt de l'électrophorèse des protéines urinaires en gel d'agarose (SDS-AGE) chez les chiens atteints de maladie rénale chronique protéinurique : un potentiel outil prédictif de la progression et de la survie
Introduction
Les maladies rénales chroniques (MRC) sont courantes chez le chien et altèrent significativement la qualité de vie ainsi que la survie. La majorité des MRC sont associées à une protéinurie, dont l'origine peut être glomérulaire, la plus fréquente, tubulaire ou mixte. La présence d'une composante tubulaire pourrait témoigner d'un dépassement fonctionnel du mécanisme de réabsorption tubulaire – secondaire à une protéinurie massive par exemple - et/ou d'une atteinte tubulaire lésionnelle - primaire ou secondaire à une toxicité des protéines urinaires, suggérant ainsi une MRC plus avancée. L'électrophorèse des protéines urinaires (EPU) constitue une méthode non invasive, accessible et peu onéreuse de caractérisation de la protéinurie. Parmi ces techniques, l'électrophorèse en gel d'agarose contenant du dodécyl sulfate de sodium (SDS-AGE) présente l'avantage d'une moindre toxicité pour l'opérateur et d'un coût réduit, mais reste peu étudiée en médecine vétérinaire. Cette étude vise à évaluer l'association entre le profil SDS-AGE (glomérulaire, mixte ou tubulaire) et l'évolution ainsi que la survie chez des chiens atteints de MRC protéinurique.
Matériel et méthodes
Une étude rétrospective a été menée sur des chiens atteints de MRC protéinurique persistante (2 rapports protéines/créatinine urinaire (RPCU) supérieurs à 0,5 à au moins 2 mois d'intervalle) ayant bénéficié d'une SDS-AGE. Un profil semi-quantitatif (glomérulaire, mixte, tubulaire) a été attribué selon une méthode préalablement validée. Les données cliniques et biologiques, les valeurs de créatininémie à 2, 6, 12, 24, 36, 60 et 84 mois (plus ou moins 25 %) ainsi que la date et le motif de décès ont été recueillis. Les analyses statistiques incluaient les tests de KRUSKAL-WALLIS et de DUNN pour les comparaisons entre profils SDS-AGE à l'admission, les courbes de KAPLAN-MEIER avec test de log-rank pour l'analyse de survie et une modélisation par régression Ordinary Least Squares (OLS) pour l'évolution de la créatininémie.
Résultats
Au total, 99 chiens ont été inclus, dont 38 % sont décédés secondairement à leur MRC. La médiane d'âge au diagnostic était de 7 ans. Les races les plus représentées étaient les Terriers (22 %), les chiens de chasse (20 %), les Bergers (12 %) et les Retrievers (9 %). Une cause systémique de la protéinurie a été identifiée dans 28 % des cas.
Les profils SDS-AGE ont été identifiés comme glomérulaires (47 %), mixtes (38 %) et tubulaires (15 %). L'albuminémie était significativement plus faible dans le groupe mixte que dans le groupe tubulaire (p = 0,0137), la créatininémie plus élevée dans les groupes mixte (p = 0,0016) et tubulaire (p = 0,0091) comparés au groupe glomérulaire, la phosphatémie plus élevée dans le groupe mixte que dans le groupe glomérulaire (p = 0,0310) et le RPCU plus faible dans le groupe tubulaire que dans le groupe mixte (p = 0,0393). La médiane de survie était significativement plus longue en cas de profil glomérulaire (10 mois) qu'en cas de profil mixte (1 mois ; p=0,0024) et tubulaire (1 mois ; p=0,00028).
Les modèles OLS prédisant la créatininémie à 2 mois (R2 0,90), à 6 mois (R2 0,94) et à 12 mois (R2 0,90) incluaient respectivement comme variables significatives, à 2 mois, la créatininémie (ß = 337), l'urémie (ß = -101) et la présence de bande tubulaire (ß = 254), à 6 mois, la créatininémie (ß = 147), la chlorémie (ß = -37) et la présence de bande tubulaire (ß = 156) et à 12 mois la créatininémie (ß = 264) et la présence de bande tubulaire (ß = 218).
Conclusion
Cette étude est la première à démontrer une corrélation entre le profil semi-quantitatif de l'EPU d'admission et la progression et la mortalité en cas de MRC. Ces résultats supportent l'utilisation de la technique SDS-AGE en pratique clinique.
Les modèles prédictifs de la créatininémie à 2, 6 et 12 mois proposés présentent des performances élevées. Ils offrent une approche simple, rapide, peu onéreuse et accessible pour le suivi des patients.
Toutefois, des études à plus large échelle restent nécessaires pour confirmer ces résultats et affiner l'intégration de la SDS-AGE dans la prise en charge des MRC protéinuriques du chien.
Bibliographie
- DORNELAS, L.R.S.M., OROZCO, A.M.O., LÓPEZ, C.J.R., et al. (2021) Application of serum and urinary electrophoresis as an aid tool for evaluating dogs at different stages of chronic kidney disease. Comparative Clinical Pathology vol. 30, n° 4, p. 593-603. [https://doi.org/10.1007/s00580-021-03231-2](https://doi.org/10.1007/s00580-021-03231-2)
- LAVOUÉ, R., TRUMEL, C., SMETS, P.M.Y., et al. (2015) Characterization of Proteinuria in Dogue de Bordeaux Dogs, a Breed Predisposed to a Familial Glomerulonephropathy: A Retrospective Study. PloS One vol. 10, n° 7, p. e0133311. [https://doi.org/10.1371/journal.pone.0133311](https://doi.org/10.1371/journal.pone.0133311)
- THÉRON, M.-L., PIANE, L., LUCARELLI, L., et al. (2017) Effects of storage conditions on results for quantitative and qualitative evaluation of proteins in canine urine. American Journal of Veterinary Research vol. 78, n° 8, p. 990-999. [https://doi.org/10.2460/ajvr.78.8.990](https://doi.org/10.2460/ajvr.78.8.990)
- ZINI, E., BONFANTI, U., ZATELLI, A. (2004) Diagnostic relevance of qualitative proteinuria evaluated by use of sodium dodecyl sulfate-agarose gel electrophoresis and comparison with renal histologic findings in dogs. American Journal of Veterinary Research vol. 65, n° 7, p. 964-971. [https://doi.org/10.2460/ajvr.2004.65.964](https://doi.org/10.2460/ajvr.2004.65.964)
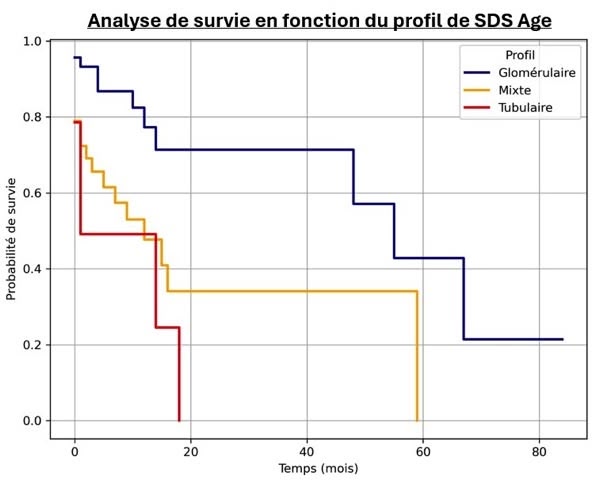
Figure 1
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Intérêt de l'examen du fond d'œil dans le diagnostic et le suivi de l'hypertension artérielle
Nîmes, France
I. Œil et hypertension artérielle
L’hypertension artérielle (HTA) est une affection fréquente chez les carnivores domestiques, notamment dans l’espèce féline. Elle se définit comme une augmentation durable de la pression artérielle systolique. L’hypertension artérielle a plusieurs origines possibles mais, quelle qu’en soit la cause, ses principaux organes cibles sont l’œil, le rein, le cœur et le cerveau.
Bien que l’HTA soit courante chez le chat âgé, cette affection reste considérée comme sous-diagnostiquée. La mesure de la pression artérielle (PA) en consultation ou au cours d’une hospitalisation est possible mais l’examen peut être difficile à réaliser sur des patients stressés et les mesures ne sont pas toujours fiables. Près de 60 % des chats hypertendus présentent des anomalies à l’examen du fond d’œil. [1] L’examen oculaire et notamment du fond d’œil offre donc une fenêtre précieuse sur l’organisme, permettant de visualiser de manière non invasive, in vivo, la vascularisation d’un des organes cibles de l’HTA. Certaines spécificités de la vascularisation oculaire sont à noter. L’œil est doté d’une barrière hémato-rétinienne. Cela correspond à la présence de jonctions serrées entre les cellules endothéliales des vaisseaux rétiniens, et entre les cellules de l’épithélium pigmentaire de la rétine EPR. En cas d’HTA, la présence d’une vasoconstriction réflexe entraîne la perte de la capacité d’autorégulation ainsi que des lésions vasculaires. Il s’ensuit la rupture de cette barrière hémato-rétinienne permettant la fuite de liquide depuis la choroïde vers la rétine ou au sein de la rétine. Les conséquences de ces phénomènes, au sein de l’œil, sont des hémorragies ainsi que de l’œdème ou un transsudat rétinien (œdème rétinien, ou décollement rétinien). Des modifications vasculaires sont également présentes. [2]
II. Quand suspecter une HTA ?
Le diagnostic de l’HTA nécessite une démarche rigoureuse. La présence de lésions oculaires associées à l’HTA doit être suspectée pour tout patient présentant une affection susceptible de provoquer une HTA ou en cas d’apparition de modifications oculaires telles qu’une perte de vision brutale, ou de changement d’aspect des yeux.
1. Présentation clinique
Fréquente chez le chat, l’HTA touche principalement des individus âgés de plus de 10 ans. Elle concerne également le chien de manière moins fréquente. On peut distinguer, l’HTA primaire ou idiopathique, de l’HTA secondaire. Les principales causes d’HTA secondaire sont la maladie rénale chronique, l’hyperthyroïdie, l’hyperaldostéronisme, l’hypercorticisme, le phéochromocytome, le diabète sucré.
2. Motif de consultation en ophtalmologie
Les signes d’appel oculaires les plus fréquents sont la perte de vision brutale en cas de décollement rétinien complet bilatéral et le changement d’aspect de l’œil. Ce dernier peut être décrit comme la présence de sang à l’intérieur de l’œil en cas d’hyphéma ou d’une mydriase en cas de lésions rétiniennes avancées. L’HTA est une cause majeure de perte de vision brutale chez le chat âgé. Le diagnostic est souvent tardif. En effet, la baisse de l’acuité visuelle reste difficile à identifier pour les propriétaires. Ainsi, plus de la moitié des chats présentant une rétinopathie hypertensive sont aveugles au moment de la première consultation [3].
L’observation des lésions de rétinopathie hypertensive peut également se faire dans le cadre d’un dépistage chez un sujet hypertendu ou suspect d’HTA. Ces observations viendront dans ce dernier cas confirmer la suspicion diagnostique.
3. Examen oculaire
Les manifestations oculaires de l’HTA peuvent être plus ou moins importantes. Les lésions oculaires associées à l’HTA sont par ordre d’apparition : la tortuosité artérielle rétinienne, l’hémorragie intra-rétinienne, pré-rétinienne ou sous-rétinienne, l’œdème sous-rétinien, le décollement bulleux, le décollement rétinien, la dégénérescence rétinienne, l’hyphéma, le glaucome secondaire. [2] Une bonne connaissance des variations physiologiques du fond d’œil chez les carnivores domestiques est un prérequis pour pouvoir détecter de manière fiable, les lésions associées à l’HTA
L’examen fonctionnel peut mettre en évidence une altération de la fonction visuelle : réponse à la menace, à l’éblouissement et réflexes photomoteurs pouvant être altérés voire une cécité totale. L’examen du segment antérieur peut quant à lui mettre en évidence un hyphéma partiel ou total (présence de sang en chambre antérieure). L’examen du fond d’œil permet de relever la présence de lésions caractéristiques, seules ou en association (Photo 1). [4][2]
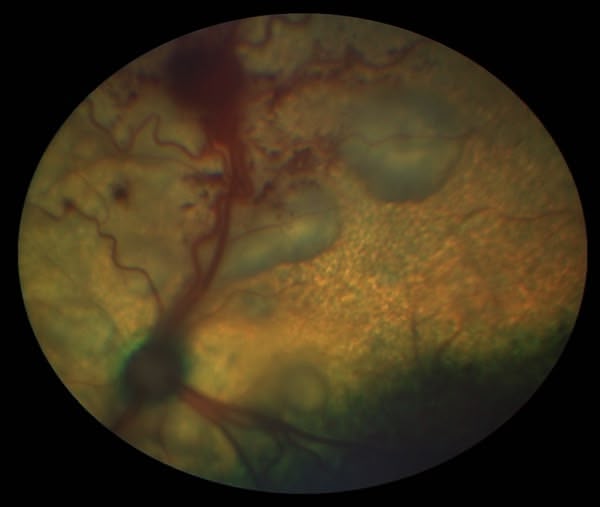
Photo 1 - Rétinopathie hypertensive chez un chat : œdème rétinien, décollements bulleux, hémorragies rétiniennes, et tortuosité vasculaire crédit ENVT
- la tortuosité des artérioles et rétrécissement des artérioles sont la conséquence d’une vasoconstriction persistante
- les hémorragies sous-rétiniennes/rétiniennes/prérétiniennes ou vitréennes sont de manière générale plus facilement visibles en région du tapis. Les hémorragies sous-rétiniennes proviennent des vaisseaux choroïdiens alors que les hémorragies rétiniennes et prérétiniennes proviennent des vaisseaux rétiniens. Les hémorragies sous-rétiniennes se présentent sous la forme de nappes rouges, sombres, surélevant les vaisseaux rétiniens. Les hémorragies rétiniennes sont caractérisées par la présence de taches rouges ponctiformes ou en flammèches. Enfin les hémorragies prérétiniennes ou vitréennes se présentent sous la forme de nappes rouges masquant le reste du fond d’œil. Lorsqu’elles sont importantes, la présence d’une teinte rouge peut être observée à distance, dans l’aire pupillaire.
- L’œdème rétinien est provoqué par la fuite de fluide depuis l’espace choroïdien. Il se manifeste par une atténuation du reflet issu du tapis. Les lésions sont souvent multifocales, rondes, grisâtres. Elles sont bien identifiables en région du tapis
- les bulles rétiniennes ou décollements bulleux (exsudation sous-rétinienne, entre la neuro-rétine et l’EPR) se manifestent sous la forme de lésion rondes, bien délimitées, légèrement surélevées, grisâtres en périphérie et claires en leur centre.
- le décollement de rétine peut être localisé ou complet. Il se présente sous la forme d’une zone floue, bien délimitée, correspondant à l’avancement du feuillet rétinien par rapport au reste du fond d’œil. Lorsqu’il est complet, on peut observer lors de l’examen à distance, la présence d’une mydriase et d’un voile vascularisé, flottant en arrière du cristallin (Photo 2)
- la dégénérescence rétinienne se manifeste par une hyperréflectivité de la zone du tapis et une atténuation du calibre vasculaire. La présence de bandes radiaires hyper réfléchives est parfois constatée. Dans les stades avancés, on peut même noter l’absence de vascularisation rétinienne identifiable et une papille optique terne.
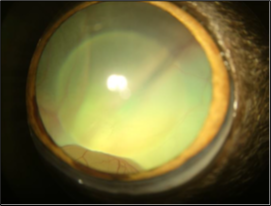
Photo 2 - Décollement rétinien chez un chat hypertendu : observation de la rétine flottant derrière le cristallin, dans l’aire pupillaire crédit ENVT
III. La place de l’examen ophtalmologique dans le diagnostic et le suivi de l’HTA
L’apparition des lésions oculaires de l’HTA peut survenir de manière aiguë (décollement rétinien par exemple en cas de dégradation marquée et brutale de la PA) mais la rétinopathie hypertensive est généralement évolutive sur plusieurs mois. Le diagnostic précoce de l’HTA offre les meilleures possibilités thérapeutiques. La prévention joue donc un rôle clé. À titre de comparaison, le dépistage, chez les sujets âgés, est réalisé en routine chez l’Homme. Il reste toutefois peu courant chez l’animal. Pour autant les lésions oculaires évoquées sont bien connues chez les carnivores domestiques et constituent les répercussions cliniques de l’HTA les plus faciles à identifier.
Faire un examen du fond d’œil de routine chez les patients à risque est donc recommandé. Par exemple, un examen du fond d’œil est recommandé annuellement chez tous les chats de plus de 10 ans, même en bonne santé. Une surveillance plus régulière doit être proposée chez tous les patients présentant une maladie chronique susceptible de favoriser l’apparition d’une HTA tous les 3 à 6 mois.
L’intérêt de l’examen ophtalmologique ne se limite pas à la prévention mais fait aussi partie intégrante du diagnostic et du grading de l’HTA. Le diagnostic et la décision de mise en place d’un traitement doivent être fondés sur des mesures fiables de la PA. Or la mesure de la PA peut connaître une grande variabilité en fonction du tempérament, de la position du patient, de la méthode de mesure, de l’expérience de l’opérateur, des conditions de stress etc. Une multiplication des mesures est donc recommandée. La présence de lésions compatibles sur les organes cibles comme l’œil est considérée comme un élément prépondérant dans la décision thérapeutique. La gravité des lésions observées au fond d’œil est par ailleurs corrélée à l’importance de l’hypertension. [1]
Enfin, une fois l’HTA diagnostiquée, le suivi du fond d’œil permet de mettre en perspective les éléments cliniques et les mesures de suivi de la PA. Si les mesures de PA en consultation ne représentent que deux mesures fixes, à un instant t, avec tous les biais de mesure que l’on connait, la recherche renouvelée des lésions rétiniennes permet un suivi précis et parfois d’objectiver un défaut de contrôle de l’HTA lorsque de nouvelles lésions apparaissent. C’est donc un outil complémentaire dans le suivi des patients hypertendus. L’ACVIM recommande de procéder à un suivi rapproché en cas de lésion sérieuse et de progression rapide sur les organes cibles comme l’œil. [5]
Bibliographie
- CIRLA A. et al., Ocular fundus abnormalities in cats affected by systemic hypertension Prevalence, characterization, and outcome of treatment, Vet. Ophthalmol., 2021, 24, pages 185-194.
- CRISPIN S. M. et al., Systemic hypertensive disease and the feline fundus. Vet Ophthalmol. 2001 4 131-40.
- YOUNG W. M. et al., Visual outcome in cats with hypertensive chorioretinopathy, Vet. Ophthalmol., 2019, 22, pages 161-167.
- MAGGIO F. et al., Ocular lesions associated with systemic hypertension in cats 69 cases 1985-1998, J. Am. Vet. Med. Assoc., 2000, 217, pages 695-702.
- ACIERNO M. J. et al., ACVIM consensus statement Guidelines for the identification, evaluation, and management of systemic hypertension in dogs and cats, J. Vet. Intern. Med., 2018, 32, pages 1803-1822.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Intérêt de l'imagerie avant, pendant et après l'intervention chirurgicale
Ollioules, France
Montpellier, France
I. Introduction
De par l’utilisation de l’échographie, du scanner ou des impressions 3D, l’imageur sera très souvent utile voire indispensable au chirurgien, que ce soit pour planifier une intervention, guider le geste opératoire ou assurer le suivi postopératoire.
II. Comment l’imageur aide le chirurgien dans la recherche des corps étranger migrants ?
La migration des corps étrangers entraine diverses lésions dépendant du site de migration et nécessite une prise en charge multidisciplinaire médicale et chirurgicale. Une évaluation par imagerie médicale incluant le plus souvent une combinaison d’échographie et tomodensitométrie ou moins fréquemment l’IRM et la radiographie est généralement effectuée en fonction de la zone concernée. L’imagerie permet de reconnaitre ces lésions, de déterminer leur extension, les conséquences de la migration et parfois de repérer le corps étranger à l’origine des signes ou son site de localisation préférentiel (Figure 1). Ainsi, elle guide le chirurgien dès la phase diagnostique en permettant la planification préopératoire. Ceci peut être illustré par le traitement du pneumothorax spontané lié à la migration d’un corps étranger où, en fin d’examen, le chirurgien connait les localisations anatomiques :
- du site de perforation à traiter et donc la latéralisation du site de thoracotomie
- du corps étranger responsable des signes et d’éventuels corps étrangers additionnels.
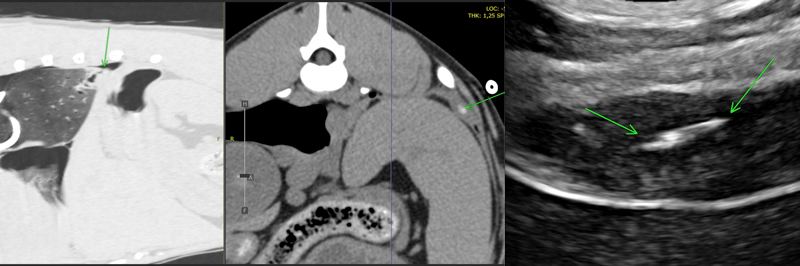
Figure 1
Un corps étranger apparait comme un élément fusiforme, hyperéchogène et provoquant un ombrage acoustique en échographie, hyperatténuant en tomodensitométrie et hypointense dans toutes les pondérations en IRM. Une fois repéré par imagerie, la localisation du corps étranger peut être indiquée au chirurgien par des procédures préopératoires additionnelles si une extraction échoguidée n’est pas possible, incluant une injection de bleu de méthylène ou la mise en place d’une ancre chirurgicale.
L’imagerie médicale peut aussi aider au retrait des corps étrangers en phase peropératoire. Après préparation de l’échographe, une échographie intracavitaire ou du site opératoire peut être effectuée et guider l’approche chirurgicale jusqu'à son extraction. Par exemple, lors d’abcès sous-lombaires, l’échographie peropératoire peut guider la dissection du chirurgien jusqu'au corps étranger et aux cavités devant être débridées voire être complétée d’une extraction échoguidée.
III. Comment l’imageur aide le chirurgien dans la recherche de nœuds lymphatiques dans un contexte oncologique ?
La prise en charge d’un cancer nécessite, dans l’immense majorité des cas, la réalisation d’un bilan d’extension, local, régional et à distance, qui s’intéresse notamment à la présence ou non de métastases nodales.
Le nœud lymphatique sentinelle est considéré comme le premier nœud lymphatique drainant une tumeur et correspond donc au nœud lymphatique d’intérêt lors du bilan d’extension. Il peut être le nœud lymphatique de drainage comme l’anatomie de la zone aurait pu le faire penser mais peut en différer, nécessitant donc de le détecter de façon spécifique pour chaque patient.
La première étape pour détecter un nœud lymphatique sentinelle par l’imagerie est la réalisation d’un lymphangioscanner indirect. En pratique, cela correspond à injecter du produit de contraste en périphérie de la tumeur d’intérêt et de réaliser des séquences au scanner jusqu’à détecter une prise de contraste dans un nœud lymphatique, identifiant ainsi le nœud lymphatique sentinelle.
Afin de parfaire le bilan d’extension, l’exérèse chirurgicale du nœud lymphatique sentinelle est alors recommandée, dans le même temps que l’exérèse chirurgicale de la tumeur primaire, pour analyse histologique. En fonction du nœud lymphatique sentinelle, de sa localisation, sa profondeur, sa taille, ce dernier peut être plus ou moins facile à détecter par le chirurgien lors de l’intervention. Certains nœuds lymphatiques sont facilement repérables par des repères anatomiques, tels que les nœuds lymphatiques mandibulaires, rétro-pharyngiens ou poplités, mais d’autres peuvent être plus complexes à disséquer et à repérer en chirurgie, tels que les nœuds lymphatiques cervicaux, médiastinaux ou lombaires. C’est dans ce cas précis que le repérage préopératoire du nœud lymphatique prend toute son importance afin de faciliter son exérèse. En pratique, le nœud lymphatique sentinelle est repéré par échographie préopératoire. Deux solutions sont communément employées pour « marquer » ce nœud lymphatique :
- utilisation d’un « harpon » ou « ancre chirurgicale.
- injection de bleu de méthylène au sein du nœud lymphatique, sous contrôle échographique.
Les nœuds lymphatiques sentinelles peuvent également être détectés par fluorescence dans le proche infrarouge. En pratique, il s’agit, comme pour le lymphangioscanner, d’injecter du vert d’indocyanine au pourtour de la tumeur primaire. Le vert d’indocyanine émettant une fluorescence dans le proche infrarouge, le nœud lymphatique sentinelle va être détecté via la fluorescence du vert d’indocyanine drainé, depuis le pourtour de la tumeur primaire, à l’aide d’une caméra spécifique illuminant dans le proche intra-rouge.
IV. Comment l’imageur aide le chirurgien à repérer certaines structures anatomiques ?
Pour certaines structures anatomiques précises, l’imagerie pré-opératoire, en particulier le scanner, est indispensable pour adapter la décision de traitement et l’acte chirurgical en lui-même. Prenons le cas de la ligature du canal thoracique dans le cadre du traitement chirurgical d’un chylothorax idiopathique pour illustrer ce propos. L’anatomie du canal thoracique en région thoracique est assez variable d’un individu à l’autre, puisqu’il peut être simple, double voire triple ou quadruple. Il est donc indispensable de préciser l’anatomie spécifique du patient à traiter pour s’assurer que toutes les branches du canal thoracique seront traitées. La réalisation d’un lymphangioscanner est là encore indispensable au chirurgien pour planifier son geste. En pratique, du produit de contraste iodé est injecté dans les coussinets des doigts des membres pelviens qui sont ensuite massés, ou bien en région péri-anale, afin de marquer les voies lymphatiques. Plusieurs séquences scanner sont alors réalisées en région thoracique jusqu’à l’obtention d’un marquage satisfaisant du ou des différentes branches du canal thoracique. En chirurgie, le canal thoracique est très difficilement repérable sans coloration. Le marquage du canal thoracique à l’aide de bleu de méthylène est une des techniques décrites: bleu de méthylène injecté dans les nœuds lymphatiques mésentériques, soit préopératoire sous contrôle échographique, soit directement par le chirurgien via une mini-laparotomie para-costale. La coloration du canal thoracique et de ses différentes branches permet alors une dissection précise et une ligature exhaustive des différentes branches.
Il en sera de même pour les shunts hépatiques. En effet, la réalisation d’un angio-scanner préopératoire est devenue incontournable avant le traitement chirurgical d’un shunt hépatique pour les raisons suivantes :
- description anatomique précise du shunt et notamment de son insertion dans la circulation systémique, afin de guider le chirurgien dans le placement du système d’occlusion du shunt,
- évaluation de la circulation portale hépatique, afin d’apprécier le risque d’hypertension portale,
- possibilité de réaliser une impression 3D du shunt pour les cas complexes.
V. Comment l’imageur aide le chirurgien lors de chirurgies orthopédiques ou neurologiques ?
Lors de chirurgies neurologiques ou orthopédiques complexes, le scanner est souvent indispensable au chirurgien pour la planification chirurgicale, notamment pour les indications suivantes :
- luxation atlanto-axiale,
- fractures ou luxation vertébrales,
- fractures acétabulaires et toute autre fracture articulaire (notamment tarses et carpes),
- déformités angulaires : radius-curvus ou pes varus …
Les reconstructions 3D permettent au chirurgien de repérer les corridors d’implantation des implants vertébraux en cas de chirurgie rachidienne, d’évaluer les axes et l’intensité des corrections angulaires à envisager en cas de déformité ou d’effectuer les choix de traitements et d’implants en cas de chirurgie articulaire.
A partir de ces reconstructions 3D au scanner, peuvent désormais être imprimés facilement et rapidement des modèles en 3D à l’aide d’imprimante 3D « de bureau ». Ces modèles aideront à la visualisation en 3D au bloc opératoire, permettront de « répéter » sur modèle la procédure chirurgicale et être la base de réalisation de guides de perçage ou de coupe pour préciser et accélérer l’acte du chirurgien lors de l’intervention (cf. figure 2).
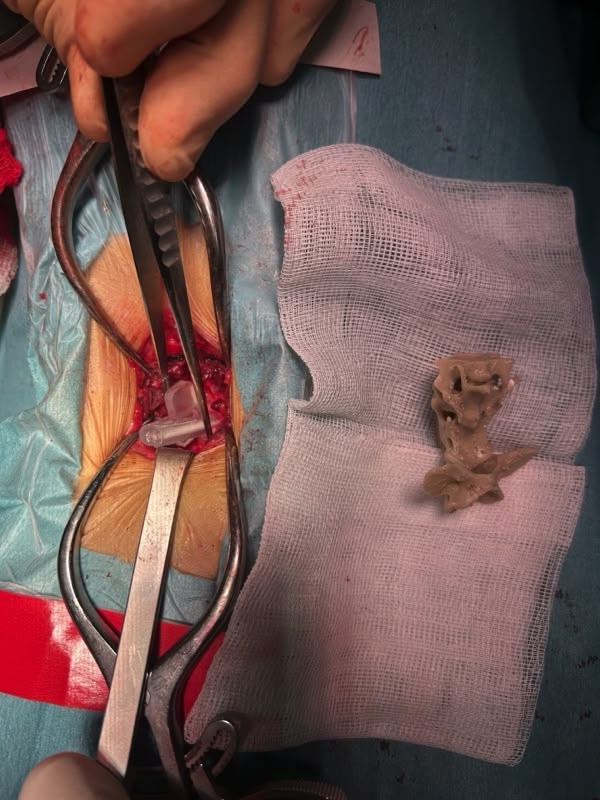
Figure 2
VI. Comment l’imageur aide le chirurgien dans le suivi postopératoire ?
L’imagerie peut enfin orienter le chirurgien lors du suivi postopératoire immédiat ou à distance des patients et indiquer la nécessité d’une ré-intervention.
Dans les cas de chirurgies orthopédiques ou neurologiques complexes précédemment développées, le scanner sera souvent répété en postopératoire car bien plus précis qu’un contrôle radiographique, pour vérifier le bon positionnement des implants et l’absence de pénétration du canal médullaire lors de chirurgies du rachis, ou la qualité des corrections de déformations angulaires des membres. Le scanner pourra aussi être utilisé pour évaluer la décompression satisfaisante et l'absence de récidive en cas de chirurgie de la colonne pour hernie discale ou empyème (discospondylite, origine autre).
En cas de chirurgie abdominale, l’échographie postopératoire est utile pour la recherche de complications précoces. Par exemple, l’échographie s’est révélée sensible et efficace pour la détection des déhiscences intestinales en période postopératoire précoce, permettant une ré-intervention plus rapide pouvant influer sur le pronostic du patient. De la même façon, une évaluation de la perméabilité des sutures peut être effectuée en cas de chirurgie sur les voies biliaires ou urinaires. L’échographie postopératoire peut également montrer un intérêt dans l’évaluation du bon positionnement et de la perméabilité des dispositifs chirurgicaux tels que les systèmes de dérivations urétérales, les dispositifs d’occlusion des shunts porto-systémiques, les stents biliaires/urinaires ou les sphincters hydrauliques.
En conclusion, les liens entre chirurgie et imagerie sont multiples et interviennent dans de nombreuses indications et à chaque étape du parcours chirurgical. Ils précisent la planification peropératoire, guident certaines chirurgies par échographie ou évaluent la nécessité d’une ré-intervention postopératoire immédiate ou à distance pour optimiser la prise en charge du patient et améliorer les résultats chirurgicaux.
Bibliographie
- BAUDIN TRÉHIOU C et coll, CT is helpful for the detection and presurgical planning of lung perforation in dogs with spontaneous pneumothorax induced by grass awn migration: 22 cases. Vet Radiol Ultrasound. 2020 Mar;61(2):157-166
- ROMANSKA M et coll. The use of sentinel lymph node mapping for canine mast cell Tumors. Animals. 2024 Apr 3;14(7):1089.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Intérêt de l'imagerie de l'appareil respiratoire avant endoscopie et prélèvements
Lyon France
Lyon France
I. Introduction
Lors d'affection respiratoire, les intérêts de l'imagerie sont multiples. Elle aide à hiérarchiser les hypothèses diagnostiques et ainsi à guider la suite de la démarche diagnostique : épreuve thérapeutique, autre(s) examen(s) complémentaire(s), choix du geste thérapeutique. [1] L'imagerie, à elle seule, ne suffit généralement pas à établir un diagnostic de certitude. Elle devra être couplée et confrontée aux autres examens complémentaires. Le diagnostic de certitude passe dans la grande majorité des cas par à la réalisation de prélèvements, que ce soit pour la cytologie ou l'histologie.
II. Différents types d'examens d'imagerie dans l'évaluation des affections respiratoires
1. Exploration du thorax
Différentes techniques d'imagerie médicale (radiographies, scanner, échographie) sont à notre disposition pour évaluer l'appareil respiratoire et affiner les hypothèses diagnostiques. Le choix de l'examen d'imagerie dépendra de la localisation suspectée de l'affection. De façon générale, la radiographie reste l'examen de première intention pour l'exploration des affections respiratoires. [1] Bien qu'elle ne permette que rarement d'établir un diagnostic de certitude (collapsus trachéal, corps étranger visible, etc.), elle reste très utile en première intention pour affiner le diagnostic différentiel en fonction de la nature et de la distribution (diffuse ou focale) des lésions et ainsi guider la suite de la démarche : épreuve thérapeutique (suspicion d'asthme non compliqué ou d'atteinte parasitaire par exemple), autres examens d'imagerie, endoscopie et/ou obtention de prélèvements, recherche de parasites, etc.
Le scanner est à réaliser dans un deuxième temps. Il est utile lors de non-évolution des lésions suite à une épreuve thérapeutique, en cas d'images atypiques, de suspicion de masse thoracique ou de corps étranger et lors de bilan d'extension. [2] À l'inverse de la radiographie, le scanner offre une visualisation 3D des structures scannées. Il a également une meilleure résolution et permet une meilleure distinction de la nature des lésions (lésions tissulaires ou liquidiennes).
Cependant, le scanner a une faible sensibilité dans le diagnostic des bronchites chroniques et n'est pas plus informatif que la radiographie . Il permet d'exclure les autres causes possibles de toux (corps étranger, masse non visible à la radiographie, …). L'autre limitation du scanner est qu'il n'est pas dynamique. Il donne une image des structures à un instant t. L'acquisition en phase inspiratoire et expiratoire peut aider à s'affranchir de cette limitation.
L'échographie est très utilisée en urgence pour le diagnostic des pneumothorax ou des épanchements pleuraux liquidiens. Elle permet également le diagnostic des nodules/masses pulmonaires superficielles, des affections interstitio-alvéolaires, des lésions médiastinales. L'échographie a une meilleure sensibilité que la radiographie dans le diagnostic précoce de lésions de pneumonie. [4] Elle permet de réaliser des cytoponctions voire des biopsies échoguidées.
2. Exploration cavités nasales, sinus et nasopharynx
L'exploration par radiographie des cavités nasales, des sinus et du nasopharynx nécessite la réalisation de multiples incidences sous anesthésie générale pour un positionnement adéquat de l'animal. L'anatomie de la face est complexe avec de multiples superpositions en 2D ; l'examen radiographique est donc d'interprétation très délicate et manque de sensibilité. De plus, la distinction entre des sécrétions et du tissu mou remplissant les cavités nasales/sinus (tumeur, muqueuse épaissie) n'est pas possible par radiographie car ces lésions ont la même opacité. Les apports de cet examen restent donc limités. À cela s'ajoutent le risque anesthésique et des coûts non négligeables si tous les clichés sont facturés. L'imagerie en coupe est donc à privilégier, même en première intention, si l'accessibilité et les coûts additionnels ne sont pas un obstacle. [1 La seule exception est la réalisation de radiographies dentaires lorsqu'une maladie parodontale est suspectée. Cependant, cela nécessite d'avoir du matériel de haute résolution.
L'examen tomodensitométrique est nettement plus sensible que l'examen radiographique pour détecter les lésions affectant les cavités nasales et les sinus. Il doit être réalisé de manière optimale : appareil de haute définition permettant des coupes fines, positionnement optimal de l'animal et acquisition supplémentaire après injection de produit de contraste par voie intraveineuse. L'examen tomodensitométrique n'apporte des informations pertinentes pour les tissus mous qu'à l'aide de l'évaluation de leur vascularisation : seule cette dernière permet de distinguer des tissus mous des sécrétions. Cependant, la prise de contraste ne permet pas toujours de différencier les lésions tumorales des lésions inflammatoires. Les corps étrangers peuvent dans certains cas être visibles au scanner. L'association de différentes lésions (lyse osseuse, effet de masse, prise de contraste, affection focale ou diffuse, etc.) permet souvent un diagnostic de présomption mais le diagnostic définitif nécessite généralement la réalisation de biopsies ou la visualisation d'un corps étranger ou de placards aspergillaires.
Face à une suspicion d'atteinte des cavités nasales, des sinus et du nasopharynx, les examens tomodensitométrique et endoscopiques sont souvent complémentaires : évaluation de l'entièreté de l'appareil respiratoire par scanner suivie d'une exploration endoscopique pour la réalisation de prélèvements ciblés pour analyse histopathologique ou pour la réalisation d'un geste thérapeutique. Cette combinaison est « confortable » pour le praticien et est souvent proposée d'emblée aux propriétaires mais s'accompagne d'une majoration des coûts. Selon le contexte, il est souvent envisageable de ne commencer que par un de ces deux examens, quitte à réaliser le deuxième de manière différée si le premier n'a permis de conclure. [5] Le choix de l'examen à privilégier en première intention est plus délicat et s'appuie sur leur disponibilité, sur la localisation suspectée (endoscopie en premier pour une suspicion d'atteinte nasopharyngée ou une recherche de corps étranger) et sur l'hypothèse principale (scanner pour une suspicion de rhinite chronique ou de tumeur suivi de biopsies à l'aveugle si les images tomodensitométriques sont compatibles, ou lors de suspicion de polype pour visualiser les bulles tympaniques et adapter la prise en charge).
III. Apports de l'imagerie dans l'obtention et l'interprétation de prélèvements de l'appareil respiratoire
Les examens d'imagerie permettent d'évaluer la distribution des lésions et de déterminer si les prélèvements de l'appareil respiratoire doivent être réalisés ou non de manière ciblée et par quel abord : voie naturelle ou ponction transpariétale.
1. Évaluer la nécessité d'une endoscopie pour obtenir des prélèvements représentatifs et guider le geste le cas échéant
Si l'examen d'imagerie révèle une lésion focale, qu'elle soit dans une cavité nasale ou dans un lobe pulmonaire, une endoscopie pourra s'avérer nécessaire pour obtenir des prélèvements ciblés. Face à des lésions multifocales ou même diffuses, l'examen d'imagerie permet également de localiser les lésions les plus significatives et donc les régions à privilégier pour la réalisation des prélèvements.
À l'inverse, face à une atteinte diffuse des cavités nasales (suspicion notamment de rhinite chronique) ou d'une masse emplissant la majeure partie d'une cavité nasale, la réalisation de biopsies à l'aveugle par une narine peut s'avérer suffisante. Lors de masse nasale, il convient de s'assurer à l'avance que la lésion est atteignable et de cibler la zone à prélever en mesurant la distance entre la narine et la lésion.
De la même manière, un lavage bronchoalvéolaire peut être réalisé à l'aveugle lorsque les lésions sont diffuses et intéressent notamment les lobes caudaux.
Il convient de rappeler, qu'en plus de l'obtention des prélèvements ciblés, l'endoscopie permet également d'inspecter la lumière et la muqueuse des voies aériennes et apporte ainsi des informations complémentaires à l'imagerie telles que l'aspect du mucus, la détection de collapsus, en particulier dynamiques, etc.
2. Réalisation des prélèvements guidés par imagerie
Face à une ou des lésions focales, des prélèvements ciblés sont nécessaires mais il peut s'avérer qu'un prélèvement transpariétal guidé par imagerie soit plus intéressant qu'un geste guidé par endoscopie :
- la lésion est située dans une zone peu atteignable par endoscopie : lobes pulmonaires crâniaux sur les animaux de petit gabarit, lésion très focale en périphérie d'un lobe pulmonaire, masse nasale caudale sans lyse des cornets, voire non atteignable (médiastin), alors qu'un abord guidé par imagerie (scanner ou échographie) est possible (lésions pulmonaires périphériques, masse nasale avec lyse osseuse) ;
- un prélèvement peu invasif (cytoponction transthoracique) est préféré à un lavage broncho-alvéolaire en première intention en raison des risques anesthésiques et/ou liés à la procédure, en particulier lors d'insuffisance respiratoire.
Si des ponctions transpariétales et une endoscopie sont envisagées de manière concomitante, il est préférable de réaliser les ponctions après l'endoscopie. En effet, les ponctions vont induire des saignements et modifier les résultats de l'endoscopie et du lavage bronchoalvéolaire.
3. Interprétation des résultats d'analyse cytologique ou histologique
Les résultats d'analyse cytologique ou histologique des prélèvements de l'appareil respiratoire doivent toujours être interprétés en prenant en compte le diagnostic différentiel de l'imagerie. Si les conclusions des deux examens diffèrent, la pertinence de leurs résultats doit être questionnée, en particulier celle des analyses cytologiques et histologiques.
Il est en effet fréquent que les prélèvements obtenus ne soient pas représentatifs de l'affection :
- prélèvement paucicellulaire ou contaminé par du sang, notamment lors de cytologie ;
- prélèvement n'ayant pas concerné la lésion primaire : réaction inflammatoire péri-tumorale ou accompagnant un corps étranger, zone de fibrose ou de nécrose, etc. ;
- agents infectieux non présents dans le prélèvement, en particulier lors de parasitisme, contamination bactérienne post prélèvements, etc. ;
- cellules inflammatoires très atypiques mimant un processus tumoral.
IV. Guider une démarche thérapeutique
L'imagerie, et notamment l'imagerie en coupe, peut aider à guider la prise en charge thérapeutique. Par exemple, lors d'aspergillose, la présence ou non d'une lyse de la lame criblée et des cornets nasaux déterminera la voie d'abord possible (endoscopique ou chirurgicale) et les risques liés à une balnéation.
De la même façon, lors de suspicion de polype nasopharyngé, on recherchera une possible extension du polype dans la bulle tympanique, face à laquelle un abord chirurgical de la bulle tympanique serait indiqué et non un simple retrait par traction/avulsion par abord buccal.
Bibliographie
- CAREY SA. Clinical Evaluation of the Respiratory Tract. In: ETTINGER SJ, FELDMAN EC, COTE E, eds, Textbook of veterinary internal medicine. 9th ed. Philadelphia : Elsevier; 2024 : 1117-27
- MASSEAU I, REINERO CR. Thoracic computed tomographic interpretation for clinicians to aid in the diagnosis of dogs and cats with respiratory disease. Vet J. 2019 ; 253 : 105388
- MORTIER JR et coll. Accuracy of and interobserver agreement regarding thoracic computed tomography for the diagnosis of chronic bronchitis in dogs. J Am Vet Med Assoc. 2018 ; 253 : 757-62
- FERNANDES RODRIGUES N et coll. Comparison of lung ultrasound, chest radiographs, C-reactive protein, and clinical findings in dogs treated for aspiration pneumonia. J Vet Intern Med. 2022 ; 36 : 743-52
- FINCK M et coll. Computed tomography or rhinoscopy as the first-line procedure for suspected nasal tumor: a pilot study. Can Vet J. 2015 ; 56 : 185-92
Liens d'intérêt : Subvention de recherche, prestations rémunérées d'expertise, frais d'hospitalité (Boehringer Ingelheim)Conférencière rémunérée (CEVA, Elanco, Bayer, Royal Canin)
📃 Intervalles de référence des ratios métanéphrines/créatinine urinaire chez le chien : comparaison des ratios sur échantillons acidifiés et non acidifiés collectés par cystocentèse
Solène NIEDERLENDER
Coauteurs : Kristina MUSEUX, Suzy VALENTIN
Introduction
Les phéochromocytomes canins sont des tumeurs fonctionnelles rares des glandes surrénales. Leur diagnostic ante mortem est un défi. La bibliographie documentant les intervalles de référence des métanéphrines urinaires est limitée. Deux études récentes [1,2] rapportent des intervalles de référence de concentrations des métanéphrines urinaires libres mesurées par chromatographie liquide couplée à la spectrométrie de masse en tandem (LC-MS/MS). Dans ces deux études, les intervalles de référence ont été déterminés sur des échantillons d'urine recueillis par miction spontanée. En médecine humaine et vétérinaire, les modalités de prélèvement urinaire et sanguin peuvent avoir un impact sur le dosage des catécholamines et de leurs métabolites. Ainsi, historiquement, l'acidification des échantillons urinaires est recommandée afin d'assurer la stabilité des catécholamines et de leurs métabolites in vitro. Malgré deux études humaines [3,4] et une étude vétérinaire [5] montrant l'absence de bénéfice de l'acidification, certains laboratoires recommandent toujours des échantillons acidifiés pour l'analyse.
L'objectif de cette étude était de déterminer les intervalles de référence des ratios métanéphrines totales/créatinine urinaires à partir d'urine collectée par cystocentèse en milieu hospitalier. Un objectif secondaire était de confirmer l'absence de nécessité d'acidifier les échantillons urinaires.
Matériels et Méthode
Quarante chiens asymptomatiques appartenant à des clients ou au personnel d'un hôpital vétérinaire ont été recrutés. Parmi eux, trente-huit chiens sont considérés comme cliniquement sains sur la base d'une analyse hémato-biochimique normale et de glandes surrénales de taille échographiquement normale. Les ratios métanéphrines/créatinine et normétanéphrines/créatinine ont été mesurés par LC-MS/MS sur des échantillons d'urine collectés par cystocentèse échoguidée. Les concentrations dans les échantillons acidifiés et non acidifiés ont été comparées chez les quarante chiens.
Résultats
Aucune différence statistiquement significative n'a été observée entre les échantillons acidifiés et non acidifiés. Une faible corrélation négative a été observée entre le poids et les ratios métanéphrine/créatinine. Sur les dosages des 38 chiens cliniquement sains, les intervalles de référence à 95 % pour les ratios métanéphrines/créatinine et normétanéphrine/créatinine sont respectivement rapportés : [16,42-131,40] et [32,15-225,49] nmol/mmol.
Discussion
Les limites de nos intervalles de référence ne peuvent pas être comparées aux valeurs des études précédentes, ces études mesurant les métanéphrines libres et non totales [1,2]. La méthode de collecte d'urine, ici par cystocentèse et non par urine recueillie spontanément, est également différente.
L'étude présente certaines limitations, notamment la taille réduite de l'échantillon de 38 chiens. De plus, la population aurait bénéficié de l'inclusion de chiens plus âgés, car l'âge médian des chiens dans l'étude était inférieur à celui du diagnostic du phéochromocytome. Enfin, les chiens ont été déterminés sains sur la base de l'absence de signe clinique, des analyses sanguines normales et de l'absence de masse sur les surrénales à l'échographie abdominale. Le risque d'avoir inclus un chien qui n'était pas sain a été jugé faible.
Conclusion
Cette étude confirme que les ratios métanéphrine/créatinine urinaires peuvent être mesurés dans l'urine collectée par cystocentèse et conservée congelée sans acidification. La mesure des métanéphrines devrait être incluse dans l'investigation d'un phéochromocytome suspecté chez le chien et peut être facilement réalisée par les praticiens vétérinaires.
Bibliographie
- NAGATA N, IKENAKA Y, SAWAMURA H, SASAKI N, TAKIGUCHI M. Reference intervals for urinary metanephrines to creatinine ratios in dogs in Japan. J Vet Med Sci. 2024;86(10):1096-1099. doi:10.1292/jvms.24-0163
- VAN DEN BERG MF, KOOISTRA HS, GRINWIS GCM, et al. Reference intervals for plasma, urinary, and salivary concentrations of free metanephrines in dogs: Relevance to the diagnosis of pheochromocytoma. J Vet Intern Med. Published online January 1, 2023. doi:10.1111/jvim.16624
- WILLEMSEN JJ, ROSS HA, LENDERS JWM, SWEEP FCGJ. Stability of urinary fractionated metanephrines and catecholamines during collection, shipment, and storage of samples. Clin Chem. 2007;53(2):268-272. doi:10.1373/clinchem.2006.075218
- PINTO LC, KRAMER CK, CAMARGO JL, CANANI LH, GROSS JL, LEITÃO CB. No effect of acidification or freezing on urinary metanephrine levels. J Endocrinol Invest. 2020;43(1):53-56. doi:10.1007/s40618-019-01076-9
- HÖGLUND K, PALMQVIST H, RINGMARK S, SVENSSON A. Quantification of normetanephrine in canine urine using ELISA: evaluation of factors affecting results. J Vet Diagn Invest. 2022;34(1):28-35. doi:10.1177/10406387211052984
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 L'alimentation, partie intégrante du traitement de maladies métaboliques chez le Chien et le Chat
Boves, France
I. Introduction
Une maladie métabolique peut être héréditaire ou acquise et implique une absence ou un dysfonctionnement d'enzyme(s) nécessaire(s) aux réactions métaboliques cellulaires. Trois exemples sont présentés pour illustrer le lien entre alimentation et traitement d'une maladie métabolique : l'encéphalose hépatique, le diabète sucré, et l'hyperparathyroïdisme secondaire.
II. Alimentation, protéines et encéphalose hépatique lors de shunt porto-systémique
L'ammoniac est produit majoritairement dans le tube digestif par dégradation des acides aminés provenant des protéines. Il provient d'abord des cellules intestinales par leur métabolisme propre, puis du microbiote intestinal. Vient secondairement l'ammoniac produit par les autres organes. Le foie, court-circuité lors de shunt, ne le détoxifie pas en urée. Cependant, si l'ammoniac a un rôle direct indéniable dans les signes neurologiques et les phénomènes inflammatoires qui les accompagnent, d'autres facteurs comme le potassium, les équilibres acido-basiques et électrolytiques sont aussi impliqués, au moins indirectement.
L'adaptation de la ration doit être mise en place rapidement, conjointement au traitement médical, en attendant un traitement chirurgical quand il est possible, ou pour une prise en charge sur le long terme. C'est d'autant plus important car l'animal est en croissance.
Le principe de la prise en charge nutritionnelle est de minimiser la production d'ammoniac conjointement à la correction des désordres acido-basiques et électrolytiques, tout en tenant compte des troubles digestifs souvent présents. Voici les grandes lignes du profil nutritionnel et le mode d'administration de la ration :
- s'assurer que le besoin en énergie est couvert ;
- couvrir sans excès le besoin protéique en fonction du stade physiologique ;
- choisir un aliment thérapeutique hyperdigestible (à visée intestinale ou hypoallergénique contenant des protéines hydrolysées) ;
- éviter si possible l'utilisation des aliments thérapeutiques à visée hépatique sur les animaux en début croissance ;
- déterminer la quantité maximale tolérée de protéines pour un repas ;
- diviser le besoin en protéines par la quantité de protéines tolérées sur un repas : vous aurez le nombre de repas nécessaire par jour ;
- séparer les repas avec 4h d'intervalle en première intention ;
- utiliser les glucides, et les lipides quand cela est possible, pour couvrir les besoins énergétiques, y compris en dehors des repas ;
- remplacer une partie de la ration de viande par des protéines lactées (fromage blanc, fromage) et des protéines végétales (lentilles, soja) dans les rations faites maison ;
- suivre le statut nutritionnel et les signes cliniques pour ajuster la ration ;
- augmenter l'apport en fibres solubles (lactulose ou naturelles) et en acides gras essentiels de la famille oméga 3 (EPA/DHA) ;
- surveiller le poids, la note d'état corporel, le score de masse musculaire ainsi que les signes cliniques et le bilan biochimique. Les apports nutritionnels sont adaptés en conséquence, que ce soit pour du court terme après une chirurgie correctrice pour le retour progressif à une ration d'entretien, ou sur le long terme.
III. Alimentation, glucides et diabète sucré
L'alimentation est indissociable de la prise en charge médicale du diabète sucré : sans ration fixée et constante dans sa composition et sa distribution, la stabilisation de la maladie est délicate, voire impossible. Les glucides sont évidemment au centre des préoccupations mais d'autres paramètres sont essentiels comme les apports en eau, en minéraux et vitamines, ou la gestion du poids et de la masse musculaire.
Les glucides représentent une famille de molécules hétéroclites et nutritionnellement incomparables. « Diminuer les glucides » en cas de diabète ne veut donc pas dire grand-chose.
Le principe de la prise en charge nutritionnelle conjointement au traitement médical lors de diabète sucré est de limiter la fluctuation de la glycémie. Voici les grandes lignes du profil nutritionnel et le mode d'administration de la ration :
- surveiller l'hydratation et supplémenter en minéraux et vitamines si nécessaire, surtout en cas de polyurie-polydipsie ;
- adapter l'apport calorique à l'état corporel de l'animal. Si, en cas d'obésité, une perte de poids est recherchée, la restriction calorique doit être progressive pour ne pas risquer un état acido-cétosique. En cas de maigreur, il faut se souvenir que tant que le traitement ne permettra pas l'entrée du glucose dans les cellules, l'animal continuera de maigrir, quelle que soit la quantité d'aliment ingérée. Lorsque le traitement devient efficace, le glucode peut être exploité et il n'est pas nécessaire de suralimenter ;
- adapter la densité énergétique de la ration à l'appétit de l'animal, faible en cas de polyphagie, élevée pour les petits mangeurs ;
- diminuer l'apport en matières grasses en cas d'hyperlipidémie chez le chien (risque de pancréatite) ;
- interdire les sources de glucides simples ;
- répartir la ration en deux repas, distribués autour de ou des injections d'insuline chez le chien. Ce n'est pas nécessaire chez le chat ;
- choisir de la viande cuite ou lyophilisée pour les friandises si nécessaire ;
- suivre au minimum le statut nutritionnel de l'animal (variation du poids), note d'état corporel, score de masse musculaire, et les signes cliniques comme la faim ou la soif ;
- se rappeler que tout changement alimentaire aura une conséquence sur le traitement médical ;
- éviter de laisser le propriétaire seul face à l'application de monitorage en continu de la glycémie, au risque d'adaptations intempestives de la ration, avec un échec thérapeutique à la clé.
Chez le chat, l'alimentation est à la fois un facteur de prévention, et un facteur pouvant aider à la rémission clinique.
IV. Alimentation, calcium/phosphore et hyperparathyroïdisme secondaire
L'hyperparathyroïdisme secondaire est une activation de la sécrétion de la parathormone due à une diminution de la calcémie. Elle est une complication commune lors de maladie rénale chronique, par altération du métabolisme de la vitamine D (absorption du calcium) et rétention du phosphore. Un déséquilibre nutritionnel peut aussi en être responsable : ration carencée en calcium et mauvais rapport phosphocalcique.
Le principe de prévention (ou la correction) de l'hyperparathyroïdisme secondaire dans le cas d'une maladie rénale chronique consite à assurer des apports phosphocalciques équilibrés. Voici les grandes lignes du profil nutritionnel et le mode d'administration de la ration :
- s'assurer que le besoin en énergie est couvert par un (des) aliment(s) complet(s) ou une ration ménagère complémentée. Attention, surtout chez le chat, de nombreux aliments humides sont complémentaires ; ce qu'ignorent souvent les propriétaires ;
- quantifier les sources de calcium, de phosphore et de vitamine D de la ration (aliment, suppléments et friandises) réellement consommées par l'animal. Attention aux compléments minéraux et vitaminiques et à toutes autres suppléments : il y a vraiment de tout !
- Éliminer de la ration tous les aliments/suppléments dont la teneur en calcium et phosphore ne sont pas connues ;
- éviter de supplémenter en calcitriol à l'aveugle, surtout en présence d'une hyperphosphatémie ;
- rééquilibrer l'apport en calcium, sans excès ;
- limiter l'apport en phosphore progressivement et selon la situation clinique, en gardant un rapport Ca/P inférieur ou égal à 2 ;
- fractionner la ration de la journée en au moins trois repas, pour augmenter la tolérance digestive et métabolique, et favoriser la prise alimentaire chez les animaux dysorexiques ;
- vérifier les constantes sanguines 1 mois après la fin de la transition vers le nouveau régime.
Le contrôle du calcium, du phosphore et du calcitriol est primordial pour la prévention de l'hyperparathyroïdisme secondaire. Par ce biais, l'alimentation fait partie intégrante de la prise en charge de la maladie rénale chronique.
Bibliographie
- CHIANG CF, VANDERSTICHEL R, STOCKMAN J, LARSEN JA, FASCETTI AJ. Diurnal variation of serum phosphorus concentrations in intact male adult domestic cats. J Vet Intern Med. 2024 Nov-Dec;38:3153-3161.GOW AG. Hepatic Encephalopathy. Vet Clin North Am Small Anim Pract. 2017 May;47:585-599.
- COOK, Audrey B. V. M. S., & DECVIM-CA, D. A. B. V. P. What's New in the Management of Feline Chronic Kidney Disease.
- GOW AG. Hepatic Encephalopathy. Vet Clin North Am Small Anim Pract. 2017 May;47:585-599.
- GRAVES, T. K., & GILOR, C. (Eds.). . Diabetes Mellitus in Cats and Dogs, An Issue of Veterinary Clinics of North America: small Animal Practice, E-Book (Vol. 53, No. 3). Elsevier Health Sciences.
- STOCKMAN J. Dietary phosphorus and renal disease in cats: where are we? J Feline Med Surg. 2024 Oct;26:1098612X241283355
Liens d'intérêt : En tant que consultante indépendante, je réalise des missions pour des fabricants d'aliments industriels, des fournisseurs d'ingrédients et des laboratoires pharmaceutiques. Aucune de ces entreprises n'est intervenue dans le cadre de cette conférence.
📃 L'entretien : le meilleur outil pour travailler le lien avec son personnel
Chozeau, France
I. Introduction
Dans un contexte où la performance collective repose autant sur l'expertise technique que sur la qualité des relations humaines, l'entretien, qu'il soit annuel, de suivi ou de recadrage – se révèle être un outil central pour construire, renforcer et ajuster le lien entre managers et collaborateurs. Trop souvent réduit à une formalité administrative ou à une obligation légale, l'entretien est pourtant l'espace privilégié où se conjuguent écoute, reconnaissance et projection et où la récolte d'informations est un enjeu clé.
II. L'entretien comme levier relationnel
Un entretien n'est jamais neutre. Pour le collaborateur, c'est un moment qui lui est consacré, lors duquel il peut se sentir reconnu, entendu, valorisé – ou au contraire jugé, incompris et déstabilisé. Pour le manager, c'est une opportunité de clarifier les attentes, d'aligner les objectifs, mais aussi de prendre la mesure du climat émotionnel et relationnel au sein de son équipe.
La relation ne se construit pas uniquement au quotidien, l'entretien constitue un moment suspendu qui donne de la profondeur au lien. Il permet de sortir de la pression opérationnelle et de créer un espace d'échange authentique, où l'on prend le temps de parler avec et non seulement à son collaborateur.
III. Les conditions de réussite
Un entretien porteur de valeur repose sur plusieurs conditions essentielles :
- Un cadre clair : le collaborateur doit savoir pourquoi il est convié, quel est l'objectif de l'entretien, les sujets qui seront abordés et ce qui est attendu de lui. La transparence préalable évite l'angoisse et favorise la confiance et l'authenticité des échanges.
- Une écoute active et sincère : l'entretien n'est pas une succession de constats unilatéraux. C'est un dialogue, où la reformulation et les questions ouvertes jouent un rôle clé.
- La reconnaissance : au-delà de l'évaluation des résultats, l'entretien doit mettre en lumière les efforts, les contributions et les qualités humaines du collaborateur. La reconnaissance sincère nourrit la motivation et renforce le sentiment d'appartenance.
- Une projection constructive : l'entretien n'a pas vocation à ressasser le passé indéfiniment, mais à construire l'avenir. Qu'il s'agisse de fixer de nouveaux objectifs, d'accompagner un développement de compétences ou d'explorer des perspectives d'évolution, la dynamique doit rester orientée vers le futur.
IV. Des formes d'entretien multiples
L'entretien n'est pas un format unique et figé. Selon le contexte et les besoins, il peut prendre des formes diverses :
- L'entretien annuel (bisannuel) ou professionnel : moment structurant, encadré par la loi pour le professionnel, il permet de faire le point global sur le parcours et les aspirations du collaborateur.
- L'entretien de suivi : plus court, plus régulier, il installe une relation continue et évite que les tensions ou frustrations ne s'accumulent.
- Le feedback constructif et le recadrage : parfois délicat mais indispensable, il vise à comprendre et réajuster des comportements, actions, ou performances, en posant ou reposant un cadre clair sans dévaloriser. Bien conduit, il peut être une étape clé pour restaurer le lien de confiance et engager le collaborateur dans une dynamique d'amélioration continue.
- Le feedback positif : souvent négligé, il contribue pourtant à la consolidation des bons comportements dans l'équipe, à la motivation et à la fidélisation des talents.
V. Quand l'entretien devient outil de prévention des conflits
Nombre de tensions en entreprise trouvent leur origine dans des malentendus, des non-dits ou un manque de reconnaissance perçu. L'entretien, parce qu'il instaure un espace d'expression, permet d'identifier en amont des signaux faibles : une démotivation, un sentiment d'injustice, une incompréhension autour des rôles et responsabilités.
En donnant la parole, le manager détecte ce qui pourrait, s'il était ignoré, évoluer à bas bruit en conflit. L'entretien devient alors un outil de régulation préventive, évitant que les liens ne se distendent irrémédiablement.
VI. Les erreurs à éviter
Mal conduit, l'entretien peut produire l'effet inverse de celui recherché. Parmi les écueils fréquents :
- le transformer en procès à charge, centré uniquement sur les erreurs,
- en faire un monologue du manager, sans laisser de place au collaborateur,
- le réduire à une simple formalité administrative,
- ou encore négliger le suivi, laissant l'entretien sans suites concrètes.
Ces erreurs fragilisent la relation et décrédibilisent le manager.
VII. Le rôle du manager-médiateur
Conduire un entretien ne s'improvise pas, il doit être anticipé et préparé pour anticiper les réactions de son interlocuteur, ses éventuelles objections et ne pas perdre le fil voire l'objectif que l'on s'est fixé pour ce temps d'échange. Cela suppose également de travailler ses compétences relationnelles : écoute active, gestion des émotions, capacité à poser des questions ouvertes, mais aussi à reformuler et recadrer sans blesser. Le manager devient, le temps de l'entretien, un médiateur entre les attentes de l'entreprise et les besoins du collaborateur.
En travaillant cette posture, il renforce non seulement la qualité du lien individuel, mais aussi la cohésion globale de l'équipe.
VIII. Conclusion
L'entretien est bien plus qu'une obligation managériale : c'est un outil stratégique de management relationnel. Il permet de reconnaître, d'aligner, de prévenir, de recadrer et de projeter. Utilisé régulièrement et avec authenticité, il devient le ciment du lien entre le manager et ses collaborateurs, favorisant à la fois l'engagement individuel et la performance collective.
Travailler le lien, c'est investir dans la confiance. Et l'entretien, lorsqu'il est mené avec soin et sincérité, reste le meilleur outil pour nourrir cette confiance au quotidien.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 L'examen cytologique spécialisé : un partenariat entre le laboratoire et le généraliste
Gentilly, France
I. Introduction
La cytologie est un outil incontournable de la pratique vétérinaire quotidienne. Elle permet d'obtenir rapidement des informations sur la nature d'une lésion ou l'état d'un organe, et d'orienter les décisions cliniques en soutenant le dialogue avec les propriétaires. Accessible et peu coûteuse, elle se distingue par sa rapidité et son faible caractère invasif par rapport à l'histologie. Pourtant, la valeur de cet examen ne repose pas uniquement sur la compétence du cytologiste. Elle dépend également de l'indication, de la qualité du prélèvement et du contexte clinique fourni par le vétérinaire prescripteur.
La cytologie spécialisée est le fruit d'une véritable collaboration : le praticien généraliste, qui connaît l'animal, son anamnèse et ses examens complémentaires, et le laboratoire, qui apporte son expertise morphologique et technique.
II. Indications et non-indications de l'examen cytologique
1. Indications de l'examen cytologique
La cytologie est l'examen de choix pour explorer les masses cutanées et sous-cutanées. Elle permet, dans un certain nombre de cas, de différencier une lésion inflammatoire d'une tumeur bénigne ou maligne, ce qui conditionne la prise en charge thérapeutique ou chirurgicale.
Elle est également indiquée en cas d'adénopathies pour distinguer adénopathies réactionnelles et lymphomes, détecter des agents infectieux (ex. leishmanies) ou mettre en évidence une infiltration métastatique dans le cadre d'un bilan d'extension.
Seul examen adapté à l'étude des liquides (épanchements, LBA, LCR, liquides synoviaux…), elle permet, associée à d'autres analyses (cellularité, protéines, biochimie), de préciser le type d'épanchement (transsudat, exsudat…) et son mécanisme physiopathologique. Si elle n'apporte pas toujours un diagnostic étiologique, elle le permet dans certains cas (épanchements tumoraux ou septiques).
En cas d'atteintes viscérales (foie, rate, poumon, pancréas, rein…), la cytologie contribue à établir un diagnostic, écarter certaines hypothèses, ou apporter des réponses cliniques utiles pour orienter rapidement la prise en charge.
Enfin, elle est indiquée dans le suivi thérapeutique, notamment pour évaluer la réponse à une chimiothérapie.
2. Non-indications et limites de l'examen cytologique
La cytologie, bien qu'extrêmement utile, ne permet pas toujours d'établir un diagnostic étiologique et n'est pas indiquée dans toutes les situations. Certaines contre-indications doivent être connues afin d'éviter des complications ou des résultats décevants.
Sur le plan médical, les troubles de l'hémostase constituent la principale limite : une cytoponction d'organes internes expose alors à un risque hémorragique sévère. Les masses très vascularisées (ex. hémangiosarcomes) ne devraient pas être ponctionnées sans évaluation préalable.
D'autres limites sont liées à la nature même d'examen. La cytologie repose sur l'étude de cellules isolées, et non sur l'architecture tissulaire. Ainsi, dans le cas de tumeurs nécessitant une évaluation histologique pour confirmer leur nature (ex : tumeurs mal différenciées), déterminer le caractère bénin ou malin (critères architecturaux…) ou établir un grading (ex : sarcomes, mastocytomes), la cytologie ne peut fournir qu'une orientation partielle. De même, les lésions fibreuses, scléreuses ou nécrotiques donnent des prélèvements pauvres en cellules, rendant l'interprétation souvent impossible. L'hémodilution est également un facteur limitant.
Il est important, avant de réaliser un examen cytologique, d'avoir une bonne compréhension de ce que cet examen peut réellement apporter. En effet, il ne faut pas attendre de la cytologie qu'elle fournisse une réponse définitive et exhaustive dans toutes les situations. Par exemple lors d'inflammations hépatiques, l'analyse histologique reste l'examen complémentaire de choix même si la cytologie peut apporter certaines informations intéressantes. La cytologie rénale est particulièrement utile en cas de suspicion de lymphome, mais peu informative pour les atteintes inflammatoires. Lors de lésions kystiques liquidiennes (hépatiques, prostatiques…), les prélèvements cytologiques sont souvent peu cellulaires.
Connaître les limites de cet examen, évite des attentes irréalistes vis-à-vis du cytologiste et permet de mieux informer les propriétaires.
III. La phase pré-analytique : un facteur déterminant de la fiabilité de l'examen
La réussite d'une cytologie repose sur un geste adapté et une préparation soignée. Le vétérinaire choisit la technique en fonction de la localisation et des caractéristiques de la lésion (cytoponction à l'aiguille fine avec ou sans aspiration, choix de la taille de l'aiguille et de la seringue…). Plus les diamètres de l'aiguille et de la seringue seront importants et plus le risque d'hémodilution sera élevé. La technique par aspiration est plus traumatisante que la technique par carottage, ce qui augmente également le risque d'hémodilution. Dans certains cas (ex : tissus fermes (fibrosarcome…)) la technique par aspiration sera à privilégier pour tenter d'obtenir du matériel cytologique en dépit du risque de contamination sanguine.
Plusieurs précautions doivent être respectées pour un prélèvement de qualité. Il convient en effet d'éviter certaines erreurs courantes qui peuvent nuire à la puissance diagnostique de l'examen.
- Étalement inadapté : éviter un frottis trop appuyé, un dépôt excessif ou sans étalement. L'étalement doit être délicat pour éviter d'écraser les cellules. L'étalement doit également être monocouche pour permettre une bonne coloration et une bonne observation des cellules. Un peu de matériel est déposé sur une lame à 1 cm du côté maté de la lame. Une autre lame est apposée sur la première. Le matériel est comprimé délicatement mais fermement entre les 2 lames, et la seconde lame est glissée le long de la première dans un mouvement contenu et délicat.
- Ponction du centre des masses volumineuses : à proscrire car souvent nécrotique. Il est préférable de ponctionner tangentiellement à la surface de la masse.
- Séchage insuffisant : les lames doivent être séchées à l'air libre ou au sèche-cheveux (en position froide). Les prélèvements gras nécessitent 24 h de séchage avant coloration. Il convient d'utiliser une boite de transport adaptée et d'éviter les boites en carton sur lesquelles les prélèvements sont susceptibles de se coller.
- Usage de gel échographique : le gel échographique se colore en violet à la cytologie et gêne fortement l'observation des cellules lorsqu'il est présent en grande quantité. Il est donc préférable, lors de cytoponctions échoguidées, d'utiliser l'alcool comme agent de contact.
- Fixateur ou vapeurs de formol : le fixateur ou le formol entraînent une coloration inadéquate des cellules. Il est préconisé, en cas d'envoi conjoint de prélèvements cytologiques et histologiques, d'utiliser deux sachets hermétiques séparés prévus à cet effet.
- Absence d'étalements des liquides ou erreur de tube : les liquides (épanchements, LBA, LCR, urines, liquides articulaires,…) doivent être prélevés sur tube EDTA. L'utilisation d'un tube sec par exemple entraîne la présence d'artefacts (activateurs de coagulation) gênant la lecture cytologique. Il est recommandé de transmettre un étalement direct et de culot réalisés au chevet de l'animal (à préciser sur les lames), afin de se prémunir d'une dégradation trop importante des cellules et d'éviter tout artefact pouvant survenir in vitro (prolifération bactérienne, érythrophagocytose…).
- Demande d'analyse incomplète : la feuille de demande d'analyse est un outil diagnostique à part entière. Elle doit mentionner le signalement de l'animal, l'anamnèse, les traitements en cours, les résultats d'imagerie ou de biologie déjà disponibles et la description précise de la lésion (pour les masses : taille, localisation, aspect macroscopique, consistance, évolution ; pour les cytoponctions organiques : modifications architecturales ou parenchymateuses…). Les lames d'étalement doivent être correctement identifiées, au crayon à papier, sur le côté maté (nom de l'animal, localisation de la lésion). Sans ces éléments, le cytologiste est privé du contexte indispensable pour affiner son interprétation.
IV. Lire et comprendre un compte rendu cytologique
Recevoir un compte rendu cytologique ne doit pas être considéré comme une fin en soi. Pour le clinicien, c'est le début d'une réflexion qui doit associer le résultat du laboratoire au contexte clinique de l'animal. La plupart des rapports suivent une structure assez constante. Ils commencent par une description morphologique détaillée : type cellulaire prédominant, présence d'éléments inflammatoires, modifications morphologiques, atypies nucléaires ou cytoplasmiques, présence d'éléments infectieux. Cette description peut paraître technique ou parfois éloignée du problème clinique initial, mais elle constitue le socle objectif de l'analyse.
La deuxième partie du compte rendu correspond à l'interprétation, où le cytologiste propose une ou plusieurs hypothèses diagnostiques. Dans certains cas, la conclusion est claire et sans ambiguïté : par exemple, un mastocytome cutané bien différencié ou un lymphome de haut grade de malignité. Dans d'autres situations, le résultat reste plus nuancé. Le cytologiste peut conclure à une lésion inflammatoire sans préciser l'agent causal, ou à une prolifération suspecte de malignité sans pouvoir affirmer le caractère malin ou la nature exacte de la tumeur. Ces nuances reflètent la réalité de l'examen : la cytologie ne permet pas toujours un diagnostic définitif.
Il est essentiel que le clinicien comprenne que ces précautions de langage ne sont pas des faiblesses, mais l'expression de la rigueur scientifique. Une conclusion du type « compatible avec » ou « en faveur de » ne doit pas être vue comme une incertitude, mais comme une orientation fondée sur les cellules disponibles. Elle invite à confronter ces données aux autres résultats (imagerie, biochimie, hématologie) et à la clinique de l'animal.
Dans certains cas, le compte rendu se termine par une recommandation explicite : refaire un prélèvement, compléter avec une histologie, envisager une immunohistochimie ou une analyse complémentaire (PCR, sérologie, biochimie…). Ces conseils doivent être pris en considération car ils traduisent la limite atteinte par l'examen cytologique et la nécessité d'une approche plus globale.
En définitive, lire un compte rendu cytologique, c'est comprendre non seulement ce qui est écrit, mais aussi ce que cela implique dans la prise en charge de l'animal. Le clinicien reste l'interprète final, celui qui fait le lien entre la description morphologique et la réalité clinique. Dans cette démarche, le dialogue avec le cytologiste est une ressource précieuse, permettant de lever un doute, d'affiner une hypothèse ou d'adapter le plan diagnostique. La valeur ajoutée de la cytologie est maximale lorsque ce dialogue existe : le laboratoire n'est pas un simple prestataire, mais un partenaire.
V. Conclusion
La cytologie spécialisée illustre l'importance du partenariat entre le vétérinaire généraliste et le laboratoire. Le premier identifie les situations où l'examen est pertinent, réalise un prélèvement de qualité et fournit un dossier complet. Le second apporte son expertise morphologique et établit des hypothèses diagnostiques.
Trois compétences clés permettent d'utiliser cet examen de façon optimale : connaître ses indications et limites, respecter les étapes pré-analytiques et interpréter correctement le compte rendu. Bien menée, cette collaboration améliore la précision diagnostique et accélère la prise en charge thérapeutique.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 L'hémorragie oculaire : quand faut-il rechercher une maladie systémique ?
Rennes France
I. Introduction
Une étude réalisée dans le Colorado, USA décrit les causes d’hyphéma dans l’espèce canine (Jinks et al. Veterinary Ophthalmology 2019). La répercussion d’une maladie systémique est rapportée chez 33/88 chiens (36%), une maladie oculaire isolée chez 28/88 chiens (33%), un traumatisme chez 23/88 chiens (26%). Chez 4/88 chiens (5%), aucune cause n’a pu être identifie. En ce qui concerne les cas d’hyphéma secondaire à une maladie générale, on retrouve une prédominance de néoplasie systémique (17/88 chiens, soit19%) dont 8/17 cas de lymphomes), suivie d’une thrombopénie à médiation immune (8/88 chiens, soit 9%), d’une hypertension artérielle systémique (4/88 chiens, sot 5%) puis des cas d’ehrlichiose (3/88 chiens,3%).
Une étude réalisée dans l’état de New York, USA décrit l’association d’hémorragies rétiniennes isolées et de maladies générales chez le chien (Violette et al. Veterinary Ophthalmology 2019). Ainsi, au moins une maladie systémique est diagnostiquée chez 50/83 chiens (60%). Cependant, bon nombre d’entre elles ne sont pas responsable des hémorragies rétiniennes. Parmi les maladies systémiques fréquemment associées à des hémorragies rétiniennes, on retiendra le diabète sucré (24/83 chiens, soit 29%), l’hypertension artérielle systémique (11/83 chiens, soit 13%), le myélome multiple (4/83 cas, soit 5%), les anémies/thrombopénies à médiation immune (3/83 cas, soit 4%) et le lymphomesou la leucémie (3/83 cas, soit 4%).
Nous ne disposons pas de données concernant les causes de saignement oculaire chez le chat mais la fréquence élevée de signes rétiniens d’hypertension artérielle systémique chez des chats âgés de plus de 8ans (12/73 chats, soit 16%) ; Carter et al. (N Z Vet J 2014) en font la principale cause à chercher dans ces cas.
II. Hypertension artérielle systémique (HTA)
L’HTA est bien plus fréquente chez le chat que chez le chien. Ceci explique en grande partie le peu de données disponibles dans l’espèce canine sur cette affection et les signes oculaires associés.
Les principales causes d’HTA secondaire chez le chien sont la maladie rénale chronique ou aiguë, le syndrome de Cushing, le phéochromocytome et le diabète sucré. Chez le chat, il convient de rechercher une maladie rénale chronique, une hyperthyroïdie ou un hyperaldénostéronisme. L’hypertension artérielle essentielle reste plus rare dans les deux espèces (entre 13-20% des cas chez le chat) (Acierno et al. JVIM 2018).
Les lésions oculaires associées à l’HTA sont la conséquence d’une vasoconstriction faisant réponse à l’augmentation de la pression artérielle. Cette dernière induit une occlusion et une nécrose ischémique des parois vasculaires, donc d’une augmentation de la perméabilité vasculaire. Les lésions rétiniennes incluent un œdème rétinien, une diminution du diamètre et une augmentation de la tortuosité des artérioles rétiniennes, et/ou des hémorragies rétiniennes. Les lésions au niveau de la vascularisation choroïdienne sont responsables de divers degrés de décollements de rétine (Veterinary Ophthalmology 6th Ed, 2021).
Chez le chien, des lésions oculaires sont diagnostiquées sur au moins un œil dans 62% de cas (26/42) d'HTA. Les hémorragies rétiniennes sont le signe oculaire le plus fréquent (17/26 chiens, soit 65%), suivi du décollement de rétine (10/26 chiens, soit 38%), de l'hyphéma (8/26 chiens, soit 30%) et de l'œdème sous-rétinien (5/26 chiens, soit 19%) (Leblanc et al. JAVMA 2011). Par ailleurs, dans cette étude, la pression artérielle des chiens présentant des lésions oculaires (220 mm Hg) est significativement supérieure à celles de chiens sans lésions oculaires (187mm Hg).
Chez le chat, la fréquence des lésions oculaires associée à l’HTA varie entre 48-58% (Chetboul et al. JVIM 2003, Cirla et al. Veterinary Ophthalmology, 2021). Par opposition à l’espèce canine, la majorité des chats (47/69 chats, soit 68%)) est présentée pour une perte de vision progressive ou aiguë (Maggio et al. JAVMA 2000). Dans cette espèce, on note une prédominance des signes de choroïdopathie hypertensive (œdème sous-rétinien, décollement bulleux et décollement complet de rétine) pouvant être associés à des signes d’hémorragie rétinienne. Des classifications cliniques fondées sur la littérature humaine ont été proposées chez le chat et revêtent un certain intérêt puisque ces stades cliniques ont été corrélés au degré d’hypertension artérielle systémique dans une étude prospective (Cirla et al. Veterinary Ophthalmology 2021) :
- stade 1. Augmentation de la tortuosité artérielle avec diminution discrète à modérée du diamètre artériel ;
- stade 2. Hémorragies rétiniennes discrètes et/ou décollement de rétine bulleux ;
- stade 3. Décollement de rétine partiel et/ou hémorragies rétiniennes ou vitréennes modérées à marquées ;
- stade 4. Décollement de rétine subtotal/total.
Ces stades cliniques sont corrélés à l’intensité de l’HTA, les chats sans anomalie oculaire ayant une pression artérielle médiane de 180 mm Hg, par comparaison à 195 mm Hg chez les chats avec anomalie rétinienne (Cirla et al. Veterinary Ophthalmology 2021).
La présence d’un hyphéma est également un motif de présentation fréquent des chats atteints d’HTA (62/206 chats, soit 30%, Linek et al. Veterinary Ophthalmology 2020). Ce signe clinique semble être la conséquence de la rupture d’anévrismes iriens (observés chez 28/206 chats, soit14%) plutôt que du déplacement de sang issu d’un saignement dans le segment postérieur (Linek et al. Veterinary Ophthalmology 2020).
III. Anémie/Thrombopénie
Une anémie marquée peut se manifester en particulier par une pâleur du contenu des vaisseaux rétiniens et des hémorragies ou un œdème rétiniens. Ces hémorragies rétiniennes seraient alors consécutives à une hypoxie des parois vasculaires. L’extrême pâleur des vaisseaux pourrait mimer une dégénérescence rétinienne (cependant avec l’absence notable d’hyperréflexion de tapis). Les lésions rétiniennes sont plus fréquentes et plus marquées si l’anémie est associée à une thrombopénie.
Dans une étude prospective menée en Israël sur des chiens atteints d’anémie (Hématocrite <20%) et/ou de thrombopénie (Plaquettes <150.000/ml), la fréquence et l’intensité des lésions oculaires était significativement associées à la présence d’une thrombopénie et non à celle de l’anémie (Shelai-Goraly et al. Vet J 2009). En effet, parmi les chiens atteints d’anémie isolée (2/17 chiens, soit12%) présentaient des lésions oculaires discrètes (œdème rétinien focal et pétéchies sous-conjonctivales), alors que parmi les chiens atteints de thrombopénie isolée, 9/36 chiens (25%) présentaient des lésions oculaires discrètes et 6/36 chiens (17%) des lésions oculaires marquées, dont 5 cas d’hyphéma.
Chez le chat, la présence d’hémorragies rétiniennes est considérée comme fréquentes chez les chats infectés par le du FeLV présentant une anémie secondaire à l’infection (Veterinary Ophthalmology 6th Ed, 2021).
IV. Syndrome d’hyperviscosité sanguine.
Il résulte de l’augmentation de la concentration sérique en immunoglobuline responsable d’une augmentation de la viscosité du sérum. Une néoplasie systémique est le plus souvent incriminée chez le chien et le chat (myélome multiple, lymphome, leucémie lymphocytaire chronique) mais certaines maladies infectieuses (ehrlichiose, leishmaniose) peuvent causer ce syndrome chez le chien.
Les lésions oculaires les plus souvent retrouvées chez le chien sont des vaisseaux rétiniens tortueux et dilatés, un œdème papillaire, des hémorragies rétiniennes et des décollements de rétine bulleux (Hendrix et al. JAAHA 1998).
Une origine multifactorielle des signes cliniques est prioritairement envisagée (nécrose et rupture des parois vasculaires par distension de ces dernières et stase sanguine, diminution de l’agrégation plaquettaire par couverture de ces dernières par les immunoglobulines, infiltration des parois vasculaires par les immunoglobulines) (Veterinary Ophthalmology 6th Ed, 2021).
V. Erhlichiose monocytaire canine.
Cette infection est due à Erhlichia canis et transmise par la tique Rhipicephalus sanguineus.
Les signes oculaires associés à cette affection sont extrêmement nombreux mais le tableau clinique oculaire est dominé par la présence d’une uvéite antérieure, postérieure ou d'une panuvéite à composante hémorragique.
Dans une étude menée en Espagne (Leiva et al. Veterinary Ophthalmology 2005), 17/46 cas (37%) présentaient des anomalies oculaires dont en particulier 11/17 cas (65%) qui ne présentaient pas de signes cliniques généraux. Les signes cliniques oculaires étaient bilatéraux chez tous les animaux, avec un décollement de rétine exsudatif 11/17 cas (65%), une uvéite antérieure exsudative 5/17 cas (29%) ou une névrite optique 1/17 cas (6%).
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 L'hydrothérapie : quand et comment la mettre en oeuvre?
Lausanne, Suisse
I. Introduction
La rééducation neurologique vise à recréer le lien fonctionnel entre le système nerveux et le muscle après une paralysie. Dès les premiers jours, l'absence de commande motrice entraîne amyotrophie, ankylose et perte de proprioception. La récupération s'appuie sur la réduction de la compression de la moelle épinière et la plasticité neuronale, qui suivent les quatre phases distinctes de récupération. [1]
II. Phase aiguë (J1–J5)
L'objectif est de diminuer l'inflammation pour réduire la compression du SNC et ainsi prévenir les complications. L'hydrothérapie se limite à des immersions passives avec ou sans mobilisations articulaires, ainsi qu'une station debout assistée et transferts de poids doux. Toutefois, immerger un chien porteur d'une plaie chirurgicale non cicatrisée reste contre-indiqué, car l'hydrothérapie trop précoce peut induire de graves complications. [2]
III. Phase subaiguë (J5–J21)
La baisse de l'inflammation et le bourgeonnement axonal permettent de réactiver les circuits locomoteurs spinaux. L'introduction de la marche sur tapis aquatique devient possible, avec assistance sécurisée. Des difficultés de bas niveau (pressions manuelles, pente douce, accentuation du pattern locomoteur) stimulent le recrutement musculaire et la plasticité neuronale. [1]
IV. Phase de consolidation (J21–J60)
La transmission neuromusculaire s'améliore et le renforcement musculaire devient prioritaire. L'hydrothérapie associe augmentation de la vitesse et de l'intensité, ajout de pente douce et variation de hauteur d'eau ainsi que des exercices aquatiques et transferts de poids dynamiques. [1]
V. Phase d'organisation (J61+)
L'apprentissage moteur et la réorganisation corticale s'affinent. Les exercices visent endurance, symétrie et fluidité, en combinant vitesse, hauteur d'eau et durée . L'ajout de résistances externes, manuelles ou par jets à contre-courant, permet d'optimiser la stabilité et d'améliorer la puissance et l'endurance musculaire. [1]
VI. Conclusion
L'hydrothérapie, intégrée dans une stratégie multimodale (exercices thérapeutiques, NMES- stimulation neuromusculaire électrique, physiothérapie manuelle), constitue ainsi une interface unique entre système nerveux et muscle. Adaptée à chaque phase de la récupération, elle est un levier majeur pour restaurer une locomotion fonctionnelle chez les patients paralysés.
Bibliographie
- BOCKSTAHLER B., LEVINE D., MILLIS D., et al. Essential Facts of Physical Medicine, Rehabilitation and Sports Medicine in Companion Animals. BE VetVerlag, 1st ed 2019.
- MOJARRADI A., DE DECKER S., BÄCKSTRÖM C., BERGKNUT N. Safety of early postoperative hydrotherapy in dogs undergoing thoracolumbar hemilaminectomy. J Small Anim Pract. 2021;62(12):1062–1069. doi:10.1111/jsap.13412.
- MILLIS D., LEVINE D. Canine Rehabilitation and Physical Therapy. 2nd ed. Elsevier, 2013
- HENEA ME, ȘINDILAR EV, BURTAN LC, MIHAI I, GRECU M, ANTON A, SOLCAN G. Recovery of Spinal Walking in Paraplegic Dogs Using Physiotherapy and Supportive Devices to Maintain the Standing Position. Animals (Basel). 2023 Apr 19;13(8):1398. doi:10.3390/ani13081398.
Liens d'intérêt : Conseiller scientifique pour la société AllCare innovations.
📃 L'hypertension pulmonaire : comment la diagnostiquer ?
Paris, France
I. Introduction
Le gold standard pour le diagnostic de l'hypertension artérielle pulmonaire (HTAP) chez le chien est le cathétérisme du cœur droit qui est rarement pratiqué en médecine vétérinaire. Les vétérinaires s'appuient fortement sur l'échocardiographie et d'autres éléments cliniques complémentaires pour poser une présomption d'HTAP.
II. Signes cliniques
Les signes cliniques associés à l'HTAP reflètent en grande partie la maladie sous-jacente qui en est à l'origine. Il n'y a pas de signes cliniques spécifiques d'HTAP et l'absence de signes cliniques ne l'exclut pas. Les syncopes, en particulier suite à un effort ou une activité, les anomalies respiratoires, la toux, la distension abdominale (insuffisance cardiaque congestive droite) et l'intolérance à l'effort sont parmi les signes cliniques les plus courants rapportés chez les chiens chez lesquels une HTAP a été diagnostiquée.
L'examen clinique peut révéler des bruits respiratoires anormaux, une tachypnée, une dyspnée, des muqueuses cyanosées ou pâles, ou une distension ou pulsation veineuse jugulaire. Un dédoublement du B2 peut apparaître. Un souffle systolique d'insuffisance tricuspidienne (souffle systolique apexien droit) et plus rarement un souffle d'insuffisance pulmonaire (souffle diastolique basal gauche) peuvent être entendus. Un souffle systolique apexien gauche d'insuffisance mitrale est fréquent s'il s'agit d'une HTAP secondaire à une cardiopathie gauche.
III. Signes radiographiques
Chez le chien, les signes radiographiques d'hypertension pulmonaire (HTAP) peuvent être subtils ou plus évidents selon la gravité. Les principaux signes visibles sur une radiographie thoracique sont les suivants.
1. Dilatation des artères pulmonaires
- Tronc pulmonaire dilaté (visible en vue dorsoventrale ou ventrodorsale).
- Artères pulmonaires élargies (comparaison de l'artère pulmonaire avec la 4ème côte sur une vue de profil et avec la 9ème côte sur une vue de face). Attention, l'artère peut être confondue avec une insuffisance cardiaque gauche, donc l'évaluation comparative veines/artères est essentielle.
- Dilatation proximale des artères pulmonaires avec un amincissement distal : les artères semblent « coupées » ou se réduisent brusquement.
- Diminution du calibre vasculaire périphérique (en cas de thromboembolie).
- Silhouette cardiaque droite modifiée.
- Hypertrophie/dilatation du ventricule droit visible : silhouette cardiaque élargie crânialement (vue latérale) ; déviation dorsale de la trachée (en absence d'augmentation du ventricule gauche) ; aspect en « D inversé » du cœur (en vue ventrodorsale, dû à l'aplatissement du septum interventriculaire et la dilatation du ventricule droit) ; dilatation de l'atrium droit.
2. Autres signes associés selon la cause
- Collapsus trachéal si HTAP secondaire à une hypoxie chronique.
- Œdème pulmonaire interstitiel ou alvéolaire si HTAP secondaire à une maladie cardiaque gauche.
- Modifications bronchiques (ex. : bronchopathie chronique).
- Lésions alvéolo-interstitielles généralisées en cas de parasitose.
- Opacification interstitielle en cas de fibrose.
- Ascite et/ou épanchement pleural (si insuffisance cardiaque droite secondaire à l'HTAP).
IV. Échocardiographie
L'échocardiographie doit être considérée comme un outil clinique pour aider à déterminer la probabilité qu'un patient ait une HTAP et non comme un test diagnostique définitif de présence et de gravité de l'HTAP. L'échocardiographie est également nécessaire pour la caractérisation hémodynamique, la classification clinique et la gestion de l'HTAP. Des recommandations pour l'évaluation échocardiographique de l'HTAP chez les chiens ont été publiées par un panel d'experts de l'American College of Veterinary Internal Medicine (ACVIM). Ces recommandations ont été influencées par les lignes directrices échocardiographiques humaines disponibles et tiennent compte des limitations de l'échocardiographie Doppler, notamment le potentiel d'inexactitude et d'imprécision dans l'estimation de la pression artérielle pulmonaire (PAP) chez le chien.
L'évaluation de la probabilité d'HTAP par échocardiographie se base d'une part sur le Doppler pour estimer de manière non invasive la PAP en évaluant la vitesse de régurgitation tricuspidienne, et d'autre part par l'évaluation de nombreux signes échocardiographiques indirects d'HTAP. Cela implique d'observer des changements structurels ou fonctionnels qui résultent couramment de l'HTAP au niveau de trois sites anatomiques importants : 1) les ventricules, 2) l'artère pulmonaire (PA), et 3) l'atrium droit/la veine cave caudale.
Une fois qu'un obstacle à l'éjection du ventricule droit est exclu (sténose pulmonaire congénitale ou acquise), la quantification de la vélocité de régurgitation tricuspidienne maximale à l'aide du Doppler continu permet d'estimer la PAP systolique ; la PAP moyenne peut être estimée aussi à partir de la vitesse de jet de régurgitation pulmonaire précoce maximale, si elle est présente. Cela suppose que la régurgitation tricuspidienne est présente, ce qui est courant même chez les chiens en bonne santé. La vélocité maximale est convertie en un gradient de pression à l'aide de l'équation de Bernoulli simplifiée (gradient de pression [mmHg] = 4 × vitesse [m/s]²) et souvent catégorisée comme suit : HTAP légère, 30-50 mmHg ; HTAP modérée, 50-75 mmHg ; et HTAP sévère, >75 mmHg. Une vitesse de reflux tricuspidien > 2,8–3,0 m/s suggère une HTAP modérée à sévère.
Concernant les autres sites anatomiques, les modifications recherchées sont les suivantes.
- Une dilatation/hypertrophie du ventricule droit. Elle est souvent associée à un aplatissement du septum interventriculaire (septum paradoxal) dû à la pression droite accrue, en systole et parfois en diastole.
- Une dilatation de l'atrium droit.
- Un ventricule gauche de diamètre diminué.
- Une dilatation du tronc pulmonaire (le rapport tronc pulmonaire/aorte (TP/Ao) > 1 est anormal).
- Une diminution de la distensibilité de l'artère pulmonaire droite (<30%).
- Une insuffisance pulmonaire avec une vélocité >2,5 m/s en début de diastole.
- Un flux pulmonaire systolique de forme anormale (temps d'accélération raccourci et <52-58 ms, ratio du temps d'accélération sur le temps d'éjection >0,30).
- Une distension de la veine cave caudale.
Plusieurs facteurs influencent la vélocité du reflux tricuspidien en plus de la PAP et de la résistance vasculaire pulmonaire, comme la fonction systolique du ventricule droit. Cette dernière peut être étudiée aussi à l'échocardiographie. Parmi les variables quantitatives qui évaluent la fonction ventriculaire droite sont : le déplacement de l'anneau tricuspidien vers l'apex en systole (TAPSE : tricuspid annular plane systolic excursion) ; l'aire ventriculaire droite en systole normalisée au poids ; la fraction de changement de l'aire du ventricule droit.
L'évaluation de la gravité de l'HTAP est idéalement basée sur une approche multifactorielle qui comprend une combinaison de vélocité du reflux tricuspidien, le degré et le nombre de signes échocardiographiques d'HTAP, et les signes cliniques. Une HTAP cliniquement significative est peu probable chez un animal qui n'a pas de signes cliniques.
L'échocardiographie permet aussi l'évaluation des signes échographiques de la cause sous-jacente. Selon la cause d'HTAP, l'échocardiographie peut mettre en évidence une cardiopathie gauche, un shunt intracardiaque (communication interatriale ou interventriculaire), ou un shunt extracardiaque (canal artériel persistant), des filaires en cas de dirofilariose.
Bibliographie
- REINERO C. et coll. ACVIM consensus statement guidelines for the diagnosis, classification, treatment, and monitoring of pulmonary hypertension in dogs. J Vet Intern Med. 2020;34:549-73.
- ETTINGER SJ, FELDMAN EC, COTE, E. (Eds). Ettinger's Textbook of Veterinary Internal Medicine-eBook. Elsevier Health Sciences, 2024.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 L'hypertension pulmonaire : définition et classification
Merignac, France
I. Introduction
L'hypertension pulmonaire (HTP) n'est pas une maladie unique, mais un syndrome physiopathologique correspondant à une élévation anormale et persistante de la pression artérielle pulmonaire.
En conditions normales, la circulation pulmonaire est un système à basse pression, faible résistance et haute compliance, capable d'accepter d'importantes variations de débit sans augmentation majeure de la pression. Cette particularité protège le ventricule droit d'une surcharge de travail excessive. Chez le chien sain, la pression artérielle pulmonaire moyenne (PAPm) reste généralement < 20 mmHg, et la pression systolique < 25-30 mmHg au repos.
L'HTP apparaît lorsque cette homéostasie hémodynamique est perturbée, soit par une augmentation du débit pulmonaire, une élévation de la pression veineuse pulmonaire, une augmentation de la résistance vasculaire pulmonaire ou une combinaison de ces mécanismes. Elle entraîne une surcharge de pression du ventricule droit pouvant aboutir à son hypertrophie, sa dilatation, puis une insuffisance cardiaque droite (cor pulmonale).
En pratique vétérinaire, l'HTP complique souvent le pronostic des maladies cardiaques gauches (maladie mitrale dégénérative (MVD), cardiomyopathies), des affections pulmonaires chroniques (fibrose pulmonaire, bronchomalacie) ou des thrombo-embolies. Chez le chien, elle est fréquente et parfois très grave ; chez le chat, elle reste plus rare mais non négligeable.
Cliniquement, l'HTP peut se manifester par de l'intolérance à l'effort, une dyspnée, des syncopes ou rester silencieuse, découverte à l'échocardiographie. Sa reconnaissance précoce est essentielle, car elle influence directement le pronostic et la prise en charge des patients atteints.
II. Définition
L'HTP correspond à une augmentation anormale de la pression dans la circulation pulmonaire.
Chez l'homme, on parle d'HTP si la pression artérielle pulmonaire moyenne (PAPm) est ≥ 25 mmHg au repos (mesurée par cathétérisme cardiaque droit).
En médecine vétérinaire, cette mesure invasive est rarement réalisée. On se base donc sur l'estimation échocardiographique (vitesse de régurgitation tricuspide) et le contexte clinique.
Deux notions clés :
- HTP précapillaire : ↑ résistance vasculaire pulmonaire en amont des capillaires pulmonaires, avec pression veineuse pulmonaire normale.
- HTP postcapillaire : secondaire à une hypertension veineuse pulmonaire, le plus souvent liée à une maladie cardiaque gauche.
III. Physiopathologie
Quatre mécanismes principaux peuvent, seuls ou combinés, conduire à l'HTP :
1. Augmentation du flux pulmonaire
Ex. : shunts cardiaques congénitaux (PCA, CIV).
Le débit pulmonaire excessif entraîne une hyperpression chronique et un remodelage vasculaire pulmonaire secondaire.
2. Augmentation de la pression veineuse pulmonaire
Ex. : maladies cardiaques gauches (MVD, cardiomyopathies).
L'élévation de la pression atriale gauche se répercute en amont, dans les veines et capillaires pulmonaires.
3. Augmentation de la résistance vasculaire pulmonaire
Ex. : maladies pulmonaires chroniques, hypoxie, thrombo-embolies, parasitoses (Dirofilaria, Angiostrongylus).
Hypoxie chronique, inflammation et remaniements vasculaires provoquent une vasoconstriction puis une vasculopathie irréversible (hypertrophie médiale, fibrose, lésions plexiformes).
4. Mécanismes combinés ou multifactoriels
Ex. : un chien atteint de MVD et de bronchomalacie sévère peut présenter une HTP post- et précapillaire.
L'augmentation chronique de la postcharge du ventricule droit induit progressivement une hypertrophie, puis une dilatation et une insuffisance cardiaque droite (cor pulmonale).
IV. Classification en six groupes
La classification ACVIM 2020 distingue six groupes selon la cause principale (Figure 1).
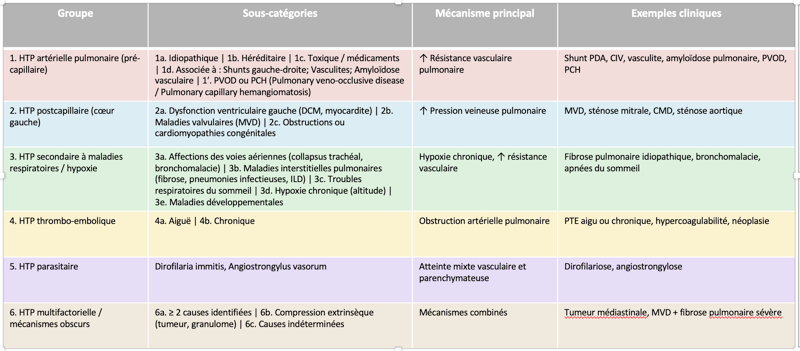
Figure 1
V. Conclusion
L'HTP n'est pas une maladie unique mais un syndrome multifactoriel. En pratique, il est essentiel de :
- reconnaître les mécanismes sous-jacents,
- classer l'HTP selon l'étiologie pour guider la prise en charge,
- traiter la cause primaire chaque fois que possible, le traitement spécifique de l'HTP étant limité.
Le diagnostic et le traitement feront l'objet d'une conférence dédiée.
Bibliographie
- REINERO C et coll. ACVIM consensus statement guidelines for the diagnosis, classification, treatment, and monitoring of pulmonary hypertension in dogs. J Vet Intern Med. 2020 ; 34 : 549-573.
- BONAGURA JD et coll. Pulmonary Hypertension. In : Cardiovascular Disease in Companion Animals, Dog, Cat and Horse. 2nd ed.; 2022 : 813-820.
- SIMONNEAU G et coll. Haemodynamic definitions and updated clinical classification of pulmonary hypertension. Eur Respir J. 2019 ; 53 : 1801913.
- KELLIHAN HB, STEPIEN RL. Pulmonary hypertension in dogs: diagnosis and therapy. Vet Clin North Am Small Anim Pract. 2010 ; 40 : 623-641.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 L'IA générative au quotidien aujourd'hui
Lorient, France
Vous retrouverez l’intégralité de cette présentation créé par un humain via ce lien : https://bit.ly/GSAFVAC2025
En attendant de pouvoir la consulter à partir du vendredi 28 novembre 2025, vous pouvez découvrir ce texte généré par l’IA à propos du sujet présenté.
L’intelligence artificielle générative s’invite désormais dans le quotidien des cliniques vétérinaires. Longtemps perçue comme un outil futuriste réservé à la recherche, elle trouve aujourd’hui des applications concrètes qui transforment la pratique, tant sur le plan médical qu’organisationnel. En s’appuyant sur des modèles capables de produire du texte, des images ou des résumés, les vétérinaires et leurs équipes gagnent en efficacité et en confort de travail, tout en améliorant l’expérience des propriétaires d’animaux.
L’un des premiers usages concerne la gestion administrative et la relation client. Les IA génératives permettent de rédiger des comptes rendus de consultation, des protocoles de soins personnalisés ou encore des courriels explicatifs destinés aux propriétaires. L’automatisation de ces tâches répétitives réduit la charge cognitive des praticiens et leur libère du temps pour se concentrer sur l’essentiel : la médecine et l’accompagnement des clients. De plus, ces outils peuvent adapter le vocabulaire selon le niveau de compréhension du destinataire, favorisant une meilleure pédagogie.
Sur le plan médical, l’IA générative contribue à l’analyse et à la synthèse des données. Elle peut par exemple aider à résumer un dossier complexe avant une consultation, ou structurer les informations issues de bilans sanguins et d’imagerie pour faciliter la prise de décision. Couplée à des bases de données spécialisées, elle offre une aide précieuse pour la recherche bibliographique, l’élaboration de diagnostics différentiels ou la mise à jour des connaissances. Bien qu’elle ne remplace pas l’expertise clinique, elle agit comme un véritable assistant intelligent.
Enfin, l’IA générative trouve sa place dans la communication interne et la formation. Les équipes peuvent l’utiliser pour créer des supports pédagogiques, simuler des cas cliniques ou générer des scénarios d’accueil pour les auxiliaires. Elle devient un levier de cohésion et de montée en compétence, dans un contexte où le recrutement et la fidélisation sont des enjeux majeurs.
L’intégration de ces technologies soulève toutefois des questions éthiques et pratiques : fiabilité des contenus générés, protection des données sensibles, coût des solutions. Mais leur potentiel est indéniable. En facilitant l’accès à l’information et en allégeant la charge administrative, l’IA générative ouvre la voie à une pratique vétérinaire plus fluide, plus centrée sur la relation avec l’animal et son propriétaire. Elle ne remplace pas le savoir-faire du vétérinaire, mais elle s’impose comme un allié de plus en plus incontournable dans la clinique du futur.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 L'influenza aviaire hautement pathogène H5N1 : un agent étiologique sous-estimé chez le chat ?
Pierre BESSIÈRE
Coauteurs : Jessie BRUN, Brandon HAYES, Amélie MARCHAND, Laura LEBOUTEILLER, Sébastien-Mathieu SOUBIES, Marie-Christine CADIERGUES, Jean-Luc GUÉRIN
Introduction
Les virus influenza aviaires hautement pathogènes H5N1 ont particulièrement circulé à la surface de la planète ces dernières années, causant notamment des épizooties records en France entre 2020 et 2023, avec des millions d'oiseaux abattus. Cette circulation accrue a mathématiquement augmenté l'exposition des mammifères à ces virus, et en particulier des chats. Alors que ces derniers n'avaient aucune chance de rencontrer un tel virus il y a quelques années, les chats français qui ont accès à l'extérieur peuvent désormais croiser leur route. L'infection se manifeste fréquemment par des troubles neurologiques et respiratoires, pouvant mener à la mort des félidés.
Matériel et méthodes
Afin d'évaluer l'exposition des chats aux virus H5N1 en France, nous avons mené une étude de séroprévalence, avec pour critères d'inclusion le fait d'avoir accès à l'extérieur, d'avoir plus d'un an et de vivre en dehors des grandes métropoles.
Un total de 728 animaux, provenant de 44 cliniques vétérinaires réparties sur toute la FRANCE, a été prélevé à l'occasion de visites de routine chez leurs vétérinaires. Les sérums ont d'abord été criblés par un test ELISA spécifique de la protéine H5, et tous les échantillons positifs ou douteux ont subi un second test de séroneutralisation virale. Chaque sérum était accompagné d'un questionnaire renseignant sur le mode de vie du chat.
Résultats
Le taux de séropositivité était de 2,6 % (19 sérums positifs sur 728), et montait jusqu'à 3,3 % en ne prenant en compte que les départements comprenant des zones considérées comme à risque vis-à-vis de l'influenza aviaire d'après le Ministère de l'Agriculture et de La Souveraineté Alimentaire. Cela permit d'estimer à 1,8 % la séroprévalence globale. L'analyse des facteurs de risque révéla que le comportement de prédation était associé à une plus forte probabilité d'être séropositif.
Conclusion
Ces résultats montrent que l'exposition des chats aux virus H5N1 a été forte en FRANCE. L'influenza aviaire doit donc faire partie du diagnostic différentiel lorsqu'un chat présente des signes cliniques évocateurs de la maladie et que le contexte épidémiologique est compatible.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 L'œil trouble : quand faut-il penser à un dysmétabolisme lipidique ?
Montréal, Canada
Ce texte est restitué tel que fourni par l'auteur.
I. Introduction
1. Trouble :
- Se dit d'un liquide qui n'est pas limpide par suite de la présence de petites particules en suspension : eau trouble. Contraires : clair - limpide - pur - transparent.
- Se dit d'une image qui n'est pas nette. Synonyme : voilé Contraires : net - translucide
- Se dit d'une surface qui n'est pas transparente.
2. Au niveau de l'œil :
- perte de limpidité des milieux liquidiens : humeur aqueuse et vitrée
- perte de transparence des surfaces : cornée, cristallin et rétine
Deux types de commentaires des vétérinaires de famille :
1. "Je vois l'iris mais je ne vois pas /difficilement la rétine/le fond d'œil"
- perte de limpidité des milieux liquidiens : vitrée
- perte de transparence des surfaces : cristallin et rétine
2. "Je ne vois pas /difficilement l'intérieur de l'œil"
- perte de limpidité des milieux liquidiens : humeur aqueuse
- perte de transparence des surfaces : cornée
3. Au cours de cette présentation :
- seules les affections de la cornée et de l'humeur aqueuse pouvant entraîner un œil "trouble" chez le chien seront abordées
- les affections de la cornée ou de la chambre antérieure se manifestant par des lésions vraiment opaques ne seront pas couvertes
Exemples : séquestre de cornée kyste de l'iris
Les affections du cristallin, du vitré et de la rétine pouvant entraîner un œil "trouble" chez le chien seront abordées lors de prochaines présentations (sclérose nucléaire, cataracte, etc.)
II. Signes cliniques et diagnostic différentiel de l'œil trouble
1. Démarche diagnostique clinique
- Anamnèse : race, traumatisme, région géographique, lieu de vie, activité/voyage ...
- Examen oculaire : signes cliniques
a) Œil "trouble" lié à la cornée
- aspect "bleuté" = œdème de la cornée
- aspect "blanc" = dépôts cornéens
b) Œil "trouble" lié à l'humeur aqueuse/chambre antérieure
- Jaune/beige rouge/rosé blanc laiteux
- Diagnostic différentiel
- transilluminateur
- lampe à fente
c) Œil "trouble" lié à la cornée
d) Œil "trouble" lié à l'humeur aqueuse/chambre antérieure :
2. Autres signes cliniques
- Photophobie, épiphora, blépharospasme, protrusion de la membrane nictitante
- Diminution de la vision
- Hyperhémie et chémose de la conjonctive
- Injection ciliaire
- Myose/synéchie/dyscorie
- Œdème/rubéose de l'iris
- Changement de couleur de l'iris
- Hypotonie
III. Étiologie de l'œil trouble
1. Œil "trouble" lié à la cornée
a) Aspect "bleuté" = œdème de la cornée
- AVEC autres signes cliniques associés
- Ulcère de cornée : traumatique, cil ectopique, KCS, entropions…
- Glaucome : primaire, secondaire à uvéite, luxation du cristallin, néoplasie
- NGE : auto-immune
- Uvéite
- SANS autre signe clinique associé
- Décompensation endothéliale de la cornée (DEC) : âge, races prédisposées (Boston Terrier, Chihuahua, Teckel)…
b) Aspect "blanc" = dépôts dans la cornée
SANS autre signe clinique associé
- Dystrophie lipidique de la cornée : races prédisposées (Husky, Beagle, Shetland)
- Pharmacologique (corticostéroïdes topiques)
- Kératopathie de Floride : étiologie non connue
- Maladies de stockage (lysosomales) : mucopolysaccharidose, gangliosidose (Shiba Inu)
c) Manifestation oculaire de maladies systémiques (MOMS)
- Hypothyroïdie :
modifications du métabolisme des lipides → hyperlipidémie, hyperlipoprotéinémie → dépôts/infiltrats lipidiques cornéens (Arcus lipoides corneae)
- Hyperlipidémie :
- Primaire (Briard, Beagle, Colley, Schnauzer)
- Secondaire (Diabète, Cushing, hypothyroïdie, pancréatite)
→ dépôts/infiltrats lipidiques cornéens
2. Œil "trouble" lié à l'humeur aqueuse/chambre antérieure => UVÉITE
a) Origine traumatique
- Traumatisme fermé (contusion, corps étranger, ulcère de cornée, brûlure chimique du globe/cornée)
- Traumatisme ouvert septique (perforation cornéenne par griffure, corps étranger) ou ouvert stérile (chirurgie)
b) Origine infectieuse
- Virale : Adenovirus canin, Herpès virus canin, maladie de Carré, rage
- Bactérienne : spécifique (tuberculose, leptospirose, brucellose, borréliose) non spécifique : endoculaire (traumatisme pénétrant) ou à distance (métrite, cystite, pneumonie, cystite, septicémie)
- Mycosique : cryptoccose, histoplasmose, aspergillose, blastomycose
c) Origine protozoaire/Algue/Parasitaire
- Toxoplasmose, leishmaniose, piroplasmose
- Rickettsiose, erlichiose
- Protothécose, géotrichose
- Larves erratiques (dirofilariose, angyostrongylose toxocarose, myase)
d) Origine thérapeutique
- Analogues de prostaglandines (latanoprost)
- Radiothérapie
e) Origine néoplasique
- Primaire (tumeur intra-oculaire)
- Secondaire (lymphosarcome, histiocytose ou métastase d'autre tumeur)
f) Origine métabolique
- Diabète mellitus (cataracte)
- Coagulopathies
- Hypothyroïdie
- Hyperlipidémie
- Primaire (Briard, Beagle, Colley, Schnauzer)
- Secondaire (Diabète, Cushing, hypothyroïdie, pancréatite)
→ dépôts/infiltrats lipidiques cornéens
→ épanchement lipidique camérulaire, blanc laiteux (aqueous lipid laden)
→ rétine lipémique (lipemia retinalis)
Hypertension systémique
g) Origine auto-immune
- Uvéite phacolytique (secondaire à une cataracte)
- Uvéite phacoclastique (secondaire à une rupture du sac cristallinien)
- Syndrome oculo-cutané (syndrome de Vogt-Koyanagi-Harada)
- Uvéite pigmentaire du Golden Retriever
- Autres (méningo-encéphalite granulomateuse)
h) Idiopathique
Conclusion : causes NOMBREUSES et VARIÉES
IV. Tests pour confirmation diagnostique
1. Œil "trouble" lié à la cornée
- Mesure des pressions intra-oculaires
- Coloration à la fluorescéine
2. Œil "trouble" lié à l'humeur aqueuse/chambre antérieure
- Mesure des pressions intra-oculaires
- Coloration à la fluorescéine
- Échographie oculaire
Diagnostic clinique généralement facile
3. Tests de diagnostic étiologique
a) Œil "trouble" lié à la cornée
- Tests oculaires : test de Schirmer
- Autres tests :
- Bilan sanguin : hémogramme et biochimie (+/- urologie)
- Triglycéridémie et cholestérolémie
- Tests "hormonaux" : T4, cortisol
- Tests génétiques si existant…
b) Œil "trouble" lié à l'humeur aqueuse/chambre antérieure => UVÉITE
- Tests complémentaires "de base" :
- Bilan sanguin : hémogramme et biochimie (+/- urologie)
- Tests "hormonaux" : T4, cortisol
- Tests sérologiques (à adapter selon anamnèse et localisation géographique : leishmaniose, maladie de Lyme…)
- Objectif de ces tests
- Débuter un traitement symptomatique de l'uvéite
- Orienter vers un traitement étiologique (basé aussi sur examen oculaire ET général)
- Proposer un traitement chirurgical si nécessaire
V. Conclusion
Œil "trouble" :
- Soit lié à la cornée
- Soit lié à l'humeur aqueuse/chambre antérieure
1. Lié à la cornée
- soit pas de douleur, pas d'autre signe clinique : dystrophie lipidique, maladie de stockage, DEC
- soit associé à d'autres signes cliniques (notamment douleur) : envisager des tests pour définir le plan de traitement. Ulcère, glaucome, uvéite…
2. Lié à l'humeur aqueuse/chambre antérieure = UVÉITE
Choix raisonné d'autre(s) test(s) à envisager en se posant au moins deux questions :
- Ce test va-t-il vraiment permettre de changer mon plan de traitement envisagé de l'uvéite chez ce chien ?
- Ce test va-t-il vraiment permettre de confirmer ou d'infirmer mon diagnostic étiologique de l'uvéite chez ce chien ?
Effectuer un minimum d'examens complémentaires ("de base") afin de mettre un traitement symptomatique en place le plus rapidement possible pour essayer de sauver l'œil et la vision et contrôler la douleur
Autre(s) test(s) à envisager selon de nombreuses considérations : l'état de l'œil/des yeux, l'état général de l'animal, l'inquiétude et le souhait des propriétaires d'investiguer plus, la région, l'environnement socio-économique et le type d'établissement où vous exercez…
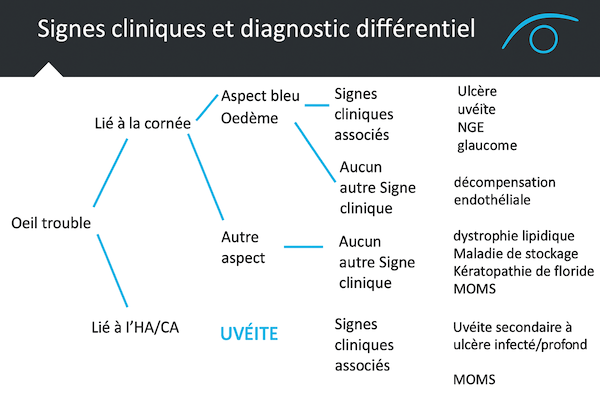
Figure 1
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 L'opacification du cristallin : sclérose ou cataracte. Quand référer à un ophtalmologue ?
Montréal, Canada
Ce texte est restitué tel que fourni par l'auteur.
I. Définition de sclérose nucléaire et de cataracte
1. Sclérose nucléaire :
- changement physiologique du cristallin lié à l'âge
- chiens de 5-6 ans et plus
- opalescence du cristallin
- vision floue mais peu/pas de déficit visuel
2. Cataracte :
- changement pathologique du cristallin
- chien de tout âge
- opacité de différentes parties du cristallin (capsule, cortex, noyau, équateur)
- différentes causes possibles (héréditaire, métabolique, traumatique…)
- déficit visuel plus ou moins marqué selon le stade
II. Diagnostic différentiel
1. Sclérose nucléaire :
- âge de l'animal (5-6 ans et plus)
- vision présente : menace +
- apparence bleutée axiale centrale (au centre de la pupille/cristallin)
- souvent associée à d'autres changements physiologiques liés à l'âge comme l'atrophie de l'iris
→ Ophtalmoscopie (directe ou indirecte)
- reflet du fond d'œil visible
- Absence d'obstacle qui empêche la visualisation du fond d'œil (qui peut cependant être "flouté")
2. Cataracte :
- à tout âge : (congénitale, juvénile, adulte, sénile)
- vision présente ou pas selon le stade : menace +/-
- opacité plus ou moins blanche du cristallin touchant différentes parties du cristallin (capsule, cortex, noyau, équateur), plus ou moins étendue selon le stade (focale, incipiente, immature, mature, hypermature)
→ Ophtalmoscopie (directe ou indirecte)
- reflet du fond d'œil visible
Plus ou moins visible selon le stade
- présence d'obstacle qui empêche, plus ou moins complètement, la visualisation du fond d'œil, selon le stade (opacité qui apparait donc blanche sur une photo, blanche en lumière directe et noire en rétro-illumination)
III. Diagnostic étiologique
1. Sclérose nucléaire :
- opalescente = changement physiologique lié à l'âge de l'animal (5-6 ans et plus), causé par un durcissement, une augmentation de densité progressifs du noyau du cristallin
2. Cataracte :
- opacité = changement pathologique causé par une désorganisation des fibrilles cristalliniennes
Cataracte : causes possibles
- héréditaire
- sénile (liée à l'âge)
- traumatique (griffe de chat, corps étranger…)
- pharmacologique (DMSO, ketoconazole), toxique (acétone, CE métallique), autres (radiations, électrocution)
- parasitaire : Encephalitozoon cuniculi
- secondaire à maladie oculaire : uvéite, luxation ou sub-luxation, APR
- maladie systémique : diabète, hypocalcémie, hypercuprémie, hypergalactosémie
IV. Démarche thérapeutique
1. Sclérose nucléaire :
- vision pas ou peu affectée
- aucun traitement
2. Cataracte : évaluation
- évaluation de l'état de l'œil
- identification de la cause
- détermination du stade
- signes cliniques associés
- évaluation de l'état de l'animal
- âge, santé générale (maladie systémique),
- tempérament, évaluation du déficit visuel associé
- évaluation de la demande du propriétaire
3. Cataracte : traitement médical
Cataracte entrainant une uvéite (uvéite phacolytique)
Mesure de pression intraoculaire (PIO)
Traitement médical :
- Anti-inflammatoire
- (systémique / topique, AINS/AIS)
- (prednisone, meloxicam, robenacoxib)
- (dexaméthasone, prednisolone, diclofenac, kétorolac)
- +/- mydriatique/cycloplégique
- (atropine 1%, tropicamide)
Traitement chirurgical ou non : l'uvéite doit être contrôlée (AINS à long terme en topique) pour que l'œil reste un bon candidat pour la chirurgie, pour réduire le risque de complications ; en l'absence d'intervention : glaucome, luxation du cristallin, décollement rétinien, uvéite grave
4. Cataracte : traitement chirurgical
Traitement chirurgical : par phaco-émulsification +/- implantation de cristallin artificiel
Seulement après une évaluation rigoureuse :
- évaluation du statut de l'œil (échographie, ERG, PIO)
- évaluation de l'état de l'animal
- évaluation des motivations du propriétaire
V. Conclusions
1. Sclérose nucléaire
- Opalescence du cristallin chez le chien de 5-6 ans et plus
- Absence de déficit visuel
- Absence d'obstacle à l'observation du fond d'œil
- Aucun traitement à envisager
2. Cataracte
- Opacité du cristallin chez le chien à n'importe quel âge
- Présence d'un déficit visuel plus ou moins marqué
- Présence d'obstacle à l'observation du fond d'œil
- Référer à un ophtalmologue vétérinaire dès que possible
- Détermination de l'étiologie et traitement de la cause (diabète)
- Détermination du stade de la cataracte et décision du traitement à mettre en place (médical +/- chirurgical)
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 L'ulcère chronique du chien : quand suspecter un ulcère à bords décollés ?
Nîmes, France
I. Introduction
L'ulcère cornéen se définit comme une perte de substance, de surface et de profondeur variable, du tissu cornéen. Il s'agit d'une affection fréquente en ophtalmologie vétérinaire. Le grading des ulcères cornéens permet de les classer en fonction de leur sévérité et de fournir des critères de décision quant à la stratégie thérapeutique à mettre en place. L'ulcère à bords décollés représente une entité bien particulière qui nécessite une prise en charge spécifique.
II. Les différents types d'ulcères cornéens chez le CN [1,2]
Chez le chien, plusieurs types d'ulcères cornéens peuvent être observés.
1. Signes cliniques
a) Signes fonctionnels
La douleur oculaire est bien souvent le signe d'appel de l'ulcère cornéen. La densité des fibres sensitives de la cornée étant plus importante dans l'épithélium et le stroma antérieur, la douleur est souvent plus marquée pour les ulcères superficiels que les ulcères profonds. Elle peut se manifester par un blépharospasme, un épiphora, une photophobie, une énophtalmie, une procidence de la membrane nictitante.
b) Signes physiques
L'examen à distance laisse souvent apparaître une tache opalescente résultant de l'œdème cornéen accompagnant l'ulcère. La présence d'une rougeur oculaire, éventuellement d'un myosis, est fréquente. L'examen de la cornée avec un système grossissant (loupe, biomicroscope) est conseillé afin de caractériser, au mieux, les propriétés physiques de l'ulcère : étendue, profondeur, forme, marges. La néovascularisation superficielle ou profonde peut également être associée. En cas de libération de collagénases, une lyse du stroma s'installe et provoque le phénomène de kératomalacie.
2. Cicatrisation épithéliale
La cicatrisation d'un ulcère épithélial se fait par épithélialisation grâce à la modification des cellules épithéliales bordant l'ulcère. En quelques heures, celles-ci s'aplatissent, perdent leurs attaches avec les cellules voisines et migrent par glissement dans le fond de l'ulcère puis s'y multiplient. L'épithélium peut ainsi être restitué en 24 à 72 h. Un ulcère épithélial non compliqué doit donc, en théorie, cicatriser en quelques jours. En cas d'ulcère périphérique ou étendu, la régénération peut se faire à partir de l'épithélium conjonctival et associer un bourgeon inflammatoire vascularisé.
3. Causes
Les principales causes et facteurs favorisants d'ulcères cornéens chez le chien sont :
- le traumatisme physique (griffure, corps étranger, entropion, distichiasis, cil ectopique, trichiasis)
- l'infection bactérienne
- la brûlure
- le déficit lacrymal qualitatif ou quantitatif (œil sec)
- le déficit de sensibilité cornéenne
- le défaut d'occlusion palpébrale (macrofente, paralysie du nerf crânien VII, exophtalmie, buphtalmie)
- l'œdème cornéen stromal chronique
- la dystrophie épithéliale
4. Diagnostic
Les critères épidémiologiques doivent être pris en compte (race, âge).
Un examen méthodique doit être conduit et consiste à rechercher les causes évoquées ci-dessus. Une analyse des annexes de l'œil doit être faite ainsi qu'une recherche de toute anomalie du film lacrymal ou de conformation des paupières. Le test de SCHIRMER et le break up time doivent être évalués. Il faut également procéder à une vérification du réflexe palpébral par attouchement palpébral et du réflexe cornéen. Il est important de systématiser l'examen des culs-de-sac conjonctivaux et de la face postérieure de la membrane nictitante.
L'examen de la cornée doit ensuite permettre de définir l'étendue de l'ulcère, sa profondeur (examen au biomicroscope en fente), la qualité des marges de l'ulcère, la présence de signes de surinfection, la présence d'une néovascularisation. La présence d'une uvéite réactionnelle doit aussi être recherchée. Le test à la fluorescéine vient compléter l'examen.
Le niveau de gravité est défini ainsi :
- grade 1 : ulcère épithélial aigu
- grade 2 : ulcère stromal antérieur
- grade 3 : ulcère profond/ kératomalacie/ descemetocèle
- grade 4 : ulcère perforé
III. Comment reconnaître un ulcère à bords décollés
1. Critères [2]
L'ulcère à bords décollés est aussi appelé ulcère superficiel chronique, ulcère du Boxer, ulcère atone ou encore SCCED (spontaneous chronic corneal epithelial defect) . L'ulcère à bords décollés est un ulcère strictement épithélial, non infecté, qui ne se résout pas spontanément dans un délai de cicatrisation normal (environ 10 jours).
Il s'agit d'une dystrophie de l'épithélium cornéen. Des prédispositions raciales sont connues : Boxer, Épagneul Breton, Bulldog Anglais et Bouledogue Français, sans prédisposition de sexe. Ce type d'ulcère peut toutefois être rencontré chez des chiens de toute race. Les chiens d'âge moyen, voire avancé semblent plus fréquemment concernés. Les deux yeux peuvent être touchés au long de la vie de l'animal et des récidives sont possibles.
Cliniquement, le signe d'appel est, comme pour la plupart des ulcères, la douleur oculaire. L'ulcère à bords décollés se présente sous la forme d'une plage grisâtre, le plus souvent axiale ou paraxiale, parfois légèrement granuleuse, bordée de lambeaux épithéliaux non adhérents et parfois surélevés. Une néovascularisation périphérique peut être présente, voire s'accompagner d'un bourgeon inflammatoire. Cependant, l'ulcère à bords décollés peut parfois rester atone pendant plusieurs mois sans engendrer d'angiogenèse.
Une coloration floue de la fluorescéine est visualisée sous la berge épithéliale signant la présence de bords décollés. L'ulcère à bords décollés se caractérise donc par une infiltration de la fluorescéine sous l'épithélium bordant l'ulcère. Ceci matérialise le décollement de l'épithélium (Photo 1).
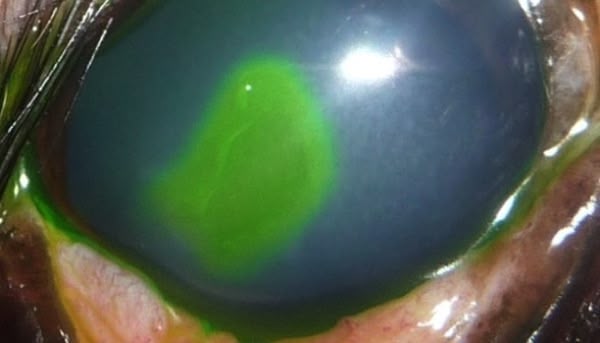
Photo 1 : visualisation de la coloration floue de la fluorescéine sous la berge épithéliale
2. Démarche diagnostique
Le diagnostic d'ulcère à bords décollés est fondé sur les éléments cliniques et anamnestiques décrits ci-dessus (présentation clinique, durée d'évolution, prédispositions raciales). Il reste toutefois important d'éliminer les causes qui pourraient expliquer ce retard de cicatrisation :
- corps étranger
- entropion/anomalie ciliaire
- surinfection
- insuffisance lacrymale
- défaut d'occlusion palpébrale (macrofente, paralysie du nerf crânien VII, exophtalmie, buphtalmie)
- œdème cornéen chronique
Dans ces cas, c'est la résolution du facteur d'entretien de l'ulcère qui permettra d'en obtenir la cicatrisation (par exemple : corriger un entropion, retirer un cil ectopique).
Une fois que toutes ces causes ont pu être exclues, l'ulcère à bords décollés peut être considéré comme un ulcère primaire. On parle de dystrophie épithélio-basale ou dystrophie épithéliale.
3. Éléments histopathologiques
L'étude des dystrophies épithéliales a montré que ces cornées présentaient [2] :
- un épithélium se détachant du stroma, caractérisé par une perte de sa structure en couche
- la présence d'une zone hyaline acellulaire à la surface du stroma composée d'un matériel amorphe et de fibrilles de collagène
- l'altération de la membrane basale épithéliale avec perte des complexes d'adhérence
- une fibroplasie du stroma superficiel
- une diminution de l'expression des facteurs de croissance impliqués dans la migration cellulaire épithéliale
IV. Prise en charge de l'ulcère à bords décollés
1. Traitement chirurgical
Le traitement médical seul n'est pas suffisant. Il doit être vu comme un complément au traitement chirurgical qui représente l'élément principal de la stratégie thérapeutique.
Le débridement ou désépithélialisation est la clef du traitement de l'ulcère à bords décollés. Le débridement de l'ulcère consiste à décoller les berges épithéliales non adhérentes entourant l'ulcère. Ce débridement peut se faire après anesthésie locale (instillation de Cébésine®), à l'aide d'un coton-tige sec. Il n'est pas rare de débrider une zone bien plus large que l'ulcère initial. Un épithélium sain est fermement attaché au stroma cornéen sous-jacent et ne peut donc pas être retiré par simple passage d'un coton-tige. Cette technique seule permet d'obtenir une cicatrisation dans 50% des cas entre 14 et 25 jours. [1,3]
Pour une plus grande efficacité, elle peut être associée à une kératotomie grillagée ou ponctuée qui consiste en une scarification linéaire ou par ponctuations, à l'aide d'une aiguille 25G, jusqu'à 2 mm au-delà des marges de l'ulcère. Pour plus de sécurité, l'aiguille peut être courbée et maintenue par une pince hémostatique afin d'éviter toute lésion profonde. Cette technique permet de créer une effraction de la couche hyaline du stroma antérieur et de favoriser les adhérences des cellules épithéliales. Cette procédure peut également être réalisée sous anesthésie locale, après désinfection à la bétadine diluée. Cette procédure présente un taux de succès de 68 à 87% après 14 jours. [1,3]
Une alternative à la kératotomie grillagée est la thermokératoplastie, réalisée avec un microcautère à pointe fine. La réalisation de ponctuations entraîne une rétraction du stroma favorisant elle aussi l'ancrage du néoépithélium.
Le débridement à la fraise diamantée (diamond burr, Algerbrush®) consiste en un débridement mécanique par fraise motorisée : il permet à la fois le décollement de l'épithélium mais aussi l'abrasion de la couche hyaline acellulaire. À l'instar du débridement au coton-tige et de la kératotomie, il se réalise a minima sous anesthésie locale. La fraise diamantée est appliquée par des mouvements circulaires sur toute la surface lésée, en appliquant une légère pression. Le taux de cicatrisation est de 75 à 85% après 15 jours [4,5]. Les complications sont rares pour cette technique (surinfection, collagénolyse, dans moins de 5% des cas). Un soin attentif au nettoyage et à la stérilisation de la fraise diamantée est conseillé.
Des méthodes de protection peuvent être associées afin de maximiser les chances de réussite. Il peut s'agir d'un recouvrement par la membrane nictitante ou de la pose d'une lentille-pansement. L'objectif de ces techniques protectrices est de favoriser la migration épithéliale en limitant les contraintes mécaniques pouvant être liées au milieu extérieur.
Enfin la kératectomie lamellaire superficielle est le retrait microchirurgical d'une fine lamelle superficielle de cornée incluant notamment la zone hyaline acellulaire et permettant ainsi la formation de nouveaux complexes d'adhérence entre le stroma et l'épithélium cornéen. Cette technique est plus invasive (anesthésie générale et fibrose cicatricielle) et plus technique, mais offre une efficacité maximale : 100% de cicatrisation à 9 jours. [3]
Le choix de l'une ou l'autre de ces techniques dépend de multiples facteurs (durée d'évolution, caractère récidivant, risque anesthésique, budget, etc.)
2. Traitement médical
Le traitement médical doit être considéré comme un complément au traitement chirurgical et non comme un traitement qui peut être utilisé seul. Une antibioprophylaxie large spectre topique est conseillée (2 à 3 fois par jour) jusqu'à cicatrisation de l'ulcère. Un traitement cycloplégique doit être prescrit en présence de signes de douleur. Les collyres à l'acide hyaluronique favorisent la migration épithéliale et limitent l'effet abrasif des paupières. Il peut être intéressant de les maintenir jusqu'à plusieurs semaines après cicatrisation.
Bibliographie
- WHITLEY RD, HAMOR RE. Diseases and Surgery of the canine cornea and sclera. Dans: Veterinary Ophthalmology 6è Ed. Hoboken, éd. John Wiley & Sons. 2021:1082-1172.
- BENTLEY E. Spontaneous chronic corneal epithelial defects in dogs: a review. J Am Anim Hosp Assoc. 2005;41;158-165.
- STANLEY R et coll. Results of grid keratotomy, superficial keratectomy and debridement for the management of persistent corneal erosions in 92 dogs. Vet Ophthalmol. 1998(1):233-238.
- GOSLING A, et coll.. Management of spontaneous chronic corneal epithelial defects (SCCEDs) in dogs with diamond burr debridement and placement of a bandage contact lens. Vet Ophthalmol. 2013(16):83-88.
- SPERTUS CB, et coll. Diamond burr debridement vs. grid keratotomy in canine SCCED with scanning electron microscopy diamond burr tip analysis. Vet Ophtalmol. 2017;20(6):505-513.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 L’épilepsie idiopathique : lien entre le chien et le vétérinaire
Saint-Laurent-du-Var, France
I. Rappel sur la nomenclature
- Crise : événement soudain, transitoire et de courte durée
- Crise épileptique : manifestation transitoire des signes moteurs/autonomiques/sensitifs, secondaire à une activité neuronale cérébrale anormale/excessive souvent autolimitant.
- Épilepsie : l'épilepsie est une maladie cérébrale, provoqué par activité soudaine et anormale des réseaux neuronaux, caractérisées par des manifestations motrices, autonomes et/ou comportementales.
- En pratique : au moins 2 crises à plus de 24 h d'intervalle
Les crises épileptiques peuvent être classifiées ou caractérisées en fonction de :
1. Aspect des crises
- Focales / généralisées
- Toniques/cloniques/tonico-cloniques/ atoniques/myocloniques
2. Fréquence des crises
- Crises isolées – crises à plus de 24 h d'intervalle
- Crises groupées (« cluster ») – plusieurs crises en 24 h (animal normal entre les crises)
- Status epilepticus - une crise > 5 min / plusieurs crises en 24 h, entre lesquelles animal ne récupère pas.
3. Selon la cause des crises
- Crises réactionnelles – secondaire à un trouble métaboliques/toxiques – réversible lorsque la cause ou le trouble est corrigé.
- Épilepsie structurelle : crises épileptiques provoquées par une pathologie intracrânienne/cérébrale, incluant des causes vasculaires, inflammatoires/infectieuses, traumatiques, anomalies/développementales, néoplasiques et dégénératives.
- Épilepsie cryptogénique/ d'origine inconnue, sans cause structurelle identifié
4. Épilepsie idiopathique
- génétique confirme (ex. Lagotto romagnolo)
- génétique suspecte (prévalence >2% de la population)
- idiopathique sans cause génétique suspecté
La prévalence de l'épilepsie chez le chien est estimée entre 0,6% et 0,75% dans la population canine générale.
II. Consultation d'un animal présentant des crises
L'approche diagnostique chez un patient présentant des antécédents de crises épileptiques suspectées comporte deux étapes fondamentales : déterminer si les événements observés chez l'animal correspondent réellement à des crises épileptiques, et, le cas échéant, identifier leur cause sous-jacente. Hormis les crises complètes tonico-cloniques, la différenciation entre les crises épileptiques et d'autres événements paroxystiques épisodiques non-épileptiques peut être complexe. Des critères permettant de nous aider dans leur différentiation :
- Signes cliniques entre les crises
- Évènement déclencheur
- Signes pré ictales
- Description détaillée de la crise
- Est-ce possible d'interrompre la crise ?
- Niveau de conscience pendant la crise
- Présence des signes autonomiques (ptyalisme, urines, défécation)
- Tonus musculaire
- Latéralisation des signes
- Durée de crises
- Réponse à un traitement antiépileptique à visée diagnostique
Évènements non-épileptiques pouvant ressembler à des crises d'épilepsie : syncopes d'origine cardiaque (ex. BAV type 3), dyskinésie paroxystique, narcolepsie/cataplexie, stéréotypies/syndrome compulsif canin, tremblement idiopathiques, hyperesthésie féline, épisodes vestibulaires, faiblesse neuromusculaire.
III. Diagnostic d'une épilepsie idiopathique (EI)
1. Trois niveaux de confiance
- Niveau de confiance I : le diagnostic d'EI est basé sur des antécédents de deux crises épileptiques non provoquées ou plus, survenant à au moins 24 heures d'intervalle, un âge de début des crises entre six mois et six ans, un examen physique et neurologique inter-ictal sans anomalies, et l'absence d'anomalies significatives aux examens sanguins de base (NFS, biochimie, ionogramme/gaz du sang) et à l'analyse d'urine.
- Niveau de confiance II : il repose sur les éléments du niveau I, ainsi que des taux d'acides biliaires à jeun et post-prandiaux normaux, une imagerie par résonance magnétique (IRM) du cerveau (conformément à un protocole spécifique à l'épilepsie), et une analyse du liquide céphalo-rachidien (LCR) sans anomalies.
- Niveau de confiance III : il inclut les critères des niveaux I et II, ainsi que l'identification d'anomalies électroencéphalographiques caractéristiques des troubles épileptiques.
Il est recommandé de réaliser une IRM cérébrale et une analyse du LCR après avoir exclu les crises d'origine métabolique, chez les chiens présentant :
- un âge de début des crises épileptiques inférieur à 6 mois ou supérieur à 6 ans
- examen inter-ictal anormal
- des anomalies neurologiques inter-ictales compatibles avec une localisation intracrânienne (pousser au mur, marche en cercle, amaurose, malpropreté, changement de comportement),
- un status epilepticus ou des crises groupées comme première manifestation épileptique
- ou un diagnostic présumé d'EI associé à une résistance aux médicaments malgré l'utilisation d'un antiépileptique à dose maximale tolérée.
IV. Traitement
1. Quand est-ce qu'on met en place le traitement ?
Les recommandations actuelles sont de commencer le traitement si :
- la fréquence des crises dépasse 2 crises en 6 mois
- l'animal est présenté avec un status epilepticus ou crises groupées
- l'animal souffre d'une période post-ictal longue et sévère
- la fréquence et/ou la durée des crises épileptiques augmentent et/ou la gravité des crises s'aggrave au cours de trois périodes inter ictales
- crises d'apparition 2 semaines après un trauma crânien
- crises avec une cause structurelle connue
2. Objectif du traitement
Obtenir zéro crise est la plupart du temps inaccessible. Des objectifs plus réalistes consistent à réduire la fréquence, la durée, la gravité des crises, ainsi que le nombre total de crises épileptiques sur une courte période, tout en limitant ou en évitant les effets indésirables des médicaments antiépileptiques, afin d'optimiser la qualité de vie du chien et de son propriétaire.
La réponse qui est actuellement considérée comme bonne, est la diminution de la fréquence des crises de 50% ou une période inter ictal d'au moins 3 mois, mais cela dépend bien évidemment des attentes des propriétaires et de la sévérité des crises initiales.
3. Quel traitement choisir ?
Plusieurs molécules sont actuellement accessibles comme un traitement de première intention. Le choix dépend de la préférence et l'expérience du vétérinaire, le mode de vie de l'animal et le propriétaire, les contraintes financières, le type de crises, les effets secondaires. Les molécules, leur dosage, effets secondaires et suivis sont résumés dans le tableau 1.
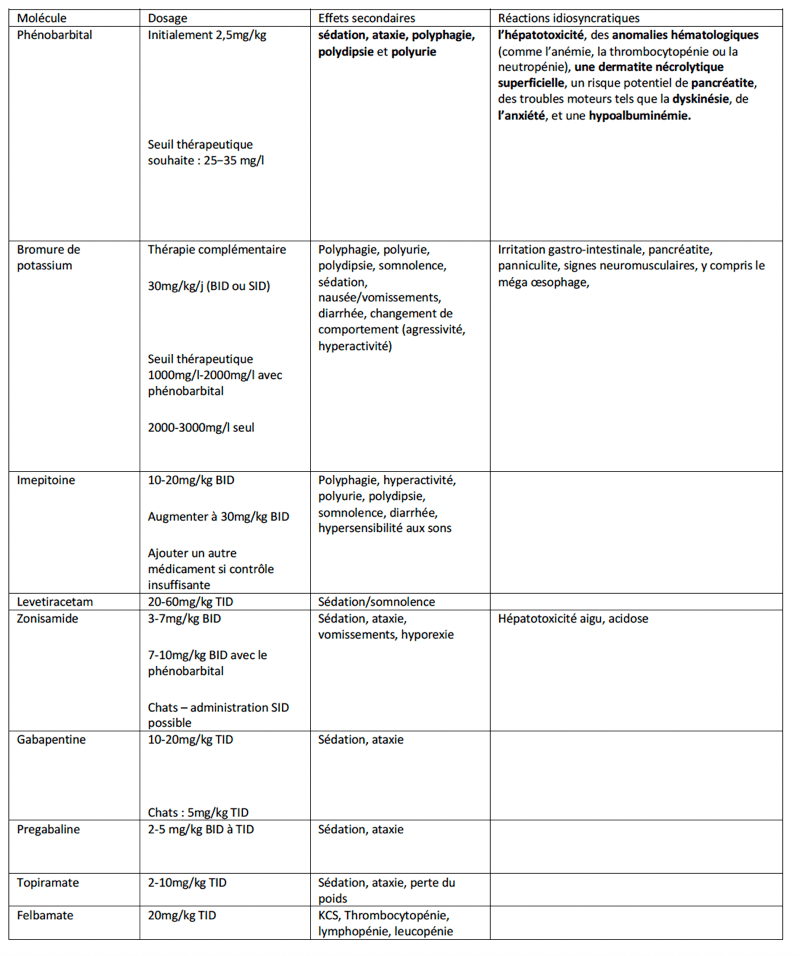
Tableau 1
En général, il est recommandé de privilégier la monothérapie et d'augmenter progressivement le dosage en absence de réponse satisfaisante.
4. Quand et pourquoi est-ce qu'on ajoute/change le traitement ?
- En absence d'amélioration significative avec le traitement de première intention après l'augmentation de doses
- En cas d'intolérance au traitement/effets secondaires trop importants
⚠ Tout changement doit se faire progressivement. On n'arrête pas le traitement antiépileptique d'un coup !
V. Suivi d'un animal épileptique
- adaptation du traitement en fonction de la fréquence de crises
- contrôle des effets secondaires cliniques +/- biochimiques/hématologiques
Possibilité de dosage pour :
1. Phénobarbital
- dosage 14 jours après la mise en place du traitement et après chaque changement de dose ;
- un deuxième dosage est conseillé après 6 semaines (évaluation d'effet de tolérance métabolique) ;
- NFS, biochimie incluant triglycéride, cholestérol et acides biliaires – 3 mois après le début du traitement et ensuite tous les 6 mois (tous les 12 mois si absence des crises)
- tolérance thérapeutique possible au bout de 30-45 jours (induction de cytochrome P450 hépatique).
2. KBr
- dosage à 3 mois ;
- biochimie de base tous les 6 mois.
3. Est-ce que l'arrêt du traitement est envisageable ?
Globalement, on considère qu'une fois le traitement mis en place, l'animal épileptique devra le suivre toute sa vie. Il existe néanmoins certaines situations particulières ou l'arrêt du traitement peut être indiqué, notamment :
- si les effets secondaires mettant la vie en danger ;
- si rémission des crises : au moins 1-2 ans sans crises, fréquence basse des crises avant la mise en place du traitement.
L'arrêt doit être progressif, sous surveillance, et le propriétaire doit être clairement informé des risques de rechute.
Bibliographie
- DE RISIO L. et coll. Canine and Feline Epilepsy, 1st ed. CAB International. 2014
- BERENDT M. et coll. International veterinary epilepsy task force consensus report on epilepsy definition, classification and terminology in companion animals. BMC Vet Res. 2015;11:182. Published 2015 Aug 28. doi:10.1186/s12917-015-0461-2
- DE RISIO L et coll. International veterinary epilepsy task force consensus proposal: diagnostic approach to epilepsy in dogs. BMC Vet Res. 2015;11:148. Published 2015 Aug 28. doi:10.1186/s12917-015-0462-1
- BHATTI SF. et coll. International Veterinary Epilepsy Task Force consensus proposal: medical treatment of canine epilepsy in Europe. BMC Vet Res. 2015;11:176. Published 2015 Aug 28. doi:10.1186/s12917-015-0464-z
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 L’épilepsie idiopathique : lien entre le propriétaire et le chien
Saint-Laurent-du-Var, France
I. Introduction
L'épilepsie idiopathique est une maladie chronique fréquemment rencontrée chez les chiens (0,62% de la population générale). Notre attention se concentre souvent sur l'aspect clinique et médical de la gestion de cette maladie. Peu d'attention est accordée aux défis émotionnels et logistiques des propriétaires.
La vie avec un animal épileptique nécessite quasiment toujours des adaptations du mode de vie, des adaptations logistiques et des compromis. Il est important de comprendre l'importance de ces aspects pour pouvoir accompagner au mieux les propriétaires, en tant que vétérinaire traitant d'un animal épileptique.
Pour nous, une consultation pour un animal épileptique fait partie des consultations courantes. En revanche, pour les propriétaires, le diagnostic d'épilepsie peut bouleverser la relation avec leur chien, leur mode de vie, ainsi que leurs attentes vis-à-vis de leur animal. Il est important de se rendre compte de toutes les limites liées à la maladie et des implications pour les propriétaires, sans négliger les aspects moins médicaux.
II. Considérations à prendre en compte
- Stress lié à l'apparition des crises et incertitudes sur le futur de l'animal
- Frustration liée à l'inefficacité du traitement et incompréhension de la maladie
- Peur de laisser l'animal sans surveillance
- Changements de mode de vie nécessaires pour maintenir la continuité des soins et liés aux effets secondaires du traitement : changements alimentaires, sanitaires, aménagement des horaires de travail
- Changement de l'activité quotidienne de l'animal
- Changements de comportement de l'animal liés aux crises et à la prise de médicaments
- Impact sur la qualité du lien entre le chien et le propriétaire
- Impact social envers les personnes hors du cadre familial
- Le lien possible entre l'épilepsie et : un syndrome de dysfonctionnement cognitif plus précoce que dans la population globale, anxiété, troubles du comportement
III. Changements liés au traitement
- Tout traitement antiépileptique a des effets secondaires plus ou moins marqués. Ces effets vont également dépendre de la dose utilisée, d'une association éventuelle avec d'autres médicaments et d'une sensibilité individuelle de l'animal.
- Certains effets secondaires peuvent significativement diminuer la qualité de vie de l'animal et de son propriétaire.
- Une prise de poids et la baisse d'activité de l'animal sont des effets secondaires parmi les plus courants.
- Polydipsie et polyurie – épisodes de malpropreté, nécessité de promenades plus fréquentes ou d'un accès facile à l'extérieur.
- Changement de comportement lié au bromure de potassium, agressivité – controversé, un effet secondaire assez rare.
- Mesures de précaution – alimentation stricte sans friandises, ration alimentaire contrôlée, ajout d'une alimentation riche en acides gras saturés à chaîne moyenne (MCT)
IV. Comment le propriétaire peut-il aider son chien épileptique pendant la crise
Il est important de préciser aux propriétaires que tous les gestes qu'ils peuvent effectuer sur leur chien en convulsion doivent servir à mettre le chien en confort ou à éviter les dangers liés à la crise, mais ne doivent surtout pas mettre en danger le propriétaire.
1. Gestes à éviter
- Mettre les mains dans la gueule du chien
- Prendre l'animal dans les bras, le coller contre soi – un geste qui réconforte le propriétaire, mais qui n'a aucun impact sur la durée ou l'arrêt de la crise
2. Gestes utiles
- Couvrir les yeux de l'animal, le garder au calme
- L'éloigner d'un endroit dangereux (ex. si la crise arrive sur un escalier, arbre à chats, etc.)
- Essayer de le refroidir si la crise est prolongée (surtout chez les animaux brachycéphales) pour éviter les complications d'un coup de chaleur
3. Est-ce que le propriétaire peut faire quelque chose pour éviter la crise
- Aucun geste hors médicaments ne peut arrêter une crise convulsive.
- Il existe de très rares exemples d'épilepsie induite par un événement externe – dans ce cas, le propriétaire peut essayer d'éviter le stimulus.
V. Question fréquente – Est-ce que mon chien peut mourir pendant la crise ?
- Les cas de décès d'animaux pendant ou directement après une crise sont très rares, sauf en cas de status epilepticus.
- Probable Sudden Unexpected Death « probable mort subite et inattendue chez les chiens épileptiques ». C'est un phénomène très rare (4,5–10% dans une étude).
- Le lien entre le décès et la crise est souvent incertain. Décès d'un animal épileptique, d'origine inexpliquée, sans status epilepticus.
- Risque plus élevé chez les brachycéphales et les chiens présentant un historique de crises groupées.
- Le risque d'un œdème non cardiogénique suite à des crises est légèrement augmenté chez les animaux brachycéphales.
- Les essais de dégagement des voies respiratoires à la maison sont à éviter (très souvent inutiles, inefficaces et dangereux).
VI. Utilisation des benzodiazépines : quand, quoi, comment ?
- La plupart des crises d'épilepsie sont auto limitantes et durent quelques secondes ou minutes (généralement moins de 2 à 3 minutes).
- Dans certains cas, les crises peuvent se prolonger, conduisant au développement d'un status epilepticus (SE).
- Le SE est défini comme des crises durant plus de 5 minutes ou comme des crises multiples sans récupération complète entre les épisodes.
- C'est une urgence neurologique fréquente, qui peut conduire à des séquelles neurologiques irréversibles et des complications systémiques si elle n'est pas traitée correctement.
- Les propriétaires jouent un rôle important dans le contrôle des crises, car l'administration appropriée de médicaments antiépileptiques à domicile peut prévenir l'évolution vers un SE ou réduire le risque de progression vers des stades plus réfractaires.
1. Quand ?
- La durée de la crise dépasse 5 minutes ? En pratique, 5 minutes deviennent un SE, donc il vaut mieux réagir avant, dès que la crise paraît plus longue qu'habituellement
- Enchaînement des crises – à partir de la deuxième crise sans récupération complète
2. Quoi ?
Benzodiazépines : les effets des benzodiazépines (BZD) proviennent de leur action sur la transmission GABAergique pré- et post-synaptique. Plus précisément, elles se lient à la sous-unité γ des récepteurs GABA_A, renforçant l'effet inhibiteur du GABA, ce qui entraîne l'ouverture des canaux chlorure et l'entrée d'ions chlorure dans les neurones.
Cet effet provoque une hyperpolarisation de la membrane cellulaire et une inhibition de la transmission des influx nerveux.
a) Diazépam
- 0,5–2 mg/kg
- Le plus fréquemment prescrit
- Enregistré pour l'utilisation chez les animaux
- Voies d'administration : intrarectale, intraveineuse, intranasale
- Inconvénients : peut provoquer des phlébites et une hypotension (administration IV – contenant du propylène glycol)
- Maximum 2–3 administrations en bolus – accumulation dans le système nerveux central pouvant provoquer une dépression cardiovasculaire
- Garder à l'abri de la lumière, doit être préparé directement avant l'administration (inefficace s'il reste trop longtemps dans la seringue, absorption sur le plastique)
b) Midazolam
- 0,2–0,5 mg/kg
- De plus en plus populaire
- Plus puissant que le diazépam
- Moins d'effets de dépression cardiovasculaire
- Prescription sur ordonnance sécurisée
- Voies d'administration : intranasale, intraveineuse, intramusculaire
3. Comment – voie d'administration ?
a) Intra-rectale
- La plus populaire
- Seulement diazépam
- Résorption variable
- Contrôle des crises obtenu après environ 2,5 min
- Difficultés d'administration variables (pertes de produit fréquentes avec l'émission de selles)
b) Intra-nasale
- Prescription d'une seringue avec atomiseur
- Diazépam et midazolam possibles (plus de données avec le midazolam)
- Difficultés chez les races brachycéphales
- Risque de morsure
- Contrôle des crises obtenu après environ 0,5–1,6 min (pour le midazolam)
- Plus efficace selon les études cliniques
- Choix des propriétaires : le midazolam intranasal était perçu par les propriétaires comme une meilleure option en termes d'efficacité et de rapidité d'arrêt des crises.
c) Autres voies – anecdotiques
- Per os, sublinguale (déconseillé pendant la crise, risque de morsure, hypersalivation)
- IM – personnel médical ?
VII. Suivi d'un animal épileptique – importance de tenir un journal
L'épilepsie est une maladie chronique qui nécessite une bonne observance à long terme. La possession d'un journal de crises permet de suivre l'évolution de la maladie, les changements éventuels d'aspect des crises et la réponse au traitement à long terme. C'est un outil important qui permet de quantifier le nombre de crises et de suivre l'évolution de la maladie de façon objective.
Une surveillance rapprochée des crises peut également rassurer certains propriétaires (sensation de contrôle de la situation). Le journal des crises est un outil utile non seulement pour les vétérinaires, mais aussi pour les propriétaires, leur permettant de suivre l'évolution de leur chien à domicile et de rechercher d'éventuels facteurs déclenchants. La tenue de ces registres permet aux propriétaires d'améliorer les soins de leur chien.
1. Informations à noter dans le journal
Dates, nombre de crises, durée, aspect, éventuellement présence de la phase pré- et post-ictale
2. Informations supplémentaires souvent notées par les propriétaires
Les doses de médicaments, changements thérapeutiques, les traitements d'appoint, les résultats d'analyses de laboratoire
VIII. Observance du médicament
- Le terme observance médicamenteuse décrit la régularité et la précision avec lesquelles un client suit le traitement prescrit par le vétérinaire.
- Une mauvaise observance est fréquente chez les chiens épileptiques et peut significativement influencer le contrôle des crises.
- Une mauvaise observance peut entraîner un échec du traitement ; il est donc important de prendre en compte les facteurs pouvant influencer la volonté ou la capacité d'un client à suivre le traitement prescrit.
- Les propriétaires peuvent surestimer de manière significative leur taux d'observance. Ainsi, des méthodes d'évaluation objectives, telles que le comptage des comprimés, sont nécessaires pour calculer le véritable taux d'observance.
Bibliographie
- CHARALAMBOUS M, VOLK HA, VAN HAM L, BHATTI SFM. First-line management of canine status epilepticus at home and in hospital-opportunities and limitations of the various administration routes of benzodiazepines. BMC Vet Res. (2021) 17:103. doi: 10.1186/s12917-021-02805
- PERGANDE AE, BELSHAW Z, VOLK HA, PACKER RMA. « We have a ticking time bomb » : a qualitative exploration of the impact of canine epilepsy on dog owners living in England
- PEEK SI, MELLER S, TWELE F, PACKER RMA, VOLK HA. Epilepsy is more than a simple seizure disorder : Parallels between human and canine cognitive and behavioural comorbidities
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 L’épilepsie idiopathique : lien entre le vétérinaire et le propriétaire
Créteil, France
I. Introduction
L'épilepsie par sa manifestation clinique préoccupante et par sa chronicité nécessite une pleine confiance et collaboration entre le vétérinaire et le propriétaire. C'est une condition importante pour la réussite de la démarche diagnostique et ensuite thérapeutique.
Ce lien se crée lors de la première consultation où le vétérinaire devra interroger le propriétaire pour :
- Reconnaitre le caractère épileptique de l'évènement et le différencier des autres évènements paroxystiques ;
- Chercher dans l'anamnèse et les commémoratifs des éléments d'orientation sur la cause de l'épisode paroxystique ;
- Expliquer la démarche diagnostique ;
- Expliquer la démarche thérapeutique, les objectifs thérapeutiques et les effets secondaires des traitements ;
- Rassurer le propriétaire sur les risques d'une crise convulsive et le devenir du chien épileptique.
Ce lien se poursuit également lors des consultations de suivi ou le vétérinaire devra vérifier :
- L'observance du traitement ;
- La vérification de l'efficacité du traitement ;
- La vérification de la tolérance du traitement (par le chien dans sa vie quotidienne et parfois aussi par le propriétaire). Le temps d'écoute du propriétaire est très important.
Il devra également expliquer les évolutions thérapeutiques.
II. Les questions pour reconnaitre la crise
Pour reconnaitre les symptômes présentés, nous allons nous appuyer sur les différentes parties qui entourent et composent l'épisode paroxystique, sur sa morphologie et sur ses circonstances d'apparition. Les circonstances d'apparition sont importantes pour nous aider à envisager un autre évènement paroxystique qu'une crise convulsive (syncope et trouble respiratoire, syncope et effort, trouble de la motricité volontaire et excitation…) mais aussi sur l'affection métabolique responsable de la crise (encéphalose hépatique et crise post prandiale, hypoglycémie et crise à l'effort).
1. Les différentes parties de la crise
Une crise connait une expression clinique variable. On peut reconnaître différentes parties au sein de la crise : les prodromes, l'aura, l'ictus et la phase post ictale. La reconnaissance de cette séquence aide à reconnaitre une crise d'épilepsie
2. Les différentes crises épileptiques
Toute manifestation involontaire inhabituelle qui est paroxystique et récurrente doit être évaluée comme une crise.
Leur morphologie est rappelée dans le texte sur la relation chien et vétérinaire.
a) La crise généralisée
b) La crise focale
- La crise focale simple
- La crise focale complexe
3. Autres syndromes paroxystiques
Ces syndromes entrent dans le diagnostic différentiel des crises de type épileptique. Il est important de les avoir à l'esprit lors de la consultation pour poser les bonnes questions et rechercher des signes qui nous aideront à définir la nature des symptômes observés. Ils sont développés dans le texte « syncopes d'origine cardiaque ».
a) La syncope
b) Le syndrome narcolepsie
c) La crise algique
d) Le syndrome vestibulaire
e) les mouvements anormaux : crampe, myoclonie, fasciculations, collapsus induit par l'exercice….
III. Les questions pour chercher la cause
Les questions posées au propriétaire sont essentielles pour nous orienter vers les bonnes hypothèses diagnostiques. L'examen général joue également un rôle essentiel pour en rechercher la cause, mais aussi les conséquences. Ceci sera abordé dans la présentation sur relation entre le chien et le vétérinaire.
Le syndrome convulsion connait trois grandes origines :
- les causes extra-crâniennes ;
- les causes intracrâniennes ;
- l'épilepsie idiopathique.
Avec des prédispositions raciales, d'âge, de circonstance différente qu'il faut connaitre afin de poser les bonnes questions.
1. L'anamnèse
a) L'âge et la race
Importants à prendre en compte, on a peu besoin du propriétaire pour les connaitre…
b) Les antécédents pathologiques et comorbidités
- Il est important de connaitre le passé médical et l'actualité médicale du patient convulsif.
- Le retrait d'une tumeur il y a quelques mois peut évoquer une métastase cérébrale.
- Des maladies non neurologiques peuvent également nous mettre sur la piste : cystite récidivante lors de shunt portosystémique, syndrome respiratoire passé et maladie infectieuse…
- La connaissance des traitements en cours est également importante : insuline et hypoglycémie, théophylline et convulsion…
c) Le mode de vie et moment d'apparition des crises
- La vie à l'extérieur rend plus favorable l'exposition des animaux à des agents infectieux (néosporose, toxoplasmose, cryptococcose…).
- Le lieu de vie du chien en France ou à l'étranger est également important à savoir dans le cadre de maladie infectieuse.
- Le moment d'apparition des crises peut aussi être un élément d'orientation : après un repas, ceci est en faveur d'une insuffisance hépatique, après un effort ceci peut évoquer une hypoglycémie.
IV. Les informations pour expliquer la démarche thérapeutique et les effets secondaires
1. Quand commencer le traitement ?
Le traitement doit être commencé le plus précocement possible afin de limiter les « remaniements » cérébraux qui contribuent à favoriser l'émergence de nouvelles crises convulsives et à provoquer une moindre efficacité des traitements. Ainsi, un status epilepticus (crise de plus de 15 minutes), des crises groupées (plus d'une crise sur une période de 24 heures) ou une fréquence de crises supérieure ou égale à une tous les six mois sont des situations nécessitant la mise en place d'un traitement.
La décision de traiter doit également prendre en compte le morphotype (les brachycéphales présentent des risques d'hyperthermie et d'hypoxie plus importantes) et la race du chien (les Border Collies et les Bergers Australiens par exemple présentent des épilepsies génétiques avec une évolution péjorative qui invite à mettre un traitement probablement plus précocement), la présence d'agressivité lors de crises ou de la phase post-ictale et l'attente des propriétaires.
2. Quels objectifs se fixe-t-on lors de l'initiation du traitement ?
L'objectif idéal est de zéro crise. Cependant, bien que celui-ci ne soit que rarement atteint, il est nécessaire de traiter. La diminution de l'incidence des crises est tout de même un élément bénéfique.
Les objectifs plus réalistes sont :
- limiter l'incidence des crises groupées ou des status epilepticus,
- diminuer la fréquence des crises d'au moins 50% par rapport à la fréquence initiale sur une période d'observation d'au moins trois périodes interictales,
- diminuer la durée et l'intensité de la crise et de la période post-ictale.
3. Comment initier le traitement : monothérapie versus bithérapie
La monothérapie doit être le traitement de première intention. Le passage à la bithérapie est indiqué lorsque l'animal est réfractaire au premier traitement initié.
Un animal réfractaire se définit comme un animal qui reçoit la dose maximale publiée de principe actif ou qu'il a atteint la concentration sérique médicamenteuse maximale ou qui présente des effets secondaires excessifs altérant significativement sa qualité de vie sans que l'objectif fixé ne soit atteint.
4. Quel principe actif choisir lors de monothérapie et quelles sont ses modalités de suivi ?
Cette hiérarchie prend en compte les obligations légales auxquelles nous sommes tenus, les données d'efficacité publiées et l'expérience des participants.
a) Le phénobarbital :
Du fait de son ancienneté et des publications disponibles, c'est la molécule de première intention.
- La phénobarbitémie est réalisée le lendemain de la dose de charge et/ou 15 jours après l'initiation du traitement. Le moment de la prise de sang dans la journée est sujet à controverse ; il est quoiqu'il en soit préférable de la faire toujours au même moment par rapport à la prise afin de comparer son évolution. Il est également nécessaire de la faire avant toute modification de dose et au minimum deux fois par an.
- Il faut préciser que le phénobarbital provoque une induction enzymatique normale des phosphatases alcalines. Cependant, une augmentation importante de leur activité sérique sans modification de la dose de phénobarbital invite à considérer l'existence d'une hépatopathie.
- La mesure biannuelle de l'albuminémie et de la concentration sérique des acides biliaires se justifie par la nécessité d'obtenir des paramètres évaluant la fonctionnalité hépatique.
- Le bilan lipidique est également indiqué comme facteur pouvant prédisposer à la survenue d'une pancréatite et nécessitant une adaptation de la ration.
- La contre-indication à la prescription de phénobarbital est l'insuffisance hépatique.
b) L'imépitoine
- Les publications récentes tendent à montrer une efficacité égale au phénobarbital avec des effets secondaires cliniques et des modifications biochimiques moindres. Cependant, sa récente mise sur le marché fait que le recul d'utilisation est plus faible en comparaison avec le phénobarbital.
- Aucun suivi biologique n'est nécessaire.
c) Le bromure de potassium
- Il est utilisable en première intention. Cependant, sa pharmacocinétique (demi-vie longue justifiant d'une évaluation possible de l'efficacité de la dose administrée au bout de trois mois seulement) et l'existence de publications rapportant une efficacité moindre que celle du phénobarbital à l'échelle d'une population de chiens épileptiques justifient d'une moindre prescription en monothérapie.
- Il est conseillé de réaliser une bromurémie trois mois après le début du traitement puis tous les six mois.
- En cas d'insuffisance rénale, la dose doit être ajustée, le bromure étant éliminé par les reins.
- La teneur en chlorure de sodium du régime alimentaire doit être stable, l'élimination du bromure se faisant en compétition avec celle des ions chlorures : une augmentation de la teneur en chlorure de sodium de la ration (ou lors de perfusion) entrainant une chute de la bromurémie et inversement.
d) Le lévétiracétam
- C'est une utilisation hors AMM qui en est faite.
- Il est indiqué lors d'hépatopathie.
- Aucun suivi biologique n'est nécessaire du fait de sa grande sécurité. Cependant, une publication récente note une augmentation des paramètres rénaux lors de son utilisation chez certains patients insuffisants rénaux, avec la survenue d'effet secondaires mineurs plus fréquents. Une surveillance de l'urémie et de la créatininémie et un suivi clinique plus « serré » sont probablement préconisés dans ce contexte.
V. Les informations pour préciser le pronostic
L'évolution la plus probable va dépendre de :
- l'état clinique de l'animal au moment de son admission et sa réponse au traitement
- les moyens mis en œuvre pour lui faire passer ce cap.
Un status epilepticus comme des crises groupées ne sont pas en soi un motif d'euthanasie et la plupart des chiens présentant ces symptômes dans le cadre d'une épilepsie essentielle s'en sortent. Une étude sur la survie moyenne semble montrer une réduction de deux ou trois ans des chiens présentant une épilepsie par rapport à des chiens témoins. Une autre étude démontre une survie normale pour les chiens atteint d'une épilepsie essentielle qui n'ont pas fait de status epilepticus et diminuée de 3 ans pour les chiens ayant présenté un status epilepticus. Une des raisons étant probablement le découragement des propriétaires face à ces situations toujours éprouvantes. L'influence raciale est également à prendre en compte dans le pronostic.
Il est également important de préciser au propriétaire que le chien ne souffre pas pendant la crise et que le risque de décès au cours d'une crise est extrêmement faible.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 La cataracte diabétique du chien : présentation clinique et particularités
Montréal, Canada
Ce texte est restitué tel que fourni par l'auteur.
I. Introduction
1. Cataracte
- changement pathologique du cristallin
- chien de tout âge
- opacité de différentes parties du cristallin (capsule, cortex, noyau, équateur) causée par une désorganisation des fibrilles cristalliniennes
- différentes causes possible (héréditaire, métabolique, traumatique…)
- déficit visuel plus ou moins marqué selon le stade
2. Étiologie de la cataracte
- héréditaire
- sénile (liée à l'âge)
- traumatique (griffe de chat, CE…)
- pharmacologique (DMSO, ketoconazole), toxique (acétone, CE métallique), autres (radiations, électrocution)
- parasitaire : Encephalitozoon cuniculi
- secondaire à maladie oculaire : uvéite, luxation ou sub-luxation, APR
- maladie systémique : diabète mellitus, hypocalcémie, hypercuprémie, hypergalactosémie
3. Manifestations oculaires du Diabète Mellitus chez le chien
a) Cataracte
Complication la plus fréquente du diabète chez le chien :
- 50-70% en 6 mois
- 75% dans les 12 mois
Pathogénie : élévation de la glycémie, saturation de la voie glycolytique aérobie, prépondérance de la voie des polyols → sorbitol, fructose → gradient osmotique → appel d'eau → désorganisation des fibres du cristallin = cataracte diabétique ou osmotique
b) Autres manifestations
- uvéite
- cicatrisation cornéenne anormale
- rétinopathies
- lipemia retinalis (rétine lipémique), aqueous lipid laden (épanchement de lipides dans l'humeur aqueuse)
- différent chez le chat
- chez l'homme (vascularite rétinienne diabétique)
II. Diagnostic différentiel et étiologique
1. Diagnostic différentiel
- Cataracte = opacité versus Sclérose nucléaire = opalescence
- Cataracte versus autres opacités du cristallin ou en avant ou en arrière
2. Diagnostic étiologique
a) Signes cliniques systémiques du diabète mellitus
- PUPD
- puis +/- perte de poids, perte d'énergie, infection urinaire, vomissements…
b) Signes cliniques oculaires
Au niveau du cristallin :
- initialement lésions équatoriales sous formes de vacuoles (importance de réaliser une dilatation des pupilles – tropicamide 1%)
- puis progression en opacité et extension rapide à l'ensemble du cristallin
- souvent opacité bilatérale et synchrone
- opacité très dense, avec souvent lignes de sutures très marquées ("crevasses")
Autres :
- uvéite antérieure marquée
Pathogénie : protéines du cristallin désorganisées et réaction de glycosylation → modifications des protéines (cristallines) et de certaines enzymes protégeant contre les radicaux libres + fuite des cristallines hors du sac et réaction endo-oculaire de type HS → inflammation = uvéite phacolytique.
Voir avec "Aqueous lipid laden".
Si rupture de capsule cristallinienne alors uvéite phacoclastique encore plus sévère… (importance de réaliser une mesure des pressions intra-oculaires)
- sensibilité cornéenne réduite / cicatrisation cornéenne compromise
Pathogénie : sensibilité cornéenne réduite → implication dans la protection de la cornée (larmes, fermeture des paupières, production de collagène) => kératite ulcérative fréquente et lente à guérir
- changements pathologiques de la cornée (perte de cellules endothéliales)
- rétinopathie diabétique
- Corrélation entre rétinopathie et contrôle glycémique
- Hémorragies rétiniennes, micro-anévrisme
- Changements histologiques : épaississement de la MB, shunts/atrophie des capillaires, perte des péricytes intra-muraux, micro-anévrismes
- Discrète chez le chien/chat ou masquée par les cataractes
- diabète et hypertension artérielle :
Incidence d'une hypertension concomitante :- Homme 40-80% - Chien 46%
- Mécanisme possible : métabolisme des lipides affecté, perméabilité des vaisseaux modifiée…
- Hypertension → rétinopathie : hémorragies, œdème, effusions sous-rétiniennes, décollement
c) Conclusion partielle
Faire un bon examen général :
- bonne anamnèse
- avec au moins mesure de la glycémie
- mais encore mieux : hématologie et biochimie +/- pression artérielle
Faire un bon examen oculaire, avec :
- transilluminateur, ophtalmoscopie (et lampe à fente) AVEC dilation de la pupille (Tropicamide 1%)
- test de Schirmer (15-25 ml/min)
- mesure des PIO (15-25 mmHg et moins de 5 mmHg de différence entre les deux yeux)
III. Démarche thérapeutique
1. Évaluation de la cataracte
a) Évaluation de l'animal
- Qualité de vie :
- âge
- douleur
- tempérament, activités
- évaluation du déficit visuel associé
- De l'animal lui-même :
- santé générale (maladie systémique : contrôle de son diabète)
- possibilité de faire les traitements post-op (observance du patient)
b) Évaluation du propriétaire
- compréhension des risques/complications, des coûts
- possibilité de faire les traitements et les suivis post-op (observance du propriétaire)
c) Évaluation de l'œil
- identification/confirmation de la cause
- détermination du stade
- signes cliniques associés (PIO, STT)
Si une chirurgie est eenvisagée,alors tests complémentaires à effectuer :
- échographie oculaire
- électrorétinogramme
2. Traitement médical de la cataracte
- Une cataracte entraîne une uvéite (uvéite phacolytique)
- Mesure de pressions intra-oculaires (PIO)
- Traitement médical :
- Anti-inflammatoire Non Stéroïdien (systémique / topique AIS court terme) (meloxicam, robenacoxib) (dexaméthasone, prednisolone, diclofénac, kétorolac)
- +/- mydriatique/cycloplégique (atropine 1%, tropicamide)
- Chirurgie ou pas, l'uvéite doit être contrôlée : AINS long terme en topique
- Pour que l'œil reste un bon candidat pour la chirurgie
- Pour réduire le risque de complications si PAS de chirurgie : glaucome, luxation, DR, uvéite sévère
3. Traitement chirurgical de la cataracte
- Phaco-émulsification +/- implantation de cristallin artificiel
- Seulement après une évaluation rigoureuse
- Particularités à considérer dues au diabète :
- uvéite post-op plus marquée (voir aqueous lipid laden)
- cicatrisation cornéenne retardée, ulcère
- rupture de capsule - possibilité de mise en place d'un implant
IV. Conclusion
Cataracte diabétique :
- ¾ des chiens diabétiques vont développer une cataracte
- Accumulation de sucre dans le cristallin → appel massif d'eau → cataracte osmotique
- Importance de diagnostiquer les cataractes le plus tôt possible (dilatation)
- Importance de traiter le diabète le mieux possible
- Importance de traiter l'uvéite phacolytique
- Référer à un ophtalmologue vétérinaire dès que possible :
- détermination du stade de la cataracte
- décision du traitement à mettre en place (médical +/- chirurgical)
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 La dentisterie, un levier de croissance économique ? (dont RX)
Bandol, France
I. Introduction
La dentisterie vétérinaire représente un domaine crucial pour la santé animale, avec une prévalence élevée de maladies parodontales chez 70% des chats et 80% des chiens de plus de trois ans à moins qu'une mesure préventive n'ait été prise [1]. Dans les populations des chats présentés en consultation pour soins dentaires, 60-70% d'entre eux sont atteints de résorptions dentaires [2]. Cependant, en France, les revenus générés par la dentisterie restent nettement inférieurs à leur potentiel, ne représentant que moins de 5% du chiffre d'affaires total des cliniques, contre 10 à 20% aux États-Unis et au Royaume-Uni. Ce constat met en lumière un levier économique considérable sous-exploité pour de nombreuses structures vétérinaires. Pour les établissements de soins vétérinaires, comprendre et optimiser cette activité est essentiel pour assurer leur viabilité et leur croissance à long terme.
II. Structurer l'examen et la prescription bucco-dentaire
La médecine préventive est un levier majeur pour la fidélisation de la clientèle et génère 60 à 70% du chiffre d'affaires des cliniques [3]. La dentisterie, en tant que composante essentielle de la médecine préventive, offre un potentiel de croissance significatif. Les bilans de santé annuels, qui incluent un examen bucco-dentaire, créent des opportunités de recommander des soins bucco-dentaires.
Pour que la dentisterie devienne un véritable moteur économique, une approche systématique de l'examen bucco-dentaire et de la prescription est fondamentale ; deux exemples pour illustrer le propos :
1. Exemple 1 : la maladie parodontale
Le protocole commence par une gradation semi-quantitative des bouches, allant de "Normal" à "Parodontite généralisée". Il est crucial d'expliquer clairement ce grade au client, idéalement en utilisant des photos pour illustrer l'état de la bouche de l'animal. L'enregistrement systématique de ce grade dans le fichier client, suivi d'une prescription adaptée, sont des étapes clés pour un suivi efficace et une meilleure acceptation par le propriétaire (Figure 1).
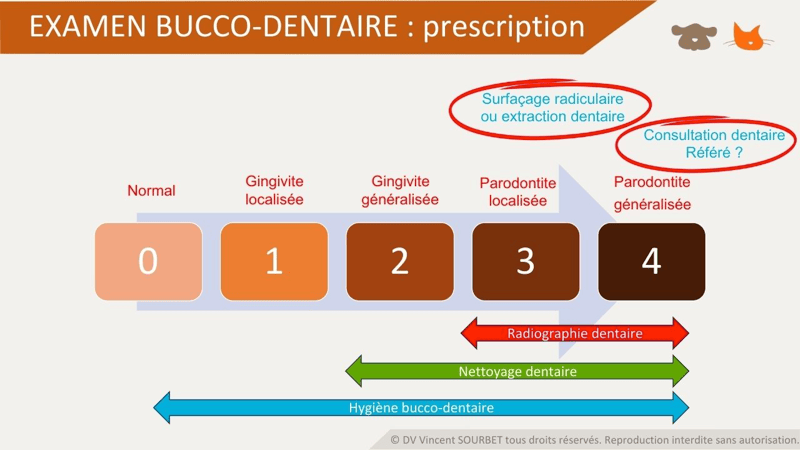
Figure 1
2. Exemple 2 : les résorptions dentaires félines
La résorption des dents est fréquente chez les chats domestiques et se présente cliniquement comme un défaut des tissus durs à la jonction cément-émail de la dent. Des taux de prévalence allant de 28,5 à 67,0% ont été signalés chez le chat et l'incidence augmente avec l'augmentation de l'âge. Tous les types de dents de la dentition féline peuvent être affectés par la résorption dentaire, mais les lésions semblent être plus fréquentes sur les premières prémolaires mandibulaires [4]. Lors de l'examen buccal, on sera attentif à compter les dents et à regarder l'aspect de la gencive libre. L'absence d'une dent ou la présence d'un tissu de granulation très vascularisée au niveau du collet de la dent doit conduire à la prescription d'un bilan lésionnel instrumental et radiographique.
La mise en place de programmes de prévention annuels, par exemple sous forme d'abonnements mensuels incluant consultations de routine, vaccinations et détartrages, permet de fidéliser les clients et d'assurer des revenus récurrents. Ces visites préventives permettent également d'aborder des sujets connexes, tels que l'alimentation et les traitements antiparasitaires, augmentant ainsi le panier moyen par client. Il est important de noter que développer la clientèle existante coûte 4 à 7 fois moins cher que d'acquérir de nouveaux clients, ce qui renforce l'importance de la fidélisation par la médecine préventive [3].
III. Améliorer la communication pour renforcer l'observance
L'efficacité des recommandations vétérinaires, en particulier pour les procédures dentaires, repose fortement sur la qualité de la communication avec le client. Les propriétaires sont 7 fois plus susceptibles de suivre une recommandation (dentaire ou chirurgicale) si celle-ci est présentée de manière claire et univoque que de manière ambigüe [5]. Cela signifie proposer explicitement une procédure nécessaire, comme un nettoyage dentaire dans le mois pour prévenir la parodontite, plutôt que de suggérer un détartrage dans un avenir proche en regardant les dents.
Une approche axée sur la relation client et une haute satisfaction client sont directement corrélées à une meilleure observance. Il s'agit d'une collaboration mutuelle où les préoccupations du client sont explorées et appréciées. Il est impératif d'expliquer la logique et le bénéfice des recommandations pour que les clients perçoivent la valeur des services. Les vétérinaires se concentrent souvent sur l'expertise et le temps investi, tandis que les propriétaires valorisent davantage les bénéfices directs pour la santé et le bien-être de leur animal. Des consultations plus longues, où un ton empathique et serein est maintenu, sont également associées à une meilleure observance.
Pour obtenir l'acceptation du client, il faut s'assurer qu'il comprenne parfaitement la recommandation et les avantages qu'elle procurera à son animal s'il agit immédiatement. Une offre claire et concrète, accompagnée d'une estimation des coûts, est indispensable. Enfin, encourager le client à poser des questions et obtenir son consentement éclairé avant de procéder est une étape cruciale pour maximiser l'observance (Figure 2).
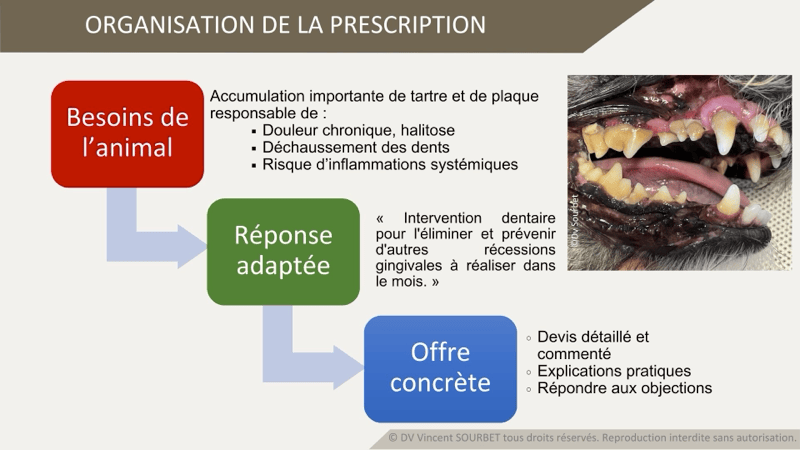
Figure 2
IV. Investir dans l'équipement dentaire
Acquérir des équipements de qualité tels que les unités dentaires ou les systèmes de radiographie est un investissement stratégique. Ces coûts fixes doivent être amortis, mais ils sont essentiels pour offrir des services spécialisés et de haute qualité en dentisterie, ce qui à son tour augmente la capacité de la clinique à générer des revenus plus élevés. En France, moins de 15% des cliniques sont équipées en radiographie dentaire. En contraste, 60% à 70% des cliniques aux États-Unis et au Royaume-Uni possèdent cet équipement. L'imagerie dentaire numérique permet d'attirer de nouveaux clients et découvrir d'autres problèmes douloureux chez l'animal lors des prophylaxies dentaires. Elle permet d'expliquer les recommandations et valorise les soins dentaires réalisés.
V. Former l'équipe pour valoriser les soins dentaires
L'optimisation de la rentabilité des actes vétérinaires repose sur un renforcement des compétences de l'ensemble du personnel soignant. Pour que les soins dentaires soient correctement prescrits, acceptés et valorisés, il est indispensable que tous les membres de l'équipe soient en mesure de comprendre et d'expliquer clairement au client les pathologies orales les plus fréquentes.
Cela inclut notamment la capacité à vulgariser la maladie parodontale, à décrire les signes d'alerte visibles (halitose, tartre, gingivite) ou les conséquences invisibles (douleur chronique, perte dentaire, infection systémique), mais aussi à reconnaître et expliquer les résorptions dentaires félines, fréquentes mais souvent méconnues du propriétaire, pour rester sur nos deux exemples d'illustrations.
Une formation de base sur l'anatomie bucco-dentaire, les maladies fréquentes, et les protocoles de soins, permet aux auxiliaires vétérinaires d'assurer une communication pédagogique homogène, cohérente avec le discours vétérinaire. Cette cohérence améliore non seulement la compréhension du client, mais renforce également sa confiance dans la recommandation.
Cette dynamique favorise l'engagement collectif, améliore l'image de la structure, et soutient l'acceptation des soins. À terme, l'impact économique est double : augmentation du taux d'acceptation des devis dentaires et amélioration de la fidélisation client par un meilleur accompagnement.
VI. Conclusion
Pour développer le potentiel économique de la dentisterie vétérinaire et faire évoluer simplement le CA de son établissement de soins, plusieurs leviers sont à activer :
- adopter une approche rigoureuse et systématique des examens et prescriptions dentaires,
- améliorer la communication pour stimuler l'adhésion,
- investir dans un équipement adapté, rapidement rentabilisé,
- former l'ensemble de l'équipe pour renforcer la cohérence et la pédagogie.
La dentisterie n'est pas seulement un enjeu de santé animale : elle est aussi un puissant vecteur de croissance économique pour les structures vétérinaires.
Bibliographie
- WIGGS RB, LOBPRISE HB. Periodontology. Veterinary Dentistry, Principals and Practice. Philadelphia: Lippincott – Raven, 1997, pp. 186–231.
- GIRARD N et coll. Feline tooth resorption in a colony of 109 cats. J Vet Dent 2008 ; 25 : 166–174.
- JEANTON L. Réflexion économique sur l'équilibre idéal de l'équipe vétérinaire française, comparaison aux modèles anglo-saxons. Médecine vétérinaire et santé animale. 2025. dumas-04967987
- GORREL C. Tooth resorption in cats : pathophysiology and treatment options. J Feline Med Surg 2015 ; 17 : 37-43
- NOUREEN Kanji et al. Effect of veterinarian-client-patient interactions on client adherence to dentistry and surgery recommendations in companion-animal practice. JAVMA 2012 ; 240 ; 4 : 427–436.
Liens d'intérêt : Contrat de consultant/conférencier avec Finapolline (Actéon Group)
📃 La mesure de l’atrium gauche en échocardiographie
Ollioules France
I. Introduction
L'évaluation de l'atrium gauche (AG) par échocardiographie est une étape clé du diagnostic et du suivi des maladies cardiaques chez le chien et le chat. La taille de l'AG est un indicateur pronostique majeur, notamment dans les cardiopathies comme la maladie valvulaire dégénérative chez le chien ou la cardiomyopathie hypertrophique chez le chat. Plusieurs méthodes de mesure existent, chacune avec ses spécificités, avantages et limites.
L'augmentation de la taille de l'AG reflète une élévation chronique de la pression de remplissage du ventricule gauche, souvent liée à une surcharge volumique (régurgitation mitrale, cardiomyopathie hypertrophique, etc). Elle est associée à un risque accru d'œdème pulmonaire, de thromboembolie et de mort subite. L'échocardiographie permet une évaluation non invasive, répétable et relativement accessible de cette structure cardiaque.
II. Mesures en mode bidimensionnel (2D)
1. Coupe petit axe transaortique, "méthode américaine"
Principe :
Mesure du diamètre de l'AG et de l'aorte (Ao) sur une coupe petit axe transaortique par abord droit, au début de la diastole (juste après l'onde T).
Procédure :
- Le diamètre aortique se mesure le long de la commissure entre la valve non coronaire et la valve coronaire droite.
- Le diamètre atrial se mesure le long de la commissure entre la valve non coronaire et la valve coronaire gauche.
- Le rapport AG/Ao est calculé.
Valeurs usuelles :
- Chien : AG/Ao = 1,31 (50e percentile), min 0,86, max 1,57
- Chat : AG/Ao = 1,18 ± 0,11
Avantages : Méthode validée chez le chien toutes races confondues et chez le chat.
Limites : La qualité de la coupe et le positionnement précis sont essentiels pour éviter les erreurs de mesure.
2. Coupe petit axe transaortique, "méthode suédoise"
Principe :
Mesure du diamètre de l'AG et de l'aorte (Ao) sur une coupe petit axe transaortique par abord droit, au début de la diastole (juste après l'onde T).
Procédure :
- Le diamètre aortique se mesure le long de la commissure entre la valve non coronaire et la valve coronaire gauche.
- Le diamètre atrial se mesure le long de la commissure entre la valve non coronaire et la valve coronaire gauche.
- Le rapport AG/Ao est calculé.
Valeurs usuelles :
- Chien : AG/Ao = 1,3 ± 0,09, max 1,27
Limites :
La qualité de la coupe et le positionnement précis sont essentiels pour éviter les erreurs de mesure, et en particulier ne pas inclure le départ des veines pulmonaires. Validée chez le chien Cavalier King Charles.
3. Coupe petit axe transaortique, méthode française
Principe :
Mesure du diamètre de l'AG et de l'aorte (Ao) sur une coupe petit axe transaortique par abord droit, en fin de diastole (début de l'onde Q).
Procédure :
- Le diamètre aortique se mesure le long de la commissure entre la valve non coronaire et la valve coronaire gauche.
- Le diamètre atrial se mesure le long de la commissure entre la valve non coronaire et la valve coronaire gauche.
- Le rapport AG/Ao est calculé.
Valeurs usuelles :
- Chien : AG/Ao = 0,9 ± 0,11, max 1,2
- Chat : AG/Ao = 0,9 ± 0,2, max 1,2
Avantages :
Méthode validée chez le chien et chez le chat. Elle est largement utilisée et recommandée pour sa reproductibilité
Limites :
La qualité de la coupe et le positionnement précis sont essentiels pour éviter les erreurs de mesure.
4. Coupe grand axe cinq cavités
Principe :
Mesure du diamètre maximal de l'AG, parallèle au plan de l'anneau mitral, juste avant l'ouverture de la valve mitrale (début de la diastole).
Procédure :
- Le diamètre de l'AG est mesuré dans l'axe longitudinal, sur la vue grand axe quatre ou cinq cavités.
- Le diamètre aortique est mesuré perpendiculairement au grand axe de l'aorte.
- Calcul du rapport AG/Ao.
Valeurs usuelles :
- Chien : AG/Ao = 1,66 (50e percentile), min 1,11, max 1,99
- Chat : AG/Ao = 1,41 ± 0,14
Avantages :
Permet une mesure directe de la plus grande dimension de l'AG, utile pour détecter des dilatations asymétriques.
Limites : Les valeurs obtenues sont généralement plus élevées que celles des autres méthodes, ce qui nécessite de bien connaître les intervalles de référence propres à cette technique.
5. Coupe grand axe quatre cavités. Mesure de AG (LAD) chez le chat
Principe :
Mesure du diamètre maximal de l'AG, parallèle au plan de l'anneau mitral, juste avant l'ouverture de la valve mitrale (fin de systole).
Procédure :
- Le diamètre de l'AG est mesuré dans l'axe longitudinal, sur la vue grand axe quatre cavités
Valeurs usuelles :
LAD (AG) < 16 mm
Avantages :
Permet une mesure directe de la plus grande dimension de l'AG. Discriminant pour le diagnostic d'insuffisance cardiaque congestive chez le chat.
6. Mesure du diamètre de l'AG (AG ou « LAD ») et indexation
Principe :
Mesure du diamètre court de l'AG (LAD) sur la vue 4 cavités par abord droit, juste avant l'ouverture de la valve mitrale
Procédure :
- Le LAD est mesuré parallèlement à l'anneau mitral.
- Il peut être indexé au poids corporel pour obtenir le LADN (AGN) : LADN (AGN) = LAD (mm) / poids (kg)^{0,324}.
Valeurs usuelles :
- Chien : LADN (AGN) < 16.
Avantages :
Simple, reproductible, bonne concordance inter-observateur chez les cardiologues
Limites :
Moins étudiée chez le chat, nécessite l'indexation pour interpréter la mesure selon la taille de l'animal.
7. Volume indexé de l'AG en systole (VAGsN)
Principe :
Calcul du volume de l'AG à partir du contour tracé en 2D sur la vue 4 cavités par abord gauche, juste avant l'ouverture de la valve mitrale (fin de systole)
Procédure :
- Tracer la surface interne de l'AG sur l'image 2D)
- Le logiciel de l'échographe calcule le volume selon une formule intégrée.
Valeurs usuelles :
- Chien : VAGsN < 0,9 ml/kg, normal au 100e percentile
Avantages :
Prise en compte de la forme réelle de l'AG, utile en cas de dilatation asymétrique. Plus sensible pour la détection de dilatations atriales gauches que les méthodes petit axe abord droit chez le Cavalier King Charles
Limites :
Dépend de la qualité de l'image et des capacités du logiciel.
III. Mesures en mode temps-mouvement (TM)
1. Coupe petit axe transaortique TM
Principe :
Mesure du diamètre de l'AG en télésystole (fin de l'onde T) et de l'aorte en télédiastole (début de l'onde Q), sur un défilement TM obtenu à partir d'une coupe petit axe transaortique.
Valeurs usuelles :
- Chien : AG/Ao = 1,01 ± 0,13 (Cavalier King Charles), toutes races : 0,99 ± 0,1
- Chat : AG/Ao = 1,29 ± 0,13
Avantages :
Méthode historique, rapide.
Limites :
Moins précise que le 2D, risque de ne pas être parfaitement perpendiculaire à la cavité, ce qui peut fausser la mesure
2. Coupe grand axe cinq cavités TM
Principe :
Même principe que la coupe petit axe, mais sur la vue grand axe cinq cavités.
Valeurs usuelles :
- Chien : AG/Ao = 0,99 ± 0,1
Avantages :
Permet une évaluation complémentaire.
Limites :
Moins utilisée en pratique courante, même inconvénient de l'axe de tir que la coupe petit axe.
3. Fraction de raccourcissement de l'AG (%FRAGTM)
Principe :
Calculée à partir des dimensions maximale et minimale de l'AG en mode TM, elle évalue la contractilité de l'AG
Valeurs usuelles chez le chat : 25,1 ± 5,0 % (17,5–35,1)
Intérêt :
Plus exploratoire, utile en recherche.
IV. Limites et précautions d'interprétation
- Variabilité inter- et intra-opérateur : la reproductibilité dépend de l'expérience de l'opérateur et de la qualité des images.
- Influence de la race, du poids et de l'âge : Les valeurs de référence peuvent varier selon les races, en particulier chez le chien (ex. Cavalier King Charles).
- Positionnement précis : une mauvaise orientation de la sonde ou un axe de tir non perpendiculaire peut fausser la mesure, surtout en mode TM.
- Moment du cycle cardiaque : il est essentiel de toujours mesurer au même moment du cycle pour comparer les résultats (début diastole ou fin de diastole…).
V. Conclusion
La mesure échocardiographique de l'atrium gauche chez le chien et le chat repose sur plusieurs méthodes complémentaires. Les techniques bidimensionnelles, en particulier la coupe petit axe transaortique (américaine, suédoise ou française), sont à privilégier pour leur précision et leur validation dans les deux espèces, en compléments d'autres mesures (volume atrial) dans certains cas ou races particuliers). Les mesures doivent toujours être réalisées de manière standardisée, au même moment du cycle cardiaque, et interprétées selon les valeurs de référence adaptées à l'espèce, à la race et à la méthode utilisée. La connaissance des avantages et limites de chaque technique est indispensable pour une évaluation fiable de la taille de l'AG, essentielle au diagnostic, au pronostic et au suivi des cardiopathies chez le chien et le chat.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 La neurolocalisation au service de l'interprétation des images
Saint-Laurent-Du-Var, France
I. Objectifs d’une consultation neurologique
1. Déterminer si le problème est d'origine neurologique
La consultation d'un patient suspecté de présenter un trouble neurologique ne doit pas se limiter à l'examen neurologique. Un examen clinique général ainsi qu'une anamnèse complète sont également essentiels pour orienter correctement les investigations.
Par exemple, certaines maladies non neurologiques peuvent imiter des troubles neurologiques :
- Faux paralysés : embolie aortique, rupture du ligament croisé antérieur bilatérale, anémie, hypovolémie, polyarthrite, panostéite.
- Faux épileptiques : syncopes d'origine cardiaque, dyskinésies paroxystiques.
2. Déterminer une neurolocalisation
Pour simplifier la démarche diagnostique, on peut diviser le système nerveux en plusieurs grandes régions :
- Prosencéphale
- Moelle épinière
- Système vestibulaire et cervelet
- Neuromusculaire
- Nerfs crâniens
Bien que certaines maladies puissent affecter plusieurs de ces zones simultanément, des gestes cliniques de base permettent généralement d'établir une neurolocalisation relativement ciblée, ce qui est une étape essentielle avant de choisir les examens complémentaires appropriés.
a) Atteinte prosencéphalique
- Crises épileptiques
- Changement de comportement, déambulation, pousser au mur
- Troubles de la vision (avec les fonctions rétiniennes conservées)
- Réponse à la menace - est diminuée ou absente du côté opposé à la lésion
- Sensibilité nasale - une hypoalgésie faciale du côté opposé à la lésion
- Déficits proprioceptives (souvent sans ataxie majeure) - (réactions posturales/sautillements) - des déficits sont visibles du côté opposé à la lésion
b) Atteinte médullaire
- Paralysie ou parésie : para/tétra/mono/hémi
- Déficits de proprioception (réactions posturales/sautillements) - des déficits sont visibles du côté de la lésion
- Absence d'atteinte des nerfs crâniens (sauf : syndrome de Claude-Bernard-Horner)
- Pas de signes d'atteinte prosencéphalique
Attention – animal non-ambulatoire – il faut le lever !! (faiblesse musculaire vs. véritable parésie)
c) Vestibulaire/cervelet
- Pertes d'équilibre
- Tête penchée
- Nystagmus
- Tremblements (cervelet)
- Hypermétrie (cervelet)
d) Atteinte neuromusculaire
- Intolérance à l'effort
- Parésie/plégie - par diminution/disparition des mouvements volontaires
- Proprioception conservée tant que l'animal a la force pour déplacer la patte
- Douleurs musculaires
- Megaœsophage
e) Nerfs crâniens (exemples)
- Paralysie faciale
- Tête penchée (syndrome vestibulaire périphérique)
- Amyotrophie des muscles masticateurs (n. trijumeau)
3. Créer une liste des hypothèses diagnostiques
Après avoir établi notre neurolocalisation suspectée, il est important de créer une liste d'hypothèses diagnostiques. Pour procéder de façon organisée, nous pouvons utiliser le schéma VITAMIN D (tableau 1).
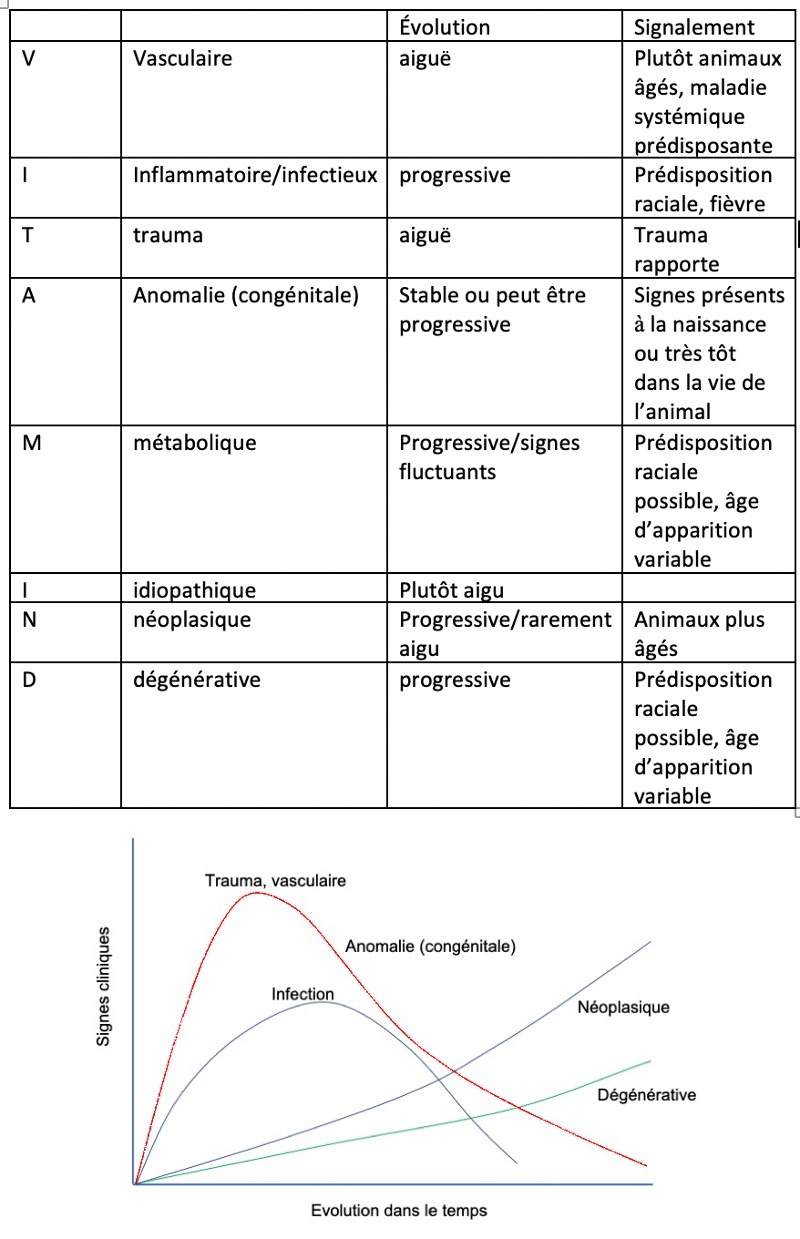
Tableau 1
4. Après avoir établi nos hypothèses diagnostiques, il est temps de choisir les examens complémentaires
Les examens d'imagerie, comme tout examen complémentaire, présentent des sensibilités et des spécificités d'exclusion ou de conformation qui dépendent de l'affection explorée.
Il apparait donc essentiel de correctement réaliser sa neurolocalisation et ses hypothèses afin de choisir le meilleur examen d'imagerie.
La radiographie est un examen facilement disponible en clinique. En neurologie, elle peut être utilisée en examen préliminaire pour l'évaluation d'un traumatisme (fracture/luxation vertébrale), chez un animal âgé pour évaluer la possibilité d'une cause tumorale ou métastatique (par exemple métastase vertébrale d'adénocarcinome pulmonaire ou mammaire), certaines lésions osseuses infectieuses (notamment spondylodiscite) ou encore pour certaines malformations chez les animaux majoritairement jeunes dans des races prédisposées (par exemple luxation atlanto-axiale). Néanmoins, il est recommandé de réaliser ces clichés sous tranquilisation légère pour obtenir des images interprétables (en faisant attention de ne pas aggraver des lésions traumatiques lors de manipulations d'un animal traumatisé). Il faut garder en tête que la radiographie peut avoir une faible sensibilité pour des lésions traumatiques subtiles et ne permet pas souvent d'évaluer la compression médullaire sans myélographie.
Le scanner et l'IRM sont deux appareils qui se ressemblent à première vue, mais qui ont des bases physiques fondamentalement différentes, ce qui leur confère des applications également différentes et parfois complémentaires :
- Le scanner, basé sur les rayons X, a les mêmes indications que la radiographie (cf. supra), mais son caractère tri-dimensionnel et son excellente résolution spatiale lui confèrent une sensibilité excellente pour ces indications. Le scanner est également une excellente modalité pour confirmer des extrusions discales pour des races chondrodystrophiques (saignements canalaires, hernies discales minéralisées). Le degré de compression médullaire peut être évident ou nécessiter une injection sous arachnoïdienne de contraste (myéloscanner).
- L'IRM est basé sur le magnétisme des atomes de proton au sein des tissus. Son excellente résolution de contraste, permettant une différenciation des tissus pathologiques par rapport aux tissus sains (ischémiques, inflammatoires, tumeurs cérébrales ou médullaires, lésions méningées …), est très nettement supérieure au scanner. L'IRM est donc l'examen de choix pour l'imagerie du système nerveux. Des séquences IRM pondérées T2-STIR permettent d'évaluer la compression médullaire de façon non invasive, en particulier pour évaluer des hernies discales de races non chondrodystrophiques ou en cas de hernies discales multiples, y compris chez les chiens chondrodystrophiques âgés.
5. Confrontation des images aux hypothèses diagnostiques
Néanmoins, les examens d'imagerie présentent certaines limites :
- La détection de lésions et l'établissement du diagnostic différentiel radiologique dépendent de l'expérience du radiologue
- Certaines maladies ne donnent aucune lésion aux examens d'imagerie
- Des variants conformationnels, surinterprétation ou découvertes de lésions fortuites, peuvent mener à un diagnostic erroné
Il est donc primordial de confronter les hypothèses radiologiques aux hypothèses diagnostiques pré-établies, afin de déterminer la pertinence des images dans le contexte clinique du patient.
Autour de cas cliniques, nous discuterons d'images concordantes ou discordantes avec l'état clinique, illustrant ainsi les liens indispensables entre la neurologie et l'imagerie.
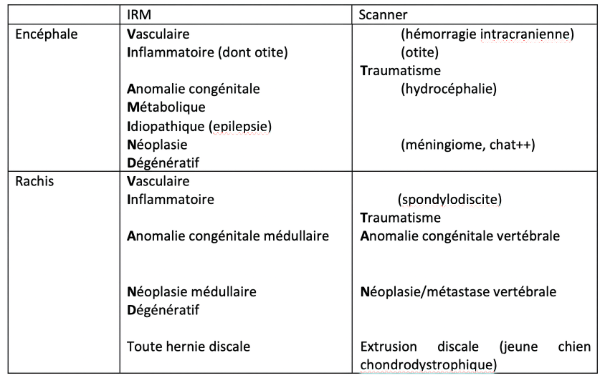 Tableau 2
Tableau 2
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 La perte de vision brutale chez le Chien : à qui référer ? à l'ophtalmologue ou au neurologue ?
Rennes France
En cas d’atteinte bilatérale de la vision et des réflexes photomoteurs (RPM) et d’absence de lésions du fond d’œil, le diagnostic différentiel doit également inclure les principales causes d’amaurose pré-chiasmatique (névrite optique bilatérale) et chiasmatique (compression chiasmatique par une masse), le syndrome de la rétine silencieuse (SARD).
L’électrorétinogramme est l’examen complémentaire de choix pour diagnostiquer ou infirmer un SARD. En effet, aucune réponse éléctrophysiologique ne pourra être mesurée en cas de SARD alors que ces réponses seront normales en cas de névrite optique ou de lésions chiasmatiques.
Les réflexes photomoteurs chromatiques peuvent être utilisés comme examen d’orientation. La réponse lors de SARD est une contraction variable en lumière rouge et une contraction normale en lumière bleue (Leis et al. Can Vet J 2017) et celle lors de névrite optique est une absence de contraction lors des deux stimulations (Grozdanic et al. Vet Ophthalmol 2013). Ainsi la présence d’une contraction en lumière bleue est un élément en défaveur d’une atteinte du nerf optique.
Aparté sur le reflexe photomoteur chromatique
Rôle de la mélanopsine
Certaines cellules ganglionnaires (2 % de toutes les cellules ganglionnaires), en relation avec le noyau suprachiasmatique, sont responsable de la régulation des cycles biologiques et du réflexe photomoteur. Ces cellules possèdent au niveau de leur dendrites un photopigment particulier (la mélanopsine) les rendant intrinsèquement photosensibles (la stimulation d’un photorécepteur n’est pas nécessaire pour son fonctionnement).
Une lumière bleue de longueur d’onde 480 nm, de forte intensité, active directement la mélanopsine. La mélanopsine peut se régénérer rapidement par absorption d’un photon dans la longueur d’onde du rouge et ce de façon continue. Ce phénomène renseigne le cerveau en permanence sur l’état de luminosité ambiante.
Réalisation du réflexe photomoteur par pupillométrie chromatique
La pupillométrie chromatique consiste à utiliser de façon sélective une lumière bleue de longueur d’onde 480 nm (stimulant ces cellules ganglionnaires intrinsèquement photosensibles) ou une lumière rouge de longueur d’onde 630 nm (stimulant exclusivement les photorécepteurs mais pas la mélanopsine), de forte intensité. Cet examen permet ainsi de stimuler de façon dissociée ces deux populations cellulaires.
Interprétation
- Chez l’animal sain, on observe une contraction normale pour chaque stimulation.
- En cas de syndrome de la rétine silencieuse (dégénérescence aigue de photorécepteurs sans atteinte des cellules ganglionnaires), la réponse typique est une absence de contraction en lumière rouge et une contraction normale en lumière bleue. Toutefois, une variabilité importante de la réponse en lumière rouge a été décrite (Leis et al. Can Vet J 2017).
- En cas d’atteinte du nerf optique, la réponse typique est une absence de contraction lors des deux stimulations.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 La pexie lors de SDTE
Gentilly, France
I. Introduction
Le syndrome de dilatation-torsion de l'estomac (SDTE) est une urgence vitale chez le chien, caractérisée par une distension gastrique aiguë suivie d'une rotation autour de l'axe gastro-oesophagien. Malgré une prise en charge rapide, la récidive après simple décompression reste élevée (jusqu'à 60%). La gastropexie constitue l'unique moyen chirurgical validé pour prévenir une nouvelle rotation.
II. Indications
La gastropexie est indiquée dans deux situations principales :
- Curative : systématiquement associée à la chirurgie de dérotation lors d'un SDTE, pour prévenir toute récidive.
- Préventive : chez des chiens à risque (grandes races, thorax profond, antécédents familiaux, anxiété, alimentation rapide). Elle peut être réalisée seule ou au cours d'une stérilisation, par voie conventionnelle ou mini-invasive.
III. Techniques chirurgicales
De nombreuses variantes de gastropexie existent :
- gastropexie incisionnelle : la plus utilisée. Une incision sur la paroi pylorique est apposée à une incision sur le muscle transverse droit ;
- gastropexie par mini incision laparotomie : technique moins invasive que par laparotomie ;
- gastropexie laparoscopique totale : technique intracorporelle utilisant des sutures barbées, plus rapide et moins traumatisante.
IV. Résultats cliniques
La gastropexie réduit drastiquement le taux de récidive du SDTE, inférieur à 5% toutes techniques confondues. Les études comparatives montrent une mortalité significativement réduite lorsque la procédure est réalisée au moment de l'intervention chirurgicale initiale. Les techniques mini-invasives sont associées à une récupération plus rapide et à une satisfaction élevée des propriétaires.
V. Complications
Les complications postopératoires sont rares mais incluent :
- déhiscence de la suture (2 à 4%) ;
- infections pariétales ;
- douleur transitoire ou troubles digestifs mineurs ;
- plus rarement, malposition du site de fixation ou échec d'adhésion.
Les techniques mini-invasives présentent globalement moins de complications majeures, mais peuvent être techniquement plus exigeantes.
VI. Conclusion
La gastropexie est une procédure sûre, efficace et essentielle dans la gestion du SDTE. Elle devrait être proposée systématiquement après toute torsion de l'estomac et discutée en prévention chez les chiens à risque. Le choix de la technique dépend de l'expérience du chirurgien, du contexte clinique et de l'équipement disponible.
Bibliographie
- GAZZOLA KM, NELSON LL. Prophylactic gastropexy: a review of indications, techniques, and outcomes. Can Vet J. 2014 ; 55 : 1037-43.
- RAWLINGS CA et coll. A comparison of laparoscopic-assisted and incisional gastropexy in dogs. Vet Surg. 2002 ; 31 : 562–70.
- BERNABE BP et coll. Laparoscopic gastropexy using barbed sutures: evaluation of 39 dogs. Vet Surg. 2021 ; 50 : 964–71.
- BROURMAN JD et coll. Evaluation of risk factors for recurrence of gastric dilatation-volvulus in dogs: 136 cases (1988–1993). J Am Vet Med Assoc. 1996 ; 208 : 229-33.
- BECK JJ et coll. Gastric dilatation-volvulus in dogs treated by gastropexy: 166 cases. J Am Anim Hosp Assoc. 2006 ; 42 : 121–25.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 La PIF vue par l'interniste...
Gentilly, France
I. Introduction
La péritonite infectieuse féline (PIF) est l’une des maladies les plus redoutées en médecine féline, en raison de son pronostic historiquement fatal et de la difficulté diagnostique qu’elle représente. Provoquée par une mutation du coronavirus entérique félin (FCoV), elle touche préférentiellement les jeunes chats vivant en collectivité, dans un contexte de stress ou d’immunodépression. Les avancées récentes dans le domaine du diagnostic moléculaire et surtout dans celui des antiviraux ont profondément modifié le paysage de la prise en charge de cette maladie.
II. Épidémiologie et pathogénie
Le coronavirus félin (FCoV) est un virus à ARN simple brin de grande taille, enveloppé, appartenant à l’ordre des Nidovirales et à la famille des Coronaviridae. Il est extrêmement répandu dans les collectivités félines, où plus de 90 % des individus sont séropositifs. Dans la majorité des cas, l’infection est bénigne et se limite à une multiplication virale dans les entérocytes, responsable d’une atteinte digestive transitoire. Toutefois, chez 1 à 5 % des chats infectés, des mutations internes du génome viral, notamment au niveau des gènes 3c et 7b (PEDERSEN et coll., 2012), entraînent un tropisme pour les monocytes et macrophages, conditionnant l’apparition de la PIF. La pathogenèse repose alors sur une réponse immunitaire inadaptée, où une immunité humorale forte mais une immunité cellulaire déficiente favorisent la dissémination du virus et l’inflammation granulomateuse.
Plusieurs facteurs de risque ont été identifiés. L’âge est déterminant, la majorité des cas survenant chez des chats de moins de deux ans. Le sexe mâle constitue un facteur de risque supplémentaire. Les conditions de vie en collectivité, l’adoption récente, les interventions chirurgicales ou les vaccinations peuvent induire un stress favorisant la maladie. Enfin, les co-infections (FIV, parvovirus) et l’immunosuppression contribuent également à l’émergence de la PIF.
III. Présentations cliniques
La PIF ne se résume pas à une dichotomie stricte entre formes humides et formes sèches : elle constitue un spectre de manifestations, où des formes mixtes sont fréquentes.
La forme humide est la plus facilement identifiable. Elle est caractérisée par des épanchements cavitaires secondaires à une vascularite pyogranulomateuse. Dans une cohorte de 25 chats étudiés par MÜLLER et coll, 2023, 88 % présentaient un épanchement abdominal ou thoracique. L’analyse du liquide révèle typiquement un exsudat riche en protéines (souvent > 35 g/L), visqueux, de densité élevée (≥1,040), mais pauvre en cellules, dominé par quelques neutrophiles dégénérés. Cliniquement, ces chats présentent une distension abdominale, une dyspnée restrictive ou une tachypnée. Une hyperbilirubinémie est rapportée chez 22 à 63 % des chats atteints, particulièrement dans les formes humides.
La forme sèche est plus insidieuse et souvent plus difficile à identifier. Elle se caractérise par des granulomes inflammatoires disséminés dans divers organes, entraînant une sémiologie polymorphe. L’atteinte hépatique peut se manifester par une hépatomégalie et une hypoéchogénicité (observée chez 48 % des chats dans l’étude de MÜLLER et al., 2023). L’atteinte rénale peut se traduire par une augmentation de taille, des contours irréguliers et la présence d’anneaux hypoéchogènes corticaux (32 % des chats). L’atteinte intestinale est rapportée dans 68 % des cas, sous forme d’épaississements asymétriques de la paroi. L’atteinte splénique est présente dans 36 % des cas, sous forme de splénomégalie ou de nodules hypoéchogènes. Les formes oculaires comprennent une uvéite antérieure, des dépôts kératiques, un hyphéma ou un décollement de rétine (TASKER et al., 2024). Les formes neurologiques se traduisent par une ataxie, des crises convulsives, des changements de comportement ou une paralysie partielle.
Enfin, il existe des formes atypiques rapportées dans la littérature : des lésions cutanées nodulaires, des kystes médiastinaux, des entérites granulomateuses, des pneumonies granulomateuses ou encore des orchites. Ces présentations inhabituelles contribuent à la complexité diagnostique de la maladie.
IV. Moyens diagnostiques
Le diagnostic de la PIF repose sur un faisceau d’arguments cliniques, biologiques, d’imagerie et moléculaires, aucun test unique ne permettant une certitude absolue en routine.
Sur le plan hématologique, une anémie est retrouvée dans une majorité de cas et constitue un facteur de pronostic défavorable. La leucocytose neutrophilique et la lymphopénie sont également fréquentes, tandis qu’une hyperglobulinémie est presque constante. Le rapport albumine/globulines (A/G) constitue un élément déterminant : dans une étude rétrospective de 100 chats, un rapport inférieur à 0,8 présentait une valeur prédictive négative (VPN) de 100 %, et un rapport inférieur à 0,6 une VPN de 99 %. En revanche, la valeur prédictive positive (VPP) restait faible (12,5 % pour un A/G <0,8). Ce paramètre permet donc surtout d’écarter la PIF lorsque le ratio A/G est normal.
L’analyse de l’épanchement, lorsqu’il est présent, est cruciale. Un épanchement suspect de PIF est un exsudat stérile, jaune et visqueux. Il présente généralement une teneur en protéines élevée (> 35 g/L), une cellularité faible à moyenne (< 50 000 cellules/µl), principalement composée de neutrophiles non dégénérés et de macrophages. Le test de Rivalta, simple (exposition d’acide acétique au liquide d’épanchement) et peu coûteux, présente une sensibilité élevée et une spécificité intermédiaire. Un test positif est compatible avec une PIF, mais des faux positifs peuvent être observés dans des épanchements septiques ou tumoraux notamment (TASKER et al., 2024). La réalisation d’une RT-PCR sur épanchement (RT pour reverse transcriptase-PCR) est recommandée, du fait de sa forte sensibilité. Le matériel biologique utilisé pour la recherche viral est critique. En effet, la recherche d’ARN viral dans le sang n’est pas spécifique, puisque jusqu’à 80–90 % des chats infectés par le FCoV entérique sans PIF peuvent être positifs. La RT-PCR sur selles n'a aucun intérêt dans le diagnostic de la PIF clinique. De nombreux chats en bonne santé excrètent le virus de manière intermittente. Une RT-PCR fécale positive ne confirme pas la maladie, et une négative ne l'exclut pas. Ce test est uniquement pertinent en élevage pour identifier les chats excréteurs chroniques afin de gérer les collectivités.
En l’absence d’épanchement, la recherche du génome viral reste un outil intéressant : elle peut être réalisée sur des lésions d’intérêt (cytoponction d’organes présentant des lésions notamment). Ainsi, l’imagerie médical est souvent en étape préalable. Dans l’étude de MÜLLER et al. (2023), 92 % des chats présentaient au moins deux anomalies échographiques. Les épanchements, les adénopathies abdominales (80 %), les lésions hépatiques (58 %), intestinales (68 %) et rénales (32 %) constituent des éléments contributifs. Dans les formes nerveuses, l’IRM est l’examen de choix, supérieur au scanner. Elle permet de mettre en évidence des hydrocéphalies obstructives, des syringomyélies et des prises de contraste méningées. Le liquide céphalorachidien, lorsqu’il est prélevé, peut paradoxalement être normal (BOETTCHER et al., 2007), ce qui limite son intérêt isolé.
Concernant la détection des mutations génétiques avec certains tests disponibles sur le marché, il est à noter que ces mutations ne sont pas toujours présentes et des mutations de virulence différentes existent, ce qui limite leur utilité pour un diagnostic de routine.
Le test sérologique permet la détection d’anticorps contre le coronavirus félin. Néanmoins, une sérologie positive ne signifie pas « maladie PIF », car elle indique une simple exposition au virus. La valeur diagnostique de la sérologie est donc faible. En revanche, une sérologie négative a une bonne valeur prédictive négative (si le chat n'est pas immunodéprimé).
Enfin, le diagnostic de certitude est obtenu par la réalisation d’un examen immunohistochimique sur prélèvement, permettant d’isoler le coronavirus au sein des macrophages dans les lésions caractéristiques : la nécessité de biopsies et les contraintes pour l’animal explique que ce test n’est pas systématique réalisé en première intention.
V. La stratégie diagnostique
Le diagnostic de la PIF repose donc sur une approche multicritère. Le cas clinique, les données épidémiologiques et les indices biologiques doivent être corrélés.
Pour la forme humide, la présence d'un épanchement à haute teneur en protéines avec une faible cellularité, associée à une RT-PCR positive sur l'épanchement, permet un diagnostic de forte présomption. Pour la forme sèche, le diagnostic est plus difficile et repose sur la corrélation des signes cliniques (fièvre, lésions oculaires/neurologiques) avec des analyses sanguines compatibles (hyperglobulinémie, rapport A/G faible), ainsi qu’un isolement du virus (RT-PCR sur épanchement ou prélèvement cytologique, immunohistochimie sur biopsie).
VI. Gestion en collectivité
La prévention de la PIF dans les structures collectives demeure un défi majeur. La réduction du stress, la limitation des contacts et l’hygiène rigoureuse des litières contribuent à réduire la circulation virale. Certaines argiles absorbantes, comme l’argile foulon, ont montré une capacité à réduire la réplication virale in vitro, sans pour autant offrir une efficacité complète in vivo.
VII. Conclusion
La PIF illustre parfaitement la complexité des interactions entre un agent viral ubiquitaire et la réponse immunitaire de l’hôte. Si son diagnostic reste difficile et repose sur une combinaison de données cliniques, biologiques, d’imagerie et moléculaires, les progrès récents ont considérablement modifié le pronostic.
Bibliographie
- BOETTCHER IC et coll. Use of anti-coronavirus antibody testing of cerebrospinal fluid for diagnosis of feline peritonitis involving the central nervous system in cats. J Am Vet Med Assoc 2007; 230(2): 199- 205
- MULLER TR et coll. Abdominal ultrasonographic findings of cats with feline infectious peritonitis: an update. J Feline Med Surg 2023; 25(12)
- PEDERSEN NC et coll. Feline infectious peritonitis: role of the feline coronavirus 3c gene in intestinal tropism and pathogenicity based upon isolates from resident and adopted shelter cats. Virus Res 2012; 165(1): 17-28
- TASKER S. Diagnosis of feline infectious peritonitis: update on evidence supporting available tests. J Feline Med Surg 2018; 20(3): 228-243
- TASKER S et coll. Feline infectious peritonitis: European Advisory Board on cat Diseases Guidelines. Viruses 2023; 15(9):1847
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 La PIF vue par l'ophtalmo
Rennes France
Une étude réalisée en Caroline du Nord, USA décrit les causes d’uvéite à dominante antérieure non traumatique et non associée à la présence d’une cataracte dans l’espèce féline (Jinks et al. Veterinary Ophthalmology 2016). Les uvéites idiopathiques ou à médiation immune sont prédominantes (70%) suivies des uvéites d’origine infectieuses (25% dont 16% de cas de péritonite Infectieuse féline - PIF-, 7% de cas d'immunodéficience féline - FIV- et 2% de cas de leucose féline - FeLV-,) puis des néoplasies (5% dont 2,5% de lymphomes). Ces résultats sont en majorité confirmés par une étude multicentrique réalisée au Royaume Uni (Wegg et al. Veterinary Ophthalmology 2021). Les uvéites idiopathiques ou à médiation immune sont prédominantes (4%), suivies des uvéites d’origine infectieuses (28% dont 16% de cas de PIF, 2% de cas de FIV et 2% de cas de FeLV), puis des néoplasies (25% dont 11% de lymphomes).
La Péritonite Infectieuse Féline (PIF) résulte de la mutation du coronavirus félin entérique (FCoV). Une majorité des chats atteints ont un âge inférieur à 2 ans, avec prédisposition pour les individus mâles (Riemer et al. JFMS 2015). La maladie systémique se manifeste par une anorexie, une perte de poids, une hyperthermie réfractaire à l’utilisation des antibiotiques. Des épanchements abdominaux et/ou thoraciques sont observés dans 78% de cas (175/224) (Riemer et al. JFMS 2015).
Des signes oculaires sont fréquemment décrits mais restent plus fréquent dans la forme sans épanchements (7/12 cas, 58%) que dans la forme avec épanchement (5/30 cas, 16%) (Tsai et al. JFMS 2011).
Les signes cliniques oculaires classiquement associés à la PIF sont une uvéite antérieure bilatérale souvent associée à des lésions de choriorétinite. La présence de précipités kératiques en « graisse de mouton » (dépôts endothéliaux de grande taille souvent de couleur jaune) et de manchons inflammatoires (infiltrat cellulaire blanchâtre) en périphérie des vaisseaux rétiniens sont deux signes considérés comme évocateur de la PIF. La progression d’une uvéite antérieure vers une panuvéite est souvent observée.
Actuellement, l’examen immunohistochimique des liquides d’épanchements ou de prélèvements tissulaires (détection d’un antigène du FCoV dans les macrophages infectés) est considéré comme la technique de diagnostic de référence. Cependant, sa sensibilité sur l’humeur aqueuse modérée (63%) et sa spécificité inférieure à 100% (80% à cause de résultats faussement positifs) rendent son utilité clinique limitée (Sangl et al. J Vet Diagn Invest 2020). La réalisation d’une RT-PCR sur humeur aqueuse a une spécificité de 100% et une sensibilité de 36%. La réalisation d’une RT-PCR spécifique du gène S (associé à la virulence de l’infection par la PIF) sur humeur aqueuse ne semble pas intéressante (Sensibilité de 16%). Ces résultats sont cependant à analyser avec prudence puisqu’uniquement 5/31 des chats atteints de PIF et 1/27 des chats témoins présentait des signes d’uvéite antérieure (Sangl et al. J Vet Diagn Invest 2020).
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 La podoplastie par fusion pour la gestion des anomalies de conformation podales et défaut d'aplomb chez le chien : étude rétrospective sur 16 cas
Introduction
La pododermatite est un syndrome fréquent et multifactoriel chez le chien [1,2]. Les chiens présentant des défauts d'aplomb, une conformation anormale des pieds et/ou un surpoids sont prédisposés au développement de zones cutanées hyperplasiques en face palmaire/plantaire des pieds [1,3]. Les traumatismes répétés induisent une inflammation chronique et la formation de kystes folliculaires interdigitaux, souvent responsables de boiterie et de prurit. Lorsque le traitement médical est inefficace, une approche chirurgicale par fusion podoplastie peut être envisagée pour restaurer une extrémité fonctionnelle et indolore [3,4,5]. Cette étude vise à évaluer les résultats cliniques et les complications associées à cette technique.
Matériel et méthodes
Les dossiers médicaux des chiens ayant subi une podoplastie par fusion pour le traitement de dermatites interdigitées pyogranulomateuses récurrentes ont été analysés rétrospectivement sur 2 structures vétérinaires.
Onze chiens ont été inclus. Les données recueillies comprenaient : signalement, antécédents médicaux, résultats des examens cliniques et dermatologiques, analyses sanguines, traitements médicaux antérieurs, techniques chirurgicales, soins péri- et postopératoires, complications et suivis à court (< 21 jours) et à long terme (> 21 jours).
Les podoplasties par fusion ont été classées en deux catégories : les podoplasties par fusion totale (PFT), impliquant la fusion du deuxième au cinquième doigt avec leurs coussinets digités associés, et les podoplasties par fusion partielle (PFP), limitée à la fusion de deux doigts adjacents.
En postopératoire, les extrémités étaient protégées par un bandage et des suivis ont été effectués jusqu'à cicatrisation complète. Les complications ont été classées en majeures (nécessitant une réintervention) ou mineures. Le suivi à long terme a été assuré par contact direct avec les propriétaires.
Résultats
Les 11 chiens inclus (dont 16 extrémités) dans cette étude présentaient tous des lésions interdigitées pyogranulomateuses chroniques affectant une ou plusieurs extrémités, fréquemment associées à une boiterie (8/11), un léchage excessif (7/11) et des postures anormales (6/11). Les membres antérieurs étaient les plus touchés (n=14/16). Le Bouledogue Anglais était la race la plus représentée (4/12).
Les comorbidités comprenaient un surpoids (2/9) et des affections dermatologiques associées chez 7 chiens (otite externe (5/7), dermatite atopique (3/7), pyodermite (2/7), dermatite allergique (1/7)). La durée moyenne des signes cliniques avant l'intervention était de 2,5 ans (0,33-5,25 ans ; n=10/11), avec un échec du traitement médical observé dans tous les cas (durée moyenne : 2,1 ans).
Dix-sept podoplasties par fusion ont été réalisées (8 PFP, 9 PFT), dont 5 bilatérales. Aucune complication peropératoire n'a été rapportée. La durée moyenne d'hospitalisation était de 33,6 heures.
Des complications postopératoires ont été observées chez 10 chiens (16 complications au total), majoritairement mineures (n=14). La déhiscence de plaie (n=7) et la récidive de lésions interdigités (n=5) étaient les plus fréquentes. Deux complications postopératoires, une déhiscence majeure du site opératoire et une récidive de lésion interdigitée, ont nécessité une réintervention chirurgicale. Toutes les plaies ont cicatrisé avec un délai médian de 28 jours (20-45 jours). Après un suivi médian de 16 mois (0,7-27 mois), une résolution complète et durable des lésions a été obtenue chez 8 chiens, tandis que 3 présentaient uniquement une résolution ou amélioration temporaire des signes cliniques.
Discussion-Conclusion
Cette étude constitue la plus grande série de cas rapportée sur la podoplastie par fusion pour le traitement des dermatites interdigitées réfractaires. Cette chirurgie de sauvetage s'est révélée efficace, bien qu'invasive et nécessitant des soins postopératoires rigoureux, notamment des bandages prolongés. Malgré un taux de complications élevé (9/11 chiens), celles-ci étaient majoritairement mineures et ont été gérées avec succès. La déhiscence de plaie était la complication la plus fréquente, en accord avec la littérature [4,5], suivie par la récidive des lésions interdigitées.
La résolution complète des lésions chez 8 chiens sur 11 souligne l'intérêt de cette technique dans la prise en charge des formes sévères et récidivantes.
Bibliographie
- DUCLOS DD, HARGIS AM, HANLEY PW. Pathogenesis of canine interdigital palmar and plantar comedones and follicular cysts, and their response to laser surgery. Vet Dermatol. 2008;19(3):134-41.
- BASDANI E, et al. Fusion Podoplasty in a Dog with Inter-digital Fibrosing Furunculosis. Aust Vet Practit. 2010;40:53.
- VAN NIMWEGEN SA, KIRPENSTEIJN J. Specific Disorders of the Skin and Subcutaneous Tissues. In: TOBIAS KM, JOHNSTON A, editors. Veterinary Surgery: Small Animal. 2nd ed. Elsevier; 2017. p. 3551.
- PAPAZOGLOU LG, et al. Fusion Podoplasty for the Management of Chronic Pedal Conditions in Seven Dogs and One Cat. J Am Anim Hosp Assoc. 2011;47:e199-e205.
- SWAIM SF, LEE AH, MACDONALD JM, et al. Fusion for the treatment of chronic fibrosing interdigital pyoderma in the dog. J Am Anim Hosp Assoc. 1991;27:264-74.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 La présence de syndromes paranéoplasiques
Ollioules, France
I. Introduction
Un syndrome paranéoplasique est un ensemble de signes cliniques ou désordres biologiques causé par un cancer de manière indirecte, autrement dit, sans lien avec l’envahissement local de la tumeur ou des métastases. Ils sont généralement causés par des messagers moléculaires (principalement des cytokines ou des hormones) sécrétés par la tumeur elle-même ou par l'organisme, notamment le système immunitaire, en réponse à la maladie néoplasique. Certains syndromes paranéoplasiques sont très généraux et peuvent accompagner presque n'importe quel cancer et d'autres, au contraire, sont très spécifiques à un type tumoral. Ils peuvent alors être d'une très grande aide au diagnostic et sont régulièrement le motif de consultation. En effet, lorsqu'ils sont présents, ils peuvent souvent être détectés bien avant les signes cliniques liés à l'envahissement local de la tumeur.
La plupart des syndromes paranéoplasiques rétrocèdent lorsque la tumeur est traitée ; toutefois, certains peuvent avoir des conséquences graves et doivent alors être traités indépendamment de la tumeur, afin d'accélérer leur gestion et de limiter leurs conséquences négatives. Dans ce cas, ils peuvent compliquer la prise en charge et aggraver le pronostic, en provoquant des signes cliniques pouvant altérer l'état général de l'animal [1].
Les principaux syndromes paranéoplasiques (SPN) chez les chiens et chats sont les suivants :
- Généraux : cachexie/anorexie, fièvre
- Digestifs : ulcérations gastro-duodénales
- Endocriniens : hypercalcémie, hypoglycémie, hyperoestrogénisme, acromégalie
- Hématologiques : syndrome d'hyperviscosité sanguine (hyperprotidémie et/ou polyglobulie), anémie, leucocytose (neutrophilique ou éosinophilique principalement), troubles de la coagulation / thrombopénie
- Cutanés : dermatofibrose nodulaire, dermatite nécrolytique supercificielle (anciennement syndrome hépato-cutané), alopécie paranéoplasique féline, dermatite exfoliative féline associée au thymome
- Neurologiques : myasthénie grave et polyneuropathie périphérique
- Ostéo-articulaires : ostéopathie hypertrophique
Les SPN soulignés sont ceux qui ont le plus fréquemment un impact sur le pronostic et que nous traiterons donc ici. À noter que la dermatite nécrolytique superficielle influence gravement le pronostic, mais est à la fois très rare et très spécifique et ne sera donc pas traitée.
II. Ulcérations gastro-duodénales
Les ulcérations gastro-intestinales paranéoplasiques sont principalement dues au mastocytome, par libération d'histamine. Elles sont mentionnées dans 35 à 83 % des rapports d'autopsie de chiens atteints de mastocytomes ; en revanche cela reste une cause minoritaire d'ulcérations puisque le mastocytome représente seulement 0 à 3 % des causes d'ulcérations gastro-duodénales chez le chien. Les gastrinomes peuvent également être incriminés, par libération de gastrine, mais sont très rares.
Le tableau clinique est dominé par les vomissements (88 %), parfois hémorragiques (35 %), et le méléna (31 %). La fièvre et la distension abdominale doivent faire envisager une perforation digestive. Une anémie est également fréquente, de degré variable et généralement régénérative [2].
Le diagnostic formel est difficile dans le contexte paranéoplasique. L'échographie et le scanner sont assez peu sensibles en l'absence de perforation (échographie : 29,5 - 65 % contre 83 % lors de perforation / scanner : 67 % contre 93 % lors de perforation). Les techniques diagnostiques de choix sont visuelles, c'est-à-dire par exploration endoscopique ou chirurgicale. Ce n'est toutefois pas approprié dans un but purement diagnostique et ces techniques sont plutôt réservées aux animaux avec une suspicion d'ulcère nécessitant une prise en charge chirurgicale. Les autres bénéficieront d'un essai thérapeutique [2].
Même lorsque la tumeur peut être prise en charge, un soutien digestif est recommandé. Les inhibiteurs de pompe à proton (IPP ; oméprazole ou pantoprazole) sont les plus efficaces pour augmenter le pH et cicatriser les lésions. Les anti-H2 (ranitidine, famotidine, cimétidine) peuvent être utilisés, mais sont globalement moins performants et leur association aux IPP peut diminuer l'efficacité de ces derniers. En cas d’ulcère avéré, il est approprié d'ajouter un protecteur mucosal (sucralfate).
III. Hypercalcémie
L’hypercalcémie maligne est l’un des principaux syndromes paranéoplasiques du chien et du chat [1]. Elle résulte principalement de la sécrétion de PTHrp, mimant l’action de la PTH et induisant une résorption osseuse accrue, une réabsorption rénale du calcium et une excrétion phosphorée, le tout à l'origine d'une hypercalcémie. Les tumeurs les plus fréquemment impliquées sont les lymphomes T et les adénocarcinomes de la glande apocrine du sac anal (AGASA) chez le chien et les lymphomes et les myélomes multiples chez le chat.
Le tableau clinique se compose d'abattement et d'anorexie, ainsi que de vomissements chez le chat et d'une polyuro-polydypsie voire de trémulations chez le chien. Sur le plan organique, l’hypercalcémie est délétère pour les reins lorsqu'elle est sévère et/ou chronique, via des dépôts phosphocalciques irréversibles.
La prise en charge repose avant tout sur le traitement de la tumeur, seul moyen de résolution durable. Cependant, si celui-ci n’est pas envisageable, en cas de signes cliniques, d’azotémie ou d’hypercalcémie marquée, une prise en charge spécifique est nécessaire. Les approches visent principalement à accroître l’excrétion urinaire du calcium (fluidothérapie, diurétiques, bisphosphonates). Aucune valeur seuil stricte n’est définie et le traitement est ajusté au cas par cas ; toutefois, une calcémie totale >160 mg/L ou ionisée >1,80 mmol/L doit alerter sur le risque de néphrotoxicité.
L'impact de l'hypercalcémie sur le pronostic est triple. D'une part, elle peut entrainer des troubles rénaux irréversibles et donc diminuer la durée de vie du patient, sans lien avec le cancer initial. D'autre part, chez le chien, il s'agit d'un facteur pronostique négatif en cas de lymphome T ou de myélome multiple (mais pas dans les AGASA ou les thymomes dans les études les plus récentes). Enfin, l'hypercalcémie paranéoplasique peut accélérer le diagnostic car les signes cliniques associés peuvent précéder ceux de la tumeur elle-même.
IV. Hypoglycémie
La principale cause d'hypoglycémie paranéoplasique chez le chien est l'insulinome–tumeur des cellules bêta du pancréas surproduisant de l'insuline. Très rarement, d'autres tumeurs peuvent causer une hypoglycémie chronique, généralement via la production d'IGF-2 [1]. Les principaux signes cliniques sont neuromusculaires (convulsions, faiblesse généralisée, ataxie, tremblements) ou comportementaux (stress, faim) et sont intermittents, plus marqués à distance des repas et rétrocèdent après le repas. Lorsque l'hypoglycémie n'est pas détectée de manière fortuite, ce sont ces signes cliniques qui constituent généralement le motif de consultation initiale. L'hypoglycémie paranéoplasique étant généralement marquée, elle doit souvent être prise en charge avant le diagnostic et la prise en charge de la tumeur elle-même avec diverses stratégies d'urgence (bolus intraveineux de glucose) ou d'entretien (fractionnement des repas, corticothérapie à faible dose, voire autres molécules hyperglycémiantes telles que le diazoxide) [1,3].
V. Myasthénie grave
La myasthénie grave (MG) paranéoplasique est relativement rare et principalement rapportée en cas de thymome chez le chien (10-20 % des cas) ou le chat (5 % des cas), bien que d'autres tumeurs puissent y être associées [1,4,5]. Comme toutes les formes acquises de MG, il s’agit d’une affection immunomédiée caractérisée par la production d’anticorps dirigés contre les récepteurs nicotiniques de l’acétylcholine, localisés sur la membrane postsynaptique des jonctions neuromusculaires. La forme généralisée de la MG se manifeste le plus souvent par une faiblesse musculaire des membres, fréquemment aggravée par l’effort. Une atteinte des muscles de l’œsophage (mégaœsophage), du pharynx, du larynx ou de la face peut également être présente. Dans la forme focale, ces groupes musculaires sont les plus souvent touchés. Les deux formes peuvent être impliquées lors de SPN.
Le diagnostic repose principalement sur la mise en évidence d’anticorps circulants dirigés contre les récepteurs de l’acétylcholine, bien qu’un petit nombre de patients puissent être séronégatifs. Chez le chien, un test à l’édrophonium ou à la pyridostigmine peut également contribuer à confirmer la suspicion de MG généralisée.
Le traitement de choix est le traitement de la tumeur, mais la MG ne rétrocède pas systématiquement après traitement. L'influence de la MG sur le pronostic est variable ; chez le chat, il semblerait que sa présence n'influe pas le pronostic, mais cela peut être lié à un manque de données ; chez le chien, l'impact pronostique est variable en fonction des études mais dans la cohorte la plus récente (51 chiens), les individus avec MG avaient une durée de vie médiane de 2 mois contre 15 pour ceux sans MG. De plus, le mégaœsophage expose à un risque élevé de pneumonie par fausse déglutition, qui augmente les risques péri-anesthésiques. En fonction des cas, des traitements systémiques avec de la pyridostigmine et/ou des immunomodulateurs peuvent être nécessaires afin de stabiliser la MG avant la prise en charge de la tumeur [1,4].
VI. Ostéopathie hypertrophique
L’ostéopathie hypertrophique (OH) ou syndrome Alamartine - Ball - Cadiot est un trouble généralisé du périoste, caractérisé par une production osseuse excessive affectant les os longs des extrémités [1]. Les lésions apparaissent d’abord au niveau des doigts, puis progressent de façon proximale. Elles sont généralement bilatérales, symétriques et concernent souvent les quatre membres.
Chez le chien, l’OH est principalement associée à des tumeurs pulmonaires (primaires ou métastatiques), mais a également été rapporté en lien avec des maladies non tumorales ou des tumeurs extra-thoraciques. La plupart des cas d'OH paranéoplasique canine présentent des métastases au diagnostic et l'ostéosarcome est fréquemment en cause. Chez le chat, l’OH est très rare (uniquement quelques cas isolés).
Cliniquement, les patients présentent le plus souvent une tuméfaction et/ou un œdème des extrémités distales, accompagné de difficultés locomotrices. Les membres sont fréquemment chauds et douloureux à la palpation. Moins de la moitié des animaux présentent des signes respiratoires au moment du diagnostic. Des troubles oculaires sont fréquemment rapportés concomitamment : écoulement oculaire séreux à mucopurulent bilatéral et inflammation épisclérale. Radiographiquement, on observe une néoformation périostée symétrique, lisse, nodulaire ou en "spicules" avec tuméfaction des tissus mous adjacents.
Le traitement repose idéalement sur la prise en charge de la tumeur sous-jacente. Cependant, la plupart des chiens sont diagnostiqués à un stade métastatique avancé et les options thérapeutiques sont souvent palliatives. L'utilisation de biphosphonates pourrait permettre de soulager la douleur, sans preuve chez le chien mais avec efficacité chez l'Homme.
Bibliographie
- BAILEY D. Paraneoplastic syndromes. In: VAIL DM, THAMM DH, LIPTAK JM, editors. In: VAIL D, THAMM D, LIPTAK J, éditeurs. Withrow and MacEwen's small animal clinical oncology. 6e éd. St Louis, Missouri: Elsevier; 2020. p. 98-112.
- PAVLOVA E et coll. Medical conditions associated with gastroduodenal ulceration or erosion in 168 dogs: 2008-2018. J Vet Intern Med. 2021;35(6):2697-704.
- BUISHAND FO. Current Trends in Diagnosis, Treatment and Prognosis of Canine Insulinoma. Vet Sci. 2022;9(10):540.
- YALE AD et coll. Thymic epithelial tumours in 51 dogs: Histopathologic and clinicopathologic findings. Vet Comp Oncol. 2022;20(1):50-8.
- MARKS TA et coll. Prognostic factors and outcome in cats with thymic epithelial tumours: 64 cases (1999-2021). J Small Anim Pract. 2024;65(1):47-55.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 La ruche, lien avec l'environnement, problématique de santé de l'abeille (généralités)
Vauvenargues, France
Neuvy, France
I. La ruche, lien entre l'environnement et la santé de l'abeille.
L’abeille mellifère (Apis mellifera) est un animal encore peu connu des vétérinaires. En France, en 2023, 63 415 apiculteurs ont déclaré détenir 1 792 420 colonies d’abeilles. 28,3 % des colonies d’abeilles sont détenues par 57 753 apiculteurs de loisir (possédant moins de 50 colonies). Ces détenteurs non professionnels sont souvent à la recherche de conseils pour les soins à porter à leurs colonies et la prévention des principales maladies. Le vétérinaire a, ici, un rôle à jouer.
Apis mellifera est un insecte eusocial. Elle forme des colonies de 15 000 à 50 000 individus qui constituent des superorganismes : les colonies d’abeilles. Alors qu’une abeille a une espérance de vie de 2 mois environ en saison, la colonie d’abeille a une espérance de vie théorique infinie. C’est cet individu que le vétérinaire va pouvoir soigner. L’abeille mellifère est souvent qualifiée de sentinelle de l’environnement, car sa physiologie, son comportement et son mode de vie collectif la rendent très sensible aux perturbations écologiques. Elle est aussi l’insecte pollinisateur le plus étudié par la communauté scientifique. L’érosion actuelle de la biodiversité se répercute sur sa santé.
Depuis les années 80, on constate une augmentation de la mortalité des colonies d’abeilles, en lien avec les 5 facteurs de dégradation de la biodiversité identifiés par l’IPBES (Intergovernmental Science-Policy Platform on Biodiversity and Ecosystem Services).
1. Facteurs 1 et 2. Changement dans l’usage des terres et des mers et surexploitation des ressources naturelles : impacts sur la nutrition et la physiologie de l’abeille
Plusieurs politiques publiques sont à l’origine de la disparition d’une grande partie de la réserve alimentaire de l’abeille depuis la fin de la Seconde Guerre mondiale : le plan Marshall, le remembrement, la Révolution Verte, la PAC, et aujourd’hui la diminution drastique du nombre d’exploitants, en particulier en élevage extensif.
Ces politiques ont eu de nombreuses conséquences : augmentation de la taille des parcelles agricoles, monoculture, disparition des haies, usage d’intrants. Autant de facteurs qui ont réduit la quantité et la diversité des ressources alimentaires disponibles. Ceci a des conséquences sur le développement des colonies et la qualité de leur système immunitaire qui se traduit par une augmentation de la sensibilité aux maladies et du risque de mortalité en hiver.
2. Facteur 3. Changements climatiques : perturbation du cycle biologique
Le changement climatique entraîne la perturbation des cycles biologiques animaux et végétaux. L’abeille domestique ayant co-évolué depuis des millénaires avec les végétaux, le changement climatique peut conduire à des situations d’abeilles sans fleurs et de fleurs sans abeilles, préjudiciables à la pérennité des abeilles et des végétaux. Aujourd’hui, des situations de famines printanières sont régulièrement enregistrées, du fait d’une saisonnalité bouleversée. Dans les cas extrêmes, les colonies meurent. L’augmentation de la température estivale entraîne un stress thermique qui se manifeste par un arrêt de la ponte, une diminution de l’activité et une augmentation de la consommation d’eau. Enfin, la modification de la température et de l’hygrométrie affecte la production de nectar des végétaux, impact supplémentaire sur la disponibilité alimentaire.
3. Facteur 4. Pollution : risques d’intoxication
Les abeilles sont des espèces collectrices. Elles collectent l’eau et leur nourriture sur les végétaux, dans une zone de 1 à 3 km de rayon autour de leur ruche. Bien que domestiques, l’apiculteur n’a que peu de contrôle sur les sources d’eau et les végétaux qu’elles visitent. De ce fait, elles sont exposées aux pollutions environnementales : produits phytopharmaceutiques utilisés en agriculture, métaux lourds, hydrocarbures, résidus industriels et médicamenteux. Les insecticides utilisés en agriculture posent particulièrement problème. À forte dose, ils provoquent la mort des abeilles. À dose sublétale, ils entraînent des perturbations de leur physiologie : diminution des capacités d’apprentissage, affaiblissement du système immunitaire, réduction de la durée de vie des individus, avec pour conséquence affaiblissement des colonies et augmentation de la sensibilité aux maladies. Il est fréquent que les abeilles soient exposées simultanément à plusieurs molécules exogènes dont les effets cocktail restent peu documentés.
4. Facteur 5. Introduction d’espèces exotiques envahissantes : nouveaux agents pathogènes
Deux introductions majeures ont affecté la santé en filière apicole dans les 50 dernières années : l’acarien Varroa destructor et le frelon Vespa velutina. Ces 2 agents pathogènes sont originaires d’Asie et ont été introduits avec l’intensification des échanges commerciaux.
Le parasite Varroa destructor a été introduit en France en 1982 et s’est rapidement étendu sur l’ensemble du territoire. Depuis, il est considéré comme l’un des principaux facteurs de mortalité des colonies d’Apis mellifera dans le monde entier. L’arrivée du varroa est à l’origine de l’augmentation de la prévalence du virus des ailes déformées DWV-A et B, car le varroa agit comme vecteur et amplificateur de ce virus. L’association de ces 2 pathogènes entraîne un affaiblissement majeur qui se traduit souvent par la mort des colonies.
Le frelon Vespa velutina a été introduit en 2004. Il est aujourd’hui présent sur la quasi-totalité du territoire hormis les zones d’altitude. Vespa velutina affecte la santé des colonies en prélevant de grandes quantités d’abeilles butineuses devant les ruches, pour nourrir sa colonie. Son comportement de prédation (vol stationnaire devant la ruche) entraîne un stress qui se traduit, dans les cas sévères, par l’effondrement des colonies d’abeilles.

Photo 1 : Vespa velutina (frelon asiatique, frelon à pattes jaunes

Photo 2 : abeille ouvrière (apis mellifera) atteinte du virus des ailes déformées-DWV
D’autres parasites exotiques menacent aujourd’hui la France métropolitaine : l’insecte Aethina tumida, originaire d’Afrique et déjà présent en Italie et à la Réunion ; et l’acarien Tropilaelaps spp.
II. Les rôles du vétérinaire en santé de l'abeille
1. OMAA : l’Observatoire des Mortalités et Affaiblissement de l’Abeille.
OMAA est un dispositif d’épidémiosurveillance événementielle, créé en 2017, à la demande de la Direction générale de l’alimentation DGAL, une des directions du Ministère de l’agriculture et de la souveraineté alimentaire. Il est déployé par les FRGTV Fédération régionale des groupements techniques vétérinaires et financé par la DGAL et FAM France Agri Mer.
En 2025, 8 régions disposent d’un OMAA : Auvergne-Rhône-Alpes, Bourgogne-Franche-Comté, Bretagne, Centre-Val de Loire, Hauts-de-France, Occitanie, Pays de la Loire, Provence-Alpes-Côte d’Azur. L’objectif d’OMAA est de faire l’inventaire et l’analyse de la dynamique spatio-temporelle des mortalités et des affaiblissements des colonies d’abeilles en France dans le but de surveiller l’état de santé du cheptel apicole français. Ce réseau s’appuie sur un réseau de vétérinaires libéraux formés en pathologie apicole pour réaliser des investigations au rucher et collecter les données.
2. Surveillance des mortalités massives aiguës d’abeilles adultes avec hypothèse d’intoxication par des produits et pratiques phytopharmaceutiques, biocides et médicamenteuses IT DGALSASPP2018-444
À partir des observations et déclarations d’apiculteurs, ce dispositif de surveillance vise à détecter et caractériser les mésusages, les effets non intentionnels et les accidents dans le process de fabrication de produits phytopharmaceutiques, de biocides et de médicaments vétérinaires en recensant et en investiguant les ruchers atteints de mortalités massives aiguës d’abeilles domestiques adultes (MMAA). Ce dispositif régalien est déployé en région par les DDetsPP et le SRAL (Service régional de l’alimentation, en charge d’organiser et de mettre en œuvre au niveau régional les politiques publiques dans le domaine de l’alimentation, de l’agriculture et de la forêt). Le vétérinaire libéral peut être missionné pour réaliser les investigations au rucher et les prélèvements nécessaires à l’enquête.
3. Missions sous mandat apicole, délivré par les DDetsPP : gestion des maladies réglementées
Depuis la parution de la Loi en Santé animale en avril 2021 (règlement (UE) 2016/429), il n’existe théoriquement plus de maladie à lutte obligatoire en apiculture. Néanmoins, en 2025, des plans de lutte obligatoire restent actifs, en charge des DDetsPP, pour 3 dangers sanitaires de l’abeille : l’acarien Tropilaelaps spp., l’insecte Aethina tumida et la bactérie Paenibacillus larvae. Lors de détection de foyers, les vétérinaires libéraux, titulaires d’un mandat sanitaire apicole, peuvent être mandatés pour mener les opérations de lutte sur les ruchers.
La France métropolitaine est aujourd’hui indemne d’Aethina tumida et de Tropilaelaps spp. Ces agents pathogènes constituent une menace pour la filière apicole et le maintien des populations d’abeilles : c’est pourquoi la DGAL a décidé de maintenir un arrêt de lutte avec indemnisation, pour se donner les chances d’une éradication rapide en cas d’introduction. La loque américaine, maladie bactérienne enzootique liée à Paenibacillus larvae, est fréquente sur le territoire. Anciennement maladie à lutte obligatoire, son statut est en cours d’évolution vers un arrêt de la prise en charge de la lutte par l’État.
4. Prescription et délivrance du médicament : la lutte contre le varroa
Les apiculteurs sont obligés d’utiliser des médicaments, chaque année, pour lutter contre le varroa. Sans lutte chimique, il est aujourd’hui impossible de maîtriser ce parasite. L’abeille est considérée comme un animal de rente, puisqu’elle produit du miel, du pollen, de la cire et de la propolis qui seront consommés ou utilisés en industrie.
Les apiculteurs ont donc l’obligation d’utiliser des médicaments disposant d’une Autorisation de Mise sur le Marché pour l’espèce abeille. L’utilisation de ces médicaments nécessite de la rigueur afin d’obtenir l’efficacité nécessaire à la bonne santé des colonies, de prévenir l’apparition de résistance et de garantir des produits de la ruche propres à la consommation. Le vétérinaire formé sera ici l’interlocuteur de choix. Il peut conseiller les apiculteurs dans sa pratique libérale, dans le cadre d’une visite de rucher, ou à titre collectif, en collaborant avec un Groupement Sanitaire Apicole disposant d’un Programme Sanitaire d’Élevage pour la lutte contre ce parasite.
L’apiculture vous tente ?
Un réseau de vétérinaires formés vous attend et répondra à vos questions. Des formations courtes sont proposées par la SNGTV et une formation diplômante est proposée par les ENVF : le Diplôme Inter Écoles "Diagnostic et gestion sanitaire d’une exploitation apicole, pathologie apicole".
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 La télé-expertise en imagerie : un échange nécessaire avec le généraliste
Montpellier, France
Les radiologues vétérinaires ont, depuis de nombreuses années, interprété des examens d’imagerie médicale en dehors des locaux des structures vétérinaires les employant. La digitalisation des modalités d’imagerie médicale au cours des dernières décennies a amplifié le phénomène et conduit à un développement important et rapide de la téléradiologie vétérinaire. Cette activité permet d’apporter un avis de spécialiste à une équipe ne disposant pas d’un service de radiologie ou de compléter le travail d’un service de radiologie en place et ne pouvant subvenir à l’ensemble de l’activité en imagerie médicale de la structure.
Les établissements d’enseignement vétérinaire dispensent aux vétérinaires une formation de base en imagerie médicale leur donnant une habilitation à l’acquisition des images, principalement en radiographie et en échographie, et dans une certaine mesure à leur interprétation. Cette formation initiale donne en revanche une capacité moindre à la description de ces images, mais aussi à l’acquisition, à l’interprétation et à la description des techniques d’imagerie avancées que sont l’IRM, la tomodensitométrie ou la fluoroscopie.
Les services proposés par la téléradiologie vont ainsi compléter ces compétences en proposant :
- Une aide à l’identification et à l’interprétation des lésions par un regard externe, sans biais clinique, et sur l’ensemble des modalités d’imagerie disponibles.
- Une validation de l’interprétation initiale d’images réalisées au sein d’une structure, avec rédaction d’un rapport dans les termes appropriés. Ainsi, la téléradiologie peut limiter les erreurs de prise en charge des patients, telle que la mise en place d’un traitement immunomodulateur chez un patient chez qui un processus infectieux n’a pas été identifié convenablement.
- L’obtention en fin d’examen de ce rapport qui constitue une pièce juridique pour le dossier médical du patient.
- La prise en charge de la responsabilité juridique de l’interprétation de l’examen d’imagerie médicale par la société de téléradiologie.
- La dispense de conseils pour la conduite des examens d’imagerie médicale et des procédures permettant une augmentation de leur qualité et une meilleure radioprotection.
- Une formation continue de l’équipe.
- Le renfort d’une équipe en place 365 jours par an, indépendamment des congés.
Il appartient au vétérinaire généraliste de choisir le service de téléradiologie avec lequel il souhaite collaborer. Quelle que soit la motivation de ce choix, il doit être accompagné d’une vérification de l’expertise en imagerie médicale des lecteurs vétérinaires amenés à interpréter les images. Cette compétence peut être validée par l’obtention des diplômes du collège européen ou américain d’imagerie médicale, ou par le suivi d’une formation au sein d’un service spécialisé pendant au moins trois ans, encadré par d’autres spécialistes, permettant d’attester d’une formation théorique suffisante.
La communication entre le vétérinaire et un service de téléradiologie est généralement assurée par l’utilisation d’une plateforme en ligne. Une fois les modalités d’inscription finalisées, ces services permettent la création d’une demande d’interprétation, l’envoi des images, la rédaction du rapport par le radiologue et finalement la consultation du rapport d’imagerie médicale par le vétérinaire. L'ensemble des liens et nécessaires sont illustrés dans la figure 1.
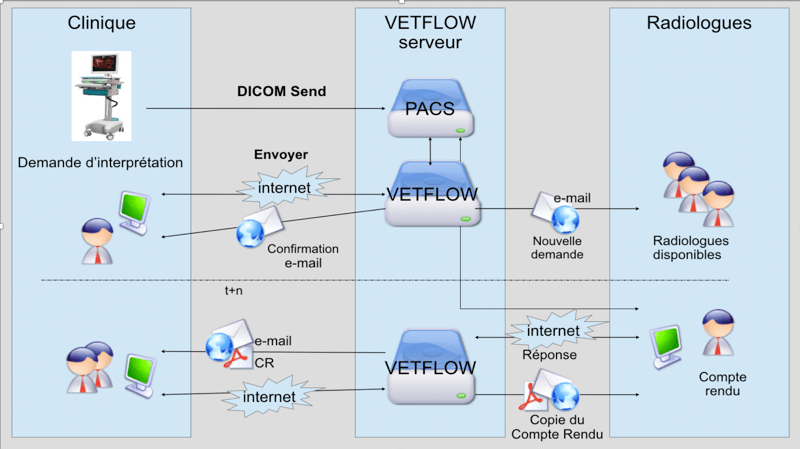
Figure 1
La création d’une demande nécessite du vétérinaire qu’il remplisse un formulaire contenant des éléments d’identification du patient, du propriétaire, des vétérinaires en charge du patient et de l’examen, et enfin qu’il fournisse des informations cliniques. Pour le patient, l’âge, la race, le poids, le genre et le statut sexuel sont des informations essentielles à l’interprétation correcte des images. Concernant les informations cliniques, un résumé clair des éléments anamnestico-cliniques est généralement suffisant, mais il doit contenir assez d’informations sans devenir trop long, ce qui le rendrait illisible. L’ajout, en fin de demande, d’une question précise à laquelle doit répondre l’examen interprété constitue une valeur ajoutée et permet de répondre au mieux aux attentes du vétérinaire référent. Il est également intéressant d’indiquer toute trouvaille pertinente ou question sur les images au sein de la demande d’interprétation.
L’envoi des images implique un transfert des fichiers depuis le dispositif de stockage de la clinique (PACS) vers le serveur du service de téléradiologie, qui se trouve en lien avec la plateforme internet. Il doit s’effectuer en format DICOM, qui est le format standard reconnu au niveau international pour visualiser, stocker, récupérer et partager des images médicales. Le transfert de l’examen requiert une connexion internet d’un débit suffisant de la part de l’ensemble des intervenants.
Une fois ces deux étapes finalisées, le radiologue vétérinaire télécharge et interprète les images, comprenant deux à trois parties : description, interprétation/conclusion et recommandations. À ce dernier sont parfois ajoutées des illustrations qui peuvent être légendées. Le délai pour l’obtention du rapport d’imagerie diffère en fonction des services de téléradiologie. En cas d’urgence, une réponse rapide est possible, et le délai varie entre quelques heures et 24 h pour une interprétation urgente. Le rapport obtenu est transmis au vétérinaire généraliste par mél et est par ailleurs accessible sur la plateforme. Un outil de communication par messagerie ou mél est en général mis à disposition du vétérinaire généraliste en cas de besoin d’informations supplémentaires ou de questions sur l’examen.
En conclusion, après un fort développement au cours de ces dernières années, la téléradiologie vétérinaire s’impose aujourd’hui comme un outil incontournable pour renforcer la qualité de la prise en charge des patients en imagerie médicale. Elle permet d’apporter une expertise spécialisée, d’améliorer la fiabilité diagnostique et de sécuriser le suivi juridique des dossiers, tout en offrant un appui logistique continu aux structures vétérinaires. Toutefois, son efficacité repose sur un ensemble de liens étroits entre vétérinaires généralistes et radiologues vétérinaires et nécessite une communication claire et une exigence de qualification reconnue des radiologues vétérinaires. En alliant flexibilité, accessibilité et haut niveau d’expertise, la téléradiologie constitue ainsi un levier majeur pour l’optimisation des pratiques vétérinaires actuelles et futures, tant généralistes que spécialistes.
Bibliographie
- ZIEMER LS, DE HAAN CE, CARDWELL AL et coll. ACVR and ECVDI consensus statement for teleradiology. Vet Radiol Ultrasound. 2024;65:288–293.
Liens d'intérêt : actuellement associé de la société Vedim
📃 La télé-expertise en nutrition : les rôles du spécialiste et du généraliste
Paris, France
I. Introduction
La télé-expertise vétérinaire est une pratique médicale à distance qui permet à un vétérinaire inscrit à l'Ordre des vétérinaires de solliciter l'avis d'un ou plusieurs confrères spécialistes inscrits eux aussi à l'Ordre via des outils de communication numérique (plateformes sécurisées, visioconférence). Elle s'inscrit dans le cadre plus large de la télémédecine vétérinaire, qui comprend aussi la téléconsultation, la télésurveillance, la télé-expertise et la téléassistance. La formation continue à distance est parfois incluse dans la télémédecine.
II. Quel est le cadre légal en France ?
Pour être possible, le vétérinaire demandeur doit avoir examiné l'animal au préalable (sauf exceptions), le propriétaire de l'animal doit avoir donné son consentement et les données échangées doivent être sécurisées et confidentielles (RGPD). Le vétérinaire demandeur reste responsable de la prise en charge finale.
À ce jour, aucun texte définitif législatif n'est publié dans le Code rural et de la pêche. Cela signifie que, strictement parlant, la télémédecine vétérinaire n'est pas autorisée par un cadre légal pérenne.
Le projet de réforme est en préparation et devrait introduire, entre autres, la primo-téléconsultation pour les vétérinaires sanitaires en activité rurale, la téléconsultation référée avec un spécialiste, la télé-expertise entre vétérinaires, ainsi qu'un référentiel pour les plateformes (arrêté du 9 février 2024).
Actuellement, l'Ordre National des Vétérinaires indique sur son site qu'il ne sanctionnera pas les vétérinaires pratiquant la télémédecine dans le cadre défini par le décret expérimental, en attendant une réglementation définitive. Cependant, en cas de plainte, les vétérinaires s'exposent à des risques juridiques et de responsabilité civile professionnelle.
III. Quels sont les objectifs de la télé-expertise ?
Elle donne un accès rapide à un avis spécialisé pour les cas complexes ou rares afin d'améliorer la prise en charge de l'animal sans contraintes géographiques, tout en réduisant les coûts et en optimisant le temps.
Dans le cas des formations, elle favorise les échanges entre professionnels et la montée en compétences, et ce en limitant les contraintes pour les professionnels.
La télé-expertise peut être facturée, mais les tarifs ne sont pas réglementés.
IV. Comment articuler la télé-expertise en nutrition ?
Le vétérinaire généraliste est en première ligne et assure le suivi médical de l'animal ainsi que l'établissement d'un diagnostic initial. En cas de doute ou de situation clinique complexe, il peut solliciter une téléexpertise auprès d'un spécialiste, que ce soit en médecine (différentes spécialités) ou en nutrition. Il transmet alors les informations cliniques et formule une demande précise.
Le spécialiste en nutrition clinique quant à lui :
- Conseille sur l'alimentation adaptée à l'état de santé de l'animal,
- Formule des rations sur mesure en fonction des besoins physiologiques ou pathologiques de l'animal,
- Forme et guide le vétérinaire généraliste ou spécialiste sur les dernières avancées en nutrition clinique,
- Évalue et ajuste les protocoles nutritionnels en fonction de l'évolution de l'animal.
V. Conclusion
La télé-expertise vétérinaire est en développement, portée par la digitalisation du secteur et les besoins croissants en expertise rapide et accessible. Elle nécessite néanmoins d'avoir un cadre légal précis.
Le vétérinaire demandeur assure le suivi médical et la coordination, tandis que le spécialiste en nutrition apporte son savoir pour adapter l'alimentation au service de la santé de l'animal. Cette synergie optimise la prise en charge, surtout pour les animaux nécessitant une alimentation spécifique et un suivi nutritionnel rigoureux.
Bibliographie
- Ordre National des Vétérinaires https://www.veterinaire.fr/je-suis-veterinaire/mon-exercice-professionnel/telemedecine-veterinaire (consulté le 24 août 2025)
Liens d'intérêt : En tant que consultante indépendante, je réalise des missions pour des fabricants d'aliments industriels, des fournisseurs d'ingrédients et des laboratoires pharmaceutiques. Aucune de ces entreprises n'est intervenue dans le cadre de cette conférence.
📃 La vie en cage et les maladies associées chez le lapin
Le Cannet, France
I. Introduction
Longtemps considéré comme un animal « de cage », le lapin de compagnie continue trop souvent à vivre confiné dans un espace restreint. Pourtant, les données scientifiques récentes convergent : ce mode de détention est délétère pour la santé physique et psychologique du lapin. Comprendre les affections associées à la vie en cage permet au vétérinaire de convaincre les propriétaires les plus réfractaires et de proposer des alternatives concrètes.
II. Besoins éthologiques du lapin
Lagomorphe grégaire et actif, le lapin a besoin de :
- se déplacer librement (sauts, courses, exploration),
- se dresser, s'étirer, se cacher,
- ronger pour user ses dents en croissance continue,
- interagir avec ses congénères.
Les cages conventionnelles (30–35 cm de haut, sols grillagés) empêchent ces comportements élémentaires. La frustration, l'ennui et les stéréotypies en sont les conséquences directes.
III. Pathologies associées à la vie en cage
1. Pododermatites
Les lapins n'ont pas de coussinets plantaires : leurs pieds sont recouverts de poils. Sur sols grillagés ou souillés, les poils s'usent, entraînant ulcérations et infections. L'obésité et l'immobilité aggravent le risque. L'EFSA rapporte une prévalence de 9–14% en cages conventionnelles.
2. Obésité et troubles musculo-squelettiques
La sédentarité entraîne une prise de poids favorisant arthrose, spondyloses et fonte musculaire. Des déformations de la colonne vertébrale sont rapportées chez 40–70% des femelles multipares logées en cage basse.
3. Troubles digestifs
La stase digestive est l'un des motifs les plus fréquents de consultation. Elle est déclenchée par stress, douleur ou alimentation à base de mélange de graines pauvres en fibres. En cage, la faible activité et les régimes riches en granulés aggravent le risque de dysbiose, d'entérites et d'iléus paralytique.
4. Affections urinaires
Le manque d'exercice réduit la fréquence des mictions et favorise la précipitation du calcium, conduisant à sludge vésical et urolithiases. Ces pathologies sont fréquentes chez les lapins obèses et sédentaires.
5. Troubles respiratoires
La promiscuité et l'accumulation d'ammoniac favorisent rhinites, conjonctivites et pneumonies. Les lapins en cage, incapables de se mouvoir pour s'isoler des zones souillées, y sont particulièrement sensibles. De plus les séjours prolongés sur certains types de litières poussiéreuses ou irritantes aggravent ces phénomènes.
6. Dermatopathies
L'humidité, l'ammoniac et l'incapacité au toilettage (souvent chez les obèses) entraînent dermatites, abcès cutanés et myiases.
7. Troubles comportementaux
La restriction d'espace et l'absence d'interactions sociales conduisent à des stéréotypies (mordillement des barreaux, hypergrooming), de l'agressivité ou au contraire une apathie marquée.
IV. Indicateurs de bien-être validés
| Indicateur | Pathologie associée | Facteurs liés à la cage | Conséquences |
| Pododermatite | Ulcères, infections | Sol grillagé, humidité, obésité | Douleur chronique, réforme prématurée |
| Libre mouvement | Arthrose, fonte musculaire | Hauteur cage <35 cm | Stress, stéréotypies |
| Densité de logement | Digestif, respiratoire | >40 kg/m² | Morbidité, mortalité accrue |
| Troubles respiratoires | Rhinites, pneumonies | Ammoniac, poussière, promiscuité | Dyspnée, mortalité |
| Animaux sales/humides | Dermatites, myiases | Litière souillée | Infections cutanées |
| Taux de réforme | Pathologies chroniques | Logement inadapté | Indicateur indirect de mal-être |
V. Solutions et enrichissements proposés
| Type d'enrichissement | Exemples concrets | Effets observés |
| Enclos spacieux | Liberté surveillée, parc intérieur | ↓ obésité, ↓ troubles urinaires, ↑ comportements naturels |
| Substrat adapté | Plancher plastique, tapis, paille | ↓ pododermatites, confort accru |
| Objets manipulables | Bâtons, blocs de luzerne, jouets, tunnels | ↓ stéréotypies, ↑ activité |
| Cachettes / plateformes | Abris, niveaux surélevés | ↓ stress, ↑ interactions sociales |
| Stimulation sensorielle | Miroirs, objets suspendus, odeurs naturelles | ↓ agressivité, ↑ exploration |
| Enrichissement alimentaire | Foin à volonté, distribution ludique, blocs fibreux | Prévention stase digestive et malocclusions |
VI. Conclusion
La vie en cage, encore trop répandue, est source de multiples pathologies : pododermatites, obésité, troubles digestifs, urinaires, respiratoires et comportementaux. Les indicateurs de bien-être validés confirment scientifiquement cette réalité. Le rôle du vétérinaire est double : alerter sur les risques et accompagner les propriétaires vers des solutions concrètes. Enclos spacieux, substrats confortables, objets à ronger, tunnels, plateformes et enrichissement alimentaire sont des mesures simples, accessibles et efficaces. Convaincre un propriétaire de passer de la cage à un environnement enrichi, c'est offrir au lapin une meilleure santé et une vie en accord avec son éthologie.
Bibliographie
- BOUSSARIE D., RUEL Y. (2016). Médecine du lapin de compagnie. Med'com.
- MEREDITH A., LORD B. (2014). BSAVA Manual of Rabbit Medicine. BSAVA.
- HARCOURT-BROWN F. (2002). Textbook of Rabbit Medicine. Elsevier.
- HARCOURT-BROWN F., CHITTY J. (2013). BSAVA Manual of Rabbit Surgery, Dentistry and Imaging. BSAVA.
- CLAUSS M., HATT J.M. (2001). The influence of diet on the occurrence of dental disorders in rabbits. J Exotic Pet Med 10(4):241–250.
- SCHEPERS F., KOENE P., BEERDA B. (2009). Welfare assessment in pet rabbits. Animal Welfare 18(4):477–485.
- PREBBLE J.L., MEREDITH A.L. (2014). Food and water intake and selective feeding in rabbits. J Anim Physiol Anim Nutr 98(5):991–1000.
- TROCINO A., XICCATO G. (2006). Animal welfare in reared rabbits: a review with emphasis on housing systems. World Rabbit Sci 14(2):77–93.
- EFSA Panel on Animal Health and Welfare (AHAW) (2005). The impact of current housing and husbandry systems on the health and welfare of farmed domestic rabbits. EFSA Journal 267:1–31.
- EFSA (2020). Health and welfare of rabbits farmed in different production systems. EFSA Journal 18(3):5944.
- EURCAW-Poultry-SFA (2022). VF List of Welfare Indicators Rabbits.
- Compassion in World Farming (2023). Higher welfare systems for rabbits – practical options.
- EL-SABROUT K., AGGAG S.A., et al. (2024). Environmental Enrichment in Rabbit Husbandry: Comparative Impacts on Performance and Welfare. Animals 14(15):2367.
- Opensanctuary.org. Creating an enriching life for rabbits.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Le bien-être au travail : clef de voûte pour des relations harmonieuses au sein des équipes
Chozeau, France
I. Introduction
Le bien-être au travail n'est plus un luxe ou un supplément optionnel. C'est une condition incontournable de la performance collective, de l'engagement durable et de la qualité des relations interpersonnelles. Loin de se réduire à des initiatives ponctuelles de convivialité ou à des avantages matériels, il constitue une véritable clef de voûte du fonctionnement d'une équipe. Sans lui, le collectif s'effrite ; avec lui, il devient capable de résilience, de solidarité et d'innovation.
II. Le bien-être comme fondation relationnelle
Un collaborateur qui se sent bien dans son environnement de travail est plus disponible, plus ouvert et plus enclin à coopérer. À l'inverse, lorsque le climat est marqué par le stress, le flou organisationnel ou le manque de reconnaissance, les tensions s'accumulent et se traduisent inévitablement par des conflits interpersonnels.
Le bien-être n'est donc pas seulement une affaire individuelle ; il est une dynamique collective qui alimente la qualité du lien entre les membres d'une équipe. C'est en ce sens qu'il devient un véritable socle relationnel.
III. Les piliers du bien-être au travail
La recherche et l'expérience de terrain montrent que plusieurs dimensions se conjuguent pour construire ce climat favorable :
- La sécurité psychologique : savoir que l'on peut s'exprimer, proposer des idées ou évoquer des difficultés sans crainte de jugement ou de sanction.
- La clarté du cadre : des rôles, des responsabilités et des procédures clairement définis réduisent l'incertitude, source fréquente de tension.
- La reconnaissance : reconnaître les efforts, les réussites, mais aussi l'engagement quotidien, nourrit la motivation et la confiance.
- L'équilibre charge / ressources : veiller à ce que la charge de travail soit soutenable et que chacun dispose des moyens nécessaires pour accomplir ses missions.
- La qualité des relations humaines : instaurer une culture d'écoute, de coopération et de respect mutuel.
Ces piliers ne sont pas indépendants : ils se renforcent mutuellement et, ensemble, construisent le climat dans lequel les relations interpersonnelles peuvent s'épanouir.
IV. Bien-être et prévention des conflits
Une part non négligeable des difficultés relationnelles en équipe prend racine dans des conditions favorisant le mal-être : surcharge de travail, stress chronique, manque de reconnaissance, absence d'objectifs ou climat relationnel dégradé. Dans ce contexte, la tolérance individuelle diminue et la propension aux malentendus augmente.
Travailler sur le bien-être, c'est donc agir en amont sur les risques de conflits. En renforçant la confiance, en donnant des repères clairs et en valorisant les contributions, on réduit considérablement les risques d'escalade conflictuelle. Le bien-être devient alors un outil de prévention relationnelle.
V. Le rôle des managers et de l'organisation
Promouvoir le bien-être au travail ne se limite pas à organiser des événements conviviaux. C'est un véritable projet managérial et organisationnel. Le rôle des dirigeants et managers est multiple :
- Écouter et réguler les tensions émergentes,
- Donner du sens aux missions et projets,
- Encourager l'autonomie tout en offrant un cadre sécurisant,
- Valoriser la coopération plutôt que la compétition interne,
- Donner un maximum de reconnaissance positive, souligner et valoriser ce qui fonctionne, plutôt que de faire ressortir uniquement ce qui dysfonctionne,
- Prendre soin du climat en instaurant des règles de respect mutuel et de communication.
Ce travail exige une attention constante : le bien-être n'est pas un état figé, mais une construction dynamique qui doit être entretenue.
VI. Les bénéfices collectifs
Investir dans le bien-être au travail, c'est investir dans la performance durable de son équipe. Les bénéfices sont multiples :
- une meilleure cohésion,
- une communication plus fluide avec moins de non-dits,
- une réduction des conflits et des absences,
- une capacité renforcée à traverser les périodes de changement ou de crise,
- et, à long terme, une attractivité accrue de l'organisation pour fidéliser et attirer les talents.
VII. Les erreurs à éviter
À l'inverse, certaines démarches fragilisent le lien au lieu de le renforcer :
- réduire le bien-être à des actions superficielles (cadeaux, événements festifs) sans traiter les causes structurelles,
- ne pas associer les équipes aux réflexions,
- confondre bien-être et confort, en oubliant que l'enjeu n'est pas de supprimer toute contrainte, mais de créer les conditions d'un travail soutenable et porteur de sens.
VIII. Conclusion
Le bien-être au travail est bien plus qu'un indicateur de satisfaction : c'est une véritable stratégie relationnelle. Il permet de consolider les liens, d'apaiser les tensions et de favoriser un climat d'harmonie qui profite à la fois aux individus et à l'entreprise.
Plutôt que de le considérer comme un objectif secondaire, il s'agit de le placer au cœur du management et de la vie collective. Car c'est bien le bien-être qui constitue la clef de voûte : sans lui, les relations se fragilisent ; avec lui, elles deviennent un moteur d'engagement, d'innovation et de réussite partagée.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Le décollement rétinien : cause oculaire ou systémique ?
Toulouse, France
Le décollement rétinien (DR) correspond à la séparation de la rétine neurosensorielle de l'épithélium pigmentaire. Chez le chien et le chat, on distingue trois mécanismes :
- les DR rhegmatogènes, liés à une déchirure laissant le vitré liquéfié s'insinuer sous la rétine ;
- les DR trans-/exsudatifs, provoqués par une accumulation sous-rétinienne de fluide ou de sang secondaire à une atteinte de la barrière hématorétinienne (uvéite, hypertension, chorio-rétinite, néoplasie) ;
- les DR tractionnels, dus à des membranes fibreuses vitréennes qui exercent une traction sur la rétine.
La reconnaissance de cette typologie permet d'orienter la recherche étiologique et la prise en charge. [1]
En pratique, les animaux sont généralement présentés chez le vétérinaire traitant pour une baisse aiguë de la vision ou une mydriase. Celui-ci peut observer des vaisseaux « flottant » dans le vitré lors de l'examen à distance ou des anomalies du fond d'œil telles qu'une modification du reflet du tapis (hyperréflexion), une disparition de la vascularisation rétinienne, la présence d'hémorragies ou de bulles séreuses grisées lors de l'examen ophtalmoscopique (direct ou indirect). Lorsque les milieux intraoculaires sont opaques (hyphéma, cataracte dense), l'échographie B-scan confirme le DR. L'OCT, disponible dans certains centres de référé, peut permettre de préciser l'architecture rétinienne et l'activité sous-rétinienne [2].
Chez le chat, la cause est le plus souvent systémique, avec en tête l'hypertension artérielle du sujet âgé, fréquemment secondaire à une maladie rénale chronique, une hyperthyroïdie ou une cardiopathie. Un dépistage doit donc être préconisé dès 10 ans lors de la consultation préventive annuelle. Le tableau clinique associe des hémorragies pré-/intra-/sous-rétiniennes, un œdème diffus en mottes coalescentes ou sous forme de bulles et un DR transsudatif souvent bilatéral. La mesure de la pression artérielle doit donc devenir un réflexe devant tout DR félin, suivie d'un bilan rénal et thyroïdien et, le cas échéant, d'un traitement antihypertenseur (amlodipine par exemple). L'échographie abdominale et cardiaque peut venir compléter l'exploration à la recherche de cardiopathie ou de phéochromocytome. Le pronostic visuel est d'autant meilleur que la réapplication de la rétine est rapide et que le décollement est partiel. Ainsi un DR total ancien compromet plus définitivement la récupération visuelle. Les choriorétinites infectieuses/inflammatoires (PIF, toxoplasmose...) constituent l'autre grand chapitre des DR exsudatifs félins [2,3]. Leur diagnostic s'appuie généralement sur une recherche PCR positive sur humeur aqueuse.
Chez le chien, ce sont les causes oculaires primaires qui dominent. Les DR rhegmatogènes surviennent lors de dégénérescence vitréenne ou à la suite d'une chirurgie de la cataracte . Ils peuvent être prévenus par rétinopexie laser notamment dans les races à risque ou plus difficilement pris en charge par une chirurgie vitréorétinienne. Les anomalies de développement (dysplasie rétinienne, anomalie de l'œil du Colley) et les uvéites traumatiques ou liées à un processus néoplasique peuvent également conduire à des DR exsudatifs ou tractionnels chez le chien. [1,2]
La démarche du praticien généraliste doit donc suivre cinq étapes :
- confirmer le DR et apprécier éventuellement son étendue ;
- définir son mécanisme pathogénique : rhegmatogène – exsudatif – tractionnel ;
- orienter la démarche étiologique en fonction de ce mécanisme et de l'anamnèse :
- mesure de la pression artérielle et recherche d'une cause systémique chez le chat ;
- recherche de déchirure / anomalie congénitale, recueil d'antécédents de traumatiques iatrogènes ou non, recherche de signes d'uvéite chez le chien ;
- mettre en place un traitement symptomatique, voire étiologique lorsque cela est possible, pour espérer une ré-apposition rapide de la rétine ;
- envisager, selon les cas, un traitement préventif pour l'œil atteint partiellement ou pour l'œil adelphe chez un ophtalmologue.
Chaque praticien doit reconnaître à quelle étape il est préférable pour lui et pour son patient de référer le cas afin d'éviter une perte de chance : en effet, plus la prise en charge est précoce, plus la rétine a des chances de se recoller et de rester fonctionnelle.
VI. Conclusion
Le DR félin doit orienter en priorité vers une cause systémique. Il doit être systématiquement dépisté lors d'un examen annuel chez le sujet âgé.
Le DR canin doit orienter en priorité vers une déchirure. Il peut nécessiter un traitement systémique ou une chirurgie en référé à titre curatif ou préventif.
Gagnez du temps, gagnez des photons !
Bibliographie
- THOMASY SM. Retinal Detachment in Small Animals. In : MSD/Merck Veterinary Manual, Merck & Co., Inc., Rahway, NJ, USA, 2024.
- BECKWITH-COHEN B. Manifestations of systemic disease in the retina and fundus of companion animals. Front Vet Sci, 2024 Feb ; 20(11):1337062.
- CARTER J. Hypertensive ocular disease in cats : a guide to fundic examination. J Feline Med Surg, 2019 Jan ;21(1):35-45.
- WEST MC et al. Evaluation of vitreous degeneration as a potential risk factor for retinal detachment in dogs after phacoemulsification. Vet Ophthalmol, 2020 Jul ;23(4):721-729.
- GRAHN BH et al. Chronic retinal detachment and giant retinal tears in 34 dogs. Can Vet J, 2007 Oct ;48(10):1031–1039.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Le glaucome chez le Chien : quand le suspecter ? Quand référer ? Quel suivi ?
Strasbourg, France
I. Introduction
Le glaucome correspond à une neuropathie optique provoquant une dégénérescence des cellules ganglionnaires de la rétine dont les axones forment le nerf optique. En ophtalmologie vétérinaire, cette entité regroupe un ensemble d'affections invariablement associées à une augmentation de la pression intraoculaire.
- L'augmentation de la pression intraoculaire (PIO) s'accompagne d'un cortège de signes cliniques, parfois très discrets ou ignorés en début d'évolution.
- Le plus souvent primaire chez le chien mais parfois secondaire.
- Évolution très rapide : le pronostic visuel dépend d'une prise en charge en urgence.
INTERVENIR VITE C'EST SAUVER LA VISION
II. Quand le suspecter ?
- Races à risque
- Douleur oculaire : blépharospasme, baisse d'activité.
- Changements d'aspect de l'œil :
- Rougeur oculaire : dilatation des veines épisclérales
- Œdème cornéen plus ou moins prononcé
- Mydriase variable selon le degré d'hypertonie
- Baisse, perte brutale de vision ou cécité chronique : évaluer la réponse à la menace et le réflexe d'éblouissement.
- Dans les formes chroniques : augmentation de volume du globe oculaire (buphtalmie), stries de HAAB ou opacité cornéenne permanente avec kératite d'exposition, luxation du cristallin. Cécité.
- Dans les glaucomes secondaires : hyphéma, luxation du cristallin, sécclusion pupillaire ou synéchies, tumeurs, infiltration ou dispersion pigmentaire…
1. La mesure de la PIO
- Intervalle de référence : 12-25 mmHg.
- Glaucome suspecté si PIO > 25 mmHg ou différence de plus de 8 mmHg entre les deux yeux.
III. Quand référer ?
Le glaucome aigu est une urgence vraie :
- Lors de glaucome aigu avec hypertonie récente, la fenêtre pour sauver la vision se compte en heures.
- En cas de glaucome chronique (historique d'évolution sur plusieurs semaines, cécité installée depuis plusieurs semaines, buphtalmie), on ne se situe plus dans le cadre de l'urgence.
La rapidité à référer et à transmettre les bonnes informations permet de dépister les « vraies » urgences et conditionne le pronostic.
1. Que faut-il faire avant de référer ? Optimiser la prise en charge initiale
- Identifier s'il s'agit d'un glaucome aigu (référé urgent) ou chronique (référé non urgent).
- Stabiliser en première intention avant transfert :
- Si PIO > 25 mmHg : traitement hypotonisant topique avec mesure de PIO très régulièrement (hospitalisation)
- dorzolamide, brinzolamide ± timolol, latanoprost (sauf contre-indications)
- systémique (mannitol IV, acetazolamide IM ou IV)
- Si PIO > 25 mmHg : traitement hypotonisant topique avec mesure de PIO très régulièrement (hospitalisation)
- Analgésie adaptée.
- Optimiser la communication avec le spécialiste.
- Transmettre un dossier clair et complet.
- Prendre contact directement avec le spécialiste :
- Appel téléphonique : évaluer le degré d'urgence et délivrer les premiers conseils.
- Une fois l'urgence confirmée avec le spécialiste, créneau d'accueil prioritaire.
- Prévenir le propriétaire qu'il s'agit d'une urgence et de l'importance de consulter rapidement un ophtalmologiste.
2. Que va faire le spécialiste : à qui référer ? Objectifs de la prise en charge spécialisée ? À quoi ça sert Pour quels résultats ?
a) À qui référer ?
Vétérinaire spécialiste en ophtalmologie ou qualifié en ophtalmologie ayant la capacité de conduire une exploration complète (mesure de la pression intraoculaire, gonioscopie, échographie…), une prise en charge intensive de l'hypertonie oculaire (possibilité d'hospitaliser, d'administrer un traitement très régulièrement, de réaliser une paracentèse et d'assurer un suivi continu de la PIO) et maîtrisant les différents traitements chirurgaux du glaucome (chirurgie filtrante, chirurgie cyclo-ablatives).
b) Objectifs de la prise en charge spécialisée ?
- Confirmer le diagnostic (examen gonioscopique, échographie, UBM : ultrasound biomicroscopy) et évaluer le stade de la maladie (tests de vision, ophtalmoscopie du fond d'œil, pupillométrie chromatique) afin d'adapter la prise en charge.
- Initier une réduction rapide de la PIO (collyres, traitements systémiques, paracentèse).
- Préserver la vision et traiter la cause sous-jacente.
- Prise en charge chirurgicale rapide si nécessaire
- Planifier le suivi à long terme de l'œil malade et la prophylaxie de l'œil controlatéral.
c) À quoi ça sert ?
Confirmer le diagnostic et évaluer le pronostic
Les tests d'évaluation de la vision évaluent la vision ou les chances de récupération :
- Réponse à la menace
- Réflexe d'éblouissement => l'œil est encore sensible à la stimulation lumineuse.
- Pupillométrie chromatique : évalue la réponse des cellules ganglionnaires.
- Électrorétinographie (ERG) : aucun intérêt car les modifications enregistrables sont très tardives
- L'ophtalmoscopie : précise si la maladie est récente ou chronique et de moins bon pronostic.
- La gonioscopie : donne une idée de l'état de l'entrée des voies de drainage de l'humeur aqueuse. Souvent impossible à pratiquer sur l'œil malade. En revanche, pratiquée sur l'œil adelphe, permet d'identifier une anomalie du ligament pectiné, l'ouverture de l'angle irido-cornéen et ainsi une prédisposition au glaucome primaire.
- L'échographie : observation des structures intraoculaires.
- L'UBM : évaluation de la fente ciliaire.
Initier une réduction rapide de la PIO
- La baisse rapide de la PIO est une priorité pour préserver ou restaurer la vision lorsque c'est encore possible : c'est une question d'heures.
- Un traitement médical est immédiatement mis en place car la PIO doit se normaliser le plus rapidement : hospitalisation avec soins très fréquents et monitoring étroit de la PIO
- Si échec → paracentèse, dernière étape avant chirurgie
- En dernier recours, on pratique une intervention ayant pour objectif de faire baisser durablement la PIO :
- Chirurgie filtrante : pose d'une valve permettant de dériver l'humeur aqueuse
- Chirurgie cyclo-affaiblissante : détruit sélectivement les procès ciliaires afin de diminuer la production d'humeur aqueuse.
- Possibilité de combiner les deux techniques
- Récidives possibles : stratégie choisie au cas par cas.
- Si glaucome secondaire : chirurgie du cristallin (luxation, cataracte), vitrectomie lors de glaucome malin…
NB : l'exérèse d'un cristallin luxé lors de buphtalmie avec cécité ne présente aucun intérêt car elle ne règle pas l'hypertonie. - Lorsque la vision est abolie : énucléation, prothèse d'éviscération, cyclophotocoagulation définitive.
d) Pour quels résultats ?
Synthèse des résultats publiés les dix dernières années dans les journaux indexés internationalement :
L'utilisation de la valve d'AHMED sur un œil encore voyant offre la meilleure chance de conservation de la vision en première intention
Sur une période comprise entre 1 et 5 ans au prix d'une surveillance étroite et de révision de la bulle de filtration à chaque fois que cela est nécessaire, on obtient des résultats intéressants. Sur 132 yeux traités, 18 yeux sont voyants après une période de 5 ans. La durée moyenne de rétention de la vision lors d'implantation médiale est d'environ 62 mois versus 45 mois en latérale (SAITO et al., 2022). Dans une autre étude portant sur 104 yeux, la durée médiane de persistance de la vision de chiens implantés par valve d'AHMED est de 39,9 mois alors que celle de chiens uniquement traités médicalement est de 1,7 mois (KUBO & ITO, 2024).
L'utilisation du laser diode est plus intéressante en deuxième intention et permet de prendre le relai de la valve.
Le laser utilisé seul :
- Cyclophotocoagulation transclérale continue (méthode externe continue), méthode la plus ancienne de cycloaffaiblissement par laser. Moins performante que les autres techniques laser pour préserver la vision d'après les résultats publiés puisqu'après une durée d'un an, la vision persiste entre 50% (HARDMAN et al. 2001 – 7/14 yeux) et 53% (COOK et al. 1997- 10/19 yeux) des cas.
- Une technique plus récente, la cyclophotocoagulation transclérale micropulsée, permet une utilisation répétée du laser. Selon le protocole utilisé, la vision est conservée dans 50% à 90% des cas durant les 6 premiers mois qui suivent la procédure (BENITEZ-VERA et al., 2025). Sur une période plus longue (médiane de suivi de 30,5 mois), 43% (6/14) des yeux restent voyants. Cependant, le faible effectif de ces études (8,11 et 14 yeux) et la courte durée d'observation postopératoire ne permettent pas de positionner précisément cette technique pour l'instant.
- En revanche, l'endocyclophotocoagulation (ECP, méthode endoculaire utilisant un micro-endoscope) a été éprouvée sur un très large effectif. Dans une série de 389 yeux, 63% des yeux traités par ECP seule sont encore voyants après 1 an de suivi, 49% après 2 ans (SOSNOWIK et al., 2025).
Le laser combiné ou en relai d'une chirurgie filtrante :
L'endocyclophotocoagulation associée à la phacoémulsification et mise en œuvre après échec d'une valve d'AHMED a permis de préserver la vision après l'intervention, respectivement dans 93% des cas à 1 an, 84% à 2 ans, 60% à 3 ans et 48% à 4 ans. Si l'on considère que les sujets (14 yeux) avaient déjà gagné du temps de vision après la mise en place de la valve, cette étude montre que l'ECP est actuellement le meilleur relai pour prolonger la vision après l'implantation d'une valve d'AHMED (TURICEA et al., 2025).
Protocole idéal :
- valve d'AHMED en première intention
- suivi régulier (avec traitement médical si nécessaire)
- en cas d'élévation de la PIO : révision de la bulle de filtration associée à l'ECP, suivi régulier (avec traitement médical si nécessaire).
Cas particulier des glaucomes secondaires :
La vitesse d'intervention impacte le pronostic d'une hypertonie. Si possible, une prise en charge prophylactique ou lors de stades précoces permettra d'optimiser le pronostic.
- Luxation du cristallin : si hypertonie au moment de la chirurgie => baisse des chances de maintien de la vision. Si possible, privilégier une extraction précoce avant luxation antérieure.
- Cataracte : cause la plus fréquente de glaucome secondaire. Une prise en charge précoce de la cataracte diminue ce risque. Lors de cataractes intumescentes s'accompagnant d'hypertonie (avec persistance d'un potentiel visuel) une prise en charge très rapide de la cataracte est conseillée. Il est conseillé d'opérer rapidement les cataractes évoluant sur un mode aigu (cataracte diabétique, traumatique, juvénile).
- Uvéite : un contrôle rapide de l'inflammation permet d'avoir une meilleure action sur la PIO. La formation de fibrine ou de synéchies constitue un risque élevé de glaucome et de perte visuelle.
- Les glaucomes pigmentaires, les syndromes de mélanose oculaire et les tumeurs intraoculaires présentent souvent des défis thérapeutiques une fois que l'hypertonie est installée.
IV. Quel suivi ?
1. Pourquoi un suivi ?
- Surveiller l'œil opéré : il est crucial de repérer les récidives d'hypertonie précocement si l'on veut préserver la vision.
- Surveiller l'œil adelphe : si glaucome primaire, œil adelphe à risque. 70,9% des chiens atteints de glaucome primaire à angle fermé unilatéral développeront un glaucome dans l'œil adelphe en moins de 5 ans avec un temps médian d'apparition de 2,15 ans bien que traités prophylactiquement (DONOHUE et al., 2025).
- Surveiller les effets secondaires des différents traitements : les collyres antiglaucomateux peuvent provoquer des réactions d'intolérance ou avoir des effets secondaires qu'il convient d'identifier et de prendre en charge
2. Améliorer le suivi en optimisant la collaboration entre praticien généraliste et ophtalmologiste
Plan de suivi partagé :
- Définir qui contrôle la PIO et à quelle fréquence.
- Décider ensemble des ajustements thérapeutiques.
- Prophylaxie sur l'œil controlatéral si indiqué.
Retour d'information :
- Le spécialiste envoie un compte-rendu complet (diagnostic précis, pronostic visuel, plan thérapeutique).
- Le généraliste informe le spécialiste du suivi
Gestion de la chronicité :
- Le généraliste peut assurer les suivis courants (PIO, confort, renouvellement traitement).
- Le spécialiste revoit le patient pour les bilans périodiques ou si aggravation.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Le syndrome cardiorénal
Paris, France
Guyancourt, France
I. Introduction
La profession médicale a adopté le terme « syndrome cardio-rénal, SCR » pour décrire les relations physiopathologiques entre le cœur et le rein en cas de maladie. Les différents types de SCR sont bien établis chez l'homme mais bien que les chiens et les chats partagent des chemins physiopathologiques essentiels communs avec l'homme pour le développement du SCR, notamment le système rénine-angiotensine-aldostérone, il y a certaines différences liées à l'espèce qui ne permettent pas toujours l'extrapolation de données.
Les problèmes cardiaques chez l'homme sont majoritairement liés à l'hypertension artérielle systémique et les coronaropathies, à la différence du chien (majoritairement maladies valvulaires, myocardiopathie dilatée et dirofilariose en Outre-mer) et du chat (myocardiopathie hypertrophique et dans un moindre degré hypertension systémique ou autres myocardiopathies). La cause la plus fréquente de maladie rénale chronique (MRC) chez l'homme est le diabète sucré (approximativement la moitié des cas nécessitant une transplantation rénale ou une dialyse) ce qui est beaucoup plus fréquent que chez le chat et le chien. Une autre cause fréquente de dysfonction rénale chez l'homme est la sténose de l'artère rénale, non préoccupant en médecine vétérinaire.
Ces différences essentielles avec la médecine ont conduit à la création d'un groupe d'experts vétérinaires incluant 16 spécialistes en cardiologie ou en néphrologie vétérinaires venant de différents pays qui ont publié en 2015 un consensus sur les « troubles de l'axe cardiovasculaire-rénal, TCvR », ce terme remplaçant l'acronyme SCR.
Selon le consensus, le TCvR est défini comme : tout défaut structurel et/ou fonctionnel du système cardiovasculaire ou du rein induit par une maladie, une toxine ou un médicament, conduisant à une perturbation des interactions normales entre ces systèmes, au détriment continu de l'un ou des deux.
II. Rappels de physiologie rénale
L'énorme débit de filtration glomérulaire requis pour le maintien de l'homéostasie nécessite un flux sanguin tout aussi conséquent. Ainsi, bien que les reins représentent 1% de la masse corporelle, ils représentent l'organe le plus perfusé avec un débit sanguin estimé chez l'humain d'environ 4 ml/mn/g de tissu rénal (soit 8x plus environ que le cerveau). Environ 20-25% du volume sanguin passe par les reins à chaque cycle cardiaque. Ceci permet de maintenir une pression élevée dans les capillaires rénaux et de maintenir un bon débit de filtration glomérulaire.
Malgré cette perfusion rénale conséquente et la quantité d'oxygène apportée aux reins, l'anatomie particulière du néphron et de sa vascularisation (vasa recta) rend certaines parties du néphron sujettes à une hypoxie fréquemment observée cliniquement. Ainsi, en cas d'hypoperfusion, certaines parties du néphron (médullaires) peuvent rapidement souffrir d'un manque d'oxygène et une insuffisance rénale aiguë peut vite s'installer.
III. Rappels de la classification IRIS
Afin de détecter le plus efficacement possible un potentiel syndrome cardio-rénal, il est important de pouvoir identifier efficacement une insuffisance rénale aiguë. Certains patients, bien que non azotémiques, peuvent tout de même présenter des signes en faveur d'une insuffisance rénale aiguë. Par ailleurs, le groupement international IRIS a établi des lignes conductrices, permettant d'identifier au plus tôt un patient développant une insuffisance rénale aiguë (tableau 1), ceci permet de pouvoir agir le plus précocement possible et de surveiller la fonction rénale notamment lors de traitement de patients cardiaques.
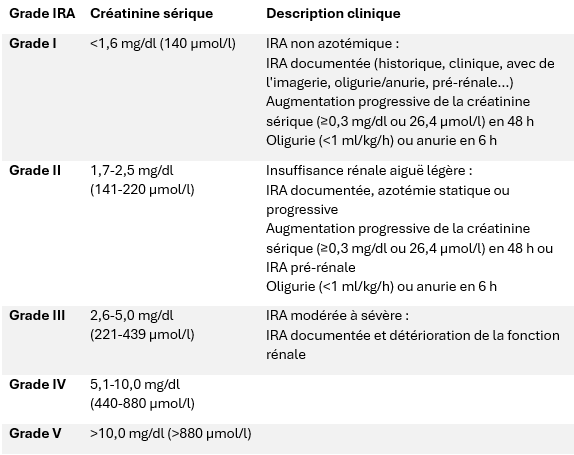
Tableau 1 : classification IRIS de l'insuffisance rénale aiguë
IV. Classification du TCvR
Le TCvR comprend les sous-groupes suivants :
- TCvRCœur, pour refléter la maladie/dysfonction rénale découlant d'une maladie impliquant le système cardiovasculaire ;
- TCvRRein, pour la maladie/dysfonction cardiovasculaire secondaire à une maladie rénale ;
- TCvRConc, pour l'altération concomitante des deux systèmes causée par des maladies cardiovasculaires et rénales primaires concomitantes, ou d'autres processus pathologiques, médicaments, toxines ou substances toxiques qui affectent respectivement les deux systèmes.
Les trois catégories peuvent être subdivisées en maladie stable ou instable en fonction de la présentation clinique de l'animal (tableau 2).
Le SCR est donc classifié en 5 types :
- Syndrome cardio-rénal aigu ou TCvRCœur avec maladie instable.
- Syndrome cardio-rénal chronique ou TCvRCœur avec maladie stable.
- Syndrome réno-cardiaque aigu ou TCvRRein avec maladie instable.
- Syndrome réno-cardiaque chronique ou TCvRRein avec maladie stable.
- Syndrome cardio-rénal secondaire ou TCvRConc secondaire à une affection systémique aiguë ou chronique.
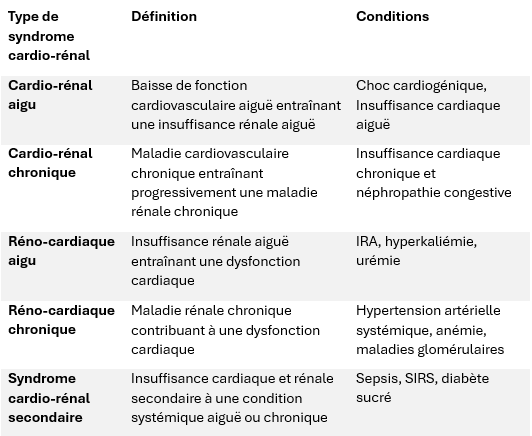
Tableau 2 : classification des divers types de syndromes cardio-rénaux.
1. Type 1
Le type 1 est caractérisé par une dégradation rapide de la fonction cardiaque menant à une lésion/dysfonction rénale aiguë. Il existe des mécanismes multiples et complexes par lesquels l'insuffisance cardiaque (IC) aiguë ou une apparition aiguë d'une IC chronique conduit à une atteinte rénale aiguë. Cette dernière peut résulter d'une réduction de la perfusion rénale due à une diminution de la fonction systolique gauche, d'une activation des systèmes neuroendocrinien et sympathique, et d'une congestion passive des reins. L'état congestif peut induire une diminution de la réactivité aux diurétiques, ce qui peut conduire à une utilisation excessive de diurétiques et à une aggravation de l'atteinte rénale.
2. Type 2
Le type 2 consiste en une maladie cardiovasculaire chronique provoquant une MRC progressive. L'insuffisance cardiaque chronique est susceptible de causer une perfusion rénale réduite de manière persistante, une congestion rénale chronique et des changements neurohormonaux associés à une stimulation sympathique chronique. Le traitement de l'ICC utilisant des diurétiques et des bloqueurs du système rénine-angiotensine-aldostérone peut provoquer une hypovolémie et une hypotension, ainsi que des changements dans l'hémodynamique rénale. Chez l'homme, la prévalence de la dysfonction rénale dans l'ICC est élevée et constitue un prédicteur indépendant de la mortalité.
3. Type 3
Le type 3 est caractérisé par une aggravation primaire aiguë de la fonction rénale qui entraîne une dysfonction cardiaque aiguë. L'insuffisance rénale aiguë (IRA) peut affecter la fonction cardiaque par plusieurs mécanismes, tels que la rétention d'eau, les troubles électrolytiques, l'activation neurohormonale et les facteurs dépresseurs myocardiques, contribuant ainsi potentiellement au développement d'arythmies, de péricardite urémique et d'insuffisance cardiaque aiguë.
4. Type 4
Le type 4 reflète une MRC primaire qui contribue à une dysfonction cardiaque secondaire. Une fonction systolique diminuée, une hypertrophie ventriculaire gauche et un état de haut débit (secondaire à l'anémie) sont quelques-unes des séquelles cardiaques potentielles à long terme de la MRC.
5. Type 5
Le type 5 est caractérisé par une dysfonction cardiaque et rénale secondaire à un état systémique aigu ou chronique indépendant. Le sepsis est la condition aiguë la plus courante qui affecte à la fois le cœur et les reins. La pancréatite et l'hyperadrénocorticisme sont des maladies chroniques typiques chez les chiens qui ont un effet similaire sur les systèmes urinaire et cardiovasculaire.
V. Étiologie du TCvR chez le chien et le chat
La liste ci-dessous résume l'étiologie du TCvR chez le chien et le chat selon le consensus.
1. TCvRCœur
- Hypertension artérielle systémique entraînant une maladie glomérulaire
- Choc cardiogénique, faible débit cardiaque et hypotension systémique entraînant une diminution de la perfusion rénale, une azotémie et une lésion rénale aiguë
- Thromboembolie artérielle systémique entraînant un infarctus rénal
- Dirofilariose ou syndrome cave entraînant une glomérulonéphrite ou une lésion rénale aiguë, respectivement
- Congestion passive du rein lors d'insuffisance cardiaque
2. TCvRRein
- Hypertension artérielle systémique médiée par les reins entraînant une augmentation de la postcharge, une hypertrophie ventriculaire gauche, une aggravation de l'insuffisance mitrale ou aortique, des arythmies, une vasculopathie ou une rétinopathie
- Surcharge volumique entraînant une congestion ou une hypertension systémique
- Hypokaliémie ou hyperkaliémie entraînant des arythmies cardiaques
- Réduction de l'élimination rénale des médicaments (par exemple, la digoxine) conduisant à une toxicité
- Hypodipsie urémique, anorexie ou vomissements entraînant une hypovolémie et une diminution du débit cardiaque et de la perfusion
- Péricardite urémique
- Activation de l'axe rénine-angiotensine-aldostérone entraînant une rétention de sodium et d'eau, un remodelage cardiaque et vasculaire ou une congestion
- Anémie secondaire à la MRC entraînant une surcharge volumique et une réduction de l'oxygénation des tissus cardiaques
3. TCvRConc
- Emboles septiques ou néoplasiques entraînant des infarctus rénaux et cardiaques
- Syndrome de dilatation/torsion de l'estomac entraînant des arythmies cardiaques et une azotémie
- Maladie infectieuse (par exemple Trypanosoma cruzi)
- Maladie de stockage du glycogène entraînant une déposition de glycogène dans les reins et le cœur
- Amyloïdose entraînant une déposition d'amyloïde dans les tissus rénaux et cardiaques
- Considérations sur la gestion d'un SCR
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Le syndrome de CBH : savoir le reconnaître
Toulouse, France
Le syndrome de Claude Bernard-Horner (SCBH) résulte d'une interruption du flux d'innervation autonome de la voie sympathique au niveau de l'œil et de ses annexes.
Chez le chien et le chat, il se manifeste par une triade quasi constante, le plus souvent unilatérale : myosis, ptosis palpébral et énophtalmie à l'origine d'une procidence de la membrane nictitante. Une vasodilatation épisclérale discrète peut également l'accompagner. La spécificité sémiologique majeure du SCBH est l'absence de douleur oculaire et l'aspect calme de la chambre antérieure. [1]
À l'inverse, il est fondamental d'écarter l'uvéite antérieure du diagnostic différentiel du SCBH. Cette affection partage en effet certains signes tels que le myosis, l'hyperhémie épisclérale (souvent plus marquée), plus rarement une énophtalmie avec procidence secondaire de la membrane nictitante. Leur origine est toutefois très différente car l'uvéite correspond à un processus inflammatoire intraoculaire douloureux qui s'accompagne de photophobie et d'un blépharospasme. L'examen approfondi de la chambre antérieure permet généralement de mettre en évidence le caractère inflammatoire de l'affection avec l'observation d'un effet Tyndall, d'un hypopion et/ou de dépôts rétrokératiques /lenticulaires. De plus, la pression intraoculaire est souvent abaissée en phase aiguë [2,3].
Ainsi, face à un œil myotique, la question est simple : la chambre antérieure est-elle calme ou enflammée ? La réponse oriente immédiatement vers le diagnostic.
Lorsque le diagnostic de SCBH est établi, sa neurolocalisation peut orienter la démarche étiologique. La voie sympathique emprunte en effet 3 neurones : depuis le tronc cérébral jusqu'à la moelle cervicale (1er neurone), de la moelle cervicale jusqu'au ganglion cervical crânial (2è neurone) et du ganglion jusqu'à l'œil (3è neurone). Le syndrome oculaire peut donc être la conséquence d'une lésion à chacun de ces étages : affection névraxiale, traumatisme brachial, compression cervicale, otite moyenne/interne, ototoxicité iatrogène ou encore forme idiopathique, particulièrement décrite dans certaines races de chiens comme le Golden Retriever. L'instillation de phényléphrine à 10% dans l'œil atteint permet dans un premier temps d'estimer ce niveau d'atteinte selon le délai de rémission des symptômes : atteinte du 3è neurone lors de rémission en moins de 20 minutes, atteinte du 2è neurone entre 20 et 40 minutes et atteinte du 1er neurone au-delà. La démarche étiologique est ensuite généralement complétée par de l'imagerie [4].
Face à un myosis anisocorique, la démarche à adopter est donc [5] :
- Une anamnèse orientée (traumatisme crânio-cervical, otite ou traitement ototoxique, chirurgie du cou/oreille, signes neurologiques ou thoraciques pour SCBH ; contexte infectieux/immunitaire, ulcère cornéen pour uvéite).
- Un examen ciblé :
- mise en évidence d'une ptose palpébrale et d'une énophtalmie associées ;
- douleur absente lors de SCBH, présente lors d'uvéite ;
- examen approfondi de la chambre antérieure à la recherche d'éléments inflammatoires.
- Des examens complémentaires choisis :
- test à la fluorescéine (éliminer un ulcère cornéen) ;
- tonométrie (normale lors de SCBH, basse lors d'uvéite aiguë).
- Une recherche étiologique :
- exploration locale, loco-régionale ou systémique à la recherche d'un foyer infectieux lors d'uvéite
- neurolocalisation par le test à la phényléphrine lors de SCBH, éventuellement accompagnée d'examens cliniques ou d'imagerie (otoscopie, imagerie des bulles tympaniques, du cou, du thorax et du névraxe).
À retenir : le SCBH se traduit entre autres par un myosis sur un œil calme alors que l'uvéite antérieure se traduit entre autres par un myosis sur un œil enflammé.
Bibliographie
- ZWUESTE DM, GRAHN BH. A review of Horner's syndrome in small animals. Can Vet J. 2019;60(12):1261-1269.
- TOWNSEND WM. Canine and Feline Uveitis. Vet Clin North Am Small Anim Pract. 2008;38:323-346.
- HÅKANSON N, FORRESTER SD. Uveitis in the dog and cat. Vet Clin North Am Small Anim Pract. 1990 May; 20(3):715-35.
- LUISA DE RISIO, JAMES FRASER MCCONNELL. Second order Horner's syndrome in a cat. J Feline Med Surg. 2009 Aug; 11(8): 714–716.
- PENDERIS J. Diagnosis of Horner's syndrome in dogs and cats. In Practice. March 2015; 37(3):107-119.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Le syndrome de Cushing : ses complications, ses « avantages »
Marseille, France
I. Introduction
Le syndrome de Cushing, ou hypercorticisme, est l'une des affections endocriniennes les plus fréquemment rencontrées chez le chien âgé, résultant d'une production excessive de glucocorticoïdes, le plus souvent d'origine hypophysaire. Son installation est progressive, sur plusieurs mois ou des années, et est souvent associée au moment du diagnostic ou au cours de l'évolution de la maladie à des comorbidités, souvent liées à des complications systémiques multiples. Au moins une comorbidité (et jusqu'à 5) a d'ailleurs été retrouvée dans environ 70% des 219 cas d'une étude rétrospective. Les complications peuvent être présentes dès le diagnostic, s'installer progressivement ou se manifester d'une manière aiguë, et peuvent provoquer le décès des chiens atteints d'hypercorticisme.
II. Complications cardiovasculaires et thromboemboliques
1. Hypertension artérielle
Parmi les plus précoces et fréquentes, on compte l'hypertension artérielle, qui touche jusqu'à 82% des chiens atteints selon une étude récente (pression systolique (PAS) ≥ 150 mm Hg), dont près de la moitié présentent une hypertension importante (PAS ≥ 180 mm Hg), avec un risque accru de lésions d'organe cible, telles que cécité, insuffisance cardiaque ou aggravation d'une néphropathie sous-jacente. Cette hypertension est multifactorielle : elle est liée à une activation apparente des récepteurs minéralocorticoïdes par le cortisol, qui entraîne une rétention sodée et une fuite potassique. La thrombocytose, fréquente dans le Cushing, et la protéinurie sont des marqueurs prédictifs forts de l'hypertension artérielle. La protéinurie, liée à une glomérulosclérose, une augmentation du DFG et de la volémie, est présente dans 45 à 70% des cas au moment du diagnostic. Elle peut persister dans 40% des cas après la mise en place du traitement. L'hypertension persiste également souvent malgré le traitement du syndrome de Cushing, avec près de 46% des chiens restant hypertendus après un an de trilostane, nécessitant un traitement antihypertenseur complémentaire, souvent à base d'IECA et/ou d'amlodipine.
2. Risque thromboembolique
À cette hypertension s'ajoute un risque thromboembolique accru, lié à un état d'hypercoagulabilité chronique, que traduit une élévation du fibrinogène, une thrombocytose, une aggravation de la viscosité sanguine et une baisse des inhibiteurs de la coagulation. Cette hypercoagulabilité est bien documentée par des études utilisant la thromboélastographie et se traduit cliniquement par des présentations cliniques comme les embolies pulmonaires, parfois fatales, des thromboembolies aortiques, mais également des thromboses veineuses profondes ou des thromboses rénales. On estime que le risque thrombotique est augmenté d'un facteur 2 à 5. L'hypercoagulabilité ne semble par ailleurs pas se résoudre avec le traitement même en cas de contrôle apparent de la maladie, exposant donc à des accidents vasculaires, survenant souvent sans signes précurseurs.
III. Complications métaboliques
1. Diabète sucré
Le diabète sucré est une autre complication majeure, touchant entre 8 et 16% des chiens atteints. L'excès de cortisol induit une résistance à l'insuline et favorise la néoglucogenèse hépatique. Une étude récente a montré que les chiens ayant à la fois un syndrome de Cushing et un diabète sucré étaient plus insulino-résistants, nécessitant des doses médianes d'insuline significativement plus élevées (0,90 U/kg/12h) que ceux ayant uniquement un diabète (0,67 U/kg/12h). De plus, leur espérance de vie est réduite, avec une médiane de survie de 892 jours contre une médiane non atteinte chez les chiens diabétiques sans Cushing.
2. Pancréatites
Les pancréatites sont également fréquemment associées au syndrome de Cushing, bien que la causalité directe reste difficile à établir. Il a en effet été démontré une augmentation non symptomatique de la lipase pancréatique et des modifications échographiques évocatrices d'une pancréatite dans le syndrome de Cushing, rendant le diagnostic de pancréatite difficile. Pour autant, même si une prévalence accrue de pancréatite subclinique a été notée dans certaines études, celles-ci peuvent évoluer vers des épisodes aigus, parfois récidivants et graves. L'hypercorticisme favorise l'hyperlipidémie, facteur de risque majeur de pancréatite. L'absence de traitement semble donc augmenter le risque de développer une pancréatite, avec ses conséquences potentiellement mortelles.
3. Complications urinaires
a) Infections urinaires
Les infections urinaires sont très fréquentes, en raison de l'immunosuppression induite par les glucocorticoïdes. Jusqu'à 18% des patients présentent une bactériurie, souvent asymptomatique ne nécessitant pas forcément de traitement, mais pouvant évoluer vers des pyélonéphrites ou des abcès rénaux. La glycosurie présente en cas de diabète associé aggrave ce risque.
b) Urolithiases
Les urolithiases, en particulier à base d'oxalate de calcium, sont également plus fréquentes chez les chiens atteints. L'hypercorticisme diminue la réabsorption tubulaire et modifie le métabolisme du calcium et du phosphore, favorisant la lithogenèse. Ces calculs exposent à une obstruction urétrale, voire urétérale, et à des cystites récidivantes.
4. Complications hépatobiliaires
Les mucocèles biliaires sont une complication redoutable, fortement associée au syndrome de Cushing, avec un odds ratio supérieur à 20. Il s'agit d'une accumulation de mucus dans la vésicule biliaire, pouvant entraîner une rupture et une péritonite biliaire, urgence chirurgicale pouvant être fatale. L'excès de corticoïde modifie la composition et la viscosité de la bile, favorisant cette accumulation.
5. Complications neurologiques
D'un point de vue neurologique, la croissance indolente mais continue des macro-adénomes hypophysaires peut conduire à l'apparition de symptômes neurologiques centraux, tels que modifications comportementales, ataxie, crises convulsives ou cécité soudaine par compression du chiasma optique, du thalamus et de l'hypothalamus. Ces signes cliniques sont décrits dans 10 à 30% des chiens atteints de Cushing hypophysaire mais jusqu'à 70% des chiens porteurs de macroadénomes sécrétants dans une étude sur la radiothérapie de ces masses hypophysaires.
6. Complications musculo-squelettiques
Les complications osseuses et tendineuses, quoique moins fréquentes, sont bien réelles : le cortisol en excès inhibe la synthèse du collagène, diminue le dépôt osseux, favorise l'ostéoporose, retarde la consolidation osseuse et favorise les ruptures tendineuses. Des fractures pathologiques ont été rapportées, ainsi que des ruptures tendineuses. La myopathie liée au Cushing, souvent considérée comme insidieuse, est assez fréquente, la prévalence des signes cliniques neuromusculaires atteignant près de 50% des chiens traités sur le long terme : le tableau associe souvent fonte musculaire généralisée, faiblesse progressive, intolérance à l'effort, démarche raide pouvant aller jusqu'à la myotonie, décrite avec des contractures et une hypertrophie paradoxale. Lorsque la maladie est bien contrôlée, les signes peuvent être atténués, mais la récupération musculaire reste partielle, voire rare lors de myotonie, d'où l'urgence d'une prise en charge précoce.
7. Complications néoplasiques
Par ailleurs, le lien entre Cushing et carcinome hépatocellulaire (HCC) est évoqué. Plusieurs études confirment que le Cushing constitue un facteur de risque pour l'apparition d'HCC, en particulier avec vacuolisation hépatique chronique et dysmétabolisme lipidique : les chiens atteint du sybdrome de Cushing développent plus d'HCC, souvent à un stade avancé, et ce risque est démultiplié chez certaines races prédisposées, même si la pathogénie exacte reste discutée.
IV. Considérations thérapeutiques
1. Situations particulières justifiant l'absence de traitement
Dans certains cas, l'imprégnation corticoïde peut être bénéfique et inciter à ne pas mettre en place de traitement. Cependant, le nombre de situations dans lesquelles il est bénéfique de ne pas traiter reste limité. Il existe quelques exceptions : certains chiens très âgés, en phase terminale d'une maladie incurable, ou présentant une pathologie dont le traitement nécessite de conserver une imprégnation glucocorticoïde (par exemple, arthrose invalidante sensible aux corticoïdes, maladies auto-immunes nécessitant un traitement stéroïdien). Chez ces patients, l'arrêt ou la réduction de la cortisone risquerait d'aggraver rapidement la pathologie d'accompagnement, alors qu'un hypercorticisme contrôlé permet d'offrir un confort temporaire, même au prix d'un compromis sur la survie à long terme. Cependant, la discussion avec le propriétaire sur la décision de ne pas traiter doit évoquer de façon transparente le risque de voir le chien évoluer vers une dégradation progressive (asthénie, fonte musculaire, aggravation des comorbidités), et parfois de manière brutale (épisodes thromboemboliques, rupture de mucocèle, crises neurologiques).
2. Bénéfice du traitement sur la survie
Plusieurs études récentes ont comparé la survie des chiens avec un syndrome de Cushing traité ou non, montrant notamment une médiane de survie de 506 jours pour les chiens non traités, contre une médiane non atteinte après deux ans pour les chiens traités par trilostane. Dans 2 autres études, la médiane de survie des chiens traités par trilostane (toutes formes confondues) varie de 521 à 998 jours, avec un bénéfice de la prise en charge active sur la qualité comme sur la durée de vie. Cette survie s'effondre à moins de 200 jours en médiane chez les chiens laissés sans traitement.
En pratique, le nombre de chiens pour lesquels un traitement n'est pas recommandé en raison d'une espérance de vie très courte ou d'une polypathologie terminale reste très faible. En dehors de ce contexte, l'instauration du traitement médical, même à faibles doses, est le choix à privilégier pour offrir le maximum de confort et d'espérance de vie au patient.
On retiendra donc que, sauf exception liée à des circonstances très particulières, il est préférable de proposer un traitement au syndrome de Cushing, l'absence de prise en charge exposant à une aggravation lente, multisystémique et souvent silencieuse, et parfois à des complications aiguës pouvant être responsables du décès de l'animal.
Bibliographie
- BENNAIM M, SHIEL RE, MOONEY CT. Diagnosis of spontaneous hyperadrenocorticism in dogs. Part 1: Pathophysiology, aetiology, clinical and clinicopathological features. Vet J. 2019;252:105342.
- SMETS P et coll. Cushing's syndrome, glucocorticoids and the kidney. Gen Comp Endocrinol. 2010;169:1-10.
- PEREZ-LOPEZ L et coll. Effects of concurrent canine Cushing's syndrome and diabetes mellitus on insulin requirements, trilostane dose, and survival time. Res Vet Sci. 2023;161:62-68.
- AICHER KM et coll. Investigation of adrenal and thyroid gland dysfunction in dogs with ultrasonographic diagnosis of gallbladder mucocele formation. PLoS One. 2019;14(2):e0212638.
- MITSUI A et coll. Hypercoagulability based on thromboelastography is common in dogs undergoing adrenalectomy. J Am Vet Med Assoc. 2025;260:439–447.
- DUPONT A et coll. Urinary tract infections in Cushing's dogs: microbiological characteristics and antibiotic susceptibility. Vet Microbiol. 2020;244:108672.
- HOFFMAN JM et coll. Canine hyperadrenocorticism associations with signalment, selected comorbidities and mortality within North American veterinary teaching hospitals. J Small Anim Pract. 2018;59:412-9.
- SCHOFIELD IS et coll. Survival analysis of 219 dogs with hyperadrenocorticism attending primary care practice in England. Vet Rec. 2022;191:e908.
- LEELA-ARPORN R et coll. Epidemiology of massive hepatocellular carcinoma in dogs: A 4-year retrospective study. Vet J. 2019;253:109314.
- RAPASTELLA S et coll. Effect of pituitary-dependent hypercortisolism on the survival of dogs treated with radiotherapy for pituitary macroadenomas. J Vet Intern Med. 2023;37:1234-42.
- GARCIA SAN JOSE P et coll. Prevalence and risk factors associated with systemic hypertension in dogs with spontaneous hyperadrenocorticism. J Vet Intern Med. 2019;33:1334-41.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Leptospirose : les formes à l'admission et leur devenir au long cours
Guyancourt, France
Guyancourt, France
I. Introduction
La leptospirose canine est une maladie infectieuse systémique, d'expression clinique extrêmement polymorphe, dont l'évolution dépend de multiples facteurs liés à l'agent infectieux (sérovar impliqué, virulence, charge infectante) et à l'hôte (statut immunitaire, âge, comorbidités). À l'admission, les chiens peuvent présenter des tableaux très variables, allant de formes subcliniques ou paucisymptomatiques à des présentations aiguës sévères marquées par une atteinte multiviscérale. À l'admission, ces tableaux cliniques conditionnent le pronostic immédiat et guident les premières décisions thérapeutiques. Toutefois, au-delà de la phase aiguë, la leptospirose peut avoir un devenir à long terme non négligeable. Certains animaux, bien que stabilisés après traitement, conservent des séquelles chroniques, notamment rénales (insuffisance rénale chronique secondaire à des lésions tubulo-interstitielles persistantes) ou hépatiques (fibrose, troubles fonctionnels résiduels). D'autres, au contraire, récupèrent complètement, du moins cliniquement, après une phase de convalescence plus ou moins prolongée. L'évolution dépend largement de la rapidité du diagnostic, de la mise en place d'un traitement de support intensif et de la sévérité des lésions initiales.
II. Quelques rappels brefs de physiopathologie
Chez le chien, la contamination est soit directe, au travers des muqueuses saines, d'une peau abrasée ou même saine, lors d'immersion longue, soit indirecte par voie transplacentaire, transmammaire, sexuelle ou par contact avec de l'urine infectée.
Puis par migration transendothéliale, le leptospire va rejoindre le torrent circulatoire et se disséminer dans l'organisme par voie hématogène, avec un tropisme plus important pour les reins et le foie. Cette phase bactériémique peut durer jusqu'à 7 jours. Les signes cliniques apparaissent lorsque le nombre de leptospires dans les différents tissus atteint un niveau « critique ». L'incubation dure de 4 à 14 jours. Les anticorps sont synthétisés à partir du 7è jour, entraînant une élimination des leptospires et une guérison clinique en l'absence de lésions tissulaires irréversibles. Concernant la bactériurie, on observe une persistance chronique des leptospires dans les tubules rénaux (sans doute plusieurs années) avec une excrétion dans les urines continue ou intermittente.
III. Manifestations cliniques aiguës
1. Une affection biphasique
De manière classique, la leptospirose est décrite comme une affection biphasique.
La phase initiale est une phase fébrile sans anomalie biochimique, avec des signes non spécifiques comme abattement, dysorexie, hyperthermie, vomissement et PUPD. Une leptospirose pouvant évoluer rapidement vers une IRA, elle doit être envisagée chez les chiens présentant un syndrome fébrile aigu, en particulier s'ils ne sont pas vaccinés contre la leptospirose. Une réévaluation clinique et des tests biochimiques sont recommandés si l'état de l'animal ne s'améliore pas dans les 24 heures. La réalisation d'une PCR est conseillée si l'incidence régionale de la leptospirose est élevée ou si les antécédents suggèrent la possibilité d'une leptospirose.
La seconde phase est celle de la défaillance multiorganique en lien avec la dissémination des leptospires et les complications (pneumonie par aspiration, pancréatite, translocations bactériennes intestinales, sepsis). Cette défaillance multiorganique peut être fatale.
2. L'atteinte rénale
Sur le plan physiopathologique, l'atteinte est dominée par une néphrite tubulo-interstitielle aiguë, associant infiltration inflammatoire, œdème interstitiel et nécrose tubulaire. Les lésions peuvent s'étendre vers une atteinte glomérulaire, par dépôts immuns ou par glomérulonéphrite secondaire, bien que ce soit plus rare. Les modifications histopathologiques sont responsables d'une altération de la fonction de filtration, de concentration et d'excrétion du rein. Cliniquement, cela se traduit par une IRA, qui peut être de type non oligurique, mais également oligo-anurique dans les formes les plus sévères.
Les signes cliniques sont souvent peu spécifiques au départ : abattement, anorexie, vomissements, diarrhée, polyuro-polydipsie. Rapidement, l'installation d'une azotémie et de troubles hydro-électrolytiques marque le stade d'insuffisance rénale. Les chiens peuvent présenter une déshydratation marquée, une halitose urémique, des ulcères buccaux, voire des troubles nerveux secondaires à l'encéphalopathie urémique. L'évolution peut être brutale, avec une aggravation rapide de l'état général dans les formes oligo-anuriques.
Les anomalies biologiques reflètent l'atteinte tubulo-interstitielle. On observe une élévation des paramètres azotés (urée, créatinine) ainsi qu'une hyperphosphatémie. L'hyperkaliémie est fréquente dans les formes oligo-anuriques et peut mettre en jeu le pronostic vital par ses conséquences cardiaques. L'hyponatrémie, l'hypochlorémie et l'acidose métabolique sont également courantes, en lien avec les pertes digestives et l'incapacité rénale à réabsorber correctement les électrolytes. L'examen urinaire met en évidence une isosthénurie ou hyposthénurie, une protéinurie de degré variable et souvent une cylindrurie et glycosurie, témoignant des lésions tubulaires. Une hématurie ou une leucocyturie peuvent être présentes en cas de néphrite active.
3. L'atteinte hépatique
Histologiquement, on décrit une hépatite aiguë nécrotique ou subaiguë, caractérisée par des foyers de nécrose hépatocytaire, une infiltration inflammatoire et, dans certains cas, des dépôts de pigments biliaires.
Cliniquement, l'atteinte hépatique se manifeste principalement par un ictère visible sur les muqueuses, conséquence d'une cholestase intra-hépatique et d'une destruction des hépatocytes. Les chiens présentent aussi anorexie, vomissements, abattement marqué, parfois douleurs abdominales. Dans les formes sévères, une encéphalopathie hépatique peut survenir, traduisant une incapacité du foie à détoxifier les substances circulantes.
Les anomalies biologiques incluent une élévation marquée des enzymes hépatiques et de la bilirubine totale. Une hypoalbuminémie et des troubles de la coagulation peuvent apparaître, conséquence de la diminution de la synthèse hépatique et de l'atteinte endothéliale. L'ictère constitue un signe d'alerte pronostique défavorable, surtout lorsqu'il est associé à une insuffisance rénale concomitante.
4. L'atteinte pulmonaire
Cette forme, également appelée LPHS (syndrome d'hémorragies pulmonaires liées à la leptospirose), bien que moins fréquente que les formes rénales et hépatiques, est redoutée en raison de sa gravité. Elle résulte de mécanismes complexes associant une atteinte directe de l'endothélium capillaire pulmonaire par les leptospires et une réaction inflammatoire exacerbée de l'hôte. Cette altération de la barrière alvéolo-capillaire favorise des fuites vasculaires massives, responsables d'hémorragies intra-alvéolaires diffuses. Cliniquement, les chiens présentent une détresse respiratoire aiguë, souvent brutale, marquée par une tachypnée, une dyspnée restrictive et parfois une toux hémoptoïque. L'évolution peut être fulminante, avec une hypoxémie sévère réfractaire aux mesures de support.
L'atteinte pulmonaire est associée à une mortalité élevée, car elle conduit rapidement à une hypoxémie sévère et à un syndrome de détresse respiratoire aiguë (SDRA).
5. L'atteinte hémostatique
Les formes hémostatiques résultent essentiellement de l'atteinte endothéliale généralisée induite par les leptospires, associée à une activation de la coagulation et à une consommation des facteurs de l'hémostase. La vascularite systémique provoque une augmentation de la perméabilité capillaire et favorise la survenue d'hémorragies spontanées. Cliniquement, ces formes se traduisent par des signes hémorragiques diffus : pétéchies et ecchymoses cutanées, épistaxis, hématémèse, hématurie ou encore hémorragies digestives et pulmonaires. Dans les cas les plus sévères, une coagulation intravasculaire disséminée peut se développer, combinant un état hémorragique et thrombotique à la fois, aggravant le pronostic vital. Les analyses biologiques révèlent alors une thrombocytopénie, un allongement des temps de coagulation, une diminution du fibrinogène et une élévation des produits de dégradation de la fibrine. Ces formes hémostatiques, bien que moins fréquentes que les atteintes rénales et hépatiques, constituent des complications redoutées car elles s'accompagnent souvent d'une évolution fulminante et sont responsables d'une mortalité élevée.
6. Les autres formes
Enfin, comme discuté précédemment, les atteintes organiques et les signes cliniques liés à la leptospirose sont divers et variés et sont directement liés à la pathophysiologie d'une leptospirose. De manière générale, une leptospirose pouvant se manifester par une vascularite, tout organe peut présenter une atteinte dans la théorie. Aussi, bien que les organismes présentent essentiellement un tropisme pour les reins et le système hépato-biliaire, l'inflammation et la vascularite liée à la présence des leptospires entraînent des signes variés à la fois respiratoire, oculaire, neurologique, pancréatique, dermatologique… Dans les faits, toute présentation clinique atypique pour laquelle des signes de vascularité, ou d'inflammation non spécifique sont visualisés pourrait bénéficier d'une recherche de leptospira en milieu endémique.
Une atteinte musculaire est parfois observée. Elle se traduit par une douleur diffuse, une démarche raide, une faiblesse généralisée et, biologiquement, par une augmentation des enzymes musculaires, notamment la créatine kinase. Cette myosite résulte probablement d'une vascularite locale et de l'action cytotoxique des leptospires sur les fibres musculaires.
Des manifestations gastro-intestinales isolées peuvent également dominer le tableau clinique : vomissements incoercibles, diarrhée parfois hémorragique, anorexie marquée et douleurs abdominales. Dans certains cas, ces signes précèdent ou masquent l'atteinte rénale et hépatique, ce qui peut retarder le diagnostic en orientant initialement vers des pathologies digestives primaires.
L'œil peut aussi être le siège de lésions, avec la survenue d'une uvéite antérieure ou postérieure, associée à une photophobie, un larmoiement et parfois une baisse de la vision. Cette atteinte oculaire est attribuée à une réaction immunitaire secondaire à la persistance de leptospires dans les tissus.
Les manifestations nerveuses constituent une autre présentation possible, bien que rare. Elles comprennent des tremblements, une ataxie, une hyperesthésie, voire des crises convulsives ou des troubles de la conscience. Ces signes peuvent être dus à une encéphalite ou à une méningite d'origine inflammatoire, mais aussi à des encéphalopathies métaboliques secondaires à l'insuffisance rénale ou hépatique.
IV. Les formes chroniques
Bien que la forme classique se présente souvent dans un contexte suraigu à aigu, un portage chronique voire possiblement asymptomatique a été décrit dans les zones endémiques. Aussi, une étude sur des chiens de refuge et de rue a montré la prévalence de portages chroniques (PCR positive pour Leptospira dans les urines) sur des chiens a priori sains à hauteur de 12-20 % de la population au Brésil. Ce portage sain de leptospires est de plus en plus suspecté responsable d'entraîner une maladie rénale chronique sur le long terme. En effet, une autre étude en zone endémique révèle que parmi les chiens ayant une maladie rénale chronique 75 % d'entre eux étaient porteurs de leptospires comparativement à des chiens sains (20 %).
Le portage chronique a également été associé à des hépatites chroniques granulomateuses sans atteinte rénale associée et pour lequel des méthodes de FISH ou PCR permettent la confirmation de leptospires dans les lésions.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Leptospirose : outils diagnostiques
Guyancourt, France
I. Introduction
La leptospirose est une maladie bactérienne zoonotique d'importance majeure en médecine vétérinaire et en santé publique. Chez le chien, elle est provoquée par différentes sérovars de Leptospira interrogans et se manifeste par un large spectre clinique, allant d'une atteinte subclinique à des formes graves responsables d'insuffisance hépatique et/ou rénale aiguë. En raison de la diversité des présentations cliniques et du chevauchement des signes avec d'autres affections infectieuses ou métaboliques, le diagnostic repose sur une combinaison d'outils complémentaires. Ceux-ci incluent les méthodes indirectes, basées sur la détection de la réponse immunitaire de l'animal (sérologie, tests rapides), et les méthodes directes, permettant d'identifier la bactérie ou son matériel génétique (culture, PCR, immunohistochimie). Chacun de ces outils présente des avantages et des limites en termes de sensibilité, de spécificité, de rapidité et de disponibilité, ce qui rend souvent nécessaire une approche diagnostique intégrée. Étant donné que tous les tests de diagnostic disponibles ont leurs limites, la réalisation d'une combinaison de tests sérologiques de détection indirecte (test de microagglutination ou immunochromatographiques rapides) et de détection directe des antigènes par PCR est recommandée pour optimiser le diagnostic de la leptospirose.
II. Les tests de laboratoire
1. La PCR
Afin d'optimiser la sensibilité diagnostique de la PCR, les échantillons doivent être prélevés avant l'administration d'antibiotiques. En effet, la PCR peut se négativer dans les 24 h qui suivent la mise en place du traitement. Il est important d'analyser des échantillons obtenus à partir de sang et d'urines. En post mortem, le rein et/ou le foie sont les organes à privilégier, la congélation n'interfère pas avec le test, en revanche les organes ne doivent pas être fixés. Une PCR positive sur sang est le signe d'une infection leptospirosique, alors qu'un résultat positif sur urines peut être éventuellement la conséquence d'un portage asymptomatique chez un chien à risque. Une vaccination même récente n'interfère pas avec la PCR car les vaccins ne contiennent pas de leptospires vivantes.
Un résultat positif d'une PCR sur sang associé à des signes cliniques cohérents, constitue un diagnostic de leptospirose. Cependant, la PCR sur sang n'est positive que dans 60% des cas de leptospirose, la bactériémie pouvant être de courte durée et/ou très faible chez certains chiens. Un résultat PCR négatif sur sang et dans une moindre mesure sur urine ne permet pas d'exclure la leptospirose, y compris sur des chiens non traités. L'ADN des leptospires pathogènes pouvant être trouvé dans l'urine de chiens apparemment sains, un résultat positif dans les urines doit être interprété en conjonction avec les signes cliniques et les résultats des autres tests.
2. Le test de microagglutination
Le test de microagglutination (MAT) détecte de façon indirecte la trace d'une infection par mise en évidence des anticorps. Il s'agit du test le plus documenté. Il est complexe et nécessite l'utilisation de cultures de leptospires pour produire les antigènes. Les résultats sont donnés par titre pour chaque sérogroupe. Ce test est considéré comme le Gold standard lors de mise en évidence d'une séroconversion (2 sérums prélevés à minimum 7 jours d'intervalle) avec une sensibilité proche de 100%, mais il manque de sensibilité en phase précoce (50%). Par ailleurs, il n'existe pas de valeurs seuils consensuelles pour établir une positivité ou une négativité. Le sérogroupe avec le titrage le plus élevé n'est pas forcément le sérogroupe infectant, notamment sur le premier sérum. Néanmoins, un titre supérieur à 800 pour un sérovar non vaccinal et supérieur à 1 600 pour un sérovar vaccinal est en faveur d'une infection leptospirosique.
L'interprétation est délicate, avec parfois des réactions croisées, et il est important de ne pas laisser les laboratoires dicter la conclusion. Il convient de savoir si l'animal est vacciné, avec quel vaccin (L2/L3/L4), s'il s'agit d'une primo-vaccination ou d'un rappel et quand (plus ou moins 12 mois), et si des signes cliniques compatibles sont présents.
La sérologie est non conclusive si on retrouve un profil vaccinal ou une réaction croisée (sérovar non vaccinal positif mais avec un titre en agglutination inférieur à 1/800) :
- L2 : sérogroupes Icterohaemorragiae et Canicola (sérovars canicola et copenhageni)
- L3 : sérogroupes Icterohaemorragiae, Canicola et Grippotyphosa
- L4 : sérogroupes Icterohaemorragiae, Canicola, Grippotyphosa et Australis (sérovar bratislava)
La vaccination peut modifier les titres en anticorps mais elle n'a en général pas d'impact sur la séroconversion (titre au moins multiplié par 4).
La mise en place d'une antibiothérapie a un impact modéré sur les titres sériques.
En cas de sérologie négative ou non conclusive, soit il n'y a pas d'infection, soit l'infection est présente mais il n'y a pas de réponse en anticorps car l'examen est trop précoce. Il convient de renouveler la sérologie 7 jours plus tard : la séroconversion est mise en évidence lorsque les titres initiaux ont au minimum quadruplé.
Ainsi, une leptospirose ne doit pas être diagnostiquée seulement sur un résultat sérologique positif, ni être exclue seulement sur la base d'un test négatif, en particulier lorsque la MAT ne comprend qu'un nombre limité de sérovars (moins de 7). Bien que la séroconversion puisse survenir dès 3-5 jours après l'admission du chien, un intervalle de 7 à 14 jours est recommandé entre les échantillons de phase aiguë et de convalescence pour identifier la séroconversion.
III. Les tests rapides
Le test Witness® Lepto (ZOETIS) détecte des anticorps IgM spécifiques de nombreux antigènes de Leptospira dérivés d'extraits de cellules entières filtrés des sérovars Grippotyphosa et Bratislava. Le test SNAP® Lepto (IDEXX) détecte lui des anticorps dirigés contre les antigènes Lip32 par Elisa (IgM et IgG). Attention à l'influence de la vaccination sur la positivité des résultats : près de 80% de faux positifs sont détectés si le test est réalisé 4 semaines après une vaccination, et près d'un quart après un délai d'un an (Figure 1).
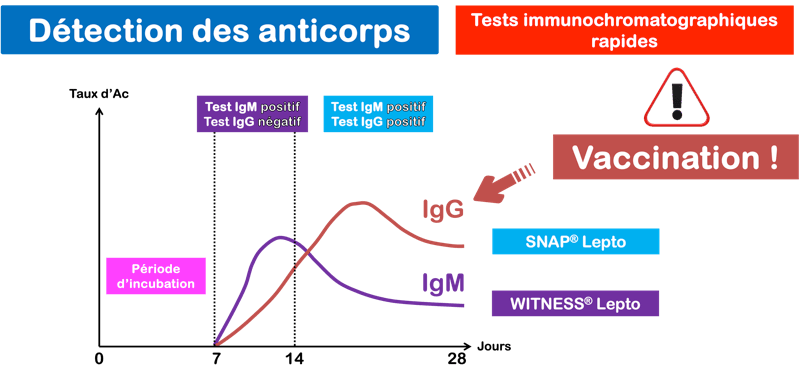
Figure 1
La sensibilité et spécificité des tests est respectivement comprise entre 68-79% et 72-85% pour le SNAP® Lepto et entre 71-76% et 98-100% pour le Witness® Lepto. C'est pourquoi d'avantages d'études de validation sont nécessaires dans différentes régions géographiques (USA, Europe…) avant que ces tests puissent être recommandés à la place de la MAT pour le diagnostic de la leptospirose.
En cas de test positif, la quantification du titre par MAT est recommandée. Un résultat négatif n'exclut pas la leptospirose et doit être suivi d'un deuxième test, 7 à 14 jours plus tard, pour documenter la séroconversion.
IV. Définition d'un cas de leptospirose
Un cas probable répond aux critères cliniques et à au moins un critère biologique spécifique en faveur :
- Titre sérologique supérieur ou égal à 800 dans au moins un échantillon de sérum
- Détection d'anticorps IgM dans un échantillon sérique en phase aiguë
- PCR sur urines positive
- Visualisation de spirochètes dans un échantillon de sang ou d'urine par microscopie sur fond noir par un laboratoire de référence.
Un cas confirmé répond aux critères cliniques et à au moins un critère biologique spécifique de confirmation :
- Séroconversion avec augmentation d'au moins 4 fois des titres MAT dans le même laboratoire
- PCR sur sang positive
- Isolement de Leptospira à partir d'un échantillon tissulaire par un laboratoire de référence.
Les tests diagnostiques doivent être effectués chez les chiens qui répondent aux critères cliniques. Bien que des antécédents d'exposition potentielle (prédation, exposition à d'autres espèces animales ou sources d'eau) devraient accroître la suspicion de leptospirose, tous les chiens doivent être considérés comme à risque, quels que soient leur signalement, leur région géographique et leur mode de vie.
Bibliographie
Références sur demande
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Leptospirose et insuffisance rénale aigue - Comment la prendre en charge ?
Guyancourt, France
I. Introduction
La leptospirose est une zoonose ré-émergente de répartition mondiale affectant de nombreuses espèces de mammifères. Chez le chien, elle est à l'origine d'un tableau clinique protéiforme dont l'intensité des signes est variable et peut s'exprimer d'un « simple » syndrome fébrile jusqu'à un syndrome de défaillance multiorganique. Le taux de mortalité rapporté chez le chien varie entre 17 et 52,5%. Ces différences de mortalité s'expliquent par une expression clinique plus grave en Europe (syndrome d'hémorragies pulmonaires associé à la leptospirose, intussusceptions, mucocèles biliaires…) qu'en Amérique du Nord, probablement à cause de l'émergence de nouveaux sérogroupes dont Australis. La prise en charge médicale de cette affection repose sur le traitement de la cause sous-jacente, l'antibiothérapie, mais également sur toutes les mesures de soutien des grandes fonctions vitales altérées par cette maladie, notamment le soutien de la fonction rénale comme détaillé dans ce document.
II. L'antibiothérapie
Étant donné la morbidité marquée et la mortalité potentielle de la maladie, ainsi que le risque de transmission zoonotique, comme le recommande le Centre de contrôle des maladies pour l'Homme, les chiens suspects ou atteints de leptospirose doivent être traités avec une antibiothérapie appropriée.
Le traitement ne doit pas être retardé en attendant les résultats des tests diagnostiques. La durée optimale de l'antibiothérapie nécessite des recherches plus approfondies.
Les chiens doivent être traités à l'aide de doxycycline à la dose de 5 mg/kg PO toutes les 12 heures pendant 2 semaines. L'absence de présentation IV et la mauvaise tolérance digestive représentent un frein à l'usage de cet antibiotique. Si des vomissements ou d'autres effets indésirables empêchent l'administration de doxycycline, les chiens doivent être traités initialement par de l'ampicilline (20-30 mg/kg IV, toutes les 6-8h), de l'amoxicilline (20-30 mg/kg IV, toutes les 6-8h) ou de la pénicilline G (25 000-40 000 U/kg IV toutes les 6-8h), mais leur utilisation IV est hors AMM. Ces doses élevées et plus fréquentes permettent de maintenir leur concentration plasmatique au-dessus de la concentration minimale inhibitrice (CMI) le plus longtemps possible, surtout en association à une fluidothérapie. Pour les pénicillines, le panel d'experts du consensus américain 2024 recommande de doubler l'intervalle d'administration chez les chiens IRIS 4 (créatininémie > 50 mg/L).
Il convient de rappeler que les leptospires sont parfaitement sensibles à ces antibiotiques et qu'aucun facteur de résistance n'a été pour le moment identifié. Les autres antibiotiques (et notamment les fluoroquinolones) ne sont pas recommandés lors de leptospirose chez le Chien.
III. Le soutien de la fonction rénale
L'objectif du traitement est de maintenir le débit sanguin rénal et le débit de filtration glomérulaire, de rétablir l'homéostasie électrolytique et acidobasique et de traiter la cause et les signes cliniques. La clé du succès de la prise en charge de l'IRA sera le monitorage en quantifiant la diurèse en mettant une sonde urinaire à demeure reliée à une poche urinaire ou en recueillant avec précaution les urines émises. On parle d'oligurie et d'anurie si elle est respectivement inférieure à 0,3 ml/kg/h et 0,08 ml/kg/h. L'évaluation de la diurèse sera réalisée au moins trois fois par jour.
1. La fluidothérapie
Les apports hydriques doivent toujours être supérieurs aux pertes. La restauration de la volémie fait appel à un soluté cristalloïde isotonique (Ringer lactate) par voie intraveineuse, par bolus de 10 ml/kg sur 5 minutes, renouvelable jusqu'à trois fois ; en l'absence de réponse, le recours aux vasopresseurs sera nécessaire. Puis il convient d'élaborer un plan de perfusion qui comprend la correction de la déshydratation extracellulaire ( % de déshydratation x 10 x PV) et des pertes hydriques (vomissements, diarrhée…), en plus des besoins d'entretien (2 ml/kg/h).
Chez un chien normohydraté qui s'abreuve, le rythme de fluidothérapie est égal à la diurèse + 1 ml/kg/h, tandis qu'il est égal à la diurèse + 2 à 4 ml/kg/h chez un chien déshydraté qui ne s'abreuve pas.
En cas d'anurie, la fluidothérapie est délétère et potentiellement fatale à cause du risque de surcharge volumique dont les signes cliniques sont un bruit de galop, une turgescence veineuse, un pouls jugulaire rétrograde, une hyperélasticité cutanée, des œdèmes en partie déclive, un souffle cardiaque, une tachypnée et une dyspnée lors d'OAP. En revanche un protocole de diurèse forcée est instauré à l'aide de furosémide (6-8 mg/kg IV) ou de mannitol 20% (0,5-1,5 g/kg IV sur 15 à 30 minutes) ou par des techniques d'épuration extrarénale (hémodialyse, hémofiltration, hémodiafiltration).
2. Les techniques d'épuration extrarénale (EER)
Ces techniques sont indiquées lors d'oligo-anurie ne répondant pas au protocole de diurèse forcée, d'hyperkaliémie ne répondant pas au traitement antikaliémiant classique, en absence de diminution des paramètres rénaux après 12-24 heures de fluidothérapie à un rythme approprié ou lors de surcharge volumique ne répondant pas au traitement diurétique.
Elles ne doivent pas être considérées comme des techniques de dernière chance ! Au contraire, le recours précoce aux techniques d'EER est recommandé pour prévenir la morbidité de l'IRA plutôt que comme un sauvetage retardé en cas d'échec de la prise en charge conventionnelle. Une orientation précoce vers des centres de référés réalisant l'ERR doit être envisagée pour les chiens IRIS 4, lorsque la créatininémie dépasse 50 mg/L (soit 440 µmol/L). Il s'agit d'un traitement palliatif en attendant le succès du traitement étiologique et donc la reprise d'une diurèse et d'une fonction rénale presque normale.
3. Le traitement des complications
a) Le traitement de l'hypertension artérielle
La pression artérielle doit être mesurée au moins deux fois par jour au cours de la phase initiale de la maladie et l'hypertension persistante, ne répondant pas à une analgésie appropriée et à une correction volémique, doit être traitée à l'aide d'amlodipine (0,25 à 0,7 mg/kg/j PO).
b) Le traitement de l'hyperkaliémie
L'hyperkaliémie doit être corrigée en raison de sa cardiotoxicité (ondes T pointues, aplatissement des ondes P, élargissement des QRS, allongement PR, bradycardie, tachycardie ventriculaire asystolie). Compte tenu de l'absence de corrélation entre la valeur de la kaliémie et les anomalies relevées sur l'ECG, il convient de toujours réaliser un ECG lors d'hyperkaliémie.
Un traitement est mis en place lors de kaliémie supérieure à 8 mmol/L et dès la présence d'une anomalie à l'ECG (incluant la bradycardie) quelle que soit la valeur de la kaliémie. Cela consiste à :
- rétablir l'électophysiologie cardiaque grâce aux sels de calcium en restaurant le potentiel de repos. Le gluconate de calcium à 10% est injecté à 0,5-1 ml/kg en IV lente sur 10-15 minutes ; son efficacité est immédiate pendant 30 à 60 minutes. Cependant, les sels de calcium ne diminuent pas la kaliémie !
- favoriser la translocation intracellulaire de potassium en agissant sur la pompe Na/K ATPase. Le protocole insuline/glucose (Actrapid à 0,125-0,25 UI/kg et 2 g de glucose 30% par UI d'Actrapid) est efficace en 15-30 minutes et dure pendant 4-6 heures. En raison du risque d'hypoglycémie, il est nécessaire de surveiller la glycémie toutes les 30 minutes pendant 6 heures. Dans les cas moins graves, une perfusion complémentée à 5% de glucose (ajout de 83 ml de glucose 30% dans une poche de 500 ml de soluté cristalloïde isotonique) est suffisante pour stimuler la synthèse d'insuline endogène. Il est important de ne pas perfuser du glucose 5% pur qui est un hypotonique ! On peut également utiliser les Beta2-agonistes : la terbutaline (0,01 mg/kg IV) ou le salbutamol inhalé (50 µg/dose en chambre d'inhalation pendant 15 cycles respiratoires) sont efficaces au bout de 20 à 40 minutes, mais leur durée d'action n'est pas connue. Enfin, le traitement à base de bicarbonates de sodium (1 à 2 mEq/kg en IV lente sur 15 minutes) est controversé et ne doit jamais être utilisé en monothérapie.
- éliminer le potassium en excès dans l'organisme seulement si la diurèse est conservée, par les diurétiques (furosémide à 1-2 mg/kg en IV, puis à 1 mg/kg/h IV en CRI).
c) Le traitement de l'acidémie
La lutte contre l'acidémie n'est à envisager que pour les cas les plus graves (pH < 7,1 et/ou [HCO3-] < 10 mmol/L) car la fluidothérapie est suffisante dans la grande majorité des cas pour diminuer progressivement l'acidémie et en raison de nombreuses complications (alcalose métabolique rebond, surcharge volumique par rétention hydrosodée, hypercapnie par inhibition des centres respiratoires, acidose intracellulaire paradoxale). Si les critères sont respectés, les bicarbonates de sodium sont utilisés à la dose de 0,5 à 2 mEq en IV sur 15 minutes, avec un contrôle immédiat de la gazométrie veineuse.
Bibliographie
Références sur demande.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Les affections hépatiques : l'imagerie et la cytologie, deux outils à relier à la clinique
Saint-Laurent du Var, France
Toulouse, France
I. Introduction, généralités
Dans un contexte clinique d'exploration de maladie hépatique, dans le cadre de la mise en évidence d'une enzymologie hépatique anormale ou lors d'un bilan d'extension, il est fréquemment indiqué de pratiquer une échographie abdominale.
L'échographie doit être réalisée de façon rigoureuse et intéresser tous les organes abdominaux. Lors de l'examen du foie en lui-même, on prête particulièrement attention à sa forme, sa taille, son échogénicité, son homogénéité, la présence d'anomalies diffuses ou focales, voire multifocales. On examine également les voies biliaires intrahépatiques, la vésicule, les voies biliaires extrahépatiques, et bien sûr les nœuds lymphatiques hépatiques.
Si l'ensemble des anomalies peut faire suspecter un processus pathologique, les images sont souvent peu spécifiques et des prélèvements peuvent être nécessaires.
La cytologie présente de nombreux avantages : exécution du prélèvement relativement simple et peu onéreuse, faible risque pour le patient et délais de réponse rapide. Mais sous certaines conditions.
1. D'abord, ne pas nuire
Les prélèvements cytologiques restent invasifs avec une possibilité de saignement, en particulier pour un foie « abîmé » ou une lésion focale. Il est alors important de vérifier a minima l'absence de thrombopénie (à l'aide de la réalisation d'un hémogramme et la lecture d'un frottis sanguin) ou un autre trouble de l'hémostase (à l'aide d'un bilan d'hémostase), et d'éviter de ponctionner au niveau d'une structure vasculaire (doppler). Les prélèvements de cavités liquidiennes au sein de masses sont d'une part souvent peu à non informatives cytologiquement, et d'autre part potentiellement dangereux pour le patient (par exemple risque d'hémoabdomen, péritonite…). Alternativement, le prélèvement d'un autre organe modifié tel que le nœud lymphatique de drainage peut présenter un intérêt diagnostique avec un risque plus faible de complications.
2. Lien avec le propriétaire
Il est important d'impliquer le propriétaire dans la décision du prélèvement, notamment pour lui faire admettre le risque, mais aussi sur le fait que la cytologie peut aider à comprendre le problème de l'animal - sans garantie quant à l'établissement d'un diagnostic lésionnel précis.
3. Bien cibler ses prélèvements : un lien indispensable entre imageur et cytologiste
Il est indispensable d'informer le cytologiste de l'ensemble des anomalies échographiques observées et du contexte clinique et biologique. Mais il est également primordial de l'informer sur l'endroit où a été effectué le prélèvement cytologique (au sein d'une lésion focale ou diffuse et , lorsque cela est envisageable, il peut être riche en information de réaliser un prélèvement de lésion focale et du parenchyme environnant échographiquement normal ou de plusieurs sites lors de lésion diffuse ). Lorsque des prélèvements cytologiques sont réalisés sur différents sites au niveau du parenchyme hépatique, il est indispensable de le mentionner et d'identifier précisément les prélèvements transmis pour analyse.
II. Un lien imageur/cytologiste en catalyse…
Comme pour tout examen complémentaire, pour que la cytologie soit utile à la démarche diagnostique, elle doit être réalisée dans un contexte pour lequel elle a un seuil de sensibilité élevé. L'utilité diagnostique de l'examen cytologique est très variable et intimement lié au processus lésionnel sous-jacent. La cytologie présente une bonne sensibilité pour certains processus tumoraux diffus ou focaux à multi-ocaux (ex : tumeur à cellules rondes, carcinomes primitifs ou métastatiques, ….). Elle peut aussi être un examen de choix (lorsqu'elle est envisageable) pour identifier certaines affections diffuses comme la lipidose hépatique féline, néanmoins le processus sous-jacent est souvent ailleurs et dans ce cas le processus hépatique est secondaire et la maladie éventuelle est à chercher ailleurs.
1. … mais avec des limites
L'imagerie peut faire état de masses focales, en particulier les adénomes/adénocarcinomes ou volumineux nodules d'hyperplasie (!), pouvant présenter des critères échographiques bénins ou évoquant au contraire une potentielle malignité (hétérogénéité, déformation des contours de l'organe, stéatite périphérique, adénopathie), mais avec une cytologie qui peut être discordante. L'examen cytologique est par ailleurs d'utilité diagnostique relativement faible pour l'exploration des lésions nodulaires uniques chez le chien. La distinction d'un nodule d'hyperplasie, d'un adénome ou hépatocarcinome hépatocellulaire pouvant s'avérer impossible d'un point de vue strictement cytologique en l'absence de critères de malignité morphologique évidents.
Alors à qui se fier ? Dans ce cas, l'histologie sera nécessaire pour trancher. De façon encore plus flagrante, la cytologie va présenter une faible utilité diagnostique pour des lésions inflammatoires, en particulier chronique, pour lesquelles l'histologie sera indispensable. En effet, l'examen histologique est souvent nécessaire pour avancer dans le diagnostic dans le cas d'exploration d'affections hépatiques inflammatoires (les prélèvements cytologiques ne permettant pas d'évaluer précisément la nature et la topographie des infiltrats inflammatoires de par l'absence d'information structurale sur les échantillons récoltés et la contamination sanguine souvent inévitable).
2. RAS à l'écho, je prélève quand même ?
Parfois, les images échographiques sont normales… C'est notamment possible lors d'infiltration tumorale diffuse à cellules rondes par un lymphome ou un mastocytome. Dans ces contextes, les cytoponctions peuvent débusquer des infiltrations malignes qui ne s'avouent pas échographiquement.
III. Lien avec la clinique
Si l'imagerie et la cytologie du foie sont des étapes souvent clés et quasiment incontournables, il reste néanmoins absolument nécessaire de corréler les résultats au contexte épidémio-clinique et biologique pour conclure ou envisager d'autres examens (ex : recherche d'agents infectieux (leptospirose, PIF..., T4, scanner, histologie…).
Autour de cas cliniques, nous aborderons ces points centraux des relations entre échographie et cytologie au cœur de l'exploration du foie.
Bibliographie
- COURTMAN, N., & QUILEZ, E. (2025). Cytologic Evaluation of the Liver. Veterinary Clinics: Small Animal Practice, 55(4), 539-558.
- MASSERDOTTI C. Canine and feline liver cytology. Wiley Blackwell. 2024, Hoboken, New Jersey.
- RASKIN RE, MEYER J.M, BOES K.M. Canine and feline cytology. A color atlas and interpretation guide. 4th edition. 2022, Elsevier.
- PENNINCK D, D'ANJOU M.-A., Atlas of small animal ultrasonography, 3rd edition, 2025.
- THRALL D, Thrall's textbook of diagnostic radiology, 8th edition, 2025.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Les dirofilarioses des carnivores domestiques en France métropolitaine et Outremer
Marseille France
La dirofilariose cardio-vasculaire, due au nématode Dirofilaria immitis, est connue chez le chien en France depuis le XVIIe siècle sans jamais avoir été éradiquée. La présence de filaires adultes dans le cœur peut rester asymptomatique. Le chien réservoir insoupçonné est ainsi à l’origine d’un foyer actif dès lors que le moustique vecteur pullule.
Du fait de l’extension constante de l’aire de répartition des Culicidés en France et de leur période d’activité, les dirofilarioses sont des parasitoses émergentes. Le diagnostic de laboratoire (examen microscopique directe du sang, test de Knott modifié, tests rapides, PCR) doit être mis en œuvre pour détecter les cas avant l’apparition de symptômes.
Les Wolbachia sont des bactéries endosymbiontes nécessaires à la croissance, au développement, à l’embryogénèse et à la survie des filaires. Depuis trente ans, elles sont la cible de traitements et du diagnostic PCR. Ainsi à l’IHU Méditerranée Infection, l’approche PCR multiplex combinée pour la détection des filaires et des Wolbachia est mise en œuvre avec une qPCR triplex ciblant D. immitis, D. repens et Acanthocheilonema reconditum et une qPCR duplex ciblant Wolbachia de D. immitis et D. repens. De plus, cette démarche est complétée par une qPCR duplex pour le diagnostic différentiel des vers du cœur (D. immitis et Angiostrongylus vasorum) et par des PCR pan-filariennes cox1 et pan-Wolbachia ftsZ pour identifier d'autres parasites filaires et leurs Wolbachia.
Nous prendrons des exemples d’études de foyers récents de dirofilarioses à D. immitis et à D. repens, en particulier, dans les Bouches-du-Rhône, l’Indre, les Pyrénées-Atlantiques, la Corse, le Var et l’Yonne. La prévalence (PCR) est de 2,3% chez 460 chiens de chenils du sud-est et de 0,8% chez 250 chiens militaires représentatifs des effectifs de l’armée. Elle est de 9% chez les chiens d’un an susceptibles d’être importés de Hongrie.
La prévalence de D. immitis est très élevée en France d’outre-mer (20% et plus). Nos enquêtes montrent que le moustique tigre (Aedes albopictus) présente un taux d’infection estimé allant jusqu’à 5% sur la Côte orientale de la Corse. Avec le réchauffement climatique, la fréquence des piqûres de moustiques va nécessairement augmenter ainsi que les cas de dirofilarioses cardio-vasculaires et cutanées, occultes et cliniques. Le dépistage sanguin régulier des chiens est conseillé de même que la combinaison de mesures de lutte contre les vecteurs et de chimioprévention parasitaire chez les chiens, potentiels réservoirs.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Les ichtyoses cutanées du Chien : diversité génétique et modèles animaux spontanés
Eric GUAGUÈRE , Catherine ANDRÉ
Les ichtyoses constituent un exemple majeur des troubles génétiques de la cornéogenèse chez le Chien.
Les ichtyoses désignent un groupe hétérogène des troubles génétiques de la cornéogenèse décrites dans diverses espèces (principalement l’Homme et le Chien). Ces génodermatoses monogéniques se caractérisent essentiellement par la présence de squames en grand nombre observées dans les premières semaines de la vie et par leur persistance pendant toute la vie.
Certaines d’entre elles sont dites « syndromiques », car associées à des signes non dermatologiques (Congenital keratoconjunctivitis sicca and ichthyosiform dermatosis du Cavalier King Charles (CKCSID)). Leur gravité est différente selon les races et leur réponse thérapeutique également variable.
Les ichtyoses résultent d’un défaut d’une ou de plusieurs étapes intervenant dans la différenciation de la couche cornée.
- Sur le plan physiopathologique, on peut distinguer les ichtyoses par prolifération des kératinocytes et les ichtyoses par rétention (par absence de desquamation).
- Sur le plan histopathologique, on peut distinguer les ichtyoses épidermolytiques caractérisées par une vacuolisation et une cytolyse des kératinocytes suprabasaux et les ichtyoses non épidermolytiques.
- Sur le plan génétique, dix gènes identifiés dans neuf races canines codent pour des kératines (KRT1, KRT10) ou des enzymes impliquées dans le compartiment lipidique, l'enveloppe cornée et la desquamation.
Certains gènes responsables d’ichtyoses (PNPLA1 et ASPRV1) ont été décrits d’abord chez le Chien avant de l’être chez l’Homme. D’une manière générale, certaines ichtyoses canines constituent d’excellents modèles spontanés animaux pour l’étude de ces génodermatoses chez l’Homme.
Les ichtyoses sont observées dans de nombreuses races mais leur prévalence au sein de celles-ci est mal connue. Les principales races concernées sont le Golden Retriever, le Jack Russell Terrier, le Bouledogue Américain, le Terrier du Norfolk, le Dogue Allemand, le Berger allemand, le Chihuahua et le Shar Pei. Chez le Cavalier King Charles, une ichtyose syndromique est décrite et est dénommée également keratoconjunctivitis sicca/ichthyosiform dermatosis. Des cas sporadiques d’ichtyoses épidermolytiques sont décrits chez un croisé Labrador Retriever et le Rhodesian Ridgeback (A.Hargis, communication personnelle) ; d’autres cas anecdotiques d'ichtyoses non-épidermolytiques sont signalés chez le West Highland White Terrier, le Soft Coated Wheaten Terrier, le Rottweiler, le Dobermann, le Manchester Terrier, l’American Staffordshire Terrier, le Yorkshire Terrier, le Colley, le Boxer, le Pékinois et quelques croisés… (la liste n’est pas limitative).
La plupart des ichtyoses décrites chez le chien possède un mode de transmission autosomique récessif (AR) ; la dénomination Autosomal Recessive Congenital Ichthyosis (ARCI) est désormais utilisée chez le chien, même si elles sont rarement congénitales. A ce jour, une seule ichtyose non épidermolytique décrite chez le Berger Allemand possède un mode de transmission autosomique dominant (AD).
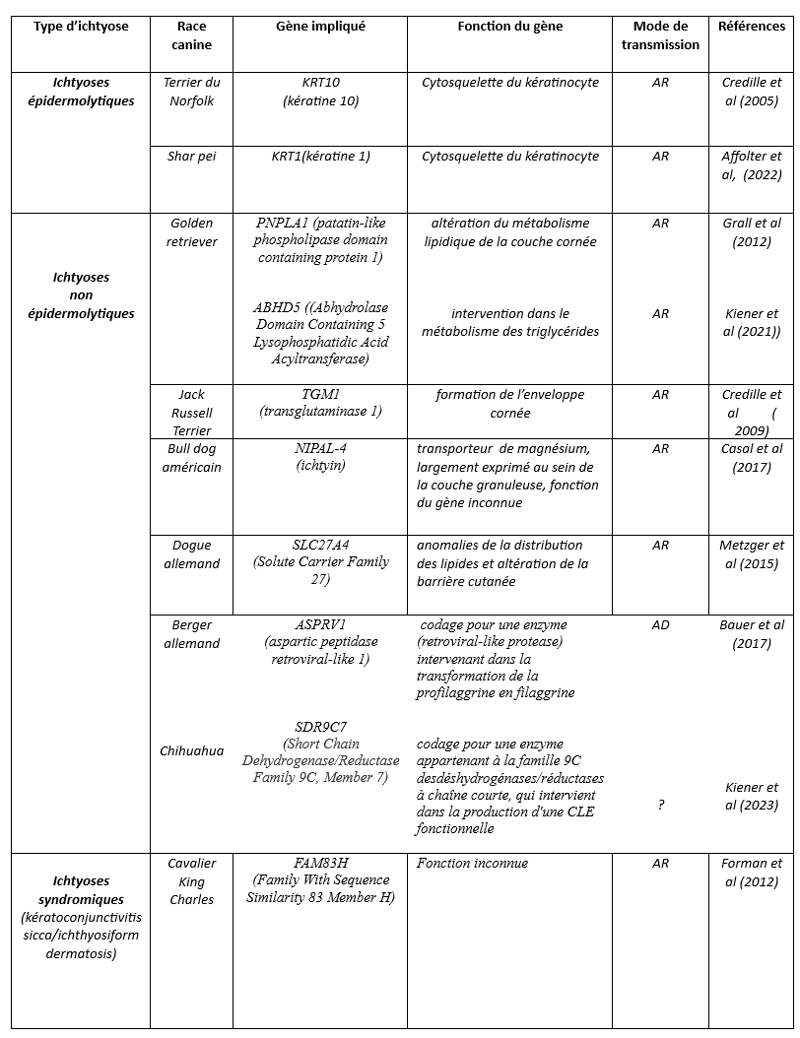
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Les lésions de la moelle osseuse affectent la majorité des grassets présentant une rupture du ligament croisé crânial chez le chien : étude prospective sur 51 chiens (87 grassets)
Mathieu JOURDAIN
Coauteurs : C. SARAZIN, M. FUSELLIER, De FOURMESTRAUX, P. MAITRE, O. GAUTHIER
Introduction
Les lésions de la moelle osseuse (LMO) sont des anomalies localisées dans l'os sous chondral et détectées à l'IRM, caractérisées par un hyposignal en T1 et un hypersignal en T2 et STIR, ayant des limites diffuses (LMO œdémateuse) ou bien définies (LMO kystique). Ces lésions sont bien décrites chez l'Homme, en particulier en cas de rupture du ligament croisé antérieur et sont associées à un développement d'arthrose précoce et à de la douleur. Chez le chien, bien que la RLCCr soit une affection orthopédique très fréquente, peu d'études se sont intéressées au développement des LMO. Les objectifs de cette étude sont de :
- déterminer l'incidence des LMO chez les chiens atteints de RLCCr ;
- déterminer les caractéristiques IRM (aspect, taille et localisation) ;
- évaluer s'il existe une association entre les lésions intra-articulaires et les caractéristiques des LMO.
Matériel et méthodes
Tous les chiens avec une suspicion de RLCCr, entre octobre 2022 et novembre 2023, ont été inclus prospectivement dans l'étude. La suspicion était basée sur le signalement et l'examen orthopédique (tests du tiroir direct et/ou indirect positif(s)). Les grassets avec un historique chirurgical ont été exclus.
Les chiens inclus ont subi une IRM sous anesthésie avec une technique standardisée (T1, T2 et STIR). L'analyse des images IRM, réalisée par un unique observateur, consistait en :
- une description de l'état du ligament croisé crânial : intact, partiellement ou complètement rompu ;
- une description des lésions méniscales et cartilagineuses (classement semi-quantitatif) ;
- une classification des LMO : aspect IRM (œdémateuse ou kystique), localisation dans les sites pré-définis (Figure 1) et taille (grade 1 : <25 % de la surface d'un site ; grade 2 : 25-50 % de la surface d'un site ; grade 3 : >50 % de la surface d'un site) [1] [2]
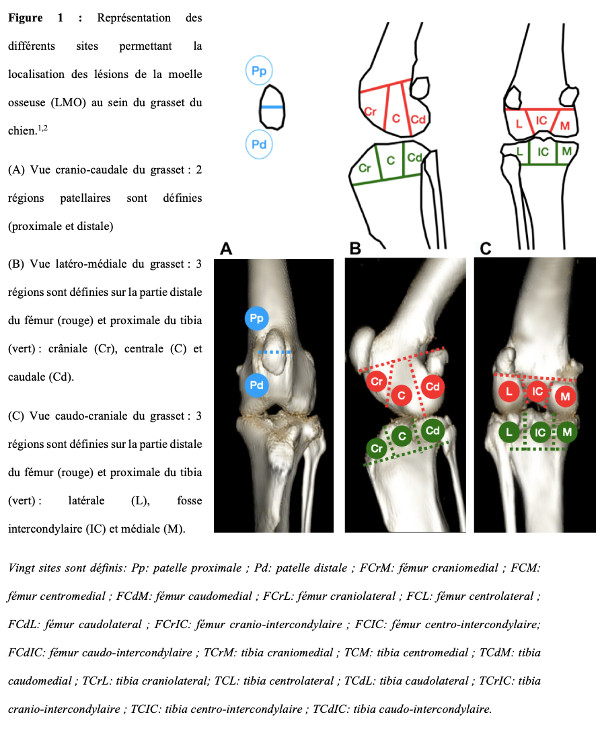
Figure 1
Après l'IRM, les grassets avec une RLCCr ont subi une arthrotomie médiale puis une TPLO. La classification IRM des lésions intra-articulaires a été comparée à celle de l'arthrotomie médiale.
Résultats
Sur les 51 chiens (87 grassets) inclus, les résultats sont: 51 grassets présentaient une RLCCr (rupture complète : 67 % (34/51) ; rupture partielle : 33 % (17/51)), avec une concordance de la classification IRM vs arthrotomie de 82 %. Des lésions méniscales ont été observées dans 63 % des grassets avec RLCCr (31/51), affectant la corne caudale du ménisque médial dans 72 % des cas, avec une concordance de la classification IRM vs arthrotomie de 86 %. Des lésions cartilagineuses ont été observées dans 20 % des grassets avec RLCCr (7/51).
Les grassets avec RLCCr étaient significativement plus affectés par les LMO que les grassets sans RLCCr (94 % (48/51) vs 56 % (20/36)). Parmi les grassets avec RLCCr, 40 % (19/48) présentaient uniquement des LMO œdémateuses, 6 % (3/48) uniquement des LMO kystiques et 54 % (26/48) les 2 types de LMO :
- LMO œdémateuses : le nombre médian de LMO par grasset était de 2, réparties équitablement entre le fémur et le tibia, avec la majorité des lésions (61 %) de grade 3. Ces lésions étaient significativement plus fréquentes dans les localisations FCIC, FCdL, FCdM, TCIC, TCdIC and TCdM (Figure 2) ;
- LMO kystiques : le nombre médian de LMO par grasset était de 1, majoritairement sur le fémur (60 % vs 40 % sur le tibia), avec 55 % des lésions de grade 1. Ces lésions étaient significativement plus fréquentes dans les localisations FCIC et TCrM (Figure 2).
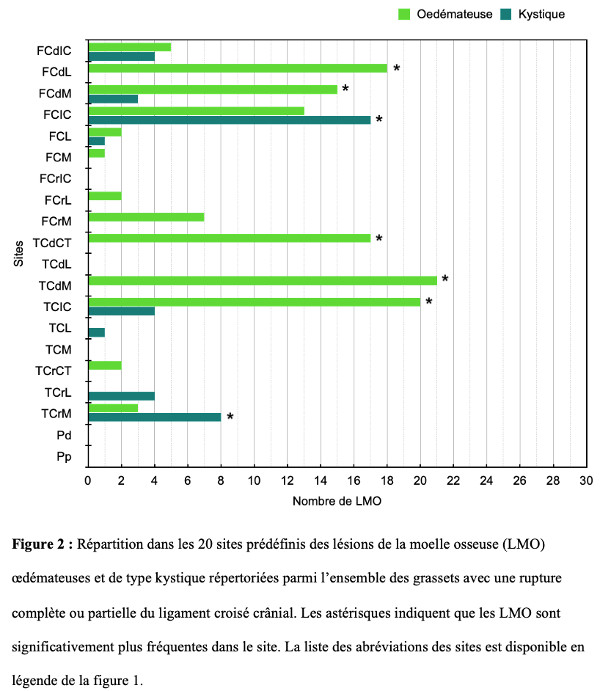
Figure 2
Une RLCCr partielle était significativement associée à des LMO de grade 1. Tous les grassets avec des lésions méniscales et/ou cartilagineuses avaient des LMO. La présence d'une lésion méniscale était significativement associée à une LMO œdémateuse de grade 3.
Parmi les grassets sans RLCCr, 20 % (5/20) présentaient uniquement des LMO œdémateuses, 70 % (14/20) uniquement des LMO kystiques et 5 % (1/20) les 2 types de LMO. La majorité des LMO œdémateuses et kystiques (63 % et 67 % respectivement) étaient de grade 1.
Discussion
Il s'agit de la première étude clinique prospective décrivant l'incidence des LMO incluant une large cohorte de chiens atteints de RLCCr. L'incidence des LMO parmi les grassets avec RLCCr concorde avec celle précédemment rapportée (entre 67 et 100 %) chez le chien [3-5]. Les LMO étaient surreprésentées dans les régions intercondylaires et caudomédiales fémorales et tibiales, ce qui concorde également aux localisations précédemment rapportées chez le chien [3-5]. Ces localisations correspondent aux sites d'insertion des ligaments croisés et aux régions adjacentes à la majorité des lésions méniscales.
La moitié des grassets sans RLCCr présentaient des LMO, ce qui peut correspondre à des lésions précoces et indicatrices d'une future RLCCr ou bien secondaires à une augmentation de la charge exercée sur ces grassets, dans le contexte d'une RLCCr controlatérale concomitante.
Conclusion
94 % des grassets avec une RLCCr présentent des LMO, particulièrement dans les régions intercondylaires et caudomédiales du tibia et du fémur. Leur impact clinique reste à établir.
Bibliographie
- PETERFY CG et al. Whole-Organ Magnetic Resonance Imaging Score (WORMS) of the knee in osteoarthritis. Osteoarthritis Cartilage. 2004;12(3):177-90
- D'ANJOU MA et al. Osteophytosis, subchondral bone sclerosis, joint effusion and soft tissue thickening in canine experimental stifle osteoarthritis: comparison between 1.5 T MRI and computed radiography. Vet Surg. 2008;37(2):166-77
- WINEGARDNER KR et al. Vet Rad 2007
- MARTIG S et al. Vet Rad 2007
- OLIVE J et al. VCOT 2014
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Les plantes, du producteur à la clinique : quels liens entre le laboratoire et le vétérinaire ?
Saint Denis
Le vétérinaire dispose aujourd'hui d'un grand choix de produits à base de plantes qu'il peut intégrer à sa pratique quotidienne, dont les statuts sont variables (médicaments, matières premières à usage pharmaceutique, aliments complémentaires...). Le laboratoire fournisseur est théoriquement le garant de produits de qualité, avec un approvisionnement correct en matières premières, l’emploi de procédés de fabrication maitrisés et reproductibles, l'élaboration de formules interprétables et raisonnées, afin d’offrir un produit fini assurant un rapport bénéfice / risque correct. Des différences ou des dysfonctionnement notables peuvent cependant être observés en pratique, le statut de la matière première et du produit constituant un facteur important dans cet état de fait.
Les objectifs de cette intervention sont de procurer des éléments pratiques d’évaluation du bien-fondé des produits finis et du sérieux des laboratoires, de clarifier les éléments taxonomiques, les dénominations usuelles des ingrédients ainsi que la précision de la définition des préparations et des formules pour les produits à base de plantes et d’huiles essentielles, dans une optique de prescription et de conseil sûrs et rationnels. Un rappel des concepts principaux, des définitions des substances actives employées (définies ou non à la pharmacopée) ainsi qu’un aperçu des référentiels existant seront proposés (accès, organisation, exploitation). Des rappels réglementaires seront effectués. Des exemples viendront illustrer les problématiques usuellement rencontrées sur le marché des produits de santé à base de plantes. La problématique des fraudes et des adultérations sera abordée, avec des données de la littérature récente.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Les troubles de la communication : comment garder le lien avec un animal agressif ?
Cabrières-d'Avignon, France
I. Introduction
Morsures et agressivité sont parmi les principales causes de rupture du lien homme–chien. Lorsque le lien est rompu, l'issue est souvent radicale : abandon ou euthanasie de l'animal. Pour le propriétaire, l'expérience d'une morsure est fréquemment vécue comme une trahison. Elle bouleverse la confiance dans le chien et constitue une voie sans issue. Pour le vétérinaire, entreprendre une prise en charge constitue une option possible, souvent ignorée par les propriétaire pour lequel le ressenti inhibe souvent toute motivation à entreprendre une prise en charge. Pour le vétérinaire, renoncer avant d'avoir tout tenté peut également être difficile à accepter, d'autant que la violence d'un acte agressif ne reflète pas toujours son niveau réel de dangerosité. La question n'est pas de minimiser la gravité de l'agression, mais de s'assurer qu'aucune décision ne soit prise sans avoir exploré l'option de la prise en charge vétérinaire de l'agression, afin de limiter le poids de la culpabilité.
L'objet de ce travail n'est pas de détailler le diagnostic différentiel des agressions, ni de proposer des protocoles thérapeutiques. Ces démarches relèvent de la consultation spécialisée, non de la gestion de la situation au cours d'une consultation généraliste. L'enjeu se situe en amont : comment convaincre un propriétaire, souvent épuisé et désabusé, d'accepter cette démarche de prise en charge, qui demande du temps, des ressources financières, une énergie émotionnelle et une gestion quotidienne du risque ? En d'autres termes, comment restaurer une motivation suffisante pour que la relation ne soit pas définitivement rompue ?
II. Le vécu du propriétaire : trahison, incompréhension et culpabilité
Lorsqu'un chien agresse, deux positions dominent chez le propriétaire. La première est celle de la victime : « pourquoi m'a-t-il fait ça ? », sentiment d'injustice et de souffrance face à un acte jugé intentionnel. La seconde est celle de la culpabilisation : « j'ai raté quelque chose dans son éducation ». Par ailleurs, le même chien peut rester affectueux et proche dans d'autres contextes, créant une dissonance qui brouille encore davantage la perception pour les premiers et alimentant le sentiment de culpabilisation pour les seconds. Dans les deux cas, le propriétaire désigne un coupable et l'émotion ressentie domine la réflexion. L'agression est interprétée comme un acte volontaire, ce qui renforce la perte de confiance envers ce chien de « mauvaise » compagnie, ou envers ses propres capacités, faisant de soi un probable « mauvais » maître. Dans cette dernière situation, l'entourage constitue souvent un facteur aggravant, fustigeant la permissivité ou l'absence de compétence communicationnelle des maîtres.
Le danger pour l'animal est qu'il perde progressivement ses « atouts relationnels » et que les conséquences négatives de ses comportements dépassent les bénéfices affectifs. Restaurer une compréhension plus nuancée de la situation est donc essentiel pour redonner une chance à la relation. [1]
III. La posture du vétérinaire : écouter, accueillir, reformuler
La première étape consiste à laisser le propriétaire exprimer son vécu. Le récit subjectif permet d'évaluer l'intensité de la souffrance et de repérer les éléments qui maintiennent encore le lien (souvenirs positifs, affection persistante). L'écoute empathique soulage, tout en fournissant des informations cliniques précieuses, en particulier sur les représentations du propriétaire, mais aussi sur les solutions déjà mises en place. Une vigilance particulière concernera l'emploi éventuel de méthodes coercitives, qui, outre leur impact négatif sur le bien-être animal, constituent toujours un facteur aggravant sur le moyen et le long-terme.
À ce stade, le vétérinaire agit comme un médiateur. Il recueille la douleur, puis introduit progressivement une autre lecture des faits, complètement nouvelle : celle d'une affection comportementale du chien. Le but est de montrer que l'agression n'est pas une trahison ni une volonté de nuire, mais une expression d'émotions ou de difficultés de régulation qui relative la responsabilité du chien et du maître dans la survenue des événements. L'émergence de cette troisième option permet de déculpabiliser le maître et/ou déresponsabiliser l'animal et peut conduire à la levée des blocages à la prise en charge.
IV. Changer les représentations : donner du sens au comportement
Sortir de la logique du « chien méchant » ou du « maître incompétent » suppose d'apporter des éléments cliniques simples, immédiatement compréhensibles. Une solution consiste à s'appuyer sur quatre grands axes fonctionnels qui structurent la sémiologie des troubles comportementaux [2] :
a) la peur
Souvent dirigée vers des visiteurs, livreurs, ou même le propriétaire lorsqu'il contraint le chien à sortir d'une cachette où il s'était réfugié. Les réactions de peur sont brutales et imprévisibles et s'il y a morsure, elle est souvent vulnérante. Cependant, le contexte de peur apparaissant de façon évidente, les maîtres comprennent aisément que leur animal ait pu réagir par vulnérabilité. L'explication génère spontanément de l'empathie : l'objectif n'est plus de sanctionner mais de réduire la peur [1] ;
b) les déficits d'autocontrôles
Ces chiens sont exubérants, impulsifs, brutaux mais hyper-affectueux. Les morsures apparaissent lors de phases d'excitation intense ou de frustration, avec souvent un regain à la puberté. Le problème n'émerge pas « d'un coup » mais s'inscrit dans un profil polyproblématique (désobéissance, hyperexcitabilité depuis l'acquisition). Ici, l'agression n'est pas préméditée mais correspond à une perte de contrôle émotionnel. Expliquer qu'il s'agit d'un déficit neuro-développemental plutôt que d'une « méchanceté » favorise une relecture bienveillante [4] ;
c) les troubles de la relation et de la gouvernance
Certains chiens s'impliquent de manière excessive dans la régulation du groupe familial. Ils contrôlent les interactions, défendent les ressources ou imposent leur lecture du fonctionnement d'un groupe à leur famille humaine. Les propriétaires interprètent cela comme de la dominance. Le rôle du vétérinaire est de souligner la charge mentale excessive que le chien s'impose, et de replacer la problématique comme la conséquence d'une pulsion contrôlante virant à l'obsession [2], souvent aggravée par des contresens éthologiques (cf point suivant) ;
d) les défauts de communication
Accès au couchage, nourriture, interactions verbales violentes ou incohérentes : autant de situations où les codes humains heurtent la logique canine. Ces erreurs de communication augmentent le risque de conflits et alimentent le cycle agressif.
Ces quatre axes ne constituent pas un diagnostic différentiel, mais offrent des points d'accroche pour modifier la représentation du maître. L'agression apparaît alors comme le symptôme d'une difficulté relationnelle, conséquence d'une affection comportementale, et non comme une intention délibérée du chien ou une incompétence du maître. À noter que chacune des possibilités développées supra est indépendante des autres et qu'elles peuvent se cumuler entre elles, ce qui peut complexifier le tableau clinique et nécessite une prise en charge individuelle adaptée.
V. Redonner envie d'agir : la motivation comme enjeu central
Pour que le propriétaire accepte une consultation spécialisée, il faut lever ses résistances. Les arguments motivants s'appuient sur trois piliers :
- ce n'est pas de la méchanceté : replacer le comportement dans la dynamique d'un trouble fonctionnel (émotion, auto-contrôles, fonctions exécutives ou communication)
- il y a des solutions : montrer que des actions concrètes de sauvegarde et de prise en charge existent, même si elles sont exigeantes (des conseils de sécurisation des situations exposées seront systématiquement proposés) ;
- vous n'êtes pas seul : souligner le rôle de l'équipe vétérinaire comme accompagnant, et non comme juge.
Ainsi, le propriétaire peut passer d'une position de victime ou de coupable à celle de partenaire engagé dans un processus de soin.
VI. Conclusion
Les agressions canines constituent l'un des motifs les plus fréquents de rupture du lien homme–animal. Pour le vétérinaire, l'enjeu est double : protéger les personnes et éviter que la décision d'abandon ou d'euthanasie ne soit prise sous le coup de l'émotion. Restaurer la motivation des propriétaires suppose d'abord une écoute empathique, puis un travail de reformulation qui déculpabilise l'animal et le maître.
En s'appuyant sur des axes cliniques simples (peur, autocontrôles, relation, communication), il devient possible de transformer la représentation de l'agression. Loin d'être une trahison, elle apparaît comme le symptôme d'un déséquilibre émotionnel, relationnel ou contextuel. Ce changement de regard permet de redonner une valeur au lien et d'ouvrir la porte à une consultation spécialisée, tout en recentrant la problématique sur la dimension médicale du comportement, dans le giron des compétences du vétérinaire.
La mission du psychiatre vétérinaire n'est pas seulement d'apporter un traitement, mais aussi de maintenir vivante la relation entre un animal et son propriétaire, même dans les moments de crise. C'est cette alliance qui conditionne, in fine, les chances de réhabilitation et de préservation du lien homme–chien.
Bibliographie
- OVERALL KL. Manual of Clinical Behavioral Medicine for Dogs and Cats. St. Louis: Elsevier; 2013.
- MASSON S et coll. Psychiatrie vétérinaire du chien. NoLedge Editions; 2023.
- CASEY RA et coll. Human directed aggression in domestic dogs (Canis familiaris): Occurrence in different contexts and risk factors. Appl Anim Behav Sci. 2014;152:52-63.
- MCPEAKE KJ et coll. The Canine Frustration Questionnaire—Development of a new psychometric tool for measuring frustration in domestic dogs (Canis familiaris). Front Vet Sci. 2019;6:152.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Les troubles liés à la séparation : comment garder le lien quand on retrouve son appartement dévasté ?
Paris, France
Face aux destructions liées à une séparation, beaucoup de propriétaires perdent patience et malgré la douleur et la culpabilité qu'ils éprouvent, préfèrent se séparer de leur chien et par conséquence rompre la relation qui les liait à leur chien. En effet, dans les causes d'abandon, les troubles du comportement liés à la séparation sont les deuxièmes les plus fréquents. Ainsi la visite chez le vétérinaire peut être la dernière étape avant l'abandon ou le replacement (Palestrini, 2010). L'analyse de l'origine de ses destructions devrait permettre leur résolution via une thérapie comportementale solide et l'usage de psychotropes efficaces.
Les destructions font partie des comportements associés à l'anxiété de séparation ou encore appelée troubles liés à la séparation. Une salivation abondante, des halètements, des vocalisations (gémissements, aboiements, hurlements), mais aussi des malpropretés urinaires et fécales sont rapportées. L'ensemble de ces comportements sont décrits lors de stress chronique ou intense (Beerda, 2000).
Canis familiaris est une espèce sociale, pour laquelle l'isolement est un défi (Beerda, 2000) et un facteur de stress. Les individus sensibles aux modifications d'environnement vont être prompt à manifester les comportements de stress intense lors d'isolement (Ogata, 2016).
Mais il est important d'ajouter que la frustration a aussi pour base physiologique une augmentation du cortisol (Dantzer, 1980). Les chiens frustrés d'être enfermés, de ne pas pouvoir sortir, de voir partir leur maitre, s'exprimeraient avec des signes similaires à ceux du stress. L'analyse du budget d'activité et du tempérament du chien doivent ainsi absolument être incluses dans les recueils des commémoratifs des troubles liés à l'isolement pour différencier ceux liés au stress et ceux liés à la frustration.
Afin de reconstruire le lien, il est nécessaire d'établir une thérapie comportementale qui permettra à la fois de satisfaire les besoins comportementaux du chien et l'apprentissage d'isolements de courte à moyenne durée. L'usage de psychotropes est fondamental, puisque sans eux la thérapie comportementale ne peut simplement pas être mise en œuvre (Korpivaraa, 2022).
La prise en charge d'un chien présentant des comportements de destructions en l'absence de ces propriétaires peut sembler simple mais les modifications de l'environnement de l'animal et de sa relation avec les humains qui l'entourent sont finalement complexes et nécessite un engagement important du praticien.
Bibliographie
- OGATA N. Separation anxiety in dogs: what progress has been made in our understanding of the most common behavioral problems in dogs? J Vet Behav. 2016;16:28–35
- PALESTRINI C, MINERO M, CANNAS S, ROSSI E, FRANK D. (2010) Video analysis of dogs with separation-related behaviours. Appl Anim Behav Sci;124(1–2):61–67
- BEERDA B, SCHILDER M. B. H., VAN HOOFF J. A. R. A. M., DE VRIES H. W.& MOL J. A. (2000) Behavioural and hormonal indicators of enduring environmental stress in dogs. Animal Welfare 9, 49–62
- DANTZER R, ARNONE M, MORMEDE P. (1980) Effects of frustration on behaviour and plasma corticosteroid levels in pigs. Physiol. Behav. 24(1) 1--4, 198
- KORPIVAARA M, MIRJA HUHTINE M, POHJANJOUSI P, OVERALL K, (2022) Tasipimidine, a novel orally administered alpha-2 adrenoceptor agonist, alleviates canine acute anxiety associated with owner departure—A pilot study. Jour of vet behav. 58,54-61. https://doi.org/10.1016/j.jveb.2022.11.003
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Les tumeurs pulmonaires primitives du chat : une étude rétrospective des caractéristiques épidémio-cliniques et tomodensitométriques sur 34 cas, recrutement multicentrique entre 2013 et 2024
Victoria LUX
Coauteurs : P. DE FORNEL, J. MORTIER, M. CANONNE-GUIBERT
Introduction
Les tumeurs pulmonaires primitives félines constituent une entité pathologique rare, associée à une présentation clinique souvent discrète, voire non spécifique, et dont la confirmation diagnostique peut s'avérer délicate. Dans de nombreux cas, la découverte de ces tumeurs est fortuite, au détour d'examens d'imagerie réalisés pour d'autres motifs cliniques. À ce jour, leur caractérisation tomodensitométrique repose essentiellement sur l'étude d'AARSVOLD et al. (2015), qui rapporte majoritairement des masses localisées dans les lobes caudaux. Toutefois, cette étude mentionne sans les détailler deux cas à présentation diffuse, alors même que d'autres travaux suggèrent une prévalence plus élevée de ce type de tumeurs (SANTOS et al., 2023).
Ce travail vise à compléter nos connaissances quant à l'aspect tomodensitométriques des tumeurs pulmonaires félines, en s'attachant à décrire des formes jusqu'ici peu documentées.
Matériel et méthodes
Une étude rétrospective multicentrique a été conduite sur 10 ans, incluant 34 cas de chats atteints de tumeurs pulmonaires primitives confirmées par examen histologique ou cytologique. Un examen tomodensitométrique thoracique était disponible pour tous les cas recrutés. Les chats présentant une tumeur d'aspect nodulaire (majoritairement des adénocarcinomes) ont constitué un premier groupe, tandis que les chats présentant des lésions diffuses ou multifocales (6 cas) ont été décrits isolément.
Résultats
L'âge moyen des chats était de 13 ans, avec un sex ratio (M/F) de 1,8. Les signes cliniques étaient le plus souvent peu spécifiques (amaigrissement, dysorexie, vomissements) et les signes respiratoires n'étaient présents que dans moins d'un tiers des cas. Les adénocarcinomes pulmonaires représentaient la majorité des tumeurs et apparaissaient sous la forme d'une masse unique, de 2,75 cm en moyenne et affectant le plus souvent les lobes caudaux. Elles étaient le plus souvent bronchocentriques, présentant des contours irréguliers et bien délimités, avec une atténuation hétérogène. Des minéralisations ou la présence de gaz intra-tumoral étaient notées dans environ un tiers des cas.
Des nodules pulmonaires suspectés métastatiques ont été identifiés chez 54 % des chats, affectant à la fois les lobes ipsilatéraux et controlatéraux (39 % et 43 % respectivement). Des métastases musculo-squelettiques ont été observées dans 18 % des cas.
Une adénomégalie médiastinale a été relevée chez 36 % des chats, impliquant systématiquement les nœuds trachéobronchiques, et dans 21 % des cas, les nœuds médiastinaux crâniaux. Un épanchement pleural était présent dans 29 % des cas. Des lésions ostéolytiques ont été observées dans 2 cas.
Parmi les 28 chats présentant des lésions nodulaires, le diagnostic avait été établi pour 14 d'entre eux par un examen histologique de la lésion, pour 10 d'entre eux par un examen cytologique de la lésion et pour 4 par un examen cytologique d'une lésion à distance (épanchement pleural carcinomateux, ponctions de métastases musculaires).
Parmi les 6 cas à présentation diffuse ou multifocale, figuraient trois cas de carcinomes diffus, un cas de lymphome, un cas de tumeur maligne d'origine indéterminée et un cas de tumeur à cellules rondes suspectées histiocytaires. Pour ces cas, tous les diagnostics ont été établis par un examen histologique des lésions observées au scanner.
Discussion et conclusion
Les résultats corroborent en grande partie les données précédemment publiées, tout en apportant de nouvelles informations sur des formes plus atypiques, dont la prévalence semble être sous-estimée. La réalisation d'un examen scanner s'est révélée précieuse pour caractériser les lésions, bien que des limites subsistent, notamment liées à l'absence de confirmation histologique de certains cas. Ces observations soulignent l'intérêt de l'utilisation d'outils diagnostiques avancés comme l'examen tomodensitométrique dans le diagnostic de ces tumeurs et l'importance d'examiner la cavité pleurale, les ganglions mais aussi le tissu musculaire.
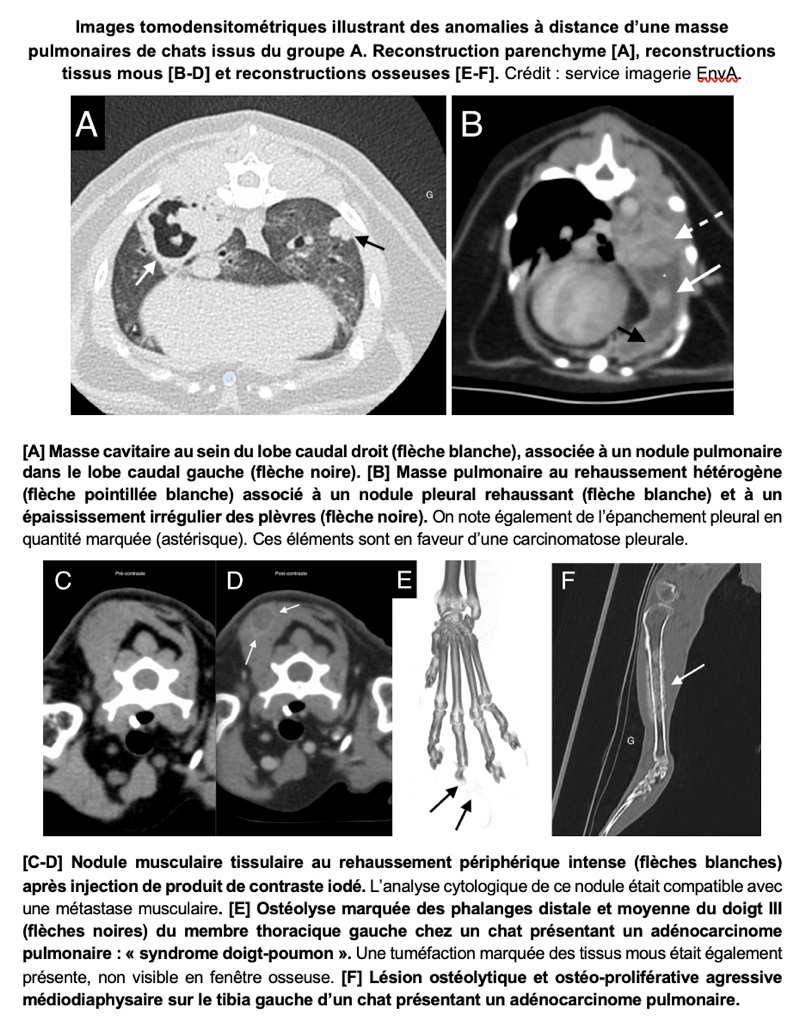
Figure 1
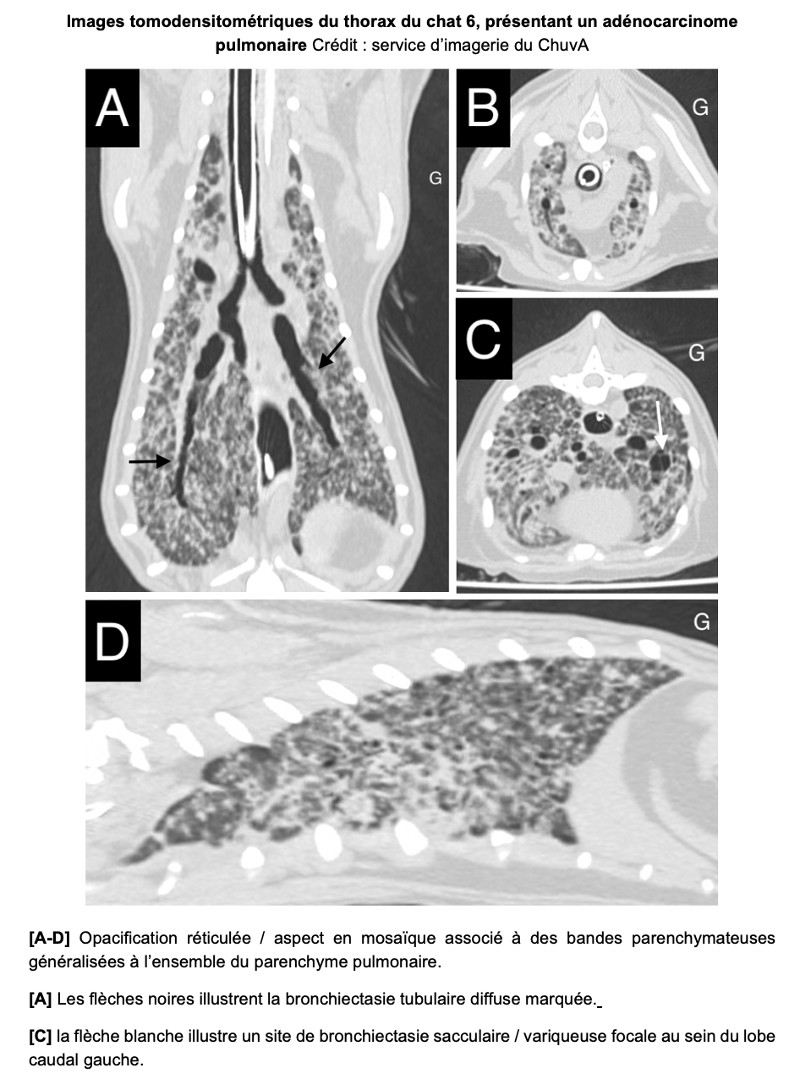
Figure 2
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Les urétérolithiases félines : médecine ou chirurgie, faisons le lien !
Guyancourt, France
Nantes, France
I. Introduction
L'obstruction urétérale chez le chat est une cause de plus en plus reconnue d'insuffisance rénale aiguë. La cause la plus fréquente d'obstruction urétérale bénigne est la présence de calcul urétéral suivi des strictures urétérales. Cette condition est de plus en plus reconnue grâce notamment aux avancées technologiques en matière d'échographie abdominale et autres procédures diagnostiques ces dernières années. Malgré les avancées technologiques, les obstructions urétérales demeurent des cas difficiles à diagnostiquer et posent souvent un challenge au clinicien en charge. Par ailleurs, une fois le diagnostic posé, il est essentiel de pouvoir recommander au propriétaire une prise en charge optimale, qu'elle soit médicale ou chirurgicale.
II. Diagnostic d'une obstruction urétérale
1. Présentation clinique
La présentation clinique de chats présentant une obstruction urétérale est très variable et dépend notamment de si l'atteinte est bilatérale ou unilatérale. Ainsi, les chats obstrués bilatéralement vont souvent présenter des signes liés au développement d'une insuffisance rénale aiguë. Lors d'atteinte unilatérale, les signes cliniques vont dépendre de la fonction rénale restante. Chez des patients pour lesquels un des reins est déjà très affecté par une maladie rénale chronique, alors les signes seront similaires à ceux d'une insuffisance rénale aiguë. En revanche, chez d'autres patients pour lesquels l'autre rein possède une bonne fonction rénale, les signes cliniques seront plus subtils.
2. Bilan sanguin
La plupart des chats présentant une obstruction urétérale ont une maladie rénale chronique sous-jacente et sont azotémiques au moment de la présentation. Une élévation du taux de créatinine, phosphore et/ou de l'urée dans le sang est alors constatée. Lorsque l'obstruction est bilatérale, une élévation du potassium sérique est aussi constatée pouvant parfois mettre en danger la vie de ces patients. Ces patients peuvent aussi présenter une anémie non régénérative modérée à très importante du fait de leur dysfonction rénale et de leur incapacité à synthétiser de l'érythropoïétine.
À noter toutefois, que des valeurs rénales dans les valeurs de référence ou dans les normes comparativement aux guidelines du groupe IRIS n'excluent pas une obstruction urétérale unilatérale ou partielle.
3. Radiographies abdominales
La radiographie abdominale permet parfois de mettre en évidence une obstruction urétérale liée à un calcul urétéral (les oxalates de calcium sont très radio-opaques). Toutefois, il s'agit d'un test très peu sensible et l'absence d'urétérolithe radio-opaque ne permet pas d'exclure une obstruction urétérale.
4. Échographie abdominale
Lors d'obstruction urétérale par un calcul de taille conséquente, ces patients peuvent alors présenter des images compatibles avec une importante pyélectasie (dilatation du pelvis rénal), des diverticules rénaux ainsi qu'une distension importante de l'uretère proximalement au calcul. Par ailleurs, ces chats présentent le plus souvent des reins de petite taille et bosselés, compatible avec un certain degré de maladie rénale chronique.
Plus récemment, il a aussi été montré que des distensions minimales (≤2 mm) du pelvis peuvent tout de même être associées à une obstruction urétérale.
5. Pyélographie antégrade
La pyélographie antégrade est l'examen de choix pour confirmer une obstruction urétérale. Cet examen diagnostique est, du fait de son caractère invasif, très fréquemment réalisé en chirurgie juste avant la pose d'un SUB dans le but de confirmer une obstruction urétérale.
III. Traitement d'une obstruction urétérale
1. Prise en charge médicale
Un antibiotique est fréquemment administré lorsque des signes évocateurs d'infections urinaires sont visualisés. De plus, environ 13-17% des chats avec une obstruction urétérale présentent une bactériurie. Une pyélonéphrite peut aussi potentiellement causer une obstruction dynamique (urétérite) +/- mécanique (potentielle obstruction par un bouchon de pus, urine purulente visqueuse).
L'utilisation d'αlpha-2 récepteur antagonistes (Prazosine, Tamsulosine, Alfuzosine) est fréquemment tentée dans le but de réduire les spasmes urétéraux et permettre l'élimination du potentiel calcul urétéral.
Environ 13-36% de chats présentant une obstruction urétérale vont avoir une amélioration de leurs valeurs rénales suite au traitement médical.
2. Prise en charge chirurgicale
En cas d'échec du traitement médical, la présence d'un calcul urétéral obstructif chez le chat nécessite une intervention chirurgicale et doit être pratiquée le plus précocement possible, afin de limiter l'évolution des lésions du parenchyme rénal, rapidement irréversibles.
Plusieurs procédures chirurgicales ont été proposées au cours des années pour permettre la levée de l'obstruction du flux urinaire et se regroupent en deux familles. D'un côté, les techniques visant à rétablir la perméabilité de l'uretère originel en retirant le calcul par urétérotomie ou en plaçant un dispositif au sein de la lumière de l'uretère permettant de lever l'obstruction au moyen d'un stent urétéral. Compte tenu du petit gabarit du chat, la mise en œuvre des techniques de retrait endoscopique, de lithotripsie intracorporelle ou extracorporelle est à l'heure actuelle anecdotique.
En alternative, des techniques de dérivation ont été proposées et permettent de rerouter le flux urinaire soit par un réabouchement des voies urinaires à la vessie en amont de l'obstruction (techniques de néourétérocystotomie end-to-side et side-to-side, réabouchement pyélovésical), soit au moyen d'un élément prothétique qui va permettre la collecte des urines dans le bassinet et leur acheminement à la vessie (Subcutaneous Ureteral Bypass) ou à l'extérieur de l'animal (sonde de néphrostomie).
Sur le papier, toutes ces techniques permettent un rétablissement de la diurèse et une gestion efficace à court et moyen termes de l'obstruction, mais elles diffèrent par leurs complications, leurs coûts et la complexité de réalisation technique et donc de temps opératoire.
Les complications générales du traitement chirurgical sont l'uroabdomen, l'anémie, les atteintes urinaires chroniques et la diurèse de levée d'obstruction. Le taux de mortalité à court terme (postopératoire immédiat ou en hospitalisation) est d'environ 10%, toutes techniques confondues.
À l'heure actuelle, le SUB est la modalité pour laquelle on dispose de plus de recul et de données. Ce dispositif a depuis plusieurs années pris une place de choix dans l'arsenal thérapeutique en raison de sa grande facilité de mise en place (accessible à de nombreux chirurgiens), de sa rapidité de mise en œuvre (durée d'anesthésie courte), de sa grande polyvalence (obstruction liée à des lithiases, des sténoses, des néoplasmes, obstructions multiples, etc.) et de sa performance dans la levée de l'obstruction à court terme.
Comme toute chirurgie, la pose d'un SUB est susceptible d'être associée à des complications au cours du suivi du patient.
À l'inverse, l'utilisation de stents ou de cathéters urétéraux n'est plus couramment pratiquée en raison de la complexité technique de mise en œuvre et d'une augmentation du risque de complications, notamment les infections urinaires chroniques.
Les techniques d'urétérotomie ont été historiquement très utilisées, mais elles requièrent une expertise chirurgicale importante, notamment en microchirurgie, et restent associées de manière significative à des complications de type sténose ou déhiscence (uroabdomen). Entre des mains expertes, elles peuvent encore être considérées lors d'obstructions focales uniques avec une dilatation importante de la lumière urétérale.
On assiste depuis quelques années à un regain de popularité des techniques de réabouchement urétéral, qui présentent l'avantage de s'affranchir des complications liées au maintien à long terme d'un dispositif prothétique (infection, obstruction, migration…).
La néourétérocystotomie (end-to-side) a été initialement recommandée pour les obstructions situées dans le tiers distal ou moyen de l'uretère pour des raisons de tension au site de l'anastomose et de vascularisation.
Il a depuis été montré qu'elle pouvait être mise en œuvre pour des obstructions plus proximales, moyennant des gestes complémentaires (néphrocystopexie, néphropexie et plastie vésicale avec création d'un tube de Boari). Des réabouchements du bassinet à l'apex de la vessie ont ainsi été réalisés avec succès chez le chat, permettant la levée d'obstructions urétérales très proximales.
Pour pallier ces limites liées à la tension exercée sur le site de réabouchement lors d'obstructions proximales, une technique de néourétérocystotomie side-to-side a été récemment développée et donne des résultats prometteurs. Ces techniques de réabouchement sont également associées à des complications (sténose, déhiscence). Elles constituent des alternatives possibles à la mise en place d'un SUB, même si elles requièrent une expertise chirurgicale et un temps opératoire souvent plus important.
IV. Le suivi à long terme
Quelle que soit la technique choisie pour permettre la résolution de l'obstruction urétérale, ces patients doivent être régulièrement réévalués dans le cadre du suivi d'une maladie rénale chronique.
De façon classique, lors de pose de SUB un entretien régulier (avec réalisation d'un rinçage/flush) tous les 3-4 mois est en général recommandé. Récemment plusieurs équipes autour du monde n'observent pas de réels avantages aux flushs et commencent à remettre en question la technique du flush à l'EDTA tous les 3-4 mois. Certains réalisent alors un flush au NaCl régulier quand d'autres ne réalisent que des flushs lorsqu'une possible complication de l'implant est détectée.
Les deux complications majeures de la pose d'un SUB à long-terme sont le développement d'une obstruction de l'implant par un « kink » (ou coude) dans la tubulure d'un des cathéters et par la minéralisation des tubulures ; et le développement d'infection urinaire (bas appareil urinaire et pyélonéphrite). À noter que seule une partie des chats présentant une obstruction de l'implant par des minéralisations (50-52%) ou par un « kink » (75%) nécessite une chirurgie de révision.
Enfin, chez ces patients possédant un SUB on constate une survie similaire à des chats diagnostiqués d'une maladie rénale et sans obstruction urétérale du même stade, démontrant que si l'obstruction est traitée et résolue, l'espérance de vie de ces patients n'est pas amoindrie par rapport à un autre chat souffrant de maladie rénale au même stade IRIS.
Le diagnostic d'une obstruction urétérale peut parfois s'avérer compliqué et délicat. La combinaison du tableau clinique, paraclinique et des examens d'imagerie permet souvent d'identifier les potentielles obstructions urétérales, avant confirmation définitive lors d'un examen de pyélographie antégrade. Toutefois, dans le cas d'un chat présentant une obstruction urétérale unilatérale sans atteinte de la fonction rénale et sans signe clinique apparent, le diagnostic peut être manqué jusqu'à apparition de signes cliniques ou, découvert fortuitement lors d'un examen échographique pour une autre condition. Diverses modalités de traitement existent lors de la prise en charge d'une obstruction urétérale chez un chat. Le traitement médical est peu efficace et présente des risques de complications pouvant être fatales pour le patient. Parmi les options chirurgicales, la pose de SUB est l'option offrant le meilleur taux de succès et la meilleure qualité de vie au patient à long terme. Toutefois, elle n'en reste pas moins coûteuse, et contraignante pour les propriétaires, avec des suivis réguliers recommandés et de possibles complications nécessitant d'être traitées par la suite. D'autres techniques chirurgicales sont également décrites comme alternatives mais ces dernières peuvent parfois s'avérer techniques et sont à considérer au cas par cas.
Bibliographie
Lectures suggérées : à demander
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Lien de la mère au petit pour faire un chien/chat équilibré
Maisons-Alfor,t France
I. Introduction
La santé, tant physique que (comporte)mentale, d'un chien ou d'un chat adulte se joue dès la naissance (et même dès avant la gestation). Dès les premiers jours de vie, le lien complexe entre la mère et sa progéniture place les nouveau-nés sur une trajectoire de santé qui se poursuit jusqu'à l'âge adulte. Cette « programmation maternelle » s'exerce sur de nombreux aspects de la santé du jeune.
L'odeur du liquide amniotique dont sont imprégnés les nouveau-nés est capitale pour établir la reconnaissance des jeunes par leur mère et développer les relations oronasales. Le comportement de léchage de la région anogénitale, indispensable pour déclencher la miction et la défécation, est probablement stimulé par des secrétions génitales des chiots et chatons.
II. Lien immunitaire
Chiots et chatons naissent agammaglobulinémiques. Grâce à la tétée du colostrum au cours des 8 premières heures de vie, ils acquièrent un stock d'immunoglobulines G circulantes qui vont assurer leur protection immunitaire au cours des 2 à 3 premières semaines de vie. Un déficit de transfert d'immunité passive est associé à une augmentation (x5-8 fois) du risque de mortalité néonatale [1].
III. Lien nutritionnel
Dès la prise colostrale, puis au cours des premières semaines de vie, la tétée du lait maternel assure les apports nutritionnels. Le lien mère-jeune qui s'établit garantit d'une part que la mère adopte une position compatible avec la tétée, et ceci suffisamment souvent au cours d'une journée, avec une production lactée suffisante (estimée à 1% à 8% du poids de la mère). Quant aux nouveau-nés, ils établissent un lien spécifique avec leur mère avec un tropisme (chimique et thermique) vers ses mamelles. Une croissance insuffisante au cours des 7 premiers jours de vie (taux de croissance entre 2 et 7 jours de vie inférieur à 18% chez le chiot) est associée à une multiplication par 17 du taux de mortalité au cours des deux premiers mois de vie. L'impact d'une forte croissance au cours des premières semaines de vie sur le risque de surpoids à l'âge adulte est encore sujet à controverses [2].
IV. Lien bactérien
En plus de l'environnement, la mère est une source de bactéries pour ses nouveau-nés. Par l'intermédiaire du colostrum, du lait, de la peau, de la salive et des fecès, elle participe à l'ensemencement du tube digestif des jeunes. Le lien mère-jeunes contribue donc à la constitution du microbiote digestif des nouveau-nés. Or un déséquilibre de celui-ci (dysbiose) est associé au développement de diarrhées, d'affections parasitaires ou virales ainsi qu'au « fading puppy syndrom » (syndrome de dépérissement) [3].
V. Lien comportemental
Le comportement maternel est bien évidemment nécessaire à la survie des jeunes, puisqu'il permet les tétées, les mictions/défécations et le maintien de la température corporelle des jeunes. Mais il conditionne également les comportements socio-émotionnels des jeunes une fois adultes. Même si la majeure partie du développement neurologique du chien a lieu durant la vie fœtale, il se poursuit jusqu'à au moins 36 semaines d'âge. Cette maturation postnatale prolongée rend le développement des comportements et des apprentissages des jeunes sensible aux influences de l'environnement et donc à celles du lien établi avec la mère . Le « comportement maternel » inclut donc l'éducation aux relations sociales avec d'autres chiens, les humains et les stimulations environnementales. La mère est par nature la première référence adulte pour les jeunes, le comportement de la mère est donc d'une importance majeure dans la formation de leurs comportements et de leurs réactions. Des chiots séparés de leur mère à l'âge de 30 à 40 jours, et recevant ainsi moins de soins maternels durant le deuxième mois de vie comparés à ceux séparés à 60 jours, étaient plus susceptibles de développer des troubles comportementaux tels que la peur, la réactivité au bruit et les aboiements excessifs. Néanmoins, il n'est pas forcément souhaitable que la mère ait un comportement maternel hyperdéveloppé. Des jeunes élevés par une mère avec un comportement de nursing limité développeraient des stratégies adaptatives, car confrontés à de petits défis dès leur plus jeune âge [5].
VI. Conclusion
L'établissement de liens entre la mère et les nouveau-nés dès la naissance est donc crucial pour la santé aussi bien à court qu'à long terme. Ces liens sont très divers et infléchissent dès le début de la vie le devenir du chiot et du chaton jusqu'à l'âge adulte.
Bibliographie
- CHASTANT S, MILA H. Passive immune transfer in puppies. Anim Reprod Sci. 2019;207:162-170.
- MUGNIER, A.; GAILLARD, V.; CHASTANT, S. Relative Impact of Birth Weight and Early Growth on Neonatal Mortality in Puppies. Animals 2023, 13, 1928.
- DEL CARRO A, CORRÒ M, BERTERO A, COLITTI B, BANCHI P, BERTOLOTTI L, ROTA A. The evolution of dam-litter microbial flora from birth to 60 days of age. BMC Vet Res. 2022 Mar 11;18(1):95
- SANTOS NR, BECK A, FONTBONNE A. A review of maternal behaviour in dogs and potential areas for further research. J Small Anim Pract. 2020;61(2):85-92.
- BRAY EE, SAMMEL MD, CHENEY DL, SERPELL JA, SEYFARTH RM. Effects of maternal investment, temperament, and cognition on guide dog success. Proc Natl Acad Sci 2017; 114:9128–9133.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Lien entre maladie parodontale et pathologie systémique, mythe ou réalité?
Vélizy-Villacoublay, France
I. Introduction
La maladie parodontale est une des pathologies les plus fréquentes chez le chien et le chat. En fonction des études, on trouve une grande variabilité de prévalence, par exemple entre 9 et 100% chez le chien [1]. Si ses conséquences locales (gingivite, halitose, mobilité dentaire, douleur chronique) sont bien connues, la question de son rôle dans l'émergence ou l'aggravation de maladies systémiques est bien souvent sous-estimée.
Ces dernières années, plusieurs études expérimentales et cliniques ont cherché à établir un lien entre parodontite et atteintes cardiaques, rénales, endocriniennes ou métaboliques. L'objectif de cette présentation est de montrer comment la parodontite peut influencer la santé générale de l'animal (cœur, reins, métabolisme, système endocrinien) et de donner aux praticiens des clés concrètes pour mieux intégrer la santé bucco-dentaire dans leur médecine de prévention et thérapeutique.
II. Physiopathologie : pourquoi un lien est plausible ?
La parodontite est une maladie caractérisée par une inflammation et infection persistante du parodonte (gencive, ligament alvéolaire, cément, os alvéolaire) menant à sa destruction progressive. Les mécanismes proposés pour expliquer le lien entre la parodontite et les pathologies systémiques incluent :
- La présence d'une bactériémie transitoire
- La présence d'une inflammation systémique chronique
- La réponse immunitaire du patient
- Les désordres métaboliques
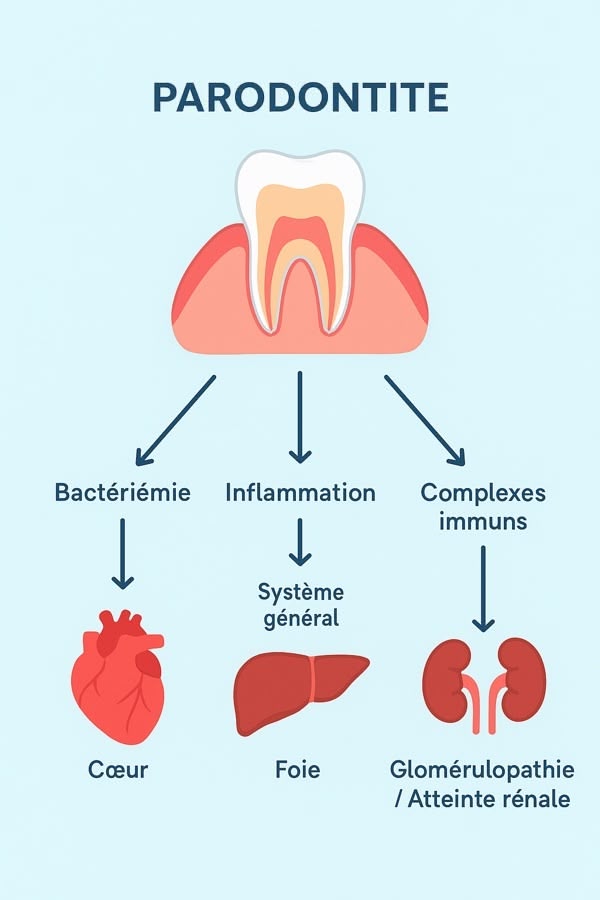
Figure 1 : liens entre parodontite et maladies systémique de façon simplifiée (image générée par intelligence artificielle)
III. Parodontite et pathologie cardiaque
Chez l'homme, le lien entre maladie parodontale et maladies cardiovasculaires est bien établi [2]. En médecine vétérinaire, les données s'accumulent :
- Endocardite infectieuse : la bactériémie d'origine orale pourrait favoriser l'adhésion bactérienne aux valves cardiaques, en particulier lorsqu'elles présentent déjà des lésions dégénératives.
- Maladie valvulaire dégénérative (endocardiose mitrale) : plusieurs études observationnelles rapportent une corrélation entre la sévérité de la parodontite et l'intensité des souffles cardiaques ou le stade clinique de la maladie mitrale. Même si la causalité directe reste difficile à établir, la parodontite apparaît comme un facteur aggravant d'une pathologie très fréquente chez le chien âgé.
- Mécanismes d'aggravation cardiaque :
- Bactériémie chronique → colonisation bactérienne des valves.
- Inflammation systémique → remodelage valvulaire et accélération du processus dégénératif.
- Réponse immunitaire croisée → dépôts de complexes immuns au niveau cardiaque.
Une étude américaine [3] a ainsi montré que les chiens atteints de parodontite sévère avaient un risque significativement accru de développer une endocardite ou une insuffisance cardiaque congestive.
Pour le clinicien, ces données justifient une surveillance cardio-respiratoire accrue des animaux présentant une maladie buccale avancée, ainsi qu'une prise en charge parodontale préventive dans les populations à risque (races prédisposées à l'endocardiose mitrale).
IV. Parodontite et atteinte rénale
Le rein apparaît comme un autre organe cible potentiel :
Les chiens atteints de parodontite sévère présentent plus fréquemment des anomalies de la fonction rénale (augmentation de l'urée et de la créatinine) [4,5].
Des dépôts immunitaires d'origine bactérienne ont été retrouvés dans les glomérules, suggérant une glomérulonéphrite à complexes immuns.
L'état inflammatoire chronique pourrait accélérer le déclin de la fonction rénale chez les animaux déjà fragiles.
V. Parodontite et désordres endocriniens : exemple de l'hyperparathyroïdisme secondaire
Un aspect moins souvent abordé, mais pourtant documenté, est le lien entre la parodontite et le métabolisme phosphocalcique :
Lors de malnutrition ou de maladie rénale sévère, un hyperparathyroïdisme secondaire peut se développer, et perturber le métabolisme phosphocalcique.
Ainsi, la parodontite n'est pas seulement une conséquence mais aussi un facteur aggravant de désordres endocriniens et osseux, avec des répercussions cliniques sur la santé générale.
VI. Autres atteintes à distance
- Hépatopathies : augmentation des enzymes hépatiques chez des chiens atteints d'une parodontite avancée. Des modifications histopathologiques ont été observées au niveau du foie.
- Diabète sucré : dans l'espèce canine, la parodontite pourrait exacerber la résistance à l'insuline, comme observé chez l'homme. Le diabète est plus difficile à stabiliser si l'animal ne mange pas de façon régulière, ce qui peut être le cas lors de douleurs bucco-dentaire.
- Douleur chronique et qualité de vie : l'inflammation buccale persistante contribue à une diminution du bien-être global.
VII. Implications cliniques
Pour le vétérinaire généraliste, ces données soulignent l'importance de :
- Considérer la santé buccodentaire dans chaque consultation de prévention, dès le plus jeune âge.
- Intégrer l'examen oral systématique lors de la consultation.
- Sensibiliser les propriétaires au rôle de l'hygiène dentaire dans la prévention non seulement des problèmes locaux mais aussi de potentielles complications systémiques.
- Associer, chez les animaux cardiaques, rénaux ou endocriniens, une prise en charge buccale adaptée et sécurisée (soins parodontaux, extractions, soins et suivi réguliers, avec notamment du brossage dentaire quotidien).
VIII. Conclusion
Le lien entre maladie parodontale et atteintes systémiques, longtemps considéré comme hypothétique, repose aujourd'hui sur un faisceau croissant de preuves expérimentales et cliniques. Sans affirmer une causalité stricte, il semble prudent d'admettre que la parodontite constitue un facteur de risque ou d'aggravation des maladies cardiaques, rénales, métaboliques et endocriniennes chez le chien et le chat.
La prévention, le dépistage précoce et la prise en charge adaptée des affections parodontales doivent donc être intégrés à la pratique quotidienne, au bénéfice de la santé générale de l'animal.
Bibliographie
- HARVEY C. The Relationship Between Periodontal Infection and Systemic and Distant Organ Disease in Dogs. Vet Clin North Am Small Anim Pract. 2022, 52(1):121-137.
- HOPKINS S. et coll. Oral Health and Cardiovascular Disease. The American Journal of Medicine. 2024; 137 (4) : 304-307
- GLICKMAN LT et coll. Evaluation of the risk of endocarditis and other cardiovascular events on the basis of the severity of periodontal disease in dogs. J Am Vet Med Assoc. 2009, 15;234(4):486-94.
- RAWLINSON JE, GOLDSTEIN RE, REITER AM, ATTWATER DZ, HARVEY CE. Association of periodontal disease with systemic health indices in dogs and the systemic response to treatment of periodontal disease. J Am Vet Med Assoc. 2011, 1;238(5):601-9.
- GLICKMAN LT, et coll. Association between chronic azotemic kidney disease and the severity of periodontal disease in dogs. Prev Vet Med. 2011, 1;99(2-4):193-200.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Lien entre la douleur orale et la dysorexie ? Et pourtant il mange Docteur
Bandol, France
I. Introduction - Un mythe à déconstruire
En médecine vétérinaire, la douleur orale est fréquente mais souvent sous-diagnostiquée. Un préjugé tenace persiste : un animal qui mange ne peut pas souffrir de la bouche. Or, chiens et chats conservent souvent une prise alimentaire malgré des douleurs sévères, leur instinct de survie l'emportant sur l'évitement de la douleur. L'absence de signes évidents n'exclut donc pas une pathologie douloureuse.
Les affections orales (maladie parodontale, fractures dentaires, résorptions, malocclusions traumatiques, tumeurs) induisent douleur, inflammation, infection chronique et altération majeure du bien-être. La gestion de cette douleur constitue un devoir éthique et un impératif médical, reconnue comme le quatrième signe vital à surveiller lors de l'examen clinique de routine, au même titre que la température, le pouls et la fréquence respiratoire [1].
II. Comprendre la douleur orale
La douleur orale est multidimensionnelle, mêlant composantes sensorielles et émotionnelles. Elle peut être aiguë (traumatisme, chirurgie) ou chronique (stomatites, maladie parodontale avancée). La douleur chronique est un état pathologique en soi et n'a pas de fonction protectrice [2].
Chez le chat, les signes sont discrets : réduction d'activité, modifications alimentaires (mastication unilatérale, passage au mou, chute de nourriture), hypersalivation, saignement oral ou nasal, altération du toilettage, isolement, changements de comportement, expressions faciales altérées. La Feline Grimace Scale est un outil validé pour évaluer la douleur post-opératoire après des extractions dentaires chez les chats. Cependant, des limites ont été notées pour la douleur orale spécifique, notamment la difficulté à évaluer l'attention à la plaie ou la réaction à la palpation buccale [3]. Chez le chien, les signes sont similaires mais souvent moins bien perçus.
L'évaluation clinique doit intégrer l'observation des propriétaires, la palpation orale (sous anesthésie si nécessaire) et l'usage d'outils validés (CMPS-SF, Feline Grimace Scale). L'observation attentive par le propriétaire est primordiale pour la détection de la douleur chronique, car ils sont les plus à même de remarquer des changements comportementaux minimes.
III. Principes de gestion de la douleur péri-opératoire
La gestion de la douleur orale, en particulier lors d'interventions dentaires, repose sur deux principes fondamentaux :
1. L'analgésie préventive : administrer des analgésiques avant que le stimulus douloureux ne se produise. Cette approche vise à réduire l'impact de l'influx nociceptif périphérique et à diminuer la sensibilisation centrale et périphérique de la moelle épinière, ce qui peut réduire la douleur aiguë post-chirurgicale et l'incidence de la douleur chronique.
2. L'analgésie multimodale (ou balancée) : combiner plusieurs substances analgésiques agissant à différentes étapes de la perception de la douleur. Cette approche permet une analgésie optimale tout en limitant les effets secondaires liés à l'utilisation de doses élevées d'une seule molécule. Les interventions dentaires, souvent associées à des douleurs modérées à sévères, bénéficient grandement de cette approche [2].
IV. Analgésiques per-opératoires : systémiques et locaux [1]
Les interventions dans la cavité buccale, même un détartrage basique, sont associées à de la douleur. Les gingivectomies, les extractions dentaires et les interventions sur les tissus mous ou osseux de la cavité orale sont souvent associées à des douleurs modérées à sévères. Une anesthésie générale avec intubation endotrachéale est indispensable.
1. Analgésiques systémiques per-opératoires
L'analgésie systémique vise à réduire les besoins en anesthésiques volatils et à stabiliser le patient.
- Morphiniques (Opioïdes) : ils sont la pierre angulaire des traitements efficaces contre la douleur modérée à sévère.
- Mécanisme d'action : ils se fixent sur des récepteurs spécifiques dans les systèmes nerveux central et périphérique, inhibant la transmission des stimuli douloureux.
- Exemples et usages (à titre indicatif) :
- Fentanyl : très puissant (50 à 150 fois la morphine), utilisé en bolus (2–5 µg/kg) ou en perfusion continue (3–6 µg/kg/h) pour une analgésie maximale, notamment pour limiter les doses d'anesthésique volatil.
- Morphine : peut être utilisée en perfusion continue (0,1 mg/kg/h) ou en bolus (0,3 mg/kg).
- Méthadone : (0,2–0,3 mg/kg IM, IV) présente des propriétés antagonistes des récepteurs NMDA, ce qui est un avantage.
- Sécurité : les opioïdes sont généralement sûrs, et la dépression respiratoire est rare chez les animaux en douleur, sauf en cas de surdosage important. Les vomissements sont courants en prémédication mais rares chez les animaux douloureux.
- Antagonistes des récepteurs NMDA (Kétamine) :
- Mécanisme d'action : la kétamine, à des doses infra-anesthésiques, module la sensibilisation centrale et a un effet anti-hyperalgique. Elle peut être utilisée pour prévenir ou traiter les douleurs neuropathiques, souvent présentes dans les cas de douleur chronique.
- Usage : administrée en bolus IV (0,5–1 mg/kg) suivi d'une perfusion continue (0,12–0,6 mg/kg/h chez le chien ; 0,3–1,2 mg/kg/h chez le chat). Elle est un traitement adjuvant aux morphiniques ou AINS.
- Alpha2-Agonistes : peuvent être inclus dans les protocoles d'analgésie multimodale pour augmenter l'analgésie et réduire la réponse au stress. Cependant, des précautions sont nécessaires en raison de leurs effets cardiovasculaires (bradycardie, hypotension).
2. Analgésiques locaux per-opératoires
Les techniques d'anesthésie locorégionale sont d'une importance capitale pour les interventions dentaires. Elles permettent de bloquer complètement la genèse et la conduction de l'influx nociceptif et de prévenir le développement de la sensibilisation.
- Molécules utilisées (figure 1) :
- Association Bupivacaïne 0,5% et Lidocaïne 2% : 1 mg/kg de chaque molécule (chien, chat).
- Articaïne 4% (hors AMM) : 4 mg/kg (chien, chat)

Figure 1
- Techniques de blocs dentaires (figure 2) : les repères pour le placement de l'aiguille (26G et au-delà) peuvent être palpés à travers la muqueuse ou la peau. Une aspiration est réalisée avant injection pour s'assurer qu'aucun vaisseau n'a été ponctionné.
- Bloc du nerf infra-orbitaire : désensibilise la partie rostrale du nez, la canine et les incisives supérieures ipsilatérales.
- Bloc du nerf mandibulaire (alvéolaire inférieur) : désensibilise la mandibule ipsilatérale, les dents, les muqueuses labiales et gingivales, et la peau de la lèvre inférieure.
- Bloc du nerf mentonnier : désensibilise la canine et les incisives inférieures ipsilatérales.
- Bloc du nerf maxillaire : désensibilise le maxillaire ipsilatéral, les dents maxillaires, le plafond de la cavité nasale et la peau de la face latérale du nez.
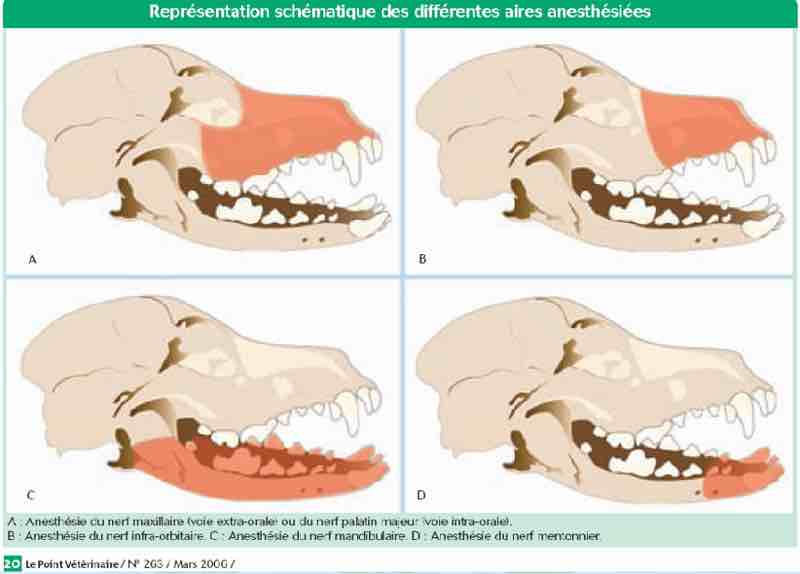
V. Analgésiques pré- et post-opératoires [1,2]
Le traitement analgésique doit être poursuivi après l'intervention jusqu'à ce que la réponse inflammatoire s'atténue significativement.
1. Analgésiques systémiques
- Anti-inflammatoires Non Stéroïdiens (AINS) : les AINS sont un des piliers de l'analgésie pour la douleur aiguë et chronique, sur 3 à 7 jours, voire plus selon indication.
- Utilisation : administrés avant (lors de l'induction de l'anesthésie), puis après la chirurgie une fois que le patient est hémodynamiquement stable et en l'absence de contre-indications. Le méloxicam, le carprofène et le robenacoxib sont les plus couramment utilisés.
- Doses (à titre indicatif et toujours vérifier la notice et le patient) :
- Méloxicam : chat : 0,3 mg/kg SC une fois ou 0,2 mg/kg SC, puis 0,05 mg/kg PO une fois par jour. Chien : 0,2 mg/kg SC, IV puis 0,1 mg/kg PO une fois par jour.
- Carprofène : chat, chien : 4 mg/kg SC, IV, puis 2 à 4 mg/kg PO une fois par jour.
- Robenacoxib : chat, chien : 2 mg/kg SC, puis 1 à 2 mg/kg PO une fois par jour.
- Précautions : toujours vérifier la fonction rénale et hépatique avant l'administration. Contre-indiqués en cas de déshydratation, hypotension, insuffisance cardiaque congestive, ou troubles de la coagulation [1,2].
- Opioïdes : le relais des morphiniques peut être pris en post-opératoire, notamment pour les douleurs modérées à sévères.
- Buprénorphine : très utile par voie transmucosale orale chez le chat et les petits chiens, offrant une gestion continue de la douleur post-opératoire .
- Dose : chat, petits chiens : 0,02 mg/kg IM, IV, PO transmucosale toutes les 6-8 h pendant 3-5 jours.
- Tramadol : peut être intéressant pour la douleur modérée à sévère, y compris neuropathique.
- Dose : chien : 5 mg/kg PO toutes les 8-12 h. Chat : 2 mg/kg PO toutes les 12 h.
- Buprénorphine : très utile par voie transmucosale orale chez le chat et les petits chiens, offrant une gestion continue de la douleur post-opératoire .
- Thérapeutiques Adjuvantes : pour les douleurs chroniques ou neuropathiques réfractaires aux traitements usuels.
- Gabapentine : efficace pour les douleurs neuropathiques (lancinantes, paroxystiques, hyperalgésie) et l'automutilation, fréquemment associée aux lésions nerveuses post-chirurgicales ou tumorales.
- Dose : chien, chat : 5 à 10 mg/kg PO toutes les 8-12 h. La dose peut être augmentée et l'effet maximal peut prendre plusieurs semaines [1].
- Gabapentine : efficace pour les douleurs neuropathiques (lancinantes, paroxystiques, hyperalgésie) et l'automutilation, fréquemment associée aux lésions nerveuses post-chirurgicales ou tumorales.
2. Approches Non Pharmacologiques [1]
Ces approches peuvent apporter un soulagement supplémentaire et améliorer la qualité de vie de l'animal.
- Thérapie par le froid : appliquée sur les lésions aiguës post-opératoires pour diminuer l'œdème et procurer une analgésie.
- Acupuncture : de plus en plus utilisée pour la douleur chronique.
VI. Conclusion
La douleur orale, souvent masquée par les patients, doit être systématiquement recherchée et traitée. Un protocole intégrant analgésie préventive et multimodale, associant analgésiques systémiques et techniques locorégionales, optimise la récupération, réduit la souffrance et améliore la qualité de vie. La compétence du vétérinaire à prescrire et combiner ces approches est déterminante pour le succès thérapeutique et la confiance du propriétaire.
Bibliographie
- MONTEIRO B.P. et coll. Pain guidelines. WSAVA 2022. Journal of Small Animal Practice · Vol 64 · Avril 2023
- POUZOT C. Nouvelles approches thérapeutiques dans la gestion de la douleur chronique arthrosique, cancéreuse et neurogène chez le chien. Université Claude-Bernard Lyon I. Thèse vétérinaire 2003.
- WATANABE et coll. Pain behaviors before and after treatment of oral disease in cats using video assessment : a prospective, blinded, randomized clinical trial. BMC Veterinary Research (2020) 16 : 100
- ANDERSON J.G., HENNET P. Management of Severe Oral Inflammatory Conditions in Dogs and Cats. Vet Clin Small Anim 52 (2022) 159–184
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Liens dans une fratrie
Cabrières-d'Avignon, France
I. Introduction
Le groupe mère–fratrie constitue le premier environnement social du chiot. Entre 2 et 8 semaines, les interactions fraternelles passent de l'exploration au jeu social organisé, avec des séquences agonistiques contrôlées et des « règles » qui évitent l'escalade [1,2]. Ces interactions soutiennent l'acquisition d'autocontrôles (dont l'inhibition de la morsure), la lecture des signaux et la gestion de la frustration [2]. Nous distinguons ci-dessous faits étayés et retours de terrain, et faisons le point à cette occasion sur le « chiot unique » et le littermate syndrome.
1. Chronologie des interactions fraternelles
Les classiques de l'éthologie canine décrivent l'ouverture sensorielle (≈ 2–3 semaines), l'émergence rapide du jeu, puis la structuration d'échanges réciproques avec arrêts spontanés et alternance des rôles [1,2]. Le cadre ludique fonctionne comme une métacommunication qui balise les comportements à risque et entraîne la régulation émotionnelle [2] et limite l'escalade symétrique.
En élevage, un bon jeu se reconnaît à des séquences courtes, des pauses fréquentes et une reprise volontaire des partenaires. Des asymétries persistantes non tolérées (même « gagnant ») appellent à fractionner les dyades, varier les partenaires et surtout insérer un adulte tuteur, qui reste de loin le meilleur gage pour réguler les interactions des chiots.
2. Effet « portée » : un micro-environnement social puissant
À 7–9 semaines, dans des tests standardisés (open-field/novel object), l'effet portée explique une part substantielle de la variance des traits (exploration, sociabilité, réactivité), parfois supérieure à l'effet race à cet âge [3]. Ce résultat souligne le poids du micro-environnement fraternel (opportunités de jeu, compétition à la tétée, micro-pratiques d'élevage).
Sur le terrain, il est régulièrement constaté que deux portées élevées dans le même contexte mais avec des dynamiques de jeu différentes produisent souvent des profils distincts à la visite des 8 semaines ; réduire la densité (sessions courtes et fréquentes) et équilibrer les dyades améliorent généralement la trajectoire.
3. Interactions avec les soins maternels
La quantité/qualité des soins maternels (léchage/contact, postures d'allaitement, réactivité au stress) est associée à des différences ultérieures de tempérament (engagement social/physique, agressivité, persévérance) [4]. Les chiots issus de mères offrant un nursing plus exigeant et un stress bas montrent des profils plus adaptés en contexte de formation [4]. Les données montrent un impact plus important de la qualité et quantité des soins maternels sur la qualité de développement des chiots que tous les paramètres liés à la fratrie.
Chez des mères très « fusionnelles », on observe parfois une autonomie moindre en sevrage ; l'introduction graduée d'adultes familiers et de micro-défis sensorimoteurs (textures, postures « debout ») compense utilement. Ce constat de terrain n'a cependant pas encore fait l'objet de travaux structurés.
4. Âge de séparation d'avec la fratrie
L'adoption avant 8 semaines est associée à davantage de comportements problématiques (peurs, réactivité, destructivité, vocalisations) plus tard [5]. Le maintien du groupe mère–fratrie au moins jusqu'à 8 semaines, avec socialisation graduée et encadrée, est donc recommandé [5].
Les observations de terrain soulignent le bénéfice net pour l'équilibre comportemental des chiots quand l'éleveur programme des sorties courtes mais fréquentes entre 8 et 10 semaines, des rencontres canines avec des adultes régulateurs spécifiquement sélectionnés et un sas pédagogique avec l'adoptant (routines stables + apprentissages calmes plutôt que « grand bain » d'excitants).
5. « Syndrome du chiot unique » (singleton) : quel intérêt pratique pour cette notion ?
Les seules études scientifiques publiées à propos de ce syndrome se limitent au domaine obstétrical, les gestations mono-fœtales sont associées à davantage de dystocies/inerties. Sur le plan comportemental, aucune preuve robuste ne démontre un syndrome nosologique spécifique au « chiot unique » dans la littérature évaluée par les pairs ; les données publiées sont rares et indirectes.
Internet rapporte cependant des réflexions de professionnels de l'élevage sur les risques d'hyperattachement ou de fragilité émotionnelle pour le chiot unique. Un environnement social pauvre avec un mode de vie relativement autarcique sont connus comme des facteurs favorisant l'hyperattachement et des réactions excessives de peur : cela est vrai pour tous les chiots et ne se limite pas au chiot unique.
6. « Littermate syndrome » : quelle solidité scientifique ?
Il n'existe pas ici non plus d'assise scientifique solide pour un « littermate syndrome » au sens nosologique strict. Cette étiquette rassemble deux difficultés : frères et sœurs manifestent des états de panique lors des séparations et développent une agressivité mutuelle intense au moment de la maturation sociale. Une première remarque permet de souligner l'absence de données sur le caractère systématique de ces observations. Ensuite, les connaissances en psychiatrie vétérinaire suggèrent que les deux difficultés observées constituent des entités connues, indépendantes (la première concernant l'axe de l'attachement et l'autre l'axe de l'insertion sociale) et qu'elles ne se limitent pas aux individus d'une même portée, bien que l'appartenance à la même portée favorise la présence d'un ou plusieurs facteurs aggravants (l'attachement réciproque nuit à l'attachement aux propriétaires dans le premier cas, la proximité de la taille nuit à l'émergence d'un leader clair dans le second cas). Pour limiter le premier phénomène, si deux frères/sœurs partent ensemble, viser des routines parallèles qui se croisent (et non confondues) est déterminant : activités, entraînements, temps de calme et d'attachement humain séparés au moins la première quinzaine.
7. Facteurs confondants et limites
On a vu précédemment l'importance des facteurs de confusion : taille de portée, ratio des sexes, lignée, pratiques d'élevage, saison, qualité des stimuli et des manipulations : tous ces facteurs modulent les mesures à 2 mois [3] et appellent à la mise en place d'études rigoureuses afin d'organiser les connaissances et hiérarchiser l'importance relative des différents facteurs influant sur le développement comportemental. Il convient de rappeler par ailleurs que les évaluations précoces ne prédisent pas parfaitement le tempérament adulte ; prudence donc dans l'extrapolation [1,3,4].
II. Conclusion
Les liens fraternels sont un levier majeur du développement socio-émotionnel. Les données confirment l'importance du jeu structuré [2], l'existence d'un effet portée notable dès 7–9 semaines [3], l'influence durable des soins maternels [4], et le risque accru lorsque la séparation survient trop tôt [5]. En revanche, ni un « syndrome comportemental du chiot unique » ni un « littermate syndrome » n'ont d'assise nosologique forte ; on parle de situations à risque qui ne se limitent pas à ces cas particuliers et qu'il convient de gérer préventivement. En pratique, la qualité des expériences sociales précoces, la gradualité des expositions et la structuration des entraînements (y compris séparés pour les fratries adoptées ensemble) sécurisent la trajectoire de la majorité des chiots.
Bibliographie
- SCOTT JP, FULLER JL. Genetics and the Social Behavior of the Dog. Chicago: University of Chicago Press; 1965.
- BEKOFF M. Play signals as punctuation: The structure of social play in canids. Behaviour. 1995;132(5–6):419–429. doi:10.1163/156853995X00649.
- BARNARD S et coll. Breed, sex, and litter effects in 2-month-old puppies' behaviour in a standardised open-field test. Sci Rep. 2017;7:1802. doi:10.1038/s41598-017-01992-x.
- FOYER P et coll. Levels of maternal care in dogs affect adult offspring temperament. Sci Rep. 2016;6:19253. doi:10.1038/srep19253.
- PIERANTONI L et coll. Prevalence of owner-reported behaviours in dogs separated from the litter at two different ages. Vet Rec. 2011;169(18):468. doi:10.1136/vr.d4967.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Luxation de la hanche : replacer, renforcer, remplacer ou tout couper ?
Isturits, France
I. Introduction
L'articulation de la hanche est composée de l'acétabulum et de la tête du fémur. Les structures primaires de stabilisation de cette articulation sont le ligament rond, la capsule et le sourcil acétabulaire. Les luxations coxo-fémorales (LCF) sont majoritairement d'origine traumatique, accident de la voie publique ou chute. Il convient donc de faire un bilan lésionnel complet, ces luxations étant régulièrement accompagnées d'autres lésions osseuses ou des tissus mous environnants. Au moins 2 des structures de contention majeures citées ci-dessus sont touchées pour qu'une LCF survienne.
Les luxations de hanches sont caractérisées par la position de la tête du fémur relativement à l'acétabulum.
Les luxations cranio-dorsales sont les plus communes et sont rapportées dans 72% des LCF. Elles sont subdivisées en sous-types A, B et C. Le type A de luxation cranio-dorsale correspond à une luxation durant laquelle la capsule articulaire s'est déchirée à mi-chemin entre l'insertion acétabulaire et fémorale. Le type B de luxation cranio-dorsale correspond à une désinsertion acétabulaire de la capsule. Le type C de luxation cranio-dorsale correspond à une désinsertion fémorale de la capsule.
Les luxations caudo-dorsales sont moins fréquentes et les luxations ventrales sont excessivement rares.
Ici sera principalement abordé le traitement des luxations cranio-dorsales.
Deux approches sont classiquement décrites. L'approche orthopédique correspond à la réduction à foyer fermé de la luxation par des manipulations extérieures. L'approche chirurgicale nécessite une approche chirurgicale de la luxation et une réduction à foyer ouvert.
II. Replacer : la réduction à foyer fermé des luxations coxo-fémorales
La réduction de la luxation à foyer fermé est envisageable dans le cadre des luxations dorsales, crâniales ou caudales. La littérature rapporte un taux de reluxation important avoisinant les 50%. Ce taux élevé est classiquement imputable à la présence dans la cavité acétabulaire d'éléments gênant la congruence correcte de l'articulation : caillots sanguins, fragments déchirés de ligament rond, capsule articulaire. La présence de fractures du sourcil acétabulaire ou de la tête du fémur augmentent également le risque de reluxation.
Dans le cadre de luxation cranio-dorsale, le type de luxation est également un facteur de risque. En effet, les types B et C présentent un risque important de reluxation. Le type B est particulièrement instable : quand la capsule se désinsère, il est fréquent que le labrum acétabulaire fibreux qui augmente classiquement le recouvrement du sourcil acétabulaire soit arraché, augmentant l'instabilité de la luxation. Dans le type C, la capsule forme un repli dans l'acétabulum au moment de la réduction et augmente la gène.
Sous anesthésie générale, l'animal est placé en décubitus latéral. Une rotation externe puis une traction du membre sont réalisées. Une fois la tête du fémur localisée en regard de l'acétabulum, une rotation interne est réalisée associée à une pression sur le grand trochanter. La tête du fémur est réintégrée dans le cotyle et plusieurs mouvements de flexion et d'extension modérés sont réalisés afin de faciliter l'expulsion des tissus mous encombrants présents dans l'acétabulum.
L'utilisation de pansements de contention type pansement de Ehmer est déconseillée. Ce type de pansement ne permet pas de diminuer le taux de récidive, est mal toléré et peut être à l'origine de complications (plaies, zone de macération).
Suite à la réduction de la luxation, le respect d'une période de repos strict (confinement dans une cage) durant 6 semaines est obligatoire.
Le taux de récidive est très important. Il convient de réserver cette technique aux cas présentés avec une luxation très récente (moins de 3 jours), sans fractures associées et avec un acétabulum de forme normale ou en cas de budget limité du propriétaire.
III. Renforcer : stabilisation chirurgicale des luxations coxo-fémorales
La réduction à foyer ouvert, chirurgicale, est conseillée en cas d'échec de la réduction orthopédique de la luxation. Une étude rétrospective, réalisée chez des chiens au sein de l'École Nationale Vétérinaire de Toulouse a montré, à propos de 33 cas traités par réduction orthopédique et 47 traités par réduction ouverte, outre un pourcentage de récidive très en faveur du traitement par réduction ouverte (3,5% contre 18,5% par réduction fermée), ainsi qu'un développement arthrosique et un taux de lyse sévère de la tête du fémur bien en faveur du traitement chirurgical.
Ces résultats sont expliqués par le nettoyage systématique et méticuleux de la cavité acétabulaire. Les fragments de ligament rond, les fragments de capsule et les caillots sanguins sont retirés, le cotyle est nettoyé.
Une fois la réduction de la luxation réalisée, si la capsule n'est pas trop endommagée, une capsulorraphie est réalisée à l'aide de points simples ou en croix. La stabilité est testée en mettant en place un davier à pointe sur le grand trochanter et en appliquant une traction sur ce davier. La capsulorraphie est suffisante dans 83 à 90% des cas.
Si elle n'est pas suffisante ou si la capsule articulaire est trop endommagée, une technique de stabilisation peut être envisagée. Il en existe de nombreuses, extra-articulaires (suture ilio-fémorale, prothèse de capsule) ou intra-articulaires (enclouage trans-articulaire, prothèse de ligament rond). Toutes ces techniques présentent des taux de succès entre 80 et 90% de bon à excellents résultats.
1. Techniques de renforcement extra-articulaires
Des techniques extra-articulaires permettent de s'affranchir de la mise en place de prothèses intra-articulaires.
Les prothèses de capsules utilisent 2 vis ou de 2 ancres dorsale et crâniale, soit à 10 et 13 heures pour une hanche gauche ou 11 et 14 heures pour une hanche droite. Ces vis, de 2 ou 2,4 mm chez les chat, associées à des rondelles crantées, ou ces ancres, servent de point d'ancrage au passage de 2 boucles de prothèses de nylon servant de prothèse de capsule. Ces prothèses sont donc ancrées au-dessus de l'acétabulum. Elles sont ensuite croisées en forme de 8. Elles viennent enfin s'ancrer dans un tunnel percé dans le col du fémur, perpendiculairement à son axe.
Cette technique donne d'excellents résultats mais demande une technicité avancée.
Une autre technique extra-capsulaire, la suture ilio-fémorale est plus simple et permet la prévention de reluxation en entrainant une rotation interne et une abduction du fémur. Une prothèse de nylon est tendue entre un trou percé dans le corps de l'ilium, juste crânialement à l'acétabulum, au niveau de l'insertion du muscle droit de la cuisse, et un trou percé à la base du grand trochanter, caudo-cranialement. La prothèse est tendue sous la masse des fessiers. Elle est rapide et simple à mettre en œuvre mais expose à un taux plus important de reluxation allant de 0 à 30% selon les études.
2. Techniques de renforcement intra-articulaires
L'enclouage trans-articulaire est réalisé après une réduction de la luxation à foyer fermé ou à foyer ouvert. Une broche de Kirschner de 1,6 à 2 mm est mise en place par voie normograde, depuis la face latérale du fémur au niveau du troisième trochanter, à travers le col et la tête du fémur au niveau de la fovea capitis puis jusqu'à la face médiale de l'acétabulum. La broche est censée dépasser de 5 mm. Un contrôle doit être fait par palpation transrectale au cours de la pose par un assistant.
Sissener et al. (JSAP 2009) rapportent sur 20 chats suivis à 21 mois post-opératoire un résultat clinique bon ou excellent dans 85% des cas. Cependant, cette technique nécessite une seconde intervention de retrait du clou après 2 à 3 semaines et les auteurs rapportent une progression de l'arthrose dans 40% des cas et un taux de complications proche de 30%. De plus, le risque de lésion de la surface articulaire de l'acétabulum ou de la tête du fémur, de perforation rectale, ou de rupture d'implants est important.
La prothèse de ligament rond ou toge pinning correspond à une prothèse de nylon tendue depuis la face latérale du fémur, jusqu'à la fovea capitis à travers le col du fémur jusqu'à un trou percé dans l'acétabulum où la prothèse est maintenue sur la face médiale à l'aide d'une ancre.
Cette technique est correctement décrite chez les chiens et a montré des résultats intéressants chez les chats. Le fil utilisé peut être de nature variée : il peut s'agir d'un fil tressé en polyester, d'un monofilament en nylon, d'un fiberwire. Cette prothèse du ligament rond permet une mobilisation immédiate post-opératoire avec un taux de récidive de 5 à 10%. Cette technique est très intéressante, notamment chez les animaux polytraumatisés.
Les complications potentielles incluent une rupture précoce de la prothèse, une récidive de la luxation, des lésions du rectum ou du nerf sciatique, des lésions de la surface cartilagineuse… De plus, en chirurgie humaine et dans le cadre de la rupture du ligament croisé, l'utilisation de prothèses synthétiques en intra-articulaire est bannie du fait des potentielles complications liées à leur utilisation.
Les retours d'expériences des chirurgiens qui pratiquent cette approche classiquement sont bons mais rapportent des lésions tardives liées à la présence de la prothèse. Une option serait de retirer la prothèse 4 à 6 semaines après sa mise en place. Cette approche demande à être validé.
Dans les cas d'atteintes chroniques, de présence d'arthrose sévère, de fractures acétabulaires comminutives concomitantes de la luxation ou encore de lésions secondaires du col du fémur, des techniques dites de sauvetage sont envisageables.
IV. Remplacer : la prothèse totale de hanche (PTH)
La PTH est le traitement de recours en cas d'échec des autres méthodes, de luxation irréductible, de dysplasie sévère ou de fracture complexe de l'acétabulum ou de la tête fémorale.
Elle permet un rétablissement fonctionnel optimal avec un confort articulaire durable. Elle reste cependant coûteuse et techniquement exigeante.
V. Tout couper : exérèse de la tête et du col du fémur
La résection de la tête et du col fémoral est une solution palliative visant à réduire la douleur sans rétablir une biomécanique normale. Elle est indiquée lorsque la PTH est contre-indiquée ou non envisageable pour des raisons économiques. Les résultats sont très variables : le retour à une fonction acceptable dépend sans doute moins du poids que ce que l'on a pensé dans le passé. L'état musculaire et de la motivation des propriétaires à stimuler la rééducation sont sans doute plus importants.
Si la procédure engendre une satisfaction client importante (> 90%), le résultat fonctionnel chez le chien n'est bon que dans 38% des patients, satisfaisant dans 20% et mauvais dans 42% des cas. Le mythe consistant à penser que cette technique fonctionne mieux sur des animaux de petits gabarits tient plus du fait qu'une boiterie est plus visible sur un gros chien à la démarche lente qu'un petit animal au pas rapide qu'à une réalité objective. Chez le chat, une étude récente sur 17 chats a montré qu'au long terme : 48% des chats avaient une boiterie visible par le vétérinaire, 77% des chats avaient une douleur à la manipulation et 100% des chats avaient un appui anormal.
Conclusion
Les luxations coxo-fémorales sont des affections fréquentes. Elles sont classiquement cranio-dorsales. Le traitement est en première intention chirurgical. Il nécessite l'abord de l'acétabulum suivi de son nettoyage méticuleux avant une stabilisation de la tête du fémur réduite. Dans les cas de luxations très récentes ou dans les cas de budget restreint des propriétaires, une réduction orthopédique peut être tentée tout en sachant que cette technique est associée à un taux de récidive important.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Luxation du coude : faut-il toujours reconstruire les ligaments ?
Montréal, Canada
I. Introduction
La luxation traumatique du coude (souvent latérale) chez le chien et le chat résulte généralement d'un traumatisme important (accident de la route, chute). Elle est plus fréquente chez le chien, rare chez le chat.
Il existe plusieurs formes selon la direction de la luxation (latérale, médiale, caudale), voire Monteggia ou luxation divergente.
II. Réduction fermée
À tenter en priorité : cette approche constitue le premier volet de la démarche thérapeutique.
Résultats cliniques : la réussite de la réduction fermée est bonne, lorsqu'elle est aigüe. Si la luxation est chronique, la réduction fermée est plus difficile voire impossible. Résultats cliniques à long terme généralement très bons chez le chien et excellents le plus souvent chez le chat.
Facteur pronostique : la stabilité articulaire immédiate post-réduction est un bon indicateur de bon pronostic.
Gestion postopératoire : immobilisation avec bandage type Spica ou plâtre (splint), généralement pendant 2 à 4 semaines.
III. Indications et techniques de réduction ouverte
1. Quand opérer ?
Indications majeures : échec de réduction fermée, instabilité résiduelle immédiatement après réduction, reluxation précoce, lésion avulsive/rupture complète d'un ligament collatéral, luxation ancienne ou atypique (divergente, caudale). Ces situations sont associées à des résultats moins bons si l'on persiste en traitement conservateur au préalable. Le taux de complications et d'arthrose est alors plus élevé.
2. Voies d'abord et évaluation per-opératoire
- Luxation latérale : arthrotomie latérale (entre anconéus et ext. carpi ulnaris), inspection du ligament collatéral latéral (LCL), du processus anconé, du bord latéral du condyle huméral ;
- Luxation médiale : arthrotomie médiale (entre fléchisseur ulnaire du carpe et pronateur rond), inspection du ligament collatéral médial (MCL) et de l'épicondyle médial.
Rechercher systématiquement : avulsion ligamentaire (fragment épicondylien), rupture intrasubstance, lésions capsulaires et cartilagineuses ; tester la stabilité en varus/valgus en flexion.
3. Réparation/refixation du ligament collatéral
a) Réinsertion d'une avulsion ligamentaire
- Principe : réduction anatomique du fragment avulsé de l'épicondyle (latéral ou médial) et fixation par vis + rondelle ou mini-plaque ; réparation capsulaire associée ;
- Pourquoi : restaure l'origine ligamentaire et l'axe de contrainte ; souvent suffisant si les tissus sont de bonne qualité.
b) Réparation d'une rupture ligamentaire
- Suture primaire du ligament (boucles verrouillées) + renfort prothétique si le tissu est fragilisé ;
- Tunnels transcondyliens (humerus) + trans-olécrâniens/ulnaires pour passer une suture haute résistance (configuration en huit ou biaxiale) et recréer l'isométrie des collatéraux.
c) Augmentations prothétiques : ancrage et sutures haute résistance
- Ancrages osseux + suture ;
- Technique : ancrages filetés (knotless ou noués) implantés aux insertions humérales/ulnaires du LCL / MCL ; pontage avec FiberWire/FiberTape ou suture tressée similaire, parfois complété par une vis d'ancrage corticale ;
- Indications : rupture complète, qualité tissulaire médiocre, luxations récidivantes ;
- Résultats rapportés (chiens) : séries et cas montrent une stabilisation fiable du LCL avec récupération fonctionnelle satisfaisante à moyen-terme.
Astuce per-op : vérifier l'isométrie de la boucle prothétique en faisant un arc de flexion–extension ; ajuster la tension en légère flexion (≈45–60°) pour éviter la sur-contrainte en extension. (Technique issue des descriptions avec tunnels transcondyliens et ancrages).
d) Stabilisations transarticulaires temporaires - Fixateur externe transarticulaire (TA-ESF)
- Mise en place : deux ou trois tiges proximales dans l'humérus distal et deux tiges proximales radius/ulna, connectées de chaque côté (type II).
- L'articulation est maintenue en 35–45° de flexion pendant 2–3 semaines, puis retrait progressif.
e) Luxations atypiques : protocole spécifique
- Luxation divergente (chien) ;
- Concept : après réduction, stabilisation mini-invasive par K-wire dirigé de l'ulna proximal vers le col radial (ou par vis corticales) pour réaligner le pivot ulno-huméral et neutraliser les forces de divergence ; immobilisation courte derrière ;
- Montages « TightRope »/suture-bouton ;
- Utilisés de manière anecdotique pour verrouiller l'arc huméro-ulnaire/radial dans les luxations complexes ou récidivantes.
f) Soins postopératoires & complications
- Immobilisation : attelle/plâtre ou TA-ESF 2–4 semaines selon la stabilité per-op et la qualité des tissus ; rééducation progressive ensuite ;
- Complications : raideur, ostéoarthrose, reluxation (surtout si l'instabilité persiste), irritation des tissus mous ou infection de broches (ESF).
Les séries canines montrent de meilleurs résultats quand une réduction fermée stable est obtenue ; les cas nécessitant une réduction ouverte cumulent souvent des lésions plus graves, ce qui biaise le pronostic avec possible développement de l'OA et boiterie résiduelle.
IV. Points pratiques (chien vs chat)
- Chien : privilégier réparation anatomique + augmentation prothétique (ancres/tunnels) lorsque le collatéral est compromis ; recourir à une stabilisation transarticulaire si la stabilité reste douteuse per-op ;
- Chat : si l'articulation reste instable après réduction, l'option TA-ESF temporaire est bien documentée et donne de bons résultats, y compris pour les luxations caudales.
V. Recommandations pratiques
- Essayez toujours la réduction fermée dès que possible — si l'articulation est stable, poursuivez avec une immobilisation adaptée ;
- Évaluez la stabilité immédiatement après réduction par des tests adaptés ;
- Recourez à la chirurgie si instabilité persistante, reluxation ou réduction impossible ;
- Après toute intervention, immobilisation pendant 2 à 4 semaines minimum, suivi d'une rééducation progressive ;
- Considérez les techniques mini-invasives quand les ressources le permettent : ancrages, vis, stabilisations ciblées ;
- Informez le propriétaire sur le pronostic, la possibilité d'ostéoarthrose et la nécessité d'un suivi à long terme.
Bibliographie
- JIFCOVICI A. et al. Outcome of traumatic elbow luxation managed with temporary transarticular external skeletal fixation in cats. JFMS Open Reports (2024).
- WILLIAMS H. et al. Multi-centre retrospective study of the long-term outcome following reduction of traumatic elbow luxation in cats. J Small Anim Pract (2020).
- LOGOTHETOU V. et al. Use of bone anchors for the treatment of partial and complete tears of the lateral collateral ligament of the elbow in dogs. Vet Rec Case Rep (2022).
- KARACA A. et al. Minimally invasive treatment of divergent elbow dislocation in a dog. AUST Vet J (2025).
- MITCHELL K.E. Traumatic elbow luxation in 14 dogs and 11 cats. Aust Vet J (2011).
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Luxation tibiotarsienne : l'ABC de la prise en charge
Marcy l'étoile, France
I. Introduction
Les lésions traumatiques du tarse sont relativement fréquentes chez les carnivores domestiques. Elles sont dans la grande majorité secondaires à des traumatismes violents notamment des AVP. L'étage talocrural est largement affecté. Cependant, la complexité anatomique du tarse rend leur exploration et leur traitement délicats. Une démarche diagnostique et thérapeutique rigoureuse doit permettre d'offrir le traitement le plus adapté.
II. Rappels
Le tarse est une articulation composée de sept os maintenus ensemble par de nombreux ligaments. Ces ligaments sont renforcés par le manchon fibro-cartilagineux de la capsule articulaire qui s'étend du tibia distal et s'attache au niveau des métatarses proximaux. Ce fibrocartilage de soutien contient tous les ligaments du tarse et est beaucoup plus fort et mieux développé sur la partie plantaire de l'articulation. Il est capital pour la stabilité du tarse.
Sept os composent l'articulation du tarse : le talus, le calcanéum, l'os central du tarse, le quatrième os du tarse et les premier, deuxième et troisième os du tarse. Ces os forment trois rangées irrégulières, le talus et le calcanéum étant situés dans la rangée proximale et les autres os dans les rangées distales.
L'ensemble de l'articulation fonctionne comme une charnière (gynglymus) avec la majorité des mouvements (90 %) située uniquement au niveau de l'articulation tibio-tarsienne.
La majorité des lésions du tarse impliquent les ligaments collatéraux des articulations tarsocrurales ou les ligaments plantaires et le fibrocartilage du tarse. Les ligaments collatéraux tibiaux et fibulaires ont des parties longues et courtes qui sont importantes pour la fonction articulaire et doivent être reconstruits de manière satisfaisante.
III. Bilan général
Les luxations du tarse sont dans la majorité des cas, la conséquence d'un traumatisme violent, ainsi un bilan complet (thoracique, abdominal, neurologique et orthopédique) est indispensable et reste prioritaire.
Ainsi, lorsque le patient a été stabilisé, la prise en charge de la luxation peut commencer. L'examen du membre atteint doit permettre d'évaluer les lésions orthopédiques, cutanées, vasculaires et/ou nerveuses.
De par sa position et sa faible couverture musculaire, les lésions du tarse sont fréquemment ouvertes. Il est actuellement prouvé qu'un traitement rapide et adapté de la plaie diminue de façon notable les complications infectieuses ultérieures. Un traitement antibiotique large spectre par voie intraveineuse est indiqué le plus précocement possible. Si possible l'os doit être recouvert et la luxation réduite. Ensuite, une tonte large et une désinfection agressive de la plaie est réalisée. Si besoin, un bandage contentif et protecteur d'attente est alors mis en place en attendant la suite de la prise en charge ultérieure.
Lors de traumatisme sévère du tarse, il est important d'évaluer la vascularisation et l'innervation distale du membre qui peuvent être lésées et obérer la récupération.
IV. Bilan orthopédique
La palpation attentive du tarse doit permettre de localiser l'étage lésionnel et les éléments de soutien lésés. La palpation après réduction est essentielle à la compréhension des instabilités. Une évaluation radiographique sera bien sûr ensuite nécessaire.
L'examen radiographique doit permettre de rechercher d'éventuelles fractures associées, notamment des malléoles. Des vues en contraintes permettent de déterminer si besoin les lésions ligamentaires.
Dans la majorité des cas, les luxations tibiotarsiennes sont la conséquence d'une fracture de la malléole latérale et d'une lésion du collatéral médial.
V. Options thérapeutiques
Une fois l'articulation réduite, les luxations tibiotarsiennes relèvent du traitement chirurgical.
Il débute par une réparation des éléments de soutien :
- Ostéosynthèse des malléoles
- Ligamentoplastie
- Suture capsulaire et ligamentaire
Ces réparations sont ensuite protégées par une immobilisation du tarse :
- Bandage de type Robert Jones modifié
- Résine
- Vis calcanéotibiale
- Broche transarticulaire
- Fixateur externe
Lors de lésions non réparables de l'articulation, une arthrodèse totale du tarse sera indiquée.
VI. Critères de choix
Le choix d'une technique doit être adapté à chaque situation. Il convient de prendre en considération :
- La sévérité des lésions cutanées
- Les lésions osseuses
- Les lésions vasculo-nerveuses
- L'espèce
De manière générale, lors de fracture des malléoles, il est conseillé de réparer ces dernières afin de stabiliser le tarse. L'utilisation de broche et hauban est la technique de stabilisation la plus fréquente.
Au contraire, lors de lésions cutanées sévères, une stabilisation par fixateur externe est le plus souvent indiquée. La réparation ligamentaire sera envisagée, si besoin, une fois la contamination et la plaie gérées. Il est à noter que chez le chat, la réparation des ligaments est souvent non nécessaire étant donné que la simple stabilisation par fixateur externe apporte dans la majorité des cas de bons résultats.
Si la stabilisation postopératoire est la règle dans la majorité des cas, des techniques permettant de s'affranchir de celle-ci ou du moins de la limiter sont en développement.
Ainsi, lors de luxation tibiotarsienne, une évaluation complète de l'articulation est indispensable pour choisir le traitement le plus adapté. La présence d'une plaie en regard de l'articulation complexifie la prise en charge.
Liens d'intérêt : Consultant ArthrexConsultant PorteVetConsultant NovetechConsultant ZoetisConsultant Elanco
📃 Malpropreté du lapin : lien avec un environnement et un mode de vie inadaptés
Le Cannet, France
I. Introduction
La malpropreté constitue un motif fréquent de consultation en pratique vétérinaire NAC. Si elle est parfois perçue comme un défaut d'éducation ou un trouble du comportement, elle traduit le plus souvent une inadéquation entre les besoins fondamentaux du lapin et les conditions de vie qui lui sont imposées.
II. Un animal naturellement propre
Le lapin est une espèce qui tend spontanément à uriner et déféquer dans une zone précise, comme le souligne Harcourt-Brown (2013). L'installation d'un bac garni de litière absorbante, idéalement accompagné de foin car les lapins aiment manger en éliminant, facilite l'apprentissage. Il est recommandé de placer le foin dans un ratelier pour éviter qu'il ne soit souillé trop rapidement. En conditions normales, la malpropreté n'est donc pas une fatalité mais un signe d'alerte d'un environnement ou d'un mode de vie inadaptés.
III. Influence du logement et de l'aménagement
Les conditions de logement constituent un facteur déterminant. Harcourt-Brown (2013) insiste sur le fait que les cages trop petites empêchent le lapin de séparer les zones de repos, d'alimentation et d'élimination, ce qui perturbe le comportement de propreté. L'étude de Rioja-Lang et al. (2019) confirme ce constat : de nombreux lapins de compagnie sont gardés dans des cages plus petites que les standards minimaux appliqués en laboratoire. Ces espaces restreints favorisent l'inactivité, les stéréotypies, et empêchent l'expression des comportements naturels tels que sauter, courir ou se redresser. Le manque d'espace et l'absence d'enrichissement conduisent alors à une élimination anarchique, faute de pouvoir organiser l'espace.
IV. Facteurs sociaux et comportements de marquage
La dimension sociale joue également un rôle central. D'après Rioja-Lang et al. (2019), 45% des lapins de compagnie sont gardés seuls, alors qu'il s'agit d'une espèce grégaire. L'isolement favorise l'ennui, la frustration et des comportements anormaux tels que le marquage urinaire. MCMahon & Wigham (2020) observent que les lapins logés en free-roam et bénéficiant d'interactions régulières avec leurs propriétaires présentent de meilleurs scores de bien-être que ceux confinés en hutch. La stérilisation est également un facteur clef : Harcourt-Brown (2013) rapporte que les animaux entiers, notamment les mâles à la puberté, marquent davantage leur territoire par des jets d'urine et des crottes hors du bac.
V. Alimentation et conséquences sur la propreté
L'alimentation influence directement la propreté par ses effets sur la santé digestive et locomotrice. Harcourt-Brown (2013) décrit les cas fréquents de cæcotrophes non consommés, confondus avec une diarrhée par les propriétaires. Ce phénomène est lié à l'obésité, aux douleurs (arthrose, pododermatite) ou à une alimentation déséquilibrée, et conduit à des souillures chroniques. Selon Rioja-Lang et al. (2019), environ 20% des lapins reçoivent encore des mélanges de graines pauvres en fibres et riches en amidon. Ces régimes favorisent l'obésité et les troubles digestifs, aggravant la malpropreté. MCMahon & Wigham (2020) confirment que les lapins nourris principalement au foin/herbe ont de meilleurs scores de bien-être et de santé, alors que ceux recevant un régime inadapté présentent davantage de problèmes, dont les souillures par cæcotrophes non ingérés.
VI. Malpropreté d'origine médicale
La malpropreté peut également être la conséquence de pathologies. Harcourt-Brown (2013) cite les affections urinaires (cystite, urolithiase, sludge urinaire), les troubles locomoteurs (arthrose, pododermatite) et l'obésité comme causes fréquentes de souillures périnéales. Ces situations entraînent des urines stagnantes, des souillures chroniques et augmentent le risque de myiase. L'incapacité à atteindre ou consommer les cæcotrophes, souvent liée à la douleur ou au surpoids, est une autre cause majeure de malpropreté.
VII. Connaissances et attentes des propriétaires
Le manque d'information et d'éducation des propriétaires est un fil conducteur majeur. Rioja-Lang et al. (2019) soulignent que l'inexpérience des nouveaux acquéreurs, souvent mal conseillés par les animaleries ou les éleveurs, est une cause fréquente de logement et de soins inadaptés. MCMahon & Wigham (2020) montrent que les propriétaires percevant leur lapin comme un animal intelligent et sensible fournissent plus d'enrichissement et d'interactions, réduisant significativement les comportements indésirables, dont la malpropreté. Enfin, la banalisation du lapin comme « animal peu coûteux » contribue à un déficit de soins vétérinaires réguliers, aggravant les problèmes liés aux affections urinaires ou locomotrices (Rioja-Lang et al., 2019).
VIII. Prise en charge médicamenteuse et approches complémentaires
Bien que la prise en charge de la malpropreté du lapin repose avant tout sur la correction des facteurs environnementaux, sociaux et médicaux, certains outils complémentaires peuvent être envisagés dans des cas particuliers.
Une étude récente (Asproni et al., 2024) a montré que l'utilisation continue de la phéromone d'apaisement du lapin (Rabbit Appeasing Pheromone, RAP) permettait de réduire le stress lié aux soins vétérinaires et à la vaccination. Les lapins exposés à la RAP étaient moins inhibés, plus confiants et plus stables au fil des visites que les lapins témoins. Même si ces résultats concernent le contexte aigu du soin et non spécifiquement la malpropreté, ils ouvrent une piste intéressante quant à l'utilisation des phéromones pour réduire les comportements liés à l'anxiété et au stress.
En revanche, il n'existe actuellement aucune étude validant l'efficacité de la phytothérapie dans le traitement de la malpropreté ou des troubles d'élimination chez le lapin. Son utilisation ne peut donc pas être recommandée à ce jour.
IX. Conclusion
La malpropreté du lapin est rarement un simple problème « d'éducation ». Elle constitue au contraire un signal d'alarme, révélant le plus souvent une inadéquation entre les besoins biologiques et sociaux de l'animal et son environnement. Les études récentes et les manuels de référence convergent vers une même conclusion : espace, alimentation, socialisation, enrichissement et soins médicaux sont les piliers de la propreté et du bien-être du lapin. Le rôle du vétérinaire est essentiel, à la fois pour exclure les causes médicales, et surtout pour éduquer les propriétaires à un mode de vie respectueux des besoins fondamentaux du lapin.
Bibliographie
- HARCOURT-BROWN F. Textbook of Rabbit Medicine. 2e éd. Elsevier, 2013.
- MCMAHON S.A., WIGHAM E.E. "All Ears": A Questionnaire of 1516 Owner Perceptions of the Mental Abilities of Pet Rabbits, Associations with Owner Care and Rabbit Welfare. Animals. 2020;10(10):1730.
- RIOJA-LANG F., BACON H., CONNOR M., DWYER C.M. Rabbit welfare: determining priority welfare issues for pet rabbits using a modified Delphi method. Vet Rec Open. 2019;6:e000363.
- ASPRONI P., PIOTTI P., DALL'OLIO S., BARAGLI P., PAGEAT P., MAZZOLA S.M. Helping Rabbits Cope with Veterinary Acts and Vaccine-Related Stress: The Effects of the Rabbit Appeasing Pheromone. Animals. 2024;14(21):3549
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Médecine complémentaire : acupuncture et phytothérapie dans la gestion de la douleur chronique
Avrille, France
I. Introduction
La douleur chronique musculosquelettique ou inflammatoire, constitue un enjeu majeur tant en santé humaine qu'en médecine vétérinaire. Les plantes médicinales permettent d'agir sur différentes cibles grâce à leurs multiples composants. L'application locale d'huiles essentielles commence à être étudiée en médecine humaine, avec des effets intéressants mais qui restent à étayer chez les animaux. L'acupuncture est une option non pharmacologique de plus en plus explorée et utilisée dans la prise en charge des douleurs chroniques. Plusieurs études, tant en médecine humaine que vétérinaire, ont montré des effets bénéfiques, notamment avec l'utilisation de l'électro-acupuncture, qui module certaines voies de la douleur et régule des processus inflammatoires. Chez le chien, des améliorations de la mobilité et de la qualité de vie ont été rapportées dans certaines affections musculosquelettiques, bien que les données restent encore hétérogènes et nécessitent des essais contrôlés de plus grande ampleur. Concernant le cannabidiol (CBD), malgré un engouement croissant, les preuves cliniques restent limitées et parfois contradictoires. Quelques études suggèrent un effet potentiel sur la douleur chronique et l'anxiété chez l'animal, et des emplois ponctuels sont rapportés, notamment dans la prise en charge des douleurs neuropathiques chez le chat. L'absence de standardisation des produits et les incertitudes réglementaires compliquent l'évaluation et l'utilisation du CBD en pratique vétérinaire.
II. Phytothérapie
Les plantes médicinales peuvent apporter une prise en charge complémentaire dans la gestion de la douleur chronique, soit par un effet anti-inflammatoire direct, avec des plantes comme le curcuma (Curcuma longa), la boswellie (Boswellia serrata), soit par une action plus axée sur le système adaptogène, avec des plantes comme l'ashwadandha (Whitania somnifera). Les méta-analyses cliniques chez l'homme soutiennent de plus en plus l'utilisation de certaines plantes adaptogènes, et les données émergentes en médecine vétérinaire ouvrent la voie à des applications intégratives dans la prise en charge de la douleur chronique chez les animaux.
Les plantes à effet anti-inflammatoire direct ciblent les voies de l'inflammation (NF-κB, COX-2, 5-LOX, cytokines), à l'origine d'une réduction de la douleur. Le Curcuma (Curcuma longa) a fait l'objet de plusieurs méta-analyses d'essais randomisés en médecine humaine, montrant une réduction significative de la douleur dans l'arthrose du genou, avec un profil de tolérance supérieur aux AINS. Des résultats similaires ont pu être retrouvés chez le chien [1]. Des études sont également disponibles chez l'homme et l'animal sur les effets bénéfiques de Boswellia serrata dans plusieurs affections à l'origine de douleur chronique comme l'arthrose ou des inflammations digestives [2].
Les plantes adaptogènes peuvent moduler la réponse au stress, ayant un effet indirect sur la perception de la douleur chronique. Les études disponibles chez le chien sont limitées (une étude sur l'ashwagandha), avec une amélioration de la tolérance au stress et une réduction des marqueurs de l'inflammation chronique [3].
III. Utilisation des huiles essentielles en application locale
L'application locale d'huiles essentielles (HE) est explorée pour la prise en charge des douleurs chroniques, notamment musculosquelettiques et inflammatoires. Certaines HE comme la lavande (Lavandula angustifolia), la menthe poivrée (Mentha piperita), la gaulthérie (Gaultheria procumbens) et son composant majoritaire, le salicylate de méthyle) ou l'eucalyptus citronné (Eucalyptus citriodora), présentent des propriétés antalgiques, anti-inflammatoires et myorelaxantes. Elles modulent certains récepteurs nociceptifs (TRPV1, TRPM8), entrainant une réduction de la production de cytokines pro-inflammatoires. Des méta-analyses humaines rapportent des bénéfices de l'application topique ou de massages aux HE de lavande ou de menthe poivrée dans l'arthrose, les céphalées ou les douleurs chroniques. Les données vétérinaires sont rapportées dans des livres mais n'ont pas encore fait l'objet de publications dans la littérature scientifique. Leur utilisation nécessite une certaine connaissance avec des dilutions appropriées pour diminuer les risques d'irritation cutanée ; leur emploi doit s'appuyer sur des produits chémotypés, correctement dilués et de qualité pharmaceutique [4].
IV. Acupuncture
L'utilisation de l'acupuncture, notamment pour la prise en charge de la douleur chronique, est de plus en plus répandue en Europe et au Royaume-Uni [5]. L'insertion d'une aiguille d'acupuncture active différentes fibres musculaires, comme les fibre Aδ, ce qui entraine une activation des interneurones à l'origine de la production d'enképhalines. Les mécanismes anti-douleur initiés par l'acupuncture peuvent aussi être expliqués par l'activation d'un contrôle inhibiteur diffus à l'origine d'une régulation du message nociceptif.
Des données plus probantes ont été mises en évidence avec l'utilisation de techniques telles que l'électro-acupuncture (EA) qui provoquerait une libération de différents types de neuropeptides analgésiques et de dérivés d'opiacés endogènes. Des études ont montré qu'en fonction des différentes fréquences appliquées, il pouvait y avoir libération des différents médiateurs comme l'enképhaline, la bêta endorphine, l'endomorphine à 2 Hz et la dynorphine à 100 Hz.
D'autres mécanismes d'action ont été explorés, comme la modulation du système adrénergique ou de la voie de signalétique de la sérotonine.
Les effets modulateurs de l'EA sur les IL et le TNF-α ont été documentés à l'aide de divers modèles expérimentaux de douleur arthrosique, de douleur inflammatoire et de douleur neuropathique [6].
V. Cannabidiol
Récemment The Journal of Pain a recensé 16 études sur le cannabidiol (CBD) dont 15 ne montraient pas d'effet supérieur à celui d'un placebo, avec de plus une balance bénéfice/risque incertaine [7]. Chez l'animal, malgré une hétérogénéité des résultats, certains produits semblent montrer une efficacité pour la prise en charge des douleurs chroniques [8]. Des utilisations anecdotiques ont été rapportées dans la prise en charge des douleurs neuropathiques chez le chat [9].
La douleur chronique nécessite une approche multimodale combinant traitements conventionnels et options complémentaires. Les plantes médicinales, certaines huiles essentielles et l'acupuncture offrent des bénéfices potentiels, via des mécanismes anti-inflammatoires et neuromodulateurs, avec des preuves particulièrement encourageantes pour l'électro-acupuncture. Le cannabidiol, malgré un intérêt croissant, reste limité par des données cliniques contradictoires et un cadre réglementaire incertain. L'intégration raisonnée de ces approches, encore à consolider par des essais cliniques de qualité, ouvre la voie à une prise en charge plus globale et personnalisée en médecine vétérinaire.
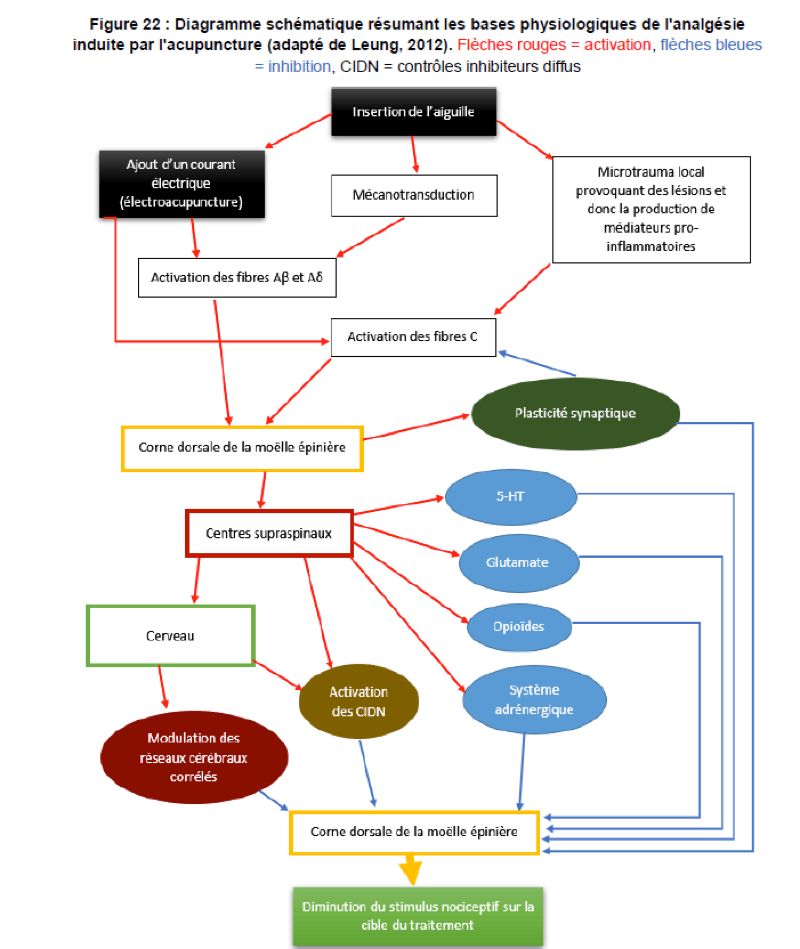
Figure 1
Bibliographie
- KĘPIŃSKA-PACELIK J, BIEL W. Turmeric and Curcumin-Health-Promoting Properties in Humans versus Dogs. Int J Mol Sci. 2023;24(19), 14561,1-24
- REICHLING J, et coll. Dietary support with Boswellia resin in canine inflammatory joint and spinal disease. Schweiz Arch Tierheilkd. 2004;146(2):71-79.
- BHARANI KK, et coll. Effects of ashwagandha (Withania somnifera) root extract on aging-related changes in healthy geriatric dogs: a randomized, double-blinded placebo-controlled study. Vet Med Sci. 2024;10(5) e1556, 1-13
- BAKÓ E, et coll. Efficacy of Topical Essential Oils in Musculoskeletal Disorders: systematic Review and Meta-Analysis of Randomized Controlled Trials. Pharmaceuticals. 2023;16(2):144.
- LAI ML, et coll. A survey study on the use of veterinary acupuncture in the UK and Europe. Vet Anaesth Analg. 2025;52(5):604-612.
- SZYMKOWIAK M. Étude préliminaire de l'intérêt de l'acupuncture dans la gestion des signes de dorsalgie chez les chevaux ayant une activité de course de haies. Thèse d'exercice vétérinaire. 2023. 86p.
- MOORE A, STRAUBE S, FISHER E, ECCLESTON C. Cannabidiol (CBD) Products for Pain: ineffective, Expensive, and With Potential Harms. The Journal of Pain. 2024;25(4):833-842. doi:10.1016/j.jpain.2023.10.009
- CORSATO ALVARENGA I, PANICKAR KS, HESS H, MCGRATH S. Scientific Validation of Cannabidiol for Management of Dog and Cat Diseases. Annu Rev Anim Biosci. 2023;11:227-246
- RUSBRIDGE C. Neuropathic pain in cats: mechanisms and multimodal management. J Feline Med Surg. 2024;26(5), 1-19
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Mesures radiographiques de l'atrium gauche et du coeur
Lyon, France
I. Introduction
La radiographie du thorax est utile lors d'exploration de pathologie cardiaque. Elle permet d'évaluer la silhouette cardiaque mais aussi d'explorer les signes de décompensation cardiaque. L'échocardiographie reste le gold standard dans l'évaluation de la taille du cœur.
II. Évaluation de la taille de la silhouette cardiaque
1. Évaluation par rapport à la taille du thorax
La taille de la silhouette cardiaque doit être évaluée dans son entièreté. Sur les vues de profil, la silhouette cardiaque occupe 2,5 (longiligne) à 3,5 (brévilignes) espaces intercostaux chez les chiens et 2 à 2,5 espaces intercostaux chez les chats. Il doit occuper moins de 70% de la hauteur du thorax. Sur les vues de face, le cœur occupe moins de 2/3 de la largeur du thorax chez le chien et moins de 50% de la largeur du thorax chez le chat.
Ces paramètres sont influencés par la race, l'âge et le score corporel des patients ainsi que par la phase respiratoire.
2. Indice de Buchanan : rapport cœur/vertèbre (VHS)
Cet indice a été le premier mis en place. Il permet d'évaluer la taille du cœur par rapport aux vertèbres thoraciques. Pour le calculer, il faut mesurer le grand axe du cœur en partant de la base à l'apex puis sa perpendiculaire dans l'axe crânio-caudal de la silhouette cardiaque, ventralement à la veine cave caudale. Les mesures sont ensuite reportées sur la colonne vertébrale en partant de T4. La valeur de référence pour un chien standard est de 9,7 +/- 0,5. Une valeur supérieure à 10,5 est en faveur d'une cardiomégalie chez 98% des chiens de l'étude. Cependant, il existe de grandes variations en fonction de la race du chien. Chez les chats, elle est de 7,5 +/- 0,3. On considère une cardiomégalie quand le VHS est supérieur à 8. Ces mesures ont été calculées sur des vues de profil droit en inspiration.
Le VHS peut également être calculé sur la vue de face, mais ces mesures sont moins utilisées et ont plus de variations que celles calculées sur les vues de profil.
a) Intérêts cliniques
L'identification correcte d'une cardiomégalie sur des radiographies thoraciques n'augmente pas significativement en utilisant le VHS par rapport à une l'interprétation subjective. Le VHS est une méthode utile pour le suivi de la taille du cœur, que ce soit pour évaluer la progression de la maladie ou la réponse au traitement, mais ne doit pas être utilisé comme dépistage chez des chiens ne présentant pas de signe clinique. Le VHS est plus sensible lors de suspicion de maladie cardiaque entrainant une dilatation des cavités cardiaques comme les maladies valvulaires.
Comme toute mesure, le VHS doit être interprété avec précaution. Dans une étude menée chez des chiens atteints de MVDM, une cardiomégalie était présente à la radiographie chez 33% des chiens ayant un atrium et un ventricule gauche normaux à l'échocardiographie. De plus, 21% des chiens présentant une dilatation légère à modérée de l'atrium gauche et 14% des chiens présentant une dilatation sévère de l'atrium gauche avaient un VHS normal.
Plusieurs études se sont intéressées aux valeurs du VHS permettant de faire la différence entre les différents stades de MVDM. Les valeurs oscillent entre 10,7 et 12 avec des sensibilités et spécificités variables. Le consensus ACVIM considère un VHS de 11,5 (ou équivalent rapporté à la race) chez un patient souffrant de MVDM comme étant en faveur d'un stade B2.
Le VHS peut être utilisé pour faire la différence entre les chiens ayant une toux d'origine cardiaque ou non. Les chiens présentant une toux non cardiaque ont un VHS significativement plus faible (11 ± 0,9) que les chiens présentant une toux secondaire à une cause cardiaque (12,8 ± 0,9). Une valeur seuil de 11,4 permettrait de distinguer les chiens ayant une toux cardiaque de ceux présentant une toux non cardiaque, avec une sensibilité de 92% et une spécificité de 75%. De même, la mesure du VHS a été évaluée chez des chiens présentant une détresse respiratoire d'origine cardiaque ou non. Le VHS est plus élevé chez les chiens atteints d'insuffisance cardiaque congestive, avec une médiane de 12,9 (11,9-14,1) par rapport aux chiens présentant une détresse respiratoire non cardiaque, avec une médiane de 11,1 (10,1-11,8).
b) Variation des mesures
La mesure du VHS est fortement influencée par la forme et la taille des vertèbres. La présence de malformations congénitales ou de processus dégénératif peut être à l'origine d'une modification du VHS.
La mesure du VHS est influencée par le décubitus. Les valeurs sont un peu plus élevées lorsqu'elles sont réalisées sur des vues de profil droit par rapport aux vues de profil gauche. Les valeurs de référence ont été obtenues sur des vues de profil droit.
Le VHS est également influencé par le cycle cardiaque. Il est plus élevé en diastole qu'en systole (0,3). Il est également plus élevé en inspiration qu'en expiration. En combinant, l'effet du cycle cardiaque et de la respiration, les variations peuvent aller jusqu'à 1,1.
Chez le chat, le VHS décroit avec la croissance jusqu'à l'âge adulte.
Les chiens ayant un score corporel plus élevé peuvent avoir un VHS plus élevé.
Le VHS est une mesure relativement reproductible, bien qu'il existe des variations inter-observateurs, notamment en ce qui concerne le point de départ de la mesure verticale.
3. Autres mesures d'évaluation de la taille de la silhouette cardiaque
D'autres mesures existent. Elles sont pour l'instant moins développée et peu utilisée.
III. Évaluation de la taille de l'atrium gauche
1. Aire de projection de l'atrium gauche
L'atrium gauche se projette en région caudo-dorsale de la silhouette cardiaque, entre 12h et 2h sur la vue de profil chez le chien et le chat. Chez le chien, sur la vue de face, l'atrium se projette entre les bronches souches caudales et l'auricule se projette entre 2 et 3h. Chez le chat, l'atrium gauche et l'auricule gauche se projettent entre 1h et 2h sur la vue de face.
Comme pour la taille du cœur, l'atrium gauche peut être évalué de façon subjective (taille, forme, déplacement des structures adjacentes).
Le gold standard pour l'évaluation de la taille de l'atrium gauche est l'échocardiographie avec le calcul du ratio Ag/Ao. C'est cette mesure qui sert de mesure de référence.
2. Vertebral Left Atrial Size (VLAS)
De la même façon que pour le VHS, la taille de l'atrium peut être reportée sur la colonne thoracique pour obtenir un ratio. La méthode consiste à mesurer, sur une vue de profil droit, la distance entre la partie ventrale du centre de la bifurcation trachéo-bronchique et le bord caudal de l'atrium à son intersection avec le bord dorsal de la veine cave caudale. Cette distance est reportée le long de l'axe vertébral à partir de l'extrémité crâniale du corps vertébral de T4. La valeur médiane établie chez les chiens sains est de 2,1 (1,8-2,3). Comme pour le VHS, des valeurs ont été établies pour certaines races.
a) Intérêts cliniques
La mesure du VLAS est corrélée à la dilatation de l'atrium gauche à l'échocardiographie. La médiane rapportée pour les chiens atteints de MVDM au stade B1 est de 2,1 (2,0-2,4), pour le stade B2, elle est de 2,6 (2,3-2,9) et pour les stades C et D, elle est de 3,0 (2,7-3,6). La valeur seuil du VLAS est de 2,3 avec une sensibilité de 67% et une spécificité de 84%. Elle permet de détecter des dilatations de l'atrium gauche, lorsqu'elles sont modérées à marquées. Le VLAS permet également de suivre l'évolution de la taille de l'atrium et de différencier les stades de la MVDM, notamment le stade B1 du stade B2.
Le VLAS a été intégré dans le consensus ACVIM pour le diagnostic des MVDM de stade B2. Les recommandations ACVIM pour le diagnostic et le traitement de la MVDM donne une valeur seuil > 3 pour diagnostiquer des MVD de stade B2 en l'absence d'échocardiographie. Chez les chiens Cavalier King Charles Spaniel atteints de MVDM, la médiane des stades B1 est de 1,8 (1,7-2,1), tandis que celle des stades B2, est de 2,3 (1,9-2,6).
Le VLAS a également été évalué chez les chiens atteints de cardiomyopathie dilatée. La valeur médiane du VLAS pour les chiens atteints de cardiomyopathie dilatée préclinique est de 2,2 (1,0-2,5), tandis que pour les chiens atteints de cardiomyopathie dilatée clinique, elle est de 2,5 (2,2-2,9).
La mesure du VLAS a été évaluée chez des chiens présentant une détresse respiratoire cardiaque et non cardiaque. La médiane du VLAS chez les chiens présentant une détresse respiratoire d'origine non cardiaque est plus basse par rapport aux chiens présentant une détresse respiratoire d'origine cardiaque (2,1 (1,9-2,2) vs 3,0 (2,8-3,2)).
Par rapport au VHS, le VLAS semble être un prédicteur significativement plus précis de l'insuffisance cardiaque congestive, avec un seuil optimal > 2,3, une sensibilité de 93% et une spécificité de 82,5%.
b) Variation des mesures
Il ne semble pas y avoir d'influence de l'âge des chiens, leur sexe, leur note d'état corporel ou la conformation de leur thorax.
Le VLAS semble être plus élevé sur les vues latérales gauches par rapport aux droites. Le cycle cardiaque et la phase respiratoire ne semblent pas avoir d'influence sur la mesure du VLAS.
Tout comme pour le VHS, la mesure du VLAS est influencée par la forme et la taille des vertèbres.
IV. Conclusion
De nombreuses mesures cardiaques sont à notre disposition pour évaluer la taille de la silhouette cardiaque sur les radiographies thoraciques. Les plus usitées sont le VHS et le VLAS. Elles sont de bons outils pour déterminer la présence d'une pathologie cardiaque et pour suspecter des MVDM de stade B2 (VHS > 11,5 et VLAS > 3). Cependant, comme toutes mesures, elles dépendent de la qualité technique des radiographies et peuvent être influencées par de nombreux paramètres. De nombreuses superpositions existent entre valeurs saines et valeurs pathologiques. Les mesures ne doivent donc pas être utilisées seules. La forme du cœur et les structures adjacentes au cœur et notamment leur déplacement sont également des indicateurs de cardiomégalie (silhouette cardiaque arrondie, déplacement dorsal de la trachée ou des bronches souches, augmentation du contact entre le cœur et le sternum, …). Comme pour l'évaluation par les mesures, l'évaluation subjective est dépendante de l'expérience et de la qualité des clichés. Ces mesures peuvent aider au suivi des patients que ce soit dans la progression de la maladie ou dans la réponse au traitement.
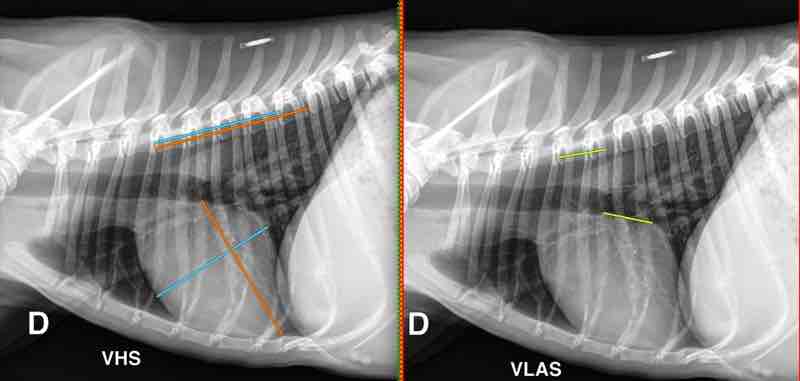
Photo 1
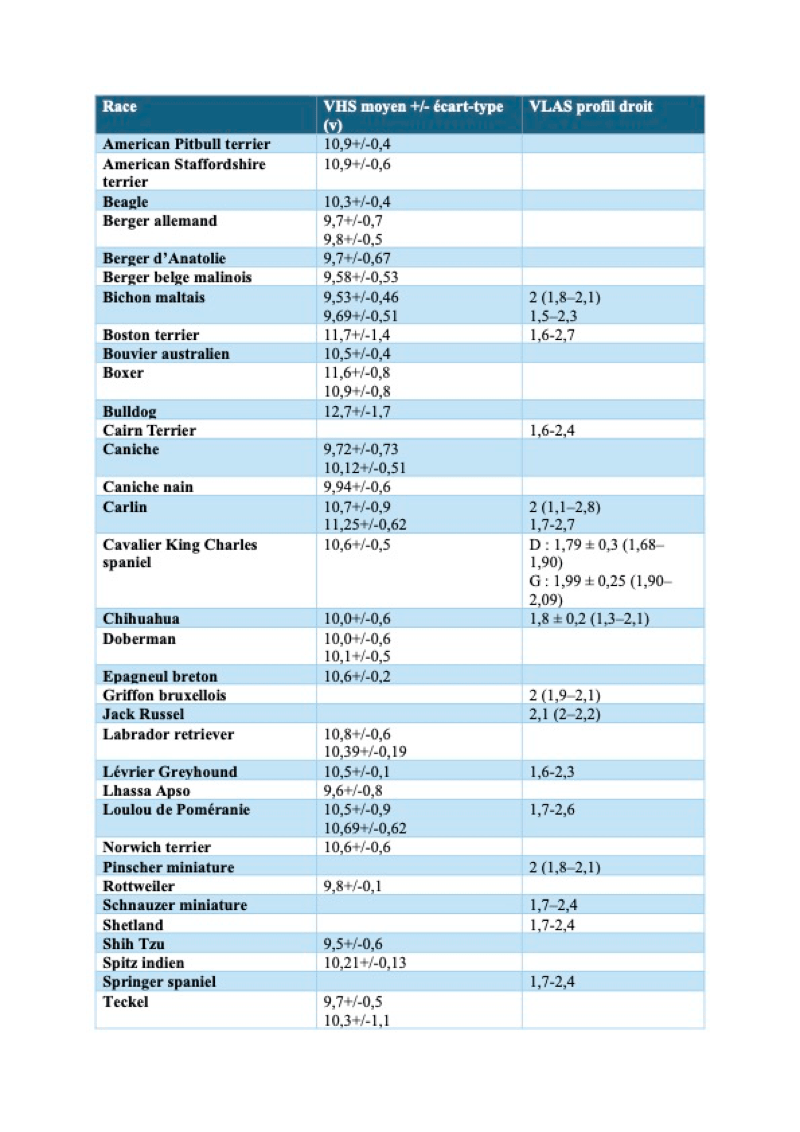
Tableau 1
Bibliographie
- Lucile MICHELLAND. Intérêt de l'examen radiographique en cardiologie chez le chien et le chat : étude bibliographique. Sciences du Vivant [q-bio]. Thèse d'exercice vétérinaire n° 20, 2024 p.207. ⟨dumas-04651871⟩
- BAISAN RA, Vulpe V. Vertebral Heart Score and Vertebral Left Atrial Size as Radiographic Measurements for Cardiac Size in Dogs-A Literature Review. Animals (Basel). 2025 Feb 26;15(5):683. doi: 10.3390/ani15050683. PMID: 40075966; PMCID: PMC11899317.
- KEENE BW, et coll. ACVIM consensus guidelines for the diagnosis and treatment of myxomatous mitral valve disease in dogs. J Vet Intern Med. 2019 May;33(3):1127-1140. doi: 10.1111/jvim.15488. Epub 2019 Apr 11. PMID: 30974015; PMCID: PMC6524084.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Mettre en évidence un signe du tiroir
Isturits, France
I. Introduction
Le grasset est une articulation complexe permettant l'articulation du fémur et du tibia. Les principales structures de contention de l'articulation du grasset sont les ligaments croisés crânial et caudal et les ligaments collatéraux, médial et latéral.
Dans le cadre d'une atteinte du ligament croisé crânial ou du ligament croisé caudal, une instabilité cranio-caudale apparait. Elle est présente dans le plan sagittal. On parle de signe du tiroir.
II. Anatomie des structures de contention principales du grasset
1. Les ligaments croisés
Le ligament croisé crânial s'attache proximalement sur la partie caudo-médiale du condyle fémoral latéral et sur la partie caudo-latérale de la fosse inter-condylienne du fémur. Il s'étend distalement dans une direction cranio-médiale pour s'attacher sur la partie crâniale de la zone inter-condylienne du tibia. Il peut être divisé en 2 parties : une bande caudo-latérale, de taille plus importante, tendue en extension et détendue en flexion et une bande cranio-médiale, de taille plus modeste, et tendue en flexion et en extension.
Le ligament croisé caudal, plus long et plus large que le ligament croisé crânial, s'attache proximalement sur la partie latérale du condyle fémoral médial et s'étend caudo-distalement jusqu'au bord médial de l'échancrure intercondylienne tibiale.
2. Les ligaments collatéraux
Le ligament collatéral latéral s'attache proximalement sur l'épicondyle latéral du fémur et distalement sur la tête de la fibula.
Le ligament collatéral médial s'attache proximalement sur l'épicondyle médial du fémur et distalement sur une aire longitudinale rectangulaire au niveau de la métaphyse tibiale. Ce ligament présente une attache au ménisque médial et à la capsule articulaire.
Une lésion d'un des quatre ligaments entraine une instabilité.
La fréquence de l'atteinte des divers ligaments est variable. Une étude rétrospective menée au sein de sa structure par le Dr CHANCRIN sur 1028 lésions ligamentaires du grasset révèle : 94,6 % de lésions du ligament croisé crânial, 0,4 % de lésions du ligament croisé caudal, 5 % d'entorses graves avec atteinte des ligaments collatéraux. L'atteinte la plus fréquente est celle du ligament croisé crânial qui engendre une instabilité cranio-caudale du grasset.
Une atteinte du ligament croisé crânial et du ligament croisé caudal entraine une instabilité cranio-caudale. On parle de signe du tiroir.
Mais attention, une atteinte du ligament collatéral médial est responsable d'une instabilité en valgus, modérée si l'atteinte est isolée. Dans ce cas, une instabilité marquée en rotation externe est présente et peut donner la fausse impression d'une instabilité cranio-caudale.
III. Signe du tiroir : manipulation clinique
L'examen clinique de l'animal est une étape primordiale.
Il débute avec l'animal debout. Le grasset affecté est palpé. Classiquement, dans le cas de rupture du ligament croisé crânial, une synovite est présente. Elle va être palpée de chaque côté du ligament tibio-rotulien. Dans les cas d'atteintes chroniques du ligament croisé crânial, une fibrose péri-articulaire est palpée sur la face médiale.
Le patient est ensuite placé en décubitus latéral. La manipulation de l'articulation est souvent douloureuse, notamment en extension. Une sédation voire une anesthésie générale peut être nécessaire afin de faciliter le diagnostic.
Dans les cas d'instabilité cranio-caudale, deux manœuvres sont décrites. Il s'agit du signe du tiroir, direct ou indirect.
1. Technique du signe du tiroir direct
Elle permet de mettre en évidence les ruptures des ligaments croisées craniaux et caudaux. Pour explorer un grasset gauche, l'animal est placé en décubitus latéral droit. Le manipulateur place sa main droite sur le fémur du patient avec le pouce sur le sésamoïde du muscle poplité et l'index sur la rotule et sa main gauche sur son tibia avec le pouce sur la tête de la fibula et l'index sur la tubérosité tibiale. En maintenant le fémur en position, la main gauche fait avancer et reculer le tibia perpendiculairement à son grand axe. S'il avance, une rupture du ligament croisé crânial est suspectée, s'il recule, une rupture du ligament croisé caudal est suspectée. Dans les cas de rupture du ligament croisé crânial, un arrêt peu franc de l'avancée du tibia est noté en fin de manipulation. Dans les cas de rupture du ligament croisé caudal, un arrêt net est noté alors que le ligament croisé crânial intact se tend.
Il est nécessaire de commencer la manipulation avec le grasset en position physiologique, neutre soit avec le pouce de chaque main globalement sur une même ligne. En effet, si la manipulation du grasset débute avec un tibia en position de tiroir antérieur, une rupture du ligament croisé caudal peut être suspectée à tort.
Tout mouvement chez un animal adulte est considéré comme anormal. Il existe un certain degré de laxité du ligament croisé crânial chez le jeune. En cas de doute, il convient de contrôler le grasset controlatéral. La différenciation physiologique / pathologique peut également être faite au cours de la manipulation. Chez le jeune sans atteinte, un arrêt franc du tiroir est noté après quelques millimètres.
Dans le cas de suspicion de rupture du ligament croisé crânial, il est primordial de manipuler le grasset en extension, position physiologique et flexion. En effet, dans les cas de rupture partielle du ligament croisé crânial, une atteinte de la bande cranio-médiale va être responsable d'une instabilité en flexion uniquement.
2. Technique du signe du tiroir indirect (ou signe de compression tibiale, signe d'Henderson)
Cette technique permet de mettre en évidence une rupture du ligament croisé crânial. Elle met en jeu les muscles gastrocnémiens et la corde du jarret. Dans le cas d'un grasset gauche, l'animal est placé en décubitus latéral droit. Le manipulateur place sa main droite sur les condyles fémoraux du patient avec l'index sur la tubérosité tibiale et le pouce derrière le sésamoïde du muscle gastrocnémien. Cette main permet de maintenir le grasset en position physiologique. La main gauche fléchit le jarret et met en tension le muscle gastrocnémien. Cela induit une force de compression dans l'axe du tibia s'exerçant au niveau du grasset. Quand le ligament croisé crânial est intact, il contre cette force de compression et rien ne se passe. S'il est rompu, cette force de compression est transformée au niveau du grasset en force de poussée crâniale résultant en un déplacement crânial de la tubérosité tibiale. Ce déplacement, même léger, est perçu par l'index de la main maintenant le fémur. Il est très important, comme au cours de la réalisation du signe du tiroir direct, de partir d'une position neutre du grasset afin de limiter les faux négatifs.
Dans le cadre de rupture du ligament croisé crânial, CARROBI et col. ont étudié la sensibilité de ces deux tests. Sur les patients vigiles, pour le test de tiroir direct, la sensibilité était de 60 % et elle était de 64 % pour le test de compression tibiale. Cette sensibilité augmentait sensiblement si les patients étaient anesthésiés, passant respectivement à 92 % et 88 %. La spécificité des deux tests était par contre excellente, allant de 82 à 100 %.
MIGHT et col. ont réalisé une étude in vitro afin de déterminer la sensibilité et la spécificité du test du tiroir direct seul ou en combinaison avec le test de compression tibiale dans le cadre de la rupture du ligament croisé crânial, du ligament croisé caudal ou des deux. Le test du tiroir direct s'est révélé avoir une sensibilité relativement faible afin d'identifier une rupture du ligament croisé crânial (69 %), du ligament croisé caudal (45 %), ou du pivot central (26 %) mais excellente afin d'identifier les grasset sains (97 %). Dans cette étude encore, la spécificité du test était bonne dans le cadre de la détection de la rupture du ligament croisé caudal (97 %) ou du pivot central (92 %) mais encore assez faible dans le cadre de la rupture du ligament croisé crânial (75 %). La combinaison des deux tests ne permettait pas d'augmenter la sensibilité ni la spécificité.
Ces deux études révèlent que, bien que la réalisation de ces manœuvres dans le cadre de l'exploration d'une instabilité cranio-caudale soit obligatoire, il faut connaître leurs limites.
IV. Signe du tiroir radiographique
Suite à l'examen clinique, un examen radiographique est réalisé. Il permet au moins de réaliser un bilan de l'atteinte arthrosique du grasset, au mieux de confirmer l'atteinte dans les cas compliqués. Il est primordial pour énoncer un pronostic au propriétaire. Afin de réaliser des radiographies en positions forcées, une sédation poussée voire une anesthésie générale du patient est souvent conseillée, ces manœuvres étant souvent douloureuses.
Dans les cas d'instabilité cranio-caudale, une radiographie réalisée de profil avec un grasset à 90° permet de mettre en évidence un tiroir radiographique. Si le fémur et le tibia sont à leur position d'origine, la tangente au bord postérieur des condyles passe à hauteur du bord postérieur du plateau tibial. Un déplacement trop restreint ne doit pas être pris en compte. Si cette tangente est déplacée caudalement et donc si le tibia est déplacé crânialement, un tiroir radiographique est présent. Il est primordial dans ce cas d'écarter une atteinte du ligament collatéral médial pouvant être responsable de ce type de lésion radiographique.
Dans le cadre de rupture du ligament croisé crânial, une manœuvre de compression tibiale permet de faire avancer le tibia sous le fémur. Des signes indirects sont également présents, notamment le déplacement caudal et distal du sésamoïde du muscle poplité associé à une synovite radiographique.
Dans le cadre d'une rupture du ligament croisé caudal, une manipulation directe du tibia caudalement en maintenant le fémur en position permet de faire reculer le plateau tibial sous les condyles fémoraux.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Mini prothèse de hanche chez le Maine Coon (7 cas)
Introduction
La prothèse totale de hanche (PTH) est un traitement régulièrement employé chez le chien de moyen et grand format souffrant d'atteintes douloureuses, irréversibles, développementales ou acquises de l'articulation coxo-fémorale. L'adaptation des ancillaires aux petits chiens et chats est encore récente. Le Maine Coon est une espèce présentant une forte prédisposition aux atteintes coxo-fémorales, en particulier la dysplasie et l'épiphysiolyse de la tête fémorale. Les options thérapeutiques les plus couramment employées se limitent le plus souvent au traitement conservateur ou la résection de la tête et du col fémoral. Les objectifs de notre étude sont : 1) de présenter une mini PTH non cimentée, 2) d'évaluer rétrospectivement les indications, résultats, suivis et complications rencontrés sur une cohorte de 7 PTH chez le Maine Coon.
Matériel et résultats
Les caractéristiques complètes des mini PTH employées dans cette étude sont disponibles sur le site www.kyon.ch. Les données cliniques recueillies sur les animaux inclus dans l'étude étaient : âge, sexe, poids, type d'atteinte coxo-fémorale, taille des implants employés, évaluation post-opératoire de la position des implants (angle d'antéversion du col fémoral, angle de rétroversion et angle d'ouverture latérale de la cupule), ajout d'implants en complément de la prothèse, complications per et post-opératoires, informations cliniques et radiographiques obtenues lors du suivi post-opératoire.
Sept PTH ont été réalisées sur 5 Maine Coon (2 chats avec interventions bilatérales étagées dans le temps). L'âge moyen au jour de l'intervention était de 31,1 mois, il n'y avait que des mâles, le poids moyen était de 8 kg. Les indications opératoires étaient une épiphysiolyse (5 cas dont 2 bilatérales), dysplasie (1 cas) et une fracture ancienne du col fémoral (1 cas). Dans tous les cas une tige de taille 5 a été posée. Une cupule acétabulaire 14 mm/8 mm a été placée dans 2 cas sur un même chat, et une cupule 14 mm/10 mm dans les autres cas. Un col fémoral medium (+0 mm) a été posé dans 6 cas et un col short (-2 mm) dans 1 cas. Dans 6 cas la tige fémorale a été verrouillée par 1 vis bicorticale et 3 vis monocorticales de 2 mm. Dans le 7è cas une fissure du fémur est apparue lors de l'alésage fémoral, il a alors été placé 2 vis bicorticales et 2 monocorticales et 5 cerclages prophylactiques ont été ajoutés sur le fémur. L'évaluation radiographique postopératoire a montré un angle d'antéversion du col fémoral moyen de 10,4°, celui de rétroversion de la cupule acétabulaire de 20,7° et l'angle d'ouverture latéral de 41,4°.
Deux complications sont intervenues en postopétaroire : une fracture du fémur non diagnostiquée par la propriétaire n'a été traitée que 18 jours après la date supposée de la fracture avec complication septique puis syndrome d'hyperextension du grasset après ostéosynthèse par plaque et cerclages. Le chat a finalement été amputé 7 mois après la pose de la prothèse. Un second chat a présenté une luxation craniodorsale de la prothèse 10 mois après implantation. Une réduction manuelle a été effectuée à 2 reprises espacées d'un mois. Une 3ème récidive a finalement conduit à une intervention chirurgicale de révision avec remplacement du col fémoral medium (+0 mm) par un col long (+2 mm). Le chat en question était le seul chat à avoir reçu des têtes fémorales de 8 mm. Le suivi moyen était de 25 mois post-opératoire. Les résultats cliniques et la satisfaction client étaient excellents dans 6 cas et catastrophique dans 1 cas.
Discussion
Le développement de la mini PTH est encore récent et les études portant uniquement sur le chat sont encore rares. La plus grande étude rétrospective multicentrique portant sur 10 ans ne comprend que 44 chats (9 Maine Coon) (RODINO et al. Vet Surg 2022 ; 51 : 763-771). Comme dans notre étude, l'épiphysiolyse apparait comme la première indication de PTH, les autres indications étaient les fractures, la dysplasie, des reprises de résection de têtes fémorales et 1 cas de luxation de la hanche. Tous les cas présentés dans cette étude ont été implantés avec une prothèse cimentée. Il n'y a à ce jour aucune étude rétrospective sur une mini PTH non cimentée chez le chat. Les complications décrites chez le chat sont : luxation, fracture fémorale, rupture d'implants.
Les luxations de prothèses interviennent généralement en post-opératoire immédiat (dans les 30 jours post-opératoires). La survenue d'une luxation 10 mois après implantation est un événement rare. Il n'a pas été possible de déterminer si elle était liée au matériel en place ou un événement traumatique sans relation avec la présence d'une PTH. Il a déjà été prouvé que le risque de luxation de prothèse était directement lié au diamètre de la tête fémorale. Le chat avait été le premier implanté dans notre étude, avec une cupule de 14 mm/8 mm. Par la suite, les chats ont reçu des têtes fémorales de 10 mm. Nous pouvons donc recommander de n'employer que des cupules de 14 mm/10 mm et pas de 14 mm/8 mm pour limiter le risque de luxation.
L'enchainement des complications consécutif à une ostéosynthèse tardive et complexe a finalement abouti à une amputation du chat s'étant fracturé le fémur en post-opératoire. Ce cas de figure extrême reste exceptionnel puisque les fractures fémorales rencontrées chez le chat sont en général de bon pronostic après ostéosynthèse.
Conclusion
Cette étude montre la faisabilité de PTH chez le Maine Coon en traitement des épiphysiolyses, dysplasies et fractures épiphysaires.
Bibliographie
- RODINO et al. Vet Surg 2022 ; 51 : 763-771.
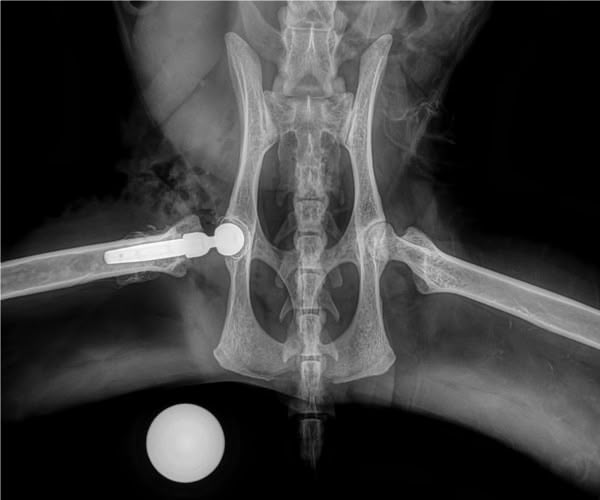
Figure 1
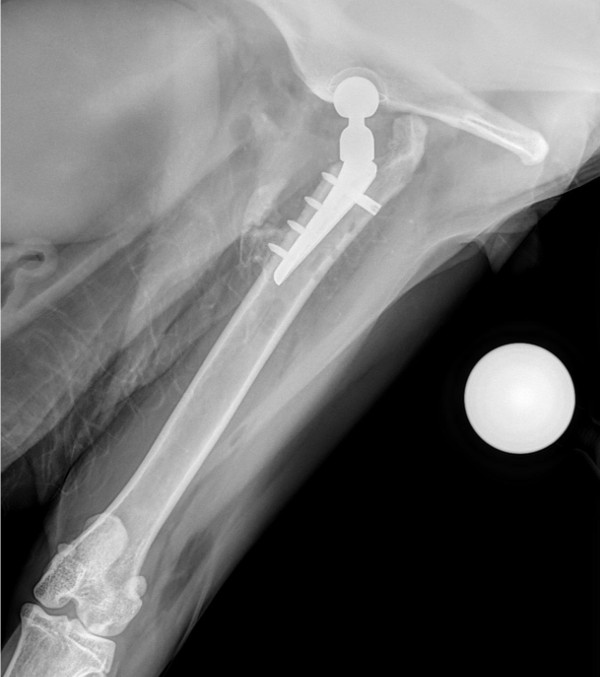
Figure 2
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Mise en place d'un drain péricardique
Nantes, France
Les épanchements péricardiques sont à l'origine d'une tamponnade cardiaque : ils compriment le cœur, ce qui gêne le retour veineux et conduit à une hypertension portale à l'origine d'une ascite. La gêne au remplissage entraîne une baisse du débit sanguin à l'origine d'une extrême faiblesse.
Le traitement d'urgence d'une tamponnade cardiaque consiste à ponctionner le sac péricardique pour en vider le contenu liquide qui comprime le cœur.
Les imageurs réalisent une ponction à l'aiguille sous guidage échographique. Cette technique ne permet pas de retirer tout le liquide car au fur et à mesure de la vidange, l'aiguille doit se rapprocher dangereusement du cœur. De plus, les manœuvres sont difficiles avec une aiguille eu égard à l'énorme quantité de liquide à retirer (souvent entre 500 ml et 1 litre) et elle nécessite un contrôle échographique permanent. Toutefois, même si le retrait du liquide n'est pas complet, les chiens sont toujours nettement améliorés.
Au service d'urgences d'ONIRIS, nous préférons réaliser un drainage péricardique : un drain est mis en place dans le sac péricardique jusqu'au retrait de tout le liquide d'épanchement. Certains d'entre nous le réalisent en aveugle, sans guidage échographique.
Une anesthésie générale est rarement nécessaire, elle n'est pas souhaitable si le chien est calme. Chez les chiens turbulents, une anesthésie légère est préférable pour éviter les syncopes et les fautes d'asepsie.
Le péricarde est facile à trouver car il est énorme et contre la paroi thoracique. Pour être certain de ponctionner vers le 4è – 6è espace intercostal, à la limite tiers inférieur - tiers supérieur, un repère est réalisé par une petite une incision cutanée au niveau du futur site de ponction avant la pose du champ. En effet, le choc précordial, souvent faible, ne pourra plus servir de repère une fois les champs en place.
Nous utilisons soit un cathéter sus-pubien (Uristil® ou Easycyst®) soit un cathéter jugulaire pour chevaux ; ils se présentent comme une grosse aiguille dans le chas de laquelle un tuyau souple perforé est glissé. Un Angiocath® conviendrait également. Il est également possible de poser un cathéter avec la technique Seldinger.
Le chien est placé en décubitus droit, un champ papier est collé sur le thorax gauche tondu et désinfecté.
L'intervention est entièrement stérile comme une intervention chirurgicale.
Pour faciliter le passage de l'aiguille, une incision cutanée de 2 mm est réalisée au niveau du repère, vers le 4è espace intercostal, à la jonction tiers inférieur-tiers moyen. L'aiguille ponctionne les muscles intercostaux puis le péricarde d'un petit coup sec. Elle ne risque par d'atteindre le cœur qui est souvent très loin. Du sang monte dans l'aiguille et dans le guide quand le péricarde est ponctionné. En effet, le liquide est presque toujours du sang en nature, il ne coagule pas. Très rarement, il peut s'agir d'un transsudat modifié ou de pus.
L'aiguille qui a servi à la ponction du péricarde n'est pas introduite davantage pour ne pas léser le cœur avec sa pointe ; elle est retirée, seul le guide reste en place.
Le sang s'écoule du guide qui entourait l'aiguille ; le pouce l'obstrue pour éviter la vidange du sac péricardique avant l'introduction du cathéter.
Le cathéter souple est glissé dans le guide aussi loin que possible.
Le guide est retiré ; la sonde est en place dans le péricarde.
Le kit Uristil® est commercialisé avec une connectique prolongée d'un robinet à 3 voies.
Le liquide péricardique est aspiré à l'aide d'une grosse seringue (50 ml).
La quantité de sang retirée est comprise entre 500 ml et 1 litre !
Vu le calibre du cathéter et le volume à retirer, cette vidange est longue : 15 minutes environ. Le recours à un cathéter souple qui ne risque pas de ponctionner le cœur permet le retrait de la totalité du liquide d'épanchement. Il se peut que l'aspiration ne fournisse plus de liquide, c'est souvent parce que l'extrémité du cathéter est plaquée contre le cœur ou le péricarde ; il suffit de retirer un peu le cathéter.
Autrefois, nous laissions le cathéter en place pour pratiquer d'autres vidanges les jours suivants, mais nous avons observé que c'était inutile car l'épanchement ne se reforme pas immédiatement.
Si le liquide coagule, c'est que le cœur a été ponctionné... (ça n'arrive jamais fort heureusement).
L'analyse du liquide d'épanchement permet parfois l'identification de cellules cancéreuses.
L'épanchement abdominal n'a pas besoin d'être retiré : il disparaîtra seul en quelques jours.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Mise en place d'un drain thoracique
Montpellier, France
I. Introduction
La pose de drains thoraciques est une procédure essentielle dans la gestion de nombreuses affections pleurales chez les carnivores domestiques. Elle permet le drainage d'air, de liquide ou de sang dans le thorax, et facilite ainsi la restauration d'une respiration efficace.
Les indications d'un drain thoracique comprennent les pneumothorax récurrents nécessitant une thoracocentèse répétée, les pneumothorax sous tension, les pyothorax, les épanchements pleuraux à formation rapide et la prise en charge postopératoire des patients ayant subi une thoracotomie. Un pneumothorax sous tension peut provoquer un arrêt respiratoire fatal en quelques secondes à minutes. En cas de pneumothorax sous tension, une thoracocentèse et la mise en place d'un drain thoracique doivent être réalisées immédiatement. Les autres indications de mise en place d'un drain thoracique permettent généralement une approche moins urgente.
La mise en place d'un drain thoracique permet soit une évacuation intermittente fréquente de la cavité pleurale, soit une évacuation continue du thorax si elle est reliée à une aspiration continue. Comme pour la thoracocentèse, une contre-indication majeure à la mise en place d'un drain thoracique est une coagulopathie sévère, qui doit être corrigée avant la mise en place d'un drain, si possible.
II. Indications de la pose de drains thoraciques
1. Épanchements pleuraux
- Hydrothorax : insuffisance cardiaque congestive, hypoprotéinémie.
- Pyothorax : infection bactérienne de la cavité pleurale.
- Hémothorax : trauma, coagulopathie, néoplasie.
- Chylothorax : idiopathique, traumatique ou secondaire à des tumeurs.
- Épanchement pleural néoplasique : carcinomatose pleurale, mésothéliome.
2. Pneumothorax
- Traumatique : contusions thoraciques, fractures de côtes perforantes.
- Spontané : rupture de bulles pulmonaires.
- Iatrogène : suite à une ponction ou intervention thoracique.
III. Types de drains thoraciques
1. Drains rigides (type Trocart) (Figure 1)
En polyvinyle rigide, souvent munis d'un mandrin (trocart). Bonne tenue mécanique, mais plus traumatiques. Indiqués en urgence (ex : hémothorax/pneumothorax traumatique). Nécessite une intubation lorsqu'il y a dissection jusqu'à l'espace pleural pour insérer le drain.

Figure 1
2. Drains souples (technique de Seldinger) (Figure 2)
Moins douloureux, plus confortables pour le patient. Fixation souvent plus délicate.
La taille du tube doit être adaptée à la taille du patient et à la présence éventuelle d'air ou de liquide. Des tubes plus petits peuvent être utilisés pour l'aspiration d'air. Si du liquide doit être aspiré par le drain thoracique, des tubes plus grands sont utilisés. Si le liquide est épais ou focal, des trous de drainage supplémentaires peuvent être pratiqués dans le tube avant la mise en place à l'aide d'une lame de scalpel, en veillant à ce que la taille des trous soit inférieure à 50% du diamètre du tube. Si les fenestrations représentent plus de 50% du diamètre ou sont trop rapprochées, il existe un risque de rupture de la partie distale de la sonde, nécessitant une ablation chirurgicale.
La technique Seldinger ne nécessite pas obligatoirement d'intubation. Cependant, si le patient est fortement dyspnéique et empire même avec la sédation, tout doit être prêt pour intuber le moment venu.
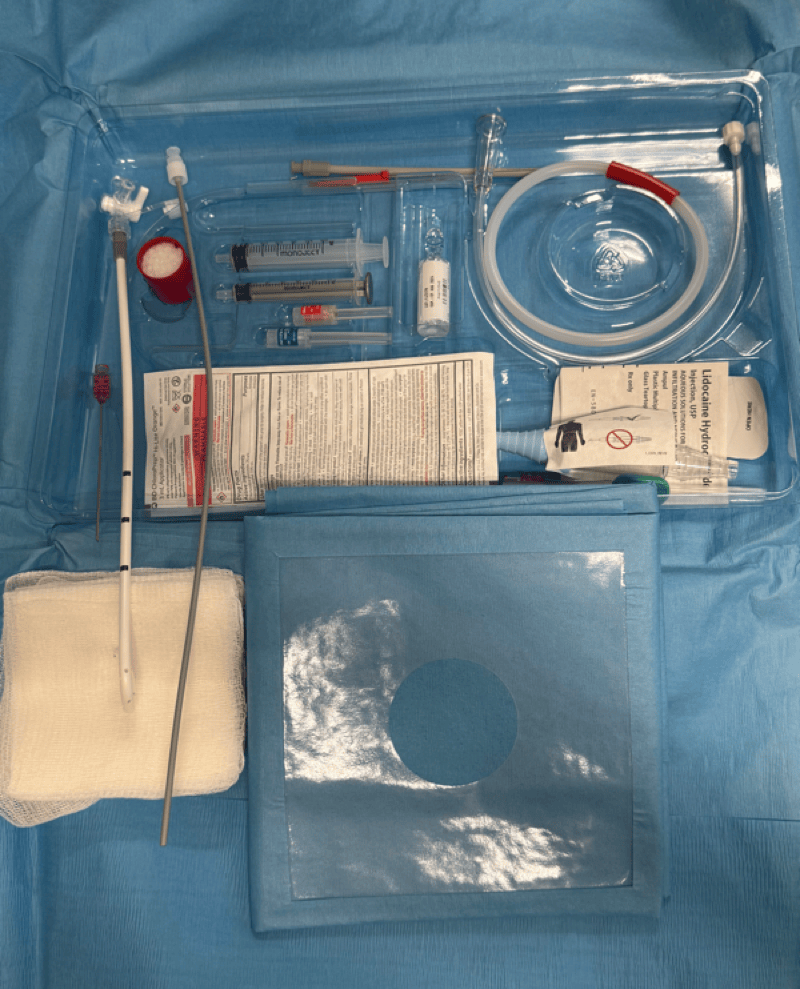
Figure 2
IV. Étapes de pose d'un drain thoracique
- Préparation du patient : tonte large, sédation ou anesthésie générale, installation en décubitus latéral.
- Localisation du site d'insertion : 7e ou 8e espace intercostal et dorsal ou milieu de thorax pour le site d'insertion selon la nature de l'épanchement.
- Incision cutanée et création d'un tunnel sous-cutané : tunnelage pour limiter les fuites (2 techniques : tirage de la peau en crânial ou tunnel avec le trocard lui-même).
- Introduction du drain : avec ou sans trocart.
- Fixation du drain : suture en bourse.
- Vérification de la perméabilité : radiographie post-pose.
V. Entretien d'un drain thoracique
La gestion d'une sonde de thoracostomie nécessite une surveillance 24 h/24 en raison du risque de détachement de la sonde, susceptible de provoquer un pneumothorax ouvert mortel. Le drain doit être fermé par un robinet à trois voies muni de bouchons d'injection. Ce robinet doit être en position FERMÉE lorsqu'il n'est pas utilisé. Idéalement, le drain thoracique lui-même doit être clampé en cas de détachement du robinet à trois voies du drain thoracique. Le drain thoracique doit également être vérifié quotidiennement pour détecter tout signe de migration.
Une technique aseptique stricte doit toujours être appliquée lors de la manipulation du drain thoracique et de l'évaluation du site d'insertion. L'utilisation prophylactique d'antibiotiques n'est pas recommandée. Le site d'insertion du drain doit être examiné au moins une fois par jour pour détecter tout signe d'inflammation ou d'infection, notamment rougeur, douleur, chaleur, gonflement, emphysème sous-cutané et/ou écoulement purulent. Le drain thoracique peut être fixé au patient de différentes manières (technique du jersey préférée par l'auteur). De plus, une collerette peut être nécessaire pour empêcher le patient de retirer le drain thoracique. L'espace pleural peut être évacué par :
- Aspiration continue
- Évacuation manuelle intermittente.
1. Aspiration manuelle
En général, si l'aspiration continue n'est pas utilisée, le drain doit être évacué manuellement toutes les 4 à 6 heures. À chaque aspiration, l'espace pleural est vidé. La cavité pleurale doit être évacuée jusqu'à l'obtention d'une pression négative, sauf chez les patients présentant un œdème pulmonaire de réexpansion. Ce problème survient le plus souvent chez les patients ayant présenté une atteinte prolongée de la cavité pleurale, comme une hernie diaphragmatique chronique postopératoire. Dans ce cas, la cavité pleurale ne doit pas être évacuée complètement initialement, afin de permettre aux poumons de se regonfler progressivement et de réduire le risque d'œdème pulmonaire.
Lors de l'évacuation du drain thoracique, la tubulure doit être évaluée afin de s'assurer de l'absence de fuites, de pliures ou d'accumulation de fibrine ou d'autres substances protéiques. Une pliure ou une accumulation non détectée dans le drain thoracique entraîne une pression négative lors de l'aspiration. Cette « fausse » pression négative est trompeuse et laisse supposer à tort que la cavité pleurale a été évacuée. Si la tubulure est obstruée, elle peut être rincée, en respectant scrupuleusement les règles d'asepsie, avec une petite quantité de sérum physiologique stérile à 0,9% pour tenter de déloger l'obstruction.
La quantité d'air et/ou de liquide prélevée par le drain thoracique doit être surveillée quotidiennement.
2. Aspiration continue
Les systèmes de drainage thoracique continu sont indiqués lorsque de grandes quantités d'air ou de liquide s'accumulent rapidement dans la cavité pleurale. Cela évite au patient de développer une détresse respiratoire entre les aspirations de la sonde et peut également favoriser la cicatrisation pulmonaire en cas de pneumothorax. Chez les patients atteints de pyothorax produisant un épanchement important, un drainage continu de la cavité pleurale est indiqué pour réduire la quantité de matériel purulent dans la cavité thoracique.
3. Systèmes de drainage par aspiration continue
Le drainage actif de la cavité pleurale peut être réalisé en connectant le patient à une source d'aspiration continue et à un système de drainage. Les différents systèmes de drainage reposent sur le système à trois bouteilles.
VI. Avantages et inconvénients
1. Avantages
- Évacuation rapide des épanchements ou de l'air
- Amélioration rapide de la fonction respiratoire
- Suivi dynamique de la production de liquide
- Possibilité de rinçage (dans le cas du pyothorax)
2. Inconvénients
- Douleur post-opératoire
- Risque de fuite d'air ou de liquide
- Surveillance intensive nécessaire
- Coût accru en cas de séjour prolongé
VII. Complications possibles
- Pneumothorax iatrogène
- Lésions pulmonaires ou vasculaires
- Infection du site de sortie
- Obstruction du drain
- Fuites d'air persistantes
VIII. Gestion de la douleur
Les drains thoraciques à demeure peuvent être très douloureux ; il est donc important d'administrer une analgésie à ces patients. La bupivacaïne 0,5% peut procurer une analgésie locale lorsqu'elle est administrée par le drain à une dose totale de 1,5 mg/kg toutes les 6 à 8 heures chez les chiens. Une dose plus faible de 1 mg/kg toutes les 6 à 8 heures est recommandée chez les chats. Les chats sont plus sensibles aux anesthésiques locaux que les chiens et doivent être surveillés attentivement s'ils sont utilisés. Après l'injection dans les drains thoraciques, 2 à 3 ml de NaCl stérile à 0,9% doivent être utilisés pour évacuer la bupivacaïne de la sonde et la faire pénétrer dans la plèvre du patient.
Le drain thoracique ne doit pas être aspiré immédiatement après l'administration d'un anesthésique local. La bupivacaïne peut provoquer une sensation de brûlure lors de la première injection en raison de l'acidité de la solution. Les opioïdes injectables offrent une excellente analgésie, mais peuvent être associés à une diminution de la fonction respiratoire à des doses plus élevées. L'association d'opioïdes (méthadone, morphine) et de bupivacaïne intrapleurale peut apporter un excellent soulagement de la douleur chez la plupart des patients. Un tranquillisant tel que l'acépromazine (0,01 mg/kg) +/- médétomidine à faible dose (1 à 2 µg/kg) +/- paracétamol peuvent compléter l'analgésie et le maintien au calme du patient.
Retrait du drain : le drain doit être retiré dès qu'une pression négative apparaît dans le thorax après plusieurs aspirations consécutives ou que le liquide prélevé lors de l'aspiration diminue significativement. Normalement, de faibles volumes de liquide (jusqu'à 1 à 2 ml/kg/jour) sont générés suite à la réponse inflammatoire naturelle de l'organisme à la présence d'un corps étranger (canule de thoracostomie) dans la cavité pleurale. En général, si l'aspiration du drain produit peu ou pas d'air et ne dépasse pas 2 à 4 ml/kg de liquide pleural sur une période de 24 heures, le drain peut être retiré. Le site d'insertion de la canule de thoracostomie doit être laissé à cicatriser en seconde intention ; aucune suture n'est généralement nécessaire.
IX. Conclusion
La pose de drains thoraciques est une procédure souvent salvatrice chez le chien et le chat, à condition d'être bien indiquée et maîtrisée techniquement. Le choix du type de drain et de la technique dépend de la nature de l'épanchement, de la durée prévue du drainage et de l'état du patient. Une surveillance attentive et une gestion rigoureuse des complications permettent d'optimiser les résultats cliniques.
Bibliographie
- KING LG, BOAG A. Pleural space disease in dogs and cats. Vet Clin North Am Small Anim Pract. 2007.
- TOBIAS KM, JOHNSTON SA. Veterinary Surgery: Small Animal. Elsevier, 2017.
- MCANULTY JF. Thoracic drainage techniques. Clin Tech Small Anim Pract. 2001.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Mise en place d'une sonde d'alimentation
Guyancourt, France
I. Introduction
La nutrition entérale fait partie intégrante de la prise en charge des animaux hospitalisés. Chez le chien et le chat, l'anorexie ou l'incapacité à maintenir une prise alimentaire spontanée est fréquente dans de nombreuses affections médicales ou chirurgicales. L'apport nutritionnel est un élément pronostique majeur car il conditionne la cicatrisation, la réponse immunitaire, le maintien de la masse musculaire et la tolérance aux thérapeutiques lourdes. Dès qu'un animal est incapable de couvrir ses besoins énergétiques par voie orale pendant plus de quelques jours, la mise en place d'une sonde d'alimentation doit être envisagée. Parmi les différentes options disponibles, deux techniques sont particulièrement utilisées en pratique quotidienne : la sonde nasogastrique et la sonde d'œsophagostomie.
II. Indications générales de la nutrition entérale
La nutrition par sonde est indiquée dès qu'une anorexie de plus de trois jours est anticipée ou constatée. Elle est également indispensable en cas de perte de poids rapide, de catabolisme marqué ou de situations où la voie orale est compromise par douleur, dysphagie, troubles nerveux ou chirurgie orale. La nutrition entérale est préférable à la nutrition parentérale car elle respecte la physiologie digestive, entretient la trophicité de la muqueuse intestinale et diminue le risque de translocation bactérienne.
III. La sonde nasogastrique
1. Mise en place
La sonde nasogastrique est introduite par une narine, chemine dans le nasopharynx puis l'œsophage pour aboutir dans l'estomac.
Elle présente l'avantage d'être mise en place rapidement et sans anesthésie générale, ce qui la rend adaptée aux animaux instables ou hospitalisés en urgence. Une tranquillisation légère et l'instillation de collyre anesthésiant dans la narine peuvent améliorer la tolérance à la pose.
Le calibre choisi varie de 3,5 à 10 French selon la taille de l'animal et la longueur est mesurée, avant l'introduction, depuis la narine jusqu'à la dernière côte. La progression est facilitée par la lubrification et par un maintien de la tête en position neutre ou légèrement fléchie, afin de limiter le risque d'introduction trachéale.
La vérification de la position est indispensable, idéalement par radiographie de contrôle, en vérifiant bien qu'il y ait une double superposition entre la paroi trachéale et la sonde.
La fixation est réalisée par une suture cutanée au niveau de la narine (laçage chinois).
2. Utilisation, limites et complications
Cette sonde permet l'administration de régimes liquides ou semi-liquides à faible viscosité, administrés en bolus fractionnés ou en perfusion entérale continue. Elle est particulièrement adaptée aux besoins de courte durée, généralement inférieure à dix jours.
Ses limites résident dans le calibre réduit qui empêche l'utilisation de régimes trop concentrés, le risque d'obstruction, l'inconfort nasal ou encore les contre-indications en cas de coagulopathie ou d'atteinte nasale ou œsophagienne.
Des complications comme la rhinite, la sinusite ou le reflux sont possibles, mais rares si les manipulations sont correctes. Un rinçage régulier avec de l'eau tiède après chaque repas est essentiel pour prévenir l'obstruction. La plupart des animaux tolèrent bien la sonde après une période initiale d'adaptation.
IV. Sonde d'œsophagostomie
1. Mise en place
Sa mise en place nécessite une anesthésie générale courte et une asepsie stricte du site chirurgical. L'animal est positionné en décubitus latéral, le cou est tondu et préparé, puis une incision cutanée est réalisée au tiers moyen du cou. Une pince introduite par la cavité orale est extériorisée par cette incision, saisit l'extrémité de la sonde puis la fait sortir par la bouche, la boucle et la réintroduit dans l'œsophage en éliminant petit à petit la bouclée créée. La sonde est ainsi redirigée vers l'estomac.
Elle est ensuite fixée par un laçage chinois. Le pansement protecteur est indispensable pour limiter les risques d'arrachement.
2. Utilisation et complications
La sonde d'œsophagostomie constitue une solution durable, adaptée aux situations où la nutrition artificielle doit se prolonger sur plusieurs semaines. Elle permet l'administration de volumes plus importants et de régimes plus concentrés grâce à un calibre plus large, généralement compris entre 12 et 20 French.
Ce type de sonde est bien toléré sur le long terme car il ne gêne ni l'olfaction ni la respiration. Il peut être maintenu plusieurs semaines à plusieurs mois, ce qui permet de nourrir efficacement les animaux atteints d'affections chroniques ou convalescents après une chirurgie majeure.
Les complications sont rares et comprennent surtout des infections locales, des obstructions par aliments insuffisamment dilués ou un déplacement accidentel. Le suivi implique une inspection et un nettoyage quotidien du site d'insertion, ainsi qu'un rinçage systématique après chaque repas. Les repas sont administrés en plusieurs fractions, quatre à six par jour, permettant une bonne couverture calorique et protéique. Les propriétaires peuvent être formés à l'utilisation et à l'entretien de la sonde, ce qui permet un retour à domicile avec une autonomie partielle.
3. Comparaison des deux techniques
La sonde nasogastrique est simple, rapide et particulièrement adaptée aux contextes aigus où l'on recherche une solution transitoire sans anesthésie. Elle est indiquée pour les anorexies brèves et pour les animaux hospitalisés instables. La sonde d'œsophagostomie, en revanche, est plus adaptée aux besoins prolongés, grâce à son confort, à son calibre plus large et à la possibilité d'administrer des régimes plus concentrés. Elle suppose cependant une anesthésie générale et un minimum de matériel chirurgical, ce qui en limite l'utilisation chez les patients très instables. Le choix doit être raisonné en fonction de la durée anticipée de la nutrition, de l'état clinique, de la densité calorique requise et des contraintes pratiques.
4. Calcul du volume des repas
Une alimentation liquide doit être utilisée. Les besoins énergétiques (BE) sont calculés selon la formule : BE = 70 x (poids0,75), le poids étant exprimé en kg. Par exemple, si on applique cette formule à un chat de 4 kg, le BE est égal à 198 Kcal soit environ 200. On va ensuite diviser ce BE en fonction du nombre de repas par jour. Si on choisit 4 repas par jour, ceci va faire 50 Kcal par repas. En fonction de la concentration des aliments liquides (la plupart sont à 1 Kcal/ml), le volume du repas va être ainsi calculé.
En fonction de la durée d'anorexie, il est conseillé, notamment chez le chat, d'initier l'alimentation entérale progressivement pour éviter un syndrome de renutrition. Par exemple, lors d'anorexie de 3 jours, on va renourrir à J1 à 33% des BE, à J2 à 66% des BE, à J3 à 100% des BE.
5. Déroulement d'un repas
a) Matériel à prévoir :
- Une seringue de 5 ml propre et vide
- Une seringue de 5 ml d'eau
- Les seringues de gavage de 20 ml ou 50 ml
- La bouteille de repas liquide
b) Procédure :
- Étape 1 : test à l'air : avec la seringue vide de 5 ml, procéder au test dit du vide pour s'assurer du bon positionnement de la sonde. Lorsque l'on tire sur le piston, il doit se remettre automatiquement à sa place. Si du liquide est présent lors de ce test, retirer tout le liquide et effectuer ensuite le test à l'air.
- Étape 2 : test à l'eau : avec la seringue de 5 ml d'eau, injecter dans la sonde l'eau doucement (environ 2 ml) pour vérifier la bonne intégrité de la sonde et qu'elle ne soit pas bouchée. L'animal ne doit pas avoir de réaction à l'injection de l'eau (pas d'éternuement, pas de signes de nausées).
- Étape 3 : gavage : avec la seringue de gavage pleine, procéder au repas, en lui injectant le volume complet dans la sonde sur une durée de 10 minutes. Surveillez durant le gavage que l'animal ne présente aucun signe de gêne.
- Étape 4 : médicaments : administrer, si nécessaire, les médicaments liquides uniquement.
- Étape 5 : nettoyage de la sonde : reprendre la seringue d'eau. Injecter doucement les 3 ml restant dans la sonde pour la rincer et s'assurer qu'elle ne se bouche pas.
V. Conclusion
La sonde nasogastrique et la sonde d'œsophagostomie représentent deux outils indispensables pour la nutrition entérale chez le chien et le chat. La première est adaptée aux situations aiguës et de courte durée, la seconde offre une solution confortable et efficace pour les affections chroniques ou les convalescences prolongées. Leur utilisation raisonnée améliore significativement le pronostic et la qualité de vie des patients hospitalisés ou suivis à domicile.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Mise en place d'une sonde rectale
Montpellier, France
I. Introduction
La sonde rectale est un outil simple, peu invasif et polyvalent en médecine vétérinaire canine. Ses applications cliniques sont diverses. Une mise en place rigoureuse et adaptée aux indications est essentielle pour garantir la sécurité du patient et la fiabilité des résultats.
II. Applications cliniques de la sonde rectale chez le chien
1. Évaluation des pertes digestives et adaptation de la fluidothérapie
Chez le chien hospitalisé, notamment en soins intensifs, les pertes digestives représentent un facteur critique dans l'évaluation du bilan hydrique global. La mise en place d'une sonde rectale permet une surveillance objective et continue des pertes liquidiennes par voie fécale, ce qui est particulièrement utile en cas de diarrhée aiguë sévère, de colite hémorragique, ou lors de maladies gastro-intestinales entraînant une perte importante de fluides et d'électrolytes.
- Parvovirose
- Syndrome diarrhée hémorragique aiguë
a) Mesure quantitative des pertes digestives
- La sonde rectale permet de collecter directement les selles liquides dans une poche de recueil étanche.
- Cette méthode évite la contamination de la cage, assurant une mesure plus fiable du volume des pertes.
- Les volumes peuvent être mesurés à intervalles réguliers (par exemple toutes les 4 à 6 heures), et intégrés au bilan hydrique journalier.
b) Surveillance de la qualité des effluents digestifs
- L'aspect, la couleur et la consistance des selles peuvent être observés plus facilement à travers le dispositif.
- La présence de sang, de mucus ou de résidus non digérés peut orienter le diagnostic ou indiquer une aggravation.
c) Adaptation du plan de fluidothérapie
En cas de diarrhée profuse, les pertes en eau, sodium, potassium et bicarbonates peuvent être significatives.
Grâce à la quantification permise par la sonde, les volumes de perfusion peuvent être ajustés en temps réel, en tenant compte :
- des pertes insensibles,
- des pertes urinaires,
- des pertes digestives recueillies.
Cela permet un ajustement précis des apports hydriques et électrolytiques, limitant les risques de déshydratation, d'hypovolémie ou de déséquilibres ioniques.
De plus, la sonde rectale connectée à une poche permet un confort du personnel et de l'animal au niveau de l'hygiène. Cela évite également une irritation anale et cutanée douloureuse qui peut être présente lorsque les selles sont en contact longtemps avec la peau.
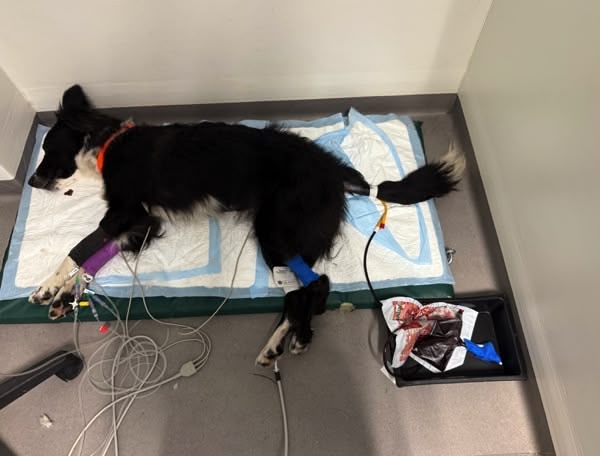
Figure 1
2. Utilisations moins fréquentes
a) Transplantation fécale
Très utile pour réaliser cette procédure. Il faut enfoncer la sonde le plus loin possible et instaurer l'échantillon de selles à transplanter (pas de consensus mais souvent 10 g d'aliquot à laisser en place avec la sonde pendant 15-20 min avant de la retirer).
Utilisée en médecine humaine et vétérinaire (parvovirose, SDAH).
b) Administration de médicaments ou de fluides
Voie rectale utilisée pour des antiépileptiques (diazépam) ou certains lavements thérapeutiques.
c) Décompression du côlon ou lavements évacuateurs
En cas de mégacôlon, constipation sévère ou intoxication digestive.
III. Mise en place d'une sonde rectale : protocole pas à pas

Figure 2
1. Matériel nécessaire
- Sonde rectale souple (PVC, silicone ou thermosensible) adaptée à la taille du chien.
- Lubrifiant hydrosoluble.
- Gants à usage unique.
- Fixation (sparadrap ou rien)
- Poche de récolte lors d'utilisation pour les diarrhées liquidiennes profuses
2. Préparation de l'animal
- Position recommandée : décubitus latéral ou sternal.
- Éviter l'agitation et l'anxiété, contenir l'animal doucement mais fermement.
- Port de gants pour garantir une hygiène rigoureuse.
3. Lubrification et inspection
- Appliquer généreusement le lubrifiant sur la sonde.
- Inspecter visuellement la région anale pour détecter toute lésion ou anomalie, ne pas hésiter à tondre la zone si nécessaire.
4. Introduction de la sonde
- Introduire délicatement la sonde dans le rectum, sur une profondeur de 5 à 10 cm selon la taille du chien, ne pas hésiter à prendre le diamètre le plus important proportionnellement au chien.
- Ne jamais forcer : arrêter immédiatement si une résistance anormale est ressentie.
- Vérifier la bonne progression de la sonde en observant une absence de gêne ou de contraction excessive.
- Instiller la quantité d'eau pour le gonflement du ballonnet comme indiqué sur la sonde elle-même.
5. Fixation
- Fixer la sonde à la base de la queue ou au pelage voisin avec un sparadrap, en évitant toute traction excessive.
6. Surveillance
- Contrôler régulièrement la tolérance de l'animal, l'absence d'irritation ou de saignement.
- Dégonfler le ballonnet et faites glisser la sonde en avant ou en arrière de quelques cm puis regonfler le ballonnet une fois par jour
- Nettoyer et désinfecter la sonde après usage si réutilisable.
IV. Précautions et contre-indications
- Contre-indiquée en cas de proctite, tumeurs anales, prolapsus rectal ou suspicion de perforation.
- Ne pas utiliser de sonde rigide ou mal lubrifiée.
- Surveiller tout signe d'inconfort ou d'hémorragie après la pose.
- Si l'animal expulse la sonde, ne pas hésiter à gonfler le ballonnet avec plus d'eau.
V. Avantages pratiques en milieu hospitalier
- Limite les risques d'escarres ou d'irritation périanale chez les animaux alités.
- Facilite l'hygiène et réduit la contamination environnementale.
- Améliore le confort de l'animal et du personnel soignant.
VI. Conclusion
La sonde rectale est un outil sous-estimé mais extrêmement utile dans la pratique quotidienne. Une bonne connaissance de ses indications et une pose méthodique permettent d'en tirer pleinement parti, tout en assurant le confort et la sécurité de l'animal.
L'utilisation d'une sonde rectale constitue également un outil précieux pour le suivi des pertes digestives. Elle permet une fluidothérapie personnalisée, adaptée à l'état clinique de l'animal, ce qui améliore significativement la prise en charge des patients critiques souffrant de troubles gastro-intestinaux.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Mise en place d'une sonde urinaire
Annecy, France
I. Indications
La mise en place d'une sonde urinaire peut être indiquée dans plusieurs situations cliniques, parmi lesquelles :
- Obstruction urétrale
- Brèche urétrale
- Rétention urinaire
- Suivi de la diurèse lors d'insuffisance rénale
- Prélèvements d'échantillons urinaires à visée diagnostique
- Facilitation de procédures diagnostiques ou chirurgicales
II. Choix de la sonde
La sonde idéale doit répondre à plusieurs critères :
- être atraumatique
- limiter l'inflammation locale
- ne pas se couder facilement
- réduire la formation de biofilms bactériens
Les sondes disponibles varient selon leur matériau (silicone, latex, ou latex recouvert de différents revêtements), chacun présentant avantages et inconvénients.
Certaines sondes sont équipées d'un ballonnet gonflable (type Foley) permettant une fixation interne, tandis que d'autres nécessitent une suture externe. Des modèles rigides avec guide d'insertion existent également, facilitant leur mise en place.
Le diamètre choisi doit être le plus petit possible, permettant néanmoins un bon débit urinaire, afin de limiter les traumatismes urétraux et vésicaux. La longueur est pré-mesurée, de l'orifice urétral jusqu'à la partie crâniale de l'aile iliaque, pour assurer un positionnement correct de l'extrémité à l'entrée de la vessie.
Une sonde urinaire placée à demeure doit être reliée à un système clos et aseptique de collecte des urines. L'idéal est d'utiliser une poche spécifique, mais une poche de perfusion vidée et connectée via une tubulure peut être employée à défaut, bien qu'elle ne constitue pas un véritable système clos. Cette solution reste toutefois préférable à l'absence de dispositif de collecte.
III. Matériel nécessaire
- Sonde urinaire stérile
- Gants stériles et gants d'examen
- Savon et solution antiseptique pour préparation de la zone
- Lubrifiant stérile
- Gel de lidocaïne 2% stérile et seringue de 1–3 ml pour administration dans le vestibule chez la femelle
- Seringue stérile pour rinçage du fourreau ou du vestibule avec chlorhexidine 0,5%
- Tondeuse
- Matériel de fixation : suture ou seringue pré-remplie d'eau stérile pour ballonnet de Foley
- Système de collecte urinaire clos.
IV. Procédure de mise en place
1. Analgésie/sédation
Envisager une sédation ou une anesthésie générale si besoin.
2. Positionnement
- Décubitus latéral : mâle et femelle
- Décubitus ventral : femelle et chat mâle
- Décubitus dorsal : souvent préféré pour le chat mâle
3. Préparation
- Déterminer la longueur de sonde à introduire
- Réaliser une tonte et un nettoyage antiseptique de la zone
- Rincer vestibule ou fourreau à la chlorhexidine 0,5%
- Instiller de la lidocaïne 2% stérile dans le vestibule
4. Mise en place aseptique
- Lavage des mains et gants stériles
- Lubrifier la sonde, vérifier le ballonnet si présent
- Chez la femelle : insertion guidée manuellement ou à l'aide d'un spéculum
- Chez le mâle : extérioriser le pénis, insérer délicatement la sonde sans instrument de préhension
5. Vérification et finalisation
- Vérification : aspiration d'urine ou contrôle échographique de la position
- Fixation : gonflage du ballonnet de Foley ou laçage chinois si absence de ballonnet
- Connexion aseptique : relier la sonde au système de collecte
- Prélèvement : un échantillon urinaire peut être recueilli si nécessaire
V. Soins d'entretien d'une sonde urinaire à demeure
À réaliser toutes les 8 heures ou dès que la sonde/le système sont souillés.
1. Matériel
- Savon chirurgical et solution de rinçage
- Gants d'examen
- Solution de chlorhexidine 0,05%
- Poche de recueil stérile (en cas de changement)
2. Procédure
- Hygiène des mains et port de gants d'examen
- Vérification de la fixation et du positionnement (le système doit rester déclive pour assurer un écoulement antérograde)
- Nettoyage des salissures externes avec savon chirurgical et rinçage
- Désinfection de la portion externe du cathéter et de la zone péri-vulvaire ou préputiale avec compresses imbibées de chlorhexidine 0,05%
- Vidange ou remplacement de la poche de recueil si nécessaire
VI. Prévention des complications infectieuses
L'instauration d'une antibioprophylaxie systématique n'est pas recommandée.
La réduction du risque d'infection repose sur :
- une sélection appropriée des patients
- le respect des pratiques aseptiques par des soignants formés, lors de la pose et de l'entretien
- l'utilisation d'un système de collecte clos
- et surtout, le retrait précoce de la sonde dès que son maintien n'est plus justifié
Bibliographie
- BURKITT JM, Urethral Catheterization In Advanced Monitoring and Procedures for Small Animal Emergency and Critical Care, 2è Edition, 2023 John Wiley & Sons, Inc. 451-466
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Myocardites du chien et du chat : comment les suspecter ?
Paris, France
I. Introduction
La myocardite est une inflammation du muscle cardiaque (myocarde), pouvant résulter de causes infectieuses, immunitaires ou toxiques. Cette affection, bien que rare, est grave car elle peut entraîner une dysfonction myocardique aiguë ou chronique, des troubles du rythme et une insuffisance cardiaque. Chez le chien et le chat, le diagnostic de myocardite reste un défi, car les signes cliniques sont souvent non spécifiques et les outils diagnostiques définitifs, comme la biopsie, sont rarement utilisés.
II. Épidémiologie
La myocardite est une affection peu fréquente mais potentiellement sous-diagnostiquée en médecine vétérinaire.
- Espèces concernées : le chien est plus souvent touché que le chat. Cependant une affection particulière connue sous le nom d’hypertrophie myocardique transitoire (HMT) est reconnue depuis quelques années chez le chat, dont l’origine est supposée être une inflammation du myocarde.
- Races prédisposées : pas de prédisposition raciale. Une prédisposition des patients humains atteints de myocardiopathie arythmogène droite à la myocardite virale ou bactérienne a été suggérée, et il est connu que la myocardite peut potentiellement imiter les lésions de la myocardiopathie arythmogène droite. Cependant, le lien entre les deux affections reste à clarifier.
- Âge/Sexe toutes les tranches d'âge peuvent être atteintes, mais les jeunes animaux sont parfois plus sensibles aux agents infectieux (par exemple, le parvovirus).
- Causes principales :
- Infectieuses :
- Bactéries : Bartonella spp., Borrelia, Ehrlichia, Clostridium, Leptospira, etc ;
- Virus : Parvovirus canin, coronavirus félin, virus de la maladie de Carré ;
- Parasites : Trypanosoma cruzi (Maladie de Chagas) ;
- Protozoaires : Leishmania, Toxoplasma gondii, Neospora caninum.
- Toxiques :
- Doxorubicine, monoxyde de carbone, intoxication aux plantes.
- Immunomédiées :
- Réaction auto-immune post-infectieuse ou idiopathique (lupus érythémateux) ;
- Traumatiques.
- Infectieuses :
Dans de nombreux cas, aucune étiologie n'est identifiée.
La myocardite est une manifestation rare de la maladie de Lyme chez les chats comme chez les chiens. Un dépistage des co-infections (bartonellose, anaplasmose, virus de la leucémie féline, virus de l'immunodéficience féline) est recommandé.
III. Signes cliniques
Les manifestations cliniques de la myocardite sont très variables, allant de formes subcliniques à une décompensation aiguë. La présentation clinique dépend de l'étiologie sous-jacente. Certains virus et protozoaires peuvent produire des manifestations aiguës ou bien chroniques : les premières se caractérisent par des arythmies, une insuffisance cardiaque aiguë et une mort subite, tandis que les secondes se traduisent par une insuffisance cardiaque ou un tableau clinique évoquant une myocardiopathie dilatée. Des signes cliniques non spécifiques, tels que la léthargie, une hyporexie et des signes gastro-intestinaux, sont fréquents, tandis que des signes liés à une dysfonction cardiaque, tels que la tachypnée, la dyspnée et l'ascite, peuvent être observés dans certains cas. Les résultats de l'examen physique reflètent généralement une inflammation systémique ou une mauvaise perfusion, bien que la tachypnée et la détection d'arythmies soient relativement courantes.
- Signes généraux :
- léthargie, anorexie, amaigrissement, fièvre (seulement chez 20 % des cas avérés).
- Signes cardiaques :
- arythmies (tachycardie, extrasystoles ventriculaires, bloc atrioventriculaire, oreillette silencieuse) ;
- syncope, intolérance à l’effort ;
- bruits de galop ou souffle cardiaque (par dysfonction valvulaire secondaire).
- Signes d’insuffisance cardiaque :
- dyspnée, toux, ascite, œdème pulmonaire.
IV. Échocardiographie
L’échocardiographie est un outil fondamental pour évaluer la fonction et la structure cardiaque. Elle peut mettre en évidence :
- une dilatation des cavités cardiaques, surtout du ventricule gauche ;
- une hypokinésie segmentaire ou globale du myocarde ;
- une diminution de la fraction de raccourcissement ou de la fraction d’éjection ;
- un épanchement péricardique (secondaire à une péricardite associée ou à une insuffisance cardiaque congestive) ;
- des parois myocardiques irrégulières ou épaissies (dans les formes inflammatoires actives comme c’est le cas des HMT) ;
- des lésions d’endocardite peuvent être présentes concomitamment.
Le suivi échocardiographique est le seul moyen de discriminer une myocardiopathie hypertrophique d’une HMT.
Limite l'échocardiographie permet de suspecter mais pas de confirmer une myocardite.
V. Marqueurs cardiaques
Les biomarqueurs sont des aides diagnostiques très utiles dans la suspicion de myocardite.
- Troponine I cardiaque (cTnI) :
- fait partie du complexe protéique qui intervient dans la régulation de la contraction musculaire en contrôlant l'interaction actine-myosine en fonction de la concentration en calcium intracellulaire ;
- protéine libérée dans le sang lors de lésions des cardiomyocytes ou leur mort ;
- très spécifique d’une atteinte myocardique ;
- préférable d’utiliser des méthodes de mesures avec une haute sensibilité (troponine I ultrasensible) ;
- taux fortement augmentés dans les myocardites aiguës ;
- permet également le suivi de l’évolution ;
- une concentration circulante élevée de cTnI est un constat courant et utile car, bien qu'elle ne soit pas spécifique à la myocardite, une majorité des cas présentent une concentration circulante bien supérieure à celle généralement observée dans les cardiomyopathies ou les maladies valvulaires.
- BNP / NT-proBNP :
- marqueurs de distension myocardique ;
- moins spécifiques que la troponine, mais utiles dans le cadre d’une insuffisance cardiaque globale.
VI. Examens complémentaires
- ECG :
- mise en évidence d’arythmies : tachycardie ventriculaire et bloc atrioventriculaire le plus fréquemment, mais aussi extrasystoles ventriculaires, fibrillation atriale, blocs de branche, oreillette silencieuse…;
- utile pour guider le traitement antiarythmique.
- Radiographie thoracique :
- cardiomégalie possible ;
- signes d’œdème pulmonaire ou d’épanchement pleural.
- Analyses infectieuses et bilan sanguin :
- sérologies, PCR, tests rapides selon les agents suspects ;
Important dans les régions endémiques (ex. leishmaniose, ehrlichiose) ; - la thrombocytopénie et la neutrophilie sont les anomalies les plus courantes sur les analyses sanguines de routine, mais elles sont présentes dans un peu plus de la moitié des cas.
- sérologies, PCR, tests rapides selon les agents suspects ;
- Biopsie myocardique :
- rare en pratique vétérinaire ;
- gold standard ;
- la biopsie myocardique confirmant l'inflammation myocardique ou son étiologie est rarement effectuée, voire jamais, en raison de l'expertise nécessaire et des risques anesthésiques et procéduraux.
VIII. Conclusion
La myocardite est une affection grave mais souvent méconnue chez le chien et le chat. Une approche diagnostique rigoureuse est essentielle, combinant clinique, imagerie, électrocardiographie et biomarqueurs. L'utilisation de la troponine I est particulièrement précieuse pour orienter le diagnostic. La prise en charge précoce améliore le pronostic, bien que l’évolution reste imprévisible selon l’étiologie et la gravité de l’atteinte myocardique.
Bibliographie
- LAKHDHIR S, VIALL A, ALLOWAY E, et col. Clinical presentation, cardiovascular findings, etiology, and outcome of myocarditis in dogs: 64 cases with presumptive antemortem diagnosis (26 confirmed postmortem) and 137 cases with postmortem diagnosis only (2004-2017). J Vet Cardiol. 2020;30:44-56.
- MOLESAN A, GOODMAN L, FORD J, et col. The causes of canine myocarditis and myocardial fibrosis are elusive by targeted molecular testing: retrospective analysis and literature review. Vet Pathol. 2019;56:761-77.
- NOVO MATOS J, PEREIRA N, GLAUS T, et col. Transient Myocardial Thickening in Cats Associated with Heart Failure. J Vet Intern Med. 2018;32:48-56.
- ROMITO G, ELMI A, GUGLIEMINI C, et col. Transient myocardial thickening: a retrospective analysis on etiological, clinical, laboratory, therapeutic, and outcome findings in 27 cats. J Vet Cardiol. 2023;50:51-62.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Myocardites du chien et du chat : rechercher la cause ?
Ollioules France
I. Introduction
La myocardite, définie comme une inflammation du muscle cardiaque (myocarde), est une maladie rare mais grave chez le chien et le chat. Elle peut entraîner une insuffisance cardiaque, des troubles du rythme, voire la mort subite. Identifier la cause de la myocardite est essentiel pour adapter le traitement, prévenir les récidives et améliorer le pronostic.
II. Définition et conséquences de la myocardite
La myocardite est une inflammation du myocarde. L'inflammation, quelle qu'en soit la cause, altère la contractilité cardiaque, pouvant conduire à une dilatation des cavités, une insuffisance cardiaque congestive et des troubles du rythme (arythmies).
III. Causes de myocardite chez le chien et le chat
Les causes de myocardite sont multiples et peuvent être classées en deux grandes catégories : infectieuses et non infectieuses.
1. Causes infectieuses
a) Bactériennes
- Extension d'une endocardite bactérienne : l'infection de la valve cardiaque peut s'étendre au myocarde ;
- Septicémie : La dissémination bactérienne à partir d'un foyer infectieux distant (abcès, pyomètre, infection urinaire, etc.) peut atteindre le myocarde ;
- Agents spécifiques : Bartonella spp., Borrelia (maladie de Lyme), Ehrlichia, Leptospira, etc.
b) Virales
- Parvovirus canin : surtout chez les chiots, responsable de myocardites fulgurantes ;
- Coronavirus, adénovirus, herpesvirus : rares, mais documentés chez le chien et le chat ;
- Virus non spécifiés chez le chat : la myocardite virale est suspectée mais rarement confirmée, faute de tests spécifiques.
c) Protozoaires
- Trypanosoma cruzi (maladie de Chagas) : endémique dans certaines régions (sud des États-Unis, Amérique centrale et du sud), provoque des myocardites sévères chez le chien ;
- Toxoplasma gondii : peut causer une myocardite chez le chat, surtout immunodéprimé ;
- Neospora caninum : principalement chez le chien.
d) Fongiques
- Blastomycose : rare, mais rapportée comme cause de myocardite chez le chien.
2. Causes non infectieuses
a) Toxiques et médicamenteuses
- Chimiques : intoxication par certaines substances (ex : doxorubicine, un agent chimiothérapeutique) ;
- Médicaments : certains antibiotiques, anti-inflammatoires, ou médicaments à visée cardiaque peuvent être impliqués [27].
b) Maladies à médiation immunitaire
- Réaction auto-immune, isolée ou associée à une maladie systémique (ex : lupus érythémateux disséminé).
c) Causes physiques
- Traumatisme thoracique : un choc violent peut léser le muscle cardiaque et induire une réaction inflammatoire ;
- Coup de chaleur : peut provoquer une nécrose myocardique et une inflammation secondaire.
d) Idiopathiques
- Dans de nombreux cas, aucune cause n'est identifiée malgré des investigations poussées.
IV. Recherche de la cause : démarche diagnostique
1. Anamnèse et examen clinique
Le recueil des antécédents est fondamental :
- âge, race, mode de vie, voyages récents, exposition à des vecteurs (tiques, moustiques), alimentation, traitements médicamenteux récents, traumatismes, maladies concomitantes ;
- symptômes : faiblesse, syncope, toux, dyspnée, intolérance à l'effort, arythmies, signes d'infection systémique (fièvre, abattement).
2. Examens complémentaires
a) Biologie
- Numération formule sanguine : recherche d'un syndrome inflammatoire, d'une infection, d'une anémie ;
- Biochimie : évaluation de la fonction rénale et hépatique, recherche d'atteinte multi-organique ;
- Marqueurs cardiaques : troponine I cardiaque (cTnI), très sensible à la nécrose myocardique ;
- Sérologies et PCR : recherche d'agents infectieux (Leishmania, Ehrlichia, Borrelia, Leptospira, Bartonella, Trypanosoma, Toxoplasma, Neospora, etc.) selon le contexte épidémiologique.
b) Imagerie
- Échocardiographie : permet de visualiser des anomalies de la contractilité, des zones d'hypokinésie, des dilatations, des épanchements péricardiques, ou des masses. Elle oriente mais ne permet pas de poser le diagnostic étiologique ;
- Radiographie thoracique : recherche d'une cardiomégalie, d'un œdème pulmonaire, d'un épanchement pleural ;
- ECG : recherche d'arythmies, fréquentes en cas de myocardite (extrasystoles, tachycardie ventriculaire, blocs auriculo-ventriculaires).
c) Biopsie myocardique
- Diagnostic de certitude : l'histopathologie du tissu myocardique est la seule méthode permettant de confirmer la myocardite et d'identifier parfois l'agent causal (colorations spéciales, PCR sur tissu) ;
- Limites : procédure invasive, rarement réalisée en pratique courante, réservée aux cas graves ou à la recherche.
V. Particularités chez le chat
Chez le chat, la myocardite est moins bien documentée, mais les causes infectieuses restent dominantes :
- Toxoplasma gondii : agent majeur chez le chat, surtout immunodéprimé ;
- Bartonella henselae : suspectée mais rarement prouvée ;
- FIV/FeLV : les virus de l'immunodéficience et de la leucémie féline peuvent indirectement favoriser une myocardite ;
- Les causes non infectieuses sont similaires à celles du chien (toxiques, médicaments, maladies auto-immunes, traumatismes).
VI. Causes secondaires et facteurs favorisants
- Maladies systémiques : l'hyperthyroïdie, l'hypertension artérielle ou des maladies auto-immunes peuvent favoriser l'apparition d'une myocardite, notamment chez le chat ;
- Carences nutritionnelles : rarement, une carence en taurine ou en carnitine peut être impliquée, surtout chez le chat ;
- Prédispositions raciales et génétiques : certaines races de chiens et de chats semblent plus à risque, probablement en raison de facteurs immunogénétiques.
VII. Synthèse de la démarche étiologique
- Recueillir les antécédents et l'environnement de l'animal : âge, race, voyages, exposition à des vecteurs, alimentation, traitements.
- Rechercher des signes cliniques évocateurs : insuffisance cardiaque, troubles du rythme, signes infectieux ou systémiques.
- Réaliser des examens complémentaires ciblés :
- bilan sanguin complet, marqueurs cardiaques (troponine I), sérologies/PCR selon les suspicions ;
- imagerie cardiaque (échocardiographie, radiographie) ;
- ECG pour dépister les arythmies.
- Envisager une biopsie myocardique en dernier recours, ou à visée de recherche, si le diagnostic reste incertain. Très peu réalisé en pratique.
- Adapter la prise en charge selon la cause identifiée ou suspectée (antibiotiques, antiparasitaires, immunosuppresseurs, arrêt des toxiques, traitement symptomatique de l'insuffisance cardiaque et des arythmies).
VIII. Conclusion
La recherche de la cause d'une myocardite chez le chien et le chat repose sur une démarche méthodique, intégrant anamnèse, examens complémentaires et, rarement, quasiment jamais, biopsie myocardique. Les causes infectieuses dominent, mais les causes non infectieuses ne doivent pas être négligées. L'identification de l'étiologie conditionne le pronostic et le choix thérapeutique.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Néphropathies et répercussions cardiaques
Merignac, France
I. Introduction
Du fait de leur fonctions propres, les reins et le cœur collaborent de façon permanente. Le but pour le cœur est de pouvoir maintenir une perfusion satisfaisante aux divers organes du corps tandis que les reins maintiennent l'homéostasie nécessaire pour permettre les diverses fonctions cellulaires, la communication et les fonctions métaboliques. Dans les syndromes cardio-rénaux, tout déséquilibre dans cet équilibre cœur/rein a des conséquences directes sur la fonction cardiaque comme sur la fonction rénale.
- Le terme de syndrome cardiorénal définit une maladie cardiaque ou rénale qui peut induire une dysfonction de l'autre système.
- Le syndrome cardiorénal est divisé en 5 types de désordres de l'axe cardiovasculaire-rénal (DCvR) :
- Le type 1 et le type 2 définissent une maladie cardiaque aigue ou chronique (respectivement) ayant des répercussions rénales
- Le type 3 et le type 4 définissent une maladie rénale aigue ou chronique ayant des répercussions cardiaques
- Le type 5 définit une affection systémique résultant en une affection cardiaque et rénale concomitante.
Nous nous intéresserons donc dans cette présentation aux types 3 et 4.
II. Rappels de physiologie rénale
L'énorme débit de filtration glomérulaire requiert pour le maintien de l'homéostasie un flux sanguin tout aussi conséquent. Ainsi, bien que les reins représentent <1% de la masse corporelle, ils représentent l'organe le plus perfusé. Environ 20% du volume sanguin passe par les reins à chaque cycle cardiaque. Ceci permet de maintenir une pression dans les capillaires rénaux élevée et de maintenir un bon débit de filtration glomérulaire.
Malgré cette perfusion rénale conséquente et la quantité d'oxygène apportée aux reins, l'anatomie particulière du néphron et de sa vascularisation (vasa recta) rend certaines parties du néphron sujettes à une hypoxie fréquemment observée cliniquement. Ainsi, en cas d'hypoperfusion, certaines parties du néphron (médullaires) peuvent rapidement souffrir d'un manque d'oxygène et une insuffisance rénale aiguë peut vite s'installer.
Le rôle primaire des reins étant le maintien de l'homéostasie, ce dernier passe par la régulation des différents ions (Potassium, Sodium, Calcium…) du milieu intérieur et par l'équilibre acido-basique de ce dernier :
La gestion du sodium et du potassium : la réabsorption du sodium et du potassium et de nombreux ions a lieu dans le tubule proximal rénal. Des pompes Na/2Cl/K sont les principales responsables de cette réabsorption ionique. Ces pompes sont notamment le site d'inhibition de médicaments diurétiques tel que le furosémide. En cas d'hyperkaliémie, une excrétion d'ions potassium en excès peut avoir lieu dans les tubules distaux et les conduits collecteurs grâce aux cellules intercalées de type B en plus des cellules principales et de leur récepteur ROMK. À l'inverse, en cas d'hypokaliémie, davantage de potassium peut être réabsorbé en ce même site par des cellules intercalées de type A.
La gestion du calcium : le maintien de la calcémie est régi par l'action de la PTH et de la vitamine D. Au niveau rénal, 99% du calcium filtré est réabsorbé (en majorité dans le tubule proximal). Cette réabsorption se fait par voie paracellulaire mais également par transport actif via des pompes sodium/calcium.
Le maintien de l'équilibre acidobasique : 80-90% des bicarbonates sont réabsorbés dans les tubules proximaux. Afin de réabsorber des bicarbonates, le rein doit sécréter des protons (H+). Les cellules intercalées de type A permettent d'augmenter la sécrétion de protons afin de réabsorber une quantité plus importante de bicarbonates. En cas d'alcalose, il n'y a pas assez de protons à sécréter et les bicarbonates ne sont pas autant réabsorbés.
La pression artérielle systémique est majoritairement contrôlée par les reins. Le maintien d'une pression artérielle satisfaisante est nécessaire à la bonne perfusion rénale, au maintien d'un bon débit de filtration glomérulaire et à la bonne fonction rénale. La rénine sécrétée par l'appareil juxta glomérulaire est la première étape du système rénine angiotensine aldostérone permettant le contrôle à moyen et long terme de la pression artérielle. Toutefois, ce système ne permet pas le contrôle d'un changement de pression brutale dans le cas d'un changement de position ou d'une perte sanguine aiguë.
Les reins sont également le siège de la synthèse de l'EPO grâce à des récepteurs sur des cellules de type fibroblastes péritubulaires pouvant ressentir l'hypoxie. En cas de maladie rénale avancée, une anémie arégénérative est fréquemment observée suite à l'absence de cellules fonctionnelles pouvant synthétiser l'EPO. Cette anémie peut à la fois avoir des conséquences sur le système cardiovasculaire et sur la perfusion rénale.
III. Répercussions cardiaques des néphropathies
1. Hypertension systémique
a) Physiopathologie
L'hypertension systémique (HTS) est la complication cardiovasculaire la plus fréquente des néphropathies chez le chien et le chat. Elle est présente chez 20 à 65% des chats atteints de maladie rénale chronique (MRC) et jusqu'à 75% des chiens souffrant d'insuffisance rénale aiguë.
Il n'existe néanmoins pas de corrélation entre la sévérité de la MRC et la prévalence ou la sévérité de l'hypertension.
La physiopathologie de l'HTS dans les néphropathies est multifactorielle :
- Activation du système rénine-angiotensine-aldostérone (SRAA), systémique et local, favorisant la vasoconstriction, une excrétion sodée diminuée et un volume intravasculaire augmenté.
- Dysfonction endothéliale, diminution de la vasodilatation NO-dépendante, augmentation des endothélines et du stress oxydatif.
- Iatrogène : surcharge en fluides, agents stimulant l'érythropoïèse.
Bien qu'aucune association nette entre les niveaux plasmatiques d'aldostérone et de rénine n'aient été mise en évidence chez les chats présentant une MRC et une hypertension, les niveaux d'aldostérone sont élevés lors de MRC, indiquant que l'aldostérone pourrait contribuer au développement de l'HTS. Ceci pourrait être indépendant du SRAA, puisque l'hypertension ne répond pas bien aux IECA chez le chat, et que les concentrations de rénine sont normaux à bas chez ces animaux.
Chez le chat, le rôle du SRAA systémique est parfois remis en cause.
La protéinurie est à la fois conséquence et facteur aggravant de l'HTS, accélérant l'inflammation et la sclérose glomérulaire. Elle est associée au pronostic chez les chats atteints de MRC et d'HTS quelle qu'en soit la cause.
b) Conséquences cardiovasculaires
L'hypertension systémique (HTS) entraîne des modifications structurelles et fonctionnelles du cœur :
- Hypertrophie ventriculaire gauche (HVG) :
- L'augmentation de la postcharge induit une hypertrophie concentrique du ventricule gauche pour normaliser le stress pariétal. Chez le chat, l'HVG est décrite dans 74–85% des cas avec différents phénotypes. Une dilatation aortique proportionnelle à la pression artérielle est fréquente. Des zones myocardiques hyperéchogènes, suggérant une fibrose, peuvent régresser sous traitement antihypertenseur.
- Chez le chien, l'HVG est plus variable (5–91% des cas selon les critères échographiques) mais souvent symétrique ; une fibrose myocardique et une dilatation de l'aorte sont également rapportées.
- Dysfonction diastolique :
- Elle peut précéder l'hypertrophie et la fibrose, avec ralentissement de la relaxation ventriculaire et anomalies Doppler (inversion du rapport E/A mitral, allongement du temps de relaxation isovolumétrique).
- Dysfonction systolique :
- Rare, caractérisée par une diminution des vitesses de raccourcissement myocardique ; la fraction d'éjection reste généralement normale.
- Troubles du rythme :
- L'HTS favorise une instabilité électrique myocardique, notamment en présence d'activation du SRAA, avec raccourcissement de la période réfractaire et arythmies auriculaires ou ventriculaires.
2. Désordres électrolytiques et acidobasiques
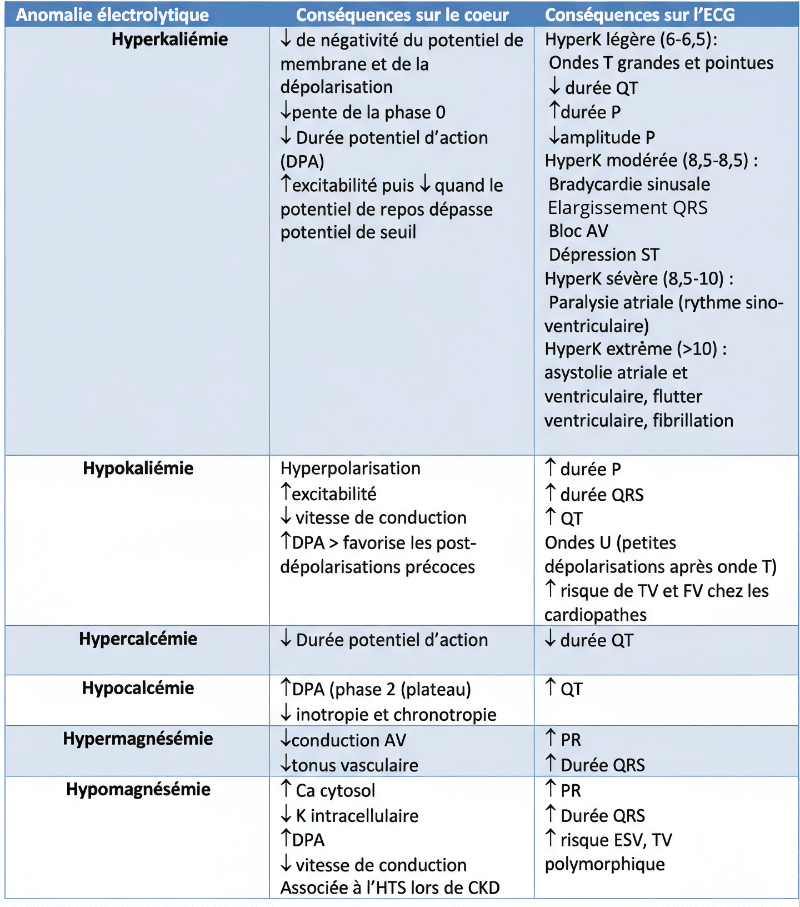
Figure 1 : Désordres électrolytiques et acidobasiques dans les néphropathies
a) Hyperkaliémie
Elle résulte d'une diminution de l'excrétion rénale lors d'insuffisance rénale aigue. Elle provoque des troubles de la conduction (ondes T pointues, élargissement du QRS, bradycardie, bloc AV) avec risque d'asystolie. Les anomalies ECG apparaissent généralement pour des kaliémies > 6,5 mEq/L.
Prise en charge :
- Gluconate de calcium IV (0,5–1,5 ml/kg)
- Insuline-glucose, bicarbonate ou β2-agonistes pour stimuler l'entrée intracellulaire du K+.
b) Hypokaliémie
Due à des pertes rénales lors de MRC, elle provoque une hyperexcitabilité myocardique : tachyarythmies auriculaires ou ventriculaires, anomalies ECG (PR et QT prolongés, onde P amplifiée, dépression ST).
c) Hypercalcémie
L'hypercalcémie peut être observée chez 20% des chats atteints de MRC et plus rarement chez le chien (< 10%). Elle résulte d'une hyperparathyroïdie secondaire, d'un apport calcique excessif (alimentation, vitamine D) ou parfois d'une hypercalcémie idiopathique féline. Sur le plan cardiovasculaire, une bradycardie, un raccourcissement du QT, voire des blocs atrioventriculaires ou une asystolie ont été rapportés lors d'hypercalcémies sévères.
d) Hypocalcémie
L'hypocalcémie est rare chez le chien et le chat atteints de MRC et se rencontre surtout aux stades avancés ou lors d'hyperphosphatémie sévère avec hyperparathyroïdie secondaire. Elle est généralement peu symptomatique sur le plan cardiovasculaire. En cas d'hypocalcémie profonde, des troubles du rythme (allongement du QT, bradycardie, bloc AV) ont été décrits, mais ils sont exceptionnels dans le contexte de la MRC chez nos animaux. La correction vise avant tout à contrôler l'hyperphosphatémie et à supplémenter en vitamine D active si nécessaire, tout en surveillant le calcium ionisé pour prévenir les complications cardiaques et la minéralisation tissulaire.
e) Désordres acido-basiques
L'acidose métabolique est fréquente lors de MRC : chez le chat, elle devient surtout manifeste aux stades avancés (pH veineux bas chez environ 50% des cas sévères), tandis que chez le chien, un déficit en bicarbonate < 22 mmol/L est observé dans environ 70% des cas, avec une fréquence croissante selon le stade IRIS. Elle reflète la baisse d'ammoniogenèse et de l'excrétion des acides et s'accompagne d'effets cardiovasculaires délétères (diminution de l'inotropie, vulnérabilité rythmique, potentialisée par l'hyperkaliémie). Chez l'homme, l'acidose est associée à un sur-risque d'événements cardiovasculaires majeurs et à un remodelage cardiaque. L'équilibre acido-basique des animaux atteints de MRC est donc à surveiller, surtout si une cardiopathie sous-jacente est présente.
IV. Conclusion
De nombreuses conséquences de néphropathies peuvent avoir un impact sur le cœur et sa fonction. Le contrôle de ces complications rénales sont essentiels afin de préserver la fonction cardiaque et l'homéostasie en général. Par ailleurs, du fait de la collaboration étroite entre le cœur et les reins, les cardiopathies peuvent également présenter de nombreuses répercussions rénales telle qu'une hypoperfusion rénale, de la surcharge volémique pouvant entraîner un œdème rénal et une perte de fonction, le risque de lésions ischémiques…
Bibliographie
- SANTILLI RA, MOÏSE NS, PEREGO M et coll. Electrocardiography of the Dog and Cat: Diagnosis of Arrhythmias. 2nde éd. Milan : Edra ; 2018.
- BUSSADORI C, PRADELLI D. Textbook of Cardiovascular Medicine in Dogs and Cats. Milan : Edra ; 2021.
- ETTINGER SJ, FELDMAN EC, CÔTÉ E. Textbook of Veterinary Internal Medicine. 9è éd. St Louis : Elsevier ; 2024.
- SYME HM. Hypertension in small animal kidney disease. Vet Clin North Am Small Anim Pract. 2011 ; 41 : 63-89.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Oncologie : une démarche diagnostique exhaustive
Ollioules, France
I. Introduction
En oncologie, la question du pronostic est au centre de toutes les préoccupations et le choix des traitements dépend des résultats que l’on peut en espérer : quelle qualité de vie ? Pour combien de temps ?
Pour répondre à ces interrogations, certains examens sont nécessaires. En effet, il n’est pas possible de connaître le pronostic précis sur la base unique d’un examen clinique ou même d’une analyse morphologique isolée. Ici, nous allons expliquer la démarche diagnostique en oncologie, sa logique et en quoi la suivre rigoureusement est indispensable pour répondre efficacement aux questionnements des membres du foyer d’un animal atteint de cancer.
La démarche se déroule en quatre étapes :
- Suspicion clinique,
- Diagnostic,
- Bilan d’extension,
- Traitement
Pour évaluer le pronostic, nous avons besoin a minima de connaître la nature tumorale, son grade et son stade. Cette conférence sera donc centrée sur les étapes du diagnostic et du bilan d’extension.
II. Le diagnostic
Le diagnostic est une convergence d’éléments, d’où l’intérêt de la suspicion initiale. Souvent, le diagnostic est suspecté sur la base d’un examen clinique et/ou d’imagerie médicale. La confirmation nécessite ensuite une analyse morphologique, c’est-à-dire cytologique et/ou histologique des cellules.
L’analyse cytologique est plus simple de réalisation qu’une analyse histologique, ne nécessite pas d’anesthésie et son résultat est connu en quelques jours contre 1 à 3 semaines pour de l’histologie conventionnelle. En revanche, l’examen cytologique est moins informatif que l’examen histologique. La cytologie est souvent suffisante pour déterminer si nous sommes face à une tumeur et généralement sa grande catégorie (épithéliale, ronde, mésenchymateuse) mais l’histologie est plus précise et permet de déterminer le type tumoral précis et généralement le grade.
Finalement, l’analyse cytologique est généralement suffisante au stade du diagnostic puisqu’elle permet, en déterminant le grand type tumoral, de réaliser un bilan d’extension adapté dans la grande majorité des cas. C’est donc très souvent la première étape.
Il existe certaines situations où il vaut tout de même mieux éviter, notamment :
- contexte d’urgence (exemple hémorragie abdominale) ? Chirurgie thérapeutique et diagnostique ;
- cavité buccale : inflammation + anesthésie ? biopsies ;
- masse surrénalienne : utilité discutable, de moins en moins conseillé. Recherche de sécrétions (chien : catécholamines maladie de Cushing) ± surranélectomie ;
- masse interne très vascularisée, cavitaire, thrombopénie, au cas par cas.
Parfois l’analyse morphologique ne suffit pas, plusieurs techniques complémentaires peuvent alors être utilisées, notamment :
- les immunomarquages permettent de déterminer la nature d’une cellule en ciblant des marqueurs spécifiques de chaque population cellulaire. Ils sont principalement utilisés pour les tumeurs peu différenciées où le caractère tumoral est certain mais le type tumoral, incertain. Ils peuvent également être utiles pour aider à différencier une population tumorale d’une population inflammatoire dans certaines situations (lymphomes digestifs félins de bas grade par exemple) ou encore pour vérifier l’absence de cellules métastatiques d’une tumeur non lymphoïde dans un nœud lymphatique. Ils peuvent également avoir une valeur pronostique, c’est le cas du marqueur de prolifération Ki-67 qui permet d’identifier l’ensemble des cellules en cycle i.e. en dehors de la phase G0, là où l’oeil humain ne détecte que les mitoses et est particulièrement utile, entre autres, pour certains mastocytomes ou lymphomes de grade incertain. Le substrat idéal des immunomarquages est l’histologie immunohistochimie mais cela peut également être réalisé en cytologie immunocytochimie...
- la cytométrie en flux utilise aussi des marqueurs cellulaires mais uniquement membranaires cette fois. Elle identifie les cellules en fonction de multiples paramètres incluant a minima la taille des cellules et la présence de marqueurs spécifiques à leur surface (clusters de différenciation). Cette technique est principalement utilisée pour les hémopathies malignes déjà diagnostiquées afin de déterminer l’immunophénotype. Elle peut aussi être utilisée dans le cadre d’une suspicion d’hémopathie maligne, non certaine, pour identifier la présence ou non de cellules du même immunophénotype et donc apporter des arguments en faveur d’une hypothèse tumorale ou non. Elle peut être réalisée sur prélèvement sanguin, liquide d’épanchement ou sucs ganglionnaires et est principalement développée chez le chien (encore peu d’anticorps disponibles chez le chat). L’autre limite est l’instabilité cellulaire : les prélèvements doivent être pris en charge par le laboratoire au plus vite et en 48 heures maximum...
- Le test de clonalité (PARR i.e. PCR for Antigen Receptor Rearrangements ou PCR pour la réorganisation des récepteurs d’antigènes en français) permet de différencier une population clonale de lymphocytes, typiquement cancéreuse, d’une population polyclonale, typiquement inflammatoire. Il n’existe un tel test que pour les cellules lymphoïdes. La PARR est utile lorsqu’il est difficile de différencier une hyperplasie lymphoïde réactionnelle d’une néoplasie lymphoïde sur la base des seules analyses morphologiques ou immunochimiques. Cette technique peut également être utilisée pour évaluer la présence de résidus de maladie après traitement, en surveillant les réarrangements clonaux spécifiques au fil du temps mais cela est encore peu applicable en médecine vétérinaire. Il s’agit d’une analyse de bonne sensibilité autour de 90 % et très spécifique chez le chien, jusqu’à 95 %, mais variable en fonction des études chez le chat (30-90 %) - plutôt 80-90 % pour les néoplasies lymphoïdes T et 30-50 % pour les néoplasies lymphoïdes B. Elle est communément réalisée sur des biopsies en formol ou congelées mais peut également être réalisée sur des lames de cytologie déjà fixées, ce qui est particulièrement intéressant pour les leucémies ou dans le cas où des biopsies sont non souhaitées ou non réalisables...
- La recherche de la mutation BRAF V595E est utilisée dans le diagnostic des carcinomes urothéliaux canins non transposable chez le chat et est réalisée par PCR sur urines. Cette mutation du gène BRAF, impliqué dans la voie de signalisation MAPK, favorise la prolifération cellulaire anormale et l’oncogenèse et est présente dans environ 80 % des carcinomes urothéliaux incluant les carcinomes prostatiques. En cas de doute l’analyse cytologique sur le caractère tumoral ou dysplasique secondaire à une inflammation marquée de la population urothéliale, la recherche de la mutation peut aider au diagnostic avec une sensibilité de l’ordre de 65-80 % et une spécificité rapportée jusqu’ici de 100 %.
III. Bilan d’extension
Une fois le diagnostic de tumeur établi, il est important d’en établir l’extension, c’est-à-dire l’impact de cette tumeur sur l’organisme. Pour cela il faut s’interroger sur l’agressivité locale et à distance. Localement, est-ce que c’est infiltrant sur les structures périphériques ? Douloureux ? Est-ce que ça peut rompre ou nécroser ? À distance, est-ce que le risque métastatique est levé ? Quels organes sont concernés ?...
Le bilan d’extension découle de ces questions et doit être adapté au cas par cas. Il comportera toujours de l’imagerie et souvent de la cytologie. Attention, un amalgame de plus en plus fréquent est la réalisation d’un scanner corps entier en guise de bilan d’extension des masses, souvent avant même l’obtention du diagnostic. En bref, on a détecté une masse, on fait un scanner et s’il n’y a rien d’inquiétant, on va la retirer chirurgicalement en vue d’une analyse histologique. En fait, le scanner corps entier permet de vérifier l’extension de la majorité des tumeurs mais il est inutile dans la quasi-totalité des cas (très rare d’avoir besoin du corps entier) et insuffisant dans un certain nombre de situations : examen cytologique du foie et de la rate en cas de tumeur à cellules rondes, recherche du nœud lymphatique (NL) sentinelle pour les mastocytomes et les tumeurs de la tête et du cou etc. Aussi, le fait de réaliser un scanner corps entier et non ciblé par région diminue la fiabilité de son interprétation. Enfin, enchaîner dans une même anesthésie un scanner corps entier, son interprétation et l'intervention chirurgicale augmente grandement le temps d’anesthésie en comparaison d’un bilan d’extension adapté puis, dans un second temps, la mise en place du traitement après réflexion et discussion avec les propriétaires.
Le Tableau 1 résume brièvement les agressivités des différents types tumoraux. Il existe énormément d’exceptions et n’est donné qu’à titre indicatif, pour permettre de se positionner dans le cas général...
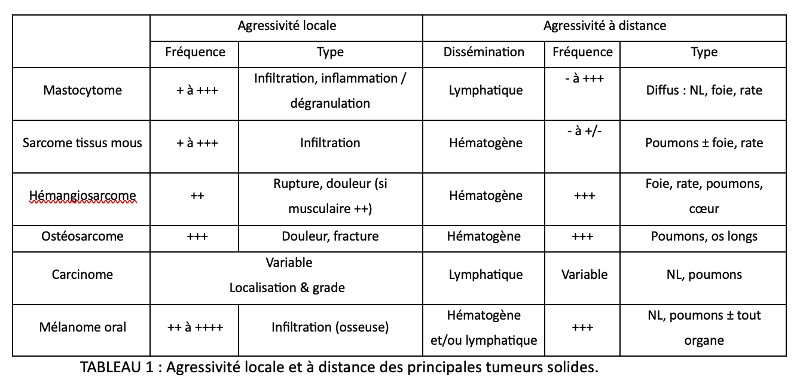
Tableau 1 : Agressivité locale et à distance des principales tumeurs solides.
À partir de la tumeur principale, les métastases diffusent par voie lymphatique et/ou hématogène. Globalement les tumeurs à cellules rondes et les carcinomes diffusent par voie lymphatique, les sarcomes diffusent par voie hématogène et les mélanomes diffusent par l’une, l’autre ou les deux. Connaître les différentes voies aide à deviner les sites métastatiques principaux et le bilan d’extension a pour objectif d’analyser ces différents sites par divers examens :
- la recherche de nodules pulmonaires est réalisée par scanner dans la mesure du possible, le seuil de détection étant de 1-2 mm contre 5-7 mm pour les radiographies thoraciques ;
- lorsque le NL est un site métastatique préférentiel, la lymphographie est utile pour rechercher le NL sentinelle. L’application principale est le cas des mastocytomes, où le NL régional n’est pas le NL sentinelle dans près de 50 % des cas. Le plus pratique est la lymphographie par scanner, elle peut être réalisée au cours du scanner de bilan d’extension en faisant quelques acquisitions supplémentaires ;l
- la cytologie a un rôle important dans le bilan d’extension pour confirmer les suspicions de métastases. C’est systématiquement recommandé et particulièrement important lors de situations particulières.
IV. Conclusion
Finalement, le cancer est un groupe de maladies très hétérogène et le pronostic est très variable d’un cancer à l’autre, d’un individu à l’autre et d’une famille à l’autre. Il est important de réaliser un diagnostic et un bilan d’extension adaptés afin d’obtenir un tableau clinique et donc un pronostic précis. Cela permet d’être le plus pertinent possible sur les possibilités thérapeutiques et donc d’optimiser la prise en charge tout en limitant le stress que ce diagnostic génère pour les propriétaires.
Bibliographie
- MARSILIO S et coll. ACVIM consensus statement guidelines on diagnosing and distinguishing low-grade neoplastic from inflammatory lymphocytic chronic enteropathies in cats. J Vet Intern Med. 2023 37 794-816.
- AESCHLIMANN L et coll. Effective detection of BRAFV595E mutation in canine urothelial and prostate carcinomas using immunohistochemistry. Vet Comp Oncol. 2024 22 295-302.
- ANNONI M et coll. Sentinel lymph node mapping in canine mast cell tumours using a preoperative radiographic indirect lymphography Technique description and results in 138 cases. Vet Comp Oncol. 2023 21 3469-81.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Pathologie hépatobiliaire du chat
Ollioules, France
Mérignac, France
I. Introduction
Les hépatites primitives et les mucocèles biliaires sont rares chez le chat. En revanche, les maladies inflammatoires des voies biliaires (cholangites) et leurs répercussions sur le parenchyme hépatique (cholangio-hépatites) sont fréquentes, aussi bien sous une forme aiguë que chronique. Une autre particularité des chats est la forte prévalence d'une association entre plusieurs maladies inflammatoires : hépatique, pancréatique et intestinale (la « triade » féline). Cela est en partie dû à l'anatomie des voies biliaires et des canaux pancréatiques (le canal cholédoque et le canal pancréatique fusionnent avant de s'ouvrir par un simple et unique canal au niveau de la papille duodénale majeure).
Au travers de cette présentation, nous allons décrire les différentes maladies hépatobiliaires félines les plus fréquentes, puis dresser un arbre décisionnel des approches médicales et chirurgicales de leur gestion.
II. Étiopathogénie
Lors de cholangite neutrophilique (ou suppurée) aiguë (ANC), une infection bactérienne des voies biliaires est suspectée en priorité. Dès lors que le flux biliaire est ralenti ou interrompu, une colonisation bactérienne des voies biliaires est très fréquente, soit par voie ascendante depuis l'intestin grêle, soit par voie hématogène (vaisseaux portes hépatiques ou circulation générale). Les bactéries identifiées sont aérobies (E. coli et Enterococcus spp.) ou anaérobies (Bacteroides et Clostridium).
Lors de cholangite neutrophilique (ou suppurée) chronique (CNC), une infection bactérienne est aussi suspectée. Il peut cependant s'agir aussi d'une réponse neutrophilique secondaire à une obstruction chronique des voies biliaires, ou une cholangite lymphocytaire associée à de la nécrose hépatique ou une infection. Lors de CNC, on trouve souvent des signes d'obstruction des voies biliaires, des cholélithes (pas toujours visibles à l'échographie) et des anomalies de la plaque ductale. Par ailleurs, des lésions inflammatoires intestinales et pancréatiques sont identifiées chez une majorité des chats souffrant de CNC.
Les facteurs prédisposants aux infections biliaires incluent détartrage, alimentation crue, FIV+, médicaments immuno-dépresseurs.
Lors de cholangite lymphocytaire (LC), une origine dysimmunitaire est suspectée en priorité. Il s'agit toutefois probablement d'un syndrome regroupant plusieurs maladies ayant un aspect histopathologique similaire, mais avec des causes différentes.
III. Signes cliniques
Le signalement et les signes cliniques des patients souffrant d'ANC, de CNC ou de LC sont très similaires. Il s'agit de chats d'âge moyen ou âgés, des 2 sexes, sans prédisposition nette de race. Léthargie, dysorexie et vomissements sont classiquement observés. L'ictère est moins fréquent (sauf en cas d'obstruction complète du canal cholédoque) et l'hyperthermie pas systématique lors des cholangites neutrophiliques. Une douleur abdominale est parfois observée (mais souvent masquée par le patient). La proportion de chats asymptomatiques est élevée (environ 50% dans une étude). Les signes cliniques sont plus fréquents lors de pancréatite ou d'entéropathie inflammatoire concomitante. La présence d'ascite a été observée chez certains chats lors de LC.
IV. Diagnostic
Le diagnostic définitif des cholangites nécessite des biopsies hépatiques, une culture bactériologique aérobie et anaérobie (sur le foie et la bile) et une analyse cytologique de la bile. Lors d'ANC, une présomption diagnostique est établie sur la base des images échographiques abdominales et d'une analyse cytologique et bactériologique de la bile. Si aucune amélioration durable n'est observée malgré une antibiothérapie adaptée à l'antibiogramme, alors la réalisation des biopsies hépatiques est indiquée pour caractériser plus précisément la maladie.
1. Bilan biologique
Une neutrophilie est identifiée chez moins de la moitié des chats. Une augmentation d'activité des enzymes hépatiques est fréquente (non systématique), avec ALAT plus fréquemment augmentée que PAL. Une hyperbilirubinémie est fréquente (non systématique). Lors de LC, une hyperglobulinémie est possible, ce qui constitue parfois un challenge diagnostique en raison des similitudes avec la PIF. Les temps de coagulation sont souvent prolongés.
2. Imagerie médicale
L'échographie abdominale peut révéler des anomalies hépato-biliaires et aussi des autres organes. Certains chats ont un foie et des voies biliaires parfaitement normaux à l'échographie, alors qu'ils souffrent bien d'une cholangite/cholangio-hépatite.
3. Analyse cytologique de la bile
Une cholécystocentèse est indiquée en l'absence de contre-indication majeure (troubles de l'hémostase, patient en état de choc septique). L'analyse bactériologique de la bile est nécessaire (plus sensible pour détecter une infection que la culture d'une biopsie ou d'une cytoponction hépatique). Une culture positive sur la bile indique une infection (sauf contamination du prélèvement). Un examen cytologique de la bile est nécessaire en complément de la culture bactérienne, pour rechercher des germes et confirmer le caractère primaire de l'infection (versus une contamination). Pour augmenter encore les chances de détecter une infection bactérienne, il est conseillé de multiplier les sites pour l'analyse bactériologique : foie, bile dans la vésicule biliaire, kystes du cholédoque (si présents), cholélithiases (en les écrasant avant de les mettre dans le tube de transport), paroi de la vésicule biliaire (biopsie ou raclage).
4. Biopsies hépatiques pour analyse histopathologique
C'est la méthode de référence pour établir un diagnostic de cholangite neutrophilique ou lymphocytaire, en vérifiant l'hémostase avant les biopsies. L'administration de vitamine K1, au cours des 2 à 3 jours précédant les biopsies, est souvent utile en raison de la forte prévalence des troubles de l'hémostase secondaire chez les chats, surtout lors de pancréatite ou d'entéropathie concomitante. La technique idéale de biopsies est par laparotomie (qui permet aussi de prélever le pancréas et l'intestin grêle) ou laparoscopie. Les trucut échoguidés donnent des biopsies non optimales et peuvent provoquer un malaise vagal chez le chat.
V. Traitement
À ce jour, les conseils thérapeutiques sont surtout empiriques et probabilistes, sans preuve scientifique formelle pour les étayer, en particulier pour les formes chroniques de cholangites.
1. Cholangite neutrophilique aiguë
Une antibiothérapie, adaptée suivant l'antibiogramme, est le traitement de choix, pendant 4 à 6 semaines, sans qu'aucune étude ne permette de valider cette recommandation de manière formelle. Lors de choc septique, une hospitalisation avec antibiothérapie IV est nécessaire au début. L'association amoxicilline +/- acide clavulanique est souvent prescrite en première intention, étant donné qu'elle se concentre dans la bile et qu'une majorité des germes identifiés y est sensible. En cas de non-réponse sur le long terme, une nouvelle culture bactériologique avec antibiogramme est indiquée pour ajuster.
L'acide urso-déoxycholique et la S-adénosyl méthionine sont prescrits en complément, sans preuve formelle de leur efficacité.
Une alimentation précoce (+/- par sonde) et la gestion de la douleur sont nécessaires chez ces patients. Un aliment hyperdigestible ou un aliment de convalescence sont préférables aux aliments pour insuffisants hépatiques (trop carencés en protéines).
Le pronostic est souvent favorable si le traitement a été adapté et précoce, avec des durées de vie de 240 à 694 jours.
2. Cholangite neutrophilique chronique et cholangite lymphocytaire
Le traitement est très empirique, associant corticoïdes, antibiotiques, acide urso-déoxycholique, antioxydants et l'alimentation.
En raison du diagnostic différentiel qui inclut la PIF et l'infection émergente chez le chat par Hepadnavirus, il est conseillé de limiter l'utilisation des corticoïdes à dose immuno-suppressive aux cas ayant eu un diagnostic sur la base de biopsies hépatiques. Lors de LC, avec cultures bactériologiques négatives, des doses immuno-suppressives de corticoïdes sont indiquées, avec l'acide urso-déoxycholique, les anti-oxydants et une alimentation de bonne qualité. Un traitement symptomatique anti-émétique (maropitant +/- métoclopramide) et antalgique (morphinique ?) est nécessaire en complément.
Un suivi des paramètres sanguins hépatiques est nécessaire. Si l'activité ALAT et PAL augmente de manière significative lors du traitement, alors l'immuno-dépression par corticothérapie doit être réduite étant donné que, contrairement au chien, le chat ne présente pas d'induction enzymatique des PAL par les corticoïdes.
Une antibiothérapie est indiquée chez les chats souffrant de LC avec une composante neutrophilique, en attendant les résultats des cultures bactériennes. Si une infection bactérienne est fortement suspectée, avec culture bactériologique négative, alors une recherche d'agents infectieux par technique d'hybridation in situ par fluorescence (FISH) est conseillée.
Le pronostic lors de cholangite chronique (neutrophilique ou lymphocytaire) est très variable (de quelques jours à plusieurs années).
VI. Approches chirurgicales
1. Cholécystectomie
Indiquée en cas de cholélithiases, cholécystite réfractaire au traitement médical, et plus rarement de traumatisme/néoplasie de la vésicule biliaire ou de mucocèle. Avant d'envisager une cholécystectomie, il est indispensable de s'assurer de la bonne perméabilité du canal cholédoque, par échographie préopératoire ou par sondage peropératoire, rétrograde par duodénotomie ou normograde par une petite cholécystotomie. La dissection de la vésicule biliaire se fera idéalement en sous-capsulaire, c'est-à-dire en disséquant dans l'épaisseur de la paroi de la vésicule biliaire afin de laisser la capsule de la vésicule biliaire adhérente au foie, pour diminuer les saignements per-opératoires. Lors de la dissection du canal cystique, il faudra veiller à réaliser l'hémostase de l'artère cystique. Une fois la vésicule biliaire et le canal cystique disséqués, ce dernier sera ligaturé par une ou deux ligatures dont une transfixante ou à l'aide d'hémoclips, en prenant soin de ne pas traumatiser les canaux hépatiques ni le canal cholédoque. Il est important de garder en tête qu'il est impossible, après une cholécystectomie, de réaliser une dérivation des voies biliaires en cas d'obstruction du canal cholédoque.
2. Stent cholédoque
Indiqué en cas de pancréatite ou d'anomalie inflammatoire ou tumorale de la papille duodénale majeure, afin de permettre l'écoulement biliaire en parallèle de la gestion et de l'amélioration du processus primaire engendrant l'obstruction biliaire, telle qu'une pancréatite. La mise en place de ces stents se fait de manière rétrograde, via une duodénotomie de quelques cm réalisée en face de la papille duodénale majeure. Il est important de bien repérer le canal cholédoque jusqu'à son abouchement duodénal afin de s'assurer de réaliser la duodénotomie au bon endroit, sous peine de devoir la prolonger. L'usage de sonde d'alimentation souple est communément recommandé. Quelques centimètres sont insérés dans le canal cholédoque, depuis la papille duodénale majeure, et son trajet au sein du canal cholédoque est alors vérifié. Un rinçage des voies biliaires peut être effectué au besoin. Une fois à la bonne longueur dans le canal cholédoque, la sonde d'alimentation est coupée afin de laisser 3 – 5 cm libres dans la lumière duodénale. Cette portion de stent est ensuite suturée à la lumière duodénale à l'aide de 2 à 3 points pris dans la paroi duodénale au monofilament résorbable décimale 1,5 ou 2. Par la suite, le stent sera naturellement éliminé par les selles une fois ces fils de maintien résorbés.
Conclusion
Les affections hépato-biliaires félines nécessitent une prise en charge médico-chirurgicale raisonnée et coordonnée, afin d'augmenter les chances de survie de ces patients.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Pathologie prostatique : médecine ou chirurgie, faisons le lien !
Gentilly, France
Gentilly, France
I. Hyperplasie bénigne de la prostate
L'Hyperplasie Bénigne de la Prostate (HBP) affecte plus de 80% des chiens mâles entiers de plus de 5 ans ou 95% des chiens de plus de 9 ans. Le processus peut se mettre en place dès l'âge de 2 ans. C'est une affection hormono-dépendante physiologique (hyperplasie des cellules épithéliales et stromale, sous effet de la testostérone convertie en DHT par l'enzyme 5-alpha-réductase). La majorité des chiens atteints d'HBP sont asymptomatiques. Des signes de syndrome prostatique peuvent être présents (ténesme, constipation, selles aplaties, dysurie, hématurie intermictionnelle ou en fin de miction). Le diagnostic de l'HBP repose sur une combinaison de l'anamnèse, de l'examen clinique et des examens complémentaires (notamment échographie abdominale). Le toucher rectal est fondamental et permet de palper la prostate : elle est généralement symétrique, non douloureuse, de taille augmentée et de consistance ferme mais non dure.
Le marqueur sanguin CPSE (canine prostatic spécific arginine esterase), une protéique sérique, peut être utilisé comme aide diagnostique. Une valeur élevée peut être associée à une HBP (Sensibilité de 95,6%, spécificité de 89,2% pour un cut off de 52,3 ng/ml, étude réalisée sur 19 chiens asymptomatiques)[1].
La castration chirurgicale est le traitement de choix et le plus efficace (atrophie rapide de la prostate, avec une réduction de taille de 50% en trois semaines et de 70% en neuf semaines). Des traitements médicaux sont également disponibles (Tableau 1). Le pronostic est excellent.
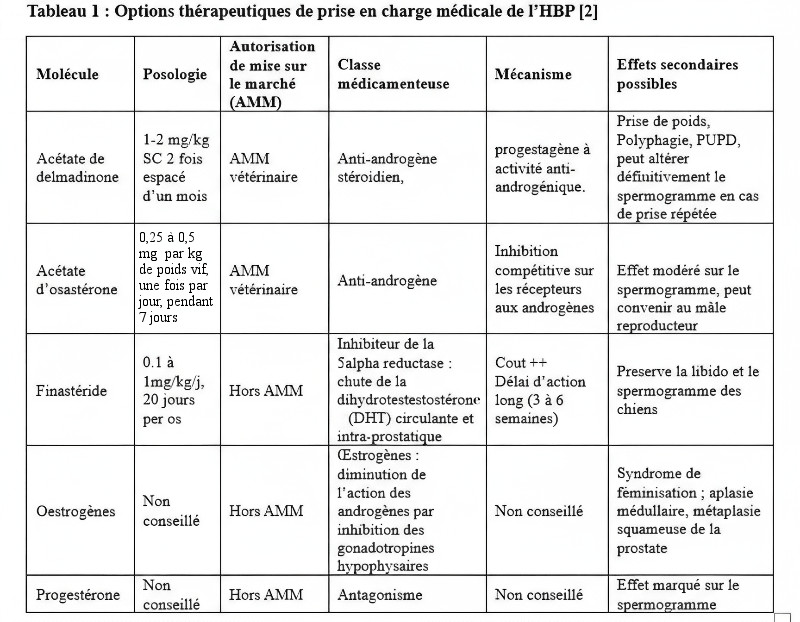
Tableau 1
II. Kystes prostatiques et paraprostatiques
Les kystes prostatiques sont des lésions cavitaires au contenu liquidien, délimitées par une paroi et situées au sein du parenchyme prostatique. Les kystes paraprostatiques sont des structures kystiques adjacentes à la prostate. Les premiers sont associés à l'HBP et issus d'une dilatation des acini ou de compression des canaux excréteurs. Les derniers sont souvent plus volumineux et cranio-latéraux à la prostate. Les signes cliniques associés aux kystes dépendent de leur taille, de leur emplacement et de l'éventuelle présence d'une complication, notamment une infection. La fièvre n'est pas présente. L'imagerie échographique et l'analyse du liquide kystique, obtenue par ponction échoguidée, sont utiles pour confirmer la nature kystique de la lésion via un prélèvement. Le traitement des kystes varie en fonction de leur taille, de leur nature (kyste simple ou compliqué) et de leur localisation. Pour les kystes prostatiques (intraparenchymateux), la castration peut entraîner une diminution significative de la taille de la prostate et des kystes associés à l'HBP. Une ponction échoguidée et un drainage de la cavité peuvent soulager temporairement les symptômes, mais la récidive est fréquente si la cause sous-jacente n'est pas traitée. Pour les kystes récidivants ou de grande taille, une marsupialisation (ouverture du kyste et suture de ses bords à la paroi abdominale pour un drainage continu) ou l'omentalisation (introduction d'un lambeau d'omentum dans la cavité kystique pour favoriser la résorption) peut être nécessaire. Pour les kystes paraprostatiques, l'exérèse chirurgicale complète est conseillé. Cette intervention peut être complexe, en raison de la taille des kystes et de leur adhérence aux structures environnantes. La castration doit être associée. Le pronostic après un traitement chirurgical approprié est généralement bon.
III. Prostatite et abcès prostatique
1. Étiologie et signes cliniques
La prostate peut être le siège d'une infection bactérienne aiguë ou chronique : on parle alors de prostatite. Un abcès prostatique est souvent secondaire à une infection bactérienne ascendante des voies urinaires ou à l'infection d'un kyste prostatique préexistant. Les bactéries les plus fréquemment isolées sont Escherichia coli (germe le plus souvent rencontré), Proteus spp., Klebsiella spp., Staphylococcus spp., Streptococcus spp., Pseudomonas sp. Les signes cliniques d'un abcès prostatique sont souvent aigus et sévères, reflétant un état septique (anorexie, déshydratation, fièvre, voire un état de choc septique).
2. Moyens diagnostiques
La démarche est similaire aux autres atteintes prostatiques. À l'échographie, l'abcès apparaît comme une structure hypoéchogène ou anéchogène, souvent irrégulière, avec des parois épaissies et un contenu hétérogène (contenant parfois des débris ou du gaz). En plus des anomalies classiques hémato-biochimiques, une augmentation de la protéine-C réactive peut aussi être recherchée. Enfin, l'analyse d'un prélèvement urinaire, ou idéalement prostatique, notamment avec une culture bactérienne, sont indispensables pour identifier l'agent pathogène et déterminer sa sensibilité aux antibiotiques.
3. Traitement
a) Traitement médical
Le traitement des prostatites aiguës est multimodal : il inclut une stabilisation médicale initiale, si nécessaire, et une antibiothérapie à large spectre par voie intraveineuse, une analgésie efficace et la castration, au moins médicale.
L'antibiotique doit être liposoluble, faiblement liés aux protéines plasmatiques avec une pharmacocinétique compatible (pKa élevé). Le sulfamide-triméthoprime et les fluoroquinolones correspondent à ces critères. Lors de prostatite aiguë néanmoins, l'inflammation favorise la pénétration des antibiotiques, rendant utilisables les classes des béta-lactamines et des céphalosporines. La durée de l'antibiothérapie est souvent longue.
b) Traitement chirurgical
Les abcès représentent une urgence médico-chirurgicale. Après stabilisation médicale, l'omentalisation de la cavité abcédée doit être envisagée. Dans des cas bien circonscrits, une lobectomie prostatique partielle peut être envisagée. La marsupialisation est déconseillée, en raison d'un fort risque de fistules chroniques. Une castration doit être associée.
4. Pronostic et risque de récidive
Le pronostic est réservé à sombre en l'absence de traitement, compte tenu du risque de péritonite septique et de choc. Il est bon en cas de prise en charge précoce. La récidive est rare après une castration et un drainage chirurgical efficace, associé à une antibiothérapie prolongée.
IV. Tumeurs prostatiques
1. Étiologie et signes cliniques
L'adénocarcinome, tumeur non hormono-dépendante, est le type de tumeur prostatique le plus fréquent chez le chien, souvent âgé, représentant entre 70 et 80% des cas. D'autres types incluent le carcinome à cellules transitionnelles, le léiomyosarcome et les fibrosarcomes. L'étiologie exacte demeure inconnue, mais des facteurs génétiques et environnementaux sont suspectés. La castration n'est pas protectrice. Les signes cliniques sont souvent insidieux initialement et peuvent générer un syndrome prostatique. Une douleur dorsolombaire en cas d'invasion osseuse est possible. Des signes de métastases plus éloignées peuvent se manifester (détresse respiratoire, adénopathie, …).
2. Moyens diagnostiques
Le diagnostic des tumeurs prostatiques requiert une approche multimodale (clinique et paraclinique), le diagnostic demeurant cytologique ou histologique. De nombreuses tumeurs prostatiques présentent la mutation génétique BRAF V600E chez l'homme. Cette mutation (BRAFV595E) a aussi été découverte chez le chien en 2015 : elle peut être recherchée chez le chien sur un liquide biologique (urine, autre) ou les tissus. Ce marqueur semble être très spécifique. Il peut être positif lors de carcinomes urothéliaux vésicaux ou prostatiques .
L'échographie abdominale est indispensable ; on observe une prostate hétérogène, avec des zones hypoéchogènes ou hyperéchogènes irrégulières, des calcifications intraparenchymateuses, une perte de symétrie, et parfois une extension aux tissus environnants (vessie, rectum). L'échographie permet également de rechercher des adénomégalies locorégionales. La radiographie abdominale (ostéolyse ou ostéosclérose du bassin ou des vertèbres lombaires) et thoracique (recherche de nodules pulmonaires) sont utiles, même si le scanner est plus précis.
3. Traitement
a) Traitement chirurgical
Les tumeurs prostatiques ne sont généralement pas curables par chirurgie, sauf en cas de rares tumeurs localisées, où une prostatectomie totale peut être envisagée : cette intervention est grevée de complications fréquentes (incontinence urinaire postopératoire dans plus de 40% des cas). En présence d'obstruction urinaire sévère, des interventions palliatives comme la cystostomie peuvent être proposées.
b) Traitement par radiologie interventionnelle
L'embolisation artérielle prostatique (PAE – Prostatic Artery Embolization), et sa variante chimiothérapique (PACE – Prostatic Artery Chemoembolization), sont des techniques interventionnelles émergentes. Ces approches mini-invasives visent à réduire la vascularisation tumorale, induire une nécrose du tissu néoplasique et donc une baisse du volume prostatique, et ainsi améliorer les symptômes cliniques (strangurie, douleur).
L'embolisation prostatique apparaît comme une alternative mini-invasive prometteuse, à ne pas envisager sans prévention des métastases, principale cause de décès. Elle permet une amélioration rapide des symptômes, une réduction du volume tumoral et une bonne tolérance. En particulier, la technique de chimioembolisation pourrait permettre d'intensifier l'effet antitumoral local tout en limitant la toxicité systémique. À l'heure actuelle, la PAE et la PACE ne doivent pas être envisagées comme des traitements curatifs.
c) Traitement palliatif
La chimiothérapie a montré une efficacité limitée pour les adénocarcinomes prostatiques, avec des réponses souvent partielles et transitoires avec des agents comme la mitoxantrone, le carboplatine et le piroxicam (AINS ayant montré une certaine efficacité dans le contrôle de la douleur grâce à ses effets antiprolifératifs et anti-inflammatoires). La radiothérapie peut être utilisée de manière palliative pour soulager la douleur ou l'obstruction, mais son accès est limité et les effets secondaires peuvent être significatifs. La pose d'un stent urétral, par endoscopie, est une option palliative de la gêne fonctionnelle urinaire. Enfin, la castration n'a aucun effet sur la croissance des tumeurs prostatiques malignes, non hormono-dépendantes.
4. Pronostic et risque de récidive
Le pronostic des tumeurs prostatiques, en particulier de l'adénocarcinome, est sombre. Le temps de survie médian après le diagnostic est généralement inférieur à 1 an, souvent entre 3 et 6 mois du fait des métastases au diagnostic. La récidive est très élevée, la chirurgie étant rarement curative et la chimiothérapie d'une efficacité limitée.
Bibliographie
- ALONGE et coll. Advances in prostatic diagnostics in dogs: the role of canine prostatitc specific esterase in the early diagnosis of prostatic disorders. Topics in Companion Animal Medicine 33(4), 2018, 105-108
- JOHNSTON, S. D. et coll. Prostatic disorders in the dog. Veterinary Clinics of North America: Small Animal Practic, 2000, 30(3), 543-562.
- AESCHLIMANN et coll. Effective detection of BRAFV595E mutation in canine urothelial and prostate carcinomas using immunochemistry, Vet Comp Oncol 2024 22(2), 295-302).
- CULP WTN et coll. Prostatic artery embolization for management of prostatic carcinoma in dogs. J Am Vet Med Assoc, 2021; 259(10):1154-1162.
- PELLERIN O et coll. Prostate artery chemoembolization with docetaxel in canine prostatic carcinoma: feasibility and tolerance study. Diagn Interv Imaging, 2021;102(12):709-715.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Performances diagnostiques de l'examen échographique dans la détection de la plaque de Randall dans l'espèce féline
Zachary PREVOST
Co-auteurs :
Christelle MAUREY,
Morgane PERTUIS,
Marine LE DUDAL
I. Introduction
La plaque de Randall est un dépôt phospho-calcique localisé sur la membrane basale de la papille urinaire jouant un rôle crucial dans la formation de néphrolithes de nature oxalo-calcique chez l'homme. Récemment décrites chez le chat à l'examen nécropsique, sa détection du vivant de l'animal avant la formation des calculs pourrait s'avérer intéressante dans la prise en charge des patients lithiasiques oxalo-calciques.
II. Objectif
Évaluer la pertinence de l'examen échographique pour la détection des plaques de Randall chez le chat.
III. Matériels et méthodes
Étude prospective portant sur 37 chats ayant reçu un examen échographique a minima urogénital par le service d'imagerie Centre Hospitalier Universitaire des Animaux de compagnie (CHUVAC) de l'École nationale vétérinaire d'Alfort (ENVA), dans un délai maximal de 2 mois avant leur décès, et pour lesquels un examen nécropsique a été réalisé a posteriori par le service d'anatomopathologie de l'ENVA. La suspicion de présence ou d'absence d'une plaque de Randall était confrontée aux résultats de l'examen histologique post-mortem.
IV. Résultats
Sur les 37 chats de l'étude, 21 présentaient une suspicion de plaque de Randall à l'examen échographique. Parmi eux, 18 (86%) présentaient effectivement une plaque de Randall à l'examen histologique post-mortem. En incluant tous les résultats, l'examen échographique présentaient une sensibilité de 86%, une spécificité de 80%, une valeur prédictive positive de 86%, et une valeur prédictive négative de 80%, pour la détection d'une plaque de Randall chez le chat.
V. Discussion
Les services d'imagerie et d'anatomopathologie de l'ENVA étaient indépendants et n'avaient pas connaissance de leurs résultats mutuels, mais il apparaitrait important de faire relire les images a posteriori par un même imageur indépendant. Par ailleurs, même si nos résultats à l'examen histologique s'appuient sur des critères publiés en médecine humaine, la distinction avec des lésions de néphrocalcinose au sens général peut poser question. Des études récentes se sont penchées sur les méthodes de détection de la néphrocalcinose chez le chat atteint de maladie rénale chronique (TANG et al. 2022, 2024). Toutefois, les chats présentant des néphrolithes étaient exclus de ces travaux, et les critères histologiques retenus étaient différents des nôtres. Néanmoins, le fait que les dépôts de néphrocalcinose soient composés majoritairement d'apatite semble montrer qu'il pourrait exister un continuum physiopathologique entre les deux entités.
VI. Conclusion
L'échographie apparaît comme un outil prometteur pour la détection des plaques de Randall chez le chat. Ses performances diagnostiques dans l'étude sont intéressantes, avec une sensibilité de 86% et une spécificité de 80%. Une meilleure caractérisation échographique pourrait permettre d'optimiser le suivi des patients à risque de lithiase urinaire oxalique.
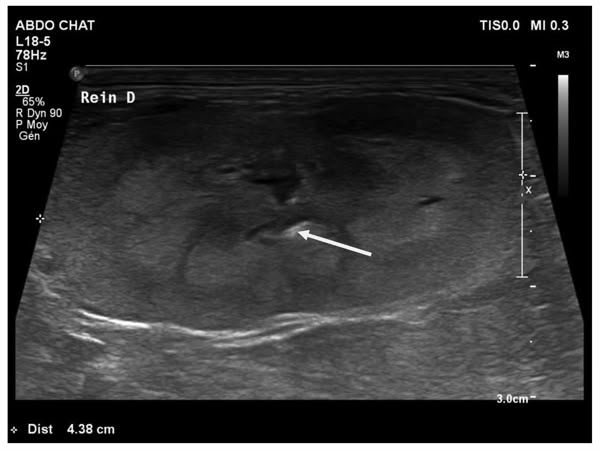
Figure 1
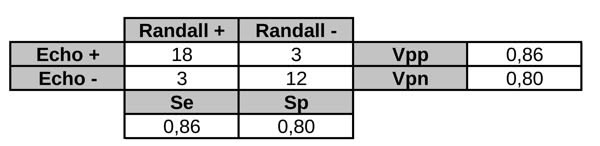
Figure 2
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 POCUS thorax insuffisance cardiaque
Guyancourt, France
I. Introduction
Les techniques d'échographie au chevet du patient POCUS (Point-Of-Care UltraSound) sont en plein essor depuis quelques années et ont permis d'améliorer la qualité et la rapidité du diagnostic à l'admission des patients les plus critiques et à traquer les complications au cours de leur hospitalisation. Ces techniques échographiques présentent de nombreux avantages et ne nécessitent pas de qualifications particulièrement poussées dans ce domaine de l'imagerie médicale, ni d'une machine sophistiquée. Il s'agit de techniques non invasives, non irradiantes, dont le rôle est d'être utilisée au chevet de l'animal, lors de l'admission, mais également lors du suivi en hospitalisation. De plus, ces examens peuvent être réalisés sans tondre le pelage, en imbibant simplement d'alcool l'interface sonde/peau. L'animal peut être placé selon sa position lors de son admission. Une sonde microconvexe est utilisée.
II. Réalisation de la POCUS thoracique
Plusieurs protocoles POCUS thoraciques ont été décrits :
- TFAST3 (Thoracic Focused Assessment with Sonography for Trauma, Triage, and Tracking – évaluation échographique thoracique ciblée pour le traumatisme, le triage et le suivi)
- Vet BLUE (Veterinary Bedside Lung Ultrasound Exam – examen échographique des poumons au chevet de l'animal)
- VetFAST-ABCDE (Veterinary-Focused Assessment with Sonography for Trauma-Airway, Breathing, Circulation, Disability and Exposure - évaluation échographique ciblée pour les fonctions vitales ABCDE)
Ces techniques POCUS se basent sur différentes fenêtres acoustiques mais les réponses apportées sont les mêmes et répondent à des questions binaires (algorithme de la Figure 1 et 2).
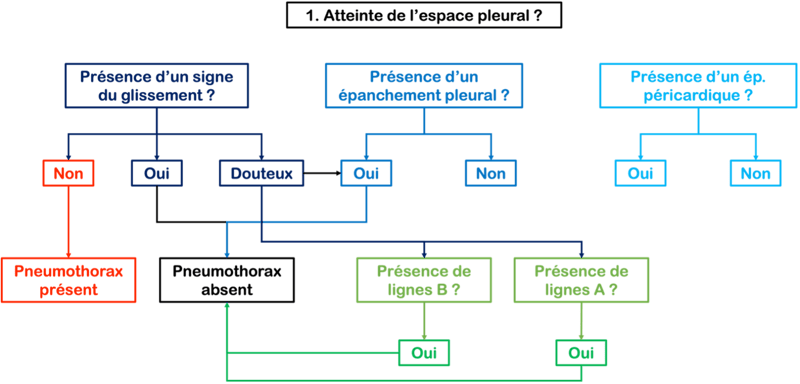
Figure 1
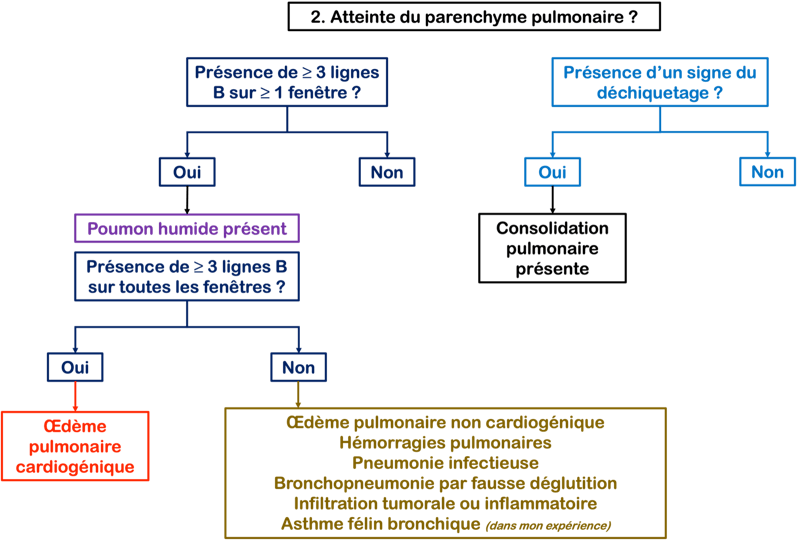
Figure 2
Historiquement, le premier protocole POCUS thoracique détaillé est la procédure TFAST. L'animal est placé en décubitus latéral ou sternal et 5 zones sont étudiées :
- Entre le 7è et le 8è espace intercostal à droite et à gauche : fenêtre CTS (Chest Tube Site) : la sonde est placée perpendiculairement à la paroi thoracique et reste immobile.
- Au niveau du choc précordial à droite et à gauche : fenêtre PCS (PeriCardial Site) : permet d'évaluer la présence ou l'absence d'un épanchement péricardique
- En arrière du processus xiphoïde : fenêtre DH (diaphragmatico-hépatique) : c'est la même zone que pour la POCUS abdominale mais le clinicien va balayer plus en avant du diaphragme afin d'explorer l'espace pleural et éventuellement la zone péricardique.
III. Signes échographiques recherchés lors d'insuffisance cardiaque congestive
Pendant très longtemps, le diagnostic de l'OAP reposait sur l'interprétation des radiographies thoraciques. Actuellement, il est déconseillé de réaliser cet examen irradiant chez un animal dyspnéique en raison de la décompensation mortelle que la procédure peut entraîner. Cette modalité diagnostique a été, en urgence, complètement remplacée par les techniques POCUS (Point-Of-Care Ultrasound – échographie au chevet de l'animal) thoraciques. L'auteur de ce chapitre ne diagnostique les OAP que sur la base seule de cette modalité (évidemment dans un contexte clinique évocateur) depuis près de 10 ans.
1. Signes échographiques recherchés : les lignes B chez le chien et le chat
Lorsque les alvéoles les plus superficiels sont emplis de liquide (quelle que soit la nature du liquide) et ne sont donc plus aérés, des artefacts échographiques vont apparaître (changement d'interface pour les ultrasons). Il s'agit des lignes B qui se manifestent sous la forme d'un triangle fin hyperéchogène dont la pointe prend naissance au niveau de la plèvre et dont la base est en profondeur (Figure 1). Il peut être physiologiquement normal d'observer 1 à 3 lignes B par fenêtre acoustique chez un animal sain. Au-delà de 3 lignes B, cette observation est considérée comme pathologique. Lorsque les lignes B sont trop nombreuses pour être comptées, elles sont qualifiées de coalescentes.
2. L'épanchement pleural et péricardique chez le chat
À l'échographie, un épanchement pleural se traduit par une zone anéchogène entre la paroi thoracique et le poumon, qui apparaît rétracté et flottant dans le liquide, avec perte du contact pleural et parfois un mouvement oscillant ("jellyfish sign"). Le liquide est généralement anéchogène (transsudat), mais peut contenir des particules échogènes. En cas de volume important, les lobes pulmonaires sont atélectasiés, triangulaires et échogènes, entourés par le liquide.
Un épanchement péricardique apparaît comme une zone anéchogène entourant le cœur et séparant le péricarde du myocarde, souvent plus marquée en région dorsale. Le liquide est habituellement homogène mais peut contenir des fibrilles ou particules échogènes (sang, exsudat). Lorsque le volume est important, on observe une compression des cavités cardiaques droites (collapsus auriculaire/ventriculaire) et une variation paradoxale du remplissage évocatrice de tamponnade, ce qui est rarissime selon mon expérience lors d'épanchement péricardique d'origine cardiogénique chez le chat.
3. Le décompte des lignes B pour le diagnostic initial
Comme écrit précédemment, chez un animal sain, l'observation de quelques lignes B (moins de 3 par fenêtre acoustique) est possible, mais leur présence devient systématique lors d'OAP. Les études rapportent une fréquence globale des lignes B de 11 à 31% chez les chiens sains et 12% chez les chats sains contre 100% chez les chiens et chats ayant un OAP. Chez le chien et chez le chat, l'OAP est la condition médicale qui s'accompagne du plus grand nombre (soit nombre total, soit nombre par fenêtre échographique) de lignes B (les autres maladies servant de comparaison sont les pneumonies infectieuses et les cancers pulmonaires).
De nombreuses études chez le chien ont déterminé la sensibilité et la spécificité des techniques POCUS thoraciques dans le diagnostic de l'OAP cardiogénique en se basant sur différents critères :
- La présence d'au moins 4 lignes B sur une seule fenêtre péricardique a une sensibilité de 91% et une spécificité de 100% pour diagnostiquer un OAP ;
- L'observation d'au moins 10 lignes B au total, dont 2 fenêtres échographiques avec au moins 3 lignes B chacune, a une sensibilité de 92% et une spécificité de 94% pour identifier un OAP ;
- La mise en évidence d'au moins 3 lignes B par hémithorax a une sensibilité de 90% et une spécificité de 93% pour le diagnostic de l'OAP chez des chiens souffrant de différents stades de maladie valvulaire dégénérative mitrale.
Une autre étude chez le chien atteint d'OAP rapporte que le nombre de fenêtres acoustiques ayant plus de 3 lignes B est corrélé positivement à la fréquence respiratoire.
Chez le chat, une étude rapporte la présence systématique de plus de 3 lignes B sur toutes les fenêtres échographiques.
Notons enfin que le décompte des lignes B n'est pas modifié par le choix de la sonde échographique (microconvexe ou linéaire) chez le chien comme chez le chat.
4. Le décompte des lignes B pour le suivi
De manière corollaire, le traitement efficace de l'OAP va s'associer à une diminution progressive du nombre de lignes B. Cette diminution apparaît plus précoce et plus importante que l'amélioration des lésions radiographiques thoraciques (80% de diminution du nombre de lignes B contre 26% de réduction du score de lésions radiographiques).
Bibliographie
Références sur demande
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Ponction échoguidée de masse cardiaque chez le chien : série de 12 cas
Yassine BEN ABDENNEBI
Introduction
Les 2 types de tumeurs cardiaques les plus fréquents sont l'hémangiosarcome (HSA) et le chémodectome (CD).
L'HSA, au comportement agressif, est souvent associé à une espérance de vie courte, de quelques semaines. Le CD, quant à lui, présente un comportement plus lent, se développant sur plusieurs mois à années.
Cet écart de pronostic impose au clinicien d'annoncer le bon diagnostic au moment de la mise en évidence de la tumeur.
Longtemps, les données anamnestiques, la localisation de la masse ainsi que son aspect faisaient foi pour classer la tumeur dans telle ou telle catégorie.
Une étude de 2013 a comparé l'examen histologique post mortem des masses cardiaques à leur suspicion échographique. Les CD sont reconnus et classés correctement dans plus de 75 % des cas. Les masses classées comme HSA à l'échographie étaient d'un autre type tumoral dans près de 50 % des cas. Près d'un chien sur 2 aurait alors peut-être été condamné à tort par un diagnostic échographique erroné.
Dans ce contexte, le recours à la ponction échoguidée pour analyse cytologique prend tout son sens.
Une étude de 2016 menée sur 6 chiens a démontré la faisabilité de la technique et un faible de taux de complication.
- Enjeux de l'étude :
- Confirmer la faisabilité technique des ponctions échoguidées de masse cardiaque chez le chien ;
- Vérifier le taux faible de complications ;
- Explorer son intérêt diagnostique.
Matériel et méthode
12 chiens ont été présentés dans un contexte d'hémopéricarde, de syncope, de bilan d'extension de masse splénique ou pour l'exploration d'un souffle cardiaque ou de toux. Une masse cardiaque a été mise en évidence.
Si celle-ci était proche de la paroi costale et peu mobile, une ponction échoguidée a été réalisée. Les chiens ont été sédatés et monitorés (ECG). Une aiguille a été insérée sous contrôle échographique au sein de la masse. La procédure a été répétée 3 fois pour chaque patient. Les lames obtenues ont été relues par un spécialiste.
Résultats
10 chiens présentaient une masse de la paroi du cœur droit (oreillette, auricule, jonction atrioventriculaire) et étaient suspects d'HSA, 1 chien présentait une masse d'apparence myocardique au sein de la chambre de chasse du ventricule droit et était suspect de rhabdomyosarcome, 1 chien présentait une masse en étroit contact avec l'auricule droite, le corps de l'oreillette droite et la base du cœur et était suspect de masse de la base du cœur (CD ou carcinome thyroïdien ectopique en priorité).
Les ponctions ont été diagnostiques pour 9/12 (75 %), 4/6 pour les 6 premiers, 5/6 pour les 6 derniers.
Les diagnostics ont été les suivants : HSA (5/12), sarcome (2/12), CD (1/12), tumeur musculaire (1/12).
La corrélation entre le diagnostic cytologique et la supposition échographique a été de 100 %, si l'on considère que le diagnostic cytologique de sarcome concorde avec la suspicion échographique d'HSA.
Aucun patient n'a subi de troubles du rythme pendant la procédure.
Aucun patient n'est décédé pendant la procédure.
1 patient a présenté un hémopéricarde récidivant le lendemain.
Discussion
La cohorte est représentée essentiellement par des suspicions échographiques d'HSA. Cette surreprésentativité est cohérente, puisque c'est cette population qui était classée à tort selon les études précédentes. L'examen cytologique a donc été proposé plus facilement sur ces types tumoraux. De plus, l'accessibilité échographique de l'oreillette droite est supérieure à celle de la base du cœur.
Les lames obtenues ont permis l'obtention d'un diagnostic dans une majorité de cas. Les résultats montrent que la probabilité de réponse augmente avec l'expérience de l'opérateur.
Dans notre cohorte, l'échographie cardiaque présente une valeur prédictive élevée. La distinction entre sarcome et HSA n'est pas toujours claire. Néanmoins, il est très probable que les cas diagnostiqués sarcome sont réellement des HSA, la proportion d'autres sarcomes affectant le cœur étant très faible (chondrosarcome dans 1 cas sur 24 lors de nécropsie).
La procédure présente un faible taux de complications et confirme sa faisabilité. Un seul animal a présenté une récidive de son hémopéricarde. Il est néanmoins judicieux de se demander si la récidive à 24 heures est réellement due à la ponction échoguidée ou à la récidive de l'hémopéricarde, possible à court terme même en l'absence de ponction.
L'absence de troubles du rythme, pourtant attendus, se justifie probablement par l'absence de tissu conductif au sein des tumeurs ponctionnées.
Conclusion
La ponction échoguidée des tumeurs cardiaques est réalisable, peu dangereuse pour un opérateur entraîné, et permet l'obtention d'un diagnostic dans une majorité de cas. Elle peut donc être proposée aux propriétaires dans l'exploration des tumeurs cardiaques afin d'affiner le diagnostic, de préciser le pronostic et d'adapter au mieux le traitement.
Limite de l'étude
Comme pour toutes les études sur les tumeurs cardiaques, la cohorte n'est pas volumineuse, même si celle-ci est supérieure aux études précédentes.
L'examen cytologique donne des résultats limités. En effet, la distinction entre les différents tissus neuro-endocrines est difficile. Différencier CD et carcinome thyroïdien ectopique est donc chose ardue. De même, la distinction entre sarcome et HSA n'est pas toujours réalisée.
Le recours à un diagnostic définitif histologique post mortem aurait été idéal.
Il n'a été possible chez aucun des patients de la cohorte.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Ponction épanchement péricardique
Montpellier, France
I. Introduction
L'épanchement péricardique est l'accumulation anormale de liquide dans le sac péricardique, le sac qui renferme le cœur et les racines des gros vaisseaux.
1. Présentation clinique
Présente sous deux formes chez le chien :
- Épanchement aigu = accumulation rapide, avec compression diastolique du cœur droit, due à une augmentation de la pression dans le sac péricardique, qui devient supérieure à celle du cœur droit qui est la partie basse pression du cœur : se développe alors la tamponnade cardiaque, entraînant une diminution du remplissage et par conséquent une diminution du débit cardiaque et de la pression artérielle (choc obstructif et hypovolémique).
- Épanchement chronique, avec augmentation compensatoire de l'eau corporelle totale possible. Lors de l’accumulation chronique, il est plus rare d’avoir une tamponnade car le sac péricardique peut avoir le temps de se distendre et de ralentir l’augmentation de la pression intrapéricardique.
La conséquence du dysfonctionnement du cœur droit entraine une congestion en amont et en donc une accumulation de fluide dans la cavité abdominale (ascite).
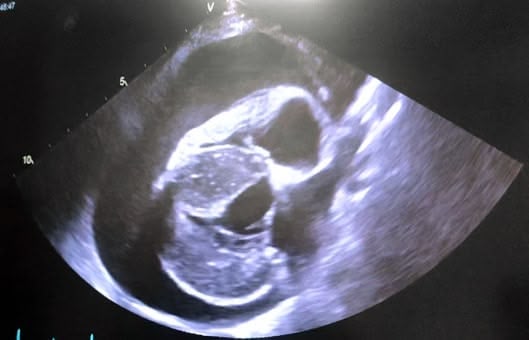
Figure 1
2. Étiologies
Les causes courantes chez le chien sont : la péricardite idiopathique, l'hémangiosarcome puis viennent plus rarement la tumeur de la base du cœur (chémodéctome), l’intoxication aux anticoagulants, rupture atrial, cause septique (corps étranger).
Le chat aussi peut souffrir d’épanchement péricardique même si cela est bien moins courant.
Les causes chez le chat sont : néoplasie (lymphome), infectieux (PIF), cardiaque.
3. Signes cliniques
L'apparence clinique et le signalement sont similaires à ceux des patients atteints d'hémoabdomen dans de nombreux cas (choc hypovolémique/obstructif). Envisagez-le sur tout chien ayant des antécédents de collapsus aigu ou sur tout chien présentant des muqueuses pâles, une tachycardie, un TRC augmenté, des extrémités pâles, un abattement, bref, les signes cliniques d’hypovolémie.
Le temps de prothrombine peut être réalisé avant la ponction pour exclure la possible cause des rodenticides. Le diagnostic échocardiographique d'une tumeur cardiaque provoquant un épanchement péricardique est pratiquement impossible sans l'épanchement. Il faut donc considérer les conséquences d'un drainage sans écho de l'épanchement, mais aussi les frais d'attente.
4. Pronostic
Le pronostic dépend de la cause. L'épanchement idiopathique se reproduira dans environ 50 % des cas, mais peut être géré avec succès dans la plupart des cas. Le pronostic avec HSA est mauvais à grave. Les tumeurs de la base du cœur se développent lentement. Des péricardiocentèses répétées peuvent être réalisées. Une péricardectomie peut également être indiquée.
5. Traitement initial
- Oxygénothérapie (flow-by, masque nasal, cage à oxygène, intubation)
- Fluide bolus : 10-20 ml/kg bolus de cristalloïdes avant la péricardiocentèse + réévaluation de la volémie pour améliorer la perfusion vasculaire. Des volumes plus importants peuvent être nécessaires.
- Les diurétiques ne sont pas indiqués pour les épanchements aigus et aggravent les choses en diminuant le débit cardiaque
7. Tests diagnostiques
- Échocardiogramme - test de choix pour la confirmation de l'épanchement
- Une masse, si elle est présente, peut souvent être identifiée par un échocardiogramme. Cependant, trouver et identifier l'emplacement correct dépend de la compétence de l'échographiste.
- La plupart des hémangiosarcomes sont situés sur l'oreillette droite, dans le sillon AV droit ou à l'intérieur de l'oreillette droite.
- La plupart des tumeurs de la base du cœur sont situées entre l'aorte et l'artère pulmonaire principale, mais elles peuvent grossir et donc sembler provenir d'autres localisations.
- L'absence de masse visible ne l'exclut pas.
- Électrocardiographie (ECG)
- Arythmies ventriculaires possibles
- Complexes QRS réduits en taille (souvent <1 mV en amplitude chez le chien)
- Alternance électrique (variation de la taille du QRS due au mouvement cardiaque)
- Radiographie thoracique — Évitez le stress !
- V/D doit être évité. Le D/V peut minimiser le stress
- Silhouette cardiaque globoïde. Peut être absent pour les cas aigus
- Veine cave caudale distendue due à des pressions diastoliques auriculaires/ventriculaires droites élevées
- Mauvais détail abdominal si présence d'une ascite
8. Équipement
Équipement pour la procédure (figure 2)
- Tondeuses/scrub/champ chirurgical/gants stériles
- Seringue 20-60 cc
- Cathéter de 14-20 Ga ou angiocathéter ou épicranienne ou kit de péricardiocentese dépendant la taille de l’animal et du matériel à disposition
- Robinet 3 voies et lignes d'extension
- Récipient de collecte
- Tube violet et rouge pour le prélèvement des échantillons
Figure 2
9. Procédure
- La sédation peut être utile en utilisant des sédatifs épargnant le système cardiovasculaire tels que les narcotiques et les benzodiazépines (évitez l'acépromazine et les agonistes alpha-2).
- Décubitus sternal ou latéral
- Un bloc local de lidocaïne peut aider avant l'insertion du cathéter. Assurez-vous d'essayer d'anesthésier la plèvre.
- Faire une petite entaille dans la peau pour faciliter l'insertion.
- ECG et/ou écho-surveillance pendant la procédure
- La ponction doit être effectuée sur le côté droit.
- Préparation chirurgicale entre les 2e et 8e côtes ; jonction sternum-costochondrale
- Le battement d'apex du cœur est palpé (entre les 4e et 5e côtes juste au-dessus de la jonction costochondrale) ou un guidage échographique peut être utilisé.
- Le cathéter est inséré et avancé du bord crânien de la côte à l'emplacement du battement de l'apex.
- Une fois que le cathéter/stylet est dans la cavité thoracique, il est avancé lentement jusqu'à ce qu'il y ait un « flash » de liquide dans l'embase du cathéter. Ne pas retirer du stylet tant que cela n'est pas observé. Si un épanchement pleural est également présent, cela peut compliquer la situation. Un « pop » doux est parfois ressenti lorsque le péricarde est perforé.
- Le cathéter et le stylet sont ensuite avancés ensemble de 2 à 3 mm supplémentaires et le cathéter est ensuite introduit sur le stylet dans le péricarde.
- Le placement peut être confirmé en injectant un petit volume de solution saline agitée à travers le cathéter tout en observant par échographie - s'ils sont correctement situés, des bulles doivent apparaître dans l'espace péricardique.
- Le stylet est ensuite retiré et le système de collecte attaché pour le drainage.
- Après le prélèvement, le liquide est évacué dans le récipient par le robinet 3 voies.
10. Notes IMPORTANTES
- Si le cathéter a été accidentellement avancé dans le ventricule, l'échantillon coagulera : examinez le récipient à la recherche de caillots ou placez une partie du liquide dans un tube sec pour voir s'il coagule.
- Pendant la ponction, si une sensation de "grattage" est ressentie sur le cathéter, cela peut indiquer un contact avec le cœur (des ESV peuvent également être observées à l'ECG). Le cathéter doit être rétracté pour éviter d'endommager le cœur.
- Un échantillon de liquide doit être conservé pour analyse (tube EDTA) et culture, bien que l'analyse du liquide péricardique soit souvent non diagnostique.
- Parfois, le volume collecté est plus petit que prévu. Cela peut se produire si le péricarde se déchire pendant le cathétérisme et que l'épanchement péricardique pénètre dans l'espace pleural. Ce n'est pas un problème.
- La réponse du patient a la procédure est souvent immédiate et très gratifiante : les muqueuses deviennent + roses, la PA et FC s'améliorent, la détresse respiratoire diminue.
11. Suivi
- Considérations post-péricardiocentèse
- Réévaluation fréquente pour rechercher une récidive d'épanchement péricardique
- Diagnostics supplémentaires s'ils n'ont pas déjà été effectués : NFS/biochimie/AU
- Radiographies thoraciques pour rechercher des signes de métastases pulmonaires
12. Pièges
- Réanimation liquidienne inadéquate avant la péricardiocentèse.
- Échec d'identification de la toxicose des rodenticides anticoagulants, en particulier lorsque l'âge / la race ne correspond pas au tableau clinique d'une masse.
- Pneumothorax dû à un traumatisme/une perforation du lobe pulmonaire.
- Tachycardie ventriculaire et arrêt cardiaque : la lidocaïne, l'adrénaline et l'atropine devraient être disponibles avec des doses calculées.
- Lacération de l'artère coronaire.
- Hémorragie continue d'une HSA rompue dans l'espace péricardique ou pleural
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Positionnement en radiographie thoracique
Lyon, France
I. Introduction
La radiographie thoracique est un outil d'imagerie de première intention, indispensable pour l'évaluation des affections cardio-respiratoires. Pour être interprétables et utiles, elles doivent être réalisées dans de bonnes conditions et avec un nombre suffisant de vues. Comme pour tout examen à base de rayons ionisants, la radioprotection doit rester la principale préoccupation.
II. Choix des constantes radiographiques
La radiographie est basée sur l'émission de rayons X générés par un tube à rayons X. Ces rayons X vont interagir avec la matière et donc être atténués. Différents critères, comme l'épaisseur des structures et leur densité, expliquent les différences d'atténuation de ces structures et leur différence d'opacité. C'est cette différence d'atténuation qui permet l'obtention d'un contraste entre les structures radiographiées. Dans le thorax, le contraste est assuré par l'air contenu dans les poumons. Le thorax est donc une région qui a naturellement un bon contraste.
1. Les kV (kilovolts)
Les kV correspondent à l'énergie des rayons X et à la différence de potentiel entre la cathode et l'anode du tube de rayons X. Les kV contrôlent la pénétration des rayons X à travers le corps de l'animal. Des kV élevés entraînent une diminution du contraste et une augmentation du noircissement de l'image. Les kV faibles entraînent une augmentation du contraste et une diminution du noircissement. Dans la mesure où le thorax a naturellement un bon contraste, l'utilisation de kV élevés est privilégiée. Cela permettra également de contrebalancer l'emploi de faibles mAs.
Pour les radiographies thoraciques, des kV relativement élevés sont généralement utilisés pour assurer une bonne pénétration des poumons et du cœur. Les kV utilisés pour une radiographie thoracique chez un chien ou un chat se situent entre 60 et 120 kV, selon la taille et l'épaisseur de l'animal.
2. Les mA (milliampères) et le temps d'exposition
Les mA correspondent à la quantité des rayons X émise par le tube de rayons X. Des mA élevés sont à l'origine d'une augmentation du noircissement de l'image et des mA faibles entraînent une diminution du noircissement.
Le temps d'exposition correspond au temps pendant lequel le patient est exposé aux rayons X. Il a un effet sur la qualité des clichés. Un temps d'exposition élevé entraîne une augmentation du noircissement et une augmentation du flou induit par les mouvements respiratoires ou cardiaques. Un temps d'exposition faible entraine une diminution du noircissement et une diminution du flou.
Les mA et temps d'exposition sont souvent choisis de façon concomitante. Ensemble, ils déterminent la dose totale de rayons X. Des mA plus élevés ou un temps d'exposition plus long augmente la densité de l'image. Pour les radiographies thoraciques, des mAs de 3,2 à 5 sont généralement utilisés et permettent de minimiser le temps d'exposition et le flou dû au mouvement.
3. Synthèse
Lors de la réalisation de radiographies thoraciques, on privilégiera des kV élevés et des mAs faibles, afin d'obtenir une image à faible contraste avec une large gamme de gris et de bien mettre en évidence les détails pulmonaires. Les faibles mAs permettent aussi de limiter le flou cinétique secondaire aux mouvements respiratoires. Seule l'utilisation de ces constantes permet une bonne évaluation du parenchyme pulmonaire et des bronches. L'aspect des bronches ne doit pas être évalué sur les radiographies abdominales (kVp faibles et mAs élevés).
4. Grille
L'utilisation d'une grille permet de limiter la diffusion des rayons X par le patient. Cette diffusion est à l'origine d'une détérioration de la qualité de l'image. Les petits patients entraînant une faible diffusion, la grille n'est utilisée que chez les grands patients. En général, on l'utilise quand l'épaisseur du patient excède 10 cm. Lors d'utilisation de la grille, les mAs doivent être augmentés. On considère qu'il faut les multiplier par 2 ou 3.
III. Radioprotection
La radioprotection du personnel réalisant les radiographies est un élément essentiel. Il prévaut sur tous les autres paramètres et notamment sur le placement du patient. Toute personne amenée à tenir un patient lors de la réalisation de radiographies devra être correctement protégée et porter un dosimètre. Le matériel de protection comprend un tablier de plomb, des gants plombés, un protège thyroïde et des lunettes de protection. Aucune partie du corps humain ne doit se trouver dans le faisceau primaire, et ce même avec des protections plombées. Le manipulateur devra toujours maintenir une distance suffisante avec le faisceau primaire. Dans la mesure du possible, il est préférable d'utiliser des contentions passives (sacs, sangles) mais cela est peu applicable aux radiographies thoraciques dans la mesure où les animaux ne sont en général pas sédatés.
Le faisceau de rayons X doit être réduit au maximum (collimaté). Cela permet de limiter les risques d'exposition des manipulateurs et aussi de limiter la diffusion des rayons X, maximisant ainsi la qualité de l'image.
IV. Technique
1. Positionnement
Le positionnement est crucial pour la bonne interprétation de l'examen. Un examen de mauvaise qualité peut nous amener à manquer des lésions ou à l'inverse à surinterpréter les images et surdiagnostiquer des lésions.
a) Vues latérales
- Décubitus latéral droit ou gauche.
- Membres thoraciques tendus vers l'avant et superposés l'un à l'autre.
- Cou en extension dans l'axe de la colonne.
- Colonne thoracique et sternum parallèles. Des coussins en mousse peuvent être placés sous le sternum des chiens afin de placer la colonne et le sternum à la même hauteur. Chez les chiens brachycéphales, le sternum devra être abaissé.
- Centrage caudalement au bord caudal des scapulas chez le chien et environ 1 cm caudalement aux scapulas chez le chat.
Critères de qualité :
Tout le thorax doit être inclus dans les clichés, que ce soit sur les vues dorso-ventrales ou latérales. Le cliché doit comprendre la partie crâniale du manubrium sternal ainsi que 2 vertèbres caudalement à l'extrémité caudo-dorsale du diaphragme. Les vertèbres et les processus épineux doivent être inclus. Si le patient est trop grand et que le thorax ne peut être inclus en entier dans son axe dorso-ventral, les processus épineux peuvent être coupés. Chez certains très grands patients, il est parfois nécessaire de réaliser les clichés en plusieurs fois.
Les têtes des côtes doivent être superposées. Les clichés doivent être réalisés en fin d'inspiration et le diaphragme doit se superposer à la 12è ou 13è vertèbre thoraciques.
b) Vues dorso-ventrale et ventro-dorsale
Dorso-ventrale :
- Décubitus ventral.
- Superposition de la colonne thoracique et du sternum.
- Cou en flexion dans l'alignement de la colonne.
- Membres thoraciques en extension crâniale.
- Centrage en partie caudale des scapulas, sur la ligne médiane.
- Ouverture du champ jusqu'en partie crâniale des épaules.
Ventro-dorsale :
- Décubitus dorsal.
- Tête en extension dans la continuité de la colonne.
- Membres pelviens placés en extension caudale.
- Membres thoraciques en extension crâniale.
- Centrage sur la ligne médiane en regard du bord caudal des scapulas.
- Ouverture crâniale du diaphragme jusqu'à l'entrée du thorax.
Critères de qualité :
Tout le thorax doit être inclus dans les clichés. La colonne thoracique et le sternum doivent être superposés l'un à l'autre. Les clichés doivent être réalisés en fin d'inspiration et la partie médiane du diaphragme doit être superposée à la 9è ou 10è vertèbre thoraciques.
Chez certains très grands patients, il sera parfois nécessaire de réaliser les clichés en plusieurs fois.
Les structures thoraciques se projettent différemment sur les différentes vues. Ces différences sont résumées dans les Tableaux 1 & 2.
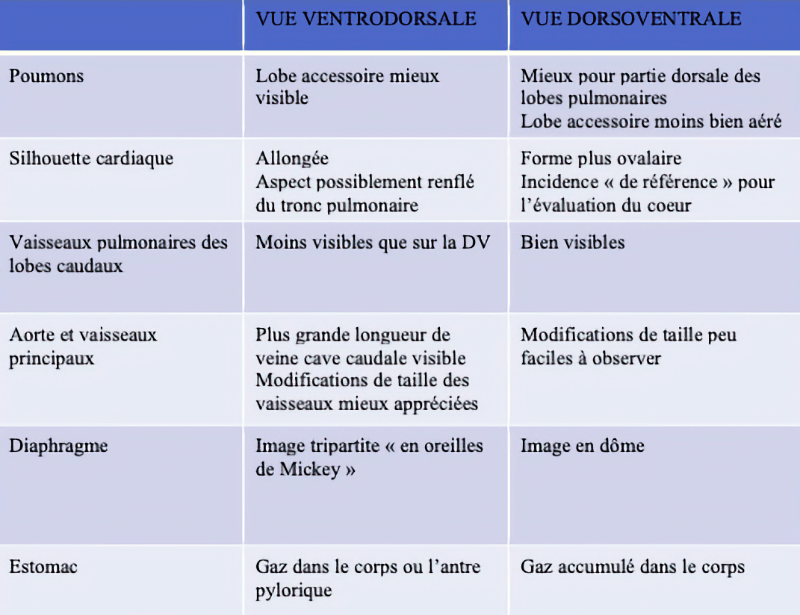
Figure 1
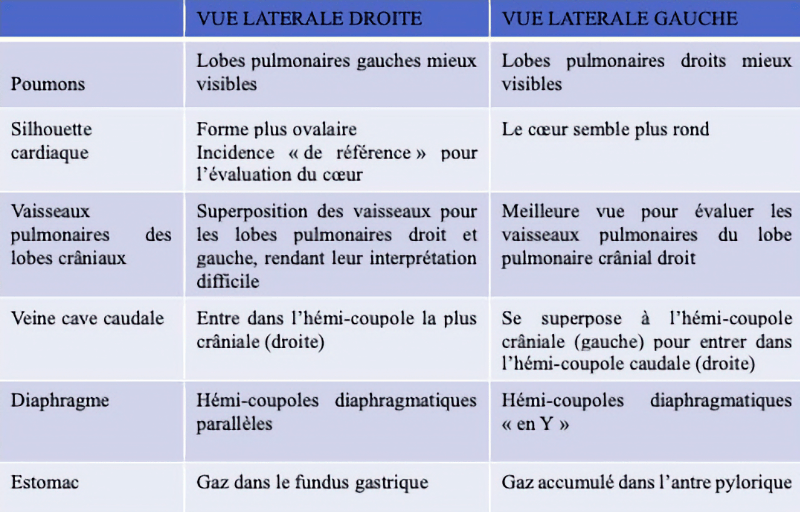
Figure 2
2. Réalisation de l'examen
Il est préférable de réaliser les vues de face en premier afin de limiter l'atélectasie induite par les vues latérales.
Les radiographies doivent être acquises à la fin de l'inspiration afin d'avoir un volume pulmonaire maximal et ainsi un meilleur contraste et limiter l'atélectasie.
Le choix des incidences et le nombre de vues dépendra du motif de la réalisation des clichés.
3. Choix des incidences radiographiques
Un examen radiographique thoracique complet nécessite au minimum deux vues, une vue latérale, souvent une vue de profil droit, et une vue de face, souvent une vue ventro-dorsale. En cas de suspicion d'atteinte trachéale ou laryngée, une vue de profil du cou est nécessaire. Dans un certain nombre de cas, il faudra ajouter une seconde vue latérale du thorax.
Lors de suspicion de collapsus trachéal ou bronchique ou de maladie interstitielle, il est intéressant de réaliser des clichés en phases inspiratoire et expiratoire. De la même façon, la réalisation de clichés en phase expiratoire peut aider à mieux visualiser un pneumothorax.
Lors de suspicion d'atteinte cardiaque, on réalise en général des vues de profil droit et dorso-ventrale.
Sur la vue de profil droit, la forme et la position de la silhouette cardiaque sont plus constantes. La silhouette cardiaque peut avoir un contact plus important avec le sternum. Sur la vue de profil gauche, la silhouette cardiaque est plus ronde et l'apex est légèrement déplacé dorsalement par rapport au sternum.
Sur la vue dorso-ventrale, la position et la forme de la silhouette cardiaque sont plus constantes. La silhouette cardiaque est plus ovale et son apex est davantage latéralisé à gauche par rapport à la vue dorso-ventrale. Sur les vues ventro-dorsales, la silhouette cardiaque est plus allongée et l'apex se projette davantage dans le plan médian. On peut, dans certains cas, voir un bombement sur l'aire de projection du tronc pulmonaire.
Les vaisseaux pulmonaires crâniaux sont mieux visibles sur les vues de profil. Ils sont mieux individualisables et identifiables sur les vues de profil gauche.
4. Évaluation de la qualité de l'image
L'évaluation de la qualité technique de l'étude passe par l'évaluation de différents critères :
- Le nombre de vues disponibles,
- L'adéquation du champ de vue et des constantes utilisées,
- Le positionnement de l'animal,
- La phase de la respiration.
Pour avoir des clichés interprétables, il est essentiel de s'affranchir le plus possible des artéfacts et superpositions.
Si l'état du patient le permet, il est préférable de faire les radiographies avant toute échographie (POCUS ou échographie thoracique). Le gel échographique et l'alcool génèrent des artéfacts de poils mouillés qui peuvent mimer des lésions. S'il n'est pas possible de réaliser les radiographies avant l'échographie, il faudra alors veiller à bien essuyer le patient avant de faire les radiographies.
Les colliers et harnais doivent être retirés. Les tubulures ne doivent pas être superposées au thorax.
V. Conclusion
La technique et le positionnement sont primordiaux dans la réalisation de radiographies. Le choix des incidences radiographiques dépendra du motif de réalisation des clichés. La radioprotection prévaut sur toute autre considération technique ou de positionnement.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Première description de myélolipome intra-osseux de l'ilium chez un chat traité par iliectomie partielle et préservation du membre.
Marie FOURNIER
Coauteur : Cyrill PONCET
Introduction
Le myélolipome est une tumeur bénigne rare décrite chez le chien et le chat, principalement au niveau du foie et, plus rarement, de la rate. Des localisations atypiques ont également été rapportées, notamment dans la glande surrénale, l'épiplon, le canal épidural et l'œil. Cette communication rapporte le premier cas de myélolipome intra-osseux en médecine vétérinaire ainsi que la deuxième description d'une iliectomie partielle chez un chat [1,2].
Anamnèse
Un chat Européen mâle castré de 8 ans est présenté à son vétérinaire traitant suite à la palpation d'une masse en région iliaque droite, détectée deux semaines auparavant. Il ne présente aucune altération de l'état général.
Examen clinique
L'examen général ne présente aucune anomalie. Aucune boiterie n'est mise en évidence. Une masse de 3 cm, sous-cutanée, non mobilisable, non douloureuse et de consistance osseuse est identifiée latéralement à l'aile de l'ilium droit.
Démarche diagnostique
Le bilan sanguin hématologique et biologique est dans les normes. Un scanner du bassin révèle une masse de densité graisseuse et tissulaire déformant l'aile de l'ilium droit (image 1). Cette lésion est en faveur d'un processus néoplasique osseux bénin, notamment un lipome intra-osseux, un ostéome, sans pouvoir exclure un liposarcome. Le bilan d'extension est négatif.
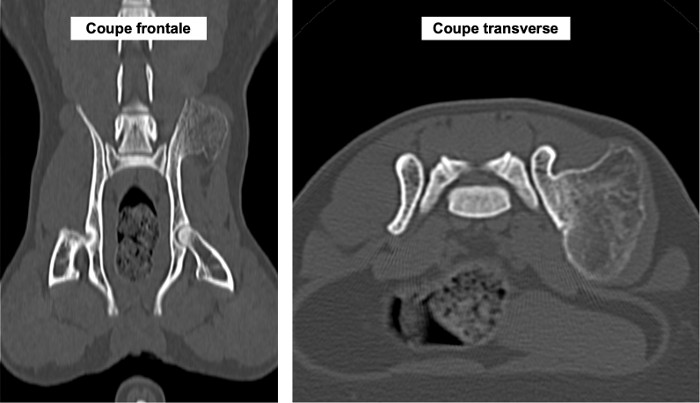
Image 1
Traitement
Compte tenu de la forte suspicion de lésion bénigne, une résection marginale de la masse par iliectomie partielle avec préservation du membre est réalisée (image 2). L'analyse histologique est revenue en faveur d'un myélolipome intra-osseux. Le patient a quitté l'hospitalisation deux jours après l'intervention. Le suivi à 15 jours post-opératoire est satisfaisant et aucune boiterie n'est rapportée. Un contrôle à six mois est attendu au moment de cette présentation.
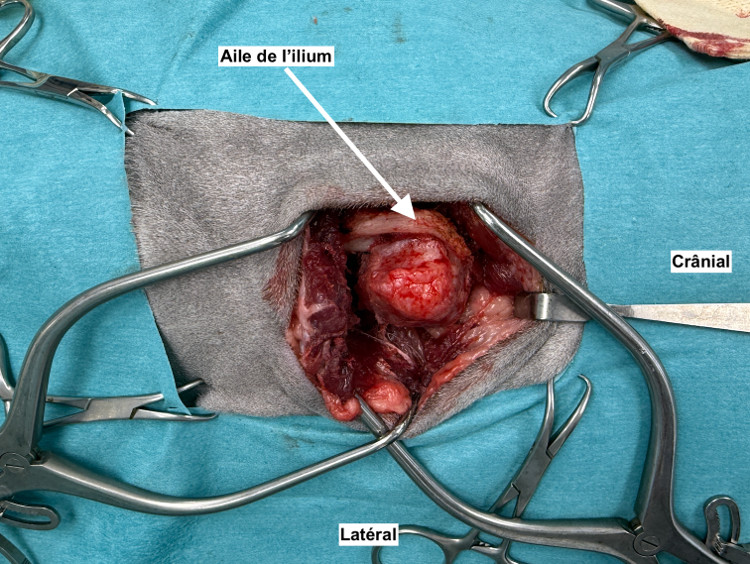
Image 2
Discussion
Le myélolipome est une tumeur bénigne rare composée de tissu adipeux et d'éléments hématopoïétiques ressemblant à la moelle osseuse, dont l'étiopathogénie reste incertaine. Chez l'humain, il se développe principalement dans les glandes surrénales, bien que des formes extra-surrénaliennes aient été rapportées dans le rein, la région périrénale, la région présacrée, le rétropéritoine, le pelvis, la rate et le thorax. Des cas plus rares ont été décrits dans l'os, notamment l'humérus, l'acétabulum, le fémur et la mandibule [3].
En médecine vétérinaire, les myélolipomes sont exceptionnels et majoritairement signalés dans le foie et la rate. Des localisations atypiques ont été rapportées dans la glande surrénale, l'épiplon, le canal épidural et l'œil. Chez le chat, seuls les myélolipomes hépatiques et spléniques ont été décrits à ce jour [1, 2].
Dans notre cas, en raison de la suspicion sur la nature de la lésion et de son potentiel évolutif, une résection en bloc a été réalisée par iliectomie partielle. Cette technique, déjà décrite chez un chat atteint d'un kyste anévrismal, permet de préserver la fonction du membre [4]. Chez le chien, des interventions similaires, incluant l'iliectomie et l'hémipelvectomie crâniale avec conservation du membre, ont été rapportées, mais avec un risque accru de complications telles que fractures de l'ischium et rétrécissement du canal pelvien [5,6].
Conclusion
Ce cas clinique illustre un diagnostic rare de myélolipome intra-osseux dans l'aile de l'ilium d'un chat domestique de 8 ans. Une résection marginale avec iliectomie partielle a été réalisée, permettant la préservation du membre et une évolution clinique favorable à court terme.
Bibliographie
- KENNEDY DJ, FERREIRA HMT, DOBROMYLSKYJ MJ, HOBI S, ALMENDROS A, BĄCZKOWSKI PM. Splenic Myelolipomas in the Domestic Cat-To Operate or Not to Operate? Animals (Basel). 2024 Jun 5;14(11):1700. doi: 10.3390/ani14111700.
- VALLI VE. Tumors of the Hemolymphatic. In: Meuten JD. System in Tumors in domestic animals. 5è édition. John Wiley & Sons, Inc., 2017, pp. 317-318.
- WEN J, CHEN H, YI W, ZHOU X. Primary costal myelolipoma: a case report and review of the literature. Int J Clin Exp Pathol. 2015 Feb 1;8(2):2202-4. PMID: 25973129; PMCID: PMC4396243.
- WINBLADH K et al. Aneurysmal bone cyst in the pelvis of a cat: successful outcome of partial iliectomy with limb preservation. JFMS Open Rep. 2020.
- ORAMAS A et al. Iliectomy with limb preservation for a dog with ilial osteosarcoma: Surgical description and case report. Vet Surg. 2020.
- DOWNEY AC et al. Cranial internal hemipelvectomy (iliectomy) with limb sparing for a dog with ilial chondrosarcoma: A case report. Clin Case Rep. 2022.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Prévalence et caractéristiques de l'hypokaliémie associée aux anémies hémolytiques à médiation immune chez le chien
Maxime DALVERNY
Coauteurs : P. BERNARD, R. LAVOUE
Introduction
Les anémies hémolytiques à médiation immune (AHMI) sont fréquemment rencontrées chez le chien et sont associées à des taux de morbidité et mortalité élevés. Chez l'homme, des hypokaliémies significatives, dont certaines sont associées à des myopathies secondaires sévères, ont été rapportées lors de diverses maladies à médiation immunitaire. Différents mécanismes sont évoqués : pertes digestives et/ou rénales (incluant des cas d'acidose tubulaire rénale distale) ou bien secondaire aux traitements immunosuppresseurs notamment. Quelques cas d'acidose tubulaire rénale distale ont été décrits lors d'AHMI chez le chien mais, à notre connaissance, aucune donnée dans la littérature ne s'est intéressée à ce jour à la prévalence et l'origine des hypokaliémies associée aux AHMI.
L'hypothèse initiale de travail est que les chiens atteints d'AHMI sont plus susceptibles de présenter une hypokaliémie à l'admission, comparée à d'autres causes d'anémie. Les objectifs de cette étude sont :
- d'estimer la prévalence de l'hypokaliémie chez les chiens atteints d'AHMI par rapport aux anémies par pertes sanguines et aux anémies secondaires aux insuffisances rénales ;
- d'explorer les mécanismes sous-jacents associés à l'hypokaliémie ;
- de déterminer si l'hypokaliémie est corrélée à la gravité de l'AHMI.
Matériel et méthodes
Cette étude rétrospective, réalisée entre 2020 et 2024, a inclus 44 chiens atteints d'AHMI, associative ou non, diagnostiquée selon les critères établis dans le consensus ACVIM dédié. Deux groupes contrôles ont également été inclus : 33 chiens avec une anémie par perte sanguine (APS) secondaire à des saignements cavitaires ou organiques d'origine variée et 27 chiens présentant une anémie associée à une atteinte rénale (AIR). Dans le groupe AHMI, les cas pour lesquels le dossier médical était incomplet ont été exclus, de même que ceux souffrant d'une affection concomitante ou recevant un traitement pouvant altérer la kaliémie (maladie rénale chronique, entéropathie exsudative, inhibiteurs du système rénine-angiotensine-aldostérone...). Dans le groupe AIR, les chiens atteints de leptospirose ou de pyélonéphrite avérée ont été exclus.
Les données cliniques, épidémiologiques, la présence ou non d'un traitement glucocorticoïde en cours, le score CHAOS (Canine Hemolytic Anemias Objective Score), ainsi que les données hémato-biochimiques (hémogramme, biochimie, ionogramme, analyse d'urine) ont été analysés. Une hypokaliémie a été définie comme une valeur de potassium plasmatique inférieure à 3,5 mmol/L.
Des régressions logistiques et des modèles linéaires généraux ont été réalisés pour évaluer l'effet des groupes, des signes cliniques, d'un traitement antérieur aux glucocorticoïdes, de la pression artérielle (PA) et des résultats hémato-biochimiques sur la valeur de potassium plasmatique.
Résultats
Dans cette étude, les chiens du groupe AHMI présentaient un rapport de chances significativement plus élevé (p<0,001) de 10,8 [2,6-44,8]95 %CI et de 3,8 [1,6-6] 95 %CI d'être présenté avec une hypokaliémie par rapport aux groupes APS et AIR, respectivement. La concentration médiane en potassium était significativement plus basse (3,2±0,5 mmol/L) comparée aux chiens des groupes APS (4,1±0,7 mmol/L) et AIR (4,5±0,8 mmol/L) (p<0,001). Chez les chiens atteints d'AHMI, la valeur de potassium plasmatique n'était pas significativement affectée par la présence de signes digestifs, la prise préalable de glucocorticoïdes, la valeur de pression artérielle, la créatinine, ni par le pH urinaire à l'admission. Les chiens atteints d'AHMI et hypokaliémiques présentaient une concentration en bicarbonate plasmatique significativement plus faible que les chiens du groupe APS, mais non significativement différente des chiens de groupe AIR (p=0,048). L'hypokaliémie n'était pas significativement associée à l'hématocrite, au score clinique CHAOS, ni au nombre de transfusions réalisées.
Discussion et conclusion
Dans cette étude, l'hypokaliémie était significativement plus fréquente chez les chiens atteints d'AHMI par rapport aux chiens présentant une anémie par perte sanguine ou associée à une atteinte rénale. Aucune association avec la gravité de l'AHMI n'a été identifiée. Bien que les mécanismes sous-jacents nécessitent de plus amples explorations prospectives, ces hypokaliémies pourraient être secondaires à des pertes rénales, notamment par acidose tubulaire rénale, dans la mesure où elle semble associée à une acidose métabolique.
Références
- SHEARER LR, BOUDREAU AE, HOLOWAYCHUK MK. Distal renal tubular acidosis and immune-mediated hemolytic anemia in 3 dogs. J Vet Intern Med. 2009;23(6):1284-1288.
- SOLEIMANI M, RASTEGAR A. Pathophysiology of renal tubular acidosis: core curriculum 2016. Am Journal Kidney Diseases. 2016;68(3):488-498.
- VELARDE-MEJÍA Y, GAMBOA-CÁRDENAS R, UGARTE-GIL M, ASURZA CP. Hypokalemic Paralysis: A Hidden Card of Several Autoimmune Diseases. Clinical Medicine Insights. 2017;10.
- BOTH, T., ZIETSE, R., HOORN, E.J. et al. Everything you need to know about distal renal tubular acidosis in autoimmune disease. Rheumatol Int. 2014 ;34, 1037-1045.
- GARDEN OA et al. ACVIM consensus statement on the diagnosis of immune-mediated hemolytic anemia in dogs and cats. J Vet Intern Med. 2019;33(2):313-334
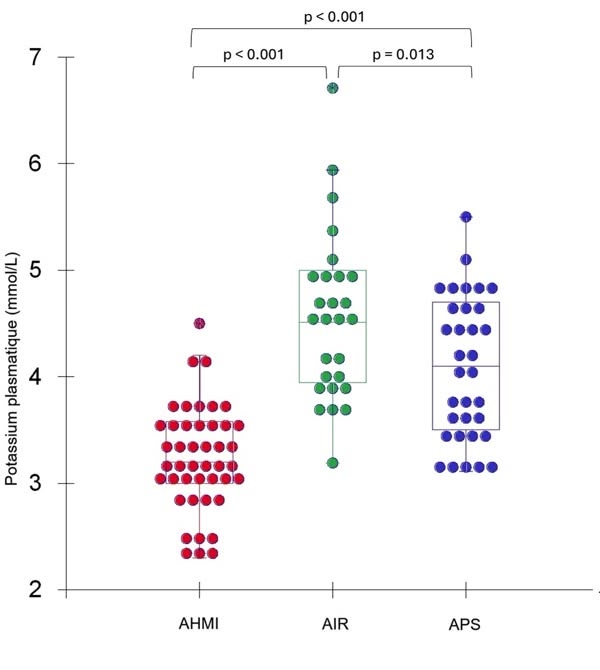
Figure 1 : Concentration plasmatique en potassium en fonction des groupes.
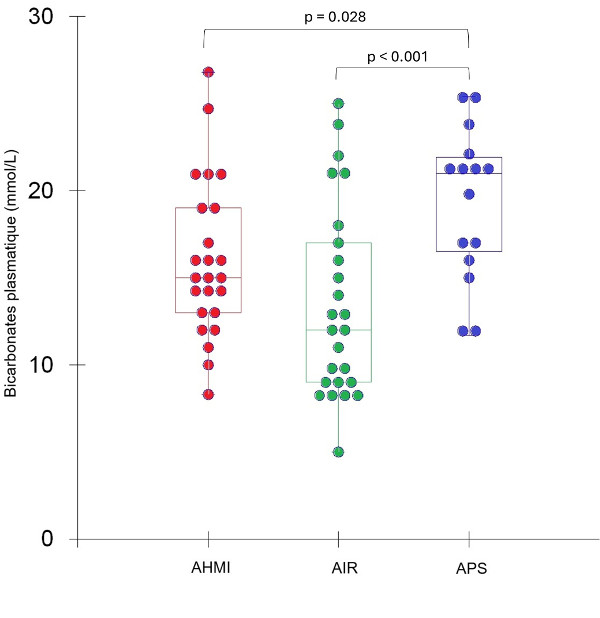
Figure 2 : Concentration plasmatique en bicarbonate en fonction des groupes.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Prise en charge d'un syndrome cardio-rénal autour d'un cas clinique
Merignac, France
I. Introduction
Le syndrome cardio-rénal (SCR) désigne l'ensemble des interactions bidirectionnelles entre cœur et reins, où une atteinte aiguë ou chronique d'un organe peut induire une dysfonction de l'autre.[1,2] Chez le chien et le chat, le SCR reste probablement sous-diagnostiqué, notamment en situation d'insuffisance cardiaque aiguë compliquée d'altérations de la fonction rénale.
Le syndrome cardiorénal est divisé en 5 types de désordres de l'axe cardiovasculaire-rénal (DCvR) :
- le type 1 et le type 2 définissent une maladie cardiaque aigue ou chronique (respectivement) ayant des répercussions rénales ;
- le type 3 et le type 4 définissent une maladie rénale aigue ou chronique ayant des répercussions cardiaques ;
- le type 5 définit une affection systémique résultant en une affection cardiaque et rénale concomitante.
Lors de la présentation, un cas de syndrome cardiorénal sera présenté.
Un chien/chat présenté en urgence pour signes d'insuffisance cardiaque gauche aiguë (dyspnée, tachypnée, crépitements pulmonaires) a bénéficié d'une prise en charge intensive :
- oxygénothérapie ;
- diurétiques de l'anse (furosémide) ;
- pimobendane.
Au cours de l'hospitalisation, une élévation progressive de la créatinine a été mise en évidence, évoquant le développement d'un syndrome cardio-rénal aigu (type 1) [2].
II. Discussion
Le SCR aigu survient fréquemment lors d'insuffisance cardiaque décompensée, via plusieurs mécanismes :
- hypoperfusion rénale liée à la baisse du débit cardiaque ;
- activation neuro-hormonale (SRAA, système sympathique) ;
- effets iatrogènes des diurétiques et vasodilatateurs sur la perfusion rénale. [1,2].
La gestion repose sur un équilibre délicat entre :
- contrôle de la congestion cardiaque (diurétiques) ;
- maintien d'une perfusion rénale suffisante ;
- ajustement thérapeutique en fonction de la fonction rénale et de la diurèse.
Le suivi doit inclure la créatinine, l'urée, les électrolytes, le monitoring de la pression artérielle.
III. Conclusion
Ce cas illustre l'importance de reconnaître précocement le syndrome cardio-rénal chez le chien et le chat hospitalisés pour insuffisance cardiaque aiguë. Une prise en charge multidisciplinaire intégrant la cardiologie, la néphrologie et les soins intensifs permet d'optimiser le pronostic.
Bibliographie
- ORVALHO JS, COWGILL LD. 2017. Cardiorenal Syndrome: Diagnosis and Management. Vet Clin North Am Small Anim Pract 47 : 1083-1102.
- POUCHELON JL, ATKINS CE, BUSSADORI C, OYAMA MA, VADEN SL, BONAGURA JD, et al. 2015. Cardiovascular–renal axis disorders in the domestic dog and cat: a veterinary consensus statement. J Small Anim Pract 56 : 537-552.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Prise en charge thérapeutique de l'hypertension artérielle
Ollioules France
I. Introduction
L'hypertension artérielle pulmonaire (HTAP) est une maladie grave chez le chien et le chat, caractérisée par une élévation anormale de la pression dans l'artère pulmonaire. Elle peut être secondaire à de nombreuses affections cardiaques ou respiratoires, et son traitement vise à améliorer la qualité de vie, réduire les signes cliniques et, si possible, corriger la cause sous-jacente. La prise en charge thérapeutique a fortement évolué ces dernières années, grâce à l'introduction de nouvelles molécules et à une meilleure compréhension de la physiopathologie de l'HTAP.
II. Principes généraux du traitement
Le traitement de l'HTAP chez le chien et le chat repose sur deux axes principaux :
- Traitement de la cause sous-jacente : il est essentiel d'identifier et de traiter, si possible, la maladie primaire responsable de l'HTAP (maladie cardiaque, maladie respiratoire chronique, thromboembolie, dirofilariose, etc.)
- Traitement symptomatique de l'HTAP : lorsque la cause n'est pas curable ou que l'HTAP persiste malgré la prise en charge étiologique, des traitements vasodilatateurs pulmonaires sont indiqués pour réduire la pression artérielle pulmonaire et améliorer les symptômes
III. Médicaments vasodilatateurs pulmonaires
1. Inhibiteurs de la phosphodiestérase de type 5 (IPDE5)
a) Sildénafil
- Mode d'action : le sildénafil inhibe la phosphodiestérase de type 5, ce qui augmente la concentration de GMPc dans les cellules musculaires lisses vasculaires pulmonaires, induisant une vasodilatation sélective du lit artériel pulmonaire.
- Indications : utilisé en première intention chez le chien et le chat pour l'HTAP, quelle que soit la cause, notamment en cas d'HTAP sévère ou symptomatique.
- Posologie : 1-4 mg/kg/j par voie orale toutes les 8 heures.
- Efficacité : de nombreuses études et cas cliniques montrent une amélioration des signes cliniques (fréquence respiratoire, intolérance à l'effort, score clinique) et une réduction de la pression pulmonaire mesurée à l'échocardiographie.
- Tolérance : généralement bien toléré, peu d'effets secondaires notables à la dose recommandée. Surveillance de la pression artérielle systémique recommandée.
b) Autres IPDE5
Le tadalafil, molécule de la même classe, peut être utilisé chez certains chiens, notamment en cas d'intolérance ou de réponse insuffisante au sildénafil.
2. Cas particuliers
HTAP réfractaire : certains chiens peuvent devenir résistants au sildénafil. L'ajout d'autres vasodilatateurs, comme l'ambrisentan (antagoniste des récepteurs de l'endothéline), a montré un bénéfice clinique dans quelques cas rapportés.
IV. Autres vasodilatateurs
1. Inhibiteurs calciques
Amlodipine : utilisée principalement chez l'homme, son usage vétérinaire est limité mais peut être envisagé dans certains cas d'HTAP chronique modérée, en particulier lorsque les autres options sont inefficaces ou contre-indiquées.
2. Théophylline
Mode d'action : bronchodilatateur, inhibiteur de la phosphodiestérase, il peut améliorer la symptomatologie respiratoire et avoir un effet bénéfique sur l'HTAP secondaire à une maladie pulmonaire obstructive chronique (MPOC) chez le chien, ou dans l'asthme et la bronchite chronique chez le chat.
Usage : surtout en association avec d'autres traitements, chez les animaux présentant une composante obstructive des voies respiratoires.
3. Le pimobendane : inhibiteur de la PDE-3 et calcium sensibilisateur
Son utilisation est intéressante car en plus de son indication pour l'insuffisance cardiaque congestive, certains auteurs l'utilisent également comme vasodilatateur artériel pulmonaire. Le pimobendane agit sur les grandes et petites artères pulmonaires par action sur les canaux potassiques et activation de la voie AMPc dépendante adrénergique. De plus, il agit également sur l'inotropie gauche et droite et permet une diminution des pressions atriales gauche et droite.
Dans une étude réalisée par Atkinson et coll. en 2009, 10 sur 10 chiens atteints de MVD et d'hypertension pulmonaire (vélocité maximale de régurgitation tricuspidienne > 3,5 m/s), la concentration sérique en NT-proBNP a diminué et la qualité de vie s'est améliorée grâce à l'administration de pimobendane (0,4-0,6 mg/kg/j). Cependant, cette amélioration n'a seulement été rapportée qu'à court terme (35 jours) mais est non significativement présente à long terme (8 semaines). Néanmoins, la vélocité de la régurgitation tricuspidienne a diminué chez tous les chiens en passant de 4,28 m/s [3,5–5,7 m/s] à 3,52 m/s [2,4–5,0 m/s].
La milrinone est également un inhibiteur de la PDE-3 mais qui n'a pas à ce jour montré d'effets cliniques probants, bien que diminuant la pression pulmonaire et améliorant la fonction ventriculaire gauche.
V. Traitement de la cause sous-jacente
- Maladie cardiaque gauche (ex : maladie valvulaire mitrale, cardiomyopathie) : Contrôle optimal de l'insuffisance cardiaque (diurétiques, inhibiteurs de l'enzyme de conversion, pimobendane, etc.).
- Maladies pulmonaires chroniques : traitement spécifique de l'affection respiratoire (corticostéroïdes, bronchodilatateurs, gestion environnementale).
- Thromboembolie pulmonaire : anticoagulants, prise en charge de la cause thrombogène.
- Dirofilariose : traitement adulticide et microfilaricide, gestion des complications.
- etc. etc.
VI. Autres mesures et traitements d'appoint
- Oxygénothérapie : indiquée en cas de décompensation aiguë ou de signes d'hypoxie marquée.
- Gestion de l'effort : limiter l'activité physique intense, éviter le stress et les situations favorisant l'hypoxie.
- Contrôle du poids : prévenir l'obésité pour limiter la surcharge cardiorespiratoire.
- Surveillance régulière : évaluation clinique, échocardiographie de suivi, mesure de la pression artérielle systémique et pulmonaire, adaptation du traitement selon l'évolution.
VII. Particularités chez le chat
L'HTAP est moins fréquente chez le chat que chez le chien, mais les principes de traitement sont similaires. Le sildénafil est également utilisé à la même posologie (1 mg/kg PO q8h), avec une bonne tolérance [7]. La théophylline peut être utile en cas de bronchopathie chronique ou d'asthme félin associé [5]. L'identification et le traitement de la cause sous-jacente restent prioritaires.
VIII. Perspectives et traitements émergents
- Antagonistes des récepteurs de l'endothéline : l'ambrisentan a montré des avantages cliniques chez des chiens réfractaires au sildénafil, mais son usage reste limité à des cas particuliers et sous surveillance rapprochée.
- Nouveaux agents : des recherches sont en cours sur d'autres classes de vasodilatateurs pulmonaires et sur la modulation de l'inflammation pulmonaire.
IX. Conclusion
Le traitement de l'hypertension artérielle pulmonaire chez le chien et le chat repose avant tout sur le sildénafil, vasodilatateur pulmonaire de référence, associé à la prise en charge de la cause sous-jacente. Une surveillance clinique et échocardiographique régulière est indispensable pour adapter le traitement et améliorer la qualité de vie des animaux atteints. La prise en charge doit toujours être individualisée, en tenant compte de la cause, de la sévérité de l'HTAP, de la tolérance au traitement et de l'évolution clinique.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Quand appétence rime avec vigilance : analyse des ingestions accidentelles de médicaments chez le Chien et le Chat (5 ans de données)
Fougères France
Si l’administration d’un médicament à un chien ou un chat peut représenter un véritable défi pour leurs propriétaires, il arrive parfois que ces produits soient au contraire particulièrement prisés par ces animaux. L’ajout de plus en plus courant de facteurs d’appétence aux médicaments vétérinaires, visant à faciliter l’observance des traitements, peut également augmenter le risque d’ingestions accidentelles par les animaux du foyer.
La pharmacovigilance surveille les effets indésirables des médicaments chez l’animal, que ceux-ci soient administrés ou non dans le cadre de leur AMM. L’Anses-ANMV et le Centre de pharmacovigilance vétérinaire de Lyon enregistrent ainsi chaque année des déclarations d’effets indésirables suite à l’ingestion accidentelle de divers médicaments par des chiens ou des chats.
Une analyse rétrospective des cas de pharmacovigilance déclarés en France chez le chien et le chat a ainsi été menée par l’Anses-ANMV sur une période de 5 ans (de 2020 à 2024). Les cas relevant d'une ingestion accidentelle de médicaments ont été identifiés et collectivement analysés en termes de profils d'animaux concernés, de médicaments impliqués et d'effets indésirables observés.
L’agence dénombre 686 cas d’ingestions accidentelles de médicaments par des animaux de compagnie entre 2020 et 2024, impliquant 603 chiens et 120 chats. Le nombre annuel de déclarations est néanmoins resté stable sur la période pour le chien comme pour le chat. Un grand nombre de médicaments sont concernés même si certaines classes thérapeutiques sont davantage représentées (antiépileptiques, certains antibiotiques et antiparasitaires).
Les jeunes animaux semblent particulièrement à risque. Chez le chat, les situations décrites relatent majoritairement des "vols" de médicaments sous forme de comprimés appétants (à base d’amoxicilline/acide clavulanique, de phénobarbital ou de saronaler notamment), alors que les situations sont plus variables chez le chien : ingestion spontanée de comprimés, mais aussi de colliers médicamenteux, ou de résidus de médicaments destinés à des grands animaux.
Le profil des réactions observées dépend des médicaments concernés. Les effets indésirables déclarés sont majoritairement bénins, mais des intoxications graves ont été rapportées avec des médicaments à base de phénobarbital, de sarolaner (chez le chat), ou lors d’ingestions accidentelles de médicaments pour grands animaux (antiparasitaires ou médicaments destinés à l'euthanasie des animaux notamment).
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Quand l'alimentation fait boiter : affections squelettiques d'origine alimentaire
Gentilly, France
I. Introduction
L'alimentation, que ce soit en quantité ou en qualité, influence la survenue et la sévérité des maladies ostéoarticulaires et à tout âge de la vie. Chez le chiot, certaines affections locomotrices présentent une origine nutritionnelle probable ou avérée. Chez le chaton, et en particulier celui de grande race, et bien que peu d'informations soient disponibles, il est prudent de considérer les mêmes précautions que chez le chiot de grande race. Les maladies ostéoarticulaires semblent largement sous-estimées dans cette espèce.
II. L'alimentation par excès fait boiter
1. Excès pendant la croissance
Un excès énergétique pendant la croissance, souvent indissociable d'un excès de l'ensemble des nutriments, est responsable ou favorise de nombreuses maladies ostéoarticulaires et musculo-tendineuses. La croissance n'est pas allométrique, et schématiquement, le squelette se développe plus rapidement que la masse musculaire : toute surcharge pondérale va donc augmenter les contraintes mécaniques et l'instabilité du squelette. Ainsi, une croissance très/trop rapide et un surpoids sont des facteurs de risque d'affections telles que la dysplasie de hanche, du coude ou le syndrome de laxité carpienne.
L'ostéopathie hypertrophique est peut-être l'exemple le plus caractéristique de l'impact de l'alimentation. Observée principalement chez les chiots de grandes races, cette maladie métaphysaire douloureuse est favorisée par une alimentation déséquilibrée, notamment un excès de calcium, de vitamine D ou encore un excès alimentaire (calories, protéines) qui optimise une croissance rapide. Les signes cliniques sont souvent marqués et nécessitent une prise en charge rapide.
Pour rappel, l'absorption de calcium chez le chiot est différente de l'adulte et le rend particulièrement sensible à tout excès en calcium.
L'hypervitaminose A peut provenir d'une supplémentation excessive, ou de façon plus insidieuse, de la consommation de foie, organe de stockage des vitamines liposolubles (donc de la vitamine D aussi). Elle se manifeste par des exostoses diffuses touchant principalement la colonne vertébrale et les membres. Ces excroissances osseuses peuvent entraîner des signes cliniques variés, tels que modification de l'amplitude de mouvement et boiterie, douleurs, et troubles neurologiques (compressions nerveuses). Le diagnostic se fait le plus souvent par une combinaison de l'anamnèse, de l'historique alimentaire et de lésions assez spécifiques à l'examen radiographique. Le traitement repose sur l'arrêt de la supplémentation en vitamine A, quelle qu'en soit la source, ce qui permet d'arrêter la progression des lésions. Leur régression est malheureusement rare.
Certaines maladies osseuses juvéniles comme la panostéite, bien que l'étiologie soit encore mal définie, pourraient être influencées par la nutrition. Une croissance rapide favorisée par une alimentation excessive est régulièrement retrouvée dans les antécédents de chiens atteints. Si le lien de causalité reste à établir, la prudence s'impose quant aux choix alimentaires durant la croissance.
La stérilisation, chimique ou chirurgicale, par son impact sur le besoin énergétique, est un facteur de risque de surpoids et d'obésité, quel que soit l'âge de l'intervention. Elle demande donc une adaptation de l'alimentation et une surveillance accrue, et comme vu précédemment, particulièrement pendant la croissance du chien et du chat, pour limiter les conséquences durables sur le système ostéoarticulaire.
Le mot d'ordre en croissance est donc de nourrir l'animal en quantité juste suffisante pour le faire grandir mince, et avec une ration équilibrée formulée pour la croissance, et un usage raisonné des suppléments. Cela évite les excès nutritionnels, ralentit la vitesse de croissance et limite les risques de troubles ostéoarticulaires sans compromettre la stature de l'animal. Pendant cette période, tout impact sur le développement de système ostéoarticulaire a un retentissement sur la qualité de vie de l'animal sur le long terme.
2. Excès énergétique tout au long de la vie
L'obésité est l'une des affections nutritionnelles les plus fréquentes chez le chien et le chat. Elle favorise l'émergence de troubles orthopédiques et la surcharge mécanique chronique imposée aux articulations, exacerbe la douleur et la boiterie chez les animaux atteints d'arthrose. En parallèle, l'excès de tissu adipeux contribue à un état pro-inflammatoire systémique, susceptible d'amplifier les processus dégénératifs articulaires. La gestion du poids corporel doit donc être considérée comme un pilier fondamental de la prévention et du traitement des troubles locomoteurs chez les carnivores domestiques.
Contrairement au chien, chez le chat c'est l'âge qui est le facteur majeur de risque de troubles musculosquelettiques, pas la note d'état corporel. Cependant, les études sont peu nombreuses dans cette espèce. De plus, le chat au-delà de 11-12 ans a tendance à perdre du poids, ce qui pourrait masquer l'incidence du surpoids chez le chat vieillissant.
III. L'alimentation par défaut fait boiter
1. Dénutrition pendant la croissance
Le calcium, le phosphore et la vitamine D participent conjointement au métabolisme du tissu osseux. Si une carence en phosphore n'est pas une préoccupation en pratique vétérinaire, une carence en calcium et/ou vitamine D se manifeste par un défaut de minéralisation osseuse et une boiterie. Il est de nouveau possible de voir du rachitisme en clinique à cause de la popularité des régimes « BARFoïdes » conduisant au remplacement des os charnus par de la viande. Pour les rations ménagères non formulées par un vétérinaire, tout est possible, excès ou carence en minéraux et vitamines. L'équilibre nutritionnel de la ration diminue rapidement les douleurs, mais les déformations osseuses sont bien souvent définitives.
2. Carence en calcium tout au long de la vie
Les rations, comme les régimes exclusivement carnés, le fait-maison non complémenté ou celles contenant beaucoup de phytates (sources végétales), sont souvent pauvres en calcium ou avec un rapport calcium/phosphore inapproprié. Il s'ensuit une hyperparathyroïdie secondaire nutritionnelle. Elle peut se traduire selon sa sévérité par des tremblements musculaires, des fractures pathologiques, une ostéopénie généralisée et parfois des signes neurologiques. Les anomalies biochimiques typiques incluent une augmentation de la parathormone et une diminution du calcium et de la vitamine D. Le pronostic est variable, mais une correction adaptée ou un changement du régime alimentaire permet généralement une amélioration clinique.
3. Carence protéique, amyotrophie et sarcopénie
Une carence protéique (et/ou énergétique) peut induire une amyotrophie généralisée, qui s'observe dans de nombreuses maladies métaboliques. La sarcopénie, ou dystrophie musculaire liée à l'âge, est une perte importante de la masse musculaire s'accompagnant d'une perte de force et de fonction. En ce sens et indirectement, une diminution de la masse musculaire peut aggraver les boiteries.
Bien qu'une diminution de la masse protéique ne soit pas toujours d'origine nutritionnelle, une restriction protéique doit être motivée, quantifiée et toujours être confrontée au stade physiologique, au statut nutritionnel et à la situation médicale de l'animal. Cela demande donc de connaître le profil nutritionnel de l'aliment prescrit et pas seulement son indication, les profils étant très différents d'une marque à une autre. Les aliments pour chats et chiens seniors en sont un bon exemple.
4. Carence nutritionnelle et cicatrisation
La boiterie ne sera pas per se d'origine alimentaire mais un retard de cicatrisation, qui lui peut être d'origine nutritionnelle (énergie, protéines, acides gras essentiels, minéraux, vitamines), va prolonger la période de convalescence ou participer aux séquelles.
IV. Conclusion
En résumé, une alimentation inadéquate peut non seulement exacerber des troubles locomoteurs existants, mais aussi en être l'origine. Un historique alimentaire détaillé, répertoriant tous les ingrédients consommés et leur quantification est indispensable. Et ce qui fonctionne dans chaque situation, la prévention (ou le traitement) du surpoids et de l'obésité est essentielle.
Bibliographie
- BONECKA J, SKIBNIEWSKI M, ZEP P, DOMINO M. Knee Joint Osteoarthritis in Overweight Cats: The Clinical and Radiographic Findings. Animals (Basel). 2023 Jul 27;13(15):2427.
- CACHON T, FRYKMAN O, INNES JF, LASCELLES BDX, OKUMURA M, SOUSA P, STAFFIERI F, STEAGALL PV, VAN RYSSEN B. COAST Development Group's international consensus guidelines for the treatment of canine osteoarthritis. Front Vet Sci. 2023 Aug 3;10:1137888.
- DEABOLD K, MONTALBANO C, MISCIOSCIA E. Feline Osteoarthritis Management. Vet Clin North Am Small Anim Pract. 2023 Mar 22:S0195-5616(23)00034-7
- DOWGRAY N, COMERFORD E. Feline musculoskeletal ageing: How are we diagnosing and treating musculoskeletal impairment? J Feline Med Surg. 2020 Nov;22(11):1069-1083.
- LEY CJ, M STRAGE E, STADIG SM, VON BRÖMSSEN C, OLSSON U, BERGH A, LEY C. Associations between body composition, metabolic mediators and osteoarthritis in cats. BMC Vet Res. 2025 Feb 25;21(1):103.
- MARCELLIN-LITTLE DJ, HULSE DA, HUNTINGFORD JL, GRUBB T, BRUNKE MW, MARKLEY AP, FRANK B. A proposed framework for practical multimodal management of osteoarthritis in growing dogs. Front Vet Sci. 2025 Apr 28;12:1565922.
- TOHOLOVA J, HORNAK S, KURICOVA M. Non-surgical pain management for hip joint disease in veterinary medicine. Vet Med (Praha). 2024 Aug 20;69(8):261-272.
Liens d'intérêt : En tant que consultante indépendante, je réalise des missions pour des fabricants d'aliments industriels, des fournisseurs d'ingrédients et des laboratoires pharmaceutiques. Aucune de ces entreprises n'est intervenue dans le cadre de cette conférence.
📃 Quand l'antibiothérapie est excessive : focus sur le tractus urinaire
Florian WUILLEMIN
CHV Hopia
Guyancourt, France
I. Introduction
Du fait de l'antibiorésistance croissante dans notre société, objectivée sur ces dernières décennies, de nombreux guides de bonnes pratiques, le plus souvent inspirés ou extrapolés de la médecine humaine, sont apparus ces derniers temps afin de guider au mieux le clinicien dans le traitement des infections urinaires et de limiter l'apparition de nouvelles résistances. L'objectif de cette présentation, axée sur le tractus urinaire, est de détailler quand un traitement antibiotique est nécessaire, le choix de ce dernier, ainsi que la durée recommandée pour le traitement d'une potentielle infection urinaire en fonction de sa localisation.
II. Bactériurie significative
La présence d'une bactériurie significative est à différencier d'une contamination de l'échantillon. Aussi, différents comptages sont proposés en fonction du mode de prélèvement des urines (cystocentèse : ≥100 ; cathétérisation : ≥1000 (≥100 000 pour la chienne) ; miction naturelle : ≥100 000 chien et ≥10 000 chat). Il est généralement accepté qu'un comptage trop faible, pouvant correspondre à une potentielle contamination du prélèvement ,est dit non significatif et ne nécessite pas d'antibiothérapie.
III. Bactériurie subclinique vs pathologique
L'urine n'étant pas un milieu stérile, l'infection urinaire est à différencier d'une bactériurie subclinique (présence d'une bactériurie significative sans signes cliniques d'infection urinaire).
Une infection urinaire se manifeste par la présence de signes cliniques (signes du bas appareil urinaire dans le cas de cystite ; signes cliniques généraux en cas de pyélonéphrite) avec mise en évidence d'une bactériurie significative. La présence d'une bactériurie subclinique est bien décrite en médecine vétérinaire (Tableau 1). De plus en plus d'études (majoritairement en médecine humaine) déconseillent le traitement d'une bactériurie subclinique pour de nombreuses raisons (genèse d'antibiorésistance, sélection de germes pathogènes au détriment d'une flore bactérienne équilibrée et diversifiée ne causant pas de signes urinaires). Il est également admis que la présence d'une bactériurie subclinique n'est pas un facteur de risque de développement d'infections plus graves telles qu'une pyélonéphrite.
Dans de récentes recommandations en médecine humaine, il est déconseillé de réaliser des cultures urinaires et/ou de traiter une bactériurie asymptomatique chez les patients âgés, juvéniles, immunodéprimés, diabétiques, enceintes ou avec des atteintes de la moelle épinière. Il est donc raisonnable de penser qu'en l'absence de signes évocateurs d'infections urinaires chez le chien et le chat, la réalisation d'une culture urinaire ou une antibiothérapie ne sont pas nécessaires.
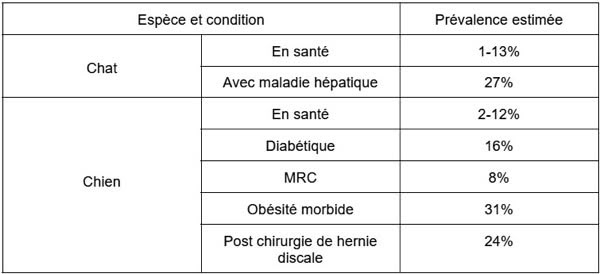
Tableau 1 : prévalence d'une bactériurie subclinique chez le chat et le chien.
IV. Cystites récurrentes
1. Rechutes
On considère comme rechute d'infection urinaire une infection urinaire se débeloppant dans les 4 semaines suivant le traitement de la première infection avec une bactérie similaire. Le premier traitement peut ne pas avoir été efficace (antibiorésistance, défaut de pénétration dans le tissu cible, durée de traitement inadaptée) et une culture urinaire avec antibiogramme est fortement recommandée afin de le réajuster. De plus, l'antibiotique choisi sera différent en cas d'atteinte concommittante de la prostate, des reins ou de la paroi vésicale.
2. Nouvelles infections
Une réinfection est le développement d'une infection urinaire après une période de rémission clinique et secondaire à un nouvel agent infectieux ou un germe similaire plus de 4 semaines après son épisode précédent. Dans le cas d'une réinfection, il est important d'identifier toute cause prédisposante d'infections urinaires. La prise en charge repose alors en la gestion de l'infection urinaire et en la correction de la cause prédisposante : correction de l'uretère ectopique, vulve encapuchonnée, extraction de calculs urinaires non traitables médicalement…
V. Choix de l'antibiotique adapté
Le choix de l'antibiotique est crucial dans la mise en place d'une antibiothérapie. Les objectifs sont : la pénétration de l'antibiotique à une dose satisfaisante dans le tissu cible, une dose adéquate, et une sensibilité du germe au traitement instauré. Une des premières questions à poser avant de choisir l'antibiotique est de savoir s'il s'agit d'une infection urinaire classique ou si l'infection est plus profonde (prostate, reins, paroi vésicale/urétrale) pour laquelle un antibiotique atteignant des doses thérapeutiques dans le tissu sera nécessaire.
De même, l'identification du germe à l'aide d'une culture urinaire ou d'une cytologie urinaire apporte de précieuses informations et permet de cibler l'antibiotique approprié. Une antibiothérapie ciblée et précise permet d'éviter le développement de résistances, ou l'utilisation de plusieurs antibiotiques pour "élargir le spectre" et risquer d'affecter encore plus la flore bactérienne du patient. Aussi, une connaissance du spectre d'action de chaque antibiotique (Tableau 2) est essentielle afin de viser au plus juste le traitement d'une infection bactérienne, soigner le patient et éviter le développement de résistances supplémentaires aux antibiotiques.
VI. Durée de traitement adaptée
Une durée de traitement adaptée est essentielle afin de complètement traiter le patient de son infection tout en évitant une surexposition de sa flore bactérienne à des antibiotiques pouvant déséquilibrer/détruire la flore saine et générer une antibiorésistance. Les dernières guidelines vétérinaires s'inspirent et extrapolent de la médecine humaine où les traitements antibiotiques sont de plus en plus courts. Toutefois, la médecine vétérinaire manque de réelles études pouvant nous conforter dans cette direction. Ainsi, là où une simple infection urinaire de type cystite bactérienne est traitée avec 1 traitement unique ou 3-5 jours d'antibiotiques en médecine humaine, les guidelines ISCAID recommandent un traitement de 3 à 5 jours d'antibiotiques. Dans le cas d'une infection profonde telle qu'une pyélonéphrite, un traitement de 7-14 jours est recommandé en médecine humaine. Bien qu'une antibiothérapie de 4-6 semaines était le plan de traitement initialement recommandé en médecine vétérinaire, les recommandations ISCAID suggèrent une durée de traitement plus courte, extrapolée de la médecine humaine de 10-14 jours. Enfin, pour des cas de prostatite, aucun consensus sur la durée de traitement n'est atteint en médecine humaine et des durées de traitement de 3, 4 ou encore 6 semaines sont reportées. En médecine vétérinaire, une antibiothérapie de 4 semaines est généralement recommandée pour une prostatite aiguë.
VII. Traitement d'une cystite bactérienne simple
Le traitement d'une cystite bactérienne simple consiste donc en une antibiothérapie courte (3-5 jours), avec un antibiotique se concentrant bien dans les urines (Tableau 2). Ainsi, l'utilisation de β-lactamines (amoxicilline seule ou en combinaison), ou de sulfonamides atteignant de fortes concentrations urinaires sont de bonnes premières intentions.
VIII. Traitement d'une infection profonde (type prostatite ou pyélonéphrite)
Le traitement d'une infection profonde consiste en une antibiothérapie plus longue avec un antibiotique pénétrant bien dans le tissu cible et pour lequel les concentrations dans le parenchyme sont assez élevées pour inhiber la croissance de la bactérie cible. Dans ce cas de figure, une bonne connaissance du germe pathogène est nécessaire et une culture urinaire peut aider à établir un plan d'action. Aussi, un germe peut présenter une sensibilité à un antibiotique en milieu urinaire (concentration importante et suffisante pour inhiber ce germe dans les urines) mais une résistance à ce même antibiotique dans le parenchyme rénal, la paroi vésicale ou la prostate par faute de concentration importante de cet antibiotique dans le tissu cible ne permettant pas d'éradiquer le germe.
L'exemple le plus concret est l'utilisation de β-lactamines dans le cadre d'une pyélonéphrite. Cet antibiotique atteint des doses suffisantes pour le traitement d'une pyélonéphrite à bactéries de type coques gram + mais la concentration dans le parenchyme n'est jamais suffisante pour permettre de traiter une pyélonéphrite de type bacilles gram - n'atteignant jamais la concentration tissulaire adéquate.
De même, seuls certains antibiotiques peuvent traverser la barrière sang/prostate (Tableau 2) et permettent le traitement d'une prostatite. En plus d'une castration chimique/physique, un antibiotique approprié est essentiel pour le traitement de ces chiens.
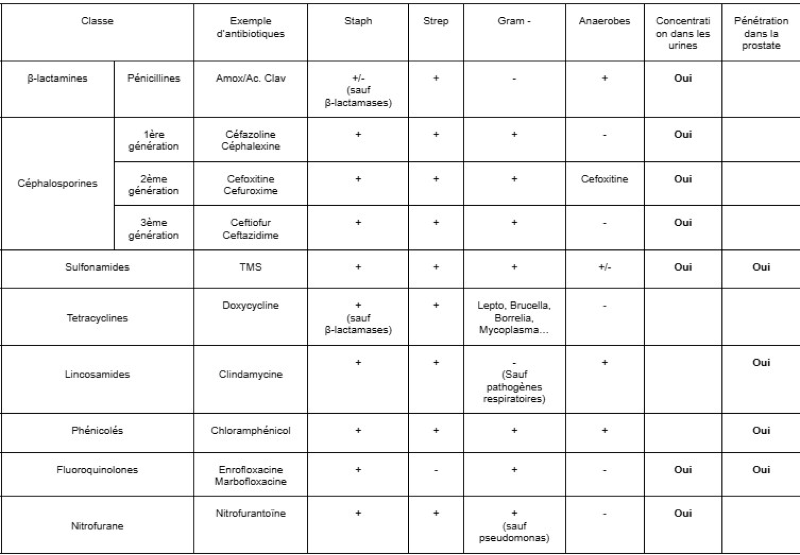
Tableau 2
L'utilisation de céfovecine (Convenia ND) pour le système urinaire est peu intéressante, du moins telle que commercialisée pour les infections cutanées. Cette céphalosporine de 3è génération permet une couverture antimicrobienne d'environ 2 semaines dans le cas d'infections cutanées et tissus mous à Streptococcus/Staphylococcus. En revanche, en cas d'infection par des Enterobacteriaceae, une injection permet une couverture d'environ 6-7 jours pour le milieu urinaire, mais uniquement de 24 h dans le tissu rénal chez le chien avec des résultats similaires chez le chat. Ainsi, une injection unique de Convenia ND chez un patient atteint de pyélonéphrite à gram -, ne peut éradiquer l'infection. De plus, elle participe activement à potentiellement sélectionner d'autres germes résistants en faisant pression sur les populations de gram +.
Les recommandations de l'ISCAID, quant au traitement de pyélonéphrite à Enterobacteriaceae sont l'usage de fluoroquinolones ou de céphalosporine de 3è génération (cefpodoxime par voie orale ou encore de céfotaxime ou ceftazidime en intraveineux). En Europe et en France plus particulièrement avec la lutte contre l'antibiorésistance, l'usage des fluoroquinolones est à éviter au maximum et un bon premier choix pour une pyélonéphrite à Enterobacteriaceae pourrait être les sulfonamides. En effet, une étude révèle qu'environ 80% des germes de pyélonéphrite seraient sensibles aux sulfonamides.
Dans le cas d'une prostatite, les recommandations sont l'usage de fluoroquinolones ou éventuellement de sulfonamides (favorisées en France où l'usage de fluoroquinolones est limité). L'utilisation de clindamycine et des macrolides est limitée pour des prostatites à bactéries gram +.
En conclusion, le traitement d'une bactériurie ne doit être considérée qu'en cas de signes cliniques évocateurs d'une infection urinaire ou profonde. Le traitement d'une bactériurie subclinique est risquée du fait d'une potentielle déstabilisation de la flore bactérienne du patient et de la sélection de bactéries plus virulentes/résistantes. Le choix du traitement antibiotique doit se faire en fonction du type d'infection (profonde ou urinaire simple), du type de bactérie (coques vs bacilles) et potentiellement d'un antibiogramme. Une évolution des pratiques de laboratoire pourrait par ailleurs aider les cliniciens dans le futur à mieux choisir leurs antibiotiques avec une mise à jour des différentes CMI (nouvelles recommandations CLSI) et une possibilité de calculer les CMI en fonction de la cible (urine vs tissu).
Bibliographie
Lectures suggérées : À demander
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Quand le comportement fait penser à la médecine, ou l'inverse... chez le chat
Tel Aviv Israël
Nantes, France
I. Du somatique au psychique, regards croisés sur le chat
Au travers du parcours d'une situation clinique réelle et fréquente, la malpropreté et les agressions, nous vous proposons d'illustrer les messages clés suivants :
1. Un signe comportemental peut traduire une cause médicale
Chez le chat, la malpropreté et l'agressivité peuvent être l'expression d'une douleur [1] [2], d'un trouble nerveux ou d'une affection organique. La dimension médicale doit donc systématiquement être incluse dans la réflexion.
2. Un signe organique peut traduire une cause comportementale ou psychiatrique
Chez le chat une maladie comportementale peut induire entre autres des troubles digestifs (vomissements, diarrhées, anorexie) en lien avec l'activation répétée de l'axe du stress et les perturbations neurovégétatives associées et des troubles urinaires (cystite idiopathique féline, marquage urinaire inapproprié) qui illustrent la somatisation des états pathologiques [3].
3. Un trouble médical peut être aggravé ou entretenu par des facteurs comportementaux et environnementaux
Un dérèglement sur un ou plusieurs des 5 axes comportementaux, peur, autocontrôles, territorialité, relation, environnement et communication [4] peut renforcer des signes liés à une affection physique, compliquant la prise en charge.
4. La démarche diagnostique doit être intégrative
Évaluer un chat présentant des troubles comportementaux suppose de croiser deux analyses :
- une évaluation comportementale structurée (axes de peur, autocontrôle, territorialité, relations, environnement et communication) ;
- un bilan médical ciblé sur les hypothèses organiques compatibles avec les signes observés.
5. La prise en charge efficace combine médecine interne et médecine du comportement
La prise en charge optimale repose sur une approche intégrative : un traitement médicamenteux destiné à soulager la douleur ou corriger un déséquilibre neurochimique gagne en efficacité lorsqu'il est associé à des aménagements environnementaux et à un programme de rééducation comportementale ; de la même façon, le traitement d'un trouble du comportement s'avère plus efficace s'il est accompagné d'une prise en charge médicale rigoureuse et, lorsque nécessaire, d'ajustements médicaux visant à corriger d'éventuels déséquilibres organiques.
II. Vignette clinique
Bella est une chatte Européenne stérilisée de 12 mois, pesant 3 kg et présentée pour malpropreté urinaire et fécale ainsi que pour agression intermittente envers les membres du foyer.
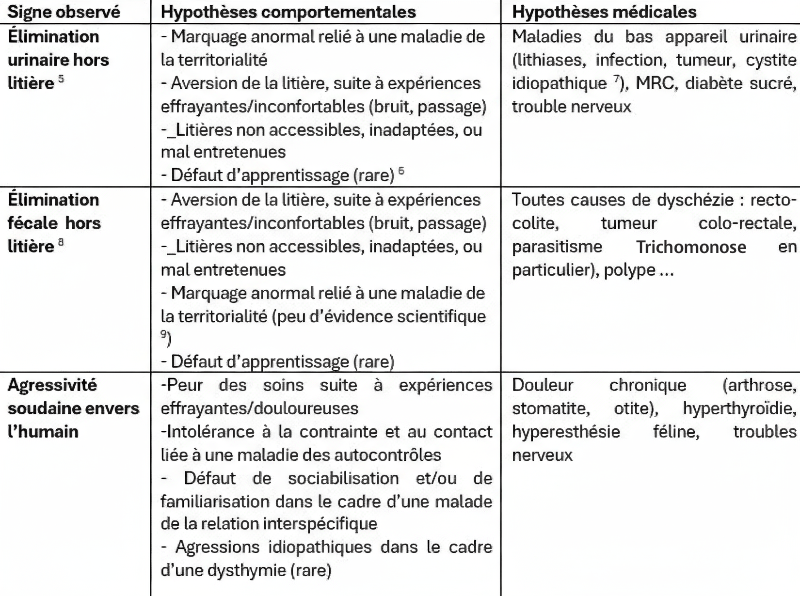
Tableau 1
Au-delà de la vignette clinique, les signes fréquemment observés en consultation de médecine.
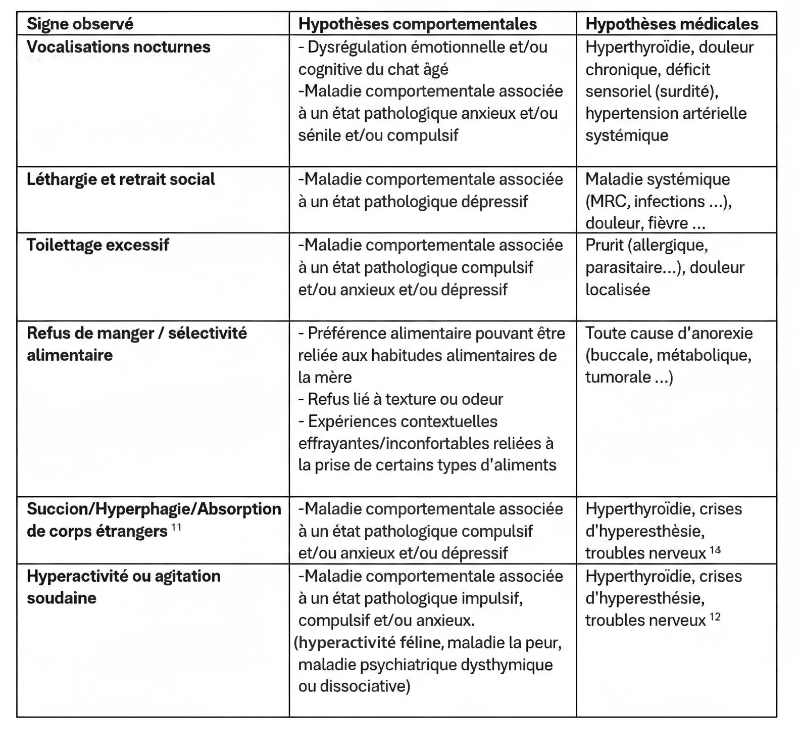 Tableau 2
Tableau 2
Il n'y a pas de barrière entre médecine interne et médecine du comportement mais de multiples liens : les penser conjointement est essentiel.
Bibliographie
- STEAGALL, P. V. et al. 2022 ISFM Consensus Guidelines on the Management of Acute Pain in Cats. J. Feline Med. Surg. 24, 4–30 (2022).
- MILLS, D. S. et al. Pain and Problem Behavior in Cats and Dogs. Animals 10, 318 (2020).
- STELLA, J., CRONEY, C. & BUFFINGTON, T. Effects of stressors on the behavior and physiology of domestic cats. Appl. Anim. Behav. Sci. 143, 157–163 (2013).
- BLEUER-ELSNER, S., MASSON, S., LACOSTE, M. & MULLER, G. Psychiatrie Vétérinaire Du Chat. (No Ledge, 2025).
- BUFFINGTON, C. A. T., WESTROPP, J. L., CHEW, D. J. & BOLUS, R. R. Risk factors associated with clinical signs of lower urinary tract disease in indoor-housed cats. J. Am. Vet. Med. Assoc. 228, 722–725 (2006).
- BRADSHAW, J. & ELLIS, S. The Trainable Cat: A Practical Guide to Making Life Happier for You and Your Cat. (Basic Books, New York, 2016).
- JONES, E., PALMIERI, C., THOMPSON, M., JACKSON, K. & ALLAVENA, R. Feline Idiopathic Cystitis: Pathogenesis, Histopathology and Comparative Potential. J. Comp. Pathol. 185, 18–29 (2021).
- BYRNE, G. et al. Prevalence of Anxiety and Depression in Patients with Inflammatory Bowel Disease. Can. J. Gastroenterol. Hepatol. 2017, 1–6 (2017).
- HOUPT, K. A. Domestic Animal Behavior for Veterinarians and Animal Scientists. (John Wiley & Sons, Inc, Hoboken, NJ, 2018).
- ARNDT, J., SMITH, N. & TAUSK, F. Stress and atopic dermatitis. Curr. Allergy Asthma Rep. 8, 312–317 (2008).
- TYNES, V. V. & SINN, L. Abnormal Repetitive Behaviors in Dogs and Cats. Vet. Clin. North Am. Small Anim. Pract. 44, 543–564 (2014).
- BORNS-WEIL, S. et al. A case-control study of compulsive wool-sucking in Siamese and Birman cats (n = 204). J. Vet. Behav. 10, 543–548 (2015).
- AMADEI, E., CANTILE, C., GAZZANO, A., PIERANTONI, L. & MARITI, C. The link between neurology and behavior in veterinary medicine: A review. J. Vet. Behav. 46, 40–53 (2021).
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Quand le comportement fait penser à la médecine, ou l'inverse...chez le chien
Paris, France
I. Introduction
Pour tout praticien, l'ensemble des symptômes présentés par un patient doit conduire à un cheminement intellectuel permettant, après l'adjonction d'examens complémentaires, à un diagnostic différentiel, voire définitif. Aujourd'hui, les avancées de la médecine du comportement ont permis d'adosser une unique cause comportementale à différents symptômes. Néanmoins, la dichotomie organique -comportement est parfois difficile. Quels sont les éléments qui permettent de s'orienter vers l'un ou l'autre lors d'un diagnostic et surtout, faut-il absolument exclure l'un de l'autre ?
II. Quand le trouble comportemental est d'origine médicale
Pour le praticien généraliste, le diagnostic différentiel des troubles du comportement inclut systématiquement une origine médicale. Certaines manifestations comportementales sont en réalité l'expression de douleurs ou de désordres organiques.
- Agressivité et douleur : la douleur, quelle qu'en soit l'origine (digestive, urinaire, ostéoarticulaire, neurologique), abaisse nettement le seuil d'agressivité. Sa prise en charge permet souvent une diminution marquée des réactions agressives (MILLS, 2020).
- Peurs soudaines et douleurs cachées : des phobies inexpliquées peuvent être la manifestation de douleurs non détectées par les examens habituels (LOPES FAGUNDES, 2018). Certaines crises d'épilepsie nocturnes, passées inaperçues, peuvent induire le lendemain des peurs intenses et soudaines (SHIHAB, 2011).
- Troubles du développement et parasitisme digestif : des comportements répétitifs précoces (pica) ou des difficultés d'apprentissage doivent conduire à explorer une origine digestive, notamment la présence de Giardia chez le jeune chien.
- Léchage répétitif et troubles digestifs : un comportement de léchage compulsif peut être le premier signe d'une affection gastro-intestinale, comme l'a montré BÉCUWE-BONNET (2015).
Ces exemples illustrent la nécessité de rechercher une cause médicale chaque fois qu'un trouble du comportement se présente.
III. Quand les signes physiques sont d'origine comportementale
À l'inverse, certains signes physiques persistants ou récidivants peuvent être entretenus, voire induits, par des troubles comportementaux.
- Pica récidivant : si l'ingestion de corps étrangers peut traduire une douleur digestive, sa répétition chronique doit alerter sur une origine comportementale. Un environnement en inadéquation avec les besoins du chien, (source de stress et/ou de frustration), une relation humain-chien fluctuante ou très contrôlante, sont des facteurs favorables pour le déclenchement de ce signe.
- Léchage cutané répétitif : lorsque toutes les causes médicales (allergiques, parasitaires …) ont été écartées, un léchage récurrent peut être l'expression d'un comportement répétitif lié à un environnement et un budget d'activité en inadéquation avec les besoins du chien.
- Comportements répétitifs et conditions de vie : de nombreux comportements stéréotypés (tournis, léchages, auto-mutilations) trouvent leur origine dans des conditions de vie frustrantes. Dans ces cas, des modifications du budget d'activité, de l'environnement et de la relation homme–chien conduisent souvent à une rémission complète des symptômes.
Le praticien doit donc savoir reconnaître que certains signes physiques ne relèvent pas d'une pathologie organique mais d'un trouble comportemental, afin d'éviter des explorations invasives inutiles.
IV. Corps et comportement : une unité – l'axe intestin-cerveau
Plutôt que d'opposer les dimensions « médicale » et « comportementale », il devient indispensable de penser le chien comme un organisme intégré où corps et comportement interagissent en permanence.
Un exemple particulièrement éclairant est celui de l'axe intestin-cerveau.
Le microbiote intestinal est aujourd'hui reconnu comme un acteur-clé de la régulation du comportement. Certaines bactéries (ex. Lactobacillus, Bifidobacterium) produisent des neurotransmetteurs comme la sérotonine, le GABA ou la dopamine, qui influencent directement l'humeur, l'anxiété et la réactivité émotionnelle de l'animal.
Dans les modèles expérimentaux, une dysbiose intestinale peut ainsi contribuer à des troubles anxieux ou dépressifs, et inversement, un stress chronique peut perturber la composition du microbiote, aggravant les troubles digestifs.
Ces éléments issus de la recherche restent toutefois insuffisants à ce jour pour envisager la modulation du microbiote comme un levier de traitement des troubles comportementaux (MILLS, Animals, 2022).
Ainsi, la dichotomie « médical » versus « comportemental » est de moins en moins pertinente. Le praticien doit intégrer dans son raisonnement la dynamique permanente entre encéphale et organes, entre douleur, microbiote, émotions et comportements. C'est cette approche globale qui permettra non seulement de diagnostiquer avec justesse mais surtout d'accompagner le chien vers une véritable guérison, respectueuse de son bien-être et de sa relation avec son propriétaire (SIRACUSA, 2023). Ce défi est à relever pour les générations futures de praticiens vétérinaires.
Bibliographie
- MILLS DS, DEMONTIGNY-BÉDARD I, GRUEN M, et al.(2020) Pain and Problem Behavior in Cats and Dogs. Animals ;10(2):318
- LOPES FAGUNDES AL, HEWISON L,MCPEAKE KJ, ZULCH H and MILLS DS(2018) Noise Sensitivities in Dogs: An Exploration of Signs in Dogs with and without Musculoskeletal Pain Using Qualitative Content Analysis. Front. Vet. Sci. 5:17. doi: 10.3389/fvets.2018.00017
- SHIHAB, N., BOWEN,J., VOLK, H;A., 2011.Behavioral changes in dogs associated with the development of idiopathic epilepsy. Epilepsy Behav,21(2)pp.160-7. doi: 10.1016/j.yebeh.2011.03.018. Epub 2011 May 4.
- BÉCUWE-BONNET, V., BÉLANGER, M.C., FRANK, D., PARENT, J. and HÉLIE, P., 2012. Gastrointestinal disorders in dogs with excessive licking of surfaces. Journal of Veterinary Behavior, 7(4), pp.194-204.
- SIRACUSA C. The False Dichotomy Between Medical and Behavioral Problems. Veterinary Clinics: Small Animal Practice 2024;54:xiii–xiv
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Quand le comportement fait penser à la médecine, ou l'inverse...chez les lapins
Eschau, France
Le Cannet, France
I. Introduction
Il est fondamental, lors d'une consultation de NAC, de garder à l'esprit que médecine et comportement ne peuvent être dissociés. L'enjeu est d'être capable de repérer, dans chaque espèce, les causes médicales pouvant être à l'origine d'une consultation pour trouble comportemental, et inversement. De nombreux pièges existent : un parasitisme cutané ou une douleur chronique peuvent se manifester par des modifications du comportement, tout comme l'anxiété peut favoriser l'apparition de dermatopathies auto-induites ou de troubles digestifs. C'est pourquoi il convient d'intégrer systématiquement l'hypothèse comportementale dans la démarche diagnostique, au même titre que l'hypothèse médicale.
Le lapin étant une proie, il a tendance à masquer ses symptômes quand il est malade, ce qui peut rendre difficile la détection précoce des affections organiques. Comme de nombreux NAC, il s'agit d'un animal dont les besoins physiologiques et éthologiques sont souvent mal respectés en captivité, ce qui entraîne des affections d'origine environnementale, médicales et comportementales. Comme le rappellent Donnelly et Vella, les conditions de vie – taille des cages, isolement social, absence de stimulations – influencent directement la santé et le bien-être de l'animal. Les besoins de locomotion, d'interactions sociales et de mastication sont fondamentaux, et leur non-respect engendre un stress qui se traduit autant par des troubles comportementaux que par des affections organiques.
II. Est-il pertinent de considérer qu'il y a une binarité et que l'atteinte est soit comportementale, soit médicale ?
Ces dernières années, de nombreuses publications chez les chats et les chiens mettent en évidence des liens clairs entre problèmes de comportement et comorbidité médicale, notamment Mills 2020 et Kwik 2025. Chez le lapin, si les publications sont plus rares, il est bien établi que la douleur modifie le comportement. Ce dernier est intégré, par exemple, dans les grilles d'évaluation de la douleur comme la Bristol Rabbit Pain Scale. Le stress a par ailleurs un impact physiologique majeur : il peut provoquer un arrêt du transit digestif, une immunosuppression et une sensibilité accrue aux infections. Il est donc illusoire d'opposer pathologie médicale et trouble comportemental, tant les deux sont étroitement imbriqués.
Déceler certains signes comportementaux peut néanmoins représenter un défi parce que les propriétaires de lapins ne sont pas toujours conscients de ce qu'est un comportement normal dans cette espèce, et inversement, certains propriétaires très investis et attentifs vont rapporter des signaux subtils qui sont difficiles à interpréter. Les douleurs chroniques, non diagnostiquées – qu'elles soient dentaires, articulaires ou digestives – génèrent de la peur et de l'anxiété qui se traduiront par des changements comportementaux, dont l'agressivité (Tynes 2024).
L'ensemble crée un enchevêtrement complexe où il est parfois impossible de distinguer la cause initiale. C'est pourquoi l'approche clinique doit envisager simultanément les deux dimensions, médicale et comportementale, avec pour objectif ultime le bien-être global du patient.
III. Causes médicales et répercussions comportementales
La douleur est la première cause de modification comportementale. Elle entraîne des altérations physiologiques (variations de fréquence cardiaque et respiratoire, modifications de la température corporelle) mais aussi de nombreux signes comportementaux : agressivité, irritabilité, diminution des déplacements, de l'exploration, du toilettage, de la prise alimentaire, modifications de la posture, de la courbure du dos, du port des oreilles, de l'ouverture palpébrale, comportement de fuite, animal qui se cache...
Il est essentiel de bien connaître le comportement basal de l'individu (en questionnant les propriétaires) pour pouvoir relever les anomalies.
De nombreuses afffections causent des douleurs et affectent le comportement du lapin. Les affections dentaires, très fréquentes, se traduisent par des modifications du comportement alimentaire (sélectivité, diminution de la prise alimentaire), une baisse du toilettage et un désintérêt pour les interactions sociales. Les troubles digestifs, qu'il s'agisse de stases, d'ulcères ou de dysbioses, génèrent irritabilité, isolement, apathie et modifications du comportement alimentaire. Dans ce contexte, Oglesbee et Lord rappellent que l'inadéquation du régime alimentaire – en particulier une carence en fibres – est une cause majeure de stase et donc de douleur abdominale, avec des répercussions directes sur le comportement. Les affections génito-urinaires, telles que les lithiases, les sabloses vésicales ou les infections, entraînent souvent une malpropreté, de l'aversion acquise pour la litière et un toilettage excessif pouvant aller jusqu'à l'arrachage de poils. Les atteintes dermatologiques, qu'elles soient d'origine bactérienne, parasitaire ou traumatique, provoquent prurit, automutilation, sensibilité accrue au contact ainsi qu'une irritabilité, voire de l'agressivité. Enfin, les affections neurologiques et musculo-squelettiques, qu'il s'agisse d'arthrose, de traumatismes ou d'encéphalitozoonose, réduisent les déplacements et peuvent induire isolement, agressivité ou dysorexie. Même les atteintes respiratoires ou cardiaques se manifestent parfois par des comportements trompeurs, tels qu'une apathie ou une diminution des interactions, facilement confondues avec une « dépression ».
IV. Problèmes comportementaux en lien avec l'état de santé des lapins
Inversement, certains comportements doivent alerter sur une possible origine médicale. L'agressivité, surtout lorsqu'elle apparaît brutalement, impose une recherche approfondie de douleur. La malpropreté doit toujours inciter à investiguer le système génito-urinaire ou l'appareil locomoteur (difficulté d'accès à la litière). Les comportements destructeurs, le pica ou la polyphagie peuvent être dus à l'ennui et à la frustration, mais aussi à des troubles digestifs ou carentiels. L'automutilation, souvent interprétée comme un trouble anxieux, peut traduire un prurit parasitaire ou une douleur neuropathique.
De nombreux troubles du comportement trouvent également leur origine dans un environnement inadapté : absence de congénères, manque d'espace, de cachettes, interactions humaines inappropriées. Le cercle vicieux est alors évident : un environnement pauvre génère peur, anxiété et frustration, qui entraînent pathologies médicales et comportements anormaux, lesquels aggravent à leur tour le stress.
V. Conclusion
Le comportement du lapin est un indicateur fiable de son état de santé. La frontière entre pathologie médicale et trouble comportemental n'est pas étanche : il s'agit de dimensions interdépendantes qui doivent être investiguées conjointement. Toute modification comportementale doit inciter à rechercher un problème organique et à évaluer la douleur, et toute pathologie médicale doit conduire à un examen attentif de l'environnement et du bien-être psychologique de l'animal. L'approche globale, intégrant médecine, éthologie et conditions de vie, est la seule qui permette d'assurer la santé et le bien-être durable des lapins de compagnie.
Bibliographie
- BRADBURY G. Behavioural Problems in Rabbits - A clinical approach. 5M publishing ; 2018.
- BRANDÃO J., GRAHAM J., QUESENBERRY K. Basic Approach to Veterinary Care of Rabbits. In: QUESENBERRY K. et al., 2020.
- CROWELL-DAVIS, S. Behavior problems in pet rabbits. Journal of Exotic Pet Medicine. 2007 ; 16, no. 1: 38–44. et CROWELL-DAVIS, S. Rabbit behavior. Vet Clin Exot Anim. 2021; 24 : 53–62.
- DI GIROLAMO N., SELLERI P. Disorders of the Urinary and Reproductive Systems. In: QUESENBERRY K. et al., 2020.
- DONNELLY T., VELLA D. Basic Anatomy, Physiology, and Husbandry of Rabbits. In: QUESENBERRY K. et al., Ferrets, Rabbits, and Rodents, 2020.
- FISHER P., KÜNZEL F., RYLANDER H. Neurologic and Musculoskeletal Diseases. In: QUESENBERRY K. et al., 2020.
- KWIK J, and al. Detection of maladaptive pain in dogs referred for behavioral complaints: challenges and opportunities. Frontiers in Behavioral Neuroscience. 2025 May 8;19:1569351.
- LENNOX A., MANCINELLI E. Respiratory Disease. In: QUESENBERRY K. et al., 2020.
- MILLS D, and al. Pain and Problem Behavior in Cats and Dogs. Animals 10, no.2. 2020; 318.
- OGLESBEE B., LORD B. Gastrointestinal Diseases of Rabbits. In: QUESENBERRY K. et al., 2020.
- ORCUTT C., MALAKOFF R. Cardiovascular Disease. In: QUESENBERRY K. et al., 2020.
- QUESENBERRY K., PILNY A., ST-VINCENT R. Lymphoreticular Disorders, Thymoma, and Other Neoplastic Diseases. In: QUESENBERRY K. et al., 2020.
- SMITH S. Gastrointestinal Physiology and Nutrition of Rabbits. In: QUESENBERRY K. et al., 2020.
- TYNES, V. The Interaction Between Behavioral and Physical Health in Rabbits. Veterinary Clinics of North America: Small Animal Practice 54, no.1. 2024 ; 169–79.
- VARGA M., PATERSON S. Dermatologic Diseases of Rabbits. In: QUESENBERRY K. et al., 2020.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Quand le lien maternel n'est pas là
Maisons-Alfort, France
I. Introduction
Le lien (ou plus exactement les liens) entre la mère et les petits est essentiel pour la survie, la santé physique et (comporte)mentale à court et à long terme des nouveau-nés. Ce lien est nutritionnel, immunitaire (via le transfert d'immunité passive d'origine colostrale), bactérien (pour l'établissement du microbiote digestif) et évidemment comportemental. Son absence doit donc être palliée, autant que possible.
II. Circonstances à risque
Le lien entre mère et jeunes risque de ne pas se développer chez les femelles primipares, en cas de dystocie, lors de césarienne et chez les mères stressées ou douloureuses en post-partum. L'intervention humaine peut également interférer avec le développement du lien : par exemple le lavage/séchage des nouveau-nés, en faisant disparaître l'odeur du liquide amniotique, est défavorable à la reconnaissance des petits par la mère ; une manipulation exagérée des nouveau-nés par l'Homme peut également perturber l'établissement du lien. Les femelles primipares ou stressées peuvent ne pas développer de lien maternel ou inversement nurser les petits de façon exagérée, les déplaçant continuellement, parfois jusqu'au cannibalisme, et refusant de s'allonger pour permettre aux nouveau-nés de téter.
III. Prise en charge de la douleur et du stress
La prise en charge de la douleur post-partum ne doit pas être négligée. Le passage d'agent analgésique dans le lait est très limité et les concentrations sanguines atteintes dans la circulation des nouveau-nés semble extrêmement limitées, de l'ordre de 1 à 10% de la dose administrée à la mère. Le butorphanol n'est pas recommandé. Le fentanyl et la morphine peuvent être administrés en surveillant tout signe de somnolence chez les petits. Parmi les anti-inflammatoires non stéroïdiens, le meloxicam n'est pas recommandé au-delà d'une administration unique lors de la césarienne ; le carprofène et le cimicoxib administrés à la chienne ne donnent qu'une faible exposition des jeunes via le lait. Un délai de 3 heures entre une injection intra-veineuse de tramadol et la tétée devrait être respecté. Pour la gestion du stress, l'acépromazine (0,01-0,02 mg/kg) présente en parallèle l'intérêt d'avoir un effet prolactinique, donc favorable à la synthèse de lait.
Veiller au calme et au confort du lieu d'élevage de la portée contribue également à l'établissement du lien mère-jeune.
IV. Prise en charge du lien immunitaire
En cas d'absence de synthèse de colostrum ou d'impossibilité de tétée au cours des 8 premières heures de vie, un substitut colostral peut être administré aux jeunes. Le plus efficace en termes de transfert de l'immunité colostrale est du colostrum (congelé) à raison d'1,5 ml/100 g chez le chiot. L'administration se fait au biberon ou mieux, par sondage orogastrique. Le sérum d'animal adulte n'a pas prouvé d'efficacité. Un substitut colostral partiel (lait maternisé canin/félin supplémenté en anticorps anti E. coli K99 et anti CPV2) peut également être utilisé aussi bien chez les chiots que chez les chatons (PUPPYPROTECH ND).
En cas de déficit de transfert de l'immunité passive (objectivé par exemple par une absence de prise de poids entre la naissance et 2 jours de vie), les jeunes doivent être élevés dans des conditions d'hygiène maximales, avec un apport énergétique important. Une vaccination précoce dès l'âge de 4 semaines est également possible, en raison de l'absence d'interférence vaccinale.
V. Prise en charge du lien nutritionnel
Que la chienne refuse de se mettre en position pour la tétée, qu'elle ne reste pas couchée suffisamment longtemps ou refuse la tétée en raison d'une douleur liée à une mammite, les apports nutritionnels devront être réalisés, totalement ou partiellement avec un lait maternisé. Néanmoins, les nouveau-nés seront laissés avec la mère pour le développement du lien comportemental. Lors de mammite, si des anti-inflammatoires non stéroïdiens sont administrés, leur concentration dans le lait est susceptible d'être très élevée en raison de la rupture de la barrière hématomammaire ; la tétée devrait alors être évitée.
En cas de production laitière insuffisante, on veillera à la mise à disposition d'eau, d'aliment appétent et à l'absence de douleur. Du métoclopramide (antidopaminergique prolactinique) à la dose anti-émétique peut être administré pendant 3 jours. Une administration systématique en fin de césarienne permet de stimuler la mise en route de la lactation. Lors de la première administration, le comportement de la mère vis-à-vis de sa portée sera surveillé, en raison de possibles effets extrapyramidaux.
Dans tous les cas, la prise de poids sera suivie à l'aide des courbes de croissance néonatales https://www.waltham.com/resources/puppy-growth-charts ; https://www.waltham.com/resources/kitten-growth-charts.
VI. Prise en charge de la mise en place du microbiote digestif
La contribution respective du colostrum/lait, de la peau, des fèces, de la salive de la mère et celle des bactéries de l'environnement dans le microbiote du nouveau-né n'est pas connue. Si la mère est absente, ou qu'elle n'assure pas l'alimentation de sa progéniture, le microbiote des jeunes nourris avec du lait maternisé est différent de celui des jeunes nourris avec le lait maternel. Les conséquences à court, moyen et long terme ne sont pas connues.
VII. Prise en charge comportementale
Si la mère n'assure pas un léchage efficace, une intervention humaine est nécessaire dès la naissance pour retirer la membrane amniotique, puis dans les jours suivants (jusqu'à 2-3 semaines de vie) pour déclencher miction et défécation avant ou après chaque repas.
La présence d'un autre adulte est importante pour l'apprentissage comportemental. La période cruciale de sociabilisation va de l'âge de 3 à 14 semaines. L'adulte doit avoir un comportement jugé approprié vis-à-vis de l'Homme et des animaux et, sur le plan sanitaire, être à jour de vaccination et de vermifugation.
VIII. Conclusion
Lorsqu'une chienne en fin de gestation ou des nouveau-nés lui sont présentés, le vétérinaire se concentre, voire se limite, souvent, à des conseils liés à la vaccination, à la vermifugation, éventuellement à la nutrition. Pourtant, un encadrement des propriétaires permettant d'accompagner le développement comportemental des jeunes permettra à ceux-ci d'être finalement plus équilibrés, diminuant ainsi le risque d'abandon ultérieur et améliorant la facilité à réaliser des soins sur ces animaux. Le conseil avant la mise à la reproduction d'une femelle fait aussi partie de l'accompagnement des propriétaires.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Quand les liens se distendent... Gestion des conflits internes
Chozeau, France
I.Introduction
Dans toute entreprise, qu'elle que soit sa taille, le tissu relationnel a le pouvoir d'être à la fois le moteur de la performance collective et mais également le maillon faible en terme de fragilité. À mesure que les équipes grandissent et que la complexité organisationnelle augmente, le nombre d'interactions explose de manière exponentielle. Or, là où il y a interactions, il y a inévitablement tensions, divergences, incompréhensions et parfois même conflits.
Les conflits interpersonnels ne sont pas nécessairement un signe de dysfonctionnement irrémédiable. Au contraire, lorsqu'ils sont identifiés et gérés à temps, ils peuvent devenir de puissants leviers de transformation, révélant des dysfonctionnements structurels, éclairant des angles morts organisationnels et ouvrant la voie à une communication plus claire et à une coopération renforcée. Mais laissés sans régulation, ils se transforment en spirales délétères qui altèrent la confiance, fragmentent les collectifs en laissant de graves séquelles et dégradent la qualité du travail.
II. Comprendre l'origine des tensions
Un conflit ne naît jamais de nulle part. Il prend racine dans des zones de friction préexistantes :
- les divergences de valeurs et de perceptions : chacun d'entre nous aborde la relation professionnelle à travers son propre système de référence. Lorsque les comportements d'autrui heurtent ce système, l'incompréhension se double de jugements et ouvre la voie au ressentiment ;
- la surcharge et le stress : des attentes clients, des délais contraints ou des pressions hiérarchiques nourrissent un climat de tension propice à l'escalade émotionnelle ;
- le manque de régulation : nier ou minimiser la présence de tensions, espérer qu'elles disparaissent d'elles-mêmes, c'est laisser s'installer les germes d'un futur conflit ;
- les difficultés de communication : imprécisions, non-dits et malentendus conduisent rapidement à une confusion entre le problème réel et la personne, ce qui rend la résolution plus difficile.
Il est essentiel de rappeler que les tensions ne sont pas toujours négatives : elles peuvent stimuler créativité, prise d'initiative et dépassement de soi. Mais lorsqu'elles se cumulent ou s'accentuent, sans prise en compte ou régulation adéquate, la situation peut dégénérer et évoluer rapidement en conflit.
III. L'escalade conflictuelle : quand l'autre devient « le problème »
Le conflit suit souvent une dynamique progressive. Tout commence par une émotion désagréable, déclenchée par un mot ou un acte perçu comme une transgression. Très vite, la situation objective est noyée sous une vague d'émotions, d'interprétation de l'intention et de biais. L'intention prêtée à l'autre devient plus importante que le fait réel. On passe de « il y a un problème » à « le problème, c'est l'autre ».
Cette évolution s'accompagne fréquemment de déshumanisation : l'autre est réduit à une étiquette négative (« incompétent », « de mauvaise foi », « toxique »). Dès lors, la possibilité d'un dialogue s'amenuise, et chaque geste ou parole, même anodins, devient source de nouvelle escalade.
IV. La résolution : agir vite et avec méthode
Contrairement à certaines croyances, un conflit ne s'éteint jamais de lui-même. Il s'interrompt, parfois, mais ne disparaît pas : il ressurgira tôt ou tard, parfois sous une forme amplifiée. C'est pourquoi la réactivité est essentielle.
Deux temporalités se conjuguent :
- le traitement à chaud : instaurer un « cessez-le-feu » immédiat pour stopper les hostilités, par exemple en réorganisant temporairement le travail ;
- la résolution à froid : prendre le temps, une fois la pression retombée, d'explorer les causes, de reconstruire un cadre de coopération et d'inventer de nouvelles règles de fonctionnement.
Cette démarche suppose plusieurs étapes clés : constater les faits objectivement, mesurer les écarts par rapport aux attentes, projeter les protagonistes vers l'avenir, définir de nouvelles règles, tester leur mise en œuvre et enfin en tirer un bilan.
V. Le rôle du manager et du tiers médiateur
Dans une équipe, la responsabilité du manager est centrale. Trop souvent, la tentation est grande de nier ou minimiser les tensions. Pourtant, c'est précisément par sa capacité à les réguler, à les prendre au sérieux et à intervenir rapidement qu'il protège la santé relationnelle du collectif.
Cependant, le manager ne peut pas toujours tout résoudre seul, surtout lorsqu'il est partie prenante du problème ou que les émotions sont trop cristallisées. Dans ce cas, le recours à un tiers neutre et formé à la médiation devient une ressource précieuse. La médiation ne vise pas à arbitrer, ni à imposer une solution, mais à restaurer la capacité des personnes concernées à redevenir acteurs d'une solution commune. Par sa posture d'impartialité et de neutralité, le médiateur facilite la réhumanisation des relations et permet de sortir de l'impasse.
VI. Prévenir plutôt que guérir
Si la gestion des conflits est un art, la prévention reste la clé. Cela passe par :
- la définition d'un cadre clair et équitable, de règles de vie partagées ;
- l'instauration et la valorisation d'une communication ouverte et respectueuse ;
- la régulation régulière des tensions inévitables.
Car, en réalité, une organisation sans tensions est une organisation qui s'éteint, où les individus se désengagent et peuvent devenir indifférents. Ce qui compte n'est pas d'éviter tout conflit, mais de cultiver une maturité collective qui permette de les traverser avec intelligence et d'en sortir renforcés.
VI. Conclusion
« Quand les liens se distendent… » n'est pas seulement une métaphore des difficultés relationnelles au travail. C'est un signal qu'il est urgent d'écouter. Derrière chaque tension se cache une opportunité de repenser le collectif, de clarifier le cadre, d'améliorer la coopération.
Loin de considérer le conflit comme une fatalité ou une menace, il peut être perçu comme une occasion de transformation. Une équipe résiliente n'est pas celle qui évite les conflits, mais celle qui sait les traverser sans se briser.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Quand les signes cutanés aident à affiner le diagnostic différentiel face à une atteinte digestive chez le Chien et le Chat
Marcy L'étoile France
Les signes cutanés peuvent être des indices précieux lorsque l’animal présente des troubles digestifs, qu’il s’agisse d’anorexie, de vomissements, de diarrhée chronique ou de perte de poids inexpliquée. Certaines affections systémiques ou dermatoses inflammatoires, métaboliques ou infectieuses s’accompagnent de manifestations dermatologiques qui orientent le clinicien. Une attention portée à la nature et à la distribution des lésions permet souvent d’affiner les hypothèses
1. Lésions buccales et ulcérations muqueuses
La cavité buccale est un site de prédilection pour de nombreuses affections systémiques. Chez le chat, l’herpèsvirose et la calicivirose provoquent des ulcères linguaux, labiaux ou palatins, souvent accompagnés d'une anorexie marquée. Ces signes peuvent être confondus avec ceux de maladies systémiques fébriles ou digestives. Les accidents médicamenteux peuvent également se manifester par des érosions ou ulcérations muqueuses, associées à des signes digestifs tels que des vomissements. Certaines formes de lupus systémique ou de pemphigus vulgaire présentent aussi des atteintes muqueuses buccales évocatrices.
2. Lésions ulcéronécrotiques douloureuses des extrémités
Chez le chien, le syndrome hépato-cutané (dermatose nécrolytique superficielle) est typiquement associé à une hépatopathie chronique ou à un glucagonome. Il se manifeste par des lésions ulcéronécrotiques douloureuses au niveau des points de pression (truffe, coussinets, zones de frottement), souvent accompagnées de vomissements et d’un amaigrissement marqué. Les signes cutanés sont souvent au premier plan et permettent de suspecter une origine digestive ou hépatique.
3. Lésions squameuses ou exfoliatives
Certaines affections systémiques telles que le lupus cutané exfoliatif, la dermatite exfoliative liée à un thymome ou les dermatoses paranéoplasiques peuvent se manifester par des squames diffuses et une alopécie non prurigineuse, parfois associées à une anorexie et un abattement. Ces lésions doivent alerter sur une possible atteinte hépatique, digestive ou tumorale.
4. Nodules, œdème et signes digestifs associés
Certaines maladies systémiques telles que la leishmaniose, l’histoplasmose ou la sporotrichose peuvent se présenter avec des nodules cutanés, parfois ulcérés, associés à des signes digestifs comme des vomissements, une diarrhée ou une anorexie. Le syndrome de Sweet-like (dermatose neutrophilique aiguë) et le syndrome de Wells-like (cellulite éosinophilique) s’accompagnent de plages œdémateuses, érythémateuses et douloureuses, souvent associées à de la fièvre et à des troubles digestifs secondaires.
5. Lésions kératosiques ou alopéciques liées à des désordres nutritionnels ou endocriniens
La dermatose répondant au zinc peut survenir secondairement à un syndrome de malabsorption ou à un déséquilibre nutritionnel, notamment chez les jeunes chiens en croissance. Elle se manifeste par une hyperkératose, des croûtes et une alopécie, parfois associées à des troubles digestifs modérés. Une hypothyroïdie peut également provoquer des lésions cutanées (alopécie bilatérale, hyperpigmentation) et s’accompagner d’une polyphagie et d’une perte de poids.
Les signes cutanés peuvent donc jouer un rôle important dans l’orientation diagnostique devant des signes digestifs. Leur reconnaissance clinique, combinée à une démarche diagnostique systémique, permet souvent de révéler des affections profondes et parfois graves.
Références
- Scott DW, Miller WH, Griffin CE. Muller and Kirk’s Small Animal Dermatology, 7th ed. Saunders Elsevier, 2013.
- Bizikova P, Linder KE, Anderson JG. Erosive and ulcerative stomatitis in dogs and cats: which immune-mediated diseases to consider? J Am Vet Med Assoc. 2023 Apr 17;261(S1):S48-S57.
- Thiry E, et al. Feline Herpesvirus Infection: ABCD Guidelines on Prevention and Management. J Feline Med Surg. 2009 Jul;11(7):547-55.
- Turek MM. Invited review – cutaneous paraneoplastic syndromes in dogs and cats: a review of the literature. Vet Dermatol 2003; 14: 279–296.
- Hensel P. Nutrition and skin diseases in veterinary medicine. Clin Dermatol. 2010 Nov-Dec;28(6):686-93.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Quand les signes cutanés aident à affiner le diagnostic différentiel face à une atteinte oculaire chez le Chien
Toulouse, France
I. Introduction
Certaines affections oculaires s'accompagnent de signes cutanés et/ou généraux qui peuvent aider au diagnostic de l'affection. Il peut s'agir de signes oculaires spécifiques comme une uvéite ou de signes moins spécifiques comme une blépharite ou encore une conjonctivite.
Connaitre ces affections et réaliser systématiquement un examen cutané et auriculaire complet va aider à mettre en place les bons examens complémentaires et affiner le diagnostic différentiel.
On distinguera les uvéites des blépharites
II. Lors d'uvéite
Il s'agit d'une inflammation de l'uvée antérieure ou postérieure ; elle génère une rougeur, un blépharospasme, un effet Tyndall et une baisse de la pression intraoculaire. Non traitée, elle peut avoir de graves conséquences comme un glaucome, des synéchies ou encore un décollement de rétine.
Nous allons porter notre attention sur deux affections oculo-cutanées à dominante uvéale.
1. Le syndrome uvéo-cutané
Improprement nommé syndrome de Vogt-Koyanagi-Harada (VKH) par analogie avec la médecine humaine, cette affection constitue une maladie auto-immune assez rare chez le chien [1]..
Cette dermatose auto-immune cible les mélanocytes et se caractérise par une uvéite granulomateuse grave, associée à des lésions cutanées dominées par de la dépigmentation. Contrairement à son équivalent humain, cette maladie chez le chien n'atteint que l'uvée et la peau. Chez l'homme, le VKH peut également affecter les mélanocytes du SNC (méningite), de la cochlée (surdité) et des cheveux. Récemment un chien a été décrit avec une méningite aseptique concomitante [2]
Les mécanismes étiopathogéniques exacts restent encore non élucidés. Un contexte génétique est suspecté à la fois chez l'homme mais également chez le chien pour qui l'Akita Inu est prédisposé. La cible demeure commune et il s'agit des mélanocytes et plus particulièrement certaines protéines impliquées dans la synthèse des pigments telle la tyrosinase ou le TRLP. Les antigènes rétiniens ont été évoqués comme cible de la réponse immunitaire. Néanmoins, ces antigènes ne sont pas forcément retrouvés en fonction du stade de la maladie (aigue versus chronique) et la synthèse d'anticorps pourrait résulter d'un relargage de ces protéines suite aux lésions rétiniennes accompagnant l'uvéite.
La prévalence chez le chien reste inconnue. La maladie est présente sur tous les continents, y compris dans les régions endémiques de leishmaniose.
Chez le chien, les signes oculaires précèdent souvent les signes cutanés, même si cette règle n'est pas absolue. Le délai d'apparition entre les deux topographies lésionnelles varie entre 12 et 20 semaines. Ainsi, les signes cutanés peuvent rapidement aider l'ophtalmologiste à affiner son diagnostic différentiel concernant la cause de l'uvéite. Celle-ci est souvent sévère et difficile à stabiliser ; elle s'accompagne souvent d'une cécité et de signes de glaucome (uvéite hypertensive). D'autres signes accompagnant l'uvéite sont fréquents comme la conjonctivite ou encore la cataracte. Les signes oculaires sont le plus souvent bilatéraux.
Les signes cutanés sont dominés par de la dépigmentation, de la poliose et de l'érythème.
Les lésions s'accompagnent également de croûtes, d'érosions et d'ulcères. Dans une publication, un chien a présenté une onychomadèse quelques semaines avant les signes cutanés classiques de VKH. Il est difficile de déterminer s'il s'agissait d'une coïncidence ou d'une manifestation de l'activation du système immunitaire (croisement antigénique). Les lésions sont majoritairement présentes sur la face, le planum nasale (86%), les paupières (74%), les babines (65%). Quelques chiens présentent des lésions dans la cavité buccale, les coussinets ou la zone génitale. Les lésions sont le plus souvent symétriques.
Les signes généraux sont inconstants et peuvent être en lien avec la douleur générée par l'uvéite ou par le glaucome. Certains ont présenté un port de tête penchée et une dysacousie. Comme précisé plus haut, une publication récente rapporte e cas d'un chien avec méningite aseptique concomitante [2].
Le diagnostic est établi sur la base d'un examen histopathologique cutané démontrant une infiltration sous-épidermique lichénoïde en bande majoritairement histiocytaire. Il est indispensable d'écarter préalablement une leishmaniose.
L'uvéite est souvent de mauvais pronostic et nombreux sont les cas ou les animaux ont dû être énucléés. Le traitement est basé sur l'utilisation d'immunomodulateurs à forte dose, en première ligne les corticoïdes, la cislosporine ou encore le mycophénolate mofétil.
2. La Leishmaniose
Il s'agit d'une maladie protéiforme entrainant une grande variété de signes cliniques. Parfois un seul symptôme est présent et il peut s'agir d'un simple ulcère des coussinets. Les signes cutanés sont fréquents et quasi systématiques. Lors de signes oculaires, la recherche et l'identification de ces signes cutanés permet d'aider au diagnostic.
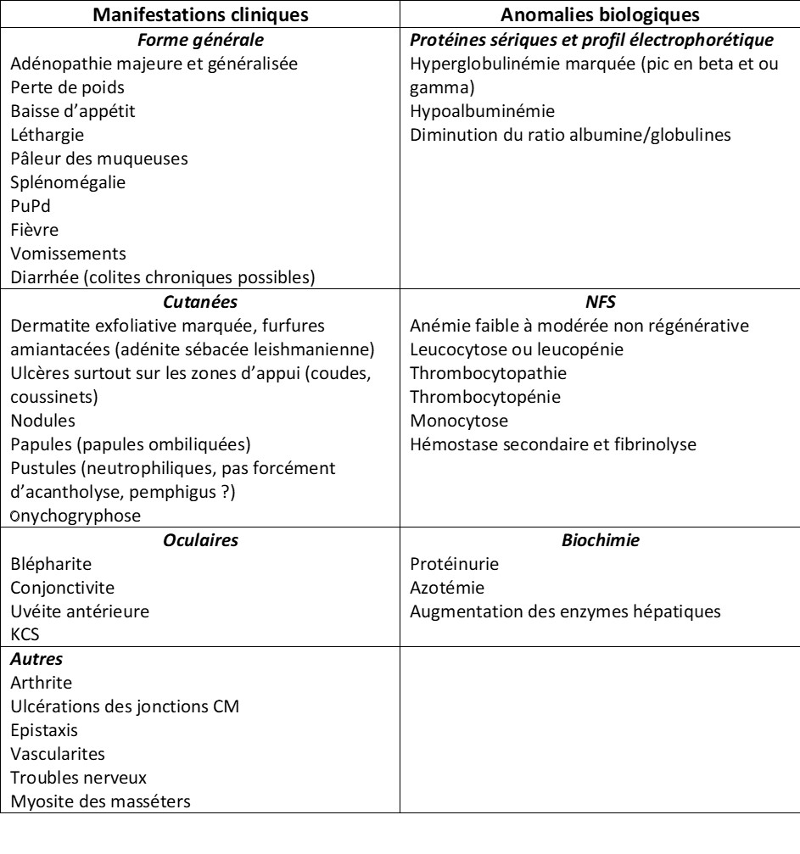
Figure 1 : les signes cliniques de leishmaniose
L'adénopathie est très fréquente, elle est présente dans 90% des cas, surtout en début d'évolution. Une colite pyogranulomateuse est présente chez plus d'¼ des chiens.
L'atteinte oculaire est fréquente (16-80% des cas) et pourrait être le seul signe dans 16% des cas. En phase chronique, la conjonctive est riche en parasites. Il s'agit d'un substrat intéressant et facile à prélever pour les études épidémiologiques en zone endémique (PCR sur cytobrosse).
L'atteinte rénale est systématique chez tous les chiens, mais l'expression est variable. L'évaluation rénale est un élément clé du pronostic et de la démarche thérapeutique. Elle conditionne la prise en charge.
En ce qui concerne les formes cutanées, la forme nodulaire est considérée comme de mauvais pronostic (Th2) et la forme papuleuse de bon pronostic (Th1) [3]. La forme pustuleuse est de description plus récente, mais est bien connue des praticiens vivant en zone endémique. Il s'agit de pustules neutrophiliques stériles plus ou moins acantholytiques.
III. Lors de blépharite
Les blépharites sont communes chez le chien et chez le chat. Il s'agit d'une inflammation de la région péri-oculaire qui peut s'accompagner d'autres signes oculaires, tels qu'une meibomite ou encore une conjonctivite.
Les ophtalmologistes peuvent être confrontés à des signes de blépharite qui sont souvent déroutants pour eux car il s'agit le plus souvent d'entités purement dermatologiques à manifestation palpébrales qu'ils n'ont pas forcément l'habitude de diagnostiquer et de traiter. L'analyse lésionnelle fine de l'atteinte palpébrale, associée à un examen précis des autres territoires cutanées ainsi que de la sphère auriculaire, est indispensable à l'établissement du diagnostic.
1. Démarche diagnostique lors de blépharite
La démarche diagnostique est identique à celle appliquée en dermatologie.
Comme l'ophtalmologie, la dermatologie est une discipline clinique au sein de laquelle la sémiologie tient une place de choix. Identifier justement les lésions cutanées est l'étape essentielle qui permet d'établir des hypothèses diagnostiques éclairées. Il ne sert à rien de multiplier les examens complémentaires en espérant que ces derniers apporteront une réponse. L'examen complémentaire ne doit servir qu'à confirmer une hypothèse étayée par des éléments cliniques.
Certaines lésions dominantes seront la clé permettant une première orientation diagnostique. D'autres examens seront alors nécessaires pour confirmer ou infirmer ce regroupement d'hypothèses.
2. Particularités diagnostiques de la blépharite
Il faut éviter les raclages en région palpébrale sur animal vigile. Pour le diagnostic de gale sarcoptique, il y a peu de chance de détecter les parasites. La sensibilité de ce test est de 20 à 50% sur 5-6 zones corporelles. En région palpébrale où la zone est difficile d'accès, la sensibilité est encore plus faible.
Pour le diagnostic de gale sarcoptique, d'autres zones corporelles pourront être prélevées ou une sérologie dosant les IgG spécifiques de Sarcoptes scabiei pourra être réalisée.
Pour la recherche de démodécie, il est préférable de privilégier un examen trichoscopique.
Lorsque des biopsies cutanées doivent être réalisées en vue d'un examen histopathologique, les fragments doivent être suffisamment larges pour être diagnostiques. Un trocart à biopsie de 6 mm sera le plus adapté. Durant le prélèvement, il faudra veiller à préserver la structure anatomique, il faudra éviter des biopsies qui occasionneront par la suite l'apparition de cicatrices vicieuses, en particulier dans la région du bord libre.
3. Un focus sera porté sur :
a) La blépharite atopique
Celle-ci est très fréquente. Non spécifique, elle est associée à d'importantes démangeaisons. Les lésions observées sont l'érythème, l'alopécie, les croûtes, les excoriations, la lichénification et l'hyperpigmentation. Les surinfections secondaires sont fréquentes, bactériennes ou fongiques ; elles sont superficielles ou de surface (Photo 1). Le diagnostic est permis par l'identification d'autres sites lésionnels et l'exclusion des imitateurs de la dermatite atopique. Il faut notamment s'affranchir d'une gale sarcoptique ou d'une démodécie.
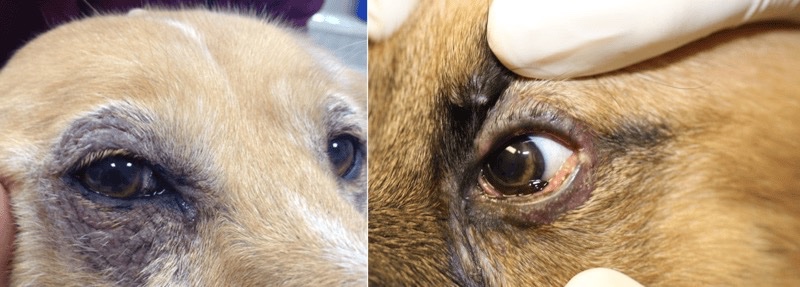
Photo 1
b) La cellulite juvénile
Il s'agit d'une dermatose dysimmunitaire pyogranulomateuse ciblant la zone péri-folliculaire près de l'isthme. Elle atteint surtout les jeunes chiens entre 3-6 mois, mais peut toucher le jeune adulte de moins de 3 ans le plus souvent. Elle est systématiquement associée à une altération de l'état général et une adénomégalie marquée rétro mandibulaire.
Les signes cutanés intéressent la face, le museau, les babines en épargnant la truffe, les paupières et la face interne des pavillons auriculaires.
Les signes oculaires sont dominés par une blépharite qui donne un aspect épaissi à la paupière sur toute la circonférence. Cette blépharite s'accompagne d'une meibomite marquée, d'une conjonctivite et d'un écoulement muco-purulent
Les signes oculaires peuvent évoluer seuls dans un premier temps, puis sont rapidement complétés par une atteinte des autres territoires cutanés précédemment cités.
Il est important de connaitre cette affection pour rapidement la traiter, car elle constitue une urgence vraie. Le traitement repose sur l'utilisation de corticoïdes à dose immunomodulatrice, plus ou moins associée à des antibiotiques. La ciclosporine peut être envisagée pour les cas réfractaires.
Bibliographie
- THAM HL, LINDER KE, OLIVRY T. Autoimmune diseases affecting skin melanocytes in dogs, cats and horses: vitiligo and the uveodermatological syndrome: a comprehensive review. BMC veterinary research. 2019;15(1):251.
- LAM JPM, ROZSA B, PAULIN MV, LUCYSHYN DR, GU J, COTTER B, et al. Uveodermatologic syndrome presenting with concurrent aseptic meningoencephalitis in a dog. The Canadian veterinary journal La revue veterinaire canadienne. 2025;66(2):130-7.
- ORDEIX L, SOLANO-GALLEGO L, FONDEVILA D, FERRER L, FONDATI A. Papular dermatitis due to Leishmania spp. infection in dogs with parasite-specific cellular immune responses. Veterinary dermatology. 2005;16(3):187-91.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Quand les signes cutanés aident à affiner le diagnostic différentiel face à une atteinte respiratoire chez le Chat
Toulouse, France
I. Introduction
Chez le chat, les signes respiratoires et cutanés/auriculaires peuvent évoluer dans une même affection, amenant les signes cutanés et auriculaires à constituer une aide au diagnostic.
Trois exemples vont être présentés dans cette conférence.
II. Les polypes nasopharyngés
Le polype auriculaire inflammatoire est un nodule d'origine bénigne prenant naissance au niveau de l'épithélium tapissant la bulle tympanique, le nasopharynx ou la trompe d'Eustache.
Le polype peut être aisément visualisé dans l'ouverture du conduit auriculaire, facilitant son retrait par traction externe. Le polype peut également s'étendre dans la portion médiale de la bulle tympanique et au-delà. Le polype peut aussi être confiné à la bulle tympanique, sans s'étendre au niveau du conduit auriculaire.
Les polypes auriculaires inflammatoires sont le plus souvent unilatéraux, bien qu'une étude récente rapporte une atteinte bilatérale dans 24% des cas [1]. Les jeunes chats sont préférentiellement atteints, mais des polypes peuvent être observés à tout âge.
Les chats atteints de polype inflammatoire peuvent initialement présenter une otite infectieuse bactérienne externe ne répondant pas à un traitement bien conduit.
Les symptômes observés sont ceux d'une otite externe et/ou d'une otite moyenne, auxquels peuvent se rajouter des symptômes respiratoires, écoulements oculaires, blépharospasme. On peut constater des ronflements, une modification de la voix…
S'ils sont visibles à l'examen otoscopique, les polypes se présentent comme des nodules roses/rouges lisses faisant protrusion dans le conduit auriculaire au niveau du tympan. Un examen tomodensitométrique est recommandé pour déterminer l'extension du polype, confirmer le diagnostic et explorer une éventuelle atteinte bilatérale. Certains polypes ne sont en effet identifiés qu'après réalisation d'un scanner ou d'une vidéo-otoscopie.
En zone rhinopharyngée, il est rare d'observer les polypes sur un simple examen de l'arrière-gorge.
Le diagnostic définitif nécessite la réalisation d'un examen histopathologique après exérèse.
Le traitement repose sur la traction-avulsion ou sur l'ostéotomie ventrale de la bulle tympanique. Dans les deux cas, des effets indésirables peuvent se produire après intervention (syndrome de Claude Bernard Horner, symptômes vestibulaires, hémorragie et paralysie du nerf facial). La bullotomie ventrale est une intervention plus invasive et peut entraîner un plus grand nombre de réactions indésirables. Le risque de récidive semble cependant plus élevé avec la technique de la traction-avulsion (jusqu'à 67% selon les études) qu'avec la bullotomie ventrale (5%) [2]. L'administration de corticoïdes après traction-avulsion permet d'éviter les récidives dans 100% des cas traités [2-4].
Deux autres techniques ont été décrites :
- Technique trans-tympanique per-endoscopique pour le retrait des polypes par traction suivi d'un curetage de la bulle. Cette technique résulterait en un taux de récidive plus faible (13,5%) que la traction-avulsion classique [3].
- Approche latérale au conduit auriculaire suivie par traction-avulsion profonde. Le taux de récidive semble varier avec l'expérience du chirurgien (de 14 à 35%) [4].
III. Les rhino-sinusites chroniques
Des otites moyennes (OM) primaires bactériennes ou stériles sont de plus en plus décrites chez le chat. Ces otites peuvent évoluer dans un contexte d'inflammation rhino-pharyngée ou rhinosinusale. Ces rhino-sinusites, le plus souvent infectieuses et chroniques (syndrome coryza), créent une inflammation ORL à l'origine d'un défaut de drainage par la trompe d'Eustache et d'une accumulation de sérosités dans la bulle tympanique. Au départ stérile, ces otites moyennes peuvent se compliquer d'une surinfection bactérienne. Lorsque ces OM sont stériles, le contenu de la bulle est gélatineux et blanchâtre et évoque le contenu des OM séreuses primaires observées surtout chez les races brachycéphales et les CKC. Il est indispensable de faire un examen tomodensitométrique pour diagnostiquer l'OM et ses complications, mais également pour identifier les lésions de rhino-sinusites associées.
Ces otites moyennes peuvent générer de la douleur, du prurit cervical, un port de tête, un syndrome vestibulaire, une paralysie faciale, un syndrome de Claude Bernard Horner ou encore de la surdité. Elles peuvent secondairement se compliquer d'une otite externe, le plus souvent bactérienne et suppurée.
Le traitement consiste à traiter la rhino-sinusite, puis à traiter l'otite moyenne par chirurgie (bullotomie ventrale) ou médicalement.
Les otites moyennes sans lyse osseuse combinent deux traitements :
- Une paracentèse qui permet de vidanger et réaliser un examen bactériologique avec antibiogramme. Celle-ci doit se réaliser dans le cadran caudo-ventral du tympan et doit se faire sous vidéo-otoscopie. Par la présence du septum quasi-complet, seule la vidange de la partie dorsale peut se faire par les voies anatomiques. Certains confrères développent des techniques avec des endoscopes pour léser le septum et permettre la vidange de la partie ventrale.
- Un traitement antibiotique ciblé le plus souvent à base d'amoxicilline acide clavulanique ou de céfalexine ou de quinolones. Il est couplé à une corticothérapie qui permet de lutter contre l'inflammation et favoriser le drainage des sécrétions via la trompe d'Eustache.
Récemment, une publication a rapporté le traitement de 26 chats présentant une otite moyenne uni ou bi (54%) latérale. Ces animaux ont fait l'objet d'un flush avec 0,5 ml-2 ml de soluté physiologique tiédi après paracentèse. Les animaux ont reçu une antibiothérapie découlée de l'examen bactériologique et une corticothérapie per os 30 jours. Dans cette étude, 73% des oreilles ont montré une guérison clinique et 19% ont fait l'objet d'une bullotomie ventrale. Néanmoins, aucun examen d'imagerie de contrôle n'a permis de confirmer la guérison de l'OM [5].
IV. L'asthme allergique
Cette entité réputée allergique se traduit par de la toux, des sifflements et des épisodes de détresse respiratoire. Sur le plan diagnostique, les critères sont basés sur la mise en évidence d'une inflammation éosinophilique de l'arbre respiratoire.
Dans un certain nombre de cas, des signes cutanés peuvent être présents. Dans une étude publiée en 2011 chez une cohorte de chats présentant des signes cutanés d'hypersensibilité, 6% présentaient des signes respiratoires de type toux ou éternuements. Les manifestations cutanées étaient variées et regroupent les patterns réactionnels félins connus tels que le prurit cervico-facial, l'alopécie extensive, la dermatite miliaire ou encore le complexe granulome éosinophilique félin.
Plus récemment, une analyse sur les syndromes atopiques félins a montré la présence de signes non cutanés, dont la fréquence est difficile à déterminer. À partir d'une analyse sur 230 cas de chats « atopiques », 19/230 soit 8,3% présentaient des signes respiratoires dont 3 des signes d'asthme, 5 des éternuements et 11 des signes respiratoires non spécifiques [7].
Il peut être pertinent de rechercher des sensibilisations aux aéroallergènes par tests intradermiques et de pratiques une désensibilisation. Les réactions sont souvent fugaces et moins œdémateuses que chez le chien et peuvent nécessiter d'avoir recours à l'injection IV de fluorescéine pour les révéler. Les résultats d'efficacité de la désensibilisation avec un protocole classique donne des résultats comparables à ceux observés chez le chien [8].
Bibliographie
- HOPPERS SE, MAY ER, FRANK LA. Feline bilateral inflammatory aural polyps: a descriptive retrospective study. Veterinary dermatology. 2020;31(5):385-e102.
- ANDERSON DM, ROBINSON RK, WHITE RA. Management of inflammatory polyps in 37 cats. The Veterinary record. 2000;147(24):684-7.
- GRECI V, VERNIA E, MORTELLARO CM. Per-endoscopic trans-tympanic traction for the management of feline aural inflammatory polyps: a case review of 37 cats. Journal of feline medicine and surgery. 2014;16(8):645-50.
- JANSSENS SD, HAAGSMAN AN, TER HAAR G. Middle ear polyps: results of traction avulsion after a lateral approach to the ear canal in 62 cats (2004-2014). Journal of feline medicine and surgery. 2017;19(8):803-8.
- DELEPORTE S, BRIAND A, PRELAUD P. Clinical outcome of cats with suppurative otitis media and intact tympanum submitted to myringotomy: retrospective findings from 26 cases. Journal of feline medicine and surgery. 2024;26(9):1098612x241275286.
- HOBI S, LINEK M, MARIGNAC G, OLIVRY T, BECO L, NETT C, et al. Clinical characteristics and causes of pruritus in cats: a multicentre study on feline hypersensitivity-associated dermatoses. Veterinary dermatology. 2011;22(5):406-13.
- SANTORO D, PUCHEU-HASTON CM, PROST C, MUELLER RS, JACKSON H. Clinical signs and diagnosis of feline atopic syndrome: detailed guidelines for a correct diagnosis. Veterinary dermatology. 2021;32(1):26-e6.
- BREMENT T, VIAUD S, VIDEMONT E, BENSIGNOR E, editors. Results of intradermal testing and effect of specific allergen immunotherapy on medication needs in cats with atopic skin syndrome: 89 cases. 33th Annual Congress of the ECVD-ESVD 2022 29 September - 1 October; Porto, Portugal.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Quand les signes cutanés aident à affiner le diagnostic différentiel face à une hyperthermie chez le chien et le chat
Marcy-L'Étoile, France
I. Introduction
L'hyperthermie est un motif fréquent de consultation, souvent interprétée comme le reflet d'un processus infectieux systémique. Cependant, certains signes cutanés, souvent négligés, peuvent s'avérer être des éléments clés du diagnostic différentiel. Reconnaître ces manifestations permet non seulement d'orienter plus rapidement les examens complémentaires, mais aussi d'établir un diagnostic plus précis.
II. Pustules et croûtes
Chez un animal présentant de l'hyperthermie, l'observation de pustules et croûtes doit en premier lieu faire penser à un pemphigus foliacé, maladie auto-immune la plus fréquente chez le chien et le chat. Elle se manifeste par des croûtes, des pustules ou des érosions localisées sur le chanfrein, les pavillons des oreilles, les extrémités, souvent accompagnées d'une fièvre, d'un abattement et d'une anorexie. Le diagnostic reposera sur l'examen cytologique sous-crustacé et l'examen histopathologique de biopsies cutanées.
III. Nodules cutanés
La présence de nodules cutanés douloureux, ulcérés ou fistulisants, doit orienter vers des infections profondes. La nocardiose, la tuberculose cutanée, ou les infections à mycobactéries atypiques (chez le chat notamment) entraînent des lésions inflammatoires profondes associées à une fièvre prolongée. Les mycoses profondes comme la sporotrichose ou l'histoplasmose se présentent également sous forme de nodules ulcérés, souvent drainants, en particulier chez les chats immunodéprimés. Certaines formes de panniculite (notamment d'origine infectieuse ou stérile) peuvent aussi générer des nodules associés à de l'hyperthermie.
IV. Furoncles et cellulites
Les furoncles et cellulites s'observent dans des pyodermites profondes généralisées ou des pyodermites post-shampoing à Pseudomonas aeruginosa. Certaines pseudopyodermites sont également caractérisées par des furoncles ou des plaques : la cellulite juvénile ou la furonculose éosinophilique du chien. Ces dermatoses peuvent s'accompagner d'hyperthermie, de douleur marquée et parfois d'une altération de l'état général. Le syndrome de WELLS (cellulite éosinophilique) et le syndrome de SWEET (dermatose neutrophilique aiguë fébrile) se traduisent par des plaques œdémateuses, érythémateuses, douloureuses, associées à une fièvre aiguë.
V. Érosions, ulcères et nécrose
Chez le chat, certaines maladies virales comme l'herpèsvirose, la calicivirose ou la poxvirose provoquent des ulcérations buccales, nasales ou cutanées, souvent accompagnées de fièvre et de signes systémiques. Le syndrome hépatocutané du chien peut s'exprimer par des lésions ulcéronécrotiques douloureuses, localisées sur les zones de pression et les jonctions mucocutanées. La fasciite nécrosante doit être suspectée en présence de lésions nécrotiques étendues, chaudes, très douloureuses et rapidement évolutives. Enfin, des ulcères peuvent aussi être présents dans le lupus érythémateux systémique, lors de vasculite ou lors de leishmaniose, accompagnées d'un état fébrile et d'un abattement.
VI. Squamosis
Chez le chien, la leishmaniose peut s'exprimer par une desquamation diffuse souvent associée à une fièvre intermittente. Le lupus cutané exfoliatif induit des squames adhérentes, parfois généralisées. Chez le chat, une dermatite exfoliative liée à un thymome doit être évoquée en cas de desquamation sévère, généralisée, associée à une hyperthermie.
En conclusion, la diversité des signes dermatologiques associés à une hyperthermie impose une analyse rigoureuse des lésions cutanées : leur type (pustule, nodule, ulcère…), leur distribution et leur localisation sont des éléments clés pour établir les hypothèses diagnostiques. Une démarche diagnostique rigoureuse s'appuyant sur des examens cytologiques, histopathologiques, microbiologiques ou moléculaires permet d'orienter rapidement vers un traitement étiologique adapté.
Bibliographie
- SCOTT DW, MILLER WH, GRIFFIN CE. Muller and Kirk's Small Animal Dermatology, 7è ed. Saunders Elsevier, 2013.
- JORDAN TJM, BIZIKOVA P. Canine and Feline Pemphigus Foliaceus-an Update on Pathogenesis and Treatment. Vet Clin North Am Small Anim Pract. 2025 Mar;55(2):321-336.
- THIRY E, et al. Feline Herpesvirus Infection: ABCD Guidelines on Prevention and Management. J Feline Med Surg. 2009 Jul;11(7):547-55.
- TUREK MM. Invited review – cutaneous paraneoplastic syndromes in dogs and cats: a review of the literature. Vet Dermatol 2003; 14: 279–296.
- FACCIN M, et al. Common superficial and deep cutaneous bacterial infections in domestic animals: A review. Vet Pathol. 2023 Nov;60(6):796-811.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Quels liens entre chanvre et douleur ?
Mont-Saint-Aignan, France
I. Introduction
Le chanvre (Cannabis sativa L.), appartenant à la famille des Cannabaceae, est cultivé et utilisé depuis des millénaires, notamment pour la fabrication de papier, l'alimentation ou encore les textiles. Il contient plus de 500 composés chimiques, parmi lesquels figurent les phytocannabinoïdes, les terpènes, les flavonoïdes ainsi que des acides gras, dont certains de la famille des oméga-3.
L'usage médical du chanvre est également ancien : les premières mentions remontent à 2900 av. J.-C. en Chine, au sein de remèdes traditionnels. On retrouve également des références dans l'Égypte ancienne ou encore chez Pline l'Ancien, qui décrivait ses propriétés antalgiques. Au fil de l'histoire, le chanvre a ainsi été employé dans des contextes variés, tels que le traitement de l'insomnie ou des migraines.
Malgré un cadre réglementaire complexe, l'utilisation du chanvre et de ses dérivés connaît aujourd'hui un essor croissant, en médecine humaine comme vétérinaire. En pratique vétérinaire, la gestion de la douleur représente l'un des principaux motifs de recours mentionnés par les propriétaires, et constitue un domaine d'investigation scientifique en plein développement.
II. Rappels sur la douleur
La douleur est une expérience sensorielle et émotionnelle désagréable, associée ou semblant être associée à une lésion tissulaire réelle ou potentielle. Elle intègre ainsi des composantes sensorielles, physiologiques, cognitives, motivationnelles et affectives. Trois grands types sont distingués.
La douleur nociceptive, liée à une lésion tissulaire, résulte de la libération de médiateurs tels que l'histamine, la sérotonine, les prostaglandines ou encore certaines cytokines pro-inflammatoires, qui activent des nocicepteurs périphériques. Le signal est transmis par des fibres afférentes à la moelle épinière puis relayé au thalamus puis au cortex.
La douleur neuropathique survient à la suite d'une lésion ou d'une pathologie du système nerveux et correspond à une transmission anormale de l'information entrainant des perceptions douloureuses inappropriées.
Enfin, la douleur nociplastique est un terme utilisé pour décrire une douleur qui survient ou est maintenue par une nociception altérée, malgré l'absence de lésion tissulaire.
III. Composition nutritionnelle du chanvre et modulation de la douleur/inflammation
Avant même de s'intéresser aux phytocannabinoïdes, il convient de rappeler que d'autres familles de molécules présentes dans le chanvre pourraient également jouer un rôle dans la modulation de la douleur.
Les graines de chanvre renferment en moyenne 25% de protéines, 38% de glucides et 25% de lipides. Parmi ces derniers, 30 à 80% sont polyinsaturés et environ 10% mono-insaturés, ce qui en fait une source notable d'oméga-3. Leur rapport oméga-6/oméga-3 (4:1) est particulièrement intéressant, grâce à des teneurs élevées en acide linoléique (oméga-6) et en acide α-linolénique (oméga-3). Dans le cadre de l'inflammation, les nocicepteurs sont sensibilisés par des médiateurs pro-inflammatoires. Agir sur l'inflammation peut diminuer la sensation de douleur. [1]
Le chanvre contient également d'autres familles de composés susceptibles de participer à la modulation de la douleur.
Les terpènes, suscitent un vif intérêt pour leur rôle potentiel dans la modulation des processus impliqués dans la douleur chronique. Des molécules comme le pinène ou encore le linalool pourraient présenter des propriétés antalgiques ou anti-inflammatoires [2].
Les flavonoïdes présentent diverses propriétés, notamment anti-inflammatoires. La cannflavine présente dans le chanvre pourrait participer à la médiation de l'activité inflammatoire en ciblant notamment les récepteurs TLR [3].
Et enfin, les alcaloïdes, comme la caféoyltyramine, semblent avoir une action antioxydantes mais le focus scientifique n'est encore que faible à ce sujet
IV. Le système endocannabinoïde, phytocannabinoïdes et modulation de la douleur
Les plus connues des molécules bioactives du chanvre sont les cannabinoïdes, composés caractéristiques du Cannabis sativa L, notamment le tétrahydrocannabinol (THC), prédominant dans le cannabis récréatif, le cannabidiol (CBD) mais aussi le CBDA (acide cannabidiolique) [4].
La découverte du THC dans les années 1960 comme principal constituant psychoactif du Cannabis sativa L. a conduit à l'étude de ses mécanismes d'action. Au début des années 1990, les récepteurs cannabinoïdes (CB1 et CB2) sont identifiés, ainsi que l'existence de ligands endogènes correspondants, désormais connus sous le nom d'endocannabinoïdes. Les deux principaux, le N-arachidonyléthanolamide (anandamide, AEA) et le 2-arachidonoylglycérol (2-AG), sont aujourd'hui les mieux décrits.
Le système endocannabinoide est exprimé à la fois dans les voies ascendantes et descendantes liés à la douleur. Les récepteurs CB1 se trouvent notamment dans le système nerveux central, dans les circuits de la douleur descendante, du stress, de la peur et de l'anxiété. Les récepteurs se trouvent notamment aux terminaisons périphériques et centrales des neurones afférents primaires et au niveau du ganglion de la racine dorsale. Le récepteur CB2 se retrouve majoritairement en périphérie, avec une forte expression dans le système immunitaire. Mais il est aussi exprimé dans une moindre mesure dans le cortex cérébral, ou encore le cervelet, notamment lors de conditions inflammatoires. L'action des cannabinoïdes ne se limite toutefois pas à ces récepteurs (action sur les récepteurs TRPV ou PPAR). Les cannabinoïdes se lient de façon compétitive aux différents récepteurs, modulant la libération de neurotransmetteurs (noradrénaline, acétylcholine, GABA) et peuvent influencer la sécrétion de peptides tels que les β-endorphines. Le ciblage de ce système, via l'augmentation des endocannabinoïdes ou l'administration de ligands exogènes, permet de réduire la transmission nociceptive.
Enfin, les endocannabinoïdes, synthétisés « à la demande » par les neurones postsynaptiques en réponse au stress ou à une stimulation nociceptive, exercent des effets antinociceptifs transitoires. Ils participent ainsi au contrôle de l'initiation et de la résolution de la douleur, mais aussi au phénomène d'analgésie induite par le stress.
Le CBD est particulièrement pléiotrope, avec plus de 76 cibles moléculaires identifiées. Certaines de ces voies sont couplées aux récepteurs opioïdes, à la sérotonine ou à la dopamine, ce qui peut contribuer à ses effets analgésiques et neuromodulateurs.
V. Quelles données cliniques chez le chien et le chat
Peu de données sont encore disponibles sur les effets et l'efficacité des flavonoïdes ou terpènes chez l'animal de compagnie, notamment dans le cadre de la douleur. La majorité des études se tourne vers le CBD et le CBDA, qui sont principalement étudiés et utilisés dans la prise en charge de la douleur chronique, notamment liée à l'arthrose [4]. Chez le chien, l'analyse du liquide synovial a révélé une concentration plus élevée de 2-AG dans les articulations arthrosiques que dans les articulations saines, suggérant une implication du système endocannabinoïde dans la modulation de la douleur. Plusieurs études cliniques ont évalué l'administration orale de CBD dans ce contexte : certaines rapportent une diminution significative de la douleur et une augmentation de l'activité locomotrice dans une approche multimodale, mais les résultats restent hétérogènes. L'efficacité clinique est encore incertaine malgré une tolérance généralement acceptable.
Les données associées à la douleur postopératoire aiguë canine et dans les cas de cancers sont également rares et contrastées.
Chez le chat, l'utilisation du CBD par voie orale dans le cadre d'un traitement multimodal, notamment lors de gingivostomatite chronique avec extraction dentaire, semble présenter un intérêt thérapeutique, tout comme dans l'arthrose féline. Toutefois, le nombre d'études disponibles reste limité et ne permet toujours pas, à ce stade, de tirer des conclusions solides.
VI. Les limites à l'utilisation et perspectives
Bien que certaines données suggèrent un rôle bénéfique du chanvre dans la prise en charge de la douleur, l'hétérogénéité des protocoles publiés – qu'il s'agisse des voies d'administration (orale, transmucosale, etc.) ou des posologies – impose au clinicien une interprétation prudente. Contrairement à une perception parfois véhiculée chez certains propriétaires, l'usage du chanvre et de ses dérivés n'est pas exempt d'effets indésirables, tels que vomissements, selles molles ou élévation des enzymes hépatiques. Plus d'études cliniques, notamment chez le chat, sont encore nécessaires pour tirer de réelles recommandations pratiques pour ces différentes molécules. Par ailleurs, la complexité du cadre réglementaire et l'incertitude concernant la composition et la concentration des produits disponibles amènent à considérer d'autres molécules modulant le système endocannabinoïde, comme le palmitoyléthanolamide (PEA) [5].
Conclusion
Le chanvre constitue une plante d'un intérêt pharmacologique croissant, dont les composés bioactifs – phytocannabinoïdes, terpènes, flavonoïdes et acides gras polyinsaturés – offrent des perspectives prometteuses dans la modulation de la douleur. Le système endocannabinoïde apparaît comme une cible privilégiée, et les fréquentes nouvelles données suggèrent un rôle potentiel du CBD et du CBDA dans la gestion de la douleur chronique chez le chien et le chat. Toutefois, l'hétérogénéité des protocoles disponibles, la variabilité des formulations et le manque de standardisation des doses limitent aujourd'hui la transposabilité de ces résultats en pratique vétérinaire courante. L'évaluation scientifique rigoureuse, à travers des études contrôlées, reste indispensable pour déterminer l'efficacité, la sécurité et la place réelle des dérivés du chanvre dans les stratégies multimodales de prise en charge de la douleur.
Bibliographie
- KAMLE M. et coll. Nutraceutical potential, phytochemistry of hemp seed (Cannabis sativa L.) and its application in food and feed: a review. Food Chem. Adv. 4, 100671; 2024.
- ALFIERI A. et coll. Phytochemical Modulators of Nociception: a Review of Cannabis Terpenes in Chronic Pain Syndromes. Pharm. Basel Switz. 18, 1100; 2025.
- FITZPATRICK JMK., et coll. Cannflavin A inhibits TLR4-induced chemokine and cytokine expression in human macrophages. Nat. Prod. Res. 1–7; 2024.
- MIRANDA-CORTÉS A. et coll. The role of cannabinoids in pain modulation in companion animals. Front. Vet. Sci. 9, 2023.
- DELLA ROCCA G., GAMBA D. Chronic Pain in Dogs and Cats: is There Place for Dietary Intervention with Micro-Palmitoylethanolamide? Animals 11, 952; 2021.
Liens d'intérêt : Travail en tant que responsable technique pour Dômes Pharma de 2020 à 2021. Actuellement en cours d'encadrement d'une thèse universitaire sur le sujet du CBD chez le chien (université de Nanterre).
📃 Quoi de neuf en pharmacovigilance chez les animaux de compagnie en 2025 ?
Sandrine ROUGIER, DMV
Département Surveillance du marché et Pharmacovigilance, Anses-ANMV
La pharmacovigilance vétérinaire consiste en la surveillance des effets indésirables survenant chez l’animal et susceptibles d’être dus à des médicaments vétérinaires ou humains, mais également de ceux survenant chez l’Homme après utilisation d’un médicament vétérinaire. La pharmacovigilance correspond ainsi au suivi post-AMM du médicament et permet de compléter la connaissance que l’on a sur le médicament.
L’objectif principal de la pharmacovigilance est ainsi la génération précoce d’hypothèses (appelés signaux) relatifs aux effets indésirables des médicaments.
Un signal est une information provenant d'une ou de plusieurs sources, qui suggère une relation à ce jour inconnue ou non documentée, ou un nouvel aspect d'une relation connue, entre un médicament et un événement ou un ensemble d'événements reliés, qu'ils soient indésirables ou bénéfiques, mais qui est jugée suffisamment probable pour justifier une action de vérification. Il s’agit donc de la détection d’un nouveau « couple » Evènement indésirable / Médicament… mais pas seulement.
La surveillance des médicaments vétérinaires est réalisée à l’échelle européenne, mais également à l’échelle nationale pour tous les médicaments avec AMM en France. Le processus est continu tout au long de l’année, pour tout médicament autorisé. Il est assuré à la fois par les laboratoires pour leurs produits et également par les agences nationales.
En cas d'incidence sur le rapport bénéfice/risque du médicament vétérinaire concerné, sur la santé et le bien-être des animaux ou la santé publique, ou sur la protection de l'environnement, diverses mesures pourront être mise en œuvre, depuis une simple surveillance lorsque le signal tend à être confirmé, à une modification du RCP, voire à une suspension du médicament dans les cas les plus à risque.
Un bilan des signaux les plus marquants sur l’année 2025 et touchant les carnivores domestiques seront détaillés lors de la présentation.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Reconstruction prothétique de la mâchoire après mandibulectomie partielle chez le chien et le chat : à propos de 2 cas
Introduction
Les cancers de la cavité orale représentent 3 à 12 % des cancers chez le chat et 6 % chez le chien. Pour les tumeurs impliquant la mandibule, le traitement fait appel à une mandibulectomie partielle ou totale en fonction de la nature et de l'étendue de la masse, associée ou non à une chimiothérapie ou radiothérapie. La mandibulectomie est relativement bien tolérée par les chiens et les chats. Cpendant suivant l'importance de la résection, des difficultés à la prise alimentaire, une gêne liée à l'interférence entre les dents et un changement esthétique peuvent se produire. Pour limiter ces complications, une reconstruction prothétique de la mandibule peut être envisagée. Le but de cette présentation est de décrire deux cas traités par cette technique et leur suivi à moyen terme.
Matériel et résultats
Caline est une chatte de 11 ans présentée en consultation suite à une récidive de sarcome de la lèvre inférieure droite retirée par son vétérinaire traitant 1 mois auparavant. L'examen clinique révèle un nodule d'environ 6 mm au niveau de la babine inférieure droite.
Biba est une Golden Retriever de 6,5 ans présentée en consultation pour une masse bourgeonnante (carcinome épidermoïde) de 4 cm de longueur, localisée au niveau de la carnassière inférieure droite.
Le scanner de Caline montre un tissu gingival focalement épaissi (7,7 mm de diamètre) et réhaussant entre les dents 404 et 407 sans atteinte osseuse visible. Celui de Biba révèle une masse gingivale agressive provoquant une lyse osseuse centrée sur la dent 409. Le nœud lymphatique mandibulaire médial droit est le nœud lymphatique sentinelle primaire.
Une mandibulectomie partielle associée à une reconstruction prothétique a été proposée et acceptée par les propriétaires. Des guides de coupe et la prothèse mandibulaire ont été réalisés à partir des images scanner. La mandibulectomie partielle s'étendait de la symphyse mandibulaire jusqu'en arrière des dernières molaires du côté droit. La prothèse en titane a été fixée avec des vis en titane (de 2 mm de diamètre pour Caline et 2,7 mm pour Biba) sur la partie caudale de la mandibule droite et sur la partie crâniale de la mandibule gauche.
Les résultats histologiques révèlent un sarcome des tissus mous peu différencié à différenciation myoïde s'étendant aux marges de l'exérèse et avec une infiltration osseuse pour Caline et un carcinome épidermoïde mandibulaire bien différencié mais infiltrant, de grade de malignité intermédiaire, à marges chirurgicales exemptes pour Biba.
Une bonne occlusion dentaire a été obtenue dans les 2 cas. Une sonde d'œsophagostomie a été placée pour éviter une alimentation orale pendant 10 jours et limiter les risques de lâchage de suture.
Dix jours après la chirurgie, Caline s'alimente normalement et présente une bonne cicatrisation intrabuccale. À 10 jours postopératoire, Biba présente un lâchage de suture partiel rostralement laissant apparaître la prothèse sur 3 cm de longueur. Un lambeau gingival est réalisé 2 semaines plus tard ainsi qu'un avancement de la commissure pour limiter le fait que la langue ne tombe du côté de la prothèse.
Le contrôle de Caline à 1 an postopératoire montre une parfaite occlusion, aucun signe de récidive locale et aucun rejet de la prothèse. Le contrôle de Biba à 4 mois postopératoires montre une exposition de la prothèse en région caudale sur environ 6 cm sans gêne associée, la partie crâniale ayant parfaitement cicatrisé, une occlusion dentaire parfaite et une prise alimentaire normale. L'examen clinique et le scanner de contrôle ne montrent pas de récidive locale ou la présence de métastases à distance.
Conclusion
Ces 2 cas montrent bien l'intérêt de l'utilisation d'une prothèse mandibulaire lors de mandibulectomie partielle. Cela permet d'éviter le déplacement médial de la mandibule controlatérale et les complications afférentes : difficultés à s'alimenter, blocage de mâchoire liée à l'interférence des dents, plaie palatine liée à l'impaction d'un croc.
Ces solutions de reconstruction prothétique nous permettent d'améliorer la qualité de vie de nos patients. Leur coût et le délai de fabrication restent les principaux facteurs limitants à leur utilisation.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Réduire une luxation du coude à foyer fermé
Tours, France
I. Introduction
La forme osseuse caractéristique du coude fait que la majorité des luxations sont latérales. Le coin caudodistal carré de l'épicondyle médial de l'humérus empêche l'ulna de dévier médialement, alors que l'épicondyle latéral, de forme arrondie, permet au processus anconé d'évoluer au-delà de la crête latérale lorsque le coude est fléchi à plus de 90°. Une luxation médiale, bien que rare, est généralement associée à une lésion ligamentaire grave.
II. Signes cliniques
1. Aspect extérieur typique
Très semblable à ceux observés dans une contracture de l'infra-épineux
2. Palpation
Le radius et l'ulna déviés latéralement sont facilement remarquables.
3. Position
L'avant-bras et la patte sont écartés (abductés), et le coude reste fléchi.
4. Douleur et limitations
Douleur marquée, élargissement de l'articulation, et résistance notable lors des mouvements de flexion et d'extension.
5. Interférence au sol
En raison de la flexion, la patte ne touche pas le sol chez l'animal debout ou assis.
III. Diagnostic
Un examen clinique permet de suspecter la luxation, mais une radiographie dans deux plans est indispensable pour détecter d'éventuelles fractures associées ou des avulsions ligamentaires.
IV. Traitement
1. Réduction fermée
a) Fenêtre temporelle
Efficace dans les premiers jours suivant la blessure ; après, les contractures musculaires compliquent la manœuvre.
b) Technique
Sous anesthésie générale, on repère d'abord la position des condyles huméraux. Souvent, le processus anconé est bloqué médialement par rapport à la crête latérale de l'humérus.
Avec le coude fléchi entre 100 et 110°, on applique une pression médiale sur l'olécrâne.
On exerce ensuite une pression sur la tête radiale pour l'insérer sous le capitulum huméral, tout en maintenant l'abduction du coude.
Si la tête radiale ne se remet pas en place : on réalise une extension mineure du coude pour verrouiller le processus anconé, puis on pratique une pronation (rotation interne de l'avant-bras), abduction et adduction successives pour déloger la tête radiale.
c) Cas où le processus anconé est déjà latéral
Coude fléchi à 100-110°, avant-bras en pronation pour forcer le processus à passer à l'intérieur de l'épicondyle latéral.
On étend légèrement le coude puis on fléchit à nouveau tout en poursuivant la pression médiale sur la tête radiale, avec pronation et abduction.
Après réduction : on évalue l'intégrité ligamentaire. La radiographie crâniocaudale des deux coudes permet de vérifier la qualité de la réduction.
2. Réduction ouverte
a) Indications
Échec de la réduction fermée, présence de débris, hématome organisé, fragments ligamentaires.
b) Technique
Abord limité à la tête radiale et dans le compartiment latéral. Nettoyage des débris, repositionnement des ligaments, éventuelle utilisation d'un levier osseux protégé.
c) Cas chroniques (6–7 jours ou plus)
Ostéotomie de l'olécrâne pour faciliter l'accès et la réduction, notamment pour libérer les tissus cicatriciels.
3. Examen des ligaments collatéraux (méthode de Campbell)
- Élasticité normale après réduction : ± 45° en rotation latérale du carpe, ± 70° en rotation médiale.
- Lésion du ligament latéral : rotation médiale possible jusqu'à ~140°.
- Lésion du ligament médial : rotation latérale possible jusqu'à ~90°.
- Un seul coude est testé à la fois, comparativement au côté sain.
- Mouvement excessif = lésion ligamentaire.
- Si le coude est reluxable facilement : réparation chirurgicale recommandée.
- Stabilité relative : la décision dépend de la taille, de l'activité et de l'usage (chien de travail/athlétique vs petit animal sédentaire).
- Réparation conservatrice possible chez les petits animaux peu actifs : immobilisation et cicatrisation par fibrose.
4. Réparation des ligaments (chirurgicale)
a) Principes
Plicature des ligaments étirés, suture des ligaments déchirés, réinsertion des ligaments avulsés.
b) Option prothétique
En cas de destruction ligamentaire importante, implantation d'un « ligament synthétique » via points de forage, vis avec rondelle ou ancrage suture.
c) Technique latérale
- Coupe du tendon de l'ulnaris lateralis.
- Refixation du ligament à l'os.
- Plicature du tendon extenseur par points en matelas.
- Si ligament déchiqueté : ligament synthétique fixé entre l'épicondyle latéral et la tête radiale.
- Réparations similaires du côté médial si nécessaire.
- Si la lésion est distale, le ligament peut être fixé à l'anneau ligamentaire.
- Lésions du corps du ligament = suture en boucle verrouillée.
V. Soins postopératoires
| Situation | Immobilisation | Repos/Exercice | Rééducation |
|---|---|---|---|
| Réduction (ouverte/fermée) sans lésion ligamentaire | Bandage souple + attelle latérale, immobilisation 5-7 jours | Maison/sur laisse 2 semaines | Exercices passifs dès retrait du bandage |
| Réduction fermée avec lésion | Attelle rigide (type « spica ») maintenue 2 semaines | Maison/sur laisse 3-4 semaines | Exercices passifs post-attelle |
| Réparation chirurgicale des ligaments | Spica 3 semaines | Maison/sur laisse jusqu'à 4 semaines | Rééducation douce progressive |
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Rééducation après chirurgie pour rupture du LCA : du confinement à la liberté
Lausanne, Suisse
I. Introduction
La rupture du ligament croisé crânial (LCA) constitue la principale cause de boiterie postérieure chez le chien. Les techniques chirurgicales actuelles principalement utilisées (DeAngelis, TTA, TPLO) permettent de stabiliser le grasset, mais la restauration d'une fonction locomotrice optimale ne dépend pas uniquement de la technique chirurgicale ni de l'implant posé. Elle exige une rééducation structurée, guidée par le physiothérapeute vétérinaire, qui accompagne l'animal depuis le post-opératoire immédiat jusqu'au retour à une activité normale, voire sportive. [1,2]
L'état initial du patient oriente la prise en charge : certains posent le membre précocement et évoluent rapidement, d'autres ne s'appuient que de manière intermittente, tandis que les plus douloureux refusent tout appui. Dans ces derniers cas, il est essentiel d'exclure une complication (défaillance de l'implant, fracture secondaire, infection) avant de poursuivre le protocole de rééducation. Cet état des lieux initial conditionne la stratégie thérapeutique.
II. Gestion de la douleur et du processus inflammatoire
Le contrôle de la nociception est fondamental pour éviter la transition vers une douleur chronique et faciliter l'appui précoce. Les techniques utilisées ciblent à la fois la modulation de la douleur (TENS) et la diminution de la réponse inflammatoire (cryothérapie, massage de drainage lymphatique, laser thérapeutique). Le laser thérapeutique stimule la production d'ATP et favorise la libération d'oxyde nitrique, ce qui améliore la circulation locale et soutient le métabolisme cellulaire. En parallèle, elle module l'expression de médiateurs pro-inflammatoires, contribuant à réduire l'inflammation locale et la douleur associée.
La physiothérapie complète ainsi l'analgésie pharmacologique et favorise un confort indispensable à la poursuite des étapes suivantes [2].
III. Promotion de la cicatrisation tissulaire
La stabilisation chirurgicale induit une cascade de réparation ligamentaire, musculaire et osseuse qui doit être soutenue. Le laser thérapeutique a montré, dans une étude récente, une amélioration de la démarche évaluée par les propriétaires après TPLO, sans pour autant influencer de manière significative la récupération fonctionnelle mesurée objectivement [3]. Les ondes de choc, appliquées immédiatement après chirurgie, ont quant à elles, permis une amélioration plus rapide de l'appui du membre opéré par rapport au groupe contrôle. Enfin, en phase tardive de cicatrisation, les ultrasons thérapeutiques peuvent améliorer la plasticité du tissu cicatriciel péricapsulaire et limiter les adhérences [4].
IV. Remobilisation et restauration de la démarche
La reprise fonctionnelle exige la prévention de la fibrose capsulaire et la réactivation des boucles neuromusculaires. Les mobilisations passives entretiennent l'amplitude articulaire, relayées rapidement par des exercices actifs doux. Ceux-ci incluent par exemple des exercices de transfert de poids, de marche contrôlée en laisse, de passages de cavaletti ou encore de slalom entre cônes. L'utilisation d'équipements spécialisés comme l'Imoove-Vet, qui sollicite la proprioception et la coordination motrice sur des plateformes dynamiques, permet une stimulation neuromusculaire fine et progressive. Ces exercices sont complétés par les thérapies de base en physiothérapie (stimulation électrique neuromusculaire, travail sur surfaces instables, exercices de posture), qui favorisent le recrutement musculaire et la symétrisation de l'appui [5]. Cette phase marque le passage de la simple tolérance de l'appui à la récupération d'une marche fonctionnelle et symétrique [2].
V. Renforcement musculaire et réintégration progressive à l'activité
Le déficit musculaire quadriceps/ischio-jambiers est un problème fréquemment rencontré après chirurgie du LCA. Le pic d'amyotrophie est atteint environ deux semaines après l'opération, ce qui justifie la mise en place précoce d'exercices adaptés. Sa correction passe par des exercices thérapeutiques ciblés, tels que les assis-debout contrôlés, les montées sur plateforme, les pas lents en montée, ou encore les exercices de cavaletti destinés à améliorer la coordination et la force [1-5]. L'utilisation de l'hydrothérapie, en particulier le tapis roulant aquatique, permet un travail musculaire intensif sans surcharge articulaire grâce à la poussée d'Archimède et à la résistance de l'eau. Le niveau d'immersion est modulé pour ajuster le poids porté et la difficulté de l'exercice, facilitant la rééducation des chiens en surpoids ou très douloureux. Des variations de vitesse et de hauteur d'eau permettent d'adapter finement l'intensité et de cibler le renforcement musculaire ou l'endurance cardiovasculaire. Le programme inclut ainsi une progression structurée, jusqu'à la reprise d'une activité physique normale, sécurisée et adaptée au niveau d'exigence de chaque patient (chien de famille ou athlète sportif) [1-2-5].
VI. Conclusion
La chirurgie stabilise, mais seule la rééducation libère. En guidant le patient étape par étape, la physiothérapie transforme l'acte chirurgical en véritable retour fonctionnel, offrant au chien la possibilité de passer du confinement imposé par la lésion à la liberté retrouvée du mouvement.
Bibliographie
- SPINELLA G, ARCAMONE G, VALENTINI S. Cranial Cruciate Ligament Rupture in Dogs: Review on Biomechanics, Etiopathogenetic Factors and Rehabilitation. Vet Sci. 2021 Sep;8(9):186
- MONK ML, PRESTON CA, MCGOWAN CM. Effects of early intensive postoperative physiotherapy on limb function after TPLO in dogs with deficiency of the cranial cruciate ligament. Am J Vet Res. 2006;67(3):529–36.
- RENWICK SM, RENWICK A, BRODBELT DC, FERGUSON J and ABREU H. Influence of class IV laser therapy on the outcomes of tibial plateau leveling osteotomy in dogs. Vet Surg. 2018;47(4):507-515.
- KIRKBY SHAW K, ALVAREZ L, FOSTER SA, TOMLINSON JE, SHAW AJ, POZZI A. Fundamental principles of rehabilitation and musculoskeletal tissue healing. Vet Surg. 2020 Jan;49(1):22–32.
- BARNES K, FALUDI A, TAKAWIRA C, et al. Extracorporeal shock wave therapy improves short-term limb use after canine tibial plateau leveling osteotomy. Vet Surg. 2019;48(8):1382-1390.
Liens d'intérêt : Conseiller scientifique pour la société AllCare innovations.
📃 Rééducation après une excision arthroplastie de la hanche : comment optimiser la récupération ?
La Madeleine, France
I. Introduction
La chirurgie d'EATF consiste à réaliser une ostéotomie de la tête et du col du fémur. Après la chirurgie, un tissu fibreux se forme et le fémur ne s'articule plus avec le bassin. Il y a formation d'une pseudarthrose. À noter, le fémur se positionne légèrement plus dorsalement, entraînant un léger raccourcissement du membre. Ce sont les masses musculaires entourant la hanche qui seront responsables de son maintien et donc influenceront le succès de l'opération. Contrairement à la plupart des interventions orthopédiques, il est contre-indiqué de restreindre les activités physiques (Harper, 2017), et d'imposer un repos strict en cage après une excision arthroplastie. Ces patients doivent être encouragés à utiliser leur membre le plus tôt et le plus souvent possible sinon le tissu fibreux qui se forme en post-opératoire sera restrictif et limitera sévèrement l'amplitude de mouvement de la hanche.
La rééducation prend ainsi tout son sens et revêt une importance cruciale.
Elle vise en priorité à réduire la douleur postopératoire afin de permettre une récupération fonctionnelle optimale. Elle a également pour but de restaurer le volume musculaire, notamment au niveau des muscles pelviens souvent rapidement atrophiés. Un travail spécifique est réalisé pour préserver l'amplitude articulaire, en particulier l'extension et l'abduction de hanche, afin d'éviter les compensations et les diminutions d'amplitude.
Les exercices encourageant un appui précoce et contrôlé sont essentiels pour limiter la formation de fibrose excessive et vont favoriser la reprise d'un appui fonctionnel. Enfin, des exercices actifs ciblés permettent de stimuler la proprioception, indispensable pour un bon contrôle postural et une locomotion efficace.
Le pronostic de récupération est en général favorable, mais il varie selon le contexte clinique, l'intensité et la chronicité de la boiterie préexistante. Le contexte médical joue un rôle important : une dysplasie accompagnée de douleur chronique n'aura pas les mêmes implications qu'une luxation ou une fracture, car les lésions des structures périarticulaires seront différentes. La récupération est plus incertaine chez les chiens de grand format ou en surpoids. (Millis, 2013)
II. Pré-opératoire
Si la chirurgie n'est pas réalisée immédiatement, il est souvent possible – et même recommandé – de débuter la rééducation en phase préopératoire. Cela présente de nombreux avantages : réduction de la douleur et des tensions musculaires, maintien de l'amplitude articulaire, et amélioration de la force et du volume musculaire. Elle permet également de limiter la fibrose et les adhérences avant l'intervention.
Puisque la perte musculaire après l'opération est quasiment inévitable, optimiser le volume musculaire en amont permet de mieux limiter l'atrophie.
La rééducation préopératoire permet aussi à l'animal de se familiariser avec les techniques de physiothérapie, ce qui renforce l'efficacité des séances après l'opération. Enfin, le physiothérapeute peut accompagner les propriétaires en leur donnant des conseils pratiques sur les gestes à adopter et les aménagements à prévoir après la chirurgie (mobilisations passives, cryothérapie, types de couchages, sols antidérapants, harnais, etc.).
III. Gestion post-opératoire
Les délais sont donnés à titre indicatif, il est évident que le protocole doit être adapté à chaque animal en fonction de sa douleur et de sa vitesse de récupération.
1. Phase inflammatoire, nursing
Au cours des premiers jours après la chirurgie (généralement entre 3 et 5 jours), la douleur et l'inflammation sont prédominantes et doivent être prises en charge efficacement. Une gestion médicamenteuse adaptée (AINS +/- opiacés) est indispensable. Certaines techniques de rééducation peuvent être mises en place dès cette phase :
- Cryothérapie : 15 minutes, 3 fois par jour, pour réduire l'œdème, la douleur et l'inflammation.
- Mobilisations passives douces : 10 répétitions, 3 fois par jour. Les mouvements doivent être lents et indolores.
- Marche lente avec harnais de soutien : jusqu'à 5 minutes, réservée aux sorties hygiéniques.
- Massages légers du membre opéré.
- Exercices de report de poids : pour encourager un appui progressif sur le membre concerné.
- Laser thérapeutique : une fois par jour, afin de diminuer douleur, inflammation et œdème
- Électrothérapie antalgique (TENS) : 2 à 4 fois par jour si la douleur est importante.
2. Phase de reprise d'appui
Lors de la phase de reprise d'appui (généralement J5 à J21), la douleur diminue et l'animal commence à récupérer un appui très léger. Les mouvements brusques sont toujours interdits. Les exercices actifs sont interdits si l'animal est encore trop douloureux. On cherche à encourager l'utilisation du membre opéré ; la proprioception a été modifiée par la chirurgie (perte de récepteurs proprioceptifs, raccourcissement du membre, changement dans la conformation, perte d'une articulation…!) : il est donc conseillé d'ajouter des exercices proprioceptifs à ce stade.
Les précédentes techniques sont ajustées ainsi :
- Laser thérapeutique 2x/semaine
- Marche lente en laisse 5 à 10 minutes, avec soutien si nécessaire
- Mouvements passifs doux
- Exercices report de poids et proprioceptifs sur surface molle ou plateforme bidirectionnelle ou plateforme proprioceptive motorisée
- Hydrothérapie 5 à 10 minutes (après retrait des fils à J15) l'hydrothérapie sur tapis roulant immergé permet de soulager le poids supporté par l'animal, d'encourager l'utilisation du membre opéré, et de renforcer la masse musculaire.
- Cryothérapie 15 min après exercices
- Électrothérapie antalgique TENS si nécessaire
- Électrothérapie NMES si fonte musculaire importante ou inhibition musculaire (quadriceps, ischio jambiers, glutéaux)
- Ultrasons si restriction de mouvements importante
3. Phase de consolidation
Lors de la phase de consolidation (généralement J21 à J60), l'animal améliore sa confiance lors de la marche. Les mouvements brusques, sauts etc. sont toujours interdits. L'objectif est d'encourager l'utilisation du membre opéré, de rétablir la force et le volume musculaire, et de récupérer la meilleure amplitude de mouvement possible. Le programme de rééducation est le suivant :
- Laser si besoin + mouvements passifs + étirements doux, l'extension de la hanche peut rester douloureuse.
- Marche 15-20 minutes (avec pentes pendant 5-10 minutes)
- Exercices actifs : choisir 2 exercices parmi ceux proposés ci-dessous
- Assis debout 5-10 répétitions 2x/j
- Exercices proprioceptifs sur coussin ou plateau
- Rails de cavalettis
- Montée descente escaliers en laisse : 1 aller-retour
- Exercices en danseuse si toléré
- Hydrothérapie sur tapis roulant immergé, durée croissante de 5 à 20 minutes
- Électrothérapie NMES si nécessaire
- Ultrasons si besoin
4. Phase de renforcement
Lors de la phase de renforcement (généralement après J60), la cicatrisation est terminée, on se concentre sur le développement musculaire.
- Étirements du membre opéré : 8 à 10 répétitions
- Marche de plus de 20-30 minutes, avec pentes, des épisodes de trot ou d'inclinaison peuvent être ajoutés. Ajout de surfaces meubles : sable, herbes hautes…
- Exercices actifs : augmentation de l'intensité des exercices précédemment demandés.
- Hydrothérapie sur tapis roulant immergé 15-20 minutes ou nage 5-10 minutes.
IV. Chronologie de récupération
Chronologie classique de récupération après une EATF (selon Millis, 2013) :
- 0-3j : sans appui à reprise d'appui très légère (doigts qui touchent/effleurent le sol)
- 3j à 2 semaines post-opératoires : début de reprise d'appui à la marche lente
- 2- 4 semaines : utilisation active du membre lors des déplacements. marche avec appui de plus en plus franc (mise en charge du membre)
- 5 à 8 semaines : appui franc au trot
- + de 9 semaines : trot rapide avec peu ou pas de boiterie.
En cas de récupération plus lente que prévue, il est essentiel d'analyser la situation et d'adapter le protocole en conséquence. Plusieurs questions doivent alors être soulevées : l'animal présente-t-il encore des douleurs ? Y a-t-il une limitation marquée de l'amplitude articulaire ? L'animal hésite-t-il à utiliser son membre malgré l'absence de douleur (kinésiophobie) ? Existe-t-il une gêne mécanique lors du mouvement ? Est-ce qu'une reprise chirurgicale est indiquée (en cas d'ablation incomplète du col fémoral et de frottement persistant) ?
V. Conclusion
En conclusion, la réussite d'une exérèse de la tête et du col fémoral repose sur une prise en charge globale, où la rééducation joue un rôle central. Une rééducation précoce, progressive et adaptée est essentielle pour limiter les complications, restaurer la fonction locomotrice et assurer un bon confort de vie. L'implication du physiothérapeute et des propriétaires est donc déterminante pour optimiser les résultats à long terme.
Bibliographie
- DYCUS, D. L., LEVINE, D., RATSCH, B. E., & MARCELLIN-LITTLE, D. J. (2022). Physical rehabilitation for the management of canine hip dysplasia: 2021 update. Veterinary Clinics: Small Animal Practice, 52(3), 719-747.
- MILLIS, D., & LEVINE, D. (2013). Canine rehabilitation and physical therapy. Elsevier Health Sciences.
- BOCKSTAHLER, B., WITTEK, K., LEVINE, D., MAIERL, J., & MILLIS, D. L. (2019). Essential facts of physical medicine, rehabilitation and sports medicine in companion animals. Munich, Germany: VBS GmbH.
- COLVERO, A. C. T., SCHWAB, M. L., FERRARIN, D. A., RIPPLINGER, A., HERCULANO, L. F. S., WRZESINSKI, M. R., ... & MAZZANTI, A. (2020). Physical therapy treatment in the functional recovery of dogs submitted to head and femoral neck ostectomy: 20 cases. Ciência Rural, 50, e20190545.
- HARPER, T. A. (2017). Femoral head and neck excision. Veterinary Clinics: Small Animal Practice, 47(4), 885-897.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Relation entre les pratiques d'hygiène dans les élevages de chats et de chiens et l'infestation par des parasites gastro-intestinaux
Hanna MILA
Coauteurs : Lou TIMMERMAN, Sofia ABEL, Mathilde MARTIN, Jeanne TASTET, Emmanuel LIÉNARD, Emilie BOUHSIRA, Hanna MILA, Aurélien GRELLET
Introduction
Le parasitisme gastro-intestinal est fréquent en élevage canin et félin et peut être à l'origine de signes cliniques tels que des troubles digestifs, un retard de croissance ou de la mortalité. Cependant, l'effet précis des pratiques d'hygiène sur la prévention de l'infestation parasitaire reste peu étudié dans les élevages de chats et de chiens. Cette étude vise à évaluer la relation entre la gestion sanitaire des élevages et l'infestation parasitaire.
Matériel et méthodes
Trente-sept élevages français ont été inclus dans cette étude entre 2019 et 2023, comprenant 19 élevages félins et 18 élevages canins. Pour chaque structure, un questionnaire a été rempli concernant les espèces hébergées, la gestion de l'établissement ainsi que les conditions d'hébergement des animaux par local. Par ailleurs, entre 1 et 7 selles ont été prélevées par les éleveurs dans chaque local de l'élevage et mélangées pour constituer un échantillon de selles poolées.
Une coproscopie par flottation avec du chlorure de sodium saturé a été réalisée sur tous les échantillons collectés. L'analyse des données a été réalisée à l'aide du logiciel JAMOVI 2,6. L'association entre la présence de parasites et sept variables au niveau du local (âge des animaux, revêtement de sol et de mur, densité animale, espèce, utilisation d'un détergent et/ou d'un désinfectant) a été testée à l'aide de tests ch², avec une valeur de P <0,05 considérée comme statistiquement significative. Un « score sanitaire de local » a ensuite été déterminé sur la base de ces variables.
Des analyses similaires ont ensuite été réalisées pour tester l'association entre la présence de parasites (œufs, oocystes excrétés dans les fèces) et six variables au niveau de l'élevage (espèce, présence de diarrhée, zone de quarantaine, infirmerie, administration d'anthelminthiques, score sanitaire moyen des salles).
Résultats
Parmi les 37 élevages étudiés, des données relatives à 149 locaux ont été recueillies, dont 77 pour les chats et 73 pour les chiens (moyenne de 4 locaux par établissement). Des œufs d'ascaris, de strongles et de trichures, ainsi que des oocystes de coccidies, ont été identifiés dans 38 % (14/37) des élevages et 17,2 % (25/149) des locaux.
La prévalence des parasites gastro-intestinaux était significativement plus élevée dans les locaux hébergeant des chiens (23 %, 17/73) que dans les logements hébergeant des chats (10 %, 8/77, p = 0,031). Des multi-infestations ont été observées dans 8 % (12/149) des locaux, uniquement dans les élevages canins (6/18), avec 2 à 3 parasites différents identifiés.
Le nombre de locaux positifs était significativement plus faible lorsque l'utilisation d'un détergent était systématique (12 %) par rapport aux locaux où aucun détergent n'était employé (27 %, p = 0,034). De même, la désinfection systématique des locaux était associée à une diminution du nombre de locaux positifs (11 % contre 44 % en l'absence de désinfection, p < 0,001).
L'âge des animaux, les revêtements de sol et de mur, la densité animale et le score sanitaire des logements ne furent pas associés à la présence de parasites. Au niveau de l'élevage, la prévalence des parasites fut significativement plus élevée lorsque le score sanitaire moyen des locaux était bas (considéré donc comme mauvais) comparativement à un score jugé bon (respectivement 22 % [8/37] et 5 % [2/37] ; p = 0,040). Un antécédent de diarrhée, la présence d'une quarantaine, d'une infirmerie ou l'administration d'anthelminthiques n'étaient pas associés à l'infestation parasitaire.
Conclusion
Cette étude met en évidence l'importance des pratiques sanitaires adaptées pour limiter l'infestation parasitaire dans les élevages canins et félins. L'utilisation systématique de détergents et de désinfectants réduit significativement la prévalence des parasites. Les visites vétérinaires et la formation des éleveurs restent essentielles pour améliorer la prophylaxie sanitaire et médicale des établissements, minimisant ainsi les risques sanitaires, et améliorant le bien-être animal.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Renforcer le lien entre le lapin et son propriétaire : jeu, agility et renforcement positif
Eschau, France
Créer un lien de confiance durable entre un lapin et son propriétaire passe par une compréhension fine de son répertoire comportemental et de ses besoins éthologiques. On cherche à mettre en place une approche respectueuse de l'espèce, basée sur des interactions agréables [1,2,3]. Le lapin, animal proie, manifeste une méfiance naturelle envers l'humain. Pourtant, avec des outils adaptés, il est tout à fait possible d'instaurer une relation de confiance et d'impliquer activement lapin et humain dans des activités ludiques et enrichissantes.
En premier lieu, il est crucial que les propriétaires comprennent bien l'impact du statut de proie des lapins sur leur comportement.
Beaucoup des manipulations que les gens font aux lapins ne leur conviennent pas. L'envie de les porter par exemple est très fréquente et pourtant c'est un acte extrêmement anxiogène car similaire à l'action des prédateurs qui les attrapent et les soulèvent [3]. Le lapin ne peut donc être porté par les humains sans angoisse que s'il a un niveau de confiance élevé et un niveau de peur très faible.
Les caresses et autres contacts physiques peuvent également être désagréables pour les lapins qui ne sont pas familiers et à l'aise avec les humains. Il est également à noter que la position dite « de transe », c'est-à-dire l'immobilité tonique lors de la mise sur le dos, cause en réalité un stress intense aux lapins et qu'elle est évitable dans la majorité des cas [3], y compris lors de la coupe des griffes et la prise de température. Notre rôle de vétérinaire est d'en informer les propriétaires car beaucoup pensent que c'est un acte anodin.
Ensuite, le lapin communiquant majoritairement par le corps et les postures, il est essentiel d'informer les propriétaires sur la lecture de leurs signaux et de leur état émotionnel afin qu'ils puissent adapter leur proposition d'interactions par rapport à leur lapin.
Après avoir supprimé les interactions désagréables, on peut mettre en place des interactions positives, afin de construire la confiance. Ces interactions doivent toujours s'adapter à la réponse obtenue de la part du lapin (fuite : ça ne lui plaît pas, lapin qui reste ou qui s'approche : il apprécie) et la lecture de sa posture pour déceler son état émotionnel.
Parmi les jeux adaptés, un des premiers, et qui est très facile à mettre en place, est la recherche de nourriture, sous forme de parcours/chasse au trésor [1,2]. Ce jeu permet au lapin de mettre en œuvre le comportement de foraging, une des composantes majeur de son budget d'activité, tout en favorisant les déplacements et l'exploration. On veillera à ne pas mettre en lapin en difficulté en le leurrant à côté de quelque chose (ou quelqu'un) qui lui fait peur.
On peut également lui apprendre des tours, en utilisant le renforcement positif et le conditionnement opérant. Cette méthode favorise la curiosité du lapin, mais lui permet également d'oser produire tel ou tel comportement. On augmente donc sa confiance en lui et en l'humain, par le biais d'interactions très positives, avec notamment des récompenses alimentaires de haute valeur. On augmente également son optimisme. L'observation attentive des signaux de confort/inconfort est essentielle, afin de s'assurer que le lapin est volontaire et que l'expérience est positive pour lui.
L'agility est une activité stimulante qui plaît souvent aux lapins car elle leur permet d'utiliser leur corps athlétique et de faire des sauts, ce qui est un comportement naturel de l'espèce. Ce sont des parcours adaptés et un travail sans contrainte mais avec des récompenses qui permettent au lapin de d'apprécier l'activité et d'avoir des interactions agréables avec les humains. L'animal doit avoir le choix de participer ou non, et le parcours doit être sécurisé et adapté à ses capacités physiques.
À l'inverse, les punitions ou contraintes physiques sont contre-productives et délétères pour la relation. Généralement mal appliquées et inadaptées, elles ne permettent pas au lapin de comprendre et d'apprendre, et ne font qu'amplifier sa peur et son anxiété face aux humains. Un cercle vicieux se met alors en place, avec l'émergence de comportements indésirables secondaires à la peur et à l'anxiété.
En conclusion, il faut retenir que la création d'un lien de confiance fort et sain entre le lapin et ses propriétaires est possible. Il se construit à travers le respect, la compréhension de l'animal et de ses besoins éthologiques, avec des interactions enrichissantes et agréables.
Bibliographie
- BRADBURY G. Behavioural Problems in Rabbits - A clinical approach. 5M publishing ; 2018.
- BUSETH M E, SAUNDERS R. Rabbit behaviour, health and care. CABI ; 2015.
- TYNES, V. The Interaction Between Behavioral and Physical Health in Rabbits. Veterinary Clinics of North America: Small Animal Practice 54, no.1. 2024 ; 169–79.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Sacro-iliite chez une chienne Golden retriever de 1,5 ans : description clinique et diagnostique, traitement et suivi IRM à long terme
Lena BLANCHOT
Coauteurs : Alexandre CARON
Introduction
La sacro-iliite, qui correspond à une inflammation de l'articulation sacro-iliaque, est peu décrite dans l'espèce canine [1-5]. Chez l'Homme, cette affection est bien décrite et est fréquemment d'origine infectieuse. Son diagnostic se fait par IRM de l'articulation sacro-iliaque, les signes radiographiques étant frustres au commencement de l'évolution de la maladie.
Anamnèse
Une chienne Golden Retriever stérilisée de 1,5 an est présentée en consultation référée pour raideur des membres pelviens et abattement. Elle présente comme antécédent une péritonite septique consécutive à un pyomètre, traité par ovario-hystérectomie et lavage abdominal un mois auparavant. La chienne présente une incapacité à sauter, une circumduction des membres pelviens à la marche et des chutes répétées depuis son adoption. Une consultation chez son vétérinaire traitant pour abattement met en évidence une hyperthermie à 39,3°C. Une numération formule sanguine met en évidence une leucocytose. Un traitement antibiotique (doxycycline) et anti-inflammatoire non stéroïdien (molécules, doses et durées non spécifiées) sont mis en place. La chienne est de nouveau présentée à son vétérinaire 13 jours plus tard pour abattement, extrême fatigabilité à l'effort et douleurs articulaires. La propriétaire est alors orientée en centre de référé et le traitement anti-inflammatoire est poursuivi.
Lors de la consultation référée en médecine, la chienne ne présente aucun signe clinique. Une exploration du syndrome fébrile et de la fatigabilité rapportés est entreprise. Un dosage de la protéine C-réactive, un ionogramme, un dosage du calcium ionisé, un dosage du cortisol basal et un dosage de la thyroxine (T4) et de la thyroid stimulating hormone (TSH) sont réalisés et sont dans les normes de l'espèce canine. Une échographie cardiaque met en évidence une hypertension pulmonaire modérée (60 mmHg) sans anomalie cardiaque. Des sérologies à la recherche d'une infestation parasitaire à Angiostrongylus vasorum et Dirofilaria immitis sont négatives. Un traitement anti-inflammatoire est initié (firocoxib, 5,3 mg/kg PO SID 10 jours). Trois jours après cette exploration, la chienne présente une boiterie et est donc référée au service de chirurgie.
Examen clinique
Lors de la consultation référée en chirurgie, l'examen clinique met en évidence une boiterie de grade 2/5 du membre pelvien droit. Un inconfort est noté à la palpation en région lombo-sacrée et la boiterie du membre pelvien droit est aggravée à 4/5 suite à l'examen. Le reste de l'examen est dans les normes.
Démarche diagnostique
Une atteinte lombo-sacrée ou sacro-iliaque est suspectée (discospondylite, hernie discale, kyste synovial, diverticule subarachnoïdien, sacro-iliite). Des radiographies orthogonales du bassin mettent en évidence une lésion osseuse agressive sacro-iliaque droite avec sclérose, prolifération périostée et lyse des surfaces articulaires sans anomalie sur le rachis lombaire et sacré.
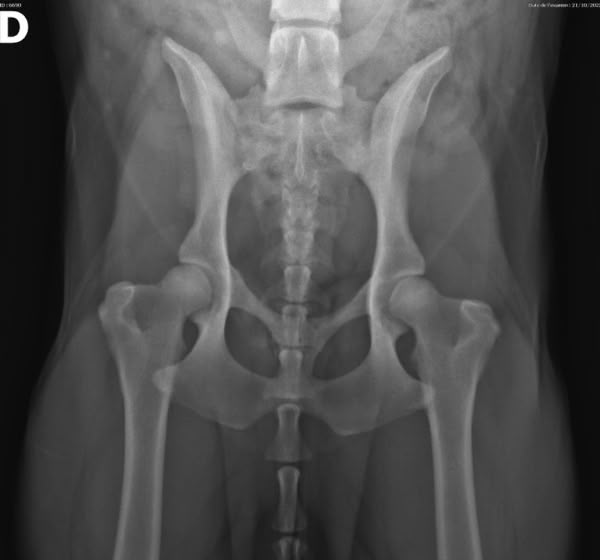
Figure 1
Une IRM de la jonction sacro-iliaque met en évidence une lésion sacro-iliaque droite compatible avec une sacro-iliite majeure dont l'origine est indéterminée. Une névrite sciatique droite secondaire est également suspectée. La lésion est de trop petite taille et trop profonde pour être ponctionnée.
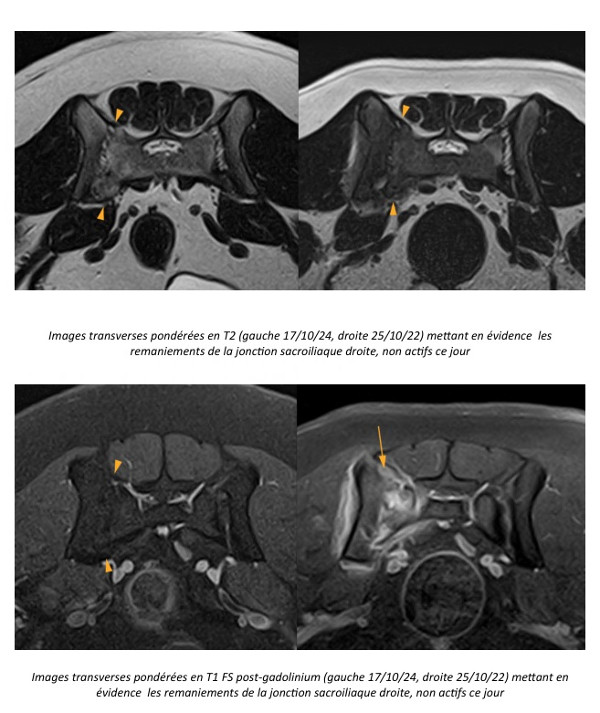
Figure 2
Traitement
Un traitement antibiotique (amoxicilline et acide clavulanique 12,5 mg/kg BID) et un traitement anti-inflammatoire non stéroïdien (firocoxib 5 mg/kg SID) sont mis en place pour 8 et 2 semaines respectivement. Les signes cliniques rétrocèdent totalement après 1 semaine de traitement. Un suivi à long terme ne montre aucun signe de récidive clinique. Un CBPI (canine brief pain inventory) complété par la propriétaire 8 mois après le diagnostic donne un score de sévérité de 4/40 et un score d'interférence de 6/60. La propriétaire qualifie la qualité de la locomotion de sa chienne d'excellente et une IRM de contrôle montre une résolution des lésions.
Discussion
La sacro-iliite est encore peu décrite chez l'espèce canine. Les quelques cas rapportés ont une origine infectieuse (Brucella canis, Pasteurella multocida,...) ou non identifiée faute d'examens diagnostiques (ponction des lésions et analyse bactériologique). Il a été rapporté la présence d'abcès rétropéritonéaux en continuité avec l'atteinte sacro-iliaque [2]. Notre chienne a présenté un historique de péritonite septique un mois auparavant, une origine infectieuse est donc très probable. La résolution des signes cliniques avec la mise en place d'un traitement antibiotique adapté va également dans ce sens, car les traitements anti-inflammatoires seuls ne permettaient qu'une amélioration transitoire avant rechute.
Conclusion
La sacro-iliite est une atteinte d'étiologie pouvant être infectieuse et pouvant causer des signes généraux frustres et des boiteries lors des stades plus avancés. Le diagnostic radiographique précoce est complexe car les signes radiographiques sont discrets [3]. Cette affection doit être envisagée en cas de boiterie et de syndrome fébrile chez un animal jeune.
Bibliographie
- Brucella canis sacroiliitis and discospondylitis in a dog. Can Vet J (2019).
- Jeong, J. et al. Case Report: Multimodality Imaging of Infectious Sacroiliitis and Retroperitoneal Abscess Causing Hindlimb Ataxia in a Young Dog. Front. Vet. Sci. 8, 732788 (2021).
- Diagnostic imaging characteristics of canine infectious sacroiliitis. Can Vet J (2019).
- Diogo, C. C., Trevail, R., Moreno-Aguado, B. & Quinn, R. Long-term outcome of infectious sacroiliiti
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Savoir utiliser l'électrothérapie pour la rééducation du membre paralysé
La Madeleine, France
I. Introduction
L'électrothérapie est une technique de physiothérapie qui utilise des courants électriques pour stimuler muscles et nerfs. En rééducation vétérinaire, elle permet de lutter contre l'amyotrophie, de soutenir la récupération motrice et de soulager la douleur. Son efficacité dépend toutefois du type de courant utilisé, des paramètres choisis et d'une mise en œuvre rigoureuse.
II. Définition
L'électrothérapie est l'application d'un courant électrique sur les tissus sous-jacents, par le biais d'électrodes placées sur la peau. Le courant électrique va passer d'une électrode à l'autre en utilisant préférentiellement les voies de moindre résistance : nerfs > muscles > tendons > graisse > os.
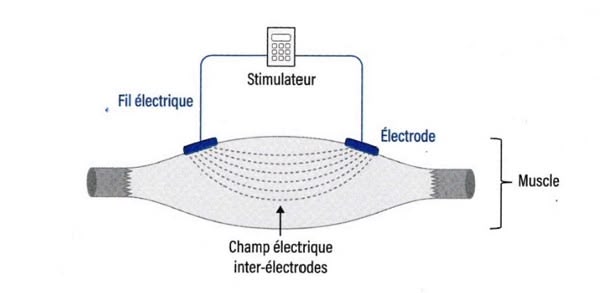
Figure 1 : (d'après PAILLARD, 2023)
On distingue 2 grands types d'électrothérapie, les courants NMES (NeuroMuscular Electrical Stimulation) ou EMS (Electrical Muscle Stimulation) qui vont générer une contraction musculaire, et les courants TENS (Transcutaneous Electrical Nerve Stimulation) qui sont utilisés pour diminuer la douleur.
Le terme NMES est utilisé lorsqu'un muscle est normalement innervé. Le terme EMS correspond à la stimulation directe du muscle, qui est utilisée lors de dénervation partielle ou totale.
Le type de courant qui est majoritairement employé lors de TENS et de NMES est bidirectionnel pulsé. Le courant bidirectionnel est dépolarisé, le pôle négatif et le pôle positif s'inversent à chaque impulsion. Il est plus confortable pour le patient car il ne produit pas d'échauffement ou d'irritation et peut être utilisé chez les patients porteurs de pièces métalliques. Un courant pulsé est une forme de stimulation électrique où le courant est délivré en impulsions brèves et répétées, plutôt que de manière continue. (CRÉPON, 2012)
Une fois les bases physiologiques comprises, il est essentiel de préciser quels effets thérapeutiques peuvent être attendus selon le type de courant appliqué.
III. Effets
L'électrothérapie de type NMES induit une contraction involontaire du muscle via des électrodes. Elle est utilisée pour lutter contre l'amyotrophie, inévitable lors de périodes d'immobilisation ou de paralysie. Cette technique favorise également le réveil moteur des fibres musculaires ayant perdu en contractilité, et stimule la circulation sanguine grâce à un effet pompe. Elle prend tout son sens en cas de paralysie, lorsque l'animal est incapable de contracter ses muscles volontairement.
L'électrothérapie type TENS va permettre de lutter contre la douleur de manière locale (gate control), mais également de manière centrale par la libération d'opioïdes endogènes (courants endorphiniques). Elle peut être intéressante lors de douleurs neurologiques, ou sur des douleurs de compensation (exemple : muscles membres antérieurs sur un chien paralysé des postérieurs).
Pour bien appréhender ces effets, il faut également comparer la contraction induite par électrothérapie à la contraction musculaire physiologique.
IV. Type de contraction et recrutement de fibres
Lors d'une contraction volontaire classique, les fibres musculaires lentes aérobies (disséminées dans tout le muscle mais un peu plus nombreuses en profondeur) s'activent en premier, le nombre de fibres recrutées augmente progressivement, puis il y a recrutement des fibres musculaires rapides (force++). Il existe un relais entre les fibres musculaires : elles se contractent de manière asynchrone, permettant aux fibres de récupérer chacune à son tour.
Lors d'une contraction musculaire par électrothérapie, le recrutement des fibres se fait de la surface vers la profondeur. Ainsi, les fibres musculaires rapides, plus nombreuses en surface, sont plutôt recrutées. Les fibres musculaires se contractent de manière synchrone : pas de relais permettant la récupération, et l'électrothérapie peut s'avérer particulièrement éprouvante pour le muscle si les durées de repos entre les contractions ne sont pas suffisantes. (risque de contracture ++). D'autant plus sur un muscle paralysé n'ayant plus aucune activité depuis plusieurs jours.
V. Contre-indications
L'électrothérapie ne doit pas être utilisée sur la zone cardiaque, le sinus carotidien et s'il y a un pacemaker (rarissime en médecine vétérinaire).
Elle est contre-indiquée en cas de gestation (zone abdominale et diaphragmatique), de troubles convulsifs, de troubles circulatoires (thromboses, phlébites…), et si la peau n'est pas intègre (plaie, peau irritée ou néoplasie). La présence de matériel d'ostéosynthèse ne contre-indique pas l'utilisation de l'électrothérapie.
Lorsqu'aucune contre-indication n'est relevée, le choix de l'appareil et des paramètres devient déterminant pour obtenir une stimulation efficace et sécurisée.
VI. Une séance d'électrothérapie en pratique
La mise en œuvre d'une séance d'électrothérapie doit suivre un protocole rigoureux afin d'en garantir l'efficacité et le confort pour l'animal.
1. Choix de l'appareil d'électrothérapie
Les appareils d'électrothérapie vétérinaires offrent des programmes préétablis adaptés au muscle de l'animal (différences de chronaxies par rapport au muscle humain) qui peuvent grandement en faciliter l'utilisation. Si un modèle humain est choisi, il devra offrir un réglage précis des paramètres :
NMES (contraction)
- fréquence : 20 à 60 Hz,
- durée de phase = chronaxie 150 à 250 µs selon le muscle,
- ratio temps de contraction/repos : 1/3 à 1/4,
- rampe ascendante/descendante 1-4 sec
Principaux paramètres lors d'une séance d'électrothérapie NMES
- TENS (gate control) : fréquence : 50-150 Hz, durée de phase 2 à 50 µs.
- TENS (endorphinique) : fréquence 1-10 Hz, durée de phase 100-400 µs.
Attention, en présence d'un muscle dénervé (ou de pathologie de la jonction neuromusculaire), les appareils classiques d'électrothérapie s'avèrent inefficaces ; l'utilisation d'un dispositif spécifique capable de délivrer des impulsions triangulaires à large durée est alors nécessaire.
2. Placement des électrodes et types d'électrodes
Le positionnement des électrodes est crucial pour cibler précisément le muscle à travailler. Une électrode est placée sur le tendon (proximal ou distal), et une sur le point moteur. Le point moteur d'un muscle est la zone de la peau sous laquelle se trouve l'endroit où le nerf pénètre dans le muscle, permettant d'obtenir la contraction la plus efficace avec une stimulation électrique minimale. Il se situe généralement au tiers proximal/moitié du corps charnu. On distingue les électrodes autocollantes (pratiques, théoriquement à usage unique) et les électrodes en carbone (réutilisables avec gel de contact).
Le placement des électrodes pour de l'électrothérapie antalgique TENS se fait de part et d'autre de la zone douloureuse ou en amont sur le trajet nerveux.
3. Préparation cutanée : tonte, dégraissage et gel de contact
La tonte de la zone ciblée est indispensable pour améliorer la conductivité et éviter les irritations. Ensuite, la peau doit être nettoyée pour éliminer toute trace de sébum ou de saleté (nettoyage puis dégraissage à l'alcool). L'application d'un gel conducteur est essentielle pour assurer un contact homogène entre la peau et l'électrode, réduisant les risques d'échauffement ou de brûlure.
4. Choix de l'intensité et vérification de la contraction
- NMES : l'intensité doit être augmentée progressivement jusqu'à l'obtention d'une contraction visible du muscle, sans provoquer de réaction douloureuse. Le paramétrage dépend du gabarit de l'animal et de l'épaisseur du muscle. Il est impératif d'observer une contraction fonctionnelle (et non un simple frémissement cutané), avec un temps de repos suffisant entre les stimulations.
- TENS : l'intensité doit être augmentée progressivement jusqu'à ce que l'animal sente des fourmillements.
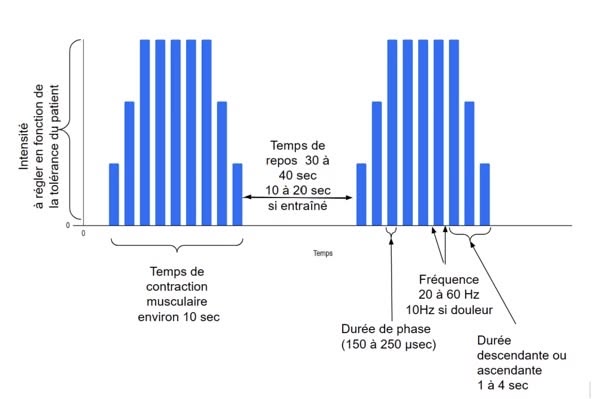
Figure 2
5. Réactions de l'animal
Une attention constante doit être portée au comportement de l'animal : agitation, fuite, vocalisation ou léchage sont des signes d'inconfort ou de douleur. Dans ces cas, il convient de réduire l'intensité ou de repositionner les électrodes. Un animal calme et détendu durant la séance est un indicateur de bonne tolérance au traitement.
Attention à l'animal paralysé ayant perdu la nociception ; la tolérance de la séance sera bonne, mais il n'aura pas de réaction en cas d'échauffement ou d'intensité trop importante, donc une surveillance accrue de la contraction musculaire et de la peau, plusieurs fois par séance est préconisée.
6. Durée de la séance
Les premières séances d'électrothérapie doivent être très progressives : quelques minutes puis augmentation à chaque séance selon tolérance. À terme, une séance dure en moyenne entre 10 et 20 minutes. La fréquence peut être quotidienne (location du matériel par le propriétaire), dans ce cas privilégier des séances courtes et de faible intensité, ou 2 à 3 fois par semaine. Le respect des phases de contraction et de repos est essentiel pour éviter la fatigue musculaire.
VII. Intégration dans le protocole de rééducation du patient paralysé
Exemple après une chirurgie de hernie discale thoraco-lombaire.
Les séances d'électrothérapie peuvent être débutées dès le lendemain de la chirurgie, sur le muscle vaste latéral et les ischio-jambiers une fois par jour (MILLIS, 2013) commencer par 2-3 minutes, et augmenter de 5 minutes toutes les semaines environ. Elles sont réalisées après massages et mouvements passifs, lorsque le muscle est échauffé.
À noter : l'électrothérapie est une technique de contraction musculaire passive, elle ne permet pas de stimuler toute la boucle sensorielle du mouvement, mais uniquement son extrémité (stimulation du nerf juste avant les plaques motrices). De plus, elle ne travaille pas la coordination des différents muscles entre eux, et ne stimule qu'un seul muscle ; contrairement aux exercices actifs qui seront beaucoup plus riches au niveau sensoriel et coordination.
De plus, la contraction induite stimule plus spécifiquement les fibres rapides, or les premières fibres musculaires à s'atrophier lors d'immobilisation sont les fibres lentes.
Elle reste néanmoins la seule façon (avec la stimulation des réflexes) de contracter un muscle lorsque l'animal n'a pas encore récupéré de motricité.
VIII. Conclusion
L'électrothérapie constitue une modalité thérapeutique intéressante dans la rééducation du patient paralysé. Bien qu'elle ne permette pas à elle seule de restaurer la motricité ou la coordination globale, elle joue un rôle dans le maintien de la masse musculaire et dans la gestion de la douleur. Son efficacité repose sur une sélection adaptée du type de courant, un réglage précis des paramètres et une intégration raisonnée dans un protocole global de rééducation.
Bibliographie
- MILLIS, D., & LEVINE, D. (2013). Canine rehabilitation and physical therapy. Elsevier Health Sciences
- BOCKSTAHLER, B., WITTEK, K., LEVINE, D., MAIERL, J., & MILLIS, D. L. (2019). Essential facts of physical medicine, rehabilitation and sports medicine in companion animals. Munich, Germany:: VBS GmbH.
- PAILLARD, T. (2023). Le guide de l'électrostimulation. Amphora.12-61
- CRÉPON, F. (2012). Électrothérapie et physiothérapie: Applications en rééducation et réadaptation. Elsevier Health Sciences.5-56
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Suivi de la fonction rénale lors d'insuffisance cardiaque
Ollioules France
I. Introduction
L'insuffisance cardiaque est une manifestation fréquente chez le chien et le chat, en particulier chez les animaux âgés ou prédisposés à certaines maladies cardiaques. L'évolution de la maladie cardiaque s'accompagne souvent de complications rénales, aboutissant à ce que l'on nomme le syndrome cardio-rénal. Ce dernier désigne l'interdépendance entre le cœur et les reins, où la défaillance de l'un peut précipiter ou aggraver la défaillance de l'autre. Dans ce contexte, le suivi régulier et rigoureux de la fonction rénale chez les animaux insuffisants cardiaques est essentiel pour optimiser la prise en charge, ajuster les traitements et améliorer la qualité de vie.
II. Pourquoi surveiller la fonction rénale en cas d'insuffisance cardiaque ?
Le cœur et les reins sont deux organes majeurs impliqués dans la régulation de l'équilibre hydrique, électrolytique et de la pression artérielle. Lorsqu'une insuffisance cardiaque s'installe, la baisse du débit cardiaque entraîne une diminution de la perfusion rénale, responsable d'une réduction du débit de filtration glomérulaire. Cette hypoperfusion peut conduire à une insuffisance rénale aiguë ou chronique, aggravant le pronostic global. À l'inverse, une maladie rénale peut accentuer la surcharge volémique et la rétention hydrosodée, compliquant la prise en charge de l'insuffisance cardiaque.
De plus, les traitements utilisés en cardiologie vétérinaire, en particulier les diurétiques et les inhibiteurs du système rénine-angiotensine-aldostérone (IECA, antagonistes des récepteurs de l'angiotensine II), peuvent impacter la fonction rénale. Les diurétiques, en augmentant l'excrétion urinaire de sodium et d'eau, peuvent induire une déshydratation et une hypoperfusion rénale. Les IECA, bien que protecteurs à long terme, peuvent aussi entraîner une élévation transitoire de la créatinine.
Ainsi, la surveillance de la fonction rénale chez les animaux insuffisants cardiaques est indispensable pour :
- Détecter précocement une atteinte rénale,
- Adapter les traitements,
- Prévenir les complications métaboliques et électrolytiques,
- Optimiser le pronostic.
III. Quand débuter le suivi rénal ?
Le suivi de la fonction rénale doit être initié dès le diagnostic d'insuffisance cardiaque, quel que soit le stade de la maladie. Même en l'absence de signes cliniques ou biologiques d'atteinte rénale, il est recommandé de disposer d'un bilan rénal de référence avant toute mise en place ou modification du traitement cardiaque.
Certaines situations imposent une vigilance accrue :
- Animaux âgés (plus de 8 ans chez le chien, plus de 10 ans chez le chat),
- Présence de facteurs de risque : hypertension artérielle, antécédents d'insuffisance rénale, races prédisposées,
- Apparition de signes cliniques évocateurs d'atteinte rénale : polyuropolydipsie, amaigrissement, vomissements, léthargie,
- Introduction ou augmentation de posologie de diurétiques ou d'IECA,
- Décompensation cardiaque aiguë.
IV. Comment surveiller la fonction rénale ?
Le suivi de la fonction rénale repose sur une approche multimodale, combinant examen clinique, analyses biologiques et examens complémentaires.
1. Examen clinique
L'examen clinique doit rechercher des signes de déshydratation, d'œdème, d'ascite, d'amaigrissement, de léthargie ou de modifications de la prise de boisson et d'appétit. L'état d'hydratation est particulièrement important à évaluer, car une déshydratation peut aggraver l'atteinte rénale.
2. Analyses sanguines
Urée et créatinine : ce sont les marqueurs classiques de la fonction rénale. Leur élévation traduit une diminution du débit de filtration glomérulaire, mais ils ne sont pas sensibles aux premiers stades de la maladie rénale.
SDMA (Symmetric Dimethylarginine) : ce biomarqueur permet de détecter plus précocement une diminution du débit de filtration glomérulaire, parfois avant même l'élévation de la créatinine.
Bilan ionique : sodium, potassium, chlorures, calcium, phosphore. Les désordres électrolytiques sont fréquents en cas d'insuffisance rénale et avec un traitement diurétique.
Protéines totales, albumine : une hypoalbuminémie peut témoigner d'une perte protéique rénale.
Hématocrite : une anémie peut s'installer en cas d'insuffisance rénale chronique.
3. Analyse d'urine
Densité urinaire : elle permet d'évaluer la capacité de concentration des reins. Une densité inférieure à 1,030 chez le chat ou 1,025 chez le chien est évocatrice d'une atteinte rénale, mais peut être abaissée avec les diurétiques.
Protéinurie : la recherche et la quantification de la protéinurie (rapport protéine/créatinine urinaire, UPC) sont essentielles. Une protéinurie persistante est un facteur de progression de maladie rénale.
Recherche d'infection urinaire : la présence de leucocytes ou de bactéries doit faire évoquer une infection, fréquente chez les animaux insuffisants cardiaques et/ou rénaux.
Recherche de cristaux ou de cylindres : pour orienter vers une cause sous-jacente.
4. Mesure de la pression artérielle
L'hypertension artérielle est fréquente chez les animaux insuffisants cardiaques ou rénaux et peut aggraver la progression de la maladie. Sa mesure régulière est donc incontournable.
5. Imagerie
L'échographie abdominale permet d'évaluer la morphologie rénale, de rechercher des anomalies structurelles (kystes, calculs, dysplasie), d'apprécier la vascularisation et d'exclure une obstruction urinaire. L'échocardiographie complète le bilan en précisant le type et la sévérité de l'atteinte cardiaque.
V. Fréquence du suivi rénal
La fréquence du suivi dépend du stade de la maladie cardiaque, de la stabilité clinique et des résultats des examens précédents.
1. Au diagnostic et lors de toute modification thérapeutique
Un bilan complet (clinique, sanguin, urinaire, pression artérielle, éventuellement imagerie) doit être réalisé au moment du diagnostic d'insuffisance cardiaque et avant toute modification majeure du traitement (introduction ou augmentation de diurétiques, d'IECA, etc.).
Après une modification de traitement, un contrôle est recommandé à 7-10 jours, puis à 1 mois si l'animal est stable.
2. En phase stable
Chez un animal équilibré, un contrôle tous les 2 à 4 mois est conseillé, incluant au minimum un examen clinique, une analyse sanguine (urée, créatinine, SDMA, ions) et une analyse d'urine (densité, UPC).
Chez les animaux à risque (âge avancé, antécédents d'atteinte rénale, protéinurie, hypertension, insuffisance cardiaque évoluée), la surveillance doit être rapprochée, tous les 1 à 2 mois.
3. En cas de décompensation ou de signes cliniques évocateurs
En cas d'apparition de symptômes évocateurs d'atteinte rénale (polyuropolydipsie, vomissements, anorexie, abattement), un bilan immédiat est indispensable.
En cas de décompensation cardiaque aiguë, le suivi doit être intensifié, avec des contrôles parfois hebdomadaires jusqu'à stabilisation.
4. Surveillance à long terme
Une fois la stabilité obtenue, l'espacement des contrôles peut être envisagé, mais il ne faut jamais dépasser 6 mois entre deux bilans chez un animal insuffisant cardiaque, même asymptomatique.
5. Points de vigilance et interprétation des résultats
a) Influence des traitements
Les diurétiques peuvent fausser l'interprétation de la densité urinaire et induire une élévation de l'urée et de la créatinine par déshydratation relative. Il est donc préférable de réaliser les prélèvements avant l'introduction ou l'augmentation des diurétiques, ou d'interpréter les résultats avec prudence.
Les IECA peuvent entraîner une élévation modérée de la créatinine (jusqu'à 30 % par rapport à la valeur de base), tolérable si l'animal reste cliniquement stable.
b) Protéinurie
Une protéinurie persistante, même modérée, doit être prise en charge car elle accélère la progression de la maladie rénale. Une recherche de causes secondaires (infection urinaire, hypertension) est nécessaire.
c) Hypertension
L'hypertension artérielle doit être recherchée systématiquement car elle aggrave les lésions rénales et cardiaques. Sa correction améliore le pronostic.
d) Hydratation
La surveillance de l'état d'hydratation est essentielle, notamment sous diurétiques. Une déshydratation aggrave la fonction rénale et peut nécessiter une adaptation du traitement.
VI. Conclusion
Le suivi de la fonction rénale chez le chien et le chat insuffisants cardiaques est un pilier de la prise en charge globale. Il doit être systématique, régulier et adapté à chaque patient. L'objectif est de dépister précocement les complications rénales, d'ajuster les traitements en conséquence, et d'optimiser la qualité et la durée de vie des animaux concernés.
En pratique :
- Initier le suivi rénal dès le diagnostic d'insuffisance cardiaque,
- Utiliser une approche multimodale (clinique, biologique, imagerie),
- Adapter la fréquence des contrôles à la stabilité clinique et à l'évolution de la maladie,
- Être particulièrement vigilant lors de l'introduction ou de la modification des traitements et en cas d'apparition de nouveaux symptômes.
Une collaboration étroite entre le vétérinaire, le propriétaire et, si besoin, le spécialiste en cardiologie ou en néphrologie vétérinaire, permet d'optimiser la prise en charge des chiens et chats souffrant d'insuffisance cardiaque et de prévenir la progression du syndrome cardio-rénal.
VII. Bibliographie
[1](https://ppl-ai-file-upload.s3.amazonaws.com/web/direct-files/attachments/46167698/7558e057-1bd4-4dc9-8b81-253ea49695cc/proceeding.txt)
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Suture digestive classique
Ollioules, France
I. Introduction
La déhiscence digestive est la complication la plus redoutée lors d'une suture digestive et survient entre 4 et 18%. [1,2] Elle est plus fréquente en cas d'entérectomie que lors d'une entérotomie [2], et reste très rare en cas de suture d'une gastrotomie. Une technique maîtrisée est essentielle pour limiter les risques de déhiscence.
II. Les bons choix de technique
1. Quel type de suture utiliser ?
Une suture digestive peut être réalisée manuellement ou à l'aide de pinces à auto-suture. Lorsqu'elle est réalisée manuellement, elle peut se faire via un surjet ou par points simples. Aucune différence significative n'existe entre ces deux dernières techniques en matière de risque de déhiscence. Une suture digestive par surjet est plus rapide, elle laisse moins de fil au sein du tissu suturé et est associée à une meilleure apposition digestive avec seulement 38% des cas qui présentent une éversion ou une inversion. La suture digestive par surjet est donc la technique de choix.
Le surjet se doit d'être le plus apposant possible, afin de permettre une guérison par première intention. En effet, on évitera les sutures éversantes, qui ont tendance à augmenter les adhérences abdominales, tout comme on évitera les sutures inversantes, qui ont tendance à réduire la lumière intestinale. Les sutures éversantes comme inversantes guérissent par seconde intention du fait de la mauvaise apposition digestive et représentent un risque augmenté de déhiscence de suture. Sur l'intestin, la suture sera réalisée en une couche, les sutures en deux couches ayant un risque trop important de sténose postopératoire. Lors d'anastomose digestive faisant suite à une entérectomie, deux hémi-surjets seront réalisés. En cas de suture gastrique, elle pourra être réalisée en une ou deux couches sans différence de résultat. Si la suture gastrique est réalisée en deux couches, le premier surjet est réalisé sur la muqueuse gastrique de manière apposante. La seconde couche intéresse alors la sous-muqueuse, la musculeuse et la séreuse et peut être soit apposante soit inversante.
La couche histologique responsable de la résistance mécanique au sein du tractus digestif est la sous-muqueuse. Il est donc indispensable que la sous-muqueuse soit intégrée à chaque passage de la suture. Lorsque la sous-muqueuse est manquée par la suture, il existe un risque augmenté de déhiscence digestive, notamment lors de la période de collagénolyse qui se déroule dans les 3 à 5 jours postopératoires.
Il est couramment recommandé de réaliser des sutures non perforantes lorsqu'il s'agit de suturer le tractus digestif. Toutefois, le risque de manquer la sous-muqueuse en s'astreignant à réaliser une suture non perforante est plus important que le risque de contamination par une suture perforante. Ainsi, il faudra toujours s'assurer du passage de la suture à travers la sous-muqueuse plutôt que de s'assurer de la non-pénétration de la muqueuse, ce qui est d'autant plus vrai sur les parois digestives fines où la distinction des couches intestinales est beaucoup plus difficile. Autrement dit, il faudra toujours privilégier une suture perforante à une suture trop superficielle qui risque de manquer la sous-muqueuse. Afin de pallier ces deux problématiques, le point de Gambee modifié, qui est un point perforant permettant d'enfouir la muqueuse, est très intéressant à utiliser lors de suture intestinale car il permet une apposition digestive optimale.
2. Quelle suture utiliser ?
Les sutures digestives seront réalisées à l'aide de monofil résorbable. En effet, les fils tressés sont associés à une adhérence bactérienne et une capillarité non adaptées aux sutures dans le tractus digestif. Les sutures irrésorbables sont quant à elles associées à une réaction inflammatoire marquée et prolongée sans que leur tenue mécanique supérieure soit bénéfique pour une suture digestive. Les fils les plus couramment utilisés sont le poliglecaprone 25 (Monocryl®), le polydioxanone (PDS II®) et le glycomer 631 (Biosyn®). Selon la taille de l'animal, la suture utilisée sera du décimale 1,5 (4-0) ou du décimale 2 (3-0).
Les aiguilles utilisées seront obligatoirement de section ronde ou tapercut afin de limiter le traumatisme et la déchirure du tractus digestif. Les aiguilles à section tranchante sont contre-indiquées.
III. En pratique : réaliser une anastomose digestive après entérectomie
1. Étape 1 : isoler l'anse digestive
La première étape consiste à isoler l'anse intestinale d'intérêt du reste de la cavité abdominale. Ceci a pour objectif de limiter la contamination, que ce soit en cas de fuite digestive, ou lors de la réalisation de l'anastomose. L'isolement est permis par l'utilisation de compresses à laparotomie humidifiées.
2. Étape 2 : ligaturer la vascularisation mésentérique
Il est important d'évaluer la zone à réséquer ainsi que la vascularisation attenante. En effet, la ligature de la vascularisation mésentérique doit être adaptée à la zone d'entérectomie. On veillera à toujours réaliser l'entérectomie en zone saine, en faisant le sacrifice de plusieurs millimètres de tissu sain en cas de lésion nécrotique, de plusieurs centimètres en cas de lésion tumorale.
Une fenestration mésentérique est réalisée au pourtour des artères et veines mésentériques à ligaturer puis celles-ci sont sectionnées. Lors de la section du mésentère le long des artères et veines, on veillera à préserver plusieurs millimètres de mésentère sain au pourtour des artères mésentériques conservées afin de ne pas les léser lors de la suture du mésentère en fin de chirurgie. La ligature/section des artères mésentériques permet de localiser rapidement la zone d'ischémie intestinale créée : on s'assurera alors de réaliser l'entérectomie en dehors de cette zone ischémique.
Il est également nécessaire de ligaturer les artères et veines que l'on trouve au bord mésentérique, au plus proche de l'anse intestinale retirée, afin d'optimiser l'hémostase.
3. Étape 3 : réaliser l'entérectomie
Avant de retirer l'anse affectée, il convient de la vider de son contenu en le repoussant manuellement oralement et aboralement. À la suite de cette manipulation, l'anse à retirer est isolée à l'aide de pinces de Doyen ou des doigts de l'assistant afin de créer une occlusion digestive temporaire le temps de l'entérectomie, dans le but de limiter la contamination abdominale par du contenu digestif. L'occlusion doit être faite à distance (3-5 centimètres) de la zone à retirer.
Une fois le tractus digestif occlus, l'entérectomie peut être réalisée, à l'aide d'une lame froide ou d'une paire de ciseaux de Metzenbaum. La section intestinale est toujours réalisée de manière oblique, afin d'optimiser la longueur du bord mésentérique aux dépens du bord anti-mésentérique. En effet, la vascularisation du bord mésentérique étant bien supérieure à celle du bord anti-mésentérique, préserver un maximum de cette vascularisation permet d'optimiser la cicatrisation. Une fois le tube digestif sectionné, l'anse intestinale retirée est extraite du site chirurgical en la maintenant occlue.
4. Étape 4 : gérer le diamètre luminal
Le diamètre des deux portions de tube digestif peut parfois être sensiblement différent, notamment lors d'une occlusion digestive qui a conduit à la dilatation de la zone en amont, ou lors de l'exérèse de la jonction iléo-caeco-colique avec anastomose iléo-colique. Dans ces cas, il peut être nécessaire d'adapter le diamètre des deux portions de tube digestif à anastomoser. Pour ce faire, 4 solutions techniques sont décrites. La première est d'espacer les sutures de manière plus importante sur l'anse la plus large, de manière à pallier progressivement la différence de diamètre. La seconde est de réaliser la section digestive de manière fortement oblique, ce qui a comme conséquence d'augmenter la surface de tractus digestif en section, et ainsi d'augmenter son diamètre. La troisième est d'inciser l'anse digestive la plus étroite sur son bord anti-mésentérique sur quelques millimètres, afin d'augmenter son diamètre. Cette technique est la plus couramment utilisée. Enfin, la quatrième technique vise à réduire le diamètre luminal de l'anse la plus large par une suture digestive.
5. Étape 5 : réaliser l'anastomose digestive
L'objectif de l'anastomose digestive est de réaliser une apposition la plus optimale que possible pour obtenir une guérison par première intention et ainsi limiter le risque de déhiscence. En effet, plus la suture sera éversante (contact muqueux) ou inversante (contact séreux), moins la guérison sera rapide et de bonne qualité.
Il est fréquent d'observer une éversion marquée de la muqueuse digestive suite à l'entérectomie. Cet « excédent » de muqueuse peut ainsi être excisé à l'aide de ciseaux de Metzenbaum afin d'obtenir une section digestive plus franche sans éversion muqueuse, ce qui facilitera la suture. La suture peut également être effectuée en utilisant le point spécifique dit de « Gambee modifié ». Ce point a pour effet d'obtenir une très bonne apposition digestive, tout en incorporant la sous-muqueuse dans la suture et en enfouissant la muqueuse. Après avoir traversé la sous-muqueuse (le plus souvent en étant perforant), le fil de suture doit ressortir superficiellement à la muqueuse sur la zone de section digestive, puis entrer à nouveau superficiellement à la muqueuse dans l'autre anse afin d'enfouir la muqueuse, pour ainsi ressortir de l'anse après avoir perforé la sous-muqueuse.
L'anastomose digestive débute par la mise en place de deux points, aux bords mésentériques et anti-mésentériques, puis ces deux points sont rejoints à l'aide de deux hémisurjets. La suture est réalisée à 3 mm de la section digestive et les points de passage de la suture sont eux-mêmes espacés de 3 mm.
6. Étape 6 : fermeture du mésentère et omentectomie
La fermeture du mésentère est indispensable pour éviter le passage d'anses intestinales à travers la fenestration mésentérique et une éventuelle strangulation. Lors de la fermeture du mésentère, il faut être très vigilant à préserver la vascularisation mésentérique restante afin de ne pas compromettre la viabilité d'une anse intestinale. Il est donc important, lors de la section initiale de mésentère, de laisser plusieurs millimètres de tissu au pourtour des artères et veines afin de faciliter la fermeture du mésentère.
L'omentum est un tissu aux propriétés angiogéniques, immunogéniques et d'adhésion. Il facilite ainsi la guérison intestinale par l'apport de nombreux facteurs de cicatrisation. Une fois apposé, l'omentum peut être fixé à l'anse digestive, à distance de quelques centimètres de la zone anastomosée.
Bibliographie
- DUELL JT et Coll. Frequency of Dehiscence in Hand-Sutured and Stapled Intestinal Anastomoses in Dogs. Vet Surg 2016 Jan;45(1):100-3.
- LOPEZ DJ et coll. Comparison of patient outcomes following enterotomy versus intestinal resection and anastomosis for treatment of intestinal foreign bodies in dogs. J Am Vet Med Assoc. 2021 Jun 15;258(12):1378-1385.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Sutures cutanées
Nantes, France
I. Introduction
La fermeture cutanée constitue une étape fondamentale de la chirurgie des tissus mous, quelle que soit l’espèce animale concernée. Bien que la phase d’exérèse ou de réparation occupe souvent le centre de l’attention du chirurgien, c’est sur la qualité de la suture cutanée que les propriétaires jugeront notre travail. Seul élément apparent, elle conditionne l’aspect esthétique de l’intervention. Une mauvaise adaptation des berges, une tension excessive ou un choix inadéquat du fil peuvent compromettre la cicatrisation et entraîner des complications telles que la déhiscence ou l’infection.
L’objectif de cette intervention est double : d’une part, rappeler les principales sutures cutanées utilisées en pratique courante, en détaillant leurs indications spécifiques ; d’autre part, présenter pas à pas leur réalisation technique, afin de permettre au praticien et à l’étudiant d’acquérir une véritable compétence gestuelle.
II. Principes généraux des sutures cutanées
Avant de détailler chaque technique, quelques principes de base méritent d’être rappelés.
1. Respect de la biologie tissulaire
La vascularisation cutanée chez le chien et le chat dépend essentiellement des plexus dermiques et sous-dermiques. Une manipulation atraumatique des tissus et une tension modérée des sutures sont donc cruciales afin de ne pas compromettre cet apport vasculaire indispensable à la cicatrisation [1-4].
2. Choix du matériel [3]
Compte tenu de la résistance du tissu cutané, on privilégiera l’utilisation d'aiguilles triangulaires ou à section inversée (cutting, reverse cutting, aiguille pointe diamant) afin de faciliter la pénétration de l’aiguille au sein du tissu. Les aiguilles rondes seront éventuellement adaptées aux plans sous-cutanés mais ne seront pas conseillées pour la suture du derme et de l’épiderme (suture cutanée ou suture intradermique)
On privilégiera des fils monofilaments synthétiques plutôt que des fils tressés en raison de leur moindre réactivité au sein des tissus (moins phlogogène) et de leur moindre capillarité (effet mèche) comparativement aux fils tressés non enduits.
En condition normale, compte tenu de la vitesse de cicatrisation relativement lente de la peau et de la faible résistance mécanique de la plaie lors des phases initiales de la cicatrisation et des possibles sollicitations de l’animal, on retiendra l’utilisation de fils irrésorbables (coût moindre) ou résorbables « lent » (polydioxanone, poliglecaprone). La taille du fil doit présenter une résistance au moins similaire à résistance du tissu suturé, un fil monofilament de décimale 1,5 ou 2 sera adapté pour une majorité des cas lors de suture d’une plaie sans tension particulière.
3. Conditions de fermeture
L’enjeu est ici d’obtenir une cicatrisation par première intention. Pour y parvenir, un certain nombre de conditions doivent être réunies :
- des conditions d’asepsie, la plaie doit être exempte de tissus dévitalisés, de corps étrangers et de germes ;
- des conditions de viabilité des tissus support de cicatrisation (intégrité, vascularisation) ;
- des conditions d’apposition et d’immobilité des berges et d’absence de collection qui vont être assurées en grande partie par la technique de suture cutanée utilisée.
D’un strict point de vue de la technique chirurgicale, il s’agit donc de trouver le bon compromis permettant d’assurer l’accolement précis des berges, de répartir les tensions, de maintenir une fermeture hermétique tout en préservant la vascularisation et l’intégrité de la peau, afin d’obtenir une cicatrice discrète et fonctionnelle. Le plan de fermeture doit tenir compte de la position naturelle de la peau. Il est recommandé d’examiner l’animal en station debout avant chirurgie afin d’évaluer la tension exercée par les tissus environnants. En peropératoire, la position du patient influence l’aspect de la plaie une fois l’animal réveillé. Des zones cutanées mobiles (tronc, flancs) peuvent être déplacées artificiellement par la gravité ou par la fermeture de l’espace mort, induisant des plis ou des saillies cutanées. Une installation correcte, sans traction parasite de la peau, est donc primordiale.
4. Sécurité des nœuds
Toute suture va reposer sur la réalisation d’un nœud qui doit être à la fois solide et peu volumineux. La sécurité va dépendre du nombre de boucles : 3-4 boucles seront suffisantes pour la plupart des fils tressés, jusqu’à 5-6 pour les fils monofilaments plus glissants.
Les extrémités des fils enfouis doivent être coupées à 3–5 mm pour éviter le relâchement, tandis que les extrémités des sutures externes peuvent être laissées plus longues afin de faciliter leur retrait. Le nœud d’Aberdeen, particulièrement adapté aux sutures continues, présente une sécurité accrue et un volume réduit.
III. Techniques de suture
1. Sutures sous-cutanées
Il est conseillé que la fermeture du plan cutané soit entreprise après une étape préalable d’apposition et de fermeture du plan sous-cutané. Si la présence d’une suture sous-cutanée va entrainer une inflammation locale temporaire et peut potentiellement compromettre la vascularisation du derme, ces inconvénients sont très largement compensés par les bénéfices attendus : elle va participer à l’apposition et à l’immobilisation des berges de la plaie, et permettre de limiter les espaces morts sous la plaie et donc le risque de collection [1-4].
Réalisée avec un fil résorbable monofilament ou tressé (plus inflammatoire), cette suture peut faire appel à des points séparés ou à un surjet continu. Le surjet continu est plus rapide et nécessite moins de fil, mais expose à une déhiscence globale en cas de rupture. Un ou deux plans peuvent être réalisés selon l’épaisseur du pannicule adipeux. Les morsures doivent correspondre à l’épaisseur du tissu pris.
Au cours de la suture du plan sous-cutané, il est possible d’ancrer le fil dans les plans sous-jacents afin de limiter la création d’espace mort. Ces points ne doivent pas être trop nombreux et seront surtout à considérer dans les zones où le risque de décollement cutané et de mobilité est important, mais il faut garder en tête qu’ils vont entrainer des adhérences potentiellement inconfortables et inesthétiques [2].
2. Sutures cutanées externes [3]
Elles vont permettre de réunir les berges de la plaie au niveau de l’épiderme et du derme. De nombreux patrons de suture peuvent être utilisés pour la fermeture cutanée.
Pour les plus courants, on retiendra :
- Points simples séparés (technique de base, sûre et modulable) ;
- Surjet simple (rapide, bonne répartition de la tension) ;
- Points en croix (améliorent l’alignement) ;
- Surjet à points passés (utilisé pour les incisions longues).
a) Points simples
- Technique : passage de l’aiguille perpendiculaire aux berges, situé à 3–5 mm des berges de la peau. Espacement des points de 5 mm à 1 cm.
- Indications : fermeture cutanée de routine, plaies de petite ou moyenne taille, zones de faible tension.
- Avantages : fiabilité, facilité d’exécution, possibilité de retirer certains points sans compromettre l’ensemble.
- Limites : temps opératoire plus long que les sutures continues, marques cicatricielles plus visibles.
b) Points en X
- Technique : croisement du fil formant une croix sur la surface cutanée. Ancrage du fil à 3–5 mm des berges de la peau. Espacement des branches du X de 5 mm à 1 cm. Chaque point en X peut être espacé de quelques millimètres du suivant.
- Indications : fermeture rapide, renforcement ponctuel de zones fragiles. Bonne reprise de la tension.
- Avantages : bonne résistance mécanique.
- Limites : moins esthétique, plus de matériel résiduel en surface. Risque de froncement des berges de plaies si point trop serré.
c) Suture continue surjet simple
- Technique : passage en spirale le long de la plaie. Ancrage à 3–5 mm des berges et espacement de 5–10 mm entre deux passages.
- Indications : plaies longues, fermeture rapide.
- Avantages : gain de temps opératoire, tension homogène.
- Limites : si rupture du fil (mutilation, tension excessive, ou nécrose ischémique de la berge cutanée) → déhiscence sur toute la ligne.
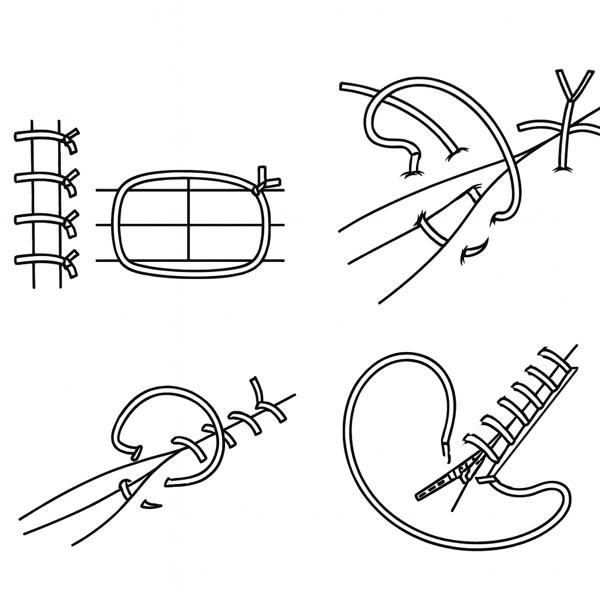
Figure 1 - Principales sutures cutanées : point simple, point en croix, surjet simple et surjet à points passés
3. Suture intradermique
- Technique : passage du fil dans l’épaisseur du derme profond en alternance droite-gauche, fil résorbable monofilament. Espacement de 4–5 mm entre chaque passage en surjet simple vertical ou horizontal.
- Indications : chirurgie de convenance (stérilisation), chirurgie esthétique, zones visibles (face).
- Avantages : très bon résultat esthétique, pas de retrait de points nécessaire.
- Limites : technique plus délicate, risque de déhiscence si rupture.
4. Gestion des « dog ears »
Gestion des « dog ears » ou oreilles de cochons... La fermeture de plaies circulaires ou ovalaires génère fréquemment des replis cutanés aux extrémités de la plaie, parfois gênants (esthétisme, favorisant séromes), même si leur impact fonctionnel reste souvent très limité. [1,2,4]
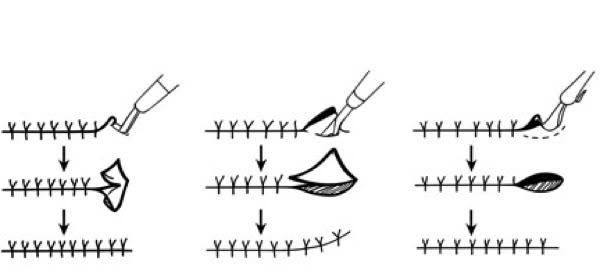
Figure 2 - Gestion des plis excédentaires ("oreilles de cochon" ou "dog ears") lors de suture cutanée
Les petits replis (<8 mm) peuvent régresser spontanément. Des techniques de suture spécifiques peuvent corriger les anomalies légères. Les excédents cutanés plus importants nécessitent une exérèse en triangle ou en côte de melon.
Lors de chirurgie reconstructrice cutanée complexe (chirurgie oncologique, utilisation de lambeau) il est judicieux de préserver ces replis cutanés qui constituent des stocks de peau utile si une chirurgie de reprise devait être réalisée ultérieurement.
Bibliographie
- PAVLETIC MM. Atlas of Small Animal Wound Management and Reconstructive Surgery. Wiley-Blackwell, 2018.
- FOSSUM TW. Small Animal Surgery. 5th ed., ELSEVIER, 2019.
- SMEAK DD. Suture materials, patterns, and principles of closure. Vet Clin North Am Small Anim Pract, 2020; 50(1): 1–23.
- SINGER AJ, DAGUM AB. Current management of acute cutaneous wounds. N Engl J Med, 2008; 359: 1037–1046.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Sutures en tension : comment relâcher
Nantes, France
I. Introduction
Chez les carnivores domestiques, comme chez l'homme, l'excès de tension au niveau d'une ligne de suture est l'un des principaux facteurs de complications postopératoires : retard de cicatrisation, déhiscence, nécrose cutanée, séromes. L'objectif du chirurgien n'est donc pas uniquement de rapprocher deux berges cutanées, mais de le faire dans des conditions optimales de répartition des forces mécaniques tout en préservant la vascularisation. Pour y parvenir, plusieurs stratégies opératoires et postopératoires ont été développées afin de réduire ou redistribuer les tensions.
II. Bases biologiques et mécaniques
La peau est un tissu viscoélastique qui va être capable d'un allongement progressif lorsqu'il est soumis à une tension constante (observé en quelques heures) et d'une capacité à se relâcher (relaxation de contrainte) qui va permettre au fil du temps de diminuer la force nécessaire pour maintenir une extension donnée, au fil du temps. Ces propriétés sont exploitées dans les techniques de pré-étirement cutané (skin stretchers, expanseurs tissulaires, ou certaines sutures qui sollicitent progressivement la peau). Elles peuvent être mises en œuvre préalablement au geste opératoire lorsqu'un problème de tension est anticipé.
La tension cutanée varie également selon la région anatomique et l'espèce : la peau est lâche sur le tronc mais tendue sur les extrémités distales ; les lévriers présentent une peau fine et peu extensible, chez le chat, la peau est globalement plus mobile et élastique.
En fonction de la région anatomique, des lignes de tension sollicitent le plan cutané selon un axe spécifique. La prise en compte de ces lignes de tension permet, lorsque cela est possible, de choisir le sens de l'incision afin de l'orienter parallèlement aux lignes de tension et de limiter les forces qui s'exerceront aux berges.
Comprendre ces variations est essentiel pour anticiper la faisabilité d'une fermeture et choisir la technique de relâchement adaptée.
III. Méthodes de réduction de tension en peropératoire
Il ne sera pas traité ici des gestes plus techniques reposant sur la réalisation de lambeaux ou de plasties complexes.
1. Positionnement du patient
La position de l'animal sur la table influence considérablement la mobilité cutanée. L'utilisation de sacs de sable/coussins permet de libérer les replis cutanés piégés par le poids du corps.
2. Décollement cutané
Il s'agit de la technique la plus utilisée. Le décollement cutané réalisé en profondeur sous le muscle panniculaire permet de libérer les adhérences de la peau aux tissus sous-jacents tout en préservant le plexus sous-dermique. Cet espace de glissement augmente la mobilité des berges. Un décollement atraumatique, aux ciseaux de Metzenbaum, est recommandé pour minimiser les lésions vasculaires.
3. Incisions de décharge
Une incision parallèle à la plaie principale permet de créer un lambeau bipédiculé qui sera avancé pour recouvrir le défaut. Le site donneur est laissé à cicatriser par seconde intention ou refermé secondairement. Cette méthode est indiquée pour des plaies en zone peu esthétique ou peu exposée.
Les variantes telles que les incisions multiples (en mesh : petites incisions parallèles disposées en quinconce) sont particulièrement utiles sur les extrémités.
IV. Méthodes de redistribution de tension
1. Sutures sous-cutanées spécifiques : walking sutures
Décrites par S.F. SWAIM, elles consistent à ancrer la peau décollée au fascia sous-jacent par une série de points progressifs, rapprochant la peau vers le centre du défaut. Ces sutures répartissent les contraintes sur une large surface et évitent que toute la tension ne repose sur la ligne cutanée. Les inconvénients incluent la formation de petites fossettes cutanées (qui disparaissent avec l'absorption du fil) et un risque théorique de perturbation vasculaire (risque limité si le nombre de points mis en place reste raisonnable)
2. Sutures cutanées spécifiques
Le point simple de matelassier (vertical) et les techniques de points « far-near-near-far » ou « far-far-near-near » permettent de répartir la force perpendiculairement à la plaie. Le point simple de matelassier horizontal est moins conseillé en raison d'un risque d'ischémie plus important. L'ajout de sutures intradermiques ou sous-cutanées permet également de renforcer la fermeture et de réduire la tension s'exerçant en superficie aux berges de la plaie.
Les points d'appui à distance : points posés à distance de la plaie, souvent appuyés sur des boutons ou tubulures, servent à répartir la pression et à limiter le risque ischémique.
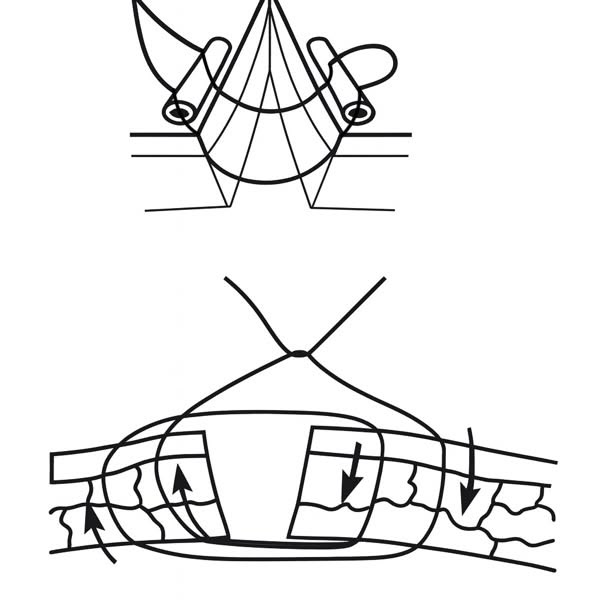
Figure 1 - Exemple de quelques sutures utilisable pour mieux repartir un excès de tension lors de la fermeture cutanée : point simple de matelassier (U horizontal) en appui sur des tubulures et point « far-far-near-near / loin-loin-près-près »
3. Utilisation de stents, pansement et bandes de tension
Les stents (rouleaux de gaze, tubulures) répartissent la charge mécanique des fils sur une surface plus large. Le stent le plus couramment employé en médecine vétérinaire consiste en rouleaux de compresses stérilisés, fixées au-dessus du site de fermeture. Plusieurs méthodes permettent de les fixer : points de rétention transfixiants, englobant toutes les couches de fermeture tissulaire, peuvent être noués par-dessus les rouleaux de gaze, ou boucles peuvent être placées à 3–4 cm de l'incision à la manière d'un pansement corbeille : un fil de suture est ensuite passé entre les boucles opposées, à la manière d'un laçage de chaussure.
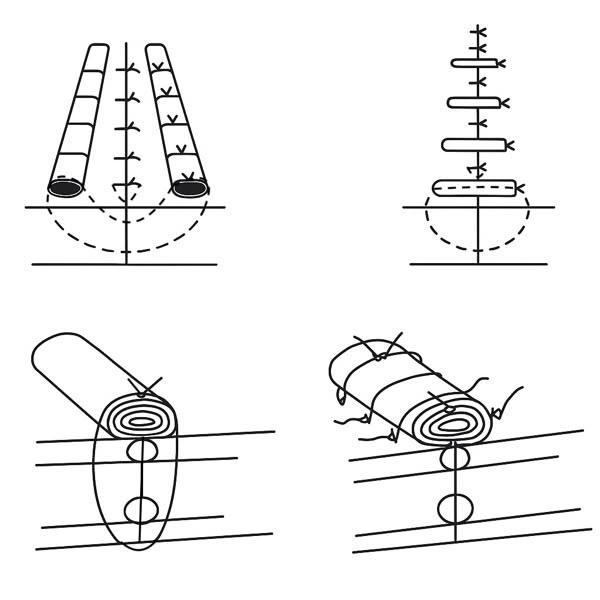
Figure 2 - Exemple de quelques points utilisable pour mieux repartir un excès de tension lors de la fermeture cutanée : points en appuis sur tubulures (stent) ou bande de gaze pour mieux répartir la tension (point en U vertical sur tubulure, points simples sur tubulure, et points en appui sur compresse ou bande de gaze)
La mise en place de bandes velcro perpendiculairement à l'axe de la plaie a également été décrite. Les scratchs sont alors suturés à distance à la manière des points d'appui et la bande est appliquée afin de reprendre la tension de part et d'autre des berges de la plaie.
Les pansements compressifs ou les attelles peuvent aussi limiter la mobilité articulaire et réduire les forces de traction sur la cicatrice lorsque celle-ci est à proximité de la base d'un membre ou sur le membre.
V. Conclusion
La gestion de la tension sur une ligne de suture est un facteur déterminant de succès en chirurgie reconstructrice vétérinaire. Les complications liées à une fermeture forcée sous tension dépassent largement les bénéfices apparents d'une couverture immédiate.
La clé réside dans une planification raisonnée, intégrant l'anticipation des lignes de tension et l'utilisation combinée de plusieurs techniques de dispersion et répartition de la tension.
En pratique, le chirurgien dispose d'un arsenal varié : du simple décollement cutané aux incisions de décharge, en passant par les plasties locales, les sutures spécifiques et les dispositifs mécaniques. Les sutures de décharge de tension ne doivent pas être utilisées en présence d'une tension cutanée modérée à sévère ; dans de tels cas, d'autres techniques de reconstruction (lambeaux, plastie complexe) sont plus appropriées.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Syncopes d'origine cardiaque
Merignac, France
I. Introduction
Une syncope correspond à une perte de conscience et de tonicité soudaine et transitoire, dont la récupération est en général spontanée et rapide. L'évaluation des syncopes est souvent un défi, les crises étant imprévisibles, espacées dans le temps, et l'animal asymptomatique entre deux épisodes.
1. Distinguer une syncope d'un autre type de malaise
Cette étape passe par un recueil rigoureux de l'anamnèse. En effet, du fait de leur nature sporadique, il est rare pour le clinicien d'observer directement les malaises dans le cadre de la consultation. C'est donc leur description par le propriétaire qui orientera la suspicion.
Le diagnostic différentiel des malaises associés à des baisses de tonus postural +/- perte de conscience inclut les crises convulsives, la narcolepsie/cataplexie, la faiblesse liée à des causes métaboliques (hypoglycémie, hypocorticisme, troubles électrolytiques, anémie…) et des affections neuromusculaires (myasthénie grave, collapsus à l'exercice du Labrador, polyneuropathie, polymyopathie…).
Des indices, répertoriés dans le Tableau 1, peuvent cependant mettre sur la voie.
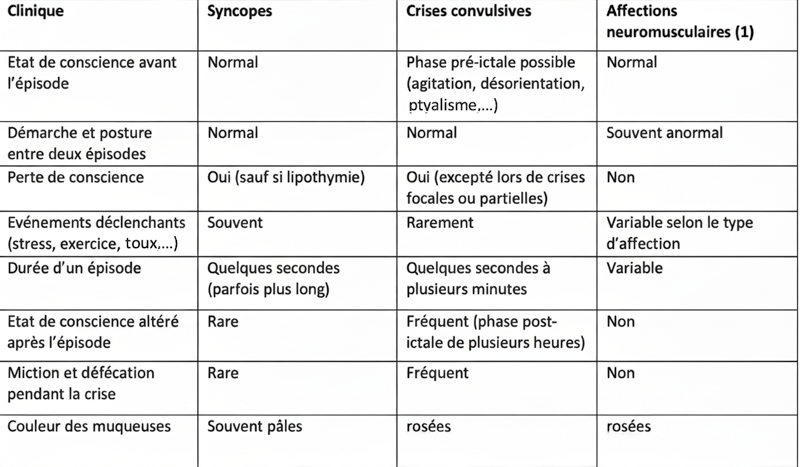
Tableau 1 : éléments aidant au diagnostic différentiel des malaises associés à des pertes de
conscience et/ou de tonus postural. D'après [4]
Notons qu'il existe des malaises de type lipothymies (ou pré-syncopes), qui sont moins intenses et sans perte de conscience associée. Inversement, certaines hypoxies cérébrales, lorsqu'elles durent, peuvent induire des crises convulsives et un temps de récupération plus long. La frontière entre syncopes et crises convulsives est alors peu évidente.
Dans certain cas, la frontière est si floue qu'il est presque impossible de trancher et il peut être intéressant de demander au propriétaire de filmer les épisodes.
II. Autres syndromes paroxystiques
Ces syndromes entrent dans le diagnostic différentiel des syncopes. Il est important de les avoir à l'esprit lors de la consultation pour poser les bonnes questions et rechercher des signes qui nous aiderons à définir la nature des symptômes observés.
1. La crise épileptique
Bien que protéiforme, c'est une manifestation plutôt « en hyper » se caractérisant par tout ou partie des signes suivants : hypertonicité focale ou généralisée, altération de la vigilance, symptômes végétatifs et modifications du comportement.
Les différentes parties de la crise
Une crise connait une expression clinique variable. On peut reconnaître différentes parties au sein de la crise : les prodromes qui sont des manifestations comportementales qui précèdent la crise pendant plusieurs heures ou plusieurs jours, l'aura qui est une manifestation motrice ou comportementale qui précède immédiatement la crise de quelques instants et qui traduit une activité électrique anormale, l'ictus qui est la crise en elle-même et la phase post-ictale qui est indépendante de l'intensité et de la durée de la crise et qui se traduit par un déficit neurologique symétrique (confusion, comportement anormal, amaurose…) Cette dernière dure généralement moins d'une heure mais peut persister plusieurs jours.
2. Le syndrome narcolepsie
Chez l'animal, il se traduit par des épisodes de cataplexie : c'est une perte brutale du tonus musculaire avec ou sans endormissement. Ces épisodes sont souvent provoqués par des jeux ou l'accès à la nourriture. En fin d'épisode, il y a un brutal retour à la normale et l'animal reprend son activité là où il l'avait arrêtée. Il existe des formes héréditaires liées à des mutations dans le gène du récepteur à l'hypocrétine (Labrador, Pinscher et Teckel). Il existe des formes acquises en particulier chez les vieux chiens.
3. La crise algique
Les crises algiques, en particulier secondaires à des hernies discales cervicales, sont parfois difficiles à différencier de crises convulsives partielles. Elles se traduisent par des épisodes où le chien, souvent un petit brachycéphale (Bouledogue Français…) ou un Beagle, pousse un cri, se contracte avec la tête basse et refuse d'avancer, comme sidéré.
4. Les mouvements anormaux
Crampe, myoclonie, fasciculations, collapsus induit par l'exercice, et autres dyskinésies…
Ces mouvements sont susceptibles d'être confondus avec une crise partielle simple. Les circonstances d'apparition ou la race sont des éléments d'aide au diagnostic différentiel.
5. Connaître l'étiologie des syncopes pour s'orienter vers une cause cardiaque ou neuro-médiée
Chez le chien et le chat, les syncopes résultent d'une baisse subite de perfusion cérébrale ou d'approvisionnement en substrats essentiels. Trois mécanismes principaux sont retenus :
- une baisse de débit cardiaque (par défaillance systolique, obstruction à l'éjection, défaut de remplissage cardiaque, bradyarythmie, tachyarythmie) ;
- une hypoxie ou une hypoglycémie avec débit cardiaque conservé ;
- une vasodilatation transitoire des artérioles systémiques.
Le Tableau 2 résume les principales causes de syncope, qu'il faut connaître afin d'adopter la démarche diagnostique adéquate. Elles sont divisées en syncopes cardiaques, neuromédiées, métaboliques et médicamenteuses.

Tableau 2 : classification, causes et prédispositions raciales lors de syncope chez le chien et le chat
a) Les causes cardiaques
Dans la plupart des cas, il s'agit d'arythmies (majoritairement des bradyarythmies, mais également des tachyarythmies).
En dehors des arythmies, des anomalies cardiaques structurales (maladies valvulaires, myocardiques, péricardiques) peuvent être la cause de syncopes (Tableau 2). Dans ce cas les syncopes sont parfois multifactorielles, puisque ces affections peuvent entraîner des arythmies ou des syncopes réflexes (cf infra).
b) Les syncopes neuro-médiées (ou réflexes)
On distingue les syncopes vasovagales (de loin les plus fréquentes), les syncopes situationnelles et l'hypotension orthostatique.
Les syncopes vasovagales sont dues à une stimulation adrénergique du baro-réflexe, initiée par une stimulation orthosympathique prolongée. Il en découle une vasoconstriction, une augmentation de la fréquence et de la contractilité cardiaque. Le volume d'éjection systolique diminue, les ventricules n'ayant pas le temps de se remplir. S'ensuit une stimulation de l'afférence vagale au niveau du tronc cérébral par les mécanorécepteurs ventriculaires et carotidiens, et donc une inhibition orthosympathique, responsable d'une vasodilatation et d'une bradycardie qui entrainent une hypoxie cérébrale, d'où la syncope . L'exemple classique est celui du chien qui tire sur sa laisse avant une course, ou d'un animal qui se lève brusquement après un sommeil prolongé.
La 1ère étape peut être shuntée dans certains cas, où c'est directement le réflexe vagal qui est déclenché (syncope situationnelle consécutive de toux, vomissements, miction, défécation…).
III. Démarche diagnostique lors de syncope
1. Anamnèse et examen clinique : des étapes cruciales
L'examen clinique et le recueil de l'anamnèse sont des étapes cruciales dans la prise en charge des syncopes ; une attention particulière sera donnée à la présence d'un souffle ou d'une arythmie cardiaque, bien qu'il ne soit pas rare que l'examen cardiovasculaire d'un animal atteint de syncope soit normal. Comme nous l'avons vu, un examen neurologique complet est aussi utile dans le cas où un doute persisterait sur la nature des crises.
L'anomalie la plus fréquemment repérée est une arythmie cardiaque. Même si le fait d'entendre une anomalie auscultatoire ne garantit pas qu'elle soit la cause des syncopes, elle doit être considérée comme telle jusqu'à preuve du contraire.
2. Examens complémentaires
Les examens complémentaires à réaliser comprennent des analyses biochimiques (incluant ionogramme, glycémie et calcémie) et une numération-formule sanguine afin d'écarter une cause métabolique de malaise.
Une mesure de pression artérielle systémique doit être réalisée afin d'exclure une hypotension, bien qu'une pression normale ne permette pas d'exclure des épisodes transitoires d'hypotension n'ayant lieu que lors des syncopes.
La réalisation d'un électrocardiogramme est primordiale. Dans certains cas il peut être diagnostique de l'origine des syncopes : c'est le cas lors de BAV 3, de syndrome de l'oreillette silencieuse, de bradycardie sévère ou de tachycardie supraventriculaire ou ventriculaire importante.
Néanmoins dans la plupart des cas, en dehors de la crise, l'ECG est normal. Lorsqu'une bradycardie est mise en évidence, il est possible de déterminer s'il s'agit ou non d'une bradycardie vagale en injectant 0,04 mg/kg d'atropine en IM et de réaliser un nouvel ECG 20 à 30 minutes plus tard. En cas d'origine vagale, la fréquence cardiaque sera alors aux alentours de 160-180 bpm. Lors de Sick Sinus Syndrome, il peut y avoir une légère augmentation de la fréquence, mais bien plus faible.
Suite à l'ECG, même s'il est normal, une échocardiographie est indiquée afin d'exclure une cause structurale ou fonctionnelle cardiaque.
La seule façon de diagnostiquer de manière certaine une arythmie responsable d'une syncope est de caractériser le rythme cardiaque au moment d'une crise. Le tracé ECG étant souvent normal entre deux syncopes, l'enregistrement d'un ECG sur 24 heures via la pose d'un moniteur Holter est le seul moyen de le mettre en évidence . Cet examen est facilement réalisable, l'appareil pouvant être envoyé au vétérinaire traitant et d'un coût raisonnable. Dans certains cas de syncopes peu fréquentes, la sensibilité du Holter peut être encore améliorée par l'utilisation de Holters sous-cutanés implantables.
Une échographie abdominale peut également être envisagée, notamment lors d'arythmie ventriculaire dont l'origine n'est pas cardiaque. Si la différence n'a pu être faite entre syncope et crise convulsive, un scanner ou un examen IRM cérébral peut être indiqué.
IV. Traiter la cause des syncopes
Le traitement est avant tout étiologique. Par ailleurs, lors de syncopes situationnelles, il est recommandé aux propriétaires d'éviter les situations provoquant les malaises autant que possible.
Lorsqu'une insuffisance cardiaque est mise en évidence, il convient également de la contrôler, celle-ci étant potentiellement arythmogène et donc génératrice de syncopes.
Quand il apparait qu'une arythmie est la cause des syncopes, un traitement anti-arythmique spécifique est à envisager. Il est à noter que tout traitement antiarythmique peut être proarythmique. Un suivi Holter est donc indispensable.
Bibliographie
- WARE WA, BONAGURA JD. Cardiovascular Disease in Companion Animals: Dog, Cat and Horse. 2ème ed.Boca Raton : CRC Press ; 2021
- SANTILLI RA, MOÏSE NS, PEREGO M et coll. Electrocardiography of the Dog and Cat: Diagnosis of Arrhythmias. 2ème ed. Milan : Edra ; 2018.
- DAVIDOW EB, PROULX J, WOODFIELD JA: Syncope: pathophysiology and differential diagnosis, Compend Contin Educ Pract Vet 23:608, 2001.
- BRIGHT JM, CALI JV: Clinical usefulness of cardiac event recording in dogs and cats examined because of syncope, episodic collapse, or intermittent weakness: 60 cases (1997-1999), J Am Vet Med Assoc 216(7):1110, 2000.
- KRAUS MS: Clinical approach to syncope. In: FUENTES VL, JOHNSON LR, DENNIS S: BSAVA Manual of Canine and Feline Cardiorespiratory Medicine, Second edition. 2010, BSAVA British small animal veterinary association, 15-19.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Syncopes et arythmies associées à l'apnée du sommeil chez le Cavalier King Charles : description chez 7 chiens
Marine DHUNPUTH
Coauteurs : Roberto SANTILLI, Manuela PEREGO, Vittorio SAPONARO
Introduction
Bien que largement décrit chez l'Homme, l'apnée du sommeil (sleep disordered-breathing, SDB) est peu connue chez le chien. Rapportée chez les brachycéphales, en association avec le syndrome obstructif des voies respiratoires (SORB) [1], elle est également décrite chez le Cavalier King Charles (CKC) [2]. Chez l'Homme, le SDB est associé des arythmies [3], alors que dans la littérature vétérinaire il n'existe pas d'information à ce sujet. L'objectif de cette série de cas est de décrire les résultats des enregistrements électrocardiographiques sur 24 heures (Holter) chez des CKC atteints de SDB et de les corréler aux signes cliniques.
Matériel et méthodes
Les données Holter de 7 chiens CKC, référés dans deux centres hospitaliers vétérinaires, souffrant de SDB et ayant montré des épisodes nocturnes de perte de conscience transitoire (PDC) ont été collectées. Le SDB a été défini comme « au moins 5 épisodes d'apnée ou d'hypopnée perçue pendant le sommeil » [1,2]. Pour tous les cas, l'âge, le sexe, les manifestations cliniques, les traitements et le suivi ont été rapportés. Les données Holter ont été analysées pour caractériser le rythme pendant les PDC (si présentes), le rythme dominant et les arythmies pendant la nuit, ainsi que la variabilité de la fréquence cardiaque sur cette période.
Résultats
Les résultats de cette série de cas sont présentés dans la Figure 1.
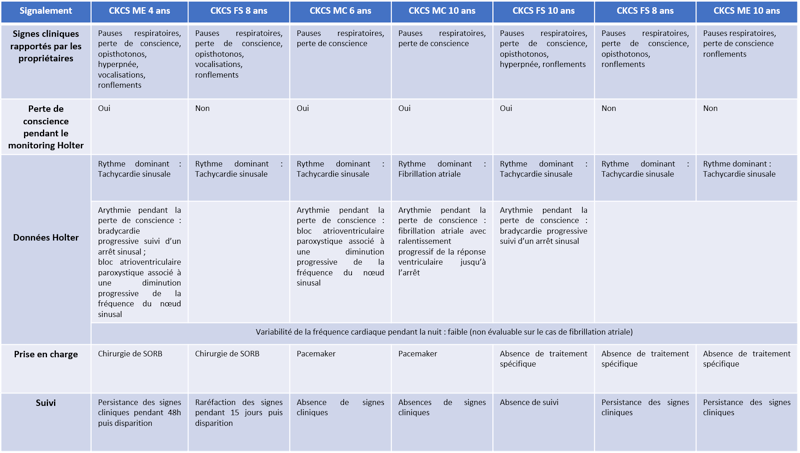
Figure 1
L'échantillon est constitué de sept chiens CKC âgés de 4 à 10 ans. Les manifestations cliniques rapportées étaient des pauses respiratoires (7/7), PDC (7/7), opisthotonos (6/7), hyperpnée après l'épisode (6/7), ronflements (5/7) et vocalisations (2/7). Parmi les 7 chiens, 6 ont présenté comme rythme dominant pendant la nuit une tachycardie sinusale, un chien une fibrillation atriale. Ce rythme était interrompu par différents types de bradyarythmies. Parmi les 7 chiens, 5 ont présenté des épisodes de PDC pendant le monitoring, caractérisés par trois types d'arythmies majeures, parfois plusieurs retrouvées chez le même patient : deux chiens ont présenté une bradycardie sinusale progressive suivie d'un arrêt sinusal (Figure 2a) ; deux ont présenté un bloc atrioventriculaire paroxystique associé à une diminution progressive de la fréquence de décharge du nœud sinusal ; un patient a présenté une fibrillation atriale suivie d'un ralentissement progressif de la réponse ventriculaire aboutissant à des arrêts ventriculaires. Toutes ces arythmies ont été considérées comme des réflexes vagaux inappropriés [4]. Chez les 6 chiens présentant comme rythme dominant une tachycardie sinusale, l'analyse de la variabilité de la fréquence cardiaque a montré des paramètres diminués par rapport aux intervalles de références (Figure 2b).
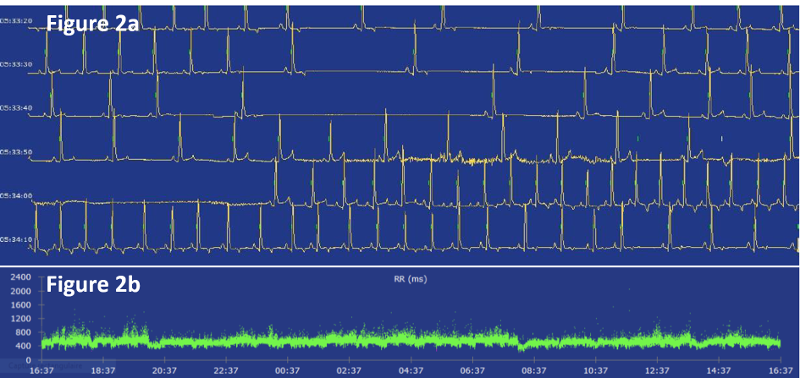
Figure 2
Suite aux résultats des monitorings Holter, deux chiens ont eu une chirurgie corrective du SORB et continué à présenter des épisodes de PDC (disparition après 15 jours de convalescence pour l'un, persistance mais raréfaction pour l'autre). Deux chiens ont reçu l'implantation d'un pacemaker et n'ont plus présenté de signes. Trois chiens n'ont eu aucun traitement : deux d'entre eux présentent encore des épisodes de PDC, un autre a été perdu de vue.
Discussion
Une première série de cas de SDB chez le CKC a été décrite en 2019 [2], sans qu'aucune donnée électrocardiographique ne soit rapportée. D'autres études ont également décrit le SDB chez d'autres races brachycéphales, sans mention d'arythmies associées [5]. En revanche, chez l'homme, le SDB est associé le plus souvent à une fibrillation atriale et des bradyarythmies déclenchées entre autres par une stimulation vagale [3]. L'originalité de la présente série est de s'intéresser à l'arythmie et à la variabilité de la fréquence cardiaque dans ce contexte clinique et racial spécifique. Il est intéressant de noter que chez les chiens qui ont présenté des épisodes de PDC, les crises correspondaient à des réflexes vagaux inappropriés, classés comme PDC de type Ia, Ib et Ic selon la classification de PEREGO et al [4]. En effet, la stimulation vagale peut ralentir la vitesse de décharge du nœud sinusal et entrainer une dépression des propriétés de conduction du nœud atrioventriculaire [4]. Une deuxième constatation est que nos chiens ont montré de façon homogène une diminution de la variabilité de la fréquence cardiaque, probablement conséquence de l'hypoxie chronique démontrée chez les chiens souffrant de SBD [5], qui peut engendrer des troubles du système nerveux autonome avec un impact hémodynamique important. La prise en charge de ces animaux, sur la base des données de ce travail, devrait prévoir la correction du SORB, source d'apnée. Mais cette seule approche ne semble pas éviter la récidive, ce qui amène à proposer l'implantation de pacemaker.
Conclusion
Cette série permet de documenter 7 cas supplémentaires de SDB chez le CKC (seulement 5 auparavant), avec un regard plus approfondi sur les possibles complications liées aux arythmies associées, et de proposer une prise en charge plus adaptée.
Bibliographie
- MONDINO. Sleep Disorders in dogs (2021)
- HINCHLIFFE. Sleep-disordered breathing in the Cavalier King Charles spaniel (2019)
- HERSI A. Obstructive sleep apnea and cardiac arrhythmias (2010)
- PEREGO. Heart rhythm characterisation during unexplained transient loss of consciousness in dogs (2020)
- Evaluation of C-reactive protein, Haptoglobin and cardiac troponin 1 levels in brachycephalic dog (2012)
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Syndrome hémophagocytaire : étude retrospective à propos de 13 cas
Introduction
La définition du syndrome hémophagocytaire (SH) en médecine vétérinaire a été établie dans les années 90 à partir de la définition utilisée alors en médecine humaine et totalement obsolète aujourd'hui. Est considéré comme SH en médecine vétérinaire, une bi- ou pancytopénie avec une infiltration médullaire par plus de 2 % de macrophages phagocytaires (WALTON 1996, WEISS 2007). Le but de cette série de cas est de décrire les cas de SH vus depuis 2010 dans notre institution et de comparer cette série à la littérature vétérinaire et humaine.
Matériel et Méthodes
Cette étude rétrospective répertorie tous les chats et les chiens avec SH identifiés par une recherche sur le logiciel clinique, avec les mots clés « bicytopénie », « pancytopénie » et « syndrome hémophagocytaire ». Les animaux ayant un dossier incomplet ou n'ayant pas eu de myélogramme ont été exclus. Les variables étudiées sont l'espèce, la race, le sexe, le motif de consultation, la présence de bi/pancytopénie, le pourcentage de macrophages dans la moelle osseuse et les causes sous-jacentes du SH.
Résultats
Treize cas ont été inclus, dont 5 chiens et 8 chats.
Parmi les chiens, 3 mâles et 2 femelles de race variée ont été inclus. L'âge médian est de 67 mois [42 - 101 mois]. Les motifs de consultation étaient : kérato-uvéite, pancytopénie, abattement, ehrlichiose, anémie. Les hémogrammes ont mis en évidence 3 cas de pancytopénie et 2 cas de bicytopénie (anémie et thrombopénie). Les macrophages représentaient en moyenne 5,0 % des cellules de la moelle osseuse [2,2 % - 11,3 %]. Les causes sous-jacentes identifiées étaient : infectieuses (bartonellose, ehrlichiose de stade 3), néoplasiques (sarcome histiocytaire, sertolinome) et idiopathique.
Parmi les chats, 4 mâles et 4 femelles avec 5 Européens, 2 Persans et 1 Chartreux ont été inclus. L'âge médian du diagnostic est de 39 mois [4 - 145 mois].
Les motifs de consultation étaient :
- abattement brutal ;
- hyperthermie récurrente avec toux ;
- pancytopénie ; dyspnée ;
- syndrome coryza avec ictère, hyperthermie et pancytopénie ;
- épistaxis ;
- suspicion d'hémopathie maligne ;
- suspicion d'aplasie médullaire secondaire au chlorambucil.
Les hémogrammes ont mis en évidence 4 cas de pancytopénie, 2 cas d'anémie et thrombopénie, et 2 cas d'anémie et leucopénie. Les macrophages représentaient en moyenne 6,8 % des cellules de la moelle osseuse [2,3 % - 20,3 %]. Les causes sous-jacentes identifiées étaient : infectieuses virales (parvovirose), bactériennes (Mycoplasma felis), parasitaires (aélurostrongylose plus ou moins associée à une toxoplasmose) ; dysimmunitaires (aplasie érythroïde isolée associée au FeLV, syndrome d'Evans) et néoplasiques (LAM6).
Discussion
Le SH est peu fréquent en médecine vétérinaire avec un faible nombre d'études rétrospectives publiées. Les causes majoritairement rapportées chez le chien sont des processus néoplasiques (sarcome histiocytaire, lymphome, etc.), dysimmunitaires (AHMI, etc.), infectieux (ehrlichiose, parvovirose, etc.) ou une origine idiopathique. Dans notre étude, en plus des causes mentionnées dans les publications, un cas de bartonellose et un sertolinome ont pu être observés (WALTON 1996, WEISS 2007). Chez le chat, les causes rapportées sont des processus infectieux (FIV, toxoplasmose, mycoplasmose, etc.), néoplasiques (sarcome histiocytaire, myélome multiple), dysimmunitaires (AHMI) ou une origine idiopathique. Dans notre étude, en plus des causes mentionnées dans les publications, des cas de parvovirose, d'aélurostrongylose, d'aplasie érythroïde isolée, de syndrome d'Evans et de LAM 6, ont pu être observés (STANDBERG 2023, TAGAWA 2023).
La définition du SH en médecine humaine a fortement évolué. La lymphohistiocytose hémophagocytaire (HLH) est une maladie rare caractérisée par une activation des lymphocytes T cytotoxiques, des natural killer (NK) et des macrophages, entraînant une hypercytokinémie et des lésions organiques à médiation immune. Ainsi, est considéré comme SH en médecine humaine tout cas correspondant aux critères HLH-2004 révisés, avec un diagnostic par méthode moléculaire, ou mise en évidence de 5 des 8 critères suivants : fièvre, splénomégalie, bi- ou pancytopénie, hypertriglycéridémie et/ou hypofibrinogénémie, hémophagocytose (dans la moelle osseuse, la rate, les nœuds lymphatiques ou le foie), activité faible ou absente de lymphocytes NK, hyperferritinémie, concentration augmentée en protéine CD25 (PONNATT 2022).
Conclusion
Compte tenu de l'hétérogénéité des cas décrits dans la littérature et dans notre étude, ainsi que de l'évolution de la définition en médecine humaine, il semblerait pertinent d'actualiser la définition du SH utilisée en médecine vétérinaire ainsi que les critères diagnostiques.
Bibliographie
- PONNATT TS, LILLEY CM, MIRZA KM. Hemophagocytic Lymphohistiocytosis. Arch Pathol Lab Med. 2022 Apr 1;146(4):507-519.
- STRANDBERG NJ, TANG KM, DOS SANTOS AP. Hemophagocytic syndrome in a cat with Mycoplasma haemofelis infection. Vet Clin Pathol. 2023 Jun;52(2):320-323.
- TAGAWA M, AOKI M, UEMURA A, YANAGAWA M, MINESHIGE T, WATANABE KI, KOBAYASHI Y. Hemophagocytic syndrome in a cat with immune-mediated hemolytic anemia. Vet Clin Pathol. 2023 Jun;52(2):313-319.
- WALTON RM, MODIANO JF, THRALL MA, WHEELER SL. Bone marrow cytological findings in 4 dogs and a cat with hemophagocytic syndrome. J Vet Intern Med. 1996 Jan-Feb;10(1):7-14.
- WEISS DJ. Hemophagocytic syndrome in dogs: 24 cases (1996-2005). J Am Vet Med Assoc. 2007 Mar 1;230(5):697-701.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Tendinite patellaire : quand la suspecter et comment la prendre en charge ?
Montréal, Canada
I. Introduction
La tendinite patellaire correspond à une inflammation ou dégénérescence du tendon reliant la patella à la tubérosité tibiale. Chez le chien, elle peut apparaître après une TPLO réalisée pour traiter une rupture du ligament croisé crânial. La chirurgie modifie la biomécanique du grasset, redistribuant les forces sur l'appareil extenseur et pouvant entraîner une surcharge tendineuse.
II. Signes cliniques fréquents
- Boiterie persistante ou réapparition après amélioration initiale post-TPLO.
- Douleur à la palpation du tendon patellaire.
- Épaississement palpable le long du tendon.
- Réduction de l'extension complète du genou.
- Apparition progressive, souvent après un excès d'activité ou un incident lors de la rééducation.
III. Facteurs favorisants
- Chien de grande taille ou en surpoids.
- Atrophie musculaire post-opératoire du quadriceps.
- Reprise d'activité trop rapide ou non contrôlée.
- Malposition ou conflit avec le matériel chirurgical.
- Fracture de la portion distale de la rotule ou d'un ostéophyte.
III. Diagnostic
1. Examen clinique
- Palpation ciblée du tendon patellaire : douleur et parfois chaleur locale.
- Évaluation de la mobilité du grasset, notamment en extension forcée.
2. Imagerie
- Radiographie : vérifier l'alignement et la position des implants, exclure fractures rotule.
- Échographie : épaississement tendineux, zones hypoéchogènes, hypervascularisation.
- IRM rarement utilisée en pratique clinique courante.
3. Diagnostics différentiels
- Douleur secondaire aux implants.
- Fibrose cicatricielle péri-patellaire.
- Lésion méniscale, infection.
IV. Prise en charge
L'objectif est de réduire la douleur et l'inflammation, de favoriser la cicatrisation tendineuse et de restaurer la fonction locomotrice.
1. Phase initiale (aiguë)
- Repos contrôlé : sorties courtes en laisse (5–10 min), éviter sauts et escaliers.
- Cryothérapie : 15 minutes, 2 à 3 fois/jour.
- AINS et antalgiques sur courte durée pour contrôler douleur et inflammation.
- Physiothérapie douce : mobilisations passives et massage pour limiter la raideur et améliorer la circulation.
- Laser et/ou shockwave thérapie.
- Injection de PRP potentiellement.
2. Rééducation progressive
- Renforcement musculaire : travail du quadriceps et de la chaîne postérieure de façon progressive.
- Proprioception : exercices sur surfaces instables, transfert de poids.
- Hydrothérapie : tapis roulant aquatique pour stimuler la musculature tout en diminuant la charge sur le tendon.
- Étirements doux des quadriceps/ischios après échauffement.
3. Mesures complémentaires
- Gestion du poids : programme nutritionnel adapté si surpoids.
- Ajustement des charges et contrôle de l'activité pour éviter les récidives.
- Surveillance régulière du site chirurgical pour détecter toute complication mécanique.
V. Suivi
- Contrôles vétérinaires toutes les 2–3 semaines pour évaluer douleur, boiterie et progression musculaire.
- Outils d'évaluation : observation vidéo, grilles de score fonctionnel, radiographie et échographie de suivi si besoin.
- Reprise d'activité libre uniquement après disparition complète de la douleur et récupération musculaire symétrique.
- Programme d'entretien : exercices de renforcement et proprioception pour prévenir les récidives.
V. Protocole de physiothérapie – Tendinite patellaire post-TPLO chez le chien
Principes généraux
- Progressivité : augmenter la charge de travail selon la tolérance et l'absence de douleur.
- Individualisation : ajuster selon la taille, le tempérament, l'évolution clinique.
- Contrôle de la douleur : indispensable pour éviter le cercle vicieux inflammatoire.
- Objectif final : retour à une fonction locomotrice optimale, sans boiterie ni douleur, avec symétrie musculaire.
Phase 1 : phase aiguë (semaines 0 à 2 après apparition des signes)
a) Objectifs
- Réduire la douleur et l'inflammation, préserver la mobilité, éviter la fonte musculaire.
b) Techniques
- Repos contrôlé : sorties en laisse 5–10 min, 3–4 fois/jour.
- Cryothérapie : application de glace 15 min, 2–3 fois/jour, surtout après activité.
- Massage doux (effleurage, pétrissage léger) pour favoriser la circulation et limiter l'œdème.
- Mobilisations passives du grasset. Amplitude faible à modérée, 10–15 mouvements lents, 2-3 fois/jour. But : maintenir la souplesse articulaire.
- Stimulation musculaire douce (électrostimulation type TENS ou NMES si disponible) sur le quadriceps pour limiter l'atrophie.
- Laser (2 fois par semaine) ou « shockwave » thérapie (1 fois par semaine) si disponible.
c) Précautions
- Éviter tout saut, montée/descente d'escalier, jeu libre.
- Surveiller l'apparition de douleur ou gonflement après les séances.
Phase 2 : phase subaiguë / renforcement initial (semaines 2 à 6)
a) Objectifs
- Restaurer progressivement la force musculaire, améliorer le contrôle moteur, réduire la sensibilité tendineuse.
b) Techniques
- Marche en laisse prolongée : commencer par 5–10 min, augmenter progressivement jusqu'à 20–30 min/jour, fractionné en 2–3 séances.
- Mobilisations passives du grasset. Amplitude modérée, 10–15 mouvements lents, 2-3 fois/jour. But : maintenir la souplesse articulaire.
- Travail proprioceptif statique. Station debout sur surface stable, puis sur coussin mousse. Tenir 10–15 sec, répéter 5–10 fois.
- Hydrothérapie (tapis roulant aquatique) : 5–10 min, 2 fois/semaine. L'eau jusqu'au grasset pour réduire les contraintes tout en travaillant le quadriceps.
- Exercices de transfert de poids. Déplacer doucement le poids latéralement, encourager l'appui sur le membre atteint.
- Renforcement excentrique doux. Marche en pente douce (3–5°) ou sur terrain souple.
- Laser (2 fois par semaine) ou « shockwave » thérapie (1 fois par semaine) si disponible.
c) Précautions
- Progression lente pour éviter la surcharge tendineuse.
- Évaluer la boiterie après chaque progression.
Phase 3 : phase de renforcement avancé et retour à l'activité (semaines 6 à 12)
a) Objectifs
- Récupération complète de la force, endurance et proprioception dynamique.
b) Techniques
- Proprioception dynamique. Passage sur surfaces instables (coussins, planches à bascule). Exercices de cavaletti à hauteur basse (10–15 cm), 6–8 barres espacées.
- Mobilisations passives du grasset. Amplitude complète, 10–15 mouvements lents, 2-3 fois/jour. But : maintenir la souplesse articulaire.
- Renforcement excentrique ciblé du quadriceps. Marche en descente douce (≤10°). Augmenter la durée de travail.
- Hydrothérapie prolongée : 15–20 min avec variations de vitesse.
- Amplitude articulaire. Montée progressive des charges : augmenter la distance de marche, introduire des courses très courtes (si absence de douleur). Jeu contrôlé : lancer de balle à courte distance sur terrain plat.
c) Précautions
- Toujours évaluer la récupération musculaire avant d'augmenter la complexité.
- Surveiller toute réapparition de boiterie.
Phase 4 : phase de maintien et prévention (au-delà de 12 semaines)
a) Objectifs
- Maintenir la condition musculaire et prévenir les récidives.
b) Techniques :
- Programme d'entretien 2–3 fois/semaine.
- Marche active 30–40 min.
- Exercices proprioceptifs (coussins, cavaletti).
- Renforcement musculaire intégré au jeu.
- Contrôle du poids et suivi physiothérapeutique au besoin.
6. Points clés du suivi
- Évaluation régulière (toutes les 2–3 semaines durant 2 mois) avec grille fonctionnelle ou vidéo pour objectiver les progrès.
- Réduction immédiate de l'intensité si douleur ou boiterie après les séances.
- Coordination vétérinaire – physiothérapeute indispensable.
Bibliographie
- ZINK MC, VAN DYKE JB. Canine Sports Medicine and Rehabilitation. 2è ed. Wiley-Blackwell; 2018.
- MILLIS DL, LEVINE D. Canine Rehabilitation and Physical Therapy. 2è ed. Elsevier; 2014.
- GALLAGHER, B., MONTAVON, P.M., VOSS, K., et al. (2012). Effects of extracorporeal shock wave therapy on patellar ligament thickening after tibial plateau leveling osteotomy. Veterinary Surgery, 41(5), 594-600
- MONK, M.L., PRESTON, C.A., MCGOWAN, C.M. (2006). Effects of early intensive postoperative physiotherapy on limb function after tibial plateau leveling osteotomy in dogs with deficiency of the cranial cruciate ligament. American Journal of Veterinary Research, 67(3), 529-536. doi:10,2460/ajvr,67,3,529
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Thérapeutique liquidienne chez l'animal cardiorénal : équilibre entre réhydratation et surcharge volémique
Annecy, France
I. Introduction
La fluidothérapie doit être envisagée comme un véritable traitement médical. Elle obéit ainsi aux mêmes exigences que tout autre médicament : définir ses indications, déterminer une posologie adaptée, anticiper les bénéfices attendus, identifier les effets indésirables et assurer un suivi rigoureux.
Chez le patient cardio-rénal, cette prise en charge se révèle particulièrement complexe. Ces animaux, fragiles, sont exposés à deux risques opposés mais tout aussi graves :
- La déshydratation, qui compromet la perfusion tissulaire et aggrave l'insuffisance rénale.
- La surcharge volémique, qui exacerbe les troubles cardiaques et peut rapidement engager le pronostic vital.
Le rôle du clinicien consiste alors à rechercher un équilibre thérapeutique subtil, corrigeant les déficits hydriques tout en évitant les excès délétères. [1]
II. Évaluation clinique initiale
La première étape demeure une évaluation clinique rigoureuse [2]. Elle permet de distinguer trois situations :
- Déshydratation
- État d'hydratation normal
- Surcharge volémique (surhydratation)
Il convient de rappeler que l'état d'hydratation reflète le volume du compartiment extracellulaire, tandis que la volémie correspond au compartiment intravasculaire et reflète la perfusion.
1. Paramètres de perfusion à examiner
- Fréquence cardiaque
- Temps de remplissage capillaire (TRC)
- Couleur des muqueuses
- Qualité du pouls périphérique
- Température des extrémités
- Statut mental du patient
2. Signes de déshydratation selon la sévérité
- 5% : muqueuses sèches
- 8% : pli cutané persistant
- 10% : énophtalmie, cornées sèches
- >14% : altération neurologique, hypovolémie sévère
3. Signes de surcharge volémique
- Prise de poids
- Œdèmes périphériques, peau d'aspect « gélatineux »
- Chemosis, jetage nasal séreux
- Pouls jugulaire rétrograde
- Œdème pulmonaire, épanchements pleural et/ou péritonéal
III. Principes de fluidothérapie adaptée
1. Choix du fluide
- Cristalloïdes isotoniques : choix de première intention. Dans le contexte cardio-rénal, il est préférable de privilégier des solutions modérément sodées, comme le Ringer Lactate, plutôt que le NaCl 0,9%.
- Solutions hypotoniques (NaCl 0,45%, glucose 2,5%) : indiquées pour limiter la charge sodée, notamment chez l'insuffisant cardiaque.
2. Dose et voie d'administration
La voie intraveineuse est la plus courante, mais son utilisation doit rester prudente. Le débit de perfusion dépend de plusieurs paramètres :
- Statut volémique : l'hypovolémie peut nécessiter des bolus de cristalloïdes isotoniques. Chez le patient cardio-rénal, la dose habituelle (10–20 ml/kg chez le chien, 5–10 ml/kg chez le chat) doit être réduite. On privilégie des boli fractionnés de 2–3 ml/kg, répétés avec réévaluation clinique entre chaque administration.
- Déshydratation : le calcul repose sur la formule : Volume(ml)= Poids(kg) x pourcentage de déshydratation x10. Alors que ce volume peut être perfusé rapidement chez l'animal sain, il convient de l'administrer plus progressivement (sur 24 heures ou davantage) chez le patient cardio-rénal, avec réévaluations régulières.
- Pertes en cours (digestives, urinaires) qui doivent être compensées.
- Besoins de maintenance : environ 40 ml/kg/j chez le chat et 60 ml/kg/j chez le chien
Lorsque cela est possible, la voie entérale constitue une alternative pertinente. L'administration d'eau ou de solutions pauvres en sodium par sonde nasogastrique permet une réhydratation efficace tout en limitant le risque de surcharge volémique.
IV. Surveillance et monitoring
Le succès thérapeutique repose sur un monitoring attentif et continu. Plusieurs paramètres simples et accessibles doivent être intégrés :
- Fréquence respiratoire : son augmentation est un signe précoce de surcharge volémique [3].
- Poids corporel : une pesée bi-quotidienne ou tri-quotidienne permet de détecter rapidement une rétention hydrosodée.
- Diurèse : mesurée par sonde urinaire avec système clos ou par récolte des mictions spontanées.
- Échographie POCUS (Point of Care Ultrasound) : évaluation de la fonction cardiaque, de la veine cave caudale, recherche d'épanchements ou de lignes B pulmonaires, signes d'œdème interstitiel.
- Pression artérielle
- Paramètres biologiques : hématocrite, protéines totales, électrolytes, urée et créatinine, qui permettent de suivre l'impact du traitement sur la fonction rénale et l'équilibre hydrique.
Malgré ces précautions, la surcharge volémique reste un risque inhérent à l'administration de fluides chez le patient cardio-rénal. Dès son apparition, l'administration doit être interrompue et l'introduction de diurétiques envisagée. Les diurétiques de l'anse, comme le furosémide, sont les molécules de première intention en médecine vétérinaire. L'objectif est de trouver la plus petite dose efficace permettant de réduire la congestion et d'optimiser le statut volémique, tout en préservant la perfusion rénale.
V. Conclusion
Chez le patient cardio-rénal, la fluidothérapie représente un outil thérapeutique à double tranchant. Sa prescription ne peut se faire qu'après une évaluation clinique approfondie, suivie d'une adaptation dynamique fondée sur l'évolution du patient.
Le choix du fluide, la dose, la voie d'administration et la surveillance rapprochée constituent les quatre piliers d'une fluidothérapie raisonnée.
L'art du clinicien réside dans cette recherche permanente d'un équilibre fragile : restaurer une perfusion tissulaire efficace tout en évitant les excès qui menaceraient la fonction cardiaque et, in fine, le pronostic vital.
Bibliographie
- POUCHELON JL, ATKINS CE, et al. Cardiovascular-renal axis disorders in the domestic dog and cat: a veterinary consensus statement. J Small Anim Pract. 2015, 56(9) : 537-52
- PARDO M, SPENCER E, et al. 2024 AAHA Fluid Therapy Guidelines for Dogs and Cats. 2024. J Am Anim Hosp Assoc, 60(4) : 131-63
- OHAD DG, RISHNIW M, et al. Sleeping and resting respiratory rates in dogs with subclinical heart disease. J Am Anim Hosp Assoc. 2013, 243 : 839-843
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Thermoablation par micro-ondes de tumeurs de la base du cœur chez 9 chiens : résultats préliminaires (2022-2025)
Introduction
La thermoablation par micro-ondes (TMO) est une technique récente utilisée en médecine humaine pour traiter les tumeurs de la thyroïde, rénale ou hépatique [1] [2]. Cette procédure consiste à appliquer un champ micro-ondes à un tissu tumoral, afin de la chauffer pour induire une nécrose de coagulation. La thermoablation a été décrite pour la première fois sur des chémodectomes canins en utilisant les radiofréquences [3], mais la TMO n'a pas encore été décrite sur les tumeurs de la base du cœur chez les chiens.
L'objectif de cette étude prospective est de
- déterminer la faisabilité et les éventuelles complications de deux techniques différentes de thermoablation de tumeurs cardiaques
- évaluer les effets à court et moyen termes de la procédure
- déterminer la survie de la population après intervention.
Matériel et méthodes
La population se compose de 9 chiens, d'âge et poids moyens (± écart type;[intervalle]) de 9,3 ans (±1,98;[7,5-13,7]) et 13,2 kg (±7,0;[7,7-31,0]). La race Bouledogue Français est surreprésentée (7/9). Tous les individus présentaient des signes cliniques (toux, syncope, fatigue), tandis que 6/9 était en insuffisance cardiaque congestive. Le diagnostic est établi sur la base de l'échocardiographie chez tous les chiens, 6 des 9 individus ayant eu un examen tomodensitométrique du thorax.
La taille de la tumeur est évaluée avant et après la procédure à l'échocardiographie et/ou au scanner par le même opérateur entrainé. Deux approches différentes ont été réalisées : échoguidée par ponction transthoracique (n=4) ou à thorax ouvert (mini-thoracotomie) au contact direct de la tumeur par ponction échoguidée après péricardectomie (n=5).
Un test de SHAPIRO-WILK permet de définir la taille des tumeurs comme suivant une distribution normale. Un test STUDENT sur données appariées compare les tailles de tumeurs avant et après intervention sur la population globale. Un test de la borne à intervalle de confiance 95 % est réalisé pour chaque individu afin d'établir si la réduction de la tumeur est significative. L'étude de survie a été conduite selon la méthode KAPLAN-MEIER.
Résultats
Le suivi à court terme (<1 mois post-opératoire) et long terme (<6 mois) est disponible chez tous les patients. Pour 2 chiens sur 9, les suivis échocardiographiques sont manquants.
La procédure s'est déroulée sans complication per-opératoire chez tous les chiens. Une complication post-opératoire majeure est observée avec l'initiation d'une bradycardie sinusale 2 heures après le réveil de l'animal, évoluant en un rythme d'échappement ventriculaire puis causant un arrêt cardiaque et le décès de l'animal. Des complications mineures comme des arythmies auto-résolutives sont rarement décrites.
La procédure est efficace pour résoudre les signes cliniques. À une semaine post-opératoire, les propriétaires rapportent une amélioration de la qualité de vie se poursuivant a minima jusqu'à moyen terme (entre 1 et 3 mois post-opératoire).
Dans les 6 mois post-opératoires, une réduction significative de la taille de la tumeur a été observée chez 3 des 9 chiens (p<0,05), avec une stabilisation de la taille chez les autres patients.
La médiane de survie après thermoablation par micro-ondes est estimée à 326 jours, 5 des 9 chiens étant toujours vivants à la date de clôture de l'étude préliminaire. 4 décès sont enregistrés sur le temps de l'étude survenant après une médiane de 246 jours post-intervention, une cause cardiogénique pouvant être identifiée dans 3 des 4 cas.
Discussion
Ces résultats sont en contradiction partielle avec ceux présentés par GOMEZ OCHUA and al. [3], mettant en évidence une réduction de la taille de la tumeur chez l'intégralité de la population ; cependant la technique de thermoablation utilisée diffère de celle de la présente étude, utilisant les radiofréquences et non les micro-ondes. En revanche, l'amélioration des signes cliniques est en concordance avec cette précédente étude.
Le nombre réduit de patients enrôlés constitue un biais d'échantillonnage pouvant fausser les conclusions. L'absence de standardisation dans la prise en charge, notamment sur les traitements administrés au cours de l'étude constitue également une limite, certains des chiens ayant notamment reçu du phosphate de tocéranib temporairement avant la prise en charge.
De plus, la réalisation concomitante d'une péricardectomie associée à la thermoablation représente un biais de confusion dans les conclusions tirées, notamment sur l'amélioration des signes cliniques pour les chiens ayant été traités par approche à thorax ouvert.
Enfin, l'absence d'examen tomodensitométrique de contrôle à 3 et/ou 6 mois post-thermoablation de manière systématique ne permet pas de confirmer la réduction tumorale significative objectivée à l'échocardiographie, les mesures échocardiographiques pouvant incorporer un biais dans la répétabilité.
Conclusion
Cette étude suggère que la thermoablation par micro-ondes des tumeurs de la base du cœur est efficace pour résoudre les signes cliniques associés et peut conduire à une réduction significative de la taille de la tumeur dans 33 % des cas.
Cependant, des limites à cette étude préliminaire justifient la réalisation d'une étude prospective avec des populations plus larges et uniformisées pour valider ces conclusions.
Bibliographie
- CHU et al, Nat Rev Cancer 2014
- VOGL et al, Rofo 2017
- GÓMEZ et al, Animals 2021
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Tonométrie : comment éviter les valeurs artéfactuelles
Strasbourg, France
I. Introduction
La tonométrie est la mesure de la pression intraoculaire (PIO). En clinique on utilise uniquement la tonométrie indirecte, c'est-à-dire qu'on la mesure de la tension cornéenne pour estimer la PIO. Elle est rapide, simple et non invasive. Cependant, de nombreuses erreurs de technique ou d'interprétation peuvent conduire à des valeurs faussement élevées ou abaissées, retardant le diagnostic ou déclenchant un traitement inapproprié.
II. Valeurs de références
La plage de PIO normale chez la plupart des espèces animales se situe entre 15 et 25 mmHg. Les valeurs moyennes et écarts varient selon les études, mais on retient généralement : chien 15–18 mmHg, chat 17–19 mmHg, lapin 15–20 mmHg et cheval 17–28 mmHg (Gum et al., 2007). De façon générale, la différence de mesure entre les deux yeux ne devrait pas excéder 8 mmHg (Lovekin, 1964). Si ce n'est pas le cas, un examen approfondi des deux yeux s'impose à la recherche d'une anomalie.
III. Rappel sur les appareils utilisés
En médecine vétérinaire, on utilise essentiellement la tonométrie à applanation ou à rebond
1. Rebond (TonoVet® / TonoVet Plus® / Tono-Vera® Vet)
- Les tonométres à rebond utilisent une micro-sonde qui est propulsée rapidement, électromagnétiquement, depuis une distance fixe vers la cornée et qui rebondit ensuite jusqu'à l'instrument. Celui-ci analyse les caractéristiques de rebond (décélération de la sonde) et les convertit en valeurs de PIO : les yeux à PIO élevée provoquent une décélération plus faible et un temps de retour plus court que les yeux à PIO basse.
- Pas d'anesthésique requis
- Alignement : instrument vertical, sonde horizontale ; distance 3–5 mm, angle ≤ 20° ; viser la cornée centrale.
- Éviter les lésions : viser la zone la plus saine.
- Répétitions : réaliser 6 lectures valides ; rejeter les valeurs aberrantes ; médiane ou moyenne des lectures cohérentes.
- Biais attendus : peut sous-estimer les hautes PIO selon conditions/modèles ; le TonoVet Plus donne des valeurs un peu plus élevées en normal que le TonoVet. Ne pas comparer directement entre modèles.
2. Aplanissement (Tono-Pen / AccuPen / Perkins)
- Les tonomètres à aplanissement mesurent la force nécessaire pour aplatir une surface cornéenne constante (pression = force/surface). Le principe dérive de la loi d'Imbert-Fick : « La pression dans une sphère remplie d'un liquide, entourée d'une membrane infiniment mince, se mesure par la contre-pression juste suffisante pour l'aplatir. » La force requise pour aplatir une aire connue permet d'estimer la PIO. le point d'aplanissement est détecté électroniquement et moyenné après multiples touches légères sur la cornée centrale.
- Anesthésie topique nécessaire : instillation d'oxybuprocaïne ou de tétracaïne préalablement à la mesure
- Pointage : les 2/3 centraux de la cornée, éviter le limbe et les zones irrégulières.
- Capuchon neuf à chaque patient ; vérifier l'étalonnage.
- Critère de qualité : viser un coefficient de variation (CV) ≤ 5% ; si > 5–10%, répéter.
- Répétitions : 5–10 touches légères ; moyenne automatique sur l'écran.
- Biais attendus : surestime les faibles PIO, sous-estime les PIO élevées (> 40–50 mmHg). Ne pas conclure à une « normalité » si le tableau clinique est compatible avec un glaucome.
IV. Conditions de mesure
- Toujours la même routine : même instrument, si possible même heure de la journée (idéalement matin), même position de la tête/corps, même opérateur. NB : Rythme circadien : chez le chien la PIO est plus basse l'après-midi/soir ; pour le suivi, rester sur le même créneau horaire si possible.
- Environnement : limiter le stress, lumière constante, salle calme.
- Avant les collyres : mesurer la PIO avant tout mydriatique/topique (surtout tropicamide et atropine qui peuvent augmenter la PIO ; privilégier la cyclopentolate si cycloplégie nécessaire).
- Collier ou harnais : retirer ou desserrer le collier (peut élever la PIO) ; préférer un harnais.
- Contention : éviter toute pression sur les paupières et la jugulaire (même brève), source d'élévation de ~15–20 mmHg.
- Position : tête au niveau du cœur ; éviter les positions basses de la tête qui augmentent la PIO.
V. Éviter les sources principales d'erreurs
1. Facteurs liés au patient
- Sujet très agité nécessitant une contention ferme
- Contre-pression sur le globe :
- Pression exercée par les doigts sur les paupières ou sur le rebord orbitaire.
- Manipulation excessive de la tête qui comprime la veine jugulaire : augmente la PIO artificiellement (attention aux colliers).
- Mouvements oculaires : clignement, retrait de l'œil dans l'orbite.
- Stress ou douleur : peuvent augmenter transitoirement la PIO (surtout chez le chat).
- Pachymétrie (Épaisseur de la cornée ) : l'épaisseur cornéenne centrale peut augmenter les lectures (par 100 µm : +1 mmHg au Tono-Pen XL ; +2 mmHg au TonoVet ; Park et al., 2011). Chez l'Homme, il existe des facteurs de corrections de la PIO en fonction de l'épaisseur cornéenne.
- Utilisation de l'anesthésie : attention à la kétamine qui augmente la PIO de façon cliniquement importante (Hofmeister et al., 2006a), effet prévenu par l'usage de diazépam ou midazolam (Ghaffari et al., 2010 ; Hofmeister et al., 2006). L'usage de médétomidine puis d'atipamézole ne modifie pas la PIO (Wallin-Hakanson & Wallin-Hakanson, 2001).
2. Facteurs liés à l'examinateur
- Mesure sur un œil non stabilisé ou mal aligné : avec le TonoVet, la mesure doit être horizontale.
- Appareil mal calibré ou mauvais réglage de la distance.
- Ordre de mesure : commencer toujours par l'œil suspect, puis le second (évite l'augmentation réflexe de la PIO après contact répété).
- Mauvais choix de l'espèce (TonoVet Plus®)
3. Facteurs liés à l'équipement
- Calibrage non vérifié selon les recommandations du fabricant.
- Batterie faible ou embout de sonde endommagé.
- Mauvaise position du tonomètre par rapport à la cornée (hors axe).
- Changer régulièrement les micro-sondes lors de tonométrie par rebond.
VI. En pratique
- Préparer l'appareil (même que d'habitude) et le vérifier (capuchon/sonde, étalonnage avant de manipuler le patient).
- Retirer collier et positionner la tête du sujet au niveau du cœur
- Calmer le patient / Rassurer le propriétaire.
- Contention souple : pas de pression sur les jugulaires, les paupières…
- Mesurer avant toute instillation de collyre.
- Viser le centre de la cornée ; 6 lectures (rebond) ou CV ≤ 5% (aplanissement).
- Répéter sur l'autre œil ; comparer : Δ > 8 mmHg = suspect.
- Attention aux incohérences : clinique incompatible avec les mesures chiffrées. Renouveler la mesure. Considérer le contexte (sujet agité, contention difficile…).
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Torsion gastrique et hernie hiatale de type IV chez deux chats
Flavie DESCHILDRE
Coauteurs : Flavie DESCHILDRE, Margaux BLONDEL, Eugénie SOLIVERES, Guillaume CHANOIT
Introduction
La dilatation-torsion gastrique est un syndrome fréquent et documenté chez le chien. De rares cas sont décrits chez d'autres espèces, et de façon sporadique chez le chat [1]. Les hernies diaphragmatiques semblent être un facteur prédisposant [2]. Les hernies hiatales correspondent au passage d'organes abdominaux dans la cavité thoracique à travers le hiatus œsophagien. Quatre types de hernies hiatales sont décrites, le type IV étant la plus sévère avec le passage de l'estomac et d'autres organes dans la cavité thoracique. Les hernies de type IV sont très rares chez le chat [3]. Cet article présente deux cas de torsion gastrique au sein d'une hernie hiatale de type IV chez des chats.
Anamnèse
Deux chattes de 4 et 5 ans sont présentées pour anorexie, abattement, efforts vomitifs infructueux et dyspnée évoluant depuis 24h.
Examen clinique
Dans le premier cas, l'examen clinique met en évidence une dyspnée expiratoire avec respiration gueule ouverte et des signes d'inconfort abdominal. Dans le second cas, le chat présente une discordance respiratoire discrète ainsi que des signes de choc obstructif (abattement, hypotension, hypothermie).
Démarche diagnostique
Dans les deux cas, des clichés radiographiques réalisés à l'admission mettent en évidence une localisation atypique de l'estomac dans la cavité thoracique. L'estomac est dilaté et présente des signes radiographiques de torsion chez un des deux chats (Figure 1). À la suite de ces examens d'imagerie médicale, le diagnostic différentiel comprend une hernie diaphragmatique ainsi qu'une hernie hiatale de type IV, la distinction entre ces deux entités restant complexe sur la base du simple examen radiographique.
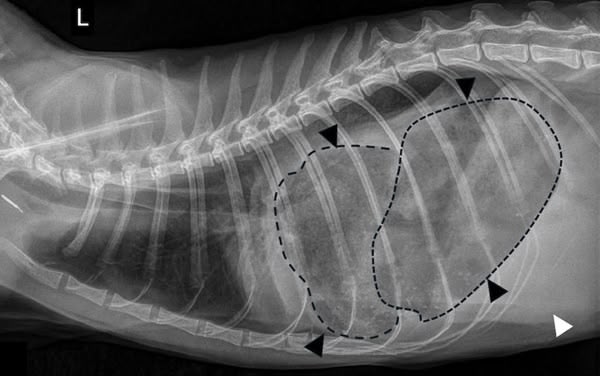
Figure 1
Radiographies préopératoires du second cas, mettant en évidence la compartimentalisation de l'estomac (têtes de flèches et pointillés noirs) au sein de la cavité thoracique. Le foie est toujours en position abdominale (tête de flèche blanche).
Traitement
Malgré la stabilisation d'urgence, la détresse respiratoire s'aggrave, motivant une prise en charge chirurgicale d'urgence dans les deux cas. Dans le premier cas, la laparotomie révèle une hernie hiatale avec incarcération de l'estomac, du duodénum, du pancréas, de la rate et du lobe hépatique droit latéral. L'estomac est tordu le long de son axe long. Après réduction des organes herniés, des gastropexies incisionnelles droite et gauche sont réalisées. Une récidive de la dilation gastrique est notée à 6 mois post-opératoire. Le vétérinaire traitant réalise une laparotomie exploratrice, l'estomac est dilaté mais n'est pas tordu. Le vétérinaire lève les adhérences des gastropexies. Par la suite, une récidive de la hernie hiatale et de la torsion est notée. La nouvelle reprise chirurgicale consiste alors en une gastropexie et reconstruction du hiatus œsophagien. Dans le second cas, la laparotomie révèle une incarcération de l'estomac, de la rate et de l'omentum au sein de la hernie hiatale. Une diaphragmotomie et une sternotomie caudale sont réalisées (Figure 2). L'estomac est tordu le long de son axe long, fortement dilaté et cyanosé. Il est détordu puis une gastropexie et une reconstruction du hiatus œsophagien sont réalisées. Le réveil anesthésique est long et la chatte fait un arrêt cardio-respiratoire entraînant son décès au cours des 12h post-opératoire.
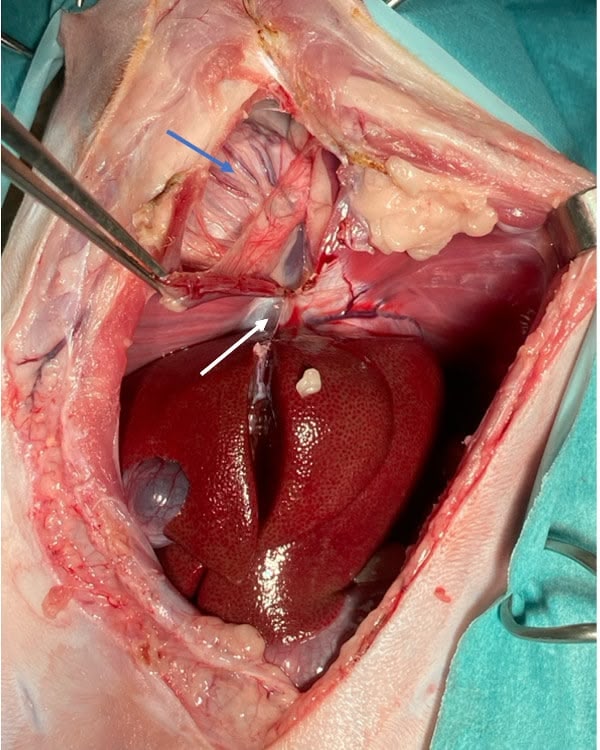
Figure 2 : Photographie per-opératoire du second cas, après réalisation de la
diaphragmotomie et sternotomie caudale. Visualisation de la torsion gastrique
dans la cavité thoracique (flèche bleue) et de la hernie hiatale (flèche blanche)
Discussion
Les hernies hiatales de type IV et les torsions gastriques sont des phénomènes rares chez le chat. Leur étiologie reste inconnue. Les hernies hiatales semblent être un facteur prédisposant à la torsion gastrique chez le chat comme elle peut l'être chez l'homme [4]. Le diagnostic est complexe. La radiographie apporte des informations précieuses mais d'autres techniques d'imagerie médicale permettent un diagnostic de certitude (œsophagogramme, endoscopie, scanner) [5]. Il s'agit des premiers cas décrivant la prise en charge chirurgicale de hernie hiatale de type IV chez le chat. La réduction des organes herniés, la gastropexie et la reconstruction du hiatus œsophagien semblent être indiqués afin d'éviter les récidives. Toutefois, l'issue fatale du second cas souligne que, malgré une prise en charge rapide et adaptée, il s'agit d'une affection grave et pouvant être difficile à traiter.
Conclusion
Le syndrome de dilatation torsion est une affection rare chez le chat. Comme précédemment décrit avec les hernies diaphragmatiques, les hernies hiatales semblent jouer un rôle dans l'apparition de cette affection. Le diagnostic radiographique peut s'avérer complexe. La prise en charge est chirurgicale, bien que le pronostic soit réservé.
Bibliographie
- LEARY ML, SINNOTT-STUTZMAN V. Spontaneous gastric dilatation-volvulus in two cats. Journal of Veterinary Emergency and Critical Care. 2018;28(4):346-55.
- FORMAGGINI L, SCHMIDT K, DE LORENZI D. Gastric dilatation-volvulus associated with diaphragmatic hernia in three cats: Clinical presentation, surgical treatment and presumptive aetiology. Journal of Feline Medicine and Surgery. 2008;10(2):198-201.
- PHILLIPS H, CORRIE J, ENGEL DM, DUFFY DJ, HOLT DE, KENDALL AR, et al. Clinical findings, diagnostic test results, and treatment outcome in cats with hiatal hernia: 31 cases (1995-2018). Veterinary Internal Medicine. 2019;33(5):1970-6.
- NAGPAL S, MAGACHA HM, GOENKA P, VEDANTAM V. Acute Gastric Volvulus: A Rare Complication of Hiatal Hernia. Cureus. 2024; 6(8): e66102.
- RANDALL E, PARK R. The Diaphragm. In: Textbook of Veterinary Diagnostic Radiology. Sixth edition. SAINT-LOUIS: ELSEVIER; 2013. p. 535-49.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Torsion humérale externe associée aux déformations angulaires antébrachiales acquises et correction par ostéotomie de dérotation humérale : à propos de 4 cas
Baptiste FROIDEFOND
Coauteurs : Alexandre GUILLEMOT, Bertrand VEDRINE
Introduction
Les déformations antébrachiales sont des anomalies angulaires du radius et de l'ulna, pouvant se manifester dans les trois plans : frontal, sagittal et axial. Le radius curvus peut être congénital ou acquis, uni ou bilatéral. L'imagerie en coupe, la reconstruction 3D, ainsi que les outils de planification virtuelle et d'impression 3D, facilitent une correction précise dans ces trois plans. Bien que leur utilisation soit bien documentée, les déformations associées de l'humérus n'ont pas été décrites jusqu'à présent. Cette étude rapporte l'observation de torsions humérales externes et leur traitement par ostéotomie de dérotation dans le cadre de déformations antébrachiales.
Matériels et méthodes
Les cas présentés concernent quatre chiens ayant bénéficié d'une planification 3D pour traiter des déformations antébrachiales unilatérales. Un examen scanner des deux membres antérieurs entiers a été réalisé. La segmentation 3D (3DSlicer®) a permis d'extraire les os, et la planification chirurgicale a été réalisée à l'aide d'un logiciel de CAO (Blender®). Le membre controlatéral sain a servi de référence pour mesurer la torsion humérale.
Cas 1
Un chien créole mâle castré de 2 ans présente une déformation antébrachiale avec boiterie chronique du membre antérieur droit. L'examen révèle une déformation complexe avec incongruence du coude (ulna court), une instabilité radiocarpienne, et un conflit avec un précédent matériel d'ostéosynthèse. L'humérus présente une déformation sagittale (recurvatum de 15°) et axiale (torsion externe de 25°). Une panarthrodèse du carpe est réalisée, motivée par la dégénérescence radiocarpienne.
Cas 2
Un Berger Allemand femelle de 4 mois est présenté pour une déformation du membre antérieur gauche. L'analyse 3D révèle une déformation antébrachiale dans les trois plans et une torsion humérale externe de 20 %. Une incongruence sévère du coude avec un ulna court et une non-union du processus anconé sont également observées. Une ostéotomie de dérotation humérale est réalisée à l'aide de guides 3D, suivie d'une ostectomie ulnaire et d'une fixation du processus anconé. Deux jours après, une correction du radius est réalisée, avec une ostéotomie distale stabilisée par plaque et une ostéotomie proximale avec fixateur externe de type ILIZAROV pour une distraction ostéogénique. Une seconde correction est réalisée en fin de croissance avec une nouvelle ostectomie ulnaire et une double ostéotomie du radius.
Cas 3
Une femelle Bouvier Bernois de 6 mois présente une déformation antébrachiale gauche. À 6 mois, une ostectomie ulnaire est réalisée. À 1 an, une analyse 3D met en évidence une torsion humérale externe de 25° et une déformation antébrachiale dans les 3 plans. Une ostéotomie de dérotation humérale et une ostectomie en coin du radius sont réalisées à 1 mois d'intervalle.
Cas 4
Un Spitz Nain mâle de 3 ans montre une déformation du membre antérieur gauche. L'analyse 3D révèle un valgus du radius distal et une torsion humérale externe de 12°. Une ostéotomie de dérotation humérale est réalisée, suivie d'une ostectomie en coin du radius quatre mois plus tard.
Résultats
Les déformations antébrachiales observées étaient associées à une torsion externe de l'humérus (de 12° à 25°). Une ostéotomie de dérotation humérale a été réalisée dans trois cas. Une complication majeure sur le cas n°4 a nécessité une reprise chirurgicale due à un débricolage et un retard de cicatrisation. Une autogreffe du fragment d'ostectomie radiale a permis la consolidation de l'humérus.
D'un point de vue fonctionnel, les cas 1 et 2 ont continué à présenter une boiterie marquée du membre affecté (incongruence sévère du coude). Les cas 3 et 4 ont un résultat fonctionnel excellent, bien qu'un valgus du carpe associé à une instabilité ait persisté dans le dernier cas.
Discussion
La planification virtuelle et l'impression 3D pour la correction des déformations antébrachiales se généralise, mais ces résultats suggèrent qu'un examen du membre entier est crucial pour évaluer toutes les déformations osseuses associées au radius curvus. Lors de radius curvus acquis par fermeture précoce du cartilage de croissance distal de l'ulna, une torsion humérale externe peut accompagner les déformations, contribuant au défaut d'alignement du membre et à la difficulté qu'un chirurgien peut rencontrer sur certains cas pour restaurer une anatomie normale en ne traitant que l'avant-bras.
Il est communément admis que les déformations sur le plan frontal (valgus/varus) et axial (torsion) peuvent être plus handicapantes que sur le plan sagittal (recurvatum/procurvatum). L'identification et le traitement de la torsion humérale peuvent donc être essentiels pour restaurer une fonction normale. Pour les cas unilatéraux, le membre sain peut servir de référence, ce qui n'est pas possible pour les déformations congénitales bilatérales. Des études supplémentaires sont nécessaires pour mieux cibler les populations susceptibles de bénéficier d'une ostéotomie de dérotation humérale, dresser des recommandations sur les méthodes de fixation et créer des bases de données sur la conformation des humérus chez les races prédisposées aux déformations angulaires des membres antérieurs.
Conclusion
Un radius curvus acquis peut être associé à une torsion humérale externe. L'ostéotomie de dérotation humérale est réalisable, et les outils de planification chirurgicale virtuelle et d'impression 3D sont efficaces pour ce type de traitement.
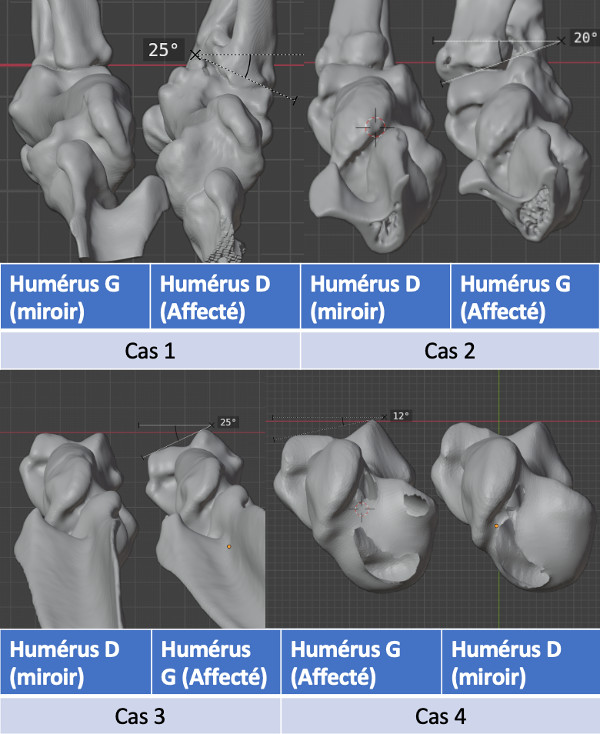
Figure 1

Figure 2
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Toxoplasmose cérébrale chez un chat immunocompétent
La toxoplasmose, une affection parasitaire occasionnée par le parasite intracellulaire coccidien Toxoplasma gondii, est la deuxième maladie infectieuse du système nerveux central la plus fréquemment diagnostiquée chez le chat.
Commémoratifs et examen clinique
Un chat européen mâle castré de 8 ans est présenté en urgence en neurologie après avoir été retrouvé inconscient en décubitus latéral. Il y a 8 mois, ce chat a présenté un épisode de 10 minutes pendant lequel il titubait puis chutait et restait flasque et inconscient. Dix jours avant la présentation, il a commencé à présenter des épisodes récurrents intermittents d'un autre type (tourner en cercle sur la gauche, vocaliser et déambuler sans but).
L'examen clinique révèle une bradycardie à 140 BPM. À l'examen neurologique, le chat est stuporeux, en décubitus latéral en posture de décérébellation, en myosis serré bilatéral associé à un nystagmus vertical et une absence de clignement à la menace. Une atteinte majeure et aiguë du cervelet est suspectée. Une hypertension intracrânienne à l'origine d'un engagement du cervelet dans le foramen magnum en raison d'un processus tumoral intracrânien est évoquée en priorité. Une prise en charge d'urgence alliant mannitol, furosémide et méthylprednisolone est instaurée dès l'admission. Un examen IRM de l'encéphale réalisé dans l'heure confirme l'engagement du cervelet dans le foramen magnum associé à un engagement des hémisphères cérébraux sous la tente du cervelet et met en évidence dans l'hémisphère gauche une volumineuse lésion à base large adossée à l'os temporal, prenant fortement le produit de contraste, évoquant en priorité un méningiome associé à un œdème péri-lésionnel important. Une deuxième lésion punctiforme du même type est observée dans l'hémisphère droit.
Traitement et suivi
Une exérèse chirurgicale de la masse est réalisé en urgence le jour même et permet une rémission des symptômes. Son examen histologique révèle que la lésion n'est pas tumorale mais compatible avec un granulome de toxoplamose (lésions inflammatoires nécrosantes, présence de bradyzoites compatibles avec Toxoplasma gondii). La sérologie toxoplasmose est fortement positive (IgG 1/2560).
Un traitement médical adjuvant associant méthylprednisolone et clindamycine est mis en place. Une IRM de contrôle 1 mois post-opératoire révèle une augmentation de taille de la lésion punctiforme précédemment observée, associée à un œdème périlésionnel important justifiant un ajustement thérapeutique avec ajout de sulfamide-triméthoprim et augmentation de la dose de clindamycine.
Les IRM de contrôle réalisés 2 et 3 mois post-op révèlent une diminution de la taille de la lésion résiduelle suggérant une rémission confirmée par l'évolution des sérologies toxoplasmose (8 semaines post-op IgG = IgM 1/640, 10 semaines post-op (IgG = IgM 1/320). À l'heure où nous écrivons cet abstract, le chat est en rémission clinique (6 mois post-op) et un suivi IRM et sérologique est prévu.
Conclusion
La toxoplasmose est une maladie très bien connue chez le chat. Bien que l'atteinte neurologique soit histologiquement présente chez presque tous les chats atteints de toxoplasmose, les signes cliniques liés à l'atteinte du SNC ne sont observés que dans environ 10 % des cas.
La plupart des chats en bonne santé développent une immunité qui empêche l'expression clinique de la maladie. Mais cette immunité ne détruit pas les kystes tissulaires et ces chats restent néanmoins infectés latents. Ainsi, la toxoplasmose cérébrale « clinique » est liée à la réactivation des bradyzoïtes latents dans le cerveau et peut se produire chez les patients qui deviennent immunodéprimés en raison d'infection ou de traitements immunosuppresseurs.
Dans la grande majorité des toxoplasmoses cérébrales félines, les lésions sont multifocales. Ces lésions multiples ont souvent des contours peu définis. Des lésions isolées plus définies (granulome) ressemblant à un processus tumoral ont été décrites chez deux chats. Dans les deux cas les chats étaient immunocompétents, les lésions IRM évoquaient un processus tumoral et c'est l'analyse histologique postexérèse chirurgicale qui a permis de faire le diagnostic. Dans les deux cas, une récidive des signes cliniques a été observée respectivement à 8 et 21 mois post-opératoire malgré un traitement à la clindamycine de 3 semaines. Un des chats a été euthanasié sans examen IRM de suivi, l'autre présentait un nodule similaire au premier et a été traité à nouveau avec de la clindamycine.
Le cas présenté est très similaire aux deux cas décrits dans la littérature et illustre la présentation neurologique possible d'une toxoplasmose cérébrale chez le chat ainsi que la nécessité d'inclure cette hypothèse dans le diagnostic différentiel de toute lésion du SNC compatible avec un granulome. Cette hypothèse n'avait pas été envisagée chez ce chat immunocompétent (Felv-Fiv négatif, absence de traitement immunosuppresseur) vivant strictement en intérieur et recevant une alimentation strictement industrielle. La contamination est supposée avoir eu lieu dans les 3 premiers mois de vie ou in utéro (chaton trouvé à la campagne vers l'âge de 3 mois). L'autre chaton trouvé en même temps que lui et supposé être son frère est également positif en sérologie. La cause du développement de granulomes cérébraux 10 ans plus tard sans baisse d'immunité objectivable chez ce chat reste inconnue d'autant plus que son supposé frère, qui vit avec lui, n'a présenté aucun signe clinique et aucune lésion visible à l'examen IRM de l'encéphale de dépistage.
Bibliographie
- DEL VECCHIO OV, GRANDE C. Toxoplasma gondii multifocal central nervous system infiltration in an apparently immunocompetent cat in Italy. Vet Parasitol Reg Stud Reports. 2021 Jul;25:100605. doi: 10.1016/j.vprsr.2021.100605. Epub 2021 Jun 24. PMID: 34474798.
- GUNN-MOORE DA, REED N. CNS disease in the cat: current knowledge of infectious causes. J Feline Med Surg. 2011 Nov;13(11):824-36. doi: 10.1016/j.jfms.2011.09.004. PMID: 22063207; PMCID: PMC10911295.
- FALZONE C, BARONI M, DE LORENZI D, MANDARA MT. Toxoplasma gondii brain granuloma in a cat: diagnosis using cytology from an intraoperative sample and sequential magnetic resonance imaging. J Small Anim Pract. 2008 Feb;49(2):95-9. doi: 10.1111/j.1748-5827.2007.00421.x. Epub 2007 Sep 3. PMID: 17784931.
- PFOHL JC, DEWEY CW. Intracranial Toxoplasma gondii granuloma in a cat. J Feline Med Surg. 2005 Dec;7(6):369-74. doi: 10.1016/j.jfms.2005.03.004. PMID: 15914056; PMCID: PMC10822423.
- NEGRIN, A., LAMB, C. R., CAPPELLO, R., & CHERUBINI, G. B. (2007). Results of magnetic resonance imaging in 14 cats with meningoencephalitis. Journal of feline medicine and surgery, 9(2), 109-116.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 TP53 as a Prognostic Biomarker in Canine Lymphoma: Insights from a Targeted Next-Generation Sequencing Approach
Introduction
The tumor suppressor gene TP53 plays a critical role in maintaining genomic stability, regulating apoptosis, and responding to cellular stress. In human oncology, TP53 mutations are frequent across many malignancies and correlate with treatment resistance and poor outcomes. Despite increasing evidence of its relevance in canine cancers, the prognostic significance of TP53 in canine lymphomas has remained scarcely explored.
Previous studies in canine diffuse large B-cell lymphoma (DLBCL) have identified TP53 as a recurrently mutated gene with potential clinical implications. However, the heterogeneity of lymphoma subtypes and the lack of large-scale, histotype-inclusive genomic datasets have limited the broader application of TP53 as a biomarker in veterinary oncology.
This study leverages a novel targeted next-generation sequencing panel, the "K9 lymphoma assay," to investigate the mutational status of TP53 and its prognostic impact across a large cohort of dogs with histologically and clinically characterized lymphomas. The K9 lymphoma assay represents a significant advancement, enabling comprehensive profiling of 31 genes recurrently mutated in canine lymphomas and facilitating genetic stratification across diverse histotypes.
Matériel et résultats
This study included 257 dogs with newly diagnosed, untreated B- and T-cell lymphomas. All cases underwent complete staging and histological classification. Genomic DNA was extracted from fresh-frozen lymph node biopsies, and libraries were prepared for sequencing using the AGILENT SureSelect XT HS2 system. The custom 196-kbp tNGS panel targeted exons and UTRs of genes implicated in lymphomagenesis. Sequencing was performed on the ILLUMINA NextSeq 550 platform, and variant calling employed GATK Mutect2, Varscan2, and FreeBayes, followed by stringent filtering and annotation using ANNOVAR and SIFT. Statistical associations between mutational status and clinical outcomes - time to progression (TTP) and lymphoma-specific survival (LSS) - were evaluated using COX proportional hazards models and regression tree analysis.
TP53 was found mutated in a significant subset of B-cell lymphomas (BCL), with mutations primarily consisting of missense and nonsense variants predicted to impair protein function. Dogs harboring TP53 mutations exhibited significantly shorter TTP and LSS across both aggressive and indolent BCLs. Specifically, in aggressive BCLs, median TTP and LSS were 52 and 113 days in TP53-mutant dogs, compared to 202 and 343 days in TP53 wild-type counterparts (p = 0,01). Similar trends were observed in indolent BCLs, where TP53 mutations predicted markedly poorer outcomes (median TTP: 78 vs. 188 days; LSS: 105 vs. 359 days, p < 0,01). Notably, TP53 mutations co-occurred with mutations in FAT4, suggesting potential cooperative oncogenic effects. Conversely, in T-cell lymphomas (TCL), TP53 mutations were rare and did not correlate with survival outcomes, indicating a histotype-specific relevance.
Conclusion
The findings firmly establish TP53 mutation status as an independent and robust negative prognostic factor in canine BCL. The consistent association with shortened survival, regardless of histologic subtype, underscores its potential as a universal biomarker to guide therapeutic decision-making. Moreover, the data support the clinical utility of integrating genomic profiling into the diagnostic and prognostic workflow for canine lymphoma. Dogs with TP53-mutant tumors may require intensified or alternative treatment strategies, including immunotherapy, which has shown benefit in previous studies. The lack of prognostic impact in TCL highlights the need for TCL-specific panels and broader genomic exploration.
Liens d'intérêt : I am a consultant for MyLav Laboratory.
📃 Traitement chirurgical d'une cyphose thoracique congénitale à l'aide de guides imprimés en 3D
Introduction
Une cyphose vertébrale congénitale est une malformation du rachis due à un défaut de développement du sclérotome à partir des somites lors de l'organogenèse. Elle se rencontre principalement chez les races brachycéphales, comme le Carlin et le Bouledogue Français. Bien qu'elle puisse être découverte fortuitement et soit parfois asymptomatique, elle induit fréquemment une myélopathie thoraco-lombaire, responsable de troubles locomoteurs des membres pelviens.
Le traitement conservateur de cette affection a montré des résultats décevants dans la littérature, tandis qu'un traitement chirurgical est souvent associé à une amélioration clinique. Plusieurs techniques chirurgicales ont été décrites, avec un abord dorsal ou transthoracique, uni ou bilatéral, avec ou sans ouverture du canal vertébral, et avec différentes méthodes de stabilisation (plaque, vis/broches et PMMA). L'impression de modèles anatomiques et de guides chirurgicaux sur mesure a également été rapportée. Nous présentons ici un cas de cyphose thoracique sévère, traitée chirurgicalement à l'aide d'outils de planification et d'impression 3D de guides chirurgicaux.
Anamnèse
Un Bouledogue Français femelle entière de 4 mois est présenté en consultation pour des troubles locomoteurs chroniques survenant depuis son adoption à 2 mois. La chienne ne semble pas douloureuse selon la propriétaire. Une radiographie du rachis thoraco-lombaire effectuée à 4 mois par le vétérinaire traitant met en évidence une cyphose thoracique marquée.
Examen clinique
La chienne est ambulatoire sur 4 membres à 4 mois, avec une ataxie marquée des membres postérieurs. Les placers proprioceptifs des membres pelviens sont fortement retardés. Le tonus, les réflexes médullaires et la nociception sont conservés. La palpation du rachis thoraco-lombaire et la manipulation des cervicales ne provoquent pas de douleur évidente. Le reste de l'examen clinique, orthopédique et neurologique est normal. À 6 mois, la locomotion s'est dégradée en une paraparésie non ambulatoire avec des plaies d'escarres sur la face dorsale des métatarses.
Démarche diagnostique
Un scanner et un myéloscanner du rachis thoraco-lombaire sont réalisés. L'examen révèle une cyphose thoracique sévère centrée sur T7 et T8 avec un angle de COBB de 102°. La moelle épinière est sévèrement comprimée à l'apex de la malformation.
Traitement
Une chirurgie de distraction-stabilisation par abord transthoracique est convenue avec la propriétaire. Il est décidé d'utiliser la planification et l'impression 3D de guides.
Les données d'imagerie sont importées dans un logiciel de segmentation (3D Slicer®) pour obtenir un modèle 3D. Un logiciel de conception assistée par ordinateur (CAO, Blender®) permet de simuler la position des implants dans les corps vertébraux et de modéliser des guides sur mesure. Ces derniers, ainsi qu'un modèle anatomique, sont imprimés en 3D en résine photopolymérisable (technologie SLA) et stérilisés à l'ozone (SterOx System, Sterilux®).
L'animal est placé en décubitus latéral gauche avec environ 30° d'inclinaison. Un abord est réalisé sur le 7e espace intercostal droit. La face ventrolatérale droite des corps vertébraux de T4 à T10 est exposée après dissection de la veine azygos, de la vascularisation intercostale et du tronc sympathique. Sept broches de 1,8 mm de diamètre sont insérées dans les corps vertébraux à l'aide des guides. Un distracteur à broches est positionné sur les deux broches les plus distantes, et une distraction est appliquée. Les autres broches sont remplacées par des vis de 2,4 mm de diamètre, et le rachis est stabilisé par du polyméthylméthacrylate. Un drain thoracique est posé et le thorax est refermé de façon conventionnelle avant de recréer le vide pleural.
Des radiographies et un scanner post-opératoire sont réalisés. Une cyphose résiduelle persiste avec un angle de COBB de 58°. Un plan de rééducation fonctionnelle est mis en place. En post-opératoire immédiat, l'examen neurologique est identique à celui réalisé avant l'opération. À 1 mois post-opératoire, la chienne est paraparétique ambulatoire. À 2 mois, les déficits sont mineurs, et la fonction locomotrice est complètement rétablie à 3,5 mois post-opératoires.
Discussion
Lors de cyphose vertébrale, un angle de COBB > 35° est associé à un risque accru de déficits neurologiques. Notre cas présentait une déformation qualifiée de sévère, avec un angle de 102°, bien qu'une différence notable puisse exister entre les modalités d'imagerie. Les techniques chirurgicales décrites ne sont pas standardisées et les résultats varient, tant en termes de réduction de la déformation que d'amélioration clinique. Cela reflète sans doute l'approche individuelle indispensable dans ces cas, et la nécessité parfois d'adjoindre la distraction du rachis à une décompression par laminectomie dorsale. La planification 3D a permis ici de choisir un abord à droite, contrairement à l'étude de référence, car une discrète scoliose associée à la cyphose exposait mieux les corps vertébraux de T7 et T8 de ce côté, et la conformation des côtes suggérait une meilleure exposition.
Conclusion
Le traitement chirurgical d'une cyphose congénitale peut permettre une résolution des troubles locomoteurs. Les outils de planification et d'impression 3D permettent une préparation individualisée de la chirurgie et augmentent la sécurité du patient.
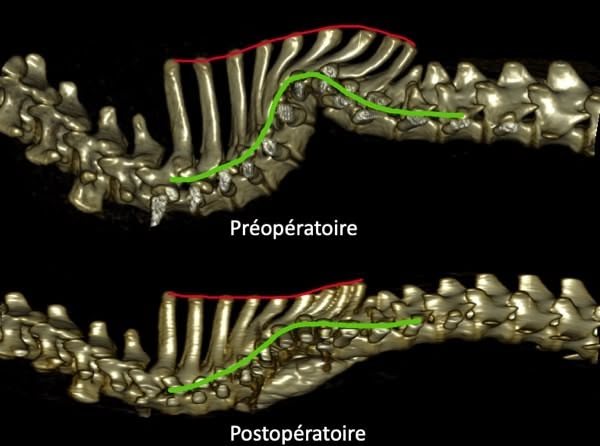
Figure 1
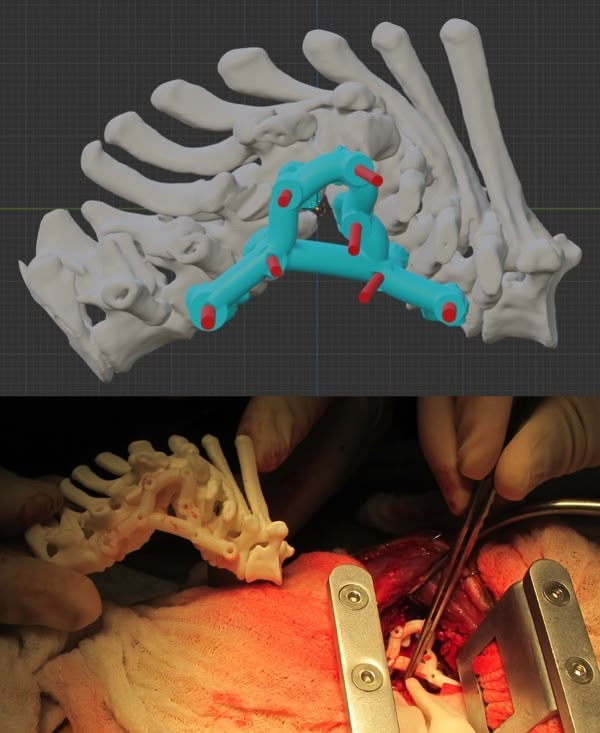
Figure 2
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Traitement de différentes affections par la phytothérapie : quelles plantes font le lien ?
I. Introduction
Les propriétaires d'animaux sollicitent souvent les vétérinaires pour explorer d'éventuelles alternatives thérapeutiques aux médicaments conventionnels. Les données concernant les effets des plantes médicinales sur les animaux de compagnie restent plus limitées que celles disponibles en médecine humaine, mais la connaissance des différents effets démontrés aussi bien chez l'homme que chez les animaux de laboratoire peut conduire le vétérinaire à explorer différentes pistes thérapeutiques à base de plantes médicinales.
Les différentes propriétés thérapeutiques des plantes médicinales reposent notamment sur la multiplicité de leurs composants qui peuvent moduler simultanément plusieurs processus physiopathologiques. Parmi elles, trois plantes suscitent un intérêt croissant pour leur potentiel à la croisée des différentes problématiques. Le curcuma (Curcuma longa L.), la réglisse (Glycyrrhiza glabra L.) et la boswellie (Boswellia serrata Roxb. ex Colebr.). Leur utilisation peut permettre au vétérinaire de faire le lien entre différentes affections, inflammatoires, digestives, métaboliques, hépatiques, articulaires, respiratoires, ou liées au stress oxydant.
II. Préambule
Au début des années 1980, le marché français comptait près de 130 médicaments à base de plantes disposant d'une autorisation de mise sur le marché (AMM). En 2025, seuls huit demeurent enregistrés. Cette réduction majeure est en partie liée à l'impossibilité de protéger les formules par brevet, ce qui limite l'intérêt économique pour les laboratoires, face aux coûts liés au développement, aux essais cliniques et au maintien des dossiers d'AMM. Le vétérinaire peut cependant avoir recours à la préparation magistrale ou extemporanée en respectant la règlementation (cascade). Les produits utilisés pour ces préparations doivent dans la mesure du possible être des matières premières à usage pharmaceutique (MPUP) ou lorsque la plante utilisée n'est pas disponible sous ce format, des poudres de plantes, soumise à de rigoureuses procédures de contrôle qualité, établies à toutes les étapes de la chaîne : de la récolte au stockage.
Des recommandations pour la réalisation de préparations extemporanées ont été éditées par le réseau de phyto-aromathérapie de l'AFVAC, AVEF, SNGTV sur le site du RéPAAS. www.repaas.org.
III. Le curcuma (Curcuma longa L.)
Le curcuma contient notamment des curcuminoïdes dont le plus connu est la curcumine. Il est traditionnellement utilisé pour ses propriétés anti-inflammatoires et antioxydantes. Son spectre d'action s'étend de la modulation des cytokines pro-inflammatoires à la protection hépatique, avec un intérêt particulier dans les maladies métaboliques et articulaires.
1. Des preuves d'efficacité chez l'homme
Un article de revue, publié en 2024, compile 11 méta-analyses portant sur l'utilisation du curcuma et des curcuminoïdes en cas d'arthrose chez l'homme. Il conclut à des effets sur la douleur, une amélioration de la mobilité et de la raideur des articulations, et à la réduction la consommation de médicaments chez les patients atteints d'arthrose. [1]
Un rôle protecteur a également été identifié pour le curcuma et ses composés en cas stéatose hépatique non alcoolique avec une amélioration des niveaux des enzymes hépatiques (ALT, AST), et une diminution du stress oxydant. Enfin, de nombreuses études portent sur les effets du curcuma sur la glycémie et l'ensemble des paramètres modifiés lors de maladie métabolique. Les premiers essais montrent des effets protecteurs à différents niveaux, avec notamment une diminution de la glycémie.
2. État des lieux chez le chien
Une revue de littérature effectuée en 2022 a permis de faire un état des lieux des différentes données publiées chez les animaux de compagnie comparées à celles disponibles chez l'homme. Le curcuma et la curcumine engendrent des effets bénéfiques dans de nombreuses situations. Des effets anti-inflammatoires systémiques et antioxydants ont été démontrés aussi bien chez l'homme que chez l'animal, via le piégeage de radicaux libres et la diminution du stress oxydatif. Les effets sur le métabolisme hépatique et les maladies métaboliques sont plus étudiés chez l'homme mais des premiers résultats encourageants sont disponibles chez le chien. Certaines études ont même mis en évidence des effets antiprurigineux lors d'atopie [2].
Les cucuminoïdes étant peu biodisponibles, des études plus approfondies seraient nécessaires pour évaluer l'absorption et la métabolisation du curcuma ainsi que des études spécifiques contre placebo sur de larges cohortes pour confirmer les effets observés dans ces premières études.
IV. La réglisse (Glycyrrhiza glabra L.)
La réglisse, dont le principal constituant actif est la glycyrrhizine, est utilisée pour la prise en charge symptomatique de différentes affections du tractus respiratoire ou gastro-intestinal. L'agence européenne du médicament (EMA) a listé les utilisations traditionnelles de la réglisse dans de nombreux pays européens pour soulager les symptômes lors d'ulcères gastriques et duodénaux et lors certains troubles respiratoires (toux, asthme) [3].
La réglisse, une fois absorbée, est métabolisée et certains de ses métabolites (dont l'acide glycyrrhétique) ont des effets similaires à ceux produits par l'aldostérone et les corticostéroïdes. Il a été démontré qu'ils inhibent la 11β-hydroxystéroïde déshydrogénase de type 2 (11β-OHSD2), au niveau des cellules rénales sans pour autant avoir d'effets directs sur les récepteurs minéralocorticoïdes. Ce mécanisme d'action serait impliqué dans les propriétés anti-inflammatoires de la réglisse, que ce soit au niveau respiratoire, cutané ou digestif.
Les publications de données relatives à l'utilisation de la réglisse sur les animaux de compagnie restent encore limitées. Des recherches ont néanmoins été menées, notamment lors d'administration d'aliments complémentés. Il a été rapporté des effets bénéfiques lors de la prise en charge de dermite atopique, dans une étude en double aveugle contre placebo menée sur 40 chiens, avec un aliment complémenté en curcuma et en réglisse [4]. Des études récentes ont également démontré que l'utilisation de réglisse à des doses considérées comme thérapeutiques chez le chien n'était pas à l'origine d'hypertension comme cela peut être le cas chez l'homme.
Au niveau de la sphère digestive, des extraits de réglisse ont montré des effets protecteurs lors d'administrations concomitantes de carprofène ou de robenacoxib. Enfin, une étude récente a démontré que la réglisse pouvait être intéressante en cas d'hypertrophie bénigne de la prostate en lien avec les effets anti-inflammatoires et antioxydants de ses composants.
Du point de vue respiratoire, une atténuation de l'inflammation pulmonaire via des médiateurs tels que NF-κB et Nrf2 a été démontrée chez des animaux de laboratoire. Un essai clinique portant sur 54 personnes atteintes d'asthme chronique a mis en évidence des effets anti-inflammatoires et bronchodilatateurs de Glycyrrhiza glabra.
Des vétérinaires qui utilisent la réglisse dans cette indication rapportent des effets bénéfiques mais ces effets seraient à confirmer dans des études à large échelle contre placebo.
V. La boswellie (Boswellia serrata)
Les propriétés anti-inflammatoires de la boswellie ont été plus spécifiquement étudiées pour certains de ses composants : les acides boswelliques. Ces acides inhibent de façon sélective la 5-lipoxygénase in vitro. La boswellie, également appelée encens indien a une longue tradition d'utilisation pour les affections articulaires chroniques. Des études récentes ont également montré des effets bénéfiques sur les maladies inflammatoires chroniques de l'intestin et les affections respiratoires comme l'asthme.
L'efficacité de la résine de Boswellia serrata a été évaluée dans une étude multicentrique chez 29 chiens atteints de maladies articulaires ou rachidiennes chroniques. Les animaux ont reçu une dose de 400 mg/10 kg/jour pendant 6 semaines. Une amélioration clinique (douleur, boiterie, raideur) a été observée chez environ 71% des chiens, avec une bonne tolérance et peu d'effets indésirables, suggérant un intérêt thérapeutique dans les affections articulaires chroniques du chien [5].
Toutefois, une étude menée en 2019 à la faculté de médecine vétérinaire de Floride a montré une forte variabilité dans la teneur en acides boswelliques actifs (AKBA et KBA) de plusieurs aliments complémentaires contenant Boswellia serrata. Les concentrations mesurées étaient souvent inférieures aux valeurs annoncées [6]. Cette hétérogénéité complique l'évaluation de la reproductibilité des effets cliniques et pose un problème majeur de fiabilité pour le vétérinaire, souvent sollicité par des propriétaires ayant recours à ce type de produits. Des contrôles qualité indépendants et une connaissance précise de la composition seraient indispensables pour juger de l'efficacité réelle de ces compléments — ce qui serait possible si des médicaments à base de plantes médicinales, standardisés et encadrés, étaient disponibles.
VI. Conclusion
L'intégration des plantes médicinales dans la pratique vétérinaire ouvre des perspectives intéressantes pour la prise en charge des affections chroniques, en particulier celles impliquant des processus inflammatoires, métaboliques ou oxydatifs. Le curcuma, la réglisse et la boswellie constituent trois exemples emblématiques de plantes capables de « faire le lien » entre plusieurs affections, en raison de la multiplicité de leurs composés bioactifs et de leurs cibles physiopathologiques.
Cependant, malgré des résultats prometteurs issus de la médecine humaine et de la recherche préclinique, les données vétérinaires demeurent limitées et parfois hétérogènes, notamment en raison de l'absence de standardisation des extraits utilisés et de la variabilité de composition des aliments complémentaires disponibles sur le marché. Cette situation met en lumière l'importance cruciale d'une meilleure régulation, d'analyses indépendantes et de contrôles qualité rigoureux, de la culture de la plante jusqu'au produit final.
Dans un contexte où le nombre de médicaments à base de plantes bénéficiant d'une AMM est extrêmement réduit, le recours à des préparations magistrales ou extemporanées, réalisées en accord avec la réglementation (cf. recommandations proposées par le RéPAAS), apparaît comme une voie indispensable pour garantir aux praticiens des outils fiables et sécurisés. Le développement de travaux cliniques robustes, associant qualité des extraits et méthodologie rigoureuse, sera essentiel pour valider scientifiquement l'intérêt de ces approches et permettre au vétérinaire d'intégrer pleinement la phytothérapie dans une médecine moderne, raisonnée et basée sur des preuves.
Bibliographie
- BIDESHKI, M. V., et coll. The efficacy of curcumin in relieving osteoarthritis : A meta-analysis of meta-analyses. Phytotherapy Research: (2024), 38(6), 2875-2891.
- KĘPIŃSKA-PACELIK J, BIEL W. Turmeric and Curcumin-Health-Promoting Properties in Humans versus Dogs. Int J Mol Sci. 2023;24(19), 14561,1-24
- Liquiritiae radix - herbal medicinal product | European Medicines Agency (EMA). Community herbal monograph https://www.ema.europa.eu/en/medicines/herbal/liquiritiae-radix
- WATSON A, et coll. A novel therapeutic diet can significantly reduce the medication score and pruritus of dogs with atopic dermatitis during a nine-month controlled study. Vet Dermatol. 2022;33, 55-63
- REICHLING J, et coll. Dietary support with Boswellia resin in canine inflammatory joint and spinal disease. Schweiz Arch Tierheilkd. 2004;146(2):71-79.
- MISCIOSCIA E, et coll. Measurement of 3-acetyl-11-keto-beta-boswellic acid and 11-keto-beta-boswellic acid in Boswellia serrata Supplements Administered to Dogs. BMC Vet Res. 2019;15(1):270, 2-7
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Traitement de l'hypertension artérielle systémique chez l'animal cardiorénal : équilibre entre efficacité et protection rénale
Guyancourt, France
Allonzier-la-Caille, France
I. Introduction
L’hypertension artérielle systémique est une affection fréquemment rencontrée en médecine vétérinaire, en particulier chez les animaux âgés. Elle se définit par une élévation persistante de la pression artérielle systolique (PAS), associée ou non à des lésions dites « organe-cible ». Son identification et sa prise en charge précoce revêtent une importance majeure, car une hypertension soutenue peut provoquer des atteintes irréversibles des reins, du cœur, des yeux et du système nerveux central. Dans le cas d’un patient cardiorénal, l’hypertension artérielle est une conséquence fréquente de la maladie rénale (jusqu’à 93 % des chiens et 65 % des chats) pouvant aggraver la maladie rénale et cardiaque et nuire au pronostic de patient.
Le consensus de l’American College of Veterinary Internal Medicine (ACVIM) [1] constitue la référence actuelle en termes de définition, classification et recommandations thérapeutiques.
II. Définition et classification
Selon le consensus de l’ACVIM, l’hypertension artérielle est définie comme une élévation persistante de la pression sanguine. Elle se décline en trois catégories principales :
- hypertension situationnelle : liée à des facteurs de stress environnementaux ou émotionnels ;
- hypertension secondaire : consécutive à un processus pathologique sous-jacent. Chez le chien, les principales causes incluent les affections rénales (chroniques ou aiguës), l’hyperadrénocorticisme, les phéochromocytomes ou encore le diabète sucré. Chez le chat, elle est le plus souvent associée à une maladie rénale chronique, un hyperthyroïdisme ou un hyperaldostéronisme. Certains médicaments (gluco- et minéralocorticoïdes), agents stimulant l’érythropoïèse ou substances illicites (cocaïne, méthamphétamines) peuvent également induire une hypertension secondaire ;
- hypertension idiopathique : diagnostiquée lorsqu’aucune cause sous-jacente n’est identifiée.
La classification de la pression artérielle systémique (PAS) chez le chien et le chat se fait selon les seuils suivants :
- normotension : PAS < 140 mmHg ;
- préhypertension : PAS 140–159 mmHg ;
- hypertension : PAS 160–179 mmHg ;
- hypertension sévère : PAS ≥ 180 mmHg.
III. Atteintes des organes cibles
Une hypertension artérielle soutenue entraîne des atteintes dites “organe-cible”, au niveau des reins, du cœur et des vaisseaux, des yeux et du système nerveux central. Les principales lésions et manifestations cliniques sont résumées dans le tableau ci-dessous dans le Tableau 1.
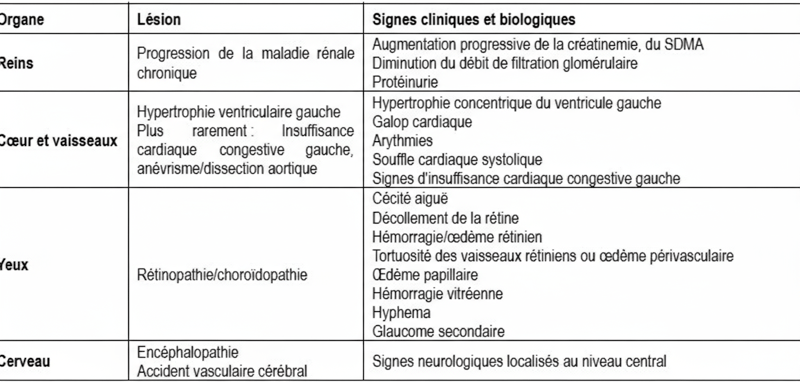
Tableau 1
IV. Mesure de la pression artérielle
La mesure invasive est le gold standard mais peu utilisée en pratique clinique. Les méthodes non invasives sont privilégiées :
- doppler : plus fiable, surtout pour les petits animaux ;
- oscillométrie : pratique mais plus sensible aux artéfacts, notamment chez les chats stressés.
Le protocole recommandé par l’ACVIM inclut un environnement calme, une période d’acclimatation, l’utilisation d’un brassard adapté (largeur = 40 % de la circonférence du membre ou de la queue) et au moins 5 mesures consécutives, dont on calcule la moyenne (hors première valeur).
V. Prise en charge thérapeutique
Les objectifs sont de limiter ou prévenir les lésions irréversibles des organes cibles, de traiter la cause sous-jacente en cas d’hypertension secondaire et de ramener la PAS en dessous de 160 mmHg (et idéalement < 150 mmHg si atteintes organiques déjà présentes).
La présence de lésions organiques (par exemple, rétinopathie et insuffisance rénale chronique) justifie le début d'un traitement après une seule séance de mesure, mais dans la plupart des cas, les résultats doivent être confirmés par des mesures répétées à plusieurs reprises (> 2).
On parle d’urgence hypertensive lorsque la PAS est ≥ 180 mmHg et/ou qu’il existe des signes cliniques liés à des lésions d’organes cibles menaçant le pronostic vital ou fonctionnel : cécité aiguë (décollement de rétine, hémorragie intraoculaire), signes neurologiques importants (convulsions, ataxie, coma), décompensation cardiaque aiguë (dyspnée, œdème pulmonaire).
VI. Prise en charge immédiate
Hospitalisation et surveillance rapprochée (monitoring tensionnel toutes les 30–60 minutes) avec pour objectif de réduire la PAS progressivement (15–25 % dans les 1–2 premières heures) afin d’éviter une hypoperfusion brutale, puis atteindre une PAS < 160 mmHg en 24–48 h.
1. Options thérapeutiques en urgence
La voie intraveineuse est théoriquement à privilégier, mais l’accès à certaines molécules reste limité, notamment en France.
- Fenoldopam IV : vasodilatateur artériel rénal favorisant la natriurèse. Peu documenté en médecine vétérinaire ;
- Hydralazine : vasodilatateur artériel efficace, mais au dosage délicat ; risque d’hypotension brutale ;
- Nitroprussiate de sodium IV : vasodilatateur puissant, utilisable en perfusion continue. Rarement disponible en pratique courante, réservé aux soins intensifs spécialisés ;
- Labetalol / Esmolol IV : bêtabloquants indiqués dans certaines situations spécifiques (ex. phéochromocytome avec tachycardie).
En pratique, lorsque l’accès aux molécules IV est limité, l’amlodipine par voie orale reste l’option la plus utilisée. Elle peut être administrée directement per os si l’animal est en mesure de déglutir, ou via une sonde nasogastrique si nécessaire.
2. Soins de support
- contrôle de la douleur et du stress (qui aggravent l’HTA) ;
- gestion de la pathologie sous-jacente ;
- surveillance neurologique, ophtalmologique et cardiorespiratoire rapprochée.
VII. Prise en charge hors urgence
Dans les situations où la PAS se situe entre 140 et 179 mmHg, sans manifestation clinique aiguë, on parle d’hypertension chronique ou modérée. Ces cas ne nécessitent pas d’hospitalisation immédiate mais doivent faire l’objet d’une prise en charge progressive et ambulatoire.
Les objectifs thérapeutiques sont de réduire la PAS en dessous de 160 mmHg (et idéalement < 150 mmHg en présence d’atteintes d’organes cibles), de prévenir l’apparition de nouvelles lésions irréversibles, d'adapter la stratégie thérapeutique à l’espèce, à l’état clinique et aux éventuelles comorbidités (maladie rénale chronique, hyperthyroïdie, diabète, etc.).
Options thérapeutiques (Tableau 2)
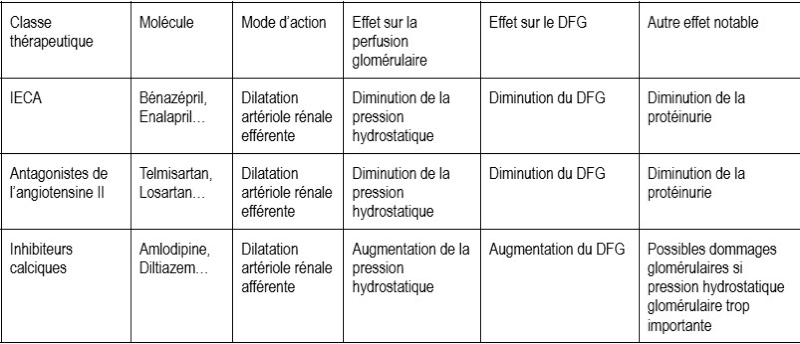
Tableau 2
Chez le chat :
- amlodipine : molécule de référence, très efficace et bien tolérée ;
- inhibiteurs de l’enzyme de conversion de l’angiotensine - IECA (bénazépril, énalapril) : indiqués principalement en cas de protéinurie, souvent utilisés en association ;
- antagonistes de l’angiotensine II (telmisartan, losartan) : alternatives intéressantes, notamment en cas de protéinurie persistante.
Chez le chien :
- IECA : généralement utilisés en première intention, en particulier si une maladie rénale protéinurique est présente ;
- amlodipine : ajoutée si l’IECA seul ne permet pas de contrôler suffisamment la PAS, ou utilisée d’emblée en cas d’hypertension importante.
Associations fréquentes IECA + amlodipine lorsque la monothérapie est insuffisante.
Dans le cas d’un patient cardiorénal :
- dans le cas d’un patient cardiaque : l’utilisation d’inhibiteurs du système rénine-angiotensine-aldostérone (SRAA) peut être intéressante pour baisser la pression artérielle en plus d’aider le cœur lors d’insuffisance cardiaque congestive ;
- dans le cas d’un patient rénal : l’utilisation d’inhibiteurs du SRAA (telmisartan, bénazépril) peut au contraire être contre-indiquée. Un patient rénal étant déjà probablement déshydraté, hypoperfusé et avec potentiellement un appétit médiocre présente déjà un débit de filtration glomérulaire (DFG) réduit. Ainsi, l’utilisation d’un SRAA, entraînant la vasodilatation de l’artériole rénale efférente réduirait encore plus le DFG et pourrait induire une crise d’insuffisance rénale aiguë. L’utilisation d’amlodipine est préférable chez les patients rénaux avancés ;
- dans le cas de patients cardiorénaux : le pour et le contre doivent être discutés au cas par cas entre les services de soins intensifs, de cardiologie et de médecine interne/néphrologie pour la gestion de ces patients à l’équilibre précaire. L’utilisation d’inhibiteurs du SRAA est en général évitée et l’amlodipine privilégiée, sauf si l'état cardiaque le justifie.
VIII. Suivi et ajustements
- Contrôles tensionnels réguliers : toutes les 1 à 2 semaines lors de l’instauration du traitement, puis tous les 1 à 3 mois après stabilisation ;
- Surveillance biologique : évaluation de la créatinine, de l’urée, de la protéinurie +/- du SDMA ;
- Suivi clinique : observation des signes d’hypotension éventuelle (léthargie, faiblesse, syncopes) et évaluation des atteintes d’organes cibles.
Le traitement doit être ajusté progressivement, en privilégiant les associations lorsque la monothérapie ne permet pas d’atteindre les objectifs.
IX. En conclusion
L’hypertension artérielle chez le chien et le chat peut entraîner des lésions graves et irréversibles des organes cibles. La détection précoce et la prise en charge adaptée sont essentielles. Les urgences hypertensives nécessitent une réduction progressive de la pression artérielle sous surveillance rapprochée, tandis que l’hypertension chronique peut être traitée de façon ambulatoire avec un suivi régulier. La prévention des complications repose sur le contrôle tensionnel, le traitement de la cause sous-jacente et une surveillance biologique adaptée. La gestion de patients cardiorénaux hypertensifs repose sur la gestion de l’hypertension artérielle systolique tout en conservant un équilibre entre les deux affections. Cette gestion se fait généralement au cas par cas et avec des discussions régulières avec les différents services concernés (soins intensifs, cardiologie, médecine interne/néphrologie).
Bibliographie
- ACIERNO MJ, BROWN S, et al. ACVIM consensus statement: Guidelines for the identification, evaluation, and management of systemic hypertension in dogs and cats. J Vet Intern Med. 2018;32:1803–1822.
- LEE Y, BAEK M, LEE D, PARK J, CHAE Y, KANG BT, YUN T, KIM H. Retrospective evaluation of risk factors for worsening renal function after angiotensin-converting enzyme inhibitor treatment in dogs. J Vet Intern Med. 2025 Jan-Feb;39(1):e17252.
- COLE LP, JEPSON R, DAWSON C, HUMM K. Hypertension, retinopathy, and acute kidney injury in dogs: A prospective study. J Vet Intern Med. 2020; 34: 1940–1947.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Traitement de non-unions du processus anconé par vissage autocompressif sans arthrotomie à l'aide de guides 3D spécifiques du patient
Bastien DEKERLE
Coauteurs : T. LARCHER, P. DE GAIL
Introduction
La non-union du processus anconé (NUPA) est un défaut de fusion de la partie proximale de l'incisure trochléaire à l'olécrane. La prise en charge chirurgicale vise à favoriser une fusion du processus anconé (PA).
Anamnèse
Deux chiens Bergers Allemands mâles issus de la même portée sont présentés respectivement à 25 et 27 semaines ; le premier pour une boiterie de l'antérieur droit évoluant depuis 1 mois et le second pour un dépistage de dysplasie des coudes.
Examen clinique
L'examen orthopédique du premier chien confirme la présence d'une boiterie de degré 2 (discrète permanente avec appui) du membre thoracique droit. La palpation révèle un coude droit volumineux avec empâtement des récessus synoviaux. La mobilisation de l'articulation témoigne d'une gêne en flexion et extension forcées et un test de Campbell positif. Du côté gauche, ce même test est douteux.
Le second chien présente comme seule anomalie à l'examen orthopédique un test de Campbell douteux bilatéralement.
Démarche diagnostique
Les hypothèses formulées à ce stade sont une dysplasie du coude ou moins probablement une fissure/fracture articulaire. Un examen tomodensitométrique confirme la première hypothèse chez les deux chiens par la mise en évidence d'une NUPA bilatérale et d'une incongruence articulaire modérée. Les processus coronoïdes sont intègres.
Traitement
Les deux chiens ont été traités similairement avec quelques jours d'écart entre les interventions de chaque coude. Premièrement, une arthroscopie « à l'aiguille » du coude par abord médial est réalisée. Elle confirme l'intégrité du processus coronoïde médial tandis que la NUPA est clairement visible et relativement stable à la palpation.
Un abord caudal de l'olécrane droit est ensuite réalisé et permet l'adaptation d'un guide 3D spécifique du patient (image 1).

Image 1 : guide 3D élaboré pour le positionnement de 3 broches de position (cylindres bleus) et d'un point de forage jusqu'au processus anconé (cylindre vert)
Celui-ci est maintenu par deux broches monocorticales de position et permet le forage du PA depuis l'olécrane caudal sous contrôle fluoroscopique sans arthrotomie. Une vis canulée autocompressive sans tête en titane est ensuite insérée jusqu'à la surface articulaire permettant une mise en compression de la NUPA. En fin d'intervention, une ostéotomie bi-oblique ulnaire proximale est réalisée et le positionnement des implants ensuite vérifié par radiographies orthogonales (image 2).
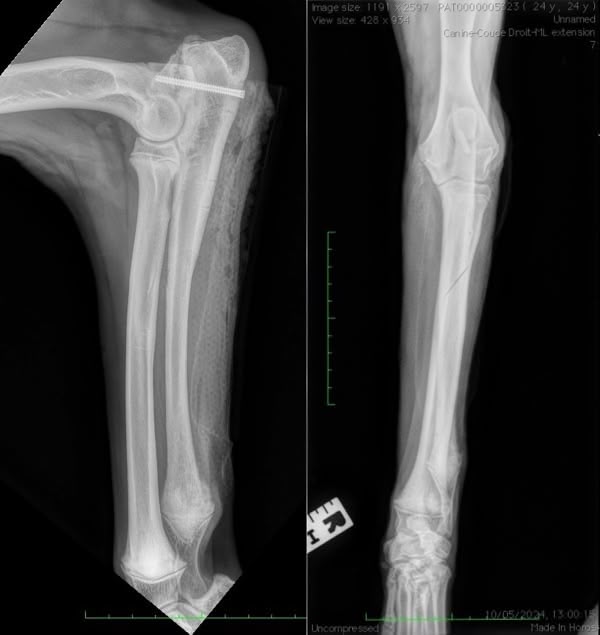
Image 2 : radiographies postopératoires orthogonales confirmant le bon positionnement de la vis ainsi que la coupe osseuse de l'ostéotomie bi-oblique.
Au contrôle à 1 mois, aucune boiterie n'est constatée et les fusions osseuses sont bien avancées en regard du PA. À 3 mois, les quatre NUPA sont totalement fusionnées et les ostéotomies bi-obliques montrent les derniers remaniements de leurs cals osseux.
Discussion
La NUPA fait partie de la dysplasie du coude au même titre que la fragmentation du processus coronoïde médial, l'ostéochondrite disséquante et l'incongruence articulaire [1]. Chez les grandes races de chien, le PA est issu d'un centre d'ossification secondaire qui fusionne avec le reste de l'olécrane après 14 semaines. Physiologiquement chez le chien, le PA est le stabilisateur primaire du coude en pronation et le stabilisateur secondaire en supination. Il semble donc essentiel de le préserver autant que possible.
Les techniques chirurgicales visant à favoriser la fusion du PA doivent être réalisées autour de l'âge de 6 mois pour maximiser leurs chances de réussite. Parmi les techniques décrites, le vissage du processus anconé permet d'obtenir une fusion jusque dans 60 % des animaux tandis que l'ostéotomie ou ostectomie ulnaire permet une fusion des processus anconés dans 70 % des cas chez des animaux de moins de 7 mois dont le processus anconé est peu déplacé [2, 3]. La combinaison de ces deux techniques assure un taux de fusion de 90 % et semble donc être la technique de choix de nos jours. Dans notre cas, l'association d'un vissage compressif et d'une ostéotomie proximale bi-oblique ulnaire a permis une fusion des quatre PA sans complication et ce malgré l'âge légèrement avancé de nos chiens (> 6 mois).
L'utilisation des guides 3D est en plein essor chez les animaux de compagnie [4]. L'intérêt majeur de cette technologie pour les NUPA est d'augmenter la précision de visée d'un relief anatomique intra-articulaire : le risque de malposition de l'implant est réduit, diminuant le risque de fracture de l'anconé et/ou le développement d'arthrose. L'objectif ultime étant aussi d'éviter un abord articulaire : la morbidité s'en voit diminuée et le temps opératoire est réduit.
Conclusion
Ces cas permettent de décrire la prise en charge chirurgicale minimalement invasive de non-union bilatérale des processus anconés. Le traitement chirurgical alliant vissage en compression après utilisation d'un guide 3D spécifique du patient et ostéotomie bi-oblique semble à ce jour le plus prometteur en termes de cicatrisation de l'anconé, particulièrement s'il est réalisé avant 7 mois.
Bibliographie
- MEYER-LINDENBERG. J Small Anim Pract. 2006;47(2):61-5.
- TROSTEL. Compend Contin Educ Pract Vet. 2003;25(10):754-62.
- NESS. J Small Anim Pract. 1998;39(1):15-8.
- ALTWAL. Vet Surg. 2022;51(1):34-51.
Liens d'intérêt : Création et gestion de l'entreprise d'impression 3D3K.
📃 Traitement des luxations de rotule : du traitement conservateur à la prothèse de trochlée.
Montréal, Canada
I. Introduction
Chez le chien, le traitement conservateur de la luxation de rotule (LR) se limite aux cas non ou peu symptomatiques, souvent de grade I, ou lorsque la chirurgie est contre-indiquée (comorbidités graves, risque anesthésique élevé). Il repose sur une gestion pondérale stricte pour réduire les forces luxantes. Le renforcement musculaire cible notamment le quadriceps avec des exercices en côte douce, assis-debout contrôlés, marche aquatique pour améliorer la stabilité active du grasset. La physiothérapie inclut mobilisation douce, proprioception sur plateaux instables, cavalettis. L’adaptation de l’activité évite les sauts, les virages brusques et les surfaces glissantes.
Éléments clés de décision pré-opératoire : la luxation de rotule est le plus souvent médiale et développementale. La gravité (grades I-IV), la présence de déformations osseuses (varus distal fémoral, torsion tibiale, dysplasie de la trochlée), l’alignement de l’appareil extenseur et les comorbidités (par exemple rupture du LCCr) guident la stratégie. Un examen orthopédique complet et l’imagerie (radiographies de l’axe mécanique, éventuellement scanner pour torsion/antéversion) orientent la combinaison d’actes. La plupart des chiens requièrent la combinaison de techniques de tissus mous et osseuses. Le pronostic est globalement favorable avec retour à une fonction satisfaisante pour la majorité des patients, mais le risque de complications et de re-luxation augmente avec le grade et le gabarit.
II. Arsenal chirurgical classique
1. Tissus mous
La libération, aussi appelée désmotomie médiale pour la luxation médiale (appelée aussi désmotomie latérale pour la luxation latérale), et l’imbrication capsulo-fasciale opposée sont généralement réalisées durant la procédure chirurgicale, mais l’excès de libération tissulaire expose à une re-luxation.
2. Tissus osseux
- Chondroplastie trochléaire réservée aux chiots avec cartilage épais. Récession en coin (wedge), en bloc ou semi-cylindrique, standards actuels, préservent le cartilage et augmentent la hauteur des lèvres trochléaires pour le guidage patellaire. Le choix dépend des habitudes et de la morphologie, sans impact clair sur le taux de complications.
- Transposition de la tubérosité tibiale : c’est le levier principal de réalignement, la translation latérale pour la luxation médiale recentre l’insertion du tendon patellaire. Fixations : broches de Kirschner (2 ou 3), hauban en 8, fils métalliques parfois, vis corticales, ou montage plaque-pin verrouillé plus récent visant à réduire la migration/avulsion, notamment chez les chiens actifs ou de moyen-grand format. Garder une attache distale permet de limiter le risque d’avulsion de la crête tibiale.
- Ostéotomie fémorale distale (DFO) souvent fermeture latérale en cas de varus métraphysaire-diaphysaire. Elle diminue la force luxante médiale et abaisse les récidives dans les formes graves et/ou grands chiens. Consolidation et amélioration fonctionnelle à long terme sont rapportées lorsque la DFO est combinée aux gestes standards. Fixation par plaques souvent verrouillées et vis ou clou verrouillé.
- Ostéotomies tibiales envisagées si torsion tibiale majeure ou valgus/varus proximaux contribuent. Ces cas sont moins fréquents que le varus fémoral.
3. Implants et considérations techniques
- Transposition de la crête tibiale. Implants : broches hauban standard, prouvé, économique, mais migration des broches/irritation sont des sources de complications mineures. Vis corticales procurent une bonne compression, profil plus bas, plus rarement utilisées. Construct plate-pin verrouillé, pensée pour limiter l’avulsion, technique encore émergente. DFO plaques verrouillées LCP : choix de plaque anatomique ou DFO-specific selon la géométrie de l’ostéotomie et la taille ; l’objectif est une correction planifiée (CT-scan et impression 3D de guide de coupe voire d’implants si nécessaire), une stabilité suffisante pour la consolidation et la reprise fonctionnelle.
- Trochléoplasties instrumentation : scie oscillante droite, maillet, ostéotome, scie cylindrique. La protection du cartilage pendant la manipulation est cruciale pour limiter l’arthrose secondaire.
4. Prothèses trochléaires et implants d’augmentation de crête
Prothèse de crête trochléaire (Trochlear Ridge Prosthesis, TRP) : des implants sur-mesure ou standardisés augmentent la hauteur des crêtes sans résection du cartilage. Indications : trochlée peu profonde/érosion, ou reprise après échec/corrosion post-sulcoplastie. Points d’attention : planification précise, profil de l’implant pour éviter le conflit des tissus mous, stabilité des vis.
Remplacement de la trochlée patellaire (Patellar Groove Replacement, PGR) : le remplacement complet de la trochlée par une prothèse est une option pour les lésions trochléaires graves, érosion/ostéophytes tendus, défauts segmentaires, trochlée en dôme, reprises complexes. Études cliniques et rapports de cas décrivent de bons résultats fonctionnels si la taille est adéquate et l’essai peropératoire rigoureux ; un surdimensionnement peut causer un conflit des tissus mous.
V. Résultats, complications et facteurs de risque
Les études récentes confirment l’amélioration clinique/biomécanique après chirurgie, analyse de posture/charges et des taux élevés de retour à une fonction acceptable. Néanmoins, les complications ne sont pas rares, globalement 13-25% selon les populations, avec re-luxation 8-21%, augmentées chez les grands chiens et les hauts grades. Les complications d’implant (migration de broches, avulsion) sont parmi les plus fréquentes.
Des variables opératoires influencent le risque : libération médiale excessive, re-luxation, préservation de l’attache corticale distale lors du traitement, complications d’implant. Les formes avec varus distal fémoral tirent avantage d’une DFO associée. En grade IV, les taux de complications sont logiquement supérieurs, mais des séries dédiées montrent des issues globalement positives si la correction osseuse est assurée.
VI. Traitement de la luxation de rotule et rupture du ligament croisé crânial
La coexistence est fréquente. La stratégie combine la stabilisation du grasset (ex. plaque TPLO spécifique pour luxation médiale de rotule) avec un step au réalignement patellaire, en évitant les interférences entre implants et en respectant l’axe de charge.
Bibliographie
- JOHNSTON SA, TOBIAS KM eds. Veterinary Surgery Small Animal. 2e d. Elsevier, St. Louis, 2018. Chapitre Stifle Joint Patellar luxation surgical management, trochleoplasty, tibial tuberosity transposition, corrective osteotomies.
- ROSSANESE M, WITTE PG, KOWALESKI MP, et al. Risk factors associated with reluxation after surgical correction of medial patellar luxation in dogs. Veterinary and Comparative Orthopaedics and Traumatology. 2019 32 293-99.
- NICETTO T, PETAZZONI M, ROVESTI GL, et al. Trochlear ridge prosthesis for the management of canine patellar luxation: multicentre clinical evaluation. Veterinary and Comparative Orthopaedics and Traumatology. 2023 36 379-387.
- DOKI? Z, BOCKSTAHLER B, LORINSON D. Patellar groove replacement in the dog a clinical report. Veterinary and Comparative Orthopaedics and Traumatology. 2015 28 193-198.
- DIGIOVANNI LC, KAPATKIN AS, GRIFFIN DJ, et al. Evaluation of limb loading and posture after surgical correction of medial patellar luxation in dogs. American Journal of Veterinary Research. 2023 84 21-10.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Traitons la PIF
Gentilly, France
I. Introduction
La péritonite infectieuse féline, ou PIF, est une maladie que nous avons tous connue comme létale pour les chats atteints. Sous sa forme dite humide ou sèche, le pronostic était généralement sombre, après une évolution de quelques jours à quelques semaines. Les derniers mois écoulés ont représenté un tournant dans la prise en charge de cette maladie. Les objectifs de ce module sont de faire un point sur cette avancée thérapeutique, de présenter le principal protocole utilisé et les points clés pour le suivi thérapeutique de cette affection.
II. Péritonite infectieuse féline : l’errance thérapeutique puis l’émergence de la classe des anti-viraux
Pendant plusieurs décennies, la péritonite infectieuse féline (PIF) est demeurée une affection à issue fatale. Les options thérapeutiques se limitaient aux soins de soutien, visant à améliorer temporairement le confort des animaux atteints, sans malheureusement influer sur la progression de la maladie. De nombreux essais médicamenteux ont été réalisés avec des molécules aussi diverses que l’itraconazole, la ribavirine, la chloroquine, la méfloquine, les corticoïdes ou encore la pentoxifylline. Bien que certaines aient présenté des mécanismes d’action théoriquement intéressants, aucune n’a permis d’obtenir une survie prolongée ni une véritable rémission clinique, le plus souvent en raison d’une toxicité importante ou d’une inefficacité antivirale réelle. Ainsi, jusqu’à la fin des années 2010, la PIF était invariablement associée à un pronostic sombre.
La compréhension plus fine des mécanismes de réplication du coronavirus félin a progressivement ouvert la voie au développement d’approches antivirales ciblées. La classe des antiviraux, développés dès 1963 en médecine humaine et ayant connu une poussée de développement dans les années 1990 avec l’étude du virus du SIDA/HIV, ont naturellement été considérées. Le remdesivir, prodrogue administrée par voie injectable, initialement développée contre l’hépatite C et le virus Ebola, a montré une activité antivirale sur les coronavirus. Toutefois, sa pharmacocinétique chez le chat, marquée par une demi-vie très courte (1 à 1h30), en limitait considérablement l’utilisation. Par ailleurs, le remdesivir reste non accessible aux vétérinaires, et réservé à la prescription hospitalière.
En revanche, son métabolite actif, le GS-441524, analogue nucléosidique de l’adénosine, s’est rapidement imposé comme un candidat thérapeutique majeur. Son mode d’action repose sur l’inhibition de l’ARN polymérase virale, empêchant la réplication du génome viral. Ses caractéristiques pharmacologiques, notamment une demi-vie prolongée d’environ 24 heures et une bonne tolérance in vivo, en ont fait une molécule adaptée au traitement de la PIF.
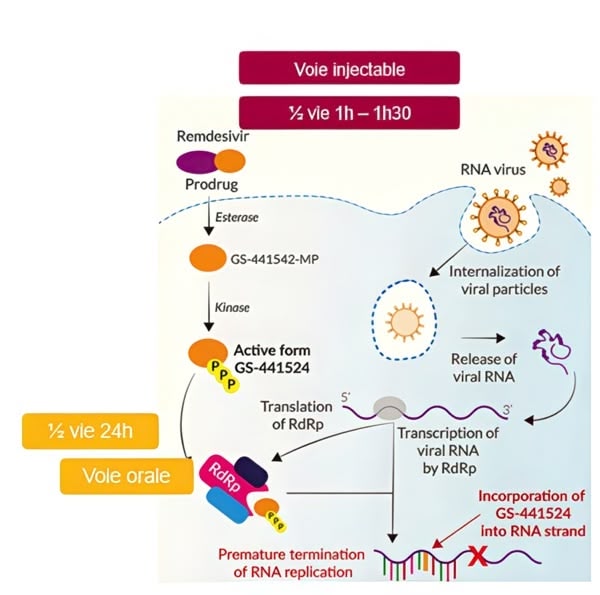
Figure 1 : Schéma action anti-viral
Les premières études cliniques menées à la fin des années 2010 ont utilisé le GS-441524 par voie injectable, avec un protocole standardisé à 4 mg/kg/jour pendant 12 semaines minimum, chez des chats atteints de PIF non oculaire et non neurologique. Les résultats, bien que reposant sur des cohortes limitées et sans groupe contrôle, ont été spectaculaires : de nombreux animaux jusque-là condamnés ont survécu plusieurs mois au cours du suivi (jusqu’à 44 semaines), avec une guérison clinique complète (Pedersen et coll., 2019). Ces travaux ont marqué une rupture nette dans la perception de la maladie, démontrant pour la première fois qu’un traitement efficace était possible.
Face à l’absence d’autorisation de mise sur le marché, le GS-441524 a rapidement circulé sur un marché parallèle. Cette période dite du « marché noir » a permis à de nombreux propriétaires désespérés d’accéder au traitement, avec une supervision plus ou moins encadrée. Cependant, la qualité incertaine des préparations, l’absence de suivi médical structuré et le risque d’apparition de résistances virales posaient de sérieux problèmes éthiques et sanitaires. Des effets secondaires récurrents de douleur sur le site d’infection, plaie ou abcès ont ainsi été rapportés (Jones et coll, 2020).
Depuis 2022, la situation a évolué vers un encadrement légal en France. Les vétérinaires ont désormais la possibilité de prescrire le GS-441524 sous forme de préparation magistrale, réalisée par des pharmacies sous-traitantes dans le respect des Bonnes Pratiques de Préparation Extemporanée (arrêté du 9 juin 2004). Cette évolution réglementaire constitue un progrès majeur, garantissant à la fois la qualité pharmaceutique du produit et la sécurité de son utilisation, tout en plaçant la prescription dans un cadre de pharmacovigilance obligatoire. Toutefois, des règles strictes encadrent ce dispositif : prescription individuelle et uniquement après certitude diagnostique, interdiction du stockage à la clinique, et proscription de toute utilisation prophylactique.
III. Le GS-441524, l'antiviral qui a tout changé
Actuellement, la molécule est approvisionnée par des fabricants internationaux (par exemple, laboratoire BOVA). Il est ensuite reconditionné par des préparatoires accrédités (par exemple, France Prep, pharmacie Delpech,…). Différentes formulations sont disponibles (notamment, suspension buvable, pâte orale dans style gradué).
Le protocole standard est un traitement continu de 84 jours minimum, soit 12 semaines. Il est administré par voie orale sous forme orale. La dose de départ est de 15 mg/kg une fois par jour pour les formes humides et sèches non neurologiques/oculaires. Pour les formes neurologiques et oculaires, une dose de 10 mg/kg deux fois par jour est recommandée, la diffusion de la molécule étant limitée par les barrières hémato-méningée et hémato-oculaire. L’absorption digestive peut être variable, le traitement doit être donné à heure fixe. Il est crucial de peser régulièrement le chat pour ajuster la dose, car une dose inadaptée est la principale cause d'échec thérapeutique.
L’accompagnement médical du chat atteint doit inclure d’autres composantes :
- fluidothérapie,
- gestion de la douleur des lésions si indiqué (uvéite, …),
- traitement des épanchements,
- stimulation de l’appétit et mise en place de protocole de réalimentation,
- traitement antiépileptique si crises convulsives,
- traitement des complications à médiation immune, …
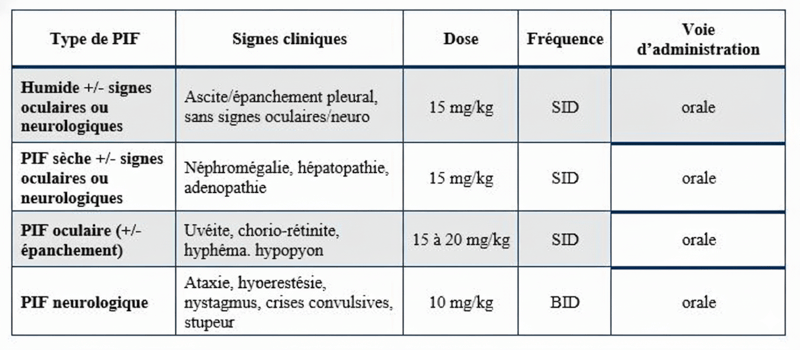
Tableau 1 : résumé indicatif des principaux protocoles utilisés
L’évolution clinique sous traitement est en général rapide. Une amélioration de l’état général, de l’appétit et de la température corporelle est observée dès les 7 à 15 premiers jours.
Le taux de succès du GS-441524 est estimé à environ 85 %. Les rechutes, rares (moins de 10 %), surviennent principalement dans les semaines suivant l’arrêt du protocole et nécessitent le plus souvent une reprise du traitement à une dose plus élevée.
Les facteurs de mauvais pronostic identifiés incluent les formes neurologiques, les atteintes oculaires et l’âge avancé des patients (supérieur à 7 ans). Les effets indésirables restent peu fréquents et généralement modérés : élévation transitoire des enzymes hépatiques, anomalies hématologiques mineures, cas isolés, d’insuffisance rénale ou de lithiases urinaires chez de jeunes chats. Les formes injectables, aujourd’hui obsolètes, étaient par ailleurs associées à des réactions locales douloureuses.
IV. Le puzzle du suivi clinique
Le suivi est la clé du succès. Les anomalies biologiques (hématocrite, albumine, rapport albumine/globulines, bilirubine) se normalisent progressivement en quelques semaines. Le suivi recommandé comprend une évaluation téléphonique 48 heures après l’instauration du traitement, puis des contrôles cliniques et biologiques à 15 jours, 4 à 6 semaines et à la fin de la cure, suivis d’un bilan un mois après l’arrêt du traitement.
La reprise de poids, la normalisation de la température et la disparition de l'épanchement sont des signes encourageants. La normalisation des paramètres sanguins, en particulier l'augmentation de l'albumine et la diminution des globulines, est attendue.
V. Que faire en cas de rechute ?
Une rechute, clinique et généralement biologique, est caractérisée par une réapparition des signes cliniques après l'arrêt du traitement. Elle peut être dépistée par une variation des marqueurs inflammatoires (AGP, SAA) ou une dégradation de l’hémogramme, la réapparition d’une hyperglobulinémie.
Il est alors recommandé de reprendre le protocole de traitement pour 84 jours, et de considérer une augmentation de la posologie du traitement. Il est néanmoins conseillé de ne pas dépasser la dose de 20 mg/kg/j.
VI. Conclusion et perspectives
La PIF est désormais traitable, mais le diagnostic précoce est un prérequis absolu. La prise en charge est longue et coûteuse, ce qui nécessite une communication transparente et un engagement total du propriétaire. Les taux de réponse sont estimés à environ 85 %, et les rechutes sont rares, survenant le plus souvent dans les semaines qui suivent l'arrêt du traitement, ou pour les formes oculaires ou neurologiques.
La recherche sur cette affection et son traitement continue. Les points d’intérêt sont l’étude de protocoles plus courts (Zuzzi-Krebitz et col, 2024), avec des doses parfois plus faibles, mais aussi l’impact de la généralisation du traitement sur l’apparition de résistance aux anti-viraux. C’est pourquoi il est impératif d'utiliser les traitements de manière raisonnée et sous un suivi vétérinaire strict.
Bibliographie
- PERDERSEN NC et coll. Efficacy and safety of the nucleoside analop GS-441524 for treatment of cats with naturally occurring feline infectious peritonitis. J Feline Med Surg 2019; 21(4): 271-281
- JONES S et coll. Unlicensed GS-441524-like antiviral therapy can be effective for at-home treatment of feline infectious peritonitis. Animal 2021, 11, 2257
- ZUZZI-KREBITZ AM et coll. Short treatment of 42 days with oral GS-441524 results in equal efficacy as the recommended 84-day treatment in cats suffering from FIP with effusion – a prospective randomized controlled study. Viruses 2024; 16(7): 1144
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Transmissibilité des affections orthopédiques : état des lieux des connaissances
Isturits, France
I. Introduction
La transmissibilité génétique désigne la part du risque d’une affection attribuable aux gènes d’un animal, par opposition aux facteurs acquis traumatismes, nutrition, croissance, activité, etc. En orthopédie, beaucoup de maladies ne sont pas purement génétiques ou purement environnementales, elles résultent d’une prédisposition héréditaire sur laquelle l’environnement agit. Deux grands types d'affections existent :
- les affections monogéniques, dites affections mendéliennes simples ; une variation identifiée sur un gène suffit à déclencher la maladie, par exemple l'ostochondrodysplasie du Scottish Fold liée au gène TRPV4 ;
- les affections polygéniques complexes : plusieurs zones du génome, chacune avec un effet faible, s’additionnent. Ici, il n’existe pas de gène unique décisif, on parle de risque plus élevé ou plus faible, modulé par le poids, la vitesse de croissance, l’exercice, la conformation, etc.
II. Définitions et principe généraux
Il est important de différencier deux notions : l’héritabilité et l’hérit. L’hérit fait référence au processus biologique par lequel les traits ou les caractéristiques sont transmis des parents à leur descendance à travers le matériel génétique ADN. Il s’agit d’un concept qualitatif. Un trait est dit hérité s’il est influencé par des facteurs génétiques et transmis à travers les générations. La présence d’une prédisposition génétique ou d’un risque familial indique une influence héréditaire. En résumé, l’hérit décrit le fait que les gènes contribuent à la manifestation d’un trait et qu’ils peuvent être passés à la génération suivante.
L'héritabilité, souvent notée h, est une mesure statistique quantitative. Elle quantifie l’étendue de l’influence génétique par rapport à la variation totale du trait au sein d’une population donnée. Elle est exprimée comme un rapport entre 0 et 1 ou 0 et 100. Un h de 1,0 signifie que le trait est entièrement déterminé par la génétique : toute la variation observée est due aux différences génétiques, tandis qu’un h de 0,0 signifie qu’il n’est pas du tout influencé par la génétique : toute la variation est due à l’environnement ou à d’autres facteurs non génétiques. L’héritabilité est spécifique à la population, à l’environnement et au moment de l’estimation. Cela signifie qu’une estimation d’héritabilité pour une race de chiens peut différer dans un environnement différent. Cela implique qu’une héritabilité élevée indique que la sélection de parents avec un phénotype souhaitable peut entraîner un progrès génétique rapide pour ce trait.
La différence fondamentale entre hérit et héritabilité réside dans ce que chaque terme décrit. L’hérit est le phénomène de la transmission génétique. L’héritabilité est la mesure statistique de l’ampleur de cette influence génétique sur la variation d’un trait au sein d’une population donnée. Dans la pratique quotidienne, le vétérinaire est responsable de l’identification de données phénotypiques qui permettront d’en tirer des données génétiques par le biais d’examens complémentaires, radiographies dans le cadre de la dysplasie de la hanche par exemple. La qualité de l’examen est primordiale pour pouvoir avoir une évaluation précise et rigoureuse du phénotype : âge d’évaluation, positionnement radiographique, sédation, formation du lecteur, lecture centralisée. Des examens non standardisés introduisent du bruit et rendent toute sélection moins efficace.
III. Méthodes d’évaluation génétique
1) Phénotypage clinique standardisé
C’est le socle. Pour la hanche, système OFA radiographies standards sous anesthésie basse sur radiographies normalisées, avec classes ou scores. Le PennHIP fournit un indice quantitatif de laxité mesurable précocement. Plus l’indice est élevé, plus le risque ultérieur d’arthrose est important. Pour le coude, grilles ordinales qui combinent lésions primaires et signes d’arthrose. En pratique, on vise un âge minimal respecté, positionnement rigoureux, sédation appropriée, matériel calibré, lecteur formé ou centre de lecture. Cela réduit les faux positifs/négatifs et améliore la valeur des données pour la sélection.
2) Données familiales et lignées
Avant tout test sophistiqué, l’examen des apparentés est très informatif : frères/sœurs, parents, descendance. Une affection qui revient dans une lignée suggère une composante génétique. Documenter proprement ces informations : comptes-rendus, copies des lectures officielles, résultats d’examens sont précieux pour le conseil aux éleveurs.
3) Tests génétiques ciblés
Ces tests sont indiqués lorsque l’affection est monogénique ou lorsqu’une mutation majeure est connue. Exemple : TRPV4 Scottish Fold. Ils paraissent très séduisants et faciles d’interprétation. Il est cependant nécessaire d’expliquer clairement au propriétaire/éleveur qu'un test positif dans une maladie mendélienne dominante peut suffire à déconseiller la reproduction. Pour les affections complexes, un panel ADN négatif ne garantit pas l’absence de risque, il ne teste que certains marqueurs connus, pas tous les gènes de la hanche par exemple.
4) Génomique et sélection précoce gEBV
La sélection génomique combine des milliers de marqueurs répartis sur le génome avec les données phénotypiques et familiales pour affiner les prédictions gEBV... L’intérêt majeur d’une telle approche est de disposer d’une prédiction très précise chez les jeunes avant l’âge des clichés définitifs, ce qui accélère l’amélioration des lignées.
IV. Revue des principales affections orthopédiques à composante génétique
1. Chez le chien
a) Dysplasie coxo-fémorale
La dysplasie de la hanche est le prototype des maladies orthopédiques polygéniques. Elle se caractérise par une laxité articulaire précoce, responsable d’un développement arthrosique. Chez le chien, l’héritabilité varie généralement de 0,11 à 0,68, avec des rapports spécifiques de 0,2 à 0,6. Des facteurs aggravants tels qu’un poids trop important, une croissance trop rapide, des exercices inadaptés ont été identifiés. Le dépistage se fait par le biais de radiographies standardisées et/ou suivant la mesure de l’index de distraction méthode PennHIP, Vezzoni, réalisée dès 16 semaines. La prévalence a diminué dans certaines races grâce aux campagnes de dépistage, mais reste élevée. La qualité du cliché, la rigueur de la lecture et la prise en compte des valeurs d’élevage EBV sont déterminantes.
b) Dysplasie du coude
La dysplasie du coude regroupe plusieurs lésions du développement : fragmentation du processus coronoïde médial FPCM, non-union du processus ancon NUPA, ostéochondrite disséquante OCD du condyle huméral, incongruence articulaire. C’est une affection polygénique, héritabilité faible à modérée. Chez le chien, l’héritabilité varie de 0,01 à 0,36 selon la race. Le dépistage se fait sur la base de radiographies à partir de 12 mois. L’utilisation d’un examen tomodensitométrique permet une détection plus fine. Les progrès de diminution de la prévalence par la sélection sont plus lents que pour la hanche, car la maladie est multifactorielle et parfois difficile à diagnostiquer avec précision.
c) Luxation médiale de la rotule
La luxation médiale de la rotule est l’une des anomalies orthopédiques les plus fréquentes, en particulier chez les races de petit format. La transmission de cette affection est multifactorielle. Des études d’héritabilité confirment un rôle génétique, mais ce dernier est encore mal caractérisé. L’héritabilité est estimée à 0,17 chez les Flat-Coated Retrievers. Une étude suédoise sur des Chihuahuas et des Bichons Frisés a montré une héritabilité de 0,42 et 0,57 respectivement. Le dépistage est basé sur la réalisation d’un examen clinique : palpation, mise en évidence de la luxation. Dans le cadre de la sélection des animaux reproducteurs, l’exclusion des animaux gravement atteints est la règle. Dans les grades légers, le choix dépend des recommandations du club de race.
d) Rupture du ligament croisé crânial
Longtemps attribuée uniquement au traumatisme, la rupture du ligament croisé crânial est maintenant reconnue comme une maladie à prédisposition génétique. L’héritabilité de l’affection reste modérée : 0,20 à 0,3. Certains facteurs phénotypiques sont soupçonnés : angle du plateau tibial, conformation du grasset, susceptibilité ligamentaire, étroitesse de la fosse intercondylienne. La rupture est bilatérale à moyen terme dans 40 à 50% des cas. Il n’existe pas de programme officiel de sélection, mais une récurrence familiale observée en consultation par exemple doit alerter et orienter les recommandations de reproduction.
e) Ostochondrose et ostéochondrite disséquante
L’ostéchondrose est un trouble de l’ossification endochondrale, aboutissant à des fissures et détachements cartilagineux. C’est une affection polygénique avec héritabilité faible à modérée 0,30 à 0,4. Une croissance rapide, une alimentation hypercalorique ou un excès d’apport calcique sont suspects comme pouvant être des facteurs aggravants, sans preuves aujourd’hui...
D’autres maladies, Maladie de Legg-Calvé-Perthes, instabilité atlanto-axoïdienne, chondrodysplasies et discopathies rétro-gènes FGF4 identifiés chez le Teckel, le Basset Hound, le Corgi ont une composante génétique fortement suspectée et sont à l’étude aujourd’hui.
2. Chez le chat
Les données sont moins abondantes que chez le chien, mais deux affections majeures sont bien documentées :
- dysplasie de la hanche présente une transmission polygénique probable ;
- ostéchondrodysplasie du Scottish Fold qui est une affection monogénique autosomique dominante. Les hétérozygotes développent des formes plus ou moins graves, les homozygotes sont systématiquement atteints et gravement handicapés.
L’ensemble des données convergent vers une conclusion claire : les affections orthopédiques les plus fréquentes chez le chien et le chat ont une base génétique significative, ce qui impose au praticien de les envisager comme telles dans son conseil aux éleveurs et aux propriétaires. Malgré tout, dans la littérature, de nombreuses limites sont identifiées : variabilité méthodologique selon les pays avec des protocoles de dépistage qui diffèrent, étude avec de faibles échantillons de population, standardisation manquante.
4. Implications pratiques pour le vétérinaire praticien
Le vétérinaire praticien est en première ligne pour la détection des affections orthopédiques héréditaires. Les consultations de primovaccination, le suivi de croissance sont des moments clés pour repérer les races prédisposées, interroger les propriétaires sur les antécédents familiaux et réaliser un examen orthopédique de base : palpation des hanches, mobilité du coude, évaluation des aplombs. Cela permet de proposer un dépistage radiographique adapté selon la race et de communiquer avec le propriétaire à propos du risque de développement de l’affection...
Il peut également avoir un rôle majeur dans le cadre de la sélection de futurs reproducteurs en déconseillant l’utilisation d’animaux gravement atteints mais pour les cas intermédiaires, en recommandant un partenaire de très bon profil.
5. Perspectives et recherche
- La génétique vétérinaire évolue rapidement
- Tests ADN : de nouveaux panels voient le jour, notamment pour les affections monogéniques.
- Sélection génomique déjà en place dans certaines espèces (bovin, ovin) ; elle commence à se développer dans l'espèce canine. Elle permettra d’estimer plus finement le risque chez un jeune animal avant même le dépistage radiographique.
- Internationalisation de la mise en commun des données à l’échelle mondiale : bases OFA, FCI, Kennel Clubs favorisent la précision des estimations et l’harmonisation des pratiques.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Trauma crânien : quand le coeur compense
Fort Collins, États-Unis
I. Résumé
Le traumatisme crânien (TC) déclenche une cascade d’effets systémiques dépassant le système nerveux central. Parmi les plus significatifs sur le plan clinique figure l’interaction cerveau–cœur, où une lésion neurologique aiguë entraîne des modifications cardiovasculaires profondes. Ce couplage neurocardiaque, largement médié par le système nerveux autonome et la libération massive de catécholamines, peut provoquer des arythmies, des lésions myocardiques et une instabilité hémodynamique. Bien que bien décrite en neuro-réanimation humaine, des données vétérinaires émergentes – issues à la fois de modèles expérimentaux et de cas cliniques – confirment que les chiens présentent des phénomènes similaires, avec des implications directes pour la prise en charge en urgence et soins intensifs.
II. Introduction
Le TC est une cause majeure de morbidité en médecine d’urgence et soins intensifs vétérinaires. Au-delà des conséquences intracrâniennes, des mécanismes de lésions secondaires affectent d’autres organes. Le myocarde est une cible fréquente mais souvent sous-reconnue. En médecine humaine, les concepts de myocarde étourdi neurogène (neurogenic stunned myocardium - NSM) et de réflexe de Cushing (hypertension artérielle et bradycardie due à une hypertension intracrânienne - HIC) sont des séquelles établies des lésions cérébrales aiguës. Des études expérimentales et cliniques chez le chien fournissent désormais des preuves d’une physiopathologie similaire, soulignant la nécessité d’une évaluation cardiovasculaire précoce et d’un soutien hémodynamique adapté.
III. Mécanismes de l’interaction cerveau–cœur
- Libération massive de catécholamines : activation de l’axe hypothalamo–hypophyso–surrénalien et du réseau autonome central, provoquant une libération importante de noradrénaline et d’adrénaline, induisant tachyarythmies, lésions myocardiques et vasoconstriction.
- Voies neuronales directes : l’augmentation expérimentale de la pression intracrânienne (PIC) chez le chien entraîne des anomalies ECG – raccourcissement de QT, inversion de l’onde T – même avec blocage sympathique, suggérant des voies non catécholaminergiques.
- Médiateurs inflammatoires : la libération de cytokines pourrait potentialiser la dépression myocardique, bien que les preuves vétérinaires soient limitées.
IV. Données vétérinaires
Les données vétérinaires sont relativement rares. Des modèles expérimentaux, notamment de Shih, montrent que l’élévation de la PIC chez le chien induit de la bradycardie, une hypertension artérielle et des anomalies ECG, compatibles avec le réflexe de Cushing et des altérations de la repolarisation. [1]
Une étude clinique chez des chiens épileptiques montre une variabilité de la fréquence cardiaque interictale prédisposant aux arythmies cardiaques. [2]
Une autre étude montre des élévations de troponine I cardiaque après des convulsions sans cardiopathie primaire, ce qui suggère une lésion myocardique d’origine neurogénique. [3]
Enfin, un cas clinique de NS a été décrit : un Boston Terrier en état de mal épileptique a développé une dyskinésie ventriculaire gauche, des arythmies et une élévation de troponine, résolues avec un traitement bêta-bloquant. [4]
4. Implications cliniques
L’implication clinique se retrouve au niveau de la surveillance : ECG précoce, télémétrie, dosage de troponine I et échocardiographie POCUS devraient être envisagés chez les patients canins atteints de TC ou ayant présenté des convulsions.
Au niveau de la prise en charge, le clinicien peut penser à traiter les tachyarythmies hémodynamiquement significatives (c.a.d associées à une baisse de pression artérielle ou à une hyperlactatémie) par bêta-bloquants lorsqu’elles sont liées à une hypercatécholaminémie. Il faut contrôler rapidement la PIC pour atténuer le cycle bradyarythmie/hypertension. Cela peut se faire à l’aide d’un traitement hyperosmotique avec un soluté hypertonique (NaCl 7,2-7,5 %) ou du mannitol. Le but est de soutenir la fonction myocardique tout en traitant l’insulte neurologique.
5. Conclusion
Les preuves vétérinaires confirment une connexion significative cerveau–cœur chez le chien, reflétant la neurocardiologie humaine. Reconnaître cette interaction dans le TC est essentiel pour optimiser le pronostic. Les recherches futures devraient explorer des stratégies cardioprotectrices ciblées en soins neurocritiques vétérinaires.
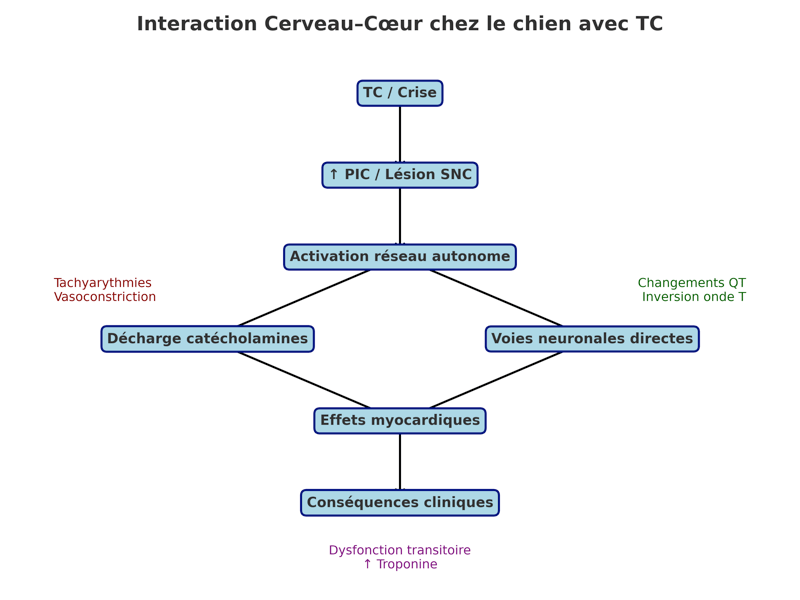
Figure 1. Schéma de l'interaction cerveau–cœur dans le trauma crânien chez le chien et le chat
Bibliographie
- SHIH AC, et coll. Cardiovascular effects of high intracranial pressure in dogs. Am J Vet Res. 2006;67(4):713–717.
- WESSMANN A, et coll. Interictal cardiac autonomic nervous system disturbances in dogs with idiopathic epilepsy. Vet J. 2017;220:44–49.
- EKENSTEDT KJ, et coll. Cardiac troponin I elevations after seizures in dogs: a potential marker for neurogenic myocardial injury. J Vet Intern Med. 2011;25(2):270–276.
- DUNHAM J, et coll. Naturally occurring neurogenic stunned myocardium in a dog secondary to status epilepticus. Front Vet Sci. 2024;11:1376107.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Un cas de colite ulcéreuse granulomateuse associée à la présence d'E. coli chez un chat
Guillaume DERRE
Introduction
La colite ulcéreuse granulomateuse est une affection inflammatoire rare chez les chats. Elle se caractérise par la formation d’ulcères et de granulomes dans le côlon. L’infection par Escherichia coli (E. coli) est une cause potentielle de cette maladie. Cet article présente un cas rare de colite ulcéreuse granulomateuse associée à la présence d’E. coli chez un chat.
Anamnèse
Un chat Birman de cinq ans a été présenté en consultation pour des symptômes de diarrhée chronique, depuis un an. Sa diarrhée est quotidienne, glaireuse et bouseuse avec parfois du sang frais. Une coproscopie a été réalisée par son vétérinaire traitant : flottation négative et recherche antigénique négative de Giardia et Cryptosporidies. Un bilan hémato-biochimique est dans les normes et le résultat du test FeLV/FIV est négatif. De la framycétine et de la sulfaguanidine (Felidiarix ND) ont été administrés sans effet. Du métronidazole a ensuite été donné sans succès.
Examen clinique
L’examen physique a révélé uniquement un inconfort abdominal modéré.
Démarche diagnostique
L’examen sonographique révèle un épaississement modéré de 3 mm de la paroi du côlon descendant sans perte d’échostructure. Une adénomégalie réactionnelle colique est visible. Le reste de l’examen est dans les normes. Une coloscopie montre la présence d’une inflammation marquée associée à une paroi colique très friable, ainsi que la présence d’ulcérations diffuses (Figure 1). Des biopsies ont été réalisées ainsi qu’une culture bactérienne des échantillons de biopsie. L’analyse anatomopathologique révèle une colite ulcéreuse pyogranulomateuse sévère avec atteinte de la sous-muqueuse par des granules PAS (periodic acid–Schiff) positifs au sein des cytoplasmes macrophagiques. Des bacilles sont visibles près de certains macrophages (Figure 2). La bactériologie sur des prélèvements isole un E. coli sensible à de nombreux antibiotiques mais résistant aux quinolones.
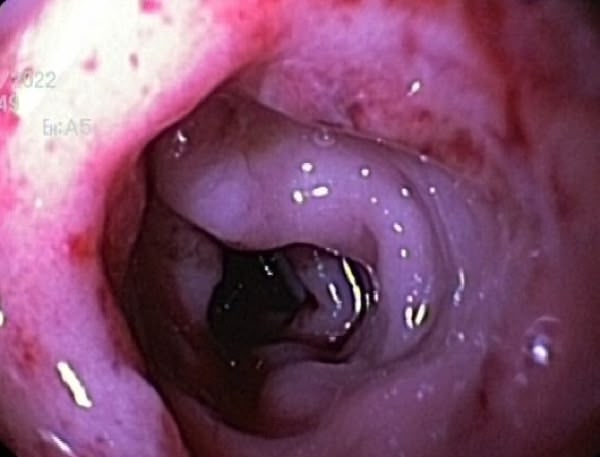
Figure 1
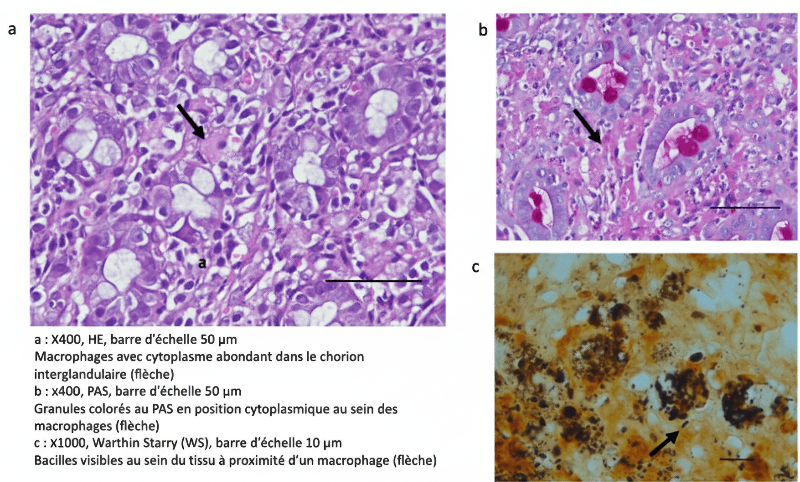
Figure 2
Traitement et suivi
Des quinolones (enrofloxacine) ont été administrées en attendant la culture bactérienne. Un régime alimentaire hyperdigestible (Id Hill’s) a été mis en place. Un problème d’observance au traitement sans amélioration de la diarrhée a conduit à considérer l’antibiogramme dès sa réception et injecter de la céfovecine deux fois à quinze jours d’intervalle. Le chat a vite repris du poids et le score fécal s’est normalisé. Après trois ans, le chat ne présente plus que de légers signes digestifs occasionnels.
Conclusion
La colite ulcéreuse granulomateuse (CG) reste rare chez le chat (deux cas décrits dans la littérature [1][2]). De nombreuses études ont démontré que la colite granulomateuse canine est étroitement liée à la présence de souches d’E. coli invasives dans la muqueuse colique. La coloration PAS permet de visualiser les macrophages chargés de glycoprotéines bactériennes dans les lésions de CG, renforçant l’implication bactérienne. La résistance d’E. coli à l’enrofloxacine est liée à des pronostics défavorables (échec thérapeutique, euthanasie), soulignant l’importance d’un antibiogramme préalable pour ajuster le traitement [3]. Les tentatives de traitement avec des antimicrobiens non ciblés ou des immunomodulateurs sont souvent inefficaces.
Bien que plus rare, la CG féline semble suivre un modèle similaire à celui observé chez le chien. Dans les deux cas de la littérature, la CG féline présentait une infiltration de macrophages PAS-positifs contenant E. coli, confirmée par immunohistochimie et culture bactérienne. Le traitement antibiotique ciblé a permis une amélioration spectaculaire, validant l’implication d’E. coli comme agent pathogène majeur. La fréquence élevée d’AIEC (Adhereht Invasive E. coli). chez les chats sains (82%) soulève des questions sur la potentielle pathogénicité latente des E. coli, qui s’activerait selon l’hôte, déterminisme génétique et/ou immunitaire [4].
Ce cas rare montre que E. coli pourrait jouer un rôle clé dans la CG féline, comme chez les chiens atteints de cette maladie. Le traitement antibiotique ciblé a démontré une efficacité significative, soulignant l’importance de considérer la CG dans les diagnostics différentiels de diarrhée chronique féline. Enfin, l’antibiorésistance peut affecter les résultats, d’où l’importance d’un antibiogramme.
Bibliographie
- Matsumoto I et al. Escherichia coli-induced granulomatous colitis in a cat. JFMS. 2019 Mar 14:51.
- Van Kruiningen HJ and Dobbins WO 3rd. Feline histiocytic colitis. A case report with electron microscopy. Vet Pathol 1979; 16:215-222.
- M. Craven et al. Antimicrobial Resistance Impacts Clinical Outcome of Granulomatous Colitis in Boxer Dogs. J Vet Intern Med 2010; 24:819-824.
- Martinez-Medina M et al. Adherent-invasive Escherichia coli phenotype displayed by intestinal pathogenic E. coli strains from cats, dogs, and swine. Appl Environ Microbiol 2011; 77:5813-5817.
Remerciements au laboratoire Vet-Histo Antech pour la collaboration.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Un cas de tremblement orthostatique « lent » chez un chat
Mathilde MORAND
Coauteurs : M. MORAND (
Introduction
Les tremblements orthostatiques sont des tremblements posturaux affectant généralement les membres pelviens en position debout dont la pathophysiologie n'est pas élucidée [2]. Ils sont surtout décrits chez les chiens de race géante avec une apparition des signes autour de 2 ans d'âge [1]. Le diagnostic repose sur des caractéristiques cliniques (signe de soustraction d'appui positif [2]) et sur un examen électromyographique (EMG) vigile révélant des décharges de haute fréquence (>13 Hz) [4]. En médecine humaine, le tremblement orthostatique dit « classique » décrit comme des tremblements posturaux à haute fréquence (entre 13 et 18 Hz) et s'oppose au « tremblement orthostatique lent », terme proposé pour décrire tous les tremblements orthostatiques de fréquence inférieure à 13 Hz [5]. Bien que les tremblements et leurs causes sous-jacentes aient été largement étudiés chez l'homme et le chien [3], leurs caractéristiques chez le chat restent mal connues. Par ailleurs, aucun cas de tremblements orthostatiques n'a encore été décrit chez cette espèce.
Anamnèse
Un chat européen mâle castré de 7 ans est référé en consultation de neurologie pour des tremblements quasi permanents des membres pelviens évoluant depuis un an. Aucune anomalie de la démarche n'est rapportée, bien qu'une discrète difficulté à sauter soit observée ponctuellement.
Examen clinique
À l'examen neurologique à distance, une démarche normale sans ataxie avec des tremblements à l'arrêt en position debout affectant exclusivement les membres pelviens sont notés. Ces tremblements disparaissent en position couchée ou lorsque l'animal est soulevé, mais persistent lorsqu'une pression manuelle est exercée sous les doigts. Les réactions posturales, les réflexes médullaires et l'examen des nerfs crâniens sont sans anomalie. L'auscultation des muscles des membres pelviens révèle un bruit distant rappelant celui d'un hélicoptère. L'examen clinique général est sans anomalie. Une atteinte neuromusculaire est suspectée sans toutefois pouvoir exclure une myélopathie L4-S1 ou une dyskinésie paroxystique.
Démarche diagnostique
L'examen biochimique et l'hémogramme sont sans anomalie. Un test FIV/FeLV et une sérologie Toxoplasma sont négatifs. Un EMG vigile est réalisé afin d'évaluer l'activité musculaire spontanée en station debout. L'examen met en évidence des décharges répétitives de basse fréquence (9 Hz) dans les muscles pelviens (figure 1). Aucune anomalie n'est détectée dans les muscles des membres thoraciques. L'EMG sous anesthésie et l'étude de la conduction motrice ne mettent pas en évidence d'anomalie. Une IRM de la colonne thoraco-lombaire s'avère normale.
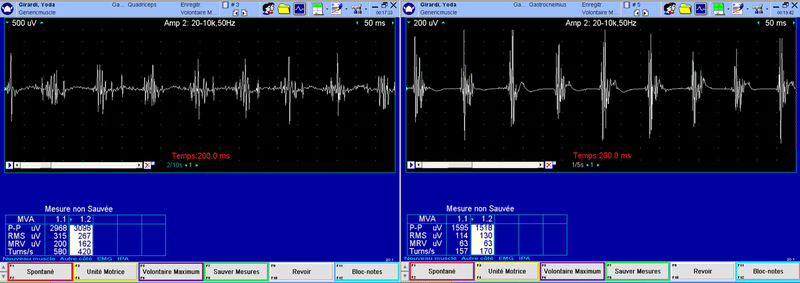
Figure 1 : EMG réalisé vigile révélant la présence de décharges répétitives de basse fréquence dans les muscles quadriceps (à gauche) et gastrocnémien (à droite).
Traitement
Un traitement à base de gabapentine à la dose de 13,5 mg/kg PO BID pendant deux semaines permet une diminution modérée de l'intensité des tremblements. Suite à une réduction progressive puis à un arrêt du traitement, une intensification des tremblements est rapportée. Une reprise du traitement à la dose initiale permet à nouveau une résolution partielle des signes cliniques.
Discussion
Ce cas clinique met en avant la démarche diagnostique lors de tremblements orthostatiques chez un chat. Ce dernier présente les signes pathognomoniques des tremblements orthostatiques observés chez le chien : tremblements posturaux des membres pelviens, test de suppression d'appui positif, auscultation des muscles révélant un bruit rappelant celui d'un hélicoptère, EMG vigile mettant en évidence des décharges répétitives dans les muscles pelviens. Une découverte étonnante est la fréquence basse (9 Hz) des décharges répétitives mises en évidence à l'examen EMG chez notre chat. En effet, La fréquence des décharges répétitives à l'EMG se situe habituellement entre 13 et 16 (nettement supérieure à celle des autres formes de tremblements) et est considérée comme presque pathognomonique du tremblement orthostatique. En médecine humaine, le terme de « tremblement orthostatique lent » a été proposé afin de décrire les tremblements de fréquence inférieure à 13 Hz [5]. Dans une revue de la littérature sur ce type de tremblement, la fréquence médiane des décharges était de 6 à 7 Hz, avec une plage allant de 3 à 12 Hz [5]. Environ deux tiers de ces tremblements « lents » étaient associés à d'autres affections neurologiques sous-jacentes mais aucune n'a été décelée chez notre chat.
Conclusion
Ce cas est, à notre connaissance, la première description d'un cas de tremblement orthostatique chez le chat, et plus spécifiquement d'un tremblement orthostatique lent. Alors que cette affection est bien documentée chez l'homme et le chien, aucune forme, qu'elle soit classique ou lente, n'avait été rapportée chez le chat jusqu'à présent. Cette observation souligne l'importance de considérer ce diagnostic dans cette espèce.
Bibliographie
- GAROSI, L.S., ROSSMEISL, J.H., DE LAHUNTA, A., et al. (2005) Primary orthostatic tremor in Great Danes.
- LIATIS, T., BHATTI, S.F.M., DECKER, S.D. (2024) Clinical approach of tremors in dogs and cats.
- LOWRIE, M., GAROSI, L. (2016) Classification of involuntary movements in dogs: Tremors and twitches.
- PLATT, S.R., DE STEFANI, A., WIECZOREK, L. (2006) Primary orthostatic tremor in a Scottish deerhound.
- HASSAN, A., CAVINESS, J. (2019) Slow Orthostatic Tremor: Review of the Current Evidence.
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Une technique simple d'examen du fond d'oeil à l'aide d'une lentille et d'un transilluminateur
Nimes, France
I. Le principe
L'examen du fond d'œil est un examen riche d'enseignements qui permet d'observer des lésions strictement intraoculaires mais aussi des anomalies qui peuvent être le reflet de nombreuses maladies générales. L'œil pouvant être comparé à une boîte noire, il s'agit d'éclairer et de focaliser sur le fond d'œil, de grossir les images obtenues et de placer l'œil de l'examinateur sur le trajet des rayons lumineux réfléchis afin de pouvoir observer de manière nette l'image du fond d'œil.
II. Techniques d'ophtalmoscopie
L’examen du fond d’œil est réalisé en ambiance lumineuse atténuée, après mydriase pharmacologique (instillations répétées de Mydriaticum ND pendant 15-20 min). Quelle que soit la technique utilisée, l'intensité de la source lumineuse est placée au minimum.
1. Ophtalmoscopie directe
L’ophtalmoscopie directe est la réalisation d’un examen du fond d’œil à l’aide d'un ophtalmoscope direct, instrument largement répandu dans la plupart des structures vétérinaires.
Il s'agit d'un instrument à main possédant une source lumineuse dont le faisceau lumineux est dévié de 90° par un miroir oblique de 45° qui le projette dans l’œil examiné. La lumière émise par l’ophtalmoscope direct est réfléchie par le fond d’œil, qui véhicule son image, traverse l’ouverture de l’ophtalmoscope et parvient à l’œil de l’examinateur placé derrière l’oculaire. Si l’ophtalmoscope direct est peu couteux et facilement disponible en structure vétérinaire, l’image du fond d’œil qu’il permet d’obtenir est limitée et ne permet pas d’avoir de vision d’ensemble du fond d’œil. Il n’est pas considéré par les ophtalmologistes comme instrument de choix pour la réalisation du fond d’œil.
2. Ophtalmoscopie indirecte
a) Principe :
En ophtalmoscopie indirecte, l’examinateur interpose une lentille convergente entre son œil et celui du patient, sur le trajet d’un faisceau lumineux qui éclaire le fond de l’œil. La lumière est ainsi projetée dans l’aire pupillaire à travers la lentille, de sorte que les rayons incidents qui divergent après passage à travers la pupille, illuminent une grande surface de la rétine. Les rayons réfléchis par le fond d’œil traversent en retour la lentille, et convergent au point focal de la lentille côté examinateur. Ce dernier voit donc se former sur la lentille une image inversée du fond d’œil. En réalité cette image se forme quelques centimètres en avant de la lentille, côté examinateur, à une distance qui représente le point focal de la lentille.
b) Concernant la lentille :
On utilise une lentille convergente. La puissance dioptrique de la lentille est :
- proportionnelle à l'étendue du champ de vision (surface du fond d’œil observée)
- inversement proportionnelle au grossissement du fond d’œil
- inversement proportionnelle au diamètre de la lentille
Chez le chien ou le chat, le choix de la lentille est classiquement porté sur une lentille plano-convexe de +20D, bon compromis entre grossissement et champ exploré. En comparaison, la lentille +30D permet d’observer une surface plus large avec un grossissement moindre
c) Concernant la source lumineuse :
On distingue l’ophtalmoscopie indirecte monoculaire et l’ophtalmoscopie indirecte binoculaire.
Pour l’ophtalmoscopie indirecte monoculaire, on utilise un transilluminateur de Finoff, ou à défaut, un stylo lumineux. Il s’agit d’une méthode simple pour réaliser un examen du fond d’œil.
Pour l’ophtalmoscopie indirecte binoculaire, on utilise casque d’ophtalmoscopie qui est muni d’une source de lumière, d’un système de vision binoculaire, de différents diaphragmes et filtres.
III. Technique d’ophtalmoscopie indirecte monoculaire pas à pas
Pour la réalisation d’un examen du fond d’œil en ophtalmoscopie indirecte monoculaire, il faut se munir de :
- Collyre Mydriaticum ND (tropicamide)
- Un transilluminateur de Finoff
- Une lentille 20D
- Le patient reçoit une goutte de Mydriaticum dans l’œil à examiner, toutes les 5 min pendant 20 min, jusqu’à obtenir une mydriase complète.
- L’examen est réalisé dans une pièce sombre
- L’animal est positionné assis sur la table d’examen. Un assistant maintient la tête du patient droite, une main sous le menton, une main derrière l’occiput
- Selon la hauteur de la table et la taille de l’animal, l’examinateur peut s’asseoir sur un tabouret de façon à avoir ses yeux à hauteur de ceux du patient.
- La luminosité du transilluminateur est réglée au minimum.
- Le faisceau de lumière du transilluminateur est dirigé vers la pupille pour obtenir le reflet du fond d’œil. Puis, la lentille est placée sur le trajet des rayons lumineux, près de l'œil de l'animal. Pendant l’examen, il faut maintenir le plan de la lentille parallèle au plan de l’iris si l’on veut conserver une image optimale du fond d’œil. L'image observée est ensuite agrandie en tirant lentement la lentille vers soi jusqu’à ce que l’image remplisse toute la lentille. L’image obtenue est inversée : verticalement et horizontalement.
Il s'agit d’un examen dynamique au cours duquel la vision du fond d’œil est parfois fugace du fait des mouvements permanents des yeux. L’examinateur doit donc constamment réadapter la position de son œil, de l’éclairage et de la lentille à la position de l’œil du patient afin de les maintenir alignés.
L’examen à l’aide d’un transilluminateur et d’une lentille nécessite un investissement limité et permet d’avoir une image de qualité, représentative et interprétable du fond d’œil. Bien qu’une courbe d’apprentissage soit nécessaire pour appréhender la coordination des gestes, celle-ci reste abordable et fait de cette technique un excellent compromis pour le vétérinaire généraliste.
IV. Variations physiologiques et recherche d'anomalie
De nombreuses variations physiologiques sont décrites chez les carnivores domestiques. Quelle que soit la technique utilisée, un examen systématique est réalisé. Un "balayage" de toute la surface du fond d'œil est donc nécessaire (Photo 1).
Photo 1
La papille est observée afin de déterminer sa taille, sa couleur, ses limites, sa position par rapport au plan de la rétine. Non myélinisée chez le chat, elle est ronde, grisâtre et de petite taille. Chez le chien, sa myélinisation rend sa taille, sa couleur et sa forme très variables. Les papilles des deux yeux sont également comparées. La papille peut apparaitre en dépression par rapport au fond d'œil (excavation, colobome) ou en surélévation (œdème, papillite). Une papille de taille diminuée peut signer une hypoplasie, ou une atrophie papillaire. Cette dernière s'accompagne généralement d’une démyélinisation.
La vascularisation est également observée afin d’évaluer le nombre de vaisseaux, leur calibre, leur tortuosité et l’éventuelle présence de lésions périvasculaires. On observe en général 3 veinules de gros calibre, radiaires, dorsales. Les vaisseaux choroïdiens, larges et à disposition régulière, peuvent être visibles en l’absence de pigmentation choroïdienne +/- de tapis.
La zone du tapis est examinée et sa réflectivité, sa texture, sa couleur sont évaluées. La couleur du tapis varie en fonction de l’âge et de la robe de l’animal chez le chien. La zone du tapis occupe généralement la moitié dorsale du fond d'œil mais sa taille est très variable d’un individu à l’autre. Chez le chat, la couleur du tapis, lorsqu’il est présent, est constante (jaune-vert), et ce, quelle que soit la robe. L’absence totale de tapis est également possible. La zone hors tapis est, par définition, déterminée par la taille du tapis et ses limites peuvent parfois être très irrégulières. L’absence de pigmentation apparente de la zone hors tapis est possible, notamment chez les individus aux yeux clairs. Une hyperréflectivité de la zone du tapis signe généralement un amincissement de la rétine (atrophie rétinienne par exemple). À l'inverse, une hyporéflectivité de la zone du tapis peut être observée sous la forme de plages grisâtres en cas de présence anormale d’éléments entre la rétine et la choroïde (œdème, décollement rétinien, etc.). La présence de plis, d’hémorragies, de pigmentation est également possible. Quelles que soient les lésions observées, leur caractère focal/multifocal/généralisé ainsi que leur taille et leur localisation doivent être précisés.
Bibliographie
- FEATHERSTONE HJ, HEINRICH CL. Ophthalmic Examination and Diagnostics, Part 1: the Eye Examination and Diagnostic Procedures. Dans: veterinary Ophthalmology 6th Ed. Hoboken, éd. John Wiley & Sons. 2021:654-661
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Urolithiase chez le chat : étude rétrospective sur 4705 calculs urinaires félins prélevés entre 2016 et 2021 en France et analysés par spectrométrie infrarouge
Hortense HÉLIER
Coauteurs : A. BOGEY (0494669990, 1128 route de Toulon 83400 Hyères,
M. CANONNE-GUIBERT (0675474201, 7 avenue du Général de Gaulle 94700 Maisons-Alfort,
G. BENCHEKROUN (0143967373, 7 avenue du Général de Gaulle 94700 Maisons-Alfort,
C. MAUREY (0682124577, 7 avenue du Général de Gaulle 94700 Maisons-Alfort,
Introduction
Les études épidémiologiques sur les différents types minéraux d'urolithiase féline sont rares en Europe. À ce jour, aucune étude à grande échelle n'avait été réalisée sur les types de calculs urinaires chez le chat en France.
Matériel et méthode
Un total de 4 705 chats appartenant à des particuliers et atteints de calculs urinaires a été inclus. La composition des calculs, déterminée par spectrométrie infrarouge, a été comparée à divers facteurs tels que la race, la note d'état corporel, l'âge, le sexe, la densité urinaire et le pH urinaire.
Résultats
Sur les 4 705 calculs analysés, 4 263 étaient des calculs purs, représentant 90,6 % des échantillons. Les calculs de struvite et d'oxalate de calcium représentaient à eux seuls environ 83 % des cas, avec des proportions quasi identiques de 46 % pour la struvite et 47 % pour l'oxalate de calcium. Les autres pourcentages concernaient des types minéraux divers (purines, phosphates, etc.).
L'analyse statistique a révélé que les chats Européens et Norvégiens présentaient un risque accru de développer des calculs de struvite (p < 0,001), tandis que les Persans, Birmans, British, Ragdolls, Scottish et Bengals étaient plutôt prédisposés aux calculs d'oxalate de calcium (p < 0,001).
Les mâles étaient plus fréquemment atteints par des calculs d'oxalate de calcium (p < 0,001), tandis que les femelles étaient plus souvent atteintes de struvite (p < 0,001). Les chats présentant des calculs d'oxalate de calcium étaient plus âgés (âge moyen de 8,2 ans) que ceux présentant d'autres types de calculs (p < 0,01 pour chaque comparaison). Ces chats avaient également une urine plus acide (p < 0,001) et plus diluée (p < 0,001) que les autres.
Enfin, 61 % des chats en sous-poids (score d'état corporel < 4) avaient des calculs d'oxalate de calcium. L'analyse morphologique des calculs d'oxalate de calcium a montré que les chats présentant des weddellites étaient significativement plus jeunes (moyenne : 6,1 ans) que ceux présentant des whewellites (moyenne : 8,5 ans, p < 0,01).
Discussion et conclusion
Les types de calculs les plus fréquents dans notre population sont la struvite et l'oxalate de calcium. Nos résultats confirment la prédisposition des Européens et des Norvégiens à la struvite et celle des Persans, Birmans, British, Ragdolls, Scottish et Bengals à l'oxalate de calcium. Une proportion significative des chats en sous-poids présentaient des calculs d'oxalate de calcium, possiblement en lien avec une fonction rénale altérée, suggérée par la dilution urinaire observée dans ce groupe. Les associations observées avec l'âge, le sexe et les paramètres urinaires soulignent l'importance d'une approche diagnostique et thérapeutique individualisée dans la prise en charge de l'urolithiase féline. Bien que non encore validée à ce jour, une classification morphologique détaillée pourrait être évaluée de manière prospective afin d'améliorer l'évaluation pronostique et d'optimiser les stratégies thérapeutiques.
Bibliographie
- BURGGRAAF, N.D., WESTGEEST, D.B., CORBEE, R.J. (2021) Analysis of 7866 feline and canine uroliths submitted between 2014 and 2020 in the Netherlands. Research in Veterinary Science vol. 137, p. 86-93.
- DAUDON, M., JUNGERS, P., TRAXER, O. (2012) Lithiase urinaire. Paris, Lavoisier.
- HOUSTON, D.M., MOORE, A.E.P. (2009) Canine and feline urolithiasis: Examination of over 50 000 urolith submissions to the Canadian Veterinary Urolith Centre from 1998 to 2008. The Canadian Veterinary Journal vol. 50, n° 2, p. 1263-1268.
- LEKCHAROENSUK, C., OSBORNE, C.A., LULICH, J.P. (2001c) Epidemiologic study of risk factors for lower urinary tract diseases in cats. Journal of the American Veterinary Medical Association vol. 218, n° 9, p. 1429-1435.
- OSBORNE, C.A., LULICH, J.P., KRUGER, J.M., et al. (2009a) Analysis of 451,891 canine uroliths, feline uroliths, and feline urethral plugs from 1981 to 2007: perspectives from the Minnesota Urolith Center. The Veterinary Clinics of North America. Small Animal Practice vol. 39, n° 1, p. 183-197.
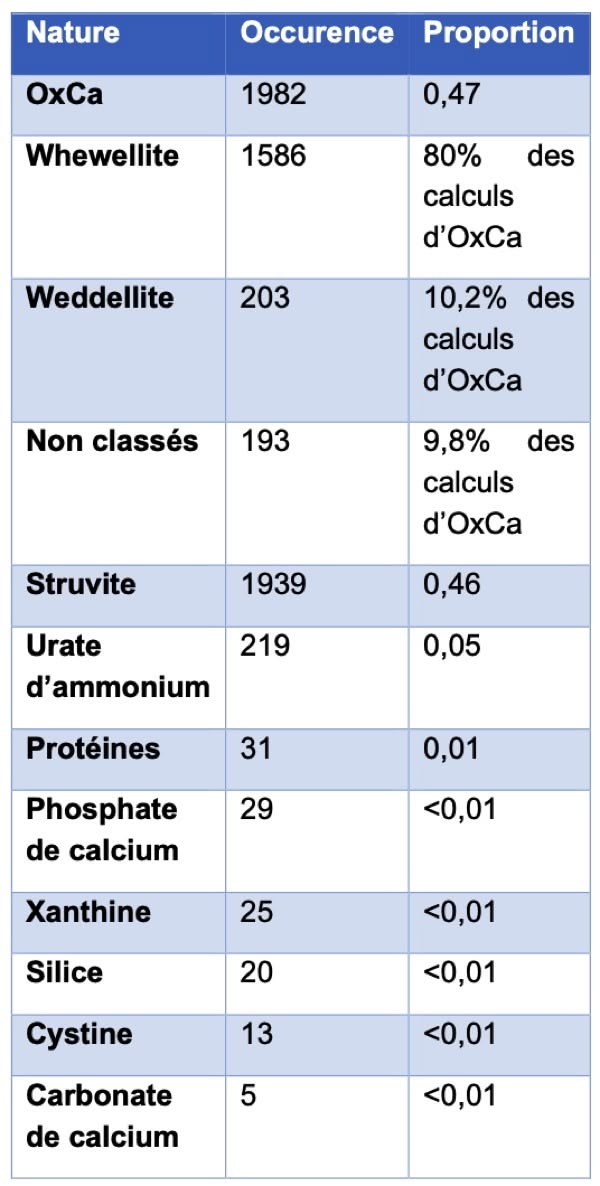
Figure 1
Liens d'intérêt : Les analyses des calculs urinaires ont été réalisées gracieusement dans le cadre d'un partenariat entre Vet'Analys et Royal Canin.
📃 Utilisation de l'endoscopie avec imagerie par bande spectrale étroite (Narrow Band Imaging ou NBI) dans la détection et le diagnostic d'affections urogénitales chez le chien : une étude préliminaire
Jeanne MONTIER
Coauteurs : J. MONTIER, R. LAVOUÉ, M. MANTELLI, V. LEYNAUD, M. KURTZ, N. JOUSSERAND
Contexte
L'examen endoscopique est couramment utilisé pour explorer les affections uro-génitales chez le chien. Habituellement réalisé en lumière blanche, il peut être complété par l'imagerie à bande étroite (Narrow-Band Imaging, NBI), qui repose sur un éclairage par des longueurs d'ondes spécifiques bleues et vertes. En médecine humaine, cette approche améliore la visualisation des structures vasculaires et pourrait ainsi renforcer la sensibilité diagnostique, notamment lors de processus néoplasiques. Toutefois, son application en médecine vétérinaire pour les affections uro-génitales canines n'a jamais été décrite au-delà de quelques rapports de cas.
Objectifs
Les objectifs de cette étude sont :
- de décrire des images normales et anormales obtenues avec la technique NBI en endoscopie urogénitale ;
- d'évaluer l'intérêt de l'emploi du NBI dans l'identification et la caractérisation d'une affection urogénitale inflammatoire, néoplasique ou vasculaire chez le chien.
Matériel et méthode
Dans cette étude rétrospective, deux groupes ont été étudiés : 8 chiens sains (groupe 1) et 23 chiens atteints d'une affection urogénitale (groupe 2) inflammatoire, néoplasique ou vasculaire. Tous ont bénéficié d'un examen endoscopique conventionnel en lumière blanche et en NBI, ainsi que d'un examen histopathologique pour les cas présentant une ambiguïté diagnostique. Les images endoscopiques obtenues avec et sans NBI ont été extraites puis analysées post-examen par l'opérateur en charge du cas selon une grille d'évaluation standardisée. De plus, des images sélectionnées ont été examinées rétrospectivement et en aveugle par un opérateur indépendant afin d'évaluer les performances diagnostiques du mode NBI en endoscopie urogénitale, en comparaison au diagnostic établi sur la base clinique, endoscopique et histologique.
Résultats
Dans le groupe 1, une banque d'images normales a été établie, caractérisant le réseau vasculaire sain. Dans le groupe 2, le NBI a facilité l'identification et la caractérisation des lésions inflammatoires, néoplasiques et vasculaires au cours de l'examen endoscopique. Lors de la lecture en aveugle des images par un opérateur indépendant, les lésions vasculaires étaient identifiées dans 100 % des cas en NBI (contre 75 % en endoscopie conventionnelle), les lésions inflammatoires dans 69 % des cas pour les deux techniques et les lésions néoplasiques dans 70 % des cas en NBI (contre 90 % en endoscopie conventionnelle). Aucune sur-interprétation n'a eu lieu, car 100 % des images normales ont été correctement identifiées par les deux techniques. De plus, lorsqu'une lésion était détectée par les deux méthodes, le NBI offrait un degré de confiance supérieur dans 55 % des cas pour les lésions inflammatoires, 25 % pour les néoplasiques et 100 % pour les vasculaires. Le NBI a également aidé à guider les biopsies en évitant les larges vaisseaux.
Le NBI a également aidé à guider la réalisation de biopsies vers la zone la plus modifiée, en évitant les larges vaisseaux pour limiter le risque de saignement iatrogène.
Conclusion
L'utilisation de la technologie NBI lors d'endoscopie urogénitale permet d'augmenter la sensibilité de l'examen en améliorant notablement le contraste entre la vascularisation et les autres structures. Ainsi, cette technique permet de guider la réalisation de biopsies et apporte des informations complémentaires lors de procédures interventionnelles. Facile d'utilisation, non invasif et compatible avec divers endoscopes, cette approche représente un outil diagnostique complémentaire utile en endoscopie uro-génitale.
Dans cette étude le NBI était moins performant que l’endoscopie conventionnelle pour l’identification des lésions tumorales. Ce résultat surprenant est possiblement impacté par les limites de notre étude : faible effectif dans le groupe néoplasique, analyses des images en aveugle sur images fixes (ce qui ne reflète pas la réalité de l'endoscopie dynamique).
Figure 1 : Exemple d'images endoscopiques vésicales obtenues en lumière blanche et en NBI lors de cystite nodulaire. À gauche : lumière blanche - À droite : NBI
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Valeur prédictive de l'urétrographie de contraste sur l'issue post-opératoire lors d'urétrostomie périnéale chez des chats dysuriques : étude rétrospective de 22 cas
Catalina LIWSZYC
Coauteurs : C. LIWSZYC ; C. MAUREY ; M. MANASSERO ; M. KURTZ
Introduction
Une urétrographie de contraste est souvent préconisée avant la réalisation d'une urétrostomie périnéale (UP) chez le chat dysurique, pour la recherche d'anomalies obstructives urétrales [1]. Toutefois, la capacité de l'urétrographie à prédire la résolution de la dysurie en période post-opératoire de l'UP reste peu étudiée.
Par ailleurs, l'UP ne permettant qu'une résection urétrale à l'aplomb des glandes bulbo-urétrales [2] (GBU), il est habituellement admis qu'une lésion obstructive située entre le col vésical et les GBU constitue une contre-indication relative à l'intervention : une résolution post-opératoire de la dysurie n'est en effet pas attendue dans ce contexte. Ces données n'ont toutefois pas été évaluées.
Objectif
Cette étude vise à évaluer l'association entre les résultats de l'urétrographie de contraste et la résolution de la dysurie après prise en charge par une UP chez les chats présentant une dysurie.
Matériels et méthodes
Une étude rétrospective a été menée sur les dossiers médicaux de chats mâles présentés pour dysurie, ayant fait l'objet d'une urétrographie et d'une UP entre le 1er janvier 2013 et le 31 décembre 2024 au CHUVA-AC (MAISONS-ALFORT). Les animaux présentant des calculs urétraux, des tumeurs urétrales, une dysurie d'origine neurogénique ou un polytraumatisme ont été exclus. Le succès (ou succès partiel) post-opératoire était défini par la résolution (ou l'amélioration) de la dysurie, à 14 jours post-opératoire. Les anomalies identifiées à l'examen de contraste étaient classées comme douteuses ou certaines.
Résultats
Vingt-deux chats mâles ont été inclus, tous castrés, et dont 21 chats Européens.
Quarante-cinq pour cent des chats (10/22) ne présentaient aucune anomalie à l'urétrographie de contraste. Une résolution postopératoire complète de la dysurie a été observée dans 100 % (10/10) des cas.
L'urétrographie identifiait une anomalie chez 45 % des chats (10/22) et deux anomalies chez 9 % (2/22).
Ces anomalies étaient antépelviennes chez 3 chats (1 brèche, 3 sténoses urétrales suspectées) : un d'entre eux a présenté une résolution complète de la dysurie à J14 postopératoire, et les deux autres ont été euthanasiés avant la sortie d'hospitalisation (l'un en raison d'un uropéritoine septique, l'autre d'une suspicion de calicivirose systémique 4 jours après l'intervention sans information disponible concernant le comportement mictionnel). Une anomalie urétrale pelvienne (sténose urétrale) a été observée chez un chat, présentant une résolution complète de la dysurie en période post-opératoire de l'UP. Neuf anomalies urétrales péniennes (5 brèches, 1 sténose, 3 sténoses suspectées) ont été identifiées chez 8 chats. Une résolution complète de la dysurie était observée chez 100 % de ces chats.
L'identification d'une anomalie à l'examen d'urétrographie n'était pas associée à la persistance de la dysurie en période post-opératoire (p = 0,24). De même, la présence d'une sténose (suspectée ou non) ou d'une brèche urétrale n'étaient pas associées à la persistance de la dysurie en période post-opératoire (p = 0,18 et p = 0,38, respectivement). La localisation de la sténose (en amont ou aval des GBU) n'était pas associée à l'issue post-opératoire (p = 0,43), cependant l'identification d'une anomalie (brèche ou sténose) proximalement aux GBU était associée au décès avant la sortie d'hospitalisation (p = 0,03).
Discussion
L'urétrographie de contraste n'a pas permis d'identifier des anomalies expliquant la dysurie que dans 55 % des cas. Des anomalies de la partie la plus distale de l'urètre pénien ne peuvent toutefois être exclues chez ces individus.
Chez les chats ne présentant pas d'anomalie urétrale, une résolution de la dysurie après réalisation d'une UP était observée dans 100 % des cas. Chez ceux présentant une anomalie obstructive urétrale, la dysurie était résolue chez 75 % (6/8) en période post-opératoire malgré la localisation proximale de certaines anomalies par rapport au site chirurgical (deux chats étant décédés dans le post-opératoire immédiat). Aucune association entre les résultats de l'urétrographie préopératoire et la résolution de la dysurie n'a été identifiée. En effet, le comportement mictionnel n'a pas pu être évalué chez les animaux décédés : ces données remettent en question la pertinence d'un examen de contraste systématique avant la réalisation d'une UP. Toutefois, le nombre très limité de cas, en particulier ceux présentant une anomalie en amont des GBU, ne permet pas de tirer de conclusion formelle et souligne la nécessité d'études prospectives incluant un effectif plus important.
L'amélioration de la dysurie malgré l'identification d'une anomalie obstructive proximalement au site chirurgical est mal expliquée. Il est possible que le raccourcissement de la longueur de l'urètre contribue à une réduction des résistances au passage de l'urine. Des faux positifs au cours de l'urétrographie (artéfacts) sont également à considérer.
Bibliographie
- RADEMACHER N. (2019) Diagnostic Imaging of the Urinary Tract. Vet Clin North Am Small Anim Pract 49(2), 261 286
- MONNET E. (2023) Urolithiasis of the Lower Urinary Tract. In Small Animal Soft Tissue Surgery, 2nd Edition. ed. John Wiley & Sons, Ltd, pp 523 532
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃 Virus et cancer : spécificités du chat
Nantes, France
I. Introduction
Depuis plus d’un demi-siècle, le rôle des rétrovirus félins dans la genèse de certains cancers, en particulier les lymphomes, est largement documenté. Trois virus principaux sont suspectés ou impliqués dans la cancérogenèse féline : le virus leucémogène félin (FeLV), le virus de l’immunodéficience féline (FIV) et certains papillomavirus félins (FcaPV). Ces infections virales présentent des caractéristiques spécifiques qui en font un modèle d’étude unique en pathologie comparée.
II. Le FeLV : modèle classique de rétrovirus oncogène
Le FeLV demeure le principal agent viral associé aux tumeurs félines. La relation entre FeLV et lymphome félin a été établie dès les années 1960, et ce virus reste un modèle pour l’étude de la transformation maligne rétrovirale. Chez les chats infectés, la prévalence des lymphomes associés au FeLV a diminué depuis la généralisation du dépistage et de la vaccination, passant d’environ 70 % dans les années 1980 à moins de 10–20 % actuellement (Feline Lymphoma and a High Correlation with FeLV, PMID 30691602). Toutefois, l’infection persistante par le virus, notamment par les sous-groupes FeLV-A et FeLV-B, continue de jouer un rôle majeur dans la leucémogenèse et la lymphomagenèse (Phylogenetic identification of FeLV-A and B in cats with lymphoma and leukemia, PMID 36924831).
Sur le plan mécanistique, le FeLV exerce son effet oncogène par insertion du provirus dans le génome de la cellule hôte, induisant la surexpression de proto-oncogènes tels que Myc ou Fos. Des études récentes ont montré que les infections mixtes par FeLV-A/FeLV-B augmentent significativement le risque de lymphomes médiastinaux et multicentriques (68,8 % de FeLV-AB chez les chats porteurs de lymphome dans l’étude de 2023, PMID 36924831). D’un point de vue clinique, les chats FeLV positifs présentent souvent un pronostic défavorable : la survie médiane est inférieure à 6 mois malgré les traitements (diffuse large B-cell lymphoma in FeLV-infected cats, PMID 38800883).
Grâce à la vaccination FeLV et à l’amélioration du contrôle des infections, la typologie des lymphomes félins a considérablement évolué. On observe une diminution des formes médiastinales FeLV-associées et une augmentation des formes digestives FeLV négatives, aujourd’hui les plus fréquentes. Cette transition reflète le passage d’une étiologie virale vers une étiologie multifactorielle, intégrant des facteurs génétiques, environnementaux et immunologiques.
III. Le FIV : un cofacteur indirect
Le virus de l’immunodéficience féline (FIV) est un lentivirus analogue au VIH. Son rôle oncogène direct est moins clair, mais plusieurs études suggèrent une augmentation du risque tumoral secondaire à l’immunodépression induite. Dans une cohorte de 1160 chats, 62 % des individus FIV positifs présentaient une néoplasie, principalement des lymphomes extraganglionnaires et des carcinomes épidermoïdes, avec parfois des co-infections FeLV/FIV (Neoplasia Associated with FIV infection, PMID 1666082). Le FIV n’induit donc pas directement la transformation, mais facilite l’expansion clonale de cellules pré-néoplasiques en contexte d’immunosuppression chronique.
IV. Les papillomavirus félins et les carcinomes épidermoïdes
Les papillomavirus félins (FcaPV) représentent une autre catégorie d’agents oncogènes. Plusieurs types (FcaPV-2, FcaPV-3, FcaPV-5 et FcaPV-6) ont été détectés dans des carcinomes épidermoïdes cutanés ou oraux (Identification of a novel papillomavirus associated with feline cutaneous squamous cell carcinoma, PMID 31968684 ; Feline oral squamous cell carcinoma and FcaPV-2, PMCID PMC10229798). Ces virus agiraient par des mécanismes analogues aux papillomavirus humains oncogènes (HPV 16/18), notamment via l’expression des oncoprotéines E6/E7 responsables de l’inactivation de p53 et Rb.
Chez le chat, les virus oncogènes représentent un modèle précieux pour comprendre les interactions entre infection chronique, immunité et cancer. Si le FeLV conserve un rôle pionnier comme modèle de transformation rétrovirale, les papillomavirus félins et le FIV élargissent la perspective de la pathologie comparée, en rapprochant le félin des mécanismes oncogéniques connus chez l’humain. Le suivi épidémiologique des infections FeLV et FcaPV demeure essentiel pour mieux comprendre l’évolution des cancers félins et affiner le pronostic des lymphomes.
Bibliographie
- NAKAMURA M, TAKAHASHI M, SAKURAI S, et al. Feline lymphoma and high correlation with FeLV. J Vet Med Sci. 2019;81(2):215–221. PMID: 30691602
- SAITO M, SATO E, SUZAKI Y, et al. Phylogenetic identification of FeLV-A and -B in cats with lymphoma and leukemia. J Feline Med Surg. 2023;25(4):310–317. PMID: 36924831
- TOMIYASU H, OHTANI M, NISHIMURA R, et al. Diffuse large B-cell lymphoma in FeLV-infected cats: clinicopathological analysis and prognosis. J Vet Med Sci. 2024;86(6):797–805. PMID: 38800883
- HARDY WD Jr, HESS PW, MACEWEN EG, et al. Neoplasia associated with feline immunodeficiency virus infection. Cancer Res. 1991;51(6):1621–1625. PMID: 1666082
- CARRAI M, DI TOMMASO M, BALBONI A, et al. Identification of a novel papillomavirus associated with feline cutaneous squamous cell carcinoma. J Gen Virol. 2020;101(2):137–145. PMID: 31968684
- ALTAMURA G, CORTEGGIO A, IOVANE V, et al. Feline oral squamous cell carcinoma and Felis catus papillomavirus-2: diagnostic and prognostic relevance of viral markers. Viruses. 2023;15(10):2012. PMCID: PMC10229798
Liens d'intérêt : Pas de conflit d'intérêt déclaré.
📃
Liens d'intérêt :
